Реакция окисления трис[(2-метокси)(5-бром)фенил]сурьмы трет-бутилгидропероксидом в присутствии 3,4-диоксибензойной кислоты
Автор: Белов Василий Васильевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 2 т.14, 2022 года.
Бесплатный доступ
Взаимодействием трис(5-бром-2-метоксифенил)сурьмы с 3,4-дигидроксибензойной кислотой в присутствии трет-бутилгидропероксида (1:2:1 мольн.) в диэтиловом эфире при комнатной температуре синтезирован и структурно охарактеризован сольват 4-карбоксипирокатехолато-О,О’-трис(5-бром-2-метоксифенил)сурьмы с хлороформом (5-Br-2-MeOC6H3)3Sb[O,O’C6H3-COOH-4] ∙ 2 CHCl3. По данным рентгеноструктурного анализа, проведенного на дифрактометре D8 QUEST фирмы Bruker, кристаллографические параметры элементарной ячейки соединения 1: пространственная группа P21/n, а = 9,302(2), b = 21,166(5), c = 19,517(6) Å, α = 90,00°, β = 96,302(13)°, γ = 90,00°, V = 3819(17) Å3, ρвыч = 1,862 г/см3, Z = 4. Атом сурьмы имеет искаженную тригонально-бипирамидальную координацию с одним из атомов кислорода пирокатехолатного лиганда в аксиальном положении. Длина связи Sb-С лежит в интервале значений 2,107(5)-2,131(5) Å. Экваториальные углы СSbC равны 95,9(2)-125,7(1)º. Длины связей Sb-O неравноценны (2,095(4) и 2,013(3) Å), но близки к сумме ковалентных радиусов атомов сурьмы и кислорода 2,05 Å. В кристалле 1 присутствуют тесные контакты атомов водорода хлороформа с атомами кислорода катехолатного лиганда (2,40 Å) и атома водорода катехолатного лиганда с атомами хлора молекул хлороформа (2,95 Å). В кристаллах соединение 1 находится в виде димеров, где две молекулы связываются между собой двумя водородными связями O(6)∙∙∙H(7) (1,864 Å) при сумме ван-дер-ваальсовых радиусов водорода и кислорода 2,57 Å. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2144306; deposit@ccdc.cam.ac.uk или http://www.ccdc.cam.ac.uk/data_request/cif).
3, 4-дигидроксибензойная кислота, трис(5-бром-2-метоксифенил)сурьма, реакция окислительного присоединения, синтез, строение, ик-спектр, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147237501
IDR: 147237501 | УДК: 547.47+546.865+548.312.5
The oxidation reaction of tris[(2-methoxy)(5-bromo)phenyl]antimony by tert-butyl hydroperoxide in the presence of 3,4-dioxybenzoic acid
The interaction of tris(5-bromo-2-methoxyphenyl)antimony with 3,4-dioxybenzoic acid, in the presence of tert-butyl hydroperoxide (1:2:1 mol.) in diethyl ether at ambient temperature has given 4-carboxypyrocatecholato-O,O’-tris(5-bromo-2-methoxyphenyl)antimony solvate with cloroform (5-Br-2-MeOC6H3)3Sb[O,O’C6H3-COOH-4] ∙ 2 CHCl3, which has been structurally characterized. According to the X-ray diffraction data obtained on a Bruker D8 QUEST diffractometer, compound 1 has the following crystallographic parameters of the unit cell: space group P21/n, а = 9.302(2), b = 21.166(5), c = 19.517(6) Å, α = 90.00°, β = 96.302(13)°, γ = 90.00°, V = 3819(17) Å3, ρcalc = 1.862 g/cm3, Z = 4. The antimony atom has a distorted trigonal-bipyramidal coordination with one of the oxygen atoms of the pyrocatecholate ligand in the axial position. The Sb-C bond length lies in the range of values 2.107(5)-2.131(5) Å. The CSbC equatorial angles are 95.9(2)-125.7(1)°. The Sb-O bond lengths are not equivalent (2.095(4) and 2.013(3) Å), but are close to the sum of the covalent radii of the antimony and oxygen atoms, 2.05 Å. Crystal 1 contains close contacts of the hydrogen atoms in chloroform with the oxygen atoms of the catecholate ligand (2.40 Å), as well as the hydrogen atoms of the catecholate ligand with the chlorine atoms of chloroform molecules (2.95 Å). Compound 1 in crystals is in the form of dimers, where two molecules are linked by two hydrogen bonds O(6)∙∙∙H(7) (1.864 Å), while the sum of the Van der Waals radii of hydrogen and oxygen is 2.57 Å. Complete tables of atomic coordinates, bond lengths, and bond angles for structure 1 have been deposited at the Cambridge structural data Dank (No. 2144306; deposit@ccdc.cam.ac.uk; https://www.ccdc.cam.ac.uk).
Текст научной статьи Реакция окисления трис[(2-метокси)(5-бром)фенил]сурьмы трет-бутилгидропероксидом в присутствии 3,4-диоксибензойной кислоты
Взаимодействием трис(5-бром-2-метоксифенил)сурьмы с 3,4-дигидроксибензойной кислотой в присутствии трет-бутилгидропероксида (1:2:1 мольн.) в диэтиловом эфире при комнатной температуре синтезирован и структурно охарактеризован сольват 4-карбоксипирокатехолато-О,О’-трис(5-бром-2-метоксифенил)сурьмы с хлороформом (5-Br-2-MeOC6H3)3Sb[O,O’C6H3-COOH-4] ∙ 2 CHCl3. По данным рентгеноструктурного анализа, проведенного на дифрактометре D8 QUEST фирмы Bruker, кристаллографические параметры элементарной ячейки соединения 1: пространственная группа P21/n, а = 9,302(2), b = 21,166(5), c = 19,517(6) Å, α = 90,00°, β = 96,302(13)°, γ = 90,00°, V = 3819(17) Å3, ρвыч = 1,862 г/см3, Z = 4. Атом сурьмы имеет искаженную тригонально-бипирамидальную координацию с одним из атомов кислорода пирокатехолатного лиганда в аксиальном положении. Длина связи Sb–С лежит в интервале значений 2,107(5)–2,131(5) Å. Экваториальные углы СSbC равны 95,9(2)–125,7(1)º. Длины связей Sb–O неравноценны (2,095(4) и 2,013(3) Å), но близки к сумме ковалентных радиусов атомов сурьмы и кислорода 2,05 Å. В кристалле 1 присутствуют тесные контакты атомов водорода хлороформа с атомами кислорода катехолатного лиганда (2,40 Å) и атома водорода катехолатного лиганда с атомами хлора молекул хлороформа (2,95 Å). В кристаллах соединение 1 находится в виде димеров, где две молекулы связываются между собой двумя водородными связями O(6)∙∙∙H(7) (1,864 Å) при сумме ван-дер-ваальсовых радиусов водорода и кислорода 2,57 Å. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2144306; или .
Синтез арильных производных пятивалентной сурьмы, основанный на реакции окислительного присоединения триарилсурьмы пероксидом в присутствии кислот НХ, впервые предложенный в работе [1], в настоящее время хорошо изучен для широкого спектра органических соединений сурьмы (дикарбоксилаты, дисульфонаты, диароксиды, диоксиматы и др. [ 2 – 7 ]). Его достоинством является одностадийность, мягкие условия проведения реакций и высокий выход единственного продукта. Реакции окислительного присоединения триарилсурьмы с органическими Н-кислотами в присутствии пероксида водорода или трет -бутилгидропероксида (могут использоваться другие органические окислители), как правило, дают производные Ar3SbX2 (при мольном соотношении триарилсурьмы и кислоты 1:2) [ 2 , 5–7] либо (Ar 3 SbX) 2 О (при соотношении 1:1) [ 8 ], где Х – остаток кислоты. Однако окислительный синтез соединений сурьмы недостаточно исследован при использовании в качестве Н-кислот би- и полифункциональных соединений, результатом которого могут быть продукты разнообразного строения. Немногочисленные примеры указанных реакций известны. Так, показано, что трифенилсурьма взаимодействует с вицинальными диолами в присутствии трет -бутилгидропероксида с образованием циклических соединений сурьмы [ 9 ]:
HO
Ph3Sb + R + t- BuOOH
HO
O
Ph 3 Sb R + t- BuOH + H2O
O
R= CHMeCHMe, CPh 2 CPh 2 , CH 2 CH 2 , CMe 2 CMe 2 , CH 2 CH(CH 2 OH), 1,2-C 6 H 4
Строение продукта реакции трифенилсурьмы с дигидроксибензолами определяется расположением гидроксильных групп в ароматическом кольце [10]. В случае пирокатехина образуется 5-членный орто -фенилендиоксид трифенилсурьмы, резорцина – макроциклическое соединение, при взаимодействии с гидрохиноном получается полимерный гидрохинолят трифенилсурьмы:
R3Sb + t -BuOOH
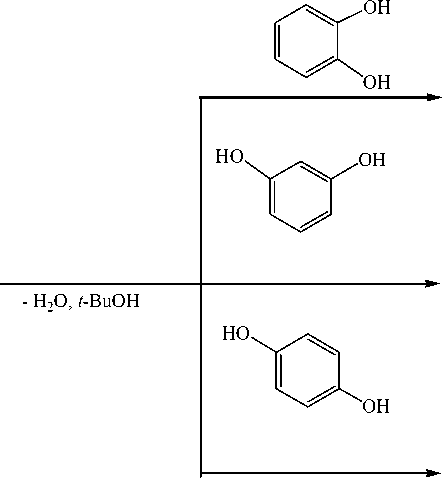
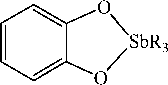
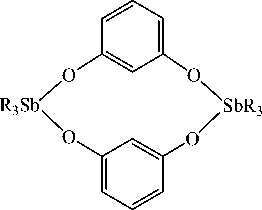
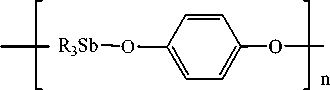
Однако при взаимодействии трифенилсурьмы с фталевой кислотой вместо ожидаемого продукта, содержащего пятичленный цикл, был получен дифталат трифенилсурьмы со свободными карбоксильными группами [11]:
Ph 3 Sb + 2 C 6 H 4 [C(O)OH] 2 -1,2 + H 2 O 2 → Ph 3 Sb[O(O)CC 6 H 4 С(O)OH-2] 2 + 2H 2 O.
В реакции дихлорида трифенилсурьмы с салицилатом серебра принимает участие только карбоксильная группа, но не гидроксильная. Продуктом реакции при мольном соотношении 1:2 является бис (2-гидроксибензоат) трифенилсурьмы [12]:
Ph 3 SbСl 2 + 2 AgOC(O)С 6 Н 4 ОН-2 → Ph 3 Sb[O(O)CC 6 H 4 OH-2] 2 + 2 AgCl.
При взаимодействии трифенилсурьмы с салициловой кислотой в присутствии окислителя образуется μ 2 -оксо- бис [(2-гидроксибензоато)фенилсурьма] [13]:
Ph 3 Sb + НOC(O)С 6 Н 4 ОН-2 + H 2 O 2 → [Ph 3 SbO(O)CC 6 H 4 OH-2] 2 O + 2H 2 O.
Взаимодействием трифенилсурьмы с диоксимом 2,2’-метиленди(циклопентан-1-она) в присутствии пероксида водорода синтезирован центросимметричный биядерный макроциклический комплекс бис - μ 2-[(метилендициклопентанон-2,2’-диоксимато)трифенилсурьмы] [14]:
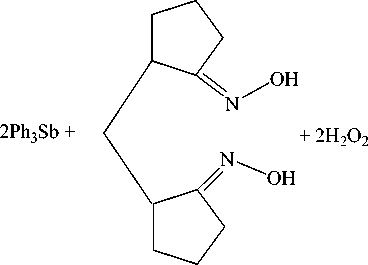
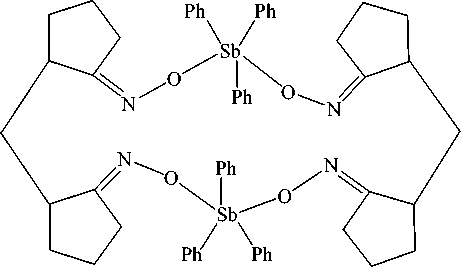
Следует отметить, что этот же продукт был выделен из реакции пентафенилсурьмы с диоксимом при нагревании (90 °С) в течение 5 часов [15].
Реакция трифенилсурьмы с 6,6,6-трифтор-2,2-диметилгександионом-3,5 в присутствии пероксида водорода в эфире протекает с образованием 6,6,6-трифтор-3-гексанон-5,5-диолатотрифенилсурьмы c выходом 59 %, где атом сурьмы гексакоординирован [16]:
CF 3
OC
Ph 3 Sb + CF 3 C(O)CH 2 C(O)C(CH 3 ) 3 + H 2 O2 ►
Ph 3 Sb O CH 2
OC
C(CH 3 ) 3
При использовании в аналогичной реакции с трифторацетилацетоном в качестве окислителя трет- бутилгидропероксида выход целевого продукта увеличивается до 93 % [17].
Взаимодействие три (мета- толил ) сурьмы с 2-гидроксибензальдоксимом в присутствии пероксида водорода сопровождается образованием макроциклического соединения – бис (µ 3 -2-гидроксибензальдоксимато-О,О’,N)-(µ 2 -оксо)- бис [ди( мета -толил)сурьмы] [18]. Аналогичные структуры получены при взаимодействии трис (5-бром-2-метоксифенил)сурьмы, три( п -толил)сурьмы, трис (3-фторфенил)сурьмы и трис (4-фторфенил)сурьмы с 2-гидрокси-бензальдоксимом [19, 20]:
HC N
O z * O
Ar
2Ar 3 Sb + 2HON=CHC 6 H 4 (OH-2) + 2H 2 O 2
Ar Sb O z Sb Ar
Ar O N -= CH O
Ar = C 6 H 2 ОМе-2-Br-5, C 6 H 4 CH 3 -4, C 6 H 4 CH 3 -3, C 6 H 4 F-3, C 6 H 4 F-4.
Очевидно, что реакции сопровождаются не только окислением сурьмы, но и разрывом связи Sb–C, в реакции принимает участие и гидроксильная, и оксиматная группы.
Интересно отметить, что при взаимодействии три( орто -толил)сурьмы с 2-гидрокси-бензальдоксимом получен 2-гидроксибензальдоксимат три( орто -толил)сурьмы [18].
Иногда реакции окислительного присоединения не требуют дополнительного введения окислителя. Например, трифенилсурьма окисляется хлоридом хлоротиодиазила в дихлорметане с образованием 1,1,1-трифенил-цикло-1λ5-стибио-1,3-дитио-2,4-диазина [21]:
5Ph 3 Sb + 2S 3 N 2 Cl 2
* Ph 3 Sb + 2Ph 3 SbS + 2Ph 3 SbCl 2 + 0.5S 4 N 4
SN
В качестве побочного продукта был выделен аддукт димера дихлорида трифенилсурьмы с тетранитридом тетрасеры [(Ph 3 SbCl 2 ) 2 ∙S 4 N 4 ].
Реакции окислительного присоединения с участием орто -хинонов, которые выступают в качестве окислителей, являются эффективным методом синтеза катехолатов трифенилсурьмы [22]:
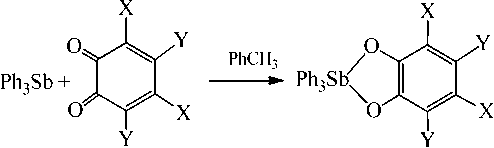
X = Cl, Br, CMe 3 , Y = Cl, Br, H
Позже по этой схеме было синтезировано большое количество катехолатов трифенилсурьмы с различными заместителями в катехолатном цикле [23–30]. В большинстве случаев реакции протекают в мягких условиях без образования побочных продуктов.
Однако при взаимодействии трифенилсурьмы и фенантренхинона-9,10 была получена (фе-нантрен-9,10-диолато)трифенилсурьма(V). Показано, что молекулярный комплекс находится в равновесии с ионным комплексом в растворе толуола [31]:
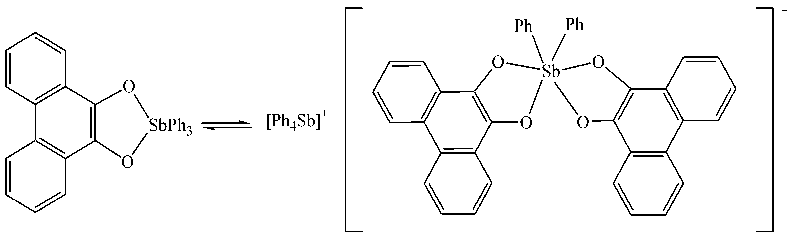
Аналогично синтезирована [4,5-(1,1,4,4-тетраметилбутан-1,4-диил)катехолато]-трифенилсурьма(V), но в отличие от предыдущего случая, превращение в ионный комплекс не является обратимым и протекает только в полярных растворителях, таких как хлороформ и ацетон [32].
Описаны реакции трифенилсурьмы с дибензохинонами, в результате которых выделены биядерные катехолатные комплексы сурьмы. Так, первый дикатехолат трифенилсурьмы получен по реакции окислительного присоединения с 4,4’-ди-(3-метил-6-трет-бутил- о -бензохиноном) при мольном соотношении 2:1 [23]:
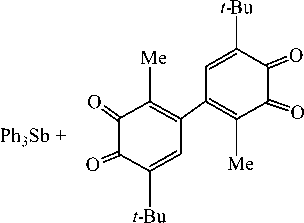
PhCH3
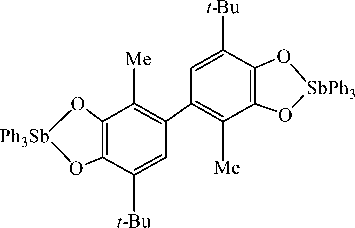
При мольном соотношении 1:1 получен монокатехолат трифенилсурьмы. Однако известны реакции трифенилсурьмы с ди- орто -хинонами, продуктами которых являются дикатехолаты вне зависимости от мольного соотношения реагентов. Например, реакции трифенилсурьмы с ди орто -хиноном, в состав которого входит этиленовый мостик, протекают с образованием дикате-холатов трифенилсурьмы [33]:
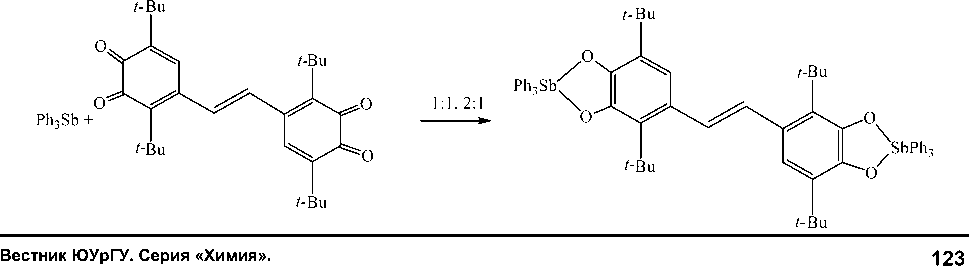
2022. Т. 14, № 2. С. 120–134
Несмотря на то, что реакции окислительного присоединения триарильных соединений сурьмы изучены достаточно хорошо, существуют отдельные реагенты, поведение которых в таких реакциях практически не исследовано. К ним относятся органические соединения с функциональными группами, содержащими атомы водорода с различной подвижностью, такие как ди-гидроксибензойные кислоты.
Установлено, что 2,3- и 2,6- дигидроксибензойные кислоты в реакциях с трифенил-, три( мета -толил)- и три( пара -толил)сурьмой в диэтиловом эфире в присутствии пероксида водорода проявляют себя как монофункциональные соединения: в реакции участвует только карбоксильная группа, при этом гидроксильные группы остаются инертными [34, 35]. Продуктами реакции являются дикарбоксилаты триарилсурьмы:
Ar 3 Sb + 2HOC(O)Ar’ + H 2 O 2 → Ar 3 Sb[OC(O)Ar’] 2 + 2H 2 O
Ar = Ph, p -Tol, m -Tol;
Ar’ = C 6 H 3 (OH) 2 -2,6, C 6 H 3 (OH) 2 -2,3.
Следует отметить, что строение продуктов реакций не зависело от мольного соотношения реагентов (1:2:1 или 1:1:1).
Теоретически реакция трифенилсурьмы с 2,3-дигидроксибензойной кислотой может протекать с образованием замещенного пирокатехолата [35]:
C(O)OH
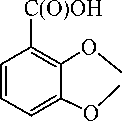
SbPh 3 + 2H 2 O
OH
Ph 3 Sb + + H 2 O 2
OH
Cогласно расчетам методом DFT (теория функционала плотности), энергия образования бис (2,3-дигидроксибензоата) трифенилсурьмы составляет –70,2 ккал/моль, в то время как аналогичное значение для пирокатехолата равно –51,1 ккал/моль. Можно предположить, что образование 2,3-дигидроксибензоата трифенилсурьмы термодинамически более выгодно по причине сохранения в его молекуле системы водородных связей С=О∙∙∙О–Н, как и в структуре 2,3-дигидроксибензойной кислоты, которая разрушилась бы при образовании пирокатехолата и сохранялась в 2,3-дигидроксибензоате трифенилсурьмы.
Показано, что 3,4-дигидроксибензойная кислота в реакции с трифенилсурьмой в присутствии пероксида водорода независимо от мольного соотношения (1:1:1 или 1:2:1) в растворе диэтилового эфира реагирует как дигидроксибензол. Продуктом реакции является тетраядерный макроцикл тетракис ( μ 2 -4-карбоксипирокатехолато-О,О’O’’)- тетракис [трифенилсурьмы(V)] [36]:
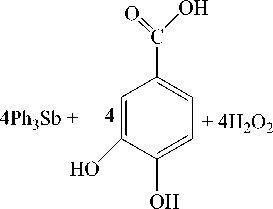
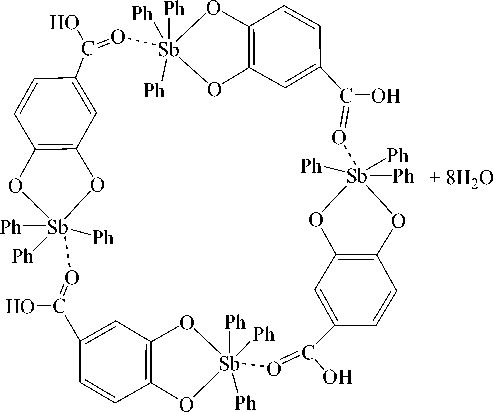
В четырехядерном макроцикле лиганды связаны с атомом сурьмы двумя гидроксильными атомами кислорода, образуя хелатный цикл, а на соседний атом сурьмы координируют атомом кислорода карбонильной группы.
Можно предположить возможность образования других продуктов взаимодействия трифе-нилсурьмы с 3,4-дигидроксибензойной кислотой, например, мономерного соединения 4-карбоксипирокатехолато-О,О’-трифенилсурьмы(V):
Ph 3 Sb + 2
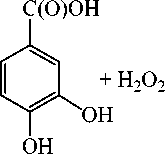
HO(O)C
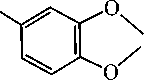
SbPh 3 + 2H 2 O
Или бис (3,4-дигидроксибензоата) трифенилсурьмы:
Ph 3 Sb + 2HOC(O)C 6 H 3 (OH) 2 -3,4 + H 2 O 2 → Ph 3 Sb[OC(O)C 6 H 3 (OH) 2 -3,4] 2 + 2H 2 O.
Согласно DFT-расчетам, энергии образования мономера и бис (3,4-дигидроксибензоата) три-фенилсурьмы очень близки (–58,6 и –56,8 ккал/моль соответственно). При этом образование макроцикла является более энергетически выгодным (–71,8 ккал/моль), поскольку при тетрамериза-ции 4-карбоксипирокатехолато-О,О’-трифенилсурьмы(V) формируются сразу две связи – водородная и координационная Sb∙∙∙O=С, что обеспечивает существенное понижение энергии (∆Е=13 ккал/моль).
При взаимодействии трис (5-бром-2-метоксифенил)сурьмы с 2,6-дигидроксибензойной кислотой вместо ожидаемого дикарбоксилата триарилсурьмы было получено биядерное сурьмаорганическое соединение – μ 2 -оксо- бис [(2,6-дигидроксибензоато) трис (5-бром-2-метоксифенил)сурьма] с мостиковым атомом кислорода, выделенное из реакционной смеси после перекристаллизации из ацетонитрила в форме сольвата:
2 (5-Br-2-MeOC 6 H 3 ) 3 Sb + 2 HO(O)CC 6 H 3 (OH) 2 -2,6 + 2H 2 O 2 →
→ [(5-Br-2-MeOC 6 H 3 ) 3 SbO(O)CC 6 H 3 (OH) 2 -2,6] 2 O + 3H 2 O.
Возможная причина образования продукта иного строения стерические затруднения, создаваемые заместителями в арильных радикалах.
Экспериментальная часть
Синтез сольвата 4-карбоксипирокатехолато-О,О’- трис (5-бром-2-метоксифенил)сурьмы с хлороформом (5-Br-2-MeOC 6 H 3 ) 3 Sb[O,O’C 6 H 3 - COOH-4]∙ 2 CHCl 3 (1).
Смесь 100 мг (0,147 ммоль) трис (5-бром-2-метоксифенил)сурьмы, 45,34 мг (0,294 ммоль) 3,4-дигидроксибензойной кислоты и 19 мг (0,15 ммоль) 70%-ного водного раствора трет бутилгидропероксида в 30 мл диэтилового эфира выдерживали при 20 °С в течение 24 ч. После медленного удаления растворителя получили 118 мг (75 %) бесцветных кристаллов, которые после перекристаллизации из смеси хлороформ–октан (2:1) имели t пл = 198 °C. ИК-спектр, ν , см - 1: 3057, 2999, 2941, 2839, 2665, 2617, 2569, 2524, 2395, 2347, 2135, 1978, 1869, 1793, 1766, 1757, 1676, 1585, 1568, 1494, 1462, 1444, 1373, 1340, 1280, 1249, 1211, 1180, 1143, 1122, 1089, 1047, 1014, 941, 885, 812, 752, 711, 665, 640, 615, 578, 549, 524, 514, 432. Найдено, %: С 33,52; Н 2,35. C 30 H 24 Br 3 Cl 6 O 7 Sb. Вычислено, %: С 33,65; Н 2,26.
ИК-спектр соединения 1 записывали на ИК-спектрометре Shimadzu IR Affinity-1S в таблетках KBr в области 4000–400 см–1.
Элементный анализ проведен на приборе Carlo-Erba 1106.
Рентгеноструктурный анализ (РСА) кристалла 1 проводили на дифрактометре D8 QUEST фирмы Bruker (Mo K α - излучение, λ = 0,71073 Å, графитовый монохроматор) при 296(2) К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [37]. Все расчеты по определению и уточнению структуры выполнены по программам SHELXL/PC [38], OLEX2 [39]. Структура определена пря-
мым методом и уточнена методом наименьших квадратов в анизотропном приближении для неводородных атомов. Кристаллографические данные и результаты уточнения структуры приведены в табл. 1. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (для 1 № 2144306; или . Кристаллографические данные и результаты уточнения структур приведены в табл. 1, основные длины связей и валентные углы – в табл. 2.
Кристаллографические данные, параметры эксперимента и уточнения структуры 1
Основные длины связей ( d ) и валентные углы ( ω ) в структуре 1
Таблица 1
|
Параметр |
1 |
|
Формула |
C 30 H 24 O 7 Br 3 SbCl 6 |
|
М |
1070,67 |
|
Сингония |
Моноклинная |
|
Пр. группа |
P2 1 /n |
|
a , Å |
9,302(2) |
|
b , Å |
21,166(5) |
|
c , Å |
19,517(6) |
|
α, град. |
90,00 |
|
β, град. |
96,302(13) |
|
γ, град. |
90,00 |
|
V , Å3 |
3819,6(17) |
|
Z |
4 |
|
ρ (выч.), г/см3 |
1,862 |
|
µ, мм–1 |
4,323 |
|
F (000) |
2072,0 |
|
Размер кристалла, мм |
0,5 × 0,15 × 0,1 |
|
Область сбора данных по 2θ, град. |
5,86–68,9 |
|
Интервалы индексов отражений |
–14 ≤ h ≤ 14, –33 ≤ k ≤ 33, –30 ≤ l ≤ 30 |
|
Измерено отражений |
142996 |
|
Независимых отражений |
16036 ( R int = 0,1400) |
|
Переменных уточнения |
428 |
|
GOOF |
1,008 |
|
R -факторы по I>2σ (I) |
R 1 = 0,0780, wR 2 = 0,1634 |
|
R -факторы по все отражениям |
R 1 = 0,1894, wR 2 = 0,2017 |
|
Остаточная электронная плотность (max/min), e/Å3 |
1,81/–1,21 |
Таблица 2
|
Связь |
d, Å |
Угол |
ω , град |
|
Sb(1)–O(4) |
2,013(3) |
O(4)Sb(1)O(5) |
78,15(13) |
|
Sb(1)–O(5) |
2,096(4) |
O(4)Sb(1)C(1) |
87,32(16) |
|
Sb(1)–C(1) |
2,152(5) |
O(4)Sb(1)C(11) |
128,92(17) |
|
Sb(1)–C(11) |
2,131(5) |
O(4)Sb(1)C(21) |
102,80(17) |
|
Sb(1)–C(21) |
2,107(5) |
O(5)Sb(1)C(1) |
165,63(16) |
|
Br(1)–C(5) |
1,901(6) |
O(5)Sb(1)C(11) |
85,08(17) |
|
Br(2)–C(15) |
1,900(6) |
O(5)Sb(1)C(21) |
90,62(18) |
|
Br(3)–C(25) |
1,889(6) |
C(11)Sb(1)C(1) |
101,22(18) |
|
C(14)–C(9) |
1,711(13) |
C(21)Sb(1)C(1) |
95,96(19) |
|
C(16)–C(9) |
1,719(14) |
C(21)Sb(1)C(11) |
125,68(19) |
|
C(15)–C(9) |
1,724(13) |
C(2)O(1)C(7) |
120,4(5) |
|
O(1)–C(2) |
1,363(7) |
C(33)O(4)Sb(1) |
114,0(3) |
Обсуждение результатов
В настоящей работе исследовано взаимодействие трис (5-бром-2-метоксифенил)сурьмы с 3,4-дигидроксибензойной кислотой в присутствии гидропероксида третичного бутила в эфире. Показано, что единственным сурьмаорганическим продуктом указанной реакции является замещенный пирокатехолат трис (5-бром-2-метоксифенил)сурьмы, выделенный из реакционной смеси после перекристаллизации из смеси хлороформ-октан в виде сольвата с хлороформом ( 1 ⋅ 2CHCl 3 ):
C(O)OH
Et2O O C(O)OH
(5-Br-2-MeOC6H3)3Sb + 2 + t -BuOOH 2 (5-Br-2-MeOC 6H3)3Sb
OH O
OH
В ИК-спектре соединения 1 присутствует интенсивная полоса поглощения при 432 см–1, относящаяся к колебаниям Sb–C. Согласно справочным данным, карбонильные полосы поглощения карбоновой кислоты находятся при 1670 см–1 [40,41], что сопоставимо с наблюдаемой в ИК-спектре соединения 1 полосой при 1676 см–1. Для 3,4-дигидроксибензойной кислоты полоса колебаний гидроксильных групп (3200 см–1) является характеристической, но в ИК-спектре синтезированного соединения 1 эта полоса отсутствует.
По данным РСА, в соединении 1 атом сурьмы имеет искаженную тригонально-бипирамидальную координацию с одним из атомов кислорода пирокатехолатного лиганда в аксиальном положении (рис. 1).
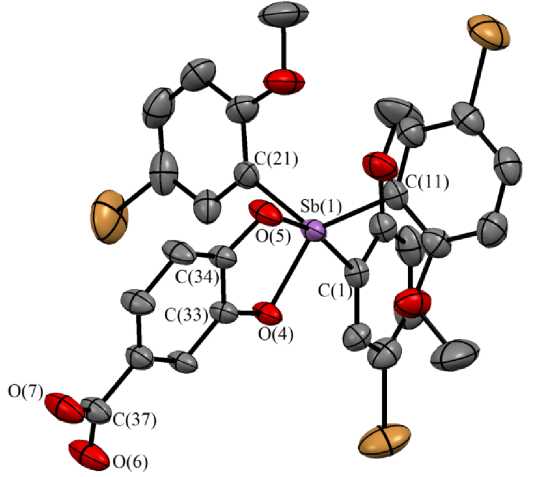
Рис. 1. Общий вид молекулы 1
(атомы водорода и молекула сольватного хлороформа не показаны)
Длины связей Sb–С в 1 изменяются в интервале 2,107(5)–2,131(5) Å, что близко к сумме ковалентных радиусов атомов сурьмы и углерода 2,12 Å [43]. Длины связей Sb–O неравноценны (2,095(4) и 2,013(3) Å), но близки к сумме ковалентных радиусов атомов сурьмы и кислорода 2,05 Å [43]. Экваториальные углы СSbC равны 95,9(2)–125,7(1)º, аксиальный угол O(5)Sb(1)C(1) составляет 165,6(2)º, что отличается от стандартной величины в идеальной тригональной бипирамиде. В кристалле 1 присутствуют тесные контакты атомов водорода хлороформа с атомами кислорода катехолатного лиганда (2,40 Å) и атома водорода катехолатного лиганда с атомами хлора молекул хлороформа (2,95 Å). В кристаллах соединение 1 находится в виде димеров, где две мо- лекулы связываются между собой двумя водородными связями O(6)∙∙∙H(7) (1,864 Å) при сумме ван-дер-ваальсовых радиусов водорода и кислорода 2,57 Å (рис. 2) [43].
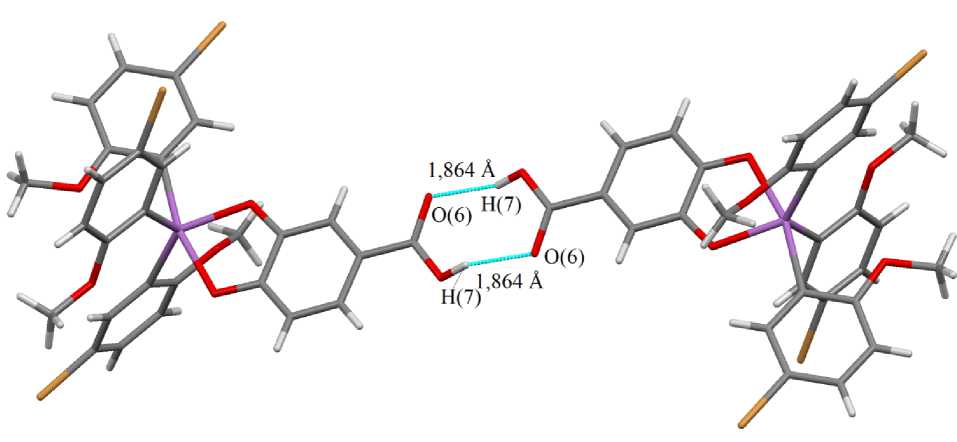
Рис. 2. Внутримолекулярные водородные связи в кристалле соединения 1 (молекула сольватного хлороформа не показана)
Выводы
Строение продукта реакции триарилсурьмы с дигидроксибензойными кислотами обусловливается как строением кислоты (расположение гидроксильных групп в бензольном кольце), так и природой арильного радикала: трис (5-бром-2-метоксифенил)сурьма реагирует с 2,6-дигидроксибензойной кислотой с образованием биядерного сурьмаорганического продукта с мостиковым атомом кислорода; 3,4-дигидроксибензойная кислота в реакции с трис (5-бром-2-метоксифенил)сурьмой выступает в качестве дигидроксибензола.
Выражаю признательность профессору В.В. Шарутину за помощь в работе над публикацией и рентгеноструктурный анализ кристалла соединения 1 .
Список литературы Реакция окисления трис[(2-метокси)(5-бром)фенил]сурьмы трет-бутилгидропероксидом в присутствии 3,4-диоксибензойной кислоты
- Brief Note Improved Methods for the Synthesis of Antimony Triacetate, Triphenylantimony Di-acetate, and Pentaphenylantimony / T.C. Thepe, R.I. Garascia, M.A. Selvoski, A.N. Pattel // Ohio S. Sci. -1977. - V. 77, № 3.- P. 134-135.
- Гущин, А.В. Синтез и строение диметакрилата триметилсурьмы / А.В. Гущин, Е.А. Лаханина, П.В. Андреев // Журн. общ. химии. - 2017. - Т. 87, № 11. - С. 1856-1859. DOI: 10.1134/S1070363217110135
- Синтез, строение акрилата тетрафенилсурьмы и введение его в полиметилметакрилат // A.В. Гущин, Д.В. Шашкин, Т.С. Щербакова, Н.В. Сомов, ЕВ. Баранов, Г.К. Фукин, АС. Шавы-рин, В.И. Рыкалин, В.А. Додонов // Вестник ННГУ. - 2010. - № 6. - С. 68-72.
- One-step Synthesis of Pentavalent Triphenylantimony Derivatives Ph3Sb(OSiR3)2, Ph3Sb(OCH2CH2)2NH and Ph3Sb(OCH2CH2NMe2)2: X-ray Molecular Structure of Ph3Sb(OSiMe3)2 / E.Y. Ladilina, V.V. Semenov, G.K. Fukin, A.V.Gushchin, V.A. Dodonov, I.V. Zhdanovich, J.-P. Finet // J. Organomet. Chem. 2007. - V. 692, № 26. - P. 5701-5708.
- Синтез и строение бис(2,5-диметилбензолсульфоната) три(орто-толил)сурьмы / B.В. Шарутин, О.К. Шарутина, В.С. Сенчурин, М.К. Карцева // Вестник ЮУрГУ. Серия «Химия». - 2017. - Т. 9, № 3. - С. 71-75.
- Синтез и строение 2,4,6-трихлорфеноксидов тетра- и трифенилсурьмы / В.В. Шарутин, О.К. Шарутина, В.С. Сенчурин, А.О. Щелоков // Журн. общ. химии. - 2016. - Т. 86, № 1. -С.92-99.
- Шарутин, В.В. Синтез и строение салицилальдоксиматов тетра- и трифенилсурьмы / B.В. Шарутин,О.К. Шарутина, О.В. Молокова // Журн. неорган. химии. - 2012. - Т. 57, № 6. - C. 902-907.
- Шарутин, В.В. ц2-Оксо-бис[(2,5-динитрофеноксо)триарилсурьма]. Синтез, строение, реакции с пентаарилсурьмой / В.В. Шарутин, О.К. Шарутина, А.Н. Ефремов // Коорд. химия. -2020. -T. 46, № 1. - С. 45-55.
- Додонов, В.А. Реакции трифенилсурьмы с а-диолами в присутствии гидропероксида третичного бутила / В.А. Додонов, С.Н. Забурдяева, Н.Н. Невкина // Металлоорг. хим. - 1989. - Т. 2, № 6. - C. 1296-1297.
- Синтезы производных сурьмы (V) из триметил- и трифенилсурьмы (III), двухатомных фенолов и гидропероксида третичного бутила / В.А. Додонов, А.Ю.Фёдоров, Р.И. Усятинский, С.Н. Забурдяева, А.В. Гущин // Изв. АН. Сер. хим. - 1995. - № 4. - С. 748-751.
- Шарутин, В.В. Синтез и строение дифталата трифенилсурьмы / В.В. Шарутин, О.К. Шарутина, В.С. Сенчурин // Журн. неорган. химии. - 2014. - Т. 59, № 9. - С. 1178-1181.
- Characterising Secondary Bonding Interactions within Triaryl Organoantimony(V) and Organo-bismuth(V) complexes / H. Baruchki, S.L. Coles, J.F. Costello, T. Gerbish, M.B. Hursthouse // Dalton Trans. - 2000. - № 14. - P. 2319-2325.
- Синтез, строение и реакции соединений сурьмы (Ar3SbX)2O, X=Hal, NO2, NO3, OSO2R, OC(O)R', OAr' / В.В. Шарутин, А.П. Пакусина, О.К. Шарутина, Н.В. Насонова, А.В. Герасименко, М.А. Пушилин // Химия и компьютерное моделирование. Бутлеровские сообщения. - 2002. -Т. 3, № 11. - С. 13-22.
- Новый метод синтеза бис-ц-[(метилендициклопентанон-2,2'-диоксимато)-трифенил-сурьмы] / В.В. Шарутин, О.В. Молокова, О.К. Шарутина, Т.И. Акимова // Журн. общ. химии. -2009. - Т. 79, № 8. - С. 1297-1300.
- Синтез и строение бис-ы-[(метилендициклопентанон-2,2'-диоксимато)трифенилсурьмы] / В.В. Шарутин, О.В. Молокова, О.К. Шарутина, Е.А. Алябова, Ю.А. Кухарев, Т.И. Акимова, М.А. Пушилин // Коорд. химия. - 2005. - Т. 31, № 3. - С. 172-176.
- Синтез и строение 6,6,6-трифтор-3-гексанон-5,5-диолатотрифенилсурьмы / В.В. Шарутин, А.П. Пакусина, О.К. Шарутина, Т.С. Почекутова // Журн. неорган. химии. -2008. - Т. 53, № 11. - С. 1857-1860.
- The One Stage Synthesis and Crystal Structure of 5,5,5-Trifluoro-2-pentanone-4,4-diolato-triphenylantimony(V) / A.V. Gushchin, R.I. Usyatinsky, G. K. Fukin, V. A. Dodonov // Main Group Chem. -1998. - V. 2, № 3. - P. 187-190.
- The Peculiarities of Tri(o-tolyl)antimony and Tri(m-tolyl)-antimony Reactions with 2-hydroxybenzaldoxime. The Molecular Structures of Tri(o-tolyl)antimony 57s(2-hydroxybenzaldoximate) and 575(^3-2-hydroxybenzaldoximato-O,O',N)-(^2-oxo)-6/5[di(m-tolyl)antimony] / V.V. Sharutin, O.K. Sharutina, E.V. Artem'eva, M.S. Makerova // Bulletin of the South Ural State University. Ser. Chemistry. - 2014. - V. 6, № 2. - P. 5-14.
- Шарутин, В.В. Особенности взаимодействия трис(5-бром-2-метоксифенил)сурьмы с 2-оксибензальдоксимом. Строение бис(ы3-2-оксибензальдоксимато-О,О',№)-(ы2-оксо)-бис(5-бром-2-метоксифенил)дисурьмы / В.В. Шарутин, О.К. Шарутина // Журн. неорган. химии. - 2014. -Т. 59, № 11. - С. 1507-1511.
- Синтез и строение бис^и^-оксибензальдоксимато-О^'^-^-оксо^тетракис^-толил)дисурьмы, -тетракис(3-фторфенил)дисурьмы и -тетракис(4-фторфенил)дисурьмы / В.В. Шарутин, О.К. Шарутина, А.Н. Ефремов, Е.В. Артемьева // Журн. неорган. химии. - 2019. -Т. 64, № 5. - С. 482-489.
- Uber die Reaktion von SbPh3 mit S3N2Cl2 Kristallstrukturen von [Ph3SbSNSN] und [(Ph3SbCl2)2-S4N4] / F. Kunkel, K. Harms, H.-C. Kang, W. Massa, K. Dehnicke // Z. Naturforsch. -1997.- V. 52 b. - 193-198.
- Tetraarylbutyldimethylantimony - a New Sb Source for Low-temperature Organometallic Vapor Phase Epitazial Growth of In Sb / C.H. Chen, G.B. Stringfellow, D.C. Gordon et al. // Appl. Phys. Lett. - 1992. - V. 61, № 2. - P. 204-206.
- Oxidative Addition Reaction of o-quinones to Triphenylantimony. Novel Triphenylantimony Catecholate Complexes / V.K. Cherkasov, E.V. Grunova, A.I. Poddel'sky, G.K. Fukin // J. Organomet. Chem. - 2005. - V. 690, № 5. - P. 1273-1281.
- Hexacoordinate Triphenylantimony(V) Complex with Tridentate Bis-(3,5-di-tert-butyl-phenolate-2-yl)-amine Ligand. Synthesis, NMR and X-ray Study / A.I. Poddel'sky, N.V. Somov, Yu.A. Kurskii, V.K. Cherkasov // J. Organomet. Chem. - 2008. - V. 693, № 21-22. - P. 3451-3455.
- The Binuclear Trimethyl/triethylantimony(V) Bis-catecholate Derivatives of Four-electron Reduced 4,4'-Di-(3-methyl-6-iert-butyl-o-benzoquinone) / A.I. Poddel'sky, N.V. Somov, N.O. Druzhkov, V.K. Cherkasov // J. Organomet. Chem. - 2011. - V. 696, № 2. - P. 517-522.
- Cyclic Endoperoxides Based on Triphenylantimony(V) Catecholates: The Reversible Binding of Dioxygen / G.A. Abakumov, V.K. Cherkasov, E.V. Grunova et al. // Doklady Chemistry. - 2005. -V. 405. - P. 222-225.
- New Dioxygen-inert Triphenylantimony(V) Catecholate Complexes Based on o-Quinones with Electron-withdrawing Groups / A.I. Poddel'sky, I.V. Smolyaninov, A.Yu. Kurskii et al. // Russ. Chem. Bull. - 2009. - V. 58. - P. 532-537.
- Redox Transformations and Antiradical Activity of Triarylantimony(V) 3,6-Di-tert-butyl-4,5-dimethoxycatecholates / I.V. Smol'yaninov, A.I. Poddel'skii, S.A. Smol'yaninova, N.O. Movchan // Russ. J. Gen. Chem. - 2014. - V. 84, № 9. - P. 1523-1529.
- Triarylantimony(V) Catecholates - Derivatives of 4,5-Difluoro-3,6-di-tert-butyl-obenzoquinone / A.I. Poddel'sky, I.V. Smolyaninov, G.K. Fukin et al. // J. Organomet. Chem. - 2016. - V. 824, № 1. -P. 1-6.
- 3,6-Di-tert-butylcatecholates of Trialkyl/triaryl-antimony(V) / A.I. Poddel'sky, I.V. Smolyaninov, G.K. Fukin et al. // J. Organomet. Chem. - 2018. - V. 867, № 15. - P. 238-245.
- Triphenylantimony(V) Catecholates and o-Amidophenolates: Reversible Binding of Molecular Oxygen / V.K. Cherkasov, G.A. Abakumov, E.V. Grunova et al. // Chem. Eur. J. - 2006. - V. 12. -P. 3916-3927.
- Antimony(V) Catecholato Complexes Based on 5,5,8,8-Tetramethyl-5,6,7,8-tetrahydronaphthalenequinone-2,3. Crystal Structure of [Ph4Sb]+[Ph2Sb(Cat)2]- / A.I. Poddel'sky, I.V. Smolyaninov, N.V. Somov et al. // J. Organomet. Chem. - 2010. - V. 695, № 4. - P. 530-536.
- New Bis--o-benzoquinoid Ligands with Ethylene Bridge and their Metal Complexes. Synthesis, Spectroscopy and X-ray Study / A.I. Poddel'sky, A.V. Piskunov, N.O. Druzhkov et al. // Z. Anorg. Allg. Chem. - 2009. - V. 635. - P. 2563-2571.
- Синтез и строение бис(дигидроксибензоатов) триарилсурьмы / В.В. Шарутин, О.К. Ша-рутина, Ю.О. Губанова, А.С. Фоминых // Журн. общ. химии. - 2020. - Т. 90, № 1. - С. 136-142.
- Пупкова, Ю.О. Особенности взаимодействия пентаарилсурьмы и триарилсурьмы с полифункциональными карбоновыми кислотами: дис. ... канд. хим. наук: 02.00.08 / Ю.О. Пупкова. -Челябинск, 2021. - 127 с.
- Synthesis and Structure of a New Tetranuclear Macrocyclic Antimony(v) Complex / V.V. Sha-rutin, O.K. Sharutina, Y.O. Gubanova et al. // Mendeleev Commun. - 2020. - V. 30, № 6. - P. 97-99.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures From Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: a Complete Structure Solution, Refinement and Analysis Program / O.V. Dolomanov, L.J. Bourhis, R.J. Gildea et al. // J. Appl. Cryst. - 2009. - V. 42. - P. 339-341. DOI: 10.1107/S0021889808042726.
- Тарасевич, Б.Н. ИК-спектры основных классов органических соединений / Б.Н. Тарасевич. - М.: МГУ, 2012. - 54 с.
- Инфракрасная спектроскопия органических и природных соединений: учебное пособие / А.В. Васильев, Е В. Гриненко, А.О. Щукин и др. - СПб.: СПбГЛТА, 2007. - 54 с.
- Covalent Radii Revisited / B. Cordero, V. Gómez, A.E. Platero-Prats et al. // Dalton Trans. -2008. - Iss. 21. - P. 2832-2838. DOI: 10.1039/B801115J.
- Consistent Van der Waals Radii for the Whole Main Group / M. Mantina, A.C. Chamberlin, R. Valero et al. // J. Phys. Chem. A. - 2009. - V. 113, iss. 19. - P. 5806-5812. DOI: 10.1021/jp8111556.

![Реакция окисления трис[(2-метокси)(5-бром)фенил]сурьмы трет-бутилгидропероксидом в присутствии 3,4-диоксибензойной кислоты Реакция окисления трис[(2-метокси)(5-бром)фенил]сурьмы трет-бутилгидропероксидом в присутствии 3,4-диоксибензойной кислоты](/file/cover/147237501/reakcija-okislenija-tris-2-metoksi-5-brom-fenil-surmy-tret-butilgidroperoksidom-v.png)
