Регуляция транскапиллярного обмена пульсовым давлением крови звена микрогемоциркуляции
Автор: Багаев С.Н., Захаров В.Н., Орлов В.А., Панов С.В., Ратушняк А.С., Запара Т.А.
Журнал: Российский журнал биомеханики @journal-biomech
Статья в выпуске: 3 (41) т.12, 2008 года.
Бесплатный доступ
Исследуются физические механизмы транскапиллярного обмена живого организма. Объектом исследования являются лабораторные животные, а в качестве экспериментальных средств используются оригинальные лазерный и электрофизиологический методы.
Микроциркуляция крови, обмен веществ, систолическое давление, диастолическое давление, пульсовое давление
Короткий адрес: https://sciup.org/146215931
IDR: 146215931 | УДК: 531/534:
Текст научной статьи Регуляция транскапиллярного обмена пульсовым давлением крови звена микрогемоциркуляции
Актуальность решения проблемы микроциркуляции крови и транскапиллярного обмена обусловлена тем, что традиционные представления о функционировании звена микрогемоциркуляции являются противоречивыми. Исследования в этой области в основном имели морфологическую направленность. Применение световой и электронной микроскопии способствовало накоплению знаний о строении микрососудов системы кровообращения. При этом изучению физических механизмов микроциркуляции крови и транскапиллярного обмена не было уделено должного внимания. Согласно традиционным представлениям газообмен и обмен веществ осуществляется за счет молекулярной физической диффузии. Этот процесс медленный и не может за короткое время, в течение которого кровь находится в капилляре, осуществить газообмен и обмен веществ.
Считают, что в просвет капилляра постоянно проникает углекислый газ, понижающий рН крови, обеспечивая биохимические условия для выхода кислорода из эритроцитов. В этой последовательности событий, которые должны происходить за короткое время, нет условий для переноса кислорода из капилляров в интерстициальное пространство. В такой модели через стенку капилляра одновременно с противоположным направлением транспортируются кислород и углекислый газ. Эти процессы рассматривались на протяжении одиночного капилляра [4, 5]. В настоящей работе представлены результаты экспериментальных исследований, направленных на выявление физических механизмов газообмена и обмена веществ в функционировании звена микрогемоциркуляции.
Оригинальные методы и результаты исследований
Методологический подход, примененный авторами, предусматривал исследование преемственных связей в функционировании сердца, магистральных кровеносных сосудов и микрососудистого русла. Обнаружение таких связей на системном уровне необходимо для более полного раскрытия механизмов, ответственных за газообмен и обмен веществ. Основанием к такому подходу исследований являются фундаментальные результаты авторов в области биомеханики кровообращения.
Использование рентгеноконтрастного метода визуализации потоков крови в кровеносном русле привело к обнаружению явления образования винтового потока крови в сердечно-сосудистой системе человека и животных [7, 8]. Изучение этого явления позволило:
-
• обосновать активную роль артерий в поддержании винтового движения крови за счет сокращения спирально упакованных мышечных элементов кровеносных сосудов [2];
-
• раскрыть природу диастолического артериального давления, связанного с энергией вращательного компонента движения крови и направленного на преодоление сосудистого сопротивления [2];
-
• установить законы ветвления кровеносных сосудов, определяющих связь морфометрических и динамических параметров кровотока в окрестности узлов сосудистых бифуркаций [1].
Для неинвазивного изучения микроциркуляции крови и транскапиллярного обмена на живых объектах использовалась специально разработанная прецизионная лазерная установка. Она позволяет измерять малые перемещения и скорости микрообъектов на основе применения оригинального фазочувствительного лазерного метода спектроскопии светового рассеяния. Принцип работы этой установки и результаты, полученные с ее помощью, изложены в работах авторов [3, 6]. Применение лазерного метода в исследовании биомеханики микроциркуляции крови привело к обнаружению явления локальных высокочастотных поперечных перемещений стенок артериол и венул [3, 6]. Изучение этого явления позволило:
-
• установить связь локальных высокочастотных перемещений стенок микрососудов с сокращением гладкомышечных клеток артериол и венул;
-
• обнаружить линейную зависимость частоты колебаний стенок микрососудов со скоростью кровотока в них;
-
• предложить описание механизма газообмена, основанного на изменении рН крови при сокращении гладкомышечных клеток артериол.
С целью изучения биоэлектрических процессов, сопровождающих микроциркуляцию крови и транскапиллярный обмен, использовался аппаратнопрограммный комплекс для регистрации электрических сигналов от одиночных гладкомышечных клеток артериол и венул, а также от стенок капилляров. Он позволил на клеточном уровне производить локальные измерения мембранных электрических потенциалов от гладкомышечных клеток стенок артериол и венул. Схема электрофизиологической установки представлена на рис. 1. Созданное устройство включает: регистрирующий электрод (Э), усилитель (У), аналогово-цифровой преобразователь (АЦП), вычислительный комплекс (ВК), визуализатор аналогового сигнала (В).
В экспериментальных условиях исследовались электрические процессы в стенках микрососудов перепонок шпорцевых лягушек, у которых дыхание преимущественно кожное. Для того чтобы обеспечить дыхание животного, достаточно было сохранять влажность ее кожных покровов путем смачивания их физиологическим
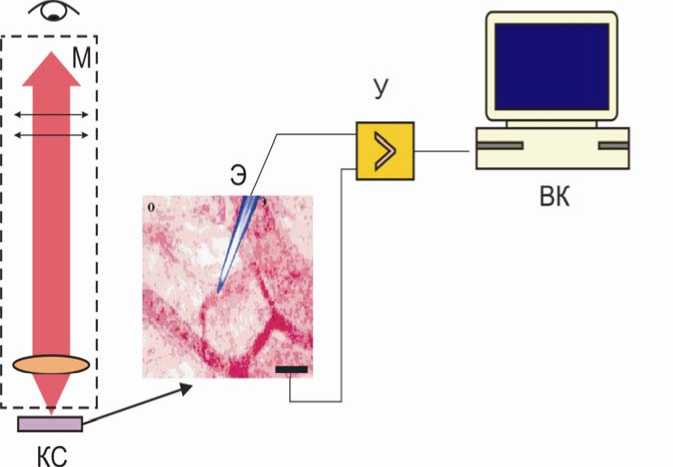
Рис. 1. Установка для электрофизиологических исследований: М – микроскоп;
КС – координатный стол с микрообъектом; У – усилитель-преобразователь;
ВК – вычислительный комплекс раствором. Полное обездвиживание лягушек достигалось внутримышечным введением раствора ардуана по расчетной схеме дозировки препарата. При этом наступала полная релаксация скелетной мускулатуры на период до 90 минут, а сердечная деятельность и функция гладкой мускулатуры сохранялись. Обездвиженный живой объект фиксировался и помещался в экспериментальную камеру. Проведение таких экспериментов на млекопитающих затруднительно, поскольку необходима искусственная вентиляция легких, которая сопровождается значительными механическими помехами.
Идентификация изучаемого микрососуда (артериола, капилляр, венула) перепонки и подведение к нему электрода осуществлялись с помощью микроскопа. Отведение электрических потенциалов производили с помощью стеклянных электродов-микропипеток с диаметром концевой части менее 1 мкм, заполненных 0,95% физиологическим раствором с сопротивлением 5–30 мОм. Регистрировались колебания интегрального экстраклеточного потенциала и мембранные потенциалы от гладкомышечных клеток стенок артериол и венул, а также от эндотелия стенок капилляров системы кровообращения. Позиционирование отводящих электродов и обеспечение их непосредственного контакта со стенкой микрососуда проводили под визуальным контролем с помощью микроманипуляторов Carl Zeiss . Сигнал усиливался с помощью стандартного экстраклеточного усилителя. В качестве индифферентного электрода использовали хлоро-серебряный прессованный электрод, помещенный в омывающий 0,95% физиологический раствор. Усиленный аналоговый сигнал переводили в цифровую форму с помощью АЦП ( L - card L 1250), регистрировали и обрабатывали с помощью вычислительного комплекса.
Проведены электрофизиологические опыты для получения данных о наличии электрических сигналов от одиночных гладкомышечных клеток микрососудов, сопровождающих их сокращения. Такие измерения выполнены на артериолах, капиллярах и венулах в условиях прямого контакта микроэлектрода со стенкой микрососуда. От всех микрососудов получены сигналы, связанные с процессами
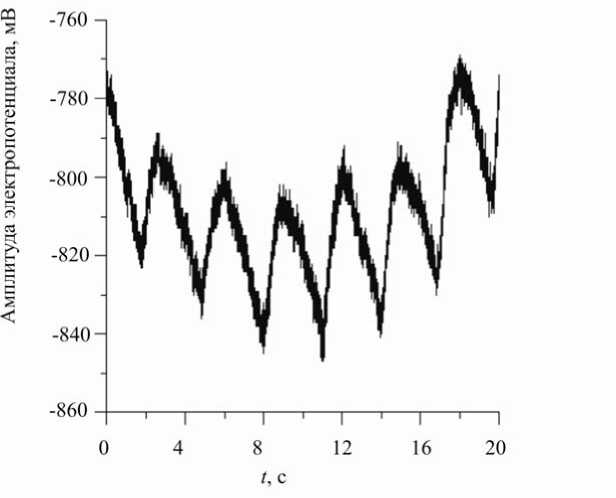
Рис. 2. Вариации электропотенциала на стенке артериолы сокращения гладкомышечных элементов. Зарегистрированные вариации сигнала указывают на сложный немонотонный характер наблюдаемого электрического потенциала, в котором наряду с медленными процессами с периодами длительностью 3–4 с существуют также и быстрые процессы с периодами Т = 10-1–10-2 с (рис. 2). Медленные квазипериодические колебания с большой амплитудой 50–200 мВ характеризуются передним крутым и задним пологим фронтами. С одной стороны, временные характеристики медленных колебаний с периодичностью, равной сердечным сокращениям, показали, что их происхождение связано с пульсовым давлением крови. С другой стороны, наблюдаемый факт требовал объяснения функциональной роли пульсового давления крови в микрососудистом русле, поскольку при микроциркуляции не наблюдается изменения скорости кровотока в артериолах, капиллярах и венулах на протяжении всего периода сердечного цикла. Действительно, прямые наблюдения кровотока в микрососудах с помощью микроскопа и результаты лазерных измерений показывают, что в звене микрогемоциркуляции кровь движется с постоянной скоростью.
Значение скорости может медленно изменяться во времени в зависимости от физиологического состояния организма, когда изменяется частота сердечных сокращений и минутный объем кровообращения. Отсутствие пульсирующего кровотока в микрососудах объясняется тем, что энергия пульсового давления, передающегося со скоростью звука в среде от сердца и магистральных артерий в микрососуды, полностью затрачивается на растяжение эластичных стенок артериол, капилляров и венул.
Прямым доказательством того, что импульсная часть давления затрачивается на растяжение упругих стенок микрососудов, являются экспериментальные данные, полученные с помощью неинвазивного высокочувствительного лазерного метода. Лазерным методом в отличие от электрофизиологического регистрировались не электрические потенциалы, а локальные радиальные механические перемещения стенок микрососудов. Ранее авторами наблюдались только высокочастотные перемещения стенок микрососудов, связанные с сокращениями их гладкомышечных элементов [3, 6]. Специально поставленными опытами с использованием лазерного
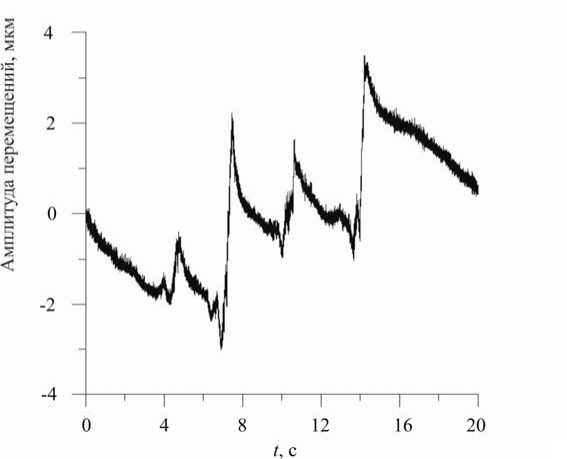
Рис. 3. Вариации амплитуды локальных перемещений метода медленные перемещения стенок микрососудов также были обнаружены и зарегистрированы (рис. 3).
Важно отметить, что амплитуды быстрых осцилляций, зарегистрированные и тем и другим методами, имеют один и тот же 10% уровень по отношению к медленным пульсациям, а их частоты находятся в одном и том же спектральном диапазоне (рис. 4, 5). Это указывает на то, что высокочастотные колебания стенок микрососудов, обнаруженные лазерным и электрофизиологическим методами, имеют одно и то же происхождение, связанное с сокращением отдельной гладкомышечной клетки. Поскольку полуширина спектральной плотности механических деформационных колебаний несколько шире электрических, это указывает на то, что последние являются следствием первых. Аналогичные измерения по регистрации медленных пульсовых колебаний с использованием двух методик проведены также на капиллярах и венулах. Таким образом, сочетание лазерного и электрофизиологического методов привело к обнаружению явления наведенного биоэлектричества на стенках микрососудов при их деформациии. Изучение этого явления позволило:
-
• обнаружить связь наведенных электрических сигналов с ритмом сердечных сокращений;
-
• установить связь электрических сигналов, регистрируемых на микрососудах, с механическими перемещениями их стенок, обусловленных пульсовой волной давления крови.
Изучение механизмов транспортной функции сердечно-сосудистой системы, а также исследования микроциркуляции крови и транскапиллярного обмена лазерным и электрофизиологическим методами позволили авторам по-новому показать функциональные преемственные связи различных отделов системы кровообращения.
Для понимания биомеханики сердца и крупных магистральных сосудов основополагающее значение имеет явление образования винтового потока крови в сердечно-сосудистой системе человека и животных [7, 8], а для биомеханики звена микрогемоциркуляции – явление локальных поперечных перемещений стенок микрососудов в акустическом диапазоне частот [3, 6]. Энергия вращательного компонента винтового потока крови обеспечивает существование распределенного диастолического градиента давления в артериях, направленного на преодоление периферического сопротивления потоку крови, и создает равномерное движение крови
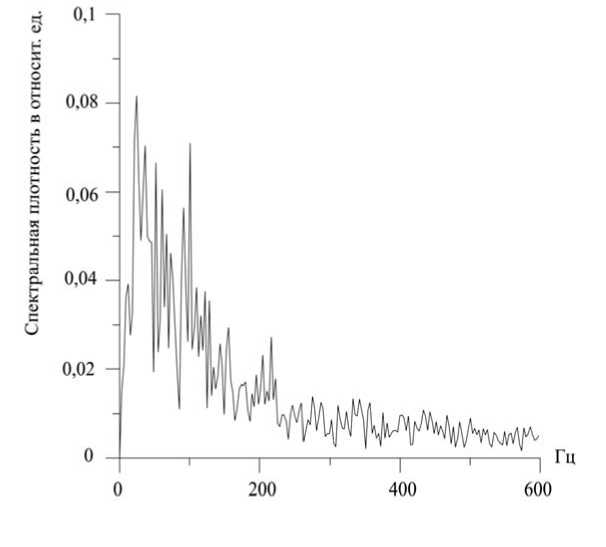
Рис. 4. Спектр механических локальных перемещений артериолы
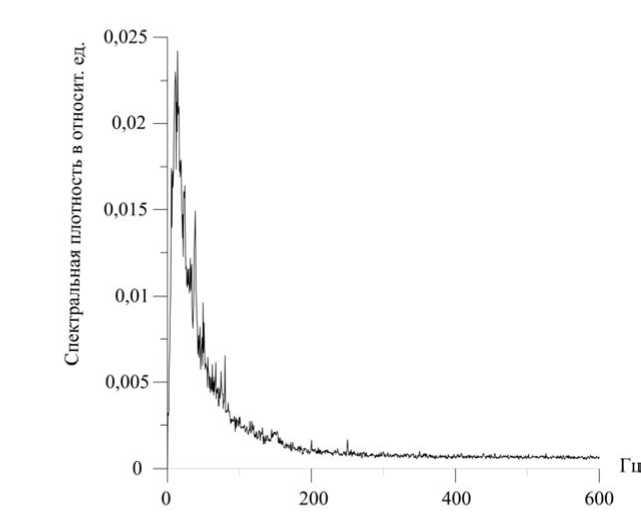
Рис. 5. Спектр электрического потенциала гладкомышечной клетки артериол в звене микрогемоциркуляции (рис. 6). Импульсное, пульсовое давление крови, связанное с сердечным выбросом и равное разности систолического и диастолического артериального давления, проникает в звено микрогемоциркуляции со скоростью звука, затрачивается на растяжение стенок микрососудов, запускает в них высокочастотные сокращения гладкомышечных клеток и реализует главнейший процесс жизнедеятельности организма – транскапиллярный обмен.
Проведенный анализ полученных результатов показывает, что регуляция транскапиллярного обмена осуществляется автоматически пульсовым давлением крови. В момент сердечного выброса в протяженном кровеносном русле возникает прирост давления крови, величина которого в начале артериального русла максимальна, а в капиллярах уменьшается вдвое. Данный быстрый импульсный прирост давления не приводит к изменению убывающего градиента диастолического давления, сохраняющего равномерность кровотока в микрососудистом русле, а аккумулируется в энергии упругой деформации стенок микрососудов при их растяжении.
При изменении давления в капиллярах от максимального до минимального значений энергия импульсной составляющей систолического артериального давления крови активно расходуется на обеспечение транскапиллярного обмена. Когда давление крови в артериальной сети капилляров превышает уровень интерстициального давления, кислород и питательные вещества направленно поступают из артериальных ветвящихся капилляров в интерстициальное пространство. Когда давление крови в венозной сети капилляров ниже интерстициального давления, углекислый газ и продукты метаболизма поступают из интерстициального пространства в венозные сходящиеся капилляры. Эти два процесса разнесены не только во времени, но и в пространстве. Существует разделение функций артериальной и венозной сетей капилляров. Наряду с этим импульсное давление крови возбуждает гладкомышечные клетки артериол, которые сокращаются в акустическом диапазоне частот. Предполагается, что при сокращении гладкомышечных элементов артериол происходит поступление ионов водорода в их просвет, источником которых является биохимическое превращение АТФ, в результате чего понижается pH плазмы крови и создаются необходимые условия для выделения кислорода из эритроцитов непосредственно в артериолах.
Интенсивность газообмена и обмена веществ регулируется по запросу тканей и клеток нейрогуморальными механизмами, изменяющими частоту сердечных сокращений, скорость кровотока и минутный объем кровообращения для обеспечения
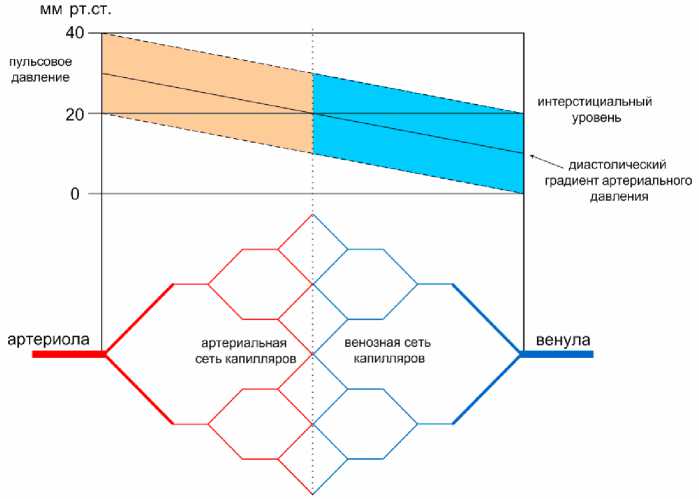
Рис. 6. Вариации давления крови в капиллярном русле: вверху – показатели давления, внизу – схематическое изображение микрососудистого русла системы кровообращения необходимого, должного уровня газообмена и обмена веществ в конкретных физиологических условиях жизнедеятельности организма.
Заключение
Проведение электрофизиологических исследований звена микрогемоциркуляции явилось важным дополнением в изучении транспортной функции сердечно-сосудистой системы в целом. Эти исследования позволили обосновать роль пульсовой волны давления крови в транскапиллярном обмене и разделении функций артериальных и венозных капилляров и предложить новую концепцию функциональной организации, регуляции и управления транскапиллярным обменом.
Список литературы Регуляция транскапиллярного обмена пульсовым давлением крови звена микрогемоциркуляции
- Багаев, С.Н. Законы ветвления кровеносных сосудов/С.Н. Багаев, В.Н. Захаров, В.А. Орлов//Российский журнал биомеханики. -2002. -Т. 6, № 4. -С. 13-29.
- Багаев, С.Н. О необходимости винтового движения крови/С.Н. Багаев, В.Н. Захаров, В.А. Орлов//Российский журнал биомеханики. -2002. -Т. 6, № 4. -С. 30-50.
- Багаев, С.Н. Исследование физических механизмов микроциркуляции крови и транскапилллярного обмена с использованием фазочувствительного лазерного метода/С.Н. Багаев, В.Н. Захаров, В.А. Орлов, С.В. Панов, Ю.Н. Фомин//Российский журнал биомеханики. -2006. -Т. 10, № 3. -С. 22-40.
- Камкин, А.Г. Фундаметальная и клиническая физиология/под ред. А.Г. Камкина и А.А. Каменского. -М.: Издательский центр «Академия», 2004.
- Чернух, А.М. Микроциркуляция/А.М. Чернух, П.Н. Александров, О.В. Алексеев. -М.: Медицина, 1975.
- Bagayev, S.N. Investigation of transcapillary exchange by the laser method/S.N. Bagayev, Yu.N. Fomin, V.A. Orlov, S.V. Panov, V.N. Zakharov, M.G. Metyolkin//Laser Physics. -2005. -Vol. 15, No. 9. -P. 1292-1298.
- Zakharov, V.N. The new conception of blood microcirculation mechanics/V.N. Zakharov//Cardiovascular Engineering. -1998. -Vol. 3, No. 2. -P. 100-104.
- Zakharov, V.N. New principles of circulation mechanics/V.N. Zakharov//European Journal for Cardiac Interventions. -1995. -Vol. 4, No. 1. -P. 3-13.


