Реваскуляризация миокарда в условиях вспомогательного искусственного кровообращения у пациентов с высокой степенью риска
Автор: Зотов Александр Сергеевич, Клыпа Татьяна Валерьевна, Борисов Даниил Валерьевич, Ильин Михаил Витальевич
Журнал: Клиническая практика @clinpractice
Рубрика: Оригинальные исследования
Статья в выпуске: 3 (27), 2016 года.
Бесплатный доступ
В нашем исследовании 107 пациентам со средней фракцией выброса 40,6±7,4% (средний возраст 68,9±7,8лет, 76 мужчин и 31 женщина) выполнено аортокоронарное шунтирование на работающем сердце в условиях вспомогательного искусственного кровообращения. В сочетании с коронарным шунтированием пяти пациентам была выполнена каротидная эндартерэктомия и двенадцати - пластика аневризмы левого желудочка. Индекс реваскуляризации составил 2,9±0,8. В послеоперационном периоде зарегистрированы следующие осложнения: острое нарушение мозгового кровообращения - 1 (0,9%), острая сердечно-сосудистая недостаточность - 1 (0,9%), дыхательная недостаточность - 2 (1,9%) и кровотечение, потребовавшее операции рестернотомия-гемостаз, - 1 (0,9%). Смертность составила 0,9% (1 пациент). Операция на работающем сердце в условиях вспомогательного искусственного кровообращения является безопасным и эффективным методом реваскуляризации миокарда, в том числе и при необходимости проведения сочетанного вмешательства (каротидная эндартерэктомия, пластика постинфарктной аневризмы левого желудочка).
Реваскуляризация миокарда, аортокоронарное шунтирование, операция на работающем сердце в условиях вспомогательного искусственного кровообращения, каротидная эндартерэктомия, пластика постинфарктной аневризмы левого желудочка
Короткий адрес: https://sciup.org/14338567
IDR: 14338567
On-pump beating heart myocardial revascularization for high risk patients
107 patients with mean ejection fraction 40,6±7,4% underwent on-pump-beating heart coronary revascularization and associated procedures. There were 76 men and 31 women, with a mean age of 68,9±7,8 years. Five patients required carotid endarterectomy and twelve patients required left ventricular aneurysm repair. 5 patients underwent carotid endarterectomy and 12 patients - left ventricular aneurysm repair. The mean number of graft/patient was 2,9±0,8. Postoperatively occurred the following complications: acute ischemic stroke - 1 (0.9%), acute heart failure - 1 (0.9%), respiratory failure - 2 (1.9%) and bleeding required surgical revision - 1 (0.9%). Hospital mortality rate was 0,9% (1 of the 107 patients). On-pump beating heart technique is a safe and efficient method for coronary artery bypass grafting and associated procedures (carotid endarterectomy, left ventricular aneurysm repair).
Текст научной статьи Реваскуляризация миокарда в условиях вспомогательного искусственного кровообращения у пациентов с высокой степенью риска
Аортокоронарное шунтирование (АКШ), применяемое в клинической практике с 60-х годов 20 в., остается наиболее часто выполняемой кардиохирургической процедурой во всем мире. Интересно отметить, что, за исключением новых методов защиты миокарда, технические аспекты процедуры остаются неизменными на протяжении уже многих лет [1].
Основное число операций АКШ выполняется либо с применением искусственного кровообращения (ИК) и кардиоплегической остановкой сердца, либо без ИК на работающем сердце (так называемая методика off-pump). Физиологические аспекты обеих методик достаточно хорошо исследованы, тем не менее, не прекращаются споры о преимуществах и недостатках их использования у пациентов различного профиля [2].
Коронарное шунтирование с ИК и кардиоплегической остановкой сердца продолжает ассоциироваться с осложнениями, которые могут свести на нет успех проведения процедуры [2]. Кроме того, остановка сердца неизбежно ведет к периоду глобальной ишемии, а современные методы кардиоплегии не всегда позволяют избежать ишемического повреждения миокарда, особенно у пациентов высокого риска, подвергающихся оперативному лечению. В настоящее время оптимальным методом интраоперационной защиты миокарда является кровяная кардиоплегия, но и она не позволяет полностью профилактировать синдром низкого сердечного выброса приблизительно в 10% случаев [3].
Операция на работающем сердце дает возможность предотвратить глобальную ишемию миокарда за счет сохранения нативного кровотока и исключить негативные последствия ИК. Многие наблюдательные исследования и мета-анализы показывают, что использование методики off-pump может снизить смертность и заболеваемость [4, 5]. Основные ограничения применения этой методики связаны с большим риском возникновения нарушений гемодинамики с уменьшением сердечного выброса и ударного объема при манипуляциях с сердцем, в частности, при позиционировании сердца для доступа к задней и заднелатеральной поверхности (для экспозиции ветвей огибающей и правой коронарной артерий).
Успехи в области инвазивной кардиологии значительно изменили профиль пациентов, нуждающихся в оперативном лечении. Теперь пациенты, направляемые кардиологом на АКШ, чаще имеют серьезные сопутствующие заболевания, большая часть из них находится в пожилом и старческом возрасте, страдает диффузным поражением коронарного русла, имеет сниженные функциональные резервы миокарда и нестабильное течение ишемической болезни сердца [6, 7]. Глобальная ишемия вследствие остановки сердца может быть очень опасной для них, равно как и манипуляции на сокращающемся, ослабленном сердцем.
Операция на работающем сердце в условиях вспомогательного ИК предлагает разумный компромисс между обычной процедурой шунтирования с ИК и кардиоплегическим арестом и off-pump процедурой для пациентов с высокой степенью операционного риска. Концепция такой операции основана на соображениях о меньшем ответе сердца и гемодинамики на хирургическое вмешательство с максимальным эффектом для пациента. Эта методика позволяет объединить безопасность и стабильность в управлении гемодинамикой, как при ИК, с эффективностью и меньшей инвазивностью, как при технике off-pump [1].
Доля таких операций в общем объеме АКШ невелика, о чем свидетельствует как ограниченное число публикаций, так и численность пациентов, которым выполнялась операция по данной методике, в каждом отдельном исследовании. В настоящей статье мы описываем собственный опыт выполнения операций коронарного шунтирования и сочетанных процедур на работающем сердце в условиях вспомогательного ИК.
Материал и методы
С 2011 по 2016 год нами было выполнено 107 операций реваскуляризации миокарда на работающем сердце в условиях вспомогательного ИК. Показаниями к операции по данной методике были: стеноз ствола левой коронарной артерии (СтЛКА) более 70%, нестабильная стенокардия, острый мелкоочаговый инфаркт миокарда, снижение фракции выброса левого желудочка (ФВ ЛЖ), постинфарктная аневризма левого желудочка (АЛЖ), диффузные изменения коронарного русла. Средний возраст пациентов составил 68,9±7,8 лет. Более половины прооперированных пациентов имели один и более инфаркт миокарда (ИМ) в анамнезе, при этом как минимум 12 из них перенесли трансмуральный ИМ, о чем свидетельствует развив- шаяся АЛЖ. Всем пациентам перед операцией было выполнено стандартное инструментальное обследование, в которое входили: электрокардиограмма, эхокардиография, ультразвуковое дуплексное сканирование артерий и вен нижних конечностей, ультразвуковая допплерография сосудов головы и шеи, рентгенография грудной клетки, коронароангиография. По данным эхокардиографии ФВ ЛЖ составила 40,6±7,4%. Коронароангиография выявила трехсосудистое поражение у 91 (85,0%) пациента. Клиническая характеристика пациентов представлена в табл. 1.
Таблица 1
Клиническая характеристика пациентов
|
Показатель |
Значение |
|
Мужчин/Женщин |
76/31 (71,0/29,0%) |
|
Возраст, лет |
68,9±7,8 (62) |
|
Возраст старше 70 лет |
16 (15,0%) |
|
ПИКС |
67 (62,6%) |
|
Стенокардия III-IV ФК |
67 (62,6%) |
|
Стеноз СтЛКА ≥ 70% |
32 (29,9%) |
|
Трехсосудистое поражение |
92 (86,9%) |
|
Сахарный диабет |
25 (23,4%) |
|
НС и ОИМ без зубца Q |
19 (17,8%) |
|
Нарушения ритма сердца |
14 (13,1%) |
|
ОНМК в анамнезе |
5 (4,7%) |
|
ХОБЛ |
3 (2,8%) |
|
АЛЖ |
12 (11,2%) |
|
Ожирение |
3 (2,8%) |
|
ЧТКА, стентирование в анамнезе |
5 (4,7%) |
|
КЭАЭ в анамнезе |
7 (6,5%) |
|
Атеросклероз БЦА |
17 (15,9%) |
|
Операция по срочным показаниям |
19 (17,8%) |
|
ФВ ЛЖ, % |
40,6±7,4 (38) |
|
EuroSCORE, баллы |
7,1±2,6 (7) |
|
Примечание: ПИКС – постинфарктный кардиосклероз; НС – нестабильная стенокардия; ОНМК – острое нарушение мозгового кровообращения; ХОБЛ – хроническая обструктивная болезнь легких; ЧТКА – чрескожная транслюминальная коронарная ангиопластика; КЭАЭ – каротидная эндартерэктомия; БЦА – брахиоцефальные артерии. |
|
Расчеты проводились с помощью программного пакета для статистического анализа Statistica 8.0. Количественные данные представлены как Среднее значение ± Стандартное отклонение (Медиана), качественные – в форме частот и процентов.
Хирургическая техника
Во всех случаях доступ к сердцу осуществлялся через срединную стернотомию. ИК подключали стандартным образом по схеме «аорта – правое предсердие». Все операции проводились в условиях нормотермии.
Первым этапом выполняли симультанное вмешательство, когда это было необходимо (табл. 2).
Таблица 2
Симультанные хирургические вмешательства
|
Вид вмешательства |
Количество |
% |
|
Каротидная эндартерэктомия |
5 |
4,7 |
|
Линейная пластика АЛЖ (по Cooley) |
3 |
2,8 |
|
Септовентрикулопластика АЛЖ |
9 |
8,4 |
|
Тромбэктомия из левого желудочка |
5 |
4,7 |
|
Эндартерэктомия из коронарных артерий |
8 |
7,5 |
Позиционирование сердца осуществляли с помощью глубокого перикардиального шва по методу Lima или системы для позиционирования сердца «StarFish» (Medtronic, США). Стабилизацию тканей миокарда проводили с помощью устройства «Octopus» (Medtronic, США). Во всех случаях применяли внутрикоронар-ные шунты (Medtronic, США) (с целью предотвращения регионарной ишемии) и систему для инсуффляции углекислого газа (Medtronic, США), которая позволяла добиться сухого операционного поля и упростить формирование дистальных анастомозов. В первую очередь выполняли шунтирование передней нисходящей артерии, для этой цели всегда применялась левая внутренняя грудная артерия (ЛВГА). В общей сложности ЛВГА была использована в 97 (90,7%) случаях. Для шунтирования последующих коронарных артерий применялись аутовенозные кондуиты. Проксимальные анастомозы накладывали как с применением зажима для бокового отжатия аорты, так и с помощью системы «HeartString», также достаточно часто использовали сложные конструкции анастомозов (Т-графты, секвенциальное шунтирование).
Индекс реваскуляризации составил 2,9±0,8, число шунтов варьировало от одного до четырех, причем три шунта и более были наложены у 82 (76,6%) пациентов. Двадцати четырем (22,4%)
пациентам было выполнено композитное шунтирование (Т-графт) и восьми (7,5%) – секвенциальное. Распределение реваскуляризованных коронарных артерий представлено на рис.1.
Среднее время операции составило 3,3±0,6 (3,3) час, а продолжительность ИК – 63,1±15,3 (62) минут. Пациенты находились в палате реанимации в среднем 23,5±8,6 (21) часов, длительность госпитализации составила 12,2±1,8 (13) дней. Подробные данные, характеризующие интра- и послеоперационный период, приведены в табл. 3.
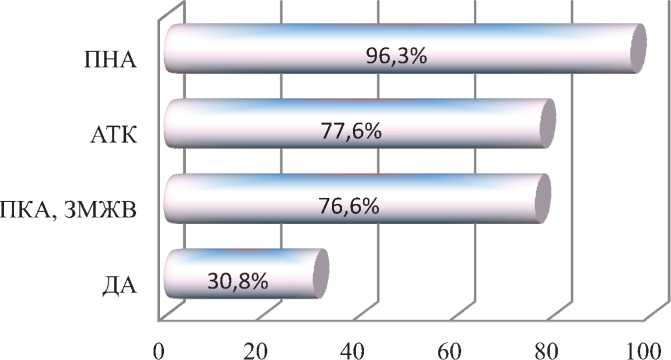
Рис. 1. Целевые сосуды,подвергшиеся шунтированию.
ПНА – передняя нисходящая артерия; АТК – артерия тупого края; ПКА – правая коронарная артерия; ЗМЖВ – задняя межжелудочковая ветвь; ДА – диагональная артерия.
Результаты и обсуждения
Полученные результаты хирургического лечения ИБС в условиях вспомогательного ИК продемонстрировали приемлемые результаты. В результате прогрессирования полиорганной недостаточности погибла одна (0,9%) пациентка 66 лет, поступившая с диагнозом нестабильная стенокардия и прооперированная по срочным показаниям. В общей сложности послеоперационные осложнения развились у пяти пациентов (табл. 4), при этом за исключением ОНМК, развившегося у одного пациента, эти осложне-
Таблица 4
Структура послеоперационных осложнений
Острое нарушение мозгового кровообращения является одним из самых тяжелых, инва-лидизирующих, а иногда и фатальных последствий операции на открытом сердце, и его профилактика должна иметь первостепенное значение. Одной из основных причин интраоперационного инсульта является церебральная эмболия атероматозными массами при манипуляциях на восходящей аорте. Методика АКШ на работающем сердце в условиях ИК минимизирует эти манипуляции, исключая наложение поперечного зажима на аорту, но не устраняет их полностью. Тем не менее, по данным литературы частота развития инсульта при использовании этой методики достаточно низкая и колеблется от 0% до 2,6% [6–15].
Tarakji и соавт. [8] провели крупное проспективное исследование, в котором проанализировали частоту инсультов, развившихся во время и после операций АКШ, проведенных в Cleveland Clinic в течение 30 лет. Рассматривались 4 различные оперативные стратегии, в том числе – методика операции на работающем сердце в условиях ИК (234 пациента). Общая частота инсультов при использовании этой методики составила 1,7% (интраоперацион-
Таблица 3
Интраоперационные и послеоперационные показатели
|
Показатель |
Mean |
Median |
Mode |
Min |
Max |
SD |
|
Количество шунтов на одного пациента |
2,9 |
3 |
3 |
1 |
4 |
0,8 |
|
Продолжительность операции, час |
3,3 |
3,3 |
3,0 |
2,0 |
4,7 |
0,6 |
|
Продолжительность ИК, мин |
63,1 |
62 |
62 |
25 |
90 |
15,3 |
|
Время пребывания в палате реанимации, час |
23,5 |
21,0 |
20,0 |
15,0 |
72 |
8,6 |
|
Кровопотеря в 1-е сутки, мл |
377,5 |
350 |
400 |
150 |
1200 |
121,5 |
|
Время между операцией и выпиской, дней |
8,1 |
8,0 |
9 |
6 |
12 |
1,6 |
|
Продолжительность госпитализации, дней |
12,0 |
11 |
11 |
10 |
16 |
1,8 |
Примечание: Mean – среднее значение; Median – медиана; Mode – мода; Min – минимум; Max – максимум; SD – стандартное отклонение.
ных инсультов не было), а сама методика была оценена авторами как сопоставимая с методикой off-pump (0,79%) и перспективная для пациентов с высоким риском интраоперационного инсульта, связанного с такими факторами как преклонный возраст или атеросклероз аорты. Эти авторы и некоторые другие отмечают, что в качестве одной из превентивных мер по предотвращению инсульта при атеросклерозе восходящей аорты можно рассматривать использование альтернативных мест для канюляции, таких как, к примеру, подмышечная или бедренная артерия [8-10].
Потенциальной причиной цереброваскулярных осложнений является гипоперфузия головного мозга во время ИК [8]. У больных с сочетанным поражением коронарных и брахиоцефальных артерий (БЦА) риск гипоперфузии заметно повышается. Критическое поражение БЦА и коронарных артерий на фоне клиники стенокардии высокого функционального класса является показанием к одномоментному вмешательству: каротидной эндартерэктомии (КЭАЭ) в сочетании с АКШ. Вспомогательное ИК позволяет поддерживать системное давление на более высоком уровне по сравнению с обычным ИК и кардиоплегическим арестом, и тем самым снизить риск системной гипоперфузии и обеспечить адекватную перфузию головного мозга. Мы выполнили три КЭАЭ в сочетании с АКШ на работающем сердце в условиях ИК. Несмотря на то, что одномоментное восстановление мозгового и коронарного кровотока имеет более высокий риск развития осложнений по сравнению с изолированным КШ, у всех пациентов наблюдалось гладкое течение послеоперационного периода.
Еще одной сопутствующей патологией, требующей дополнительного хирургического вмешательства, была АЛЖ, диагностированная у 12 пациентов. Основной причиной смертности после пластики АЛЖ является низкий сердечный выброс [9]. Это происходит из-за неадекватной защиты миокарда, неполной реваскуляризации или некорректного уменьшения объема ЛЖ. Использование ИК без введения кардиоплегии сводит к минимуму ишемическое повреждение миокарда, гарантирует стабильность гемодинамики и позволяет добиться полной реваскуляризации при дилатации ЛЖ [11]. Одновременно с этим операция на работающем сердце дает возможность точно дифференцировать жизнеспособный миокард и рубцовую ткань непосредственно пальпацией и визуально смоделировать адекватную геометрию ЛЖ. Во время сокращений сердца можно оценить необходимость использования и размеры заплаты. Все это позволяет добиться оптимальной геометрии ЛЖ и оптимального послеоперационного результата [9]. Мы провели 12 процедур пластики АЛЖ в сочетании с АКШ на работающем сердце в условиях ИК. В одном случае у пациента развилась дыхательная недостаточность, потребовавшая пролонгированной искусственной вентиляции легких (более 12 часов).
Отсутствие глобальной ишемии миокарда во время пережатия аорты и реперфузии после кардиоплегического ареста в сочетании с гемодинамической стабильностью, гарантированной во время манипуляций с сердцем, является основным преимуществом операции на работающем сердце в условиях ИК. Исследования, проводившиеся с целью изучения данной методики, в большинстве своем свидетельствуют о том, что для пациентов со сниженными резервами миокарда такой подход является залогом хороших результатов процедуры реваскуляризации миокарда.
Так, Perrault и соавт. [12], проведя исследование, в которое было включено 37 пациентов с низкой ФВ ЛЖ, прогрессирующей ишемией, инфарктом миокарда и в возрасте около 80 лет, обнаружили, что использование ИК без пережатия аорты и кардиоплегического ареста связано с низкой частотой отека и ишемии миокарда. Авторы пришли к выводу, что методика является эффективной для предотвращения повреждения миокарда и может быть приемлемой альтернативой для пациентов высокого риска, которые могут не перенести кардиоплегический арест, или в том случае, когда использование метода off-pump является технически невозможным.
Edgerton и соавт. [13] сравнивали результаты применения 4 методик АКШ у 4733 пациентов. Авторы заключили, что методика АКШ в условиях вспомогательного ИК может быть методом выбора для пациентов с кардиогенным шоком, недавно перенесенным ОИМ, низкой ФВ ЛЖ, нестабильной гемодинамикой, аритмией, или при повторной операции АКШ.
Сравнение стандартного АКШ и АКШ на работающем сердце в условиях вспомогательного ИК в основном демонстрирует превосходство последнего в отношении 30-дневной летальности для пациентов с высоким уровнем риска (низкая ФВ, экстренная операция при ОИМ, кардиогенный шок) [10, 14-17]. Одновре- менно с этим отдельные исследования показывают, что при сниженной сократительной функции левого желудочка операция прямой реваскуляризации миокарда на работающем сердце в условиях ИК связана с лучшим ремоделированием сердца в ранние сроки после операции, сопровождается менее выраженными и кратковременными метаболическими нарушениями в миокарде, и нормализация обменных процессов при такой операции происходит быстрее, чем при операции с ИК и кардиоплегией [18-20].
На сегодняшний день ИК с кардиоплегической остановкой сердца по-прежнему остается методом выбора для большинства хирургов [21]. Без использования ИК (off-pump) проводится лишь около четверти всех операций АКШ [1]. Техническая сложность самой операции и противоречивые результаты исследований ведут к тому, что многие хирурги до сих пор не принимают технику off-pump и ждут появления большего количества данных в пользу этой методики [22]. Вероятно, этим же объясняется и то, что методика АКШ на работающем сердце в условиях ИК применяется довольно редко. Анализ немногочисленных публикаций по этой тематике показывает нам, что в большинстве исследований количество пациентов не превышает ста человек.
В своей практике мы отдаем предпочтение выполнению АКШ на работающем сердце, поскольку считаем, что при наличии достаточного опыта у оперирующей бригады и профессионального послеоперационного ухода эта методика дает лучшие результаты, чем стандартное шунтирование с кардиоплегической остановкой сердца, у большинства пациентов. Мы согласны с Perrault и соавт. [12], что инвазивность операции АКШ определяется не только и не столько местом и типом разреза, сколько ишемией миокарда, развивающейся в течение периода пережатия аорты. АКШ на работающем сердце в условиях ИК исключает ишемический компо- нент инвазивности, но продолжая использовать ИК, гарантирует стабильность гемодинамики на протяжении всей операции. Это, с одной стороны, помогает защитить исходно инвалидизи-рованный миокард, а с другой – дает возможность провести его полную реваскуляризацию.
Список литературы Реваскуляризация миокарда в условиях вспомогательного искусственного кровообращения у пациентов с высокой степенью риска
- Glauber M., Farneti A., Bevilacqua S. and Karimov Pump-assisted beating heart surgery. Multimedia Manual of Cardiothoracic Surgery 2004.
- Mohr F-W. To beat or not to beat? From one size fits it all to an individual coronary revascularization strategy. European Heart Journal 2012; 31: 2441-3.
- Pegg T. J., Selvanayagam J. B., Francis J. M. et al. A randomized trial of on-pump beating heart and conventional cardioplegic arrest in coronary artery bypass surgery patients with impaired left ventricular function using cardiac magnetic resonance imaging and biochemical markers. Circulation 2008; 118: 2130-2138.
- Sedrakyan A., Wu A.W., Parashar A. et al. Off-pump surgery is associated with reduced occurrence of Stroke and other morbidity as compared with traditional coronary artery bypass grafting: a meta-analysis of systematically reviewed trials. Stroke 2006; 37: 2759-2769.
- Ascione R., Caputo M., and Angelini G. D. Off-pump coronary artery bypass grafting: not a flash in the pan. The Annals Of Thoracic Surgery 2003; 75: 306-313.
- Fouda M. Coronary artery bypass surgery with on-pump beating-heart technique. Asian Cardiovascular & Thoracic Annals 2007; 15: 392-395.
- Darwazah A.K., Bader V., Isleem I., Helwa K. Myocardial revascularization using on-pump beating heart among patients with left ventricular dysfunction. Journal of Cardiothoracic Surgery 2010; 5: 109-114.
- Tarakji K.G., Sabik III J. F., Bhudia S. K. et al. Temporal onset, risk factors, and outcomes associated with stroke after coronary artery bypass grafting. JAMA 2011, 305 (4): 381-390.
- Gulcan O., Turkoz R., Turkoz A. et al. On-pump/beating-heart myocardial protection for isolated or combined coronary artery bypass grafting in patients with severe left ventricle dysfunction: assessment of myocardial function and clinical outcome. The Heart Surgery Forum 2005; 8 (3): 1-6.
- Miyahara K., Matsuura A., Takemura H. et al. On-pump beating-heart coronary artery bypass grafting after acute myocardial infarction has lower mortality and morbidity. Journal of Thoracic And Cardiovascular Surgery 2008; 135: 521-526.
- Cheng Z., Zhao Z., Quan X. et al. On-Pump Beating Heart coronary artery bypass grafting: a safe and efficacious technique for high risk patients. International Coronary Congress 2015.
- Perrault L. P., Menasché P., Peynet J. et al. On-pump, beating-heart coronary artery operations in high-risk patients: an acceptable trade-off? The Annals Of Thoracic Surgery 1997; 64: 1368-1373.
- Edgerton J. R., Herbert M. A., Jones K.K. et al. On-Pump Beating Heart Surgery offers an alternative for unstable patients undergoing coronary artery bypass grafting. The Heart Surgery Forum 2004; 7 (1): E88-E95.
- Mizutani S., Matsuura A., Miyahara K. et al. On-pump beating-heart coronary artery bypass: a propensity matched analysis. The annals of thoracic surgery 2007; 83: 1368-1373.
- Erkut B., Dag O., Kaygin M.A. et al. On-pump beating-heart versus conventional coronary artery bypass grafting for revascularization in patients with severe left ventricular dysfunction: early outcomes. Can J Surg 2013; 56: 398-404.
- Izumi Y., Magishi K., Ishikawa N., and Kimura F. On-pump beating-heart coronary artery bypass grafting for acute myocardial infarction. The Annals of Thoracic Surgery 2006; 81: 573-576.
- Prifti E, Bonacchi M., Frati G. et al. Beating heart myocardial revascularization on extracorporeal circulation in patients with end-stage coronary artery disease. Cardiovasc Surg 2001; 9: 608-614.
- Чернявский А.М., Несмачный А.С., Бобошко А.В. и др. Хирургическое лечение ишемической болезни сердца у пациентов с низкой фракцией выброса левого желудочка на работающем сердце в условиях искусственного кровообращения: непосредственные результаты. Патология кровообращения и кардиохирургия 2015; 19(1): 51-58.
- Урюжников В.В., Сидоров Р.В., Молочков А.В. и др. Аортокоронарное шунтирование на работающем сердце в условиях параллельного искусственного кровообращения у больных со сниженной сократительной функцией левого желудочка. Вестник Национального медико-хирургического Центра им. Н.И. Пирогова 2010; 5 (4): 25-28.
- Сидоров Р. В. Современная стратегия коронарного шунтирования у больных ишемической болезнью сердца. Дисс…. докт. мед. наук. М., 2005.
- Ferrari E., Stalder N. and von Segesser L.K. On-Pump Beating Heart coronary surgery for high risk patients requiring emergency multiple coronary artery bypass grafting. Journal of Cardiothoracic Surgery 2008; 3: 38-43.
- Letsou G.V., Wu Y.X., Grunkemeier G. et al. Off-pump coronary artery bypass and avoidance of hypothermic cardiac arrest improves early left ventricular function in patients with systolic dysfunction. European Journal of Cardio-Thoracic Surgery 2011; 40: 227-232.
- Elnahal N. On-pump beating heart coronary bypass surgery; Is it the right choice in left main coronary artery disease. Abstracts of the 21st Scientific Session of the Saudi Heart 2010; 93.


