Резервные возможности сердечно-сосудистой и дыхательной систем у пациентов с хронической тромбоэмболической легочной гипертензией
Автор: Васильцева О.Я., Зейналов Д.Ф., Едемский А.Г., Гранкин Д.С., Лавров А.Г., Сирота Д.А., Чернявский А.М.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 1 т.40, 2025 года.
Бесплатный доступ
Хроническая тромбоэмболическая легочная гипертензия (ХТЭЛГ) является тяжелым заболеванием, связаннымс тромботическим поражением легочных артерий и вторичной микроваскулопатией, которые приводят к прогрессированию легочной гипертензии и сердечной недостаточности. Легочная эндартерэктомия (ЛЭЭ) - приоритетный способ лечения ХТЭЛГ.Цель исследования: изучить резервные возможности сердечно-сосудистой и дыхательной систем у пациентов с ХТЭЛГ.Материал и методы. В ретроспективное когортное обсервационное исследование включены 403 пациента в возрасте от 19 до 77 лет с ХТЭЛГ, которым была выполнена ЛЭЭ в ФГБУ «НМИЦ им. ак. Е.Н. Мешалкина» с 2004 по 2021 гг. Параметры трансторакальной эхокардиографии (ЭхоКГ), тензиометрии малого круга кровообращения (МКК), легочных функциональных тестов, теста шестиминутной ходьбы (Т6МХ) и шкалы Борга оценивались до операции, после проведенной ЛЭЭ перед выпиской и спустя 12 мес. после операции.Результаты. При сравнении данных трансторакальной ЭхоКГ после ЛЭЭ перед выпиской выявлено снижение систолического давления в правом желудочке (СДПЖ) с 82,2 ± 23,1 до 44,9 ± 16,2 мм рт. ст., что привело к улучшению показателей внутрисердечной гемодинамики, характеризующих работу правых отделов сердца. Эти улучшения сохранялись и в отдаленном периоде. Анализ показателей тензиометрии МКК у пациентов с ХТЭЛГ после проведенной ЛЭЭ перед выпиской показал, что у всех пациентов имело место значительное снижение среднего давления в легочной артерии (СрДЛА) - с 48,3 ± 14,5 до 27,1 ± 10,7 мм рт. ст. (в 1,8 раза), что сопровождалось снижением легочного сосудистого сопротивления (ЛСС) в 2,8 раза и повышением сердечного выброса (СВ). В отдаленном периоде после проведенной ЛЭЭ также регистрировалось улучшение показателей тензиометрии МКК. При сравнении показателей легочных функциональных тестов выявлено статистически значимое снижение дыхательного и минутного объемов дыхания. После ЛЭЭ по Т6МХ пройденная дистанция увеличилась на 19,0 м, в отдаленном периоде - на 60,6 м. Одышка по шкале Борга снизилась с «тяжелой» до «умеренной», в отдаленном периоде - до «легкой».Заключение. Полученные результаты демонстрируют продолжение восстановительных процессов сердечно-сосудистой и дыхательной систем в ближайшем послеоперационном периоде и далее в течение года наблюдения после ЛЭЭ, что свидетельствует о значительных резервных возможностях сердечно-сосудистой и дыхательной систем, а также о потенциальной излечимости пациентов с ХТЭЛГ.
Легочная эндартерэктомия, хроническая тромбоэмболическая легочная гипертензия, резидуальная легочная гипертензия, трансторакальная эхокардиография, тензиометрия малого круга кровообращения, легочные функциональные тесты, толерантность к физической нагрузке
Короткий адрес: https://sciup.org/149147880
IDR: 149147880 | УДК: 616.12-008.331.3:616.24-005.6-002.2-053 | DOI: 10.29001/2073-8552-2025-40-1-85-94
Reserve Capabilities of the Cardiovascular and Respiratory Systems in Patients with Chronic Thromboembolic Pulmonary Hypertension
Chronic thromboembolic pulmonary hypertension (CTEPH) is a serious disease associated with thrombotic lesions of the pulmonary arteries and secondary microvasculopathy, leading to the progression of pulmonary hypertension and heart failure. Pulmonary endarterectomy (PEA) is the preferred treatment for CTEPH.Aim: To study the reserve capabilities of the cardiovascular and respiratory systems in patients with CTEPH.Material and Methods. The retrospective cohort observational study included 403 patients aged 19 to 77 years with CTEPH who underwent PEA at the National Medical Research Center named after. ak. E.N. Meshalkin from 2004 to 2021. Parameters of transthoracic echocardiography, pulmonary circulation tensiometry, pulmonary function tests, six-minute walk test and Borg scale were assessed before surgery, after PEA before discharge and after surgery 12 months later.Results. When comparing transthoracic echocardiography data at the hospital stage after PEA, a decrease in right ventricular systolic pressure was revealed from 82.2 ± 23.1 to 44.9 ± 16.2 mm Hg, leading to an improvement in intracardiac hemodynamics, characterizing the right heart function. These improvements continued into the long-term follow-up. Analysis of pulmonary circulation tensiometry in CTEPH patients after PEA showed that all patients had a significant decrease in mean pulmonary artery pressure from 48.3 ± 14.5 to 27.1 ± 10.7 mmHg (by 1.8 times), which was accompanied by a decrease in pulmonary vascular resistance by 2.8 times and an increase in cardiac output. In the long-term follow-up improvements in the pulmonary circulation tensiometry indicators also persisted. When comparing the indicators of pulmonary function tests, a statistically significant decrease in tidal and minute respiratory volumes was revealed. After PEA six-minute walk test distance increased by 19.0 meters, in the long-term follow-up by 60.6 meters; shortness of breath according to the Borg scale decreased from “severe” to “moderate”, in the long-term follow-up to “mild”.Conclusion. The results obtained demonstrate the continuation of the cardiovascular and respiratory systems recovery processes in the immediate postoperative period, and further during the year of observation after PEA, indicate significant reserve capabilities of the cardiovascular and respiratory systems, and the potential cure of patients with CTEPH.
Текст научной статьи Резервные возможности сердечно-сосудистой и дыхательной систем у пациентов с хронической тромбоэмболической легочной гипертензией
КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ / CLINICAL INVESTIGATIONS
Хроническая тромбоэмболическая легочная гипертензия (ХТЭЛГ) является тяжелым заболеванием, связанным с тромботическим поражением легочных артерий и вторичной микроваскулопатией, которые приводят к прогрессированию легочной гипертензии, сердечной недостаточности и в конечном итоге к летальному исходу [1–3].
В лечении ХТЭЛГ легочная эндартерэктомия (ЛЭЭ) сохраняет статус приоритетного способа лечения1, 2, 3 [4– 6]. Несмотря на исходную тяжесть состояния операбельных пациентов, они потенциально излечимы при своевременно выполненной ЛЭЭ [3, 7].
Одной из главных причин послеоперационной летальности после ЛЭЭ является резидуальная легочная гипертензия (ЛГ). Данные о резидуальной ЛГ после ЛЭЭ достаточно разноречивы [8–11], и, согласно мнению экспертов, ее частота недооценивается. При этом наличие резидуальной ЛГ в отдаленном послеоперационном периоде во многом определяет качество жизни и дальнейшее течение заболевания у пациентов с ХТЭЛГ [5].
Ввиду структурных изменений сердечно-сосудистой и дыхательной систем при длительном анамнезе ХТЭЛГ пациенты имеют ограничения активности, обусловленные ведущим симптомом данного заболевания – одышкой [2, 4]. Представляет интерес исследование резервных возможностей восстановления функции сердечно-сосудистой и дыхательной систем у пациентов с ХТЭЛГ после ЛЭЭ и способов их определения для разработки более эффективных стратегий диагностики и профилактики резидуальной ЛГ [6].
Цель исследования: изучить резервные возможности сердечно-сосудистой и дыхательной систем у пациентов с ХТЭЛГ с помощью неинвазивных и инвазивных методов исследования после ЛЭЭ.
Материал и методы
Ретроспективно в обсервационное когортное исследование включены пациенты с ХТЭЛГ (n = 403), госпитализированные в клинику ФГБУ «НМИЦ им. ак. Е.Н. Мешалкина» Минздрава России в период с 22.11.2004 по 31.12.2021 гг. для оперативного лечения в объеме ЛЭЭ. Протокол исследования был одобрен локальным этическим комитетом Центра.
Диагноз ХТЭЛГ устанавливался согласно действующим клиническим рекомендациям4 и подтверждался данными комплексного клинико-инструментального обследования, включающего общеклиническое обследование, лабораторные и инструментальные методы исследования. В качестве критериев ХТЭЛГ использовали: 1) гемодинамические показатели – среднее давление в легочной артерии (СрДЛА) ≥ 25 мм рт. ст.; давление заклинивания в легочной артерии ≤ 15 мм рт. ст.; легочное сосудистое сопротивление > 3 ЕД Вуда, измеренные при катетеризации правых отделов сердца (КПОС); 2) данные визуализирующих методов исследования (выявленный дефект перфузии); 3) наличие в анамнезе антикоагулянтной терапии в течение не менее 3 мес. после перенесенной тромбоэмболии легочной артерии5, 6.
Всем пациентам до хирургического вмешательства проводилось общее клиническое обследование, трансторакальная эхокардиография (ЭхоКГ); КПОС и тензиометрия малого круга кровообращения (МКК); бодиплетизмография и определение диффузионной способности легких; кардиопульмональное нагрузочное тестирование; тест 6-минунтной ходьбы (Т6МХ) с оценкой уровня одышки по шкале Борга.
После ЛЭЭ на третьи сутки после операции выполнялась контрольная тензиометрия МКК, перед выпиской из стационара – трансторакальная ЭхоКГ, а также Т6МХ с оценкой уровня одышки по шкале Борга. Дыхательные тесты в процессе госпитализации после проведения ЛЭЭ не проводились в связи с невозможностью адекватной оценки результатов исследований, связанной с отеком области хирургического вмешательства, способностью адекватного выполнения тестов в раннем послеоперационном периоде.
После проведенной ЛЭЭ пациентам с сохраняющейся резидуальной ЛГ была рекомендована повторная госпитализация через 12 мес. после ЛЭЭ для контрольного обследования. А у пациентов со снижением СрДЛА до физиологических значений повторная госпитализация через 12 мес. после ЛЭЭ не рекомендовалась. Было достаточно амбулаторного наблюдения и контроля трансторакальной ЭхоКГ в динамике.
В отдаленном послеоперационном периоде (через 12 мес.) повторно проводился тот же комплекс исследований, что и перед ЛЭЭ.
Трансторакальная ЭхоКГ выполнялась по стандартной методике в положении на левом боку. Проанализированы следующие показатели: систолическое давление в правом желудочке (СДПЖ); конечный диастолический объем правого желудочка (КДО ПЖ); площадь правого желудочка; фракционное изменение площади правого желудочка (ФИП ПЖ); систолическая экскурсия кольца трикуспидального клапана (TAPSE); систолическое дав-
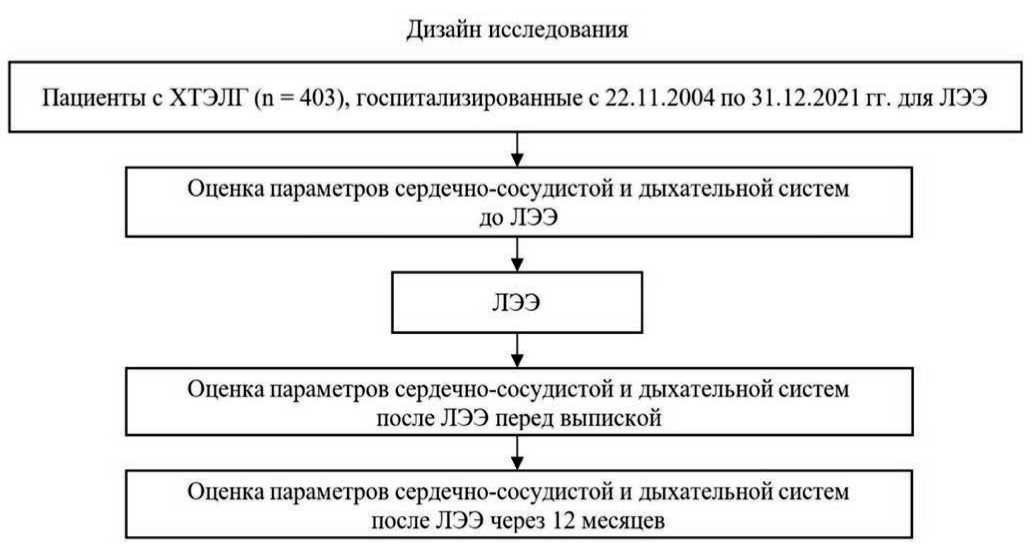
Рис. 1. Дизайн исследования
Примечание: ХТЭЛГ – хроническая тромбоэмболическая легочная гипертензия; ЛЭЭ – легочная эндартерэктомия.
Fig. 1. Study design
Note: CTEPH – chronic thromboembolic pulmonary hypertension; PEA – pulmonary endarterectomy.
ление в легочной артерии (PASP); отношение TAPSE к PAS; конечный диастолический объем левого желудочка (КДО ЛЖ); фракция выброса левого желудочка (ФВ ЛЖ).
Катетеризация правых отделов сердца и тензиометрия МКК выполнялись по стандартной методике с помощью катетера Swan-Ganz 7 Fr (B. Braun, США) – через интродьюсер 7 Fr, стоящий в правой внутренней яремной вене. Определялось систолическое, диастолическое и СрДЛА, давление заклинивания легочной артерии (ДЗЛА), давление в правом предсердии, сердечный выброс (СВ), сердечный индекс (СИ), легочно-сосудистое сопротивление (ЛСС) МКК.
Бодиплетизмография и определение диффузионной способности легких по монооксиду углерода (DLCO) методом одиночного вдоха выполнялись на компьютерном бодиплетизмографе MasterScreen Body (JAEGER, Германия). Обследование и оценка результатов проводились в соответствии с действующими клиническими рекомендациями Европейского респираторного и Американского торакального обществ7. Были проанализированы следующие параметры: бронхиальное сопротивление; остаточный объем легких (ООЛ); общая емкость легких (ОЕЛ); внутригрудной объем (ВГО); жизненная емкость легких (ЖЕЛ); форсированная жизненная емкость легких (ФЖЕЛ); объем форсированного выдоха за 1-ю секунду (ОФВ1); ОФВ1 / ЖЕЛ (индекс Тиффно); максимальная объемная скорость выдоха: 25% ФЖЕЛ (МОС25), 50% ФЖЕЛ (МОС50), 75% ФЖЕЛ (МОС75); минутный объем дыхания (МОД); DLCO, альвеолярный объем.
Кардиопульмональное нагрузочное тестирование выполнялось по стандартной методике на аппарате для спировелоэргометрии (нагрузочный тест) Oxycon-Pro (JAEGER, Германия). Обследование и оценка результатов проводились в соответствии с клиническими рекомендациями Европейского респираторного и Американского торакального обществ8. Проанализированы параметры восстановления легочной вентиляции и газообмена: пиковое потребление кислорода, метаболический эквивалент (МЕТ).
Оценка толерантности к физической нагрузке осуществлялась с помощью Т6МХ, количественная оценка уровня одышки – непосредственно после окончания Т6МХ на пике физической нагрузки с использованием шкалы Борга.
На основании данных проведенного исследования пациентам выполнено хирургическое вмешательство в объеме ЛЭЭ в условиях глубокой гипотермии (18 °С) и циркуляторного ареста. Дизайн исследования представлен на рисунке 1.
Статистический анализ полученных результатов проводился с использованием пакетов статистических программ IBM SPSS STATISTICS 23 и R. Проверка нор- мальности распределения количественных показателей выполнялась с помощью критериев Колмогорова – Смирнова с поправкой Лиллиефорса, Шапиро – Уилка и визуально с помощью построения гистограмм. Однородность дисперсий количественных показателей на этапах наблюдения оценивалась с помощью критерия Левена. При попарных сравнениях количественных показателей на этапах наблюдения использовался парный критерий Стьюдента. При множественных сравнениях для контроля над групповой вероятностью ошибки первого рода применялся метод Холма – Бонферрони. Количественные показатели представлены средним значением (M), стандартным отклонением (SD) и 95% доверительным интервалом (95% ДИ) для среднего значения. Критический уровень значимости p для всех используемых процедур статистического анализа принимался равным 0,05.
Результаты
С 22.11.2004 по 31.12.2021 гг. на базе ФГБУ «НМИЦ им. ак. Е.Н. Мешалкина» Минздрава России ЛЭЭ выполнена 403 пациентам с диагнозом ХТЭЛГ, из которых 58% мужчины. Средний возраст пациентов на момент операции был 49,9 ± 12,7 года. Госпитальный период составлял 28,9 ± 13,9 сут. ТЭЛА в анамнезе выявлена у 395 пациентов (98%) c ХТЭЛГ. Временной интервал от последнего эпизода ТЭЛА до прогрессирования клинических проявлений ХТЭЛГ составлял 24,8 ± 27,1 мес. (95% ДИ 22,1; 27,4), время от прогрессирования клинических проявлений ХТЭЛГ до установления диагноза ХТЭЛГ в экспертном центре, согласно действующим рекомендациям, – 6,9 ± 8,4 мес. (95% ДИ 6,1; 7,7). Временной интервал от прогрессирования клинических проявлений ХТЭЛГ до операции ЛЭЭ был равен 10,2 ± 10,1 мес. (95% ДИ 9,2; 11,2). Временной интервал от установления диагноза ХТ-ЭЛГ до проведения ЛЭЭ составлял 3,2 ± 4,0 мес. (95% ДИ 2,8; 3,5). Временные интервалы от последнего эпизода ТЭЛА (через 3 мес. непрерывной оптимальной антикоагулянтной терапии) до установления диагноза ХТЭЛГ в экспертном центре были объединены в общий показатель – «время задержки диагноза», который был равен 28,7 ± 32,5 мес. А временные интервалы от последнего эпизода
ТЭЛА (через 3 мес. непрерывной оптимальной антикоагулянтной терапии) до проведения ЛЭЭ были объединены в общий показатель – «время задержки лечения», который соответствовал 32,0 ± 34,5 мес. Послеоперационная летальность пациентов на госпитальном этапе составляла 30 человек (7,4%), в отдаленном периоде – 19 человек (5,1%). Всего в течение 17 лет было зарегистрировано 49 летальных случаев.
У всех пациентов ( n = 403) с ХТЭЛГ до операции проанализированы основные показатели как внутрисердечной гемодинамики, так и гемодинамики МКК, функции дыхания, результаты Т6МХ и шкалы Борга.
После проведенной ЛЭЭ у пациентов ( n = 373) также исследованы основные показатели внутрисердечной гемодинамики и гемодинамики МКК, результаты Т6МХ и шкалы Борга. Согласно данным тензиометрии МКК, резидуальная ЛГ после операции сохранялась у 103 человек (27,6%).
Проанализированы основные показатели внутрисердечной гемодинамики у 354 пациентов в отдаленном послеоперационном периоде (через 12 мес. после ЛЭЭ). У 78 пациентов в отдаленном послеоперационном периоде также исследованы основные показатели гемодинамики МКК, функции дыхания, результаты Т6МХ и шкалы Борга.
При сравнении данных трансторакальной ЭхоКГ после ЛЭЭ перед выпиской выявлено снижение СДПЖ с 82,2 ± 23,1 до 44,9 ± 16,2 мм рт. ст. Снижение СДПЖ привело к улучшению внутрисердечной гемодинамики, которое сопровождалось уменьшением КДО ПЖ с 97,3 ± 42,0 до 56,6 ± 24,5 мл и площади ПЖ с 30,6 ± 8,4 до 22,8 ± 5,7 см2, повышением ФИП ПЖ с 28,8 ± 7,5 до 36,8 ± 6,2% и TAPSE с 13,4 ± 3,1 до 14,7 ± 3,1 мм. При этом снижение давления в ПЖ и повышение TAPSE привело к экспоненциальному росту отношения TAPSE / PASP (с 0,169 ± 0,079 до 0,391 ± 0,139 мм/мм рт. ст.) – параметра, являющегося независимым маркером оценки тяжести и прогнозирования исходов ХТЭЛГ. Его повышение характеризуется низким риском клинического ухудшения, а снижение – высоким риском [12]. В процессе госпитализации также выявлено увеличение КДО ЛЖ с 67,5 ± 26,9 до 78,3 ± 24,5 мл (табл. 1).
Таблица 1. Показатели трансторакальной эхокардиографии у пациентов с хронической тромбоэмболической легочной гипертензией до операции и перед выпиской после проведенной легочной эндартерэктомии
Table 1. Indicators of transthoracic echocardiography in patients with chronic thromboembolic pulmonary hypertension before surgery and before discharge after PEA
|
Показатели |
До ЛЭЭ ( n = 403) |
После ЛЭЭ перед выпиской ( n = 373) |
p-value |
||
|
M ± SD |
95% ДИ |
M ± SD |
95% ДИ |
||
|
СДПЖ, мм рт. ст. |
82,2 ± 23,1 |
[79,9; 84,6] |
44,9 ± 16,2 |
[43,2; 46,6] |
< 0,001 |
|
КДО ПЖ, мл |
97,3 ± 42,0 |
[92,5; 102,2] |
56,6 ± 24,5 |
[53,8; 59,4] |
< 0,001 |
|
Площадь ПЖ, см2 |
30,6 ± 8,4 |
[29,3; 32,0] |
22,8 ± 5,7 |
[21,7; 23,9] |
< 0,001 |
|
ФИП ПЖ, % |
28,8 ± 7,5 |
[27,8; 29,8] |
36,8 ± 6,2 |
[36,0; 37,6] |
< 0,001 |
|
TAPSE, мм |
13,4 ± 3,1 |
[12,9; 13,9] |
14,7 ± 3,1 |
[14,2; 15,2] |
< 0,001 |
|
TAPSE / PASP, мм/мм рт. ст. |
0,169 ± 0,079 |
[0,151; 0,187] |
0,391 ± 0,139 |
[0,364; 0,417] |
< 0,001 |
|
КДО ЛЖ, мл |
67,5 ± 26,9 |
[64,8; 70,2] |
78,3 ± 24,5 |
[75,8; 80,8] |
< 0,001 |
|
ФВ ЛЖ, % |
65,4 ± 8,1 |
[64,6; 66,2] |
63,4 ± 7,4 |
[62,7; 64,2] |
< 0,001 |
Примечание: здесь и далее в таблице 2: ЛЭЭ – легочная эндартерэктомия; М – среднее значение показателя; SD – среднеквадратичное отклонение; 95% ДИ – 95% доверительный интервал; СДПЖ – систолическое давление в правом желудочке; КДО ПЖ – конечный диастолический объем правого желудочка; ПЖ – правый желудочек; ФИП ПЖ – фракционное изменение площади правого желудочка; TAPSE – систолическая экскурсия кольца трехстворчатого клапана; PASP – систолическое давление в легочной артерии; КДО ЛЖ – конечный диастолический объем левого желудочка; ФВ ЛЖ – фракция выброса левого желудочка.
При сравнении данных трансторакальной ЭхоКГ у пациентов c ХТЭЛГ до ЛЭЭ и в отдаленном послеоперационном периоде (через 12 мес.) сохранялось статистически значимое улучшение показателей внутрисердечной гемодинамики, характеризующих работу правых отделов сердца в виде снижения СДПЖ с 82,2 ± 23,1 до 44,8 ± 17,1 мм рт. ст., КДО ПЖ с 97,3 ± 42,0 до 56,6 ± 24,5
мл, площади ПЖ с 30,6 ± 8,4 до 22,8 ± 5,7 см2, что привело к повышению ФИП ПЖ с 28,8 ± 7,5 до 36,8 ± 6,2%, а TAPSE – с 13,4 ± 3,1 до 16,7 ± 3,4 мм. При этом TAPSE / PASP как интегральный показатель возрос в 2,3 раза (с 0,169 ± 0,079 до 0,403 ± 0,174 мм/мм рт. ст.). Также зафиксировано увеличение КДО ЛЖ в динамике (табл. 2, рис.2 и 3).
Таблица 2. Показатели трансторакальной эхокардиографии у пациентов с хронической тромбоэмболической легочной гипертензией до операции и через 12 месяцев после проведенной легочной эндартерэктомии
Table 2. Indicators of transthoracic echo-cardiography in patients with chronic thromboembolic pulmonary hypertension before surgery and 12 months after PEA
|
Показатели |
До ЛЭЭ ( n = 403) |
После ЛЭЭ перед выпиской ( n = 373) |
p-value |
||
|
M ± SD |
95% ДИ |
M ± SD |
95% ДИ |
||
|
СДПЖ, мм рт. ст. |
82,2 ± 23,1 |
[79,9; 84,6] |
44,8 ± 17,1 |
[40,9; 48,7] |
< 0,001 |
|
КДО ПЖ, мл |
97,3 ± 42,0 |
[92,5; 102,2] |
59,6 ± 27,2 |
[52,7; 66,5] |
< 0,001 |
|
Площадь ПЖ, см2 |
30,6 ± 8,4 |
[29,3; 32,0] |
20,7 ± 5,7 |
[18,8; 22,6] |
< 0,001 |
|
ФИП ПЖ, % |
28,8 ± 7,5 |
[27,8; 29,8] |
38,7 ± 6,8 |
[37,1; 40,4] |
< 0,001 |
|
TAPSE, мм |
13,4 ± 3,1 |
[12,9; 13,9] |
16,7 ± 3,4 |
[15,8; 17,6] |
< 0,001 |
|
TAPSE / PASP, мм/мм рт. ст. |
0,169 ± 0,079 |
[0,151; 0,187] |
0,403 ± 0,174 |
[0,339; 0,467] |
< 0,001 |
|
КДО ЛЖ, мл |
67,5 ± 26,9 |
[64,8; 70,2] |
83,6 ± 26,2 |
[77,5; 89,6] |
< 0,001 |
|
ФВ ЛЖ, % |
65,4 ± 8,1 |
[64,6; 66,2] |
63,4 ± 6,7 |
[61,9; 64,9] |
0,123 |
Динамика показателей трансторакальной ЭхоКГ
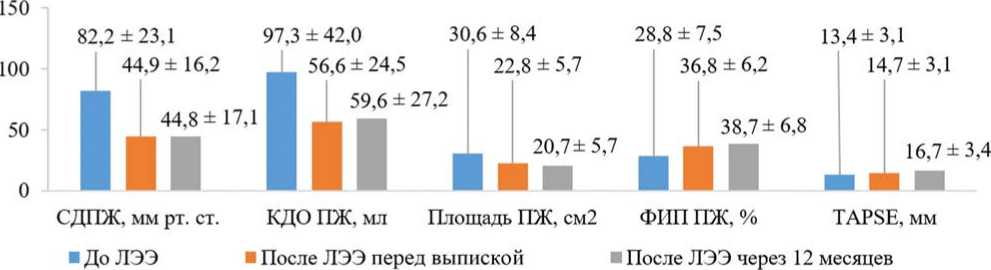
Рис. 2. Динамика показателей трансторакальной эхокардиографии
Примечание: ЛЭЭ – легочная эндартерэктомия; ПЖ – правый желудочек; СДПЖ – систолическое давление в ПЖ; КДО ПЖ – конечный диастолический объем ПЖ; ФИП ПЖ – фракционное изменение площади ПЖ; TAPSE – систолическая экскурсия кольца трехстворчатого клапана.
Fig. 2. Dynamics of transthoracic EchoCG parameters
Note: PEA – pulmonary endarterectomy; RV – right ventricle; RVSP – right ventricular pressure systolic; EDV RV – end-diastolic volume of the right ventricle; FAC RV – fractional change in right ventricular area; TAPSE - tricuspid annular plane systolic excursion.
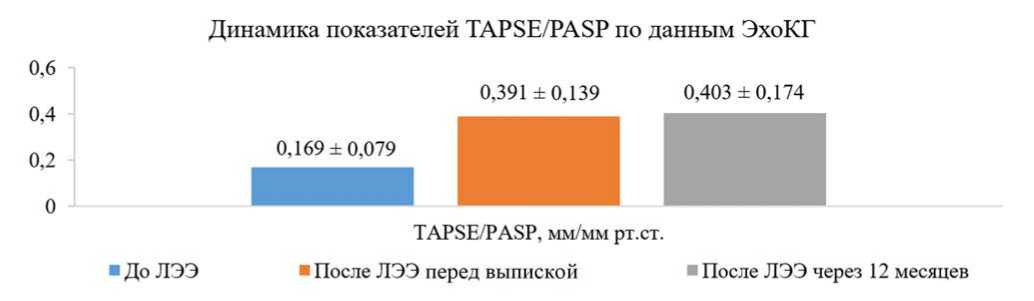
Рис. 3. Динамика показателей TAPSE / PASP по данным эхокардиографии
Примечание: ЛЭЭ – легочная эндартерэктомия; TAPSE – систолическая экскурсия кольца трехстворчатого клапана;
PASP – систолическое давление в легочной артерии.
Fig. 3. Dynamics of TAPSE / PASP indicators according to EchoCG data
Note: PEA – pulmonary endarterectomy; EchoCG – echo-cardiography; TAPSE – tricuspid annular plane systolic excursion;
PASP – pulmonary artery systolic pressure.
Анализ показателей тензиометрии МКК у пациентов с ХТЭЛГ до операции и после проведенной ЛЭЭ перед выпиской показал, что у всех обследуемых имело место значительное снижение СрДЛА – с 48,3 ± 14,5 до
27,1 ± 10,7 мм рт. ст. (в 1,8 раза), что привело к повышению СВ с 4,0 ± 1,3 до 5,2 ± 1,7 л/мин. Кроме того, выявлено снижение ЛСС в 2,8 раза – с 812,3 ± 462,6 до 288,5 ± 200,9 дин × с × см–5 (табл. 3).
Таблица 3. Показатели тензиометрии малого круга кровообращения при катетеризации правых отделов сердца у пациентов с хронической тромбоэмболической легочной гипертензией до операции и перед выпиской после проведенной легочной эндартерэктомии
Table 3. Indicators of pulmonary circulation tensiometry during RHC in patients with chronic thromboembolic pulmonary hypertension before surgery and before discharge after PEA
|
Показатели |
До ЛЭЭ ( n = 403) |
После ЛЭЭ перед выпиской ( n = 373) |
p-value |
||
|
M ± SD |
95% ДИ |
M ± SD |
95% ДИ |
||
|
СрДЛА, мм рт. ст. |
48,3 ± 14,5 |
[46,7; 50,0] |
27,1 ± 10,7 |
[24,9 29,3] |
< 0,001 |
|
СВ, л/мин |
4,0 ± 1,3 |
[3,9; 4,2] |
5,2 ± 1,7 |
[4,9; 5,5] |
< 0,001 |
|
ЛСС, дин × с × см–5 |
812,3 ± 462,6 |
[759,9; 864,6] |
288,5 ± 200,9 |
[248,9; 328,2] |
< 0,001 |
Примечание: здесь и далее в таблице 4: ЛЭЭ – легочная эндартерэктомия; М – среднее значение показателя; SD – среднеквадратичное отклонение; 95% ДИ – 95% доверительный интервал; КПОС – катетеризация правых отделов сердца; СрДЛА – среднее давление в легочной артерии; ДЗЛА – давление заклинивания легочной артерии; СВ – сердечный выброс; ЛСС – легочное сосудистое сопротивление.
При сравнении показателей тензиометрии МКК у пациентов с ХТЭЛГ до операции и в отдаленном периоде после проведенной ЛЭЭ сохраняются статистически зна- чимые улучшения в виде снижения СрДЛА, ЛСС и повы шения СВ (табл. 4, рис. 4 и 5).
Таблица 4. Показатели тензиометрии малого круга кровообращения при катетеризации правых отделов сердца у пациентов с хронической тромбоэмболической легочной гипертензией до операции и через 12 месяцев после проведенной легочной эндартерэктомии
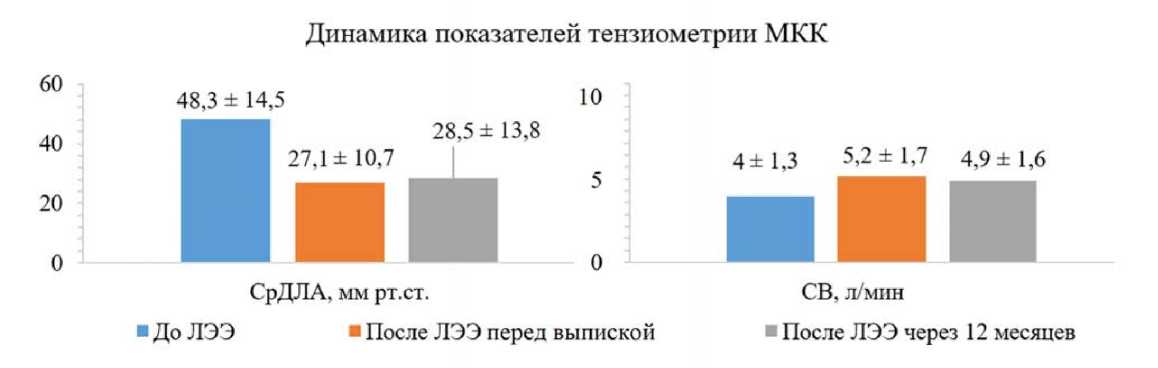
Table 4. Indicators of pulmonary circulation tensiometry during RHC in patients with chronic thromboembolic pulmonary hypertension before surgery and after PEA 12 months later
|
Показатели |
До ЛЭЭ ( n = 403) |
После ЛЭЭ через 12 мес. ( n = 78) |
p-value |
||
|
M ± SD |
95% ДИ |
M ± SD |
95% ДИ |
||
|
СрДЛА, мм рт. ст. |
48,3 ± 14,5 |
[46,7; 50,0] |
28,5 ± 13,8 |
[25,4-31,6] |
< 0,001 |
|
СВ, л/мин |
4,0 ± 1,3 |
[3,9; 4,2] |
4,9 ± 1,6 |
[4,5; 5,3] |
0,002 |
|
ЛСС, дин × с × см–5 |
812,3 ± 462,6 |
[759,9; 864,6] |
328,4 ± 323,8 |
[254,4; 402,4] |
< 0,001 |
Рис. 4. Динамика показателей тензиометрии малого круга кровообращения
Примечание: ЛЭЭ – легочная эндартерэктомия; МКК – малый круг кровообращения; СрДЛА – среднее давление в легочной артерии;
СВ – сердечный выброс.
-
Fig. 4. Dynamics of pulmonary circulation tensiometry indices
Note: PEA – pulmonary endarterectomy; mPAP – mean pulmonary arterial pressure; CO – cardiac output.
При сравнении показателей легочных функциональных тестов (бодиплетизмографии, диффузионной способности легких и кардиопульмонального нагрузочного тестирования) у пациентов с ХТЭЛГ до операции и в отдаленном периоде после проведенной ЛЭЭ выявлено снижение дыхательного объема с 1,8 ± 7,4 до 1,6 ± 2,9 л и минутного объема дыхания с 16,4 ± 5,0 до 15,7 ± 5,4 л/мин. При анализе остальных показателей бодиплетиз- мографии, таких как бронхиальное сопротивление, ООЛ, ОЕЛ, ВГО, ЖЕЛ, ФЖЕЛ, ОФВ1, ОФВ1 / ФЖЕЛ, МОС25, МОС50, МОС75 и при оценке DLCO, а также показателей кардиопульмонального теста (пиковое потребление кислорода, метаболический эквивалент (МЕТ)) до и после операции ЛЭЭ в отдаленном периоде через 12 мес. значимых изменений не наблюдалось (табл. 5).
Динамика показателей ЛСС по данным тензиометрии МКК
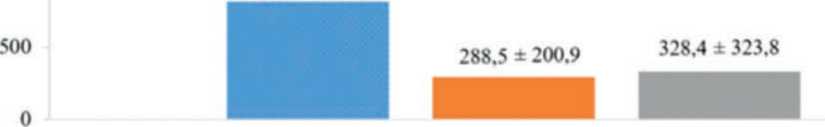
ЛСС. дин*схсм’’
■ До ЛЭЭ ■ После ЛЭЭ перед выпиской • После ЛЭЭ через 12 месяцев
Рис. 5. Динамика показателей легочной эндартерэктомии по данным тензиометрии малого круга кровообращения
Примечание: ЛЭЭ – легочная эндартерэктомия; МКК – малый круг кровообращения; ЛСС – легочное сосудистое сопротивление.
-
Fig. 5. Dynamics of PVR parameters according to tensiometry of the pulmonary circulation
Note: PEA – pulmonary endarterectomy; PVR – pulmonary vascular resistance.
Таблица 5. Динамика показателей функции внешнего дыхания и эффективности легочной вентиляции у пациентов с хронической тромбоэмболической легочной гипертензией до операции и через 12 месяцев после операции легочной эндартерэктомии
Table 5. Dynamics of external respiratory function indicators and pulmonary ventilation efficiency in patients with chronic thromboembolic pulmonary hypertension before surgery and after PEA 12 months later
|
Показатели |
До ЛЭЭ ( n = 403) |
После ЛЭЭ через 12 мес. ( n = 78) |
p-value |
||
|
M ± SD |
95% ДИ |
M ± SD |
95% ДИ |
||
|
Дыхательный объем, л |
1,8 ± 7,4 |
[0,8; 2,7] |
1,6 ± 2,9 |
[0,5; 2,8] |
< 0,001 |
|
Минутный объем дыхания, л/мин |
16,4 ± 5,0 |
[15,8; 17,1] |
15,7 ± 5,4 |
[13,6; 17,9] |
< 0,001 |
Примечание: ЛЭЭ – легочная эндартерэктомия; М – среднее значение показателя; SD – среднеквадратичное отклонение; 95% ДИ – 95% доверительный интервал.
При сопоставлении показателей Т6МХ с оценкой уровня одышки по шкале Борга у пациентов с ХТЭЛГ до операции и после проведенной ЛЭЭ перед выпиской пройденная дистанция увеличилась на 19,0 м – с 375,4 ± 64,3 м, 95% ДИ [360,6; 390,1] до 394,1 ± 61,3 м, 95% ДИ [379,9; 408,2]; p < 0,001. При этом значение уровня одышки по шкале Борга исходно составляло 4,9 ± 0,9 балла, 95% ДИ [4,6; 5,1], что характеризовалось как «тяжелая» одышка после выполненного Т6МХ, а в динамике после проведенной ЛЭЭ оно снизилось до 3,2 ± 0,7 балла, 95% ДИ [3,0; 3,4]; p < 0,001, что оценивалось уже как «умеренная» одышка.
При сопоставлении показателей Т6МХ с оценкой уровня одышки по шкале Борга у пациентов с ХТЭЛГ до операции и в отдаленном периоде (12 мес.) после проведенной ЛЭЭ пройденная дистанция увеличилась на 60,6 м (с 375,4 ± 64,3 до 436,1 ± 53,6 м, 95% ДИ [423,7; 448,5]; p < 0,001). При этом значение уровня одышки по шкале Борга снизилось до 2,4; 95% ДИ [2,3; 2,6]; p < 0,001, что соответствует градации «легкая» одышка.
Обсуждение
Несмотря на достижения в хирургии ХТЭЛГ, частота резидуальной ЛГ остается высокой в силу множества факторов, оказывающих влияние на течение ХТЭЛГ как в предоперационном, интраоперационном, так и послеоперационном периодах, играющих важную роль в патофизиологической перестройке сердечно-сосудистой и дыхательной систем [13]. Основными причинами резидуальной ЛГ принято считать недостаточную дезоблитерацию легочных артерий после ЛЭЭ и дистальную микроваскулопатию, характеризующуюся прежде всего гипертрофией и утолщением средней оболочки артериол с ее фиброзной и клеточной гиперплазией, а также нарушением кислородтранспортной функции альвеолярно-капиллярной мембраны [14, 15]. Однако ввиду относительной редкости патологии, объективных трудностей верификации ХТЭЛГ и, соответственно, ограниченного количества пациентов, направляемых на оперативное вмешательство (ЛЭЭ), возможности изучения механизмов формирования резидуальной гипертензии, ее профилактики и коррекции ограничены [16].
В настоящем исследовании были проанализированы клинико-функциональные особенности сердечно-сосудистой и дыхательной систем до операции, после проведенной ЛЭЭ и в отдаленном периоде через 12 мес. после операции. Проведена сравнительная оценка предоперационных и послеоперационных исследований, определены особенности адаптационно-регуляторных механизмов.
Результаты нашей работы продемонстрировали продолжение восстановительных процессов сердечно-сосудистой и дыхательной систем в ближайшем послеоперационном периоде и далее в течение года наблюдения после ЛЭЭ. При этом в отношении гемодинамики МКК и внутрисердечной гемодинамики более выраженные изменения показателей зарегистрированы в ближайшем послеоперационном периоде с постепенной дальнейшей стабилизацией в течение года. В отношении толерантности к физической нагрузке, оцениваемой Т6МХ и шкалой Борга, более значительные изменения установлены в отсроченное время – уже после выписки из стационара в отдаленном послеоперационном периоде. После проведенной ЛЭЭ, несмотря на то, что основные гемодина- мически значимые изменения в МКК происходят еще на госпитальном этапе лечения, более выраженное и значимое улучшение клинико-функциональных показателей происходит в отдаленном периоде – через 12 мес. после операции. С патофизиологической точки зрения это может быть объяснено постепенным восстановлением газообмена и изменением вентиляционно-перфузионных соотношений, приводящих к постепенному и последовательному устранению артериальной и венозной гипоксемии органов и систем, несущих долгосрочные перспективы в отношении качества жизни и прогноза пациентов с ХТЭЛГ.
Ограничения исследования
Данное исследование является ретроспективным. Несомненно, полученные непосредственные клинические и гемодинамические результаты важны и интересны, однако для более детального изучения особенностей резидуальной ЛГ необходим дальнейший набор материала.
Выводы
Представленные данные демонстрируют серьезные резервные возможности сердечно-сосудистой и дыхательной систем и потенциальную излечимость ХТЭЛГ или, по крайней мере, возможность значительного улучшения гемодинамики МКК и функции дыхания посредством выполнения ЛЭЭ в оптимальные сроки.


