Результаты хирургической изоляции левого предсердия в лечении фибрилляции предсердий у пациентов с ИБС и патологией митрального клапана
Автор: Арутюнян В.Б., Чрагян Ваге Ашотович
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.12, 2017 года.
Бесплатный доступ
Ретроспективно были проанализированы истории болезней 100 пациентов, прооперированных за период с января 2009 по октябрь 2010 г. Все больные подверглись левопредсердной процедуре «лабиринт» в сочетании с хирургией митрального клапана. Левопредсердная операция «лабиринт» для лечения фибрилляции предсердий в сочетании с коррекцией патологии митрального клапана является эффективным методом восстановления синусового ритма по результатам раннего периода наблюдения, и ее результаты сопоставимы с результатами других модификаций процедуры «лабиринт».
Операция "лабиринт", фибрилляция предсердий, хирургия митрального клапана
Короткий адрес: https://sciup.org/140188670
IDR: 140188670 | УДК: 616.125.2-008.313.2/.3-089:
The results of surgical isolation of the left atrium in the treatment of atrial fibrillation in patients with coronary artery disease and pathology of the mitral valve
Case histories of 100 patients operated on during the period from January 2009 to October 2010 were analyzed retrospectively. All the patients underwent left atrial procedures «maze» in the treatment of atrial fibrillation combined with bicuspid valve surgery. Left atrial procedure «maze» in the treatment of atrial fibrillation combined with mitral valve pathology correction is an effective technique of sinus rhythm restoration based on the results of the early follow-up and its results are comparable with those of other modifications of the «maze» procedure.
Текст научной статьи Результаты хирургической изоляции левого предсердия в лечении фибрилляции предсердий у пациентов с ИБС и патологией митрального клапана
Фибрилляция предсердий (ФП) – наиболее распространенное нарушение ритма, частота которого увеличивается с возрастом и наличием патологии митрального клапана. Cвязанные с ФП ухудшение гемодинамики, увеличение случаев тромбоэмболии могут приводить к инвалидизации, летальным исходам и большим финансовым затратам на лечение пациентов [5]. Операция «лабиринт», которую внедрили J. Cox и соавт. для лечения ФП, и ее дальнейшие модификации показали эффективность применения данной процедуры при хронической ФП, сочетающейся с болезнью митрального клапана (МК). Ранняя летальность при изолированных операциях «лабиринт» составляет менее 1% и повышается до 2,7% при сочетании с другими видами вмешательств на сердце [5]. В связи с трудностью технического исполнения и большим количеством осложнений некоторыми авторами предложены упрощенные левопредсердные процедуры (модификации левопредсердных разрезов процедуры «лабиринт») или гибридные (в сочетании с РЧА, криодеструкцией) вмешательства для пациентов с ФП и патологией МК. Уже первые клинические результаты показали эффективность хирургических левопредсердных процедур «лабиринт» у пациентов с патологией МК [6] (рис. 1). На сегодняшний день имеются единичные работы о ранних или среднесрочных результатах при применении как чисто хирургических методов, так и различных гибридных процедур. Целью настоящего исследования явился анализ результатов операций левопредсердного «лабиринта» в сочетании с хирургией МК.
Материал и методы
С января 2009 по октябрь 2010 г. 135 пациентам выполнена процедура «лабиринт» в различных модификациях (100 – левопредсердный «лабиринт», 28 – полный «лабиринт», 3 – полный «лабиринт» с криодеструкцией, 4 – левопредсердный «лабиринт» с криодеструкцией). Все участники исследования предоставили информированное согласие, а само исследование было одобрено локальным этическим комитетом учреждения. Операция «лабиринт» производилась как в изолированном варианте, так и в сочетании с другими кардиохирургическими вмешательствами.
Объектом нашего исследования явилась группа из 100 пациентов, которым были произведены левопредсердные операции «лабиринт» с вмешательствами на МК. Хирургические разрезы, произведенные при левопредсердном «лабиринте», были идентичны разрезам, производимым на левом предсердии (ЛП) при операциях «лабиринт», предложенных J. Cox и соавт. [4].
Средний возраст пациентов составил 55 ± 7,5 года (от 33 до 69 лет), 69 пациентов были мужчины. Длительность течения ФП составляла в среднем по группе 24,5 ± 2,9 мес. (от 0 до 98 мес.). Классификация ФП производилась согласно номенклатуре, предложенной Американской ассоциацией сердца и Европейским советом кардиологов [5]. Пароксизмальная ФП наблюдалась у 15 пациентов, персистирующая – у 19 и перманентная – у 66 пациентов; 12 больных в прошлом перенесли вмешательства по поводу аритмий: имплантация ЭКС – у 6 пациентов (причина имплантации у всех паци-

Арутюнян В.Б., Чрагян В.А.
РЕЗУЛЬТАТЫ ХИРУРГИЧЕСКОЙ ИЗОЛЯЦИИ ЛЕВОГО ПРЕДСЕРДИЯ В ЛЕЧЕНИИ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ У ПАЦИЕНТОВ С ИБС И ПАТОЛОГИЕЙ МИТРАЛЬНОГО КЛАПАНА
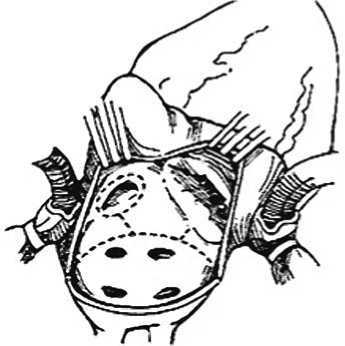
Рис. 1. Левопредсердные разрезы при Cox-Maze III (J. Fukada et al. // Ann. Thorac. Surg. – 1998. – Vol. 65. – P. 1566–1569)
ентов – постоянная форма ФП с редким желудочковым ритмом), РЧА – у 2 пациентов и кардиоверсия – у 4. По данным ЭхоКГ в режиме M-mоde по парастернальной длинной оси диаметр ЛП в среднем составил 6,47 ± 7 см (4,5–8,7 см), у 58% пациентов диаметр ЛП превышал 6,0 см (у пациентов с диаметром ЛП более 9 см процедура «лабиринт» не производилась или выполнялись редукционные вмешательства на ЛП). Объем ЛП высчитывали по методу эллипса (длина – диаметр) [11]. Средний объем ЛП в группе составил 94,6 ± 24,9 мл (46–155 мл). По этиологии поражения МК больные распределялись следующим образом: дегенеративная болезнь – у 66 пациентов, ишемическая дисфункция – у 30, ревматическая – у 4. Стеноз МК установлен у 7 пациентов, недостаточность – у 39, стеноз/недостаточность – у 54 больных.
Хирургическая техника. Операции проводились в условиях искусственного кровообращения при нормо-термии с использованием гиперкалиевой кристаллоидной кардиоплегии. Посредством правостороннего разреза ЛП, вдоль атриовентрикулярной борозды с расширением под верхнюю и нижнюю полые вены открывали полость ЛП. Инвагинированное в полость ЛП ушко резецировали, продолжали разрез вокруг легочных вен. В проекции участка Р2–Р3 МК от окружного разреза выполняли дополнительный, идущий к фиброзному кольцу МК в месте контакта участков Р2–Р3. После сшивания краев указанных разрезов производили вмешательства на МК (пластика или протезирование). Протезирование было выполнено 10 пациентам, аннулопластика (гибкими незамкнутыми кольцами) – 80, аннулопластика и вальвулопластика с использованием неохорд из нитей Gore-Tex – 10. У 31 больного выполнено сочетанное коронарное шунтирование (среднее число дистальных анастомозов – 3,8 ± 1,2), у 33 пациентов – пластика трикуспидального клапана по Де Вега. Среднее время искусственного кровообращения составило 59 ± 14,9 мин. (34–96 мин.), время ишемии миокарда – 41,6 ± 11,9 мин. (23–71 мин.).
Послеоперационное динамическое наблюдение Стандартная ЭКГ в 12 отведениях проводилась ежедневно в течение послеоперационного внутрибольничного периода, затем через 1, 3, 6, 12 мес. и в дальнейшем два раза в год. Для исследования сердечной функции и степени восстановления транспортной функции предсердий производилась трансэзофагеальная ЭхоКГ непосредственно после отключения аппарата ИК, а впоследствии трансторакальная ЭхоКГ перед выпиской пациента из стационара, через 1, 6, 12 мес. и затем два раза в год. Наличие механической функции правого и левого предсердий определялось присутствием на допплер-ЭхоКГ А- и Е-волн на митральном и трикуспидальном клапанах, соответственно. В случаях наличия сомнительной волны желудочкового притока оценивались системный или легочный венозные потоки на присутствие обратной предсердной волны. Оценивалась средняя величина пяти последовательных пиков скоростей А- и Е-волн, а также соотношение А/Е [11].
Результаты
В раннем послеоперационном периоде умерли 4 (4%) пациента (у 2 больных – острая сердечная недостаточность, у 1 больного – острое нарушение мозгового кровообращения, у 1 – кровотечение). На сходе с ИК синусовый ритм был у 59 пациентов, ритм ЭКС по причине полной АВ-блокады – у 26, ФП – у 11. Осложнения раннего послеоперационного периода: кровотечения, потребовавшие реторакотомии, – у 8 (8%) пациентов, транзиторные нарушения мозгового кровообращения – у 2 (2%) пациентов, почечная недостаточность – у 3 (3%) пациентов (в одном случае потребовалось подключение гемодиализа), имплантация ЭКС – у 12 (12%) пациентов. Средняя продолжительность пребывания пациентов в ОРИТ и в стационаре составила 2,8 ± 1,1 сут (1,4–10,8 сут.) и 12,9 ± 6,2 сут. (7–30 сут.) соответственно. По сердечному ритму пациенты перед выпиской из стационара распределились следующим образом: синусовый ритм – 72 (75%) пациента, ритм ЭКС – 12 (12,5%) пациентов, ФП/ТП – 12 (12,5% пациентов).
Средняя длительность и полнота динамического наблюдения составили 10,1 ± 4,1 мес. (0,5–15 мес.) и 93, 75% (связь с 6 пациентами отсутствует), соответственно. Динамика изменения сердечного ритма по данным ЭКГ за послеоперационные периоды, равные 1, 6 и 12 мес., приведена в таблице 1.
Число пациентов и степень восстановления транспортной функции предсердий (наличие А- и Е-волн) за те же временные интервалы приведены в таблице 2.
По истечении 6 мес. после вмешательства ФП наблюдалась у 11 (15,5%) пациентов, 12 мес. – у 5 (12,8%) больных (у 5 пациентов без изменений наблюдалась ФП за первый послеоперационный год, у 3 – восстановился синусовый ритм); ритм ЭКС – у 8 (11,3%) пациентов на 6 мес. и у 4 (10,2%) – на 12 мес. (из 8 пациентов лишь у 3 была ФП с брадикардией, у остальных 5 пациентов наблю-
Арутюнян В.Б., Чрагян В.А.
РЕЗУЛЬТАТЫ ХИРУРГИЧЕСКОЙ ИЗОЛЯЦИИ ЛЕВОГО ПРЕДСЕРДИЯ В ЛЕЧЕНИИ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ У ПАЦИЕНТОВ С ИБС И ПАТОЛОГИЕЙ МИТРАЛЬНОГО КЛАПАНА
Табл. 1. Динамика изменения сердечного ритма на 1, 6 и 12 мес. послеоперационного периода
За весь период динамического наблюдения был лишь один случай острого нарушения мозгового кровообращения (ОНМК) с левосторонней гемиплегией через месяц после оперативного вмешательства. Свобода от ОНМК по истечении первого послеоперационного года составила 98,7% (рис. 3). С целью выявления предикторов наличия ФП по истечении 6 и 12 послеоперационных месяцев была проведена статистическая обработка периоперационных данных путем логистической регрессии, или унивари-абельного анализа, результаты которого приведены в таблице 3.
По результатам унивариабельного анализа статистически значимыми предикторами наличия ФП являлись: на 6-й послеоперационный месяц – увеличение диаметра фиброзного кольца МК (ОШ 1,47; р = 0,027; ДИ 1,04–2,08); на 12-й послеоперационный месяц – размер задней стенки левого желудочка (ОШ 0,34; р = 0,01; ДИ 0,15–0,774); использование β -блокаторов в послеоперационном периоде (ОШ 0,076; р = 0,01; ДИ 0,01–0,34); недостаточность трикуспидального клапана, равная 2+ и более (ОШ 11; р = 0,038; ДИ 1,13–106,4).
В финальной модели многофакторного регрессионного анализа периоперационными факторами риска наличия ФП на 6-й и 12-й послеоперационные месяцы являлись: увеличение диаметра фиброзного кольца МК (ОШ 1,47; р = 0,027; ДИ 1,04–2,08); недоста-
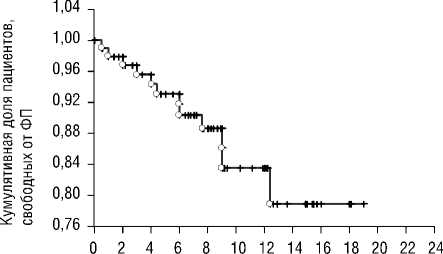
Месяцы о Заверш. + Цензурир.
Рис. 2. Свобода от ФП на первый послеоперационный год
Табл. 2. Динамика изменения сократительной функции ЛП и/или ПП по ЭхоКГ-данным на 1, 6 и 12 мес. послеоперационного периода
|
Сократительная функция ЛП и/или ПП |
Число пациентов, абс. (%) |
||
|
1 мес. (n = 96) |
6 мес. (n = 71) |
1 год (n = 39) |
|
|
Есть |
2 (2) |
32 (45) |
18 (46,2) |
|
Отсутствует |
94 (94) |
39 (55) |
21 (53,8) |
Табл. 3. Результаты унивариабельного анализа периоперационных факторов риска наличия ФП
|
Показатель |
6-й послеоперационный месяц |
12-й послеоперационный месяц |
||||
|
ОШ |
p |
95% ДИ |
ОШ |
p |
95% ДИ |
|
|
Возраст |
0,98 |
0,77 |
0,91–1,07 |
0,95 |
0,281 |
0,87–1,04 |
|
Артериальная гипертония |
0, 47 |
0,471 |
0,13–2,41 |
0,97 |
0,782 |
0,22–4,14 |
|
СН, ФК по NYHA ≥ II |
0,47 |
0,297 |
0,11–1,94 |
0,23 |
0,094 |
0,043–1,27 |
|
ББС |
0,47 |
0,556 |
0,39–5,67 |
0,312 |
0,359 |
0,02–3,765 |
|
ППТ |
1,64 |
0,813 |
0,26–103,1 |
0,405 |
0,671 |
0,006-23,1 |
|
КДО ЛЖ |
1,01 |
0,856 |
0,98–1,01 |
1,01 |
0,165 |
0,99–1,03 |
|
КСО ЛЖ |
1,006 |
0,545 |
0,98–1,02 |
1,01 |
0,140 |
0,99–1,04 |
|
КДР ЛЖ |
0,88 |
0,272 |
0,70–1,12 |
1,1 |
0,384 |
0,88–1,36 |
|
КСР ЛЖ |
0,666 |
0,152 |
0,38–1,16 |
1,03 |
0,729 |
0,84–1,27 |
|
МЖП, размер |
0,876 |
0,466 |
0,61–1,24 |
0,63 |
0,065 |
0,39–1,02 |
|
ЗСЛЖ, размер |
0,77 |
0,291 |
0,47–1,24 |
0,34 |
0,010 |
0,15–0,774 |
|
ЛП, размер |
1,08 |
0,110 |
0,98–1,20 |
1,02 |
0,430 |
0,93–1,11 |
|
ЛП, объем |
1,004 |
0,710 |
0,97–1,03 |
1,001 |
0,929 |
0,97–1,02 |
|
ФВ ЛЖ |
0,97 |
0,370 |
0,91–1,03 |
0,96 |
0,365 |
0,90–1,03 |
|
ПП, размер |
1,03 |
0,347 |
0,95–1,12 |
1,05 |
0,235 |
0,96–1,14 |
|
ФКМК, размер |
1,47 |
0,027 |
1,04–2,08 |
1,14 |
0,323 |
0,87–1,54 |
|
КТК, размер |
1,31 |
0,905 |
0,99–1,73 |
3,53 |
0,176 |
0,56 -22,2 |
|
Давление в ЛА |
1,003 |
0,905 |
0,94–1,06 |
1,000 |
0,976 |
0,93–1,06 |
|
Вмешательство на ТК |
2,2 |
0,215 |
0,63–7,66 |
1,33 |
0,650 |
0,38–4,62 |
|
КШ |
1,06 |
0,939 |
0,22–4,98 |
1,22 |
0,800 |
0,25–6,01 |
|
Время пережатия Ао |
0,92 |
0,833 |
0,47–1,83 |
0,99 |
0,978 |
0,95–1,04 |
|
Время ИК |
0,79 |
0,675 |
0,32–1,95 |
0,55 |
0,141 |
0,24–1,22 |
|
Время ИВЛ |
0,76 |
0,089 |
0,55–1,04 |
0,892 |
0,292 |
0,72–1,10 |
|
Бета-блокаторы в п/о периоде |
0,45 |
0,215 |
0,13–1,58 |
0,076 |
0,001 |
0,01–0,34 |
|
НТК 0–1+ |
1,16 |
0,876 |
0,16–8,09 |
1,81 |
0,538 |
0,27–12,1 |
|
НТК ≥ 2+ |
0,75 |
0,757 |
0,12–4,67 |
11 |
0,038 |
1,13–106,7 |
|
НМК 0–1+ |
0,6 |
0,748 |
0,026–13,5 |
1,285 |
0,814 |
0,15–10,4 |
|
НМК ≥ 2+ |
1,44 |
0,804 |
0,079–26,2 |
0,514 |
0,413 |
0,10–2,52 |
Примечание : СН – сердечная недостаточность, ФК – функциональный класс, НМК – недостаточность митрального клапана, НТК – недостаточность трикуспидального клапана, ИК – искусственное кровообращение, ИВЛ – искусственная вентиляция легких, ФКМК фиброзное кольцо митрального клапана, КТК – кольцо трикуспидального клапана, ПП – правое предсердие, ЛП – левое предсердие, ЛА – легочная артерия, МЖП – межжелудочковая перегородка, ЗСЛЖ – задняя стенка левого желудочка, КДО – конечный диастолический объем, КСО – конечный систолический объем, КДР – конечный диастолический размер, КСР – конечный систолический размер, ББС – болезнь брахиоцефальных сосудов.
Арутюнян В.Б., Чрагян В.А.
РЕЗУЛЬТАТЫ ХИРУРГИЧЕСКОЙ ИЗОЛЯЦИИ ЛЕВОГО ПРЕДСЕРДИЯ В ЛЕЧЕНИИ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ У ПАЦИЕНТОВ С ИБС И ПАТОЛОГИЕЙ МИТРАЛЬНОГО КЛАПАНА
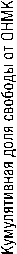
1,002 .
1,000
0,998
0,996
0,994
0,992
0,990
0,988
0,986

8 W 12 14 16 18
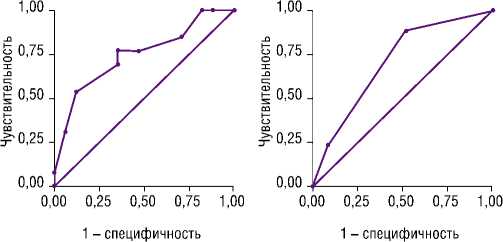
Рис. 4. Кривые RОС: А – область под кривой ROC равна 0,74 для дискриминации модели увеличения диаметра ФК МК; Б – область под кривой ROC равна 0,70 для дискриминации модели недостаточности трикуспидального клапана 2+ и более
Месяцы о Заверш. + Цензурир.
Рис. 3. Свобода от ОНМК на первый послеоперационный год
точность трикуспидального клапана, равная 2+ и более (ОШ 11; р = 0,038; ДИ 1,13–106,4).
Для разработки окончательной модели использовался тест «отношение правдоподобия» (Likelihood Ratio test; р = 0,001). Калибровка заключительной модели была измерена с использованием теста «критерий согласия» (Hosmer-Lemeshow goodness-of-fit test; p = 0,35) для 10 групп, что указывает на хорошую калибрацию модели. Дискриминация модели была измерена кривой ROC (Receiver Operating Characteristic – функциональные характеристики приемника). Для данных моделей области под кривой ROC равнялась 0,74 (увеличение диаметра ФК МК) и 0,70 (регургитация на ТК ≥ 2+), что указывает на хорошую дискриминацию моделей (рис. 4).
Обсуждение
ФП является наиболее частой, а порой и фатальной аритмией. Операция «лабиринт», разработанная J. Сox, способствует в большинстве случаев восстановлению синусового ритма. Однако выполнение данной процедуры занимает много времени, сопровождается определенными осложнениями, и множество хирургов отказываются от ее применения у полиморбидных пациентов, при низкой сократительной функции ЛЖ, в случаях необходимости дополнительных кардиохирургических процедур. С целью уменьшения потенциальных рисков некоторыми хирургами были предложены различные модификации данной процедуры, призванные минимизировать количество хирургических разрезов [8, 14]. Ранняя летальность в нашей группе больных составила 4%, что выше аналогичных данных в мировой литературе как при полных, так и при модифицированных операциях «лабиринт» при патологии МК (от 0,9 до 2,7%) [7, 8]. Характерно, что 4 случая смерти мы наблюдали у первых 44 пациентов, последующие 56 пациентов прооперированы без летальных исходов и ранних послеоперационных кровотечений. Большее накопление опыта позволит нам выявить реальные цифры летальности и осложнений.
Модифицированная процедура левопредсердного «лабиринта» с коррекцией патологии МК по результатам нашей работы показала суммарные для разных форм ФП удовлетворительные результаты со свободой от ФП, равной 83,5% на первый послеоперационный год. По результатам трехгодичного наблюдения, которое провели E. Raanani и соавт., восстановление синусового ритма наблюдалось также у 75% пациентов после операции «лабиринт» и вмешательств на МК [12]. По данным H. Izumoto и соавт., лишь 64,8% больных имели синусовый ритм после операций «лабиринт» с вмешательствами на МК на средний период линамического наблюдения сроком в 1,5 года [7]. Более низкие показатели восстановления синусового ритма в сравнении с результатами изолированного «лабиринта» связаны с наличием значимых сочетанных сердечных патологий [1, 2]. В нашем исследовании восстановление транспортной функции с наличием А- и Е-волн по данным допплер-ЭхоКГ на 1, 6 и 12 мес. составило 2, 45 и 46%, соответственно. Данное явление наблюдали K.B. Kim и соавт., у которых после процедуры лабиринт восстановление транспортной функции левого и правого предсердий наблюдалось в среднем через 69 ± 93 и 126 ± 135 дней, соответственно [11]. По результатам K.-G. Shyu и соавт., сократительная функция ЛП восстанавливается гораздо позднее ПП, что связано с большим вовлечением в ревматический процесс ЛП и наличием пораженного МК [13]. Именно по данной причине пациентам с аннулои вальвулопластикой МК, как при ишемической, так и при ревматической этиологии клапанных поражений, и с зафиксированным по ЭКГ синусовым ритмом мы назначаем антикоагулянтную терапию в послеоперационном периоде сроком на 3–4 мес., оставляя их в дальнейшем на приеме дезагрегантов. Нарушение мозгового кровообращения в нашем исследовании наблюдалось у 1 пациента, и свобода от неврологических нарушений составила на год 98,7%. В работе Z.A. Szalay и соавт. за 50 мес. динамического наблюдения лишь у одного пациента после процедуры «лабиринт» было
Арутюнян В.Б., Чрагян В.А.
РЕЗУЛЬТАТЫ ХИРУРГИЧЕСКОЙ ИЗОЛЯЦИИ ЛЕВОГО ПРЕДСЕРДИЯ В ЛЕЧЕНИИ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ У ПАЦИЕНТОВ С ИБС И ПАТОЛОГИЕЙ МИТРАЛЬНОГО КЛАПАНА острое нарушение мозгового кровообращения [15]. Нарушение мозгового кровообращения – редкое явление после операций «лабиринт».
В нашем исследовании независимыми периоперационными предикторами наличия ФП на 6-й и 12-й послеоперационные месяцы являлись увеличение диаметра фиброзного кольца МК и недостаточность трикуспидального клапана 2+ и более. Наличие такого предиктора, как увеличение диаметра фиброзного кольца МК, по всей вероятности объясняется тем, что в нашем исследовании 30% пациентов были с ишемической кардиомиопатией, ремоделированием левого желудочка и недостаточностью атриовентрикулярных клапанов. В исследовании Z.A. Szalay и соавт. независимыми предикторами невосстановления синусового ритма являлись наличие митральной регургитации и большой диаметр ЛП [15]. Большой диаметр ЛП также расценивался как независимый фактор риска в работе J. Kamata и соавт., однако в нашей работе пациентам с диаметром ЛП более 9 см процедура «лабиринт» не проводилась [9].
Наличие недостаточности трикуспидального клапана 2+ и более в предоперационном периоде является независимым предиктором невосстановления синусового ритма через 12 мес после операции вне зависимости от вида произведенной пластики. Видимо, данное явление связано с расширением фиброзного кольца ТК и расширением диаметра ПП. В некоторых исследованиях поздняя послеоперационная регургитация на ТК является фактором риска для возвратной ФП, и авторы советуют выполнять аннулопластику ригидными кольцами взамен пластики по Де Вега при оперативном вмешательстве [3, 16]. Мы придерживаемся превентивного подхода и производим аннулопластику по Де Вега в случае незначительной или умеренной регургитации с расширением кольца ТК.
Заключение
Операция левопредсердного «лабиринта» при ФП в сочетании с коррекцией патологии МК является эффективным методом восстановления синусового ритма по результатам раннего послеоперационного периода, которые сопоставимы с результатами других модификаций процедуры «лабиринт». Независимыми предикторами наличия ФП на 6 и 12 мес. являются увеличение диаметра фиброзного кольца МК и наличие трикуспидальной недостаточности 2+ и более в предоперационном периоде. Показания к проведению левопредсердного «лабиринта» остаются дискутабельными, и их определение требует дальнейшего накопления данных и более длительного периода наблюдения.
Список литературы Результаты хирургической изоляции левого предсердия в лечении фибрилляции предсердий у пациентов с ИБС и патологией митрального клапана
- Бокерия Л.А. Изолированная форма фибрилляции предсердий/Л.А. Бокерия, В.А. Базаев, А.Г. Филатов и др.//Анналы аритмологии. -2006. -№ 2. -С. 39-47.
- Бокерия Л.А. Опыт хирургического лечения фибрилляции предсердий в сочетании с коррекцией порока митрального клапана/Л.А. Бокерия, А.Ш. Ревишвили, Р.М. Муратов др.//Грудная и серд.-сосуд. хир. -2003. -№ 6. -С. 12-17.
- Beukema W.P. Predictive factors of sustained sinus rhythm and recurrent atrial fibrillation after a radiofrequency modified maze procedure/W.P. Beukema, H.T. Sie, A.R. Misier, P. P. Delnoy//Eur. J. Cardiothorac. Surg. -2008. -Vol. 34. -P. 771-775.
- Cox J.L. Modification of the maze procedure for atrial flutter and atrial fibrillation. II. Surgical technique of the maze III procedure/J. L. Cox, J. P. Boineau, R. B. Schues-sler et al.//J. Thorac. Cardiovasc. Surg. -1995. -Vol. 110. -P. 485-495.
- Fuster V. ACC/AHA/ESC guidelines for the management of patients with atrial fibrillation; executive summary/V. Fuster, L.E. Ryden, R.W. Asinger et al.//J. Am. Coll. Cardiol. -2001. -Vol. 38. -P. 1231-1266.
- Imai K. Clinical analysis of results of a simple left atrial procedure for chronic atrial fibrillation/K. Imai, T. Sueda, K. Orihashi et al.//Ann. Thorac. Surg. -2001. -Vol. 71. -P. 577-581.
- Izumoto H. Operative results after the Cox-Maze procedure combined with a mitral valve operation/H. Izumoto, K. Kawazoe, H. Kitahara, J. Kamata//Ann. Thorac. Surg. -1998. -Vol. 66. -P. 800-804.
- Johnson D.C. Early experience with the modified maze operation for atrial fibrillation with and without mitral valve surgery/D. C. Johnson//Aust. Assoc. J. Cardiac. Thorac. Surg. -1992. -Vol. 1. -P. 13-16.
- Kamata J. Predictors of sinus rhythm restoration after CoxMaze procedure concomitant with other cardiac operations/J. Kamata, K. Kawazoe, H. Izumoto et al.//Ann. Thorac. Surg. -1997. -Vol. 64. -P. 394-398.
- Ki-Bong K. Modifications of the Cox-Maze III procedure/K. Ki-Bong, H. Jae-Hak, H. K. Chang et al.//Ann. Thorac. Surg. -2001. -Vol. 71. -P. 816-822.
- Kim Y.H. Preoperative left atrial volume index is a predictor of successful sinus rhythm restoration and maintenance after the maze operation/Y. H. Kim, S.-C. Lee, A. Y. Her//J. Thorac. Cardiovasc. Surg. -2007. -Vol. 134. -P. 448-453.
- Raanani E. The efficacy of the Cox-Maze procedure combined with mitral valve surgery: a matched control study/E. Raanani, A. Albage, T.E. David et al.//Eur. J. Cardiothorac. Surg. -2001. -Vol. 19. -P. 438-442.
- Shyu K.-G. Recovery of atrial function after atrial compartment operation for chronic atrial fibrillation in mitral valve disease/K.-G. Shyu, J.-J. Cheng, J.-J. Chen et al.//J. Am. Coll. Cardiol. -1994. -Vol. 24. -P. 392-398.
- Sueda T. Efficacy of a simple left atrial procedure for chronic atrial fibrillation in mitral valve operations/T. Sueda, H. Nagata et al.//Ann. Thorac. Surg. -1997. -Vol. 63. -P. 1070-1075.
- Szalay Z.A. Long-term follow-up after the mini-maze procedure/Z. A. Szalay, W. Skwara, W. P. Kloevekorn et al.//Ann. Thorac. Surg. -2004. -Vol. 77. -P. 1277-1281.
- Tager R. Long-term follow-up of rheumatic patients undergoing left-sided valve replacement with tricuspid, annuloplasty validity of preoperative echocardiographic criteria in the decision to perform tricuspid annuloplasty/R. Tager, D. Skudicky, U. Mueller et al.//Am. J Cardiol. -1998. -Vol. 81. -P. 1013-1016.
- The National Heart, Lung, and Blood Institute Working Group on Atrial Fibrillation. Atrial fibrillation: current understandings and research imperatives/J. Am. Coll. Cardiol. -1993. -Vol. 22. -P. 1830-1834.


