Результаты эзофагэктомии с одномоментной пластикой пищевода в рамках программы РУПОР: одноцентровой опыт лечения 500 пациентов
Автор: Ручкин Д.В., Ковалерова Н.Б., Струнин О.В., Козлов В.А.
Журнал: Клиническая практика @clinpractice
Рубрика: Оригинальные исследования
Статья в выпуске: 4 т.16, 2025 года.
Бесплатный доступ
Обоснование. Эзофагэктомия с одномоментной эзофагопластикой — вмешательство высокого риска, сопряжённое с высокой частотой осложнений (до 74%) и госпитальной летальности (до 10% в высокопотоковых центрах). Для улучшения результатов лечения хирургических пациентов научное сообщество по ускоренной послеоперационной реабилитации (ERAS) выпустило рекомендации по периоперационному ведению пациентов. На основании элементов ERAS нами создана гибкая программа рациональной ускоренной периоперационной реабилитации (РУПОР), основанная на индивидуальном, командном, междисциплинарном подходе. Цель исследования — изучить результаты лечения пациентов после эзофагэктомии с одномоментной пластикой пищевода в рамках программы РУПОР. Методы. Проведено одноцентровое нерандомизированное ретроспективное исследование. В Национальном медицинском исследовательском центре хирургии имени А.В. Вишневского (НМИЦХ) в 2012–2024 годах выполнено 500 плановых первичных эзофагэктомий с одномоментной эзофагопластикой по поводу доброкачественных (54%) и злокачественных (46%) заболеваний пищевода. Медиана возраста прооперированных пациентов составила 59 лет, при этом 12,8% пациентов были старше 70 лет. Медиана индекса массы тела составила 23,5 кг/м2, но у 5,6% пациентов индекс был ниже 17 кг/м2. Медиана по стандартам Американского общества анестезиологов (ASA) составила 3, а ASA 4 набрали 8,6% пациентов. Предоперационную подготовку провели 27,8% пациентов, в 21,8% случаев выполнили коррекцию нутритивной недостаточности, в 7% — коррекцию заболеваний сердечно-сосудистой системы. На основании анализа данных историй болезней оценили согласно стандартам Консенсусной группы по осложнениям при эзофагэктомии (ECCG) летальность, частоту и тяжесть послеоперационных осложнений. Результаты. Послеоперационные осложнения наблюдали в 29,2% случаев (чаще диагностировали лёгочные осложнения — 22,4%; пневмония выявлена у 10% пациентов, желудочно-кишечные осложнения — у 7,8%), из них субтотальный/апикальный некроз трансплантата и несостоятельность пищеводного анастомоза развились в равном числе случаев — по 11 (по 2,2%). Инфекционные осложнения выявлены у 9,6% больных, урологические — у 7%, кардиальные — у 6,2%, тромбоэмболические — у 3%, неврологические — у 6,6 %, раневые — у 1,4%, прочие — у 4,8%. Послеоперационный хилоторакс развился в 0,2% наблюдений. Осложнения IIIb степени и тяжелее по Clavien-Dindo выявлены у 10,8% больных. Послеоперационная летальность составила 1,4%. Заключение. Внедрение программы РУПОР в практику НМИЦХ позволило расширить границы операбельности за счёт возрастных и коморбидных пациентов, отойти от критериев отбора пациентов в пользу выявления факторов риска и их коррекции.
Эзофагэктомия, эзофагопластика, ускоренная реабилитация, периоперационное обеспечение, рак пищевода, ахалазия, стриктура пищевода
Короткий адрес: https://sciup.org/143185362
IDR: 143185362 | DOI: 10.17816/clinpract689950
The results of esophagectomy with simultaneous esophagoplasty within the framework of the RAPOR program. Single-center experience of treating 500 patients
BACKGROUND: Esophagectomy (EE) with simultaneous esophagoplasty is a high risk intervention accompanied by the high rate of complications (up to 74%) and hospital mortality (up to 10% in the high-flow centers). For improving the results of treating the surgery patients, the Enhanced Recovery After Surgery (ERAS) society has issued the recommendations on the perioperative management of patients. Based on the ERAS elements, we have compiled a flexible program for rational accelerated perioperative rehabilitation (RAPOR) based on the individual, team-based and interdisciplinary approach. AIM: to evaluate the treatment results in the patients after the esophagectomy with simultaneous esophagoplasty within the frameworks of the RAPOR program. METHODS: a single-center non-randomized retrospective research was arranged. Within the premises of the National Medical Research Center of Surgery named after A.V. Vishenvsky (NMRCS), during the period of 2012–2024, 500 scheduled primary EE were performed with simultaneous esophagoplasty due to the presence of the benign (54%) and the malignant (46%) diseases of the esophagus. The median age was 59 years. With this, 12.8% of the patients were older than 70 years. The median BMI was 23.5 kg/m2, but in 5.6% of the patients it was lower than 17 kg/m2. The median ASA was grade 3, while ASA grade 4 was reported in 8.6% of the patients. The pre-operative preparation was carried out in 27.8% of the patients. A total of 21.8% had a correction of nutritional insufficiency, 7% — correction of the cardiovascular diseases. Based on the analysis of case history data, further evaluation included the mortality, the rate and the severity of post-operative complications using the Esophagectomy Complications Consensus Group (ECCG) score. RESULTS: post-operative complications were observed in 29.2% of the patients. The more often diagnosed complications were the pulmonary ones (22.4%). Pneumonia was found in 10% of the patients. The gastro-intestinal complications were verified in 7.8% of the patients. Of them, the subtotal necrosis of the transplant was developing in 11 (2.2%) patients, the apical necrosis of the transplant and the esophageal anastomosis failure were reported in 11 (2.2%) and 11 (2.2%) respectively. The infectious complications were observed in 9.6% of the patients, urological — in 7%, cardial — in 6.2%, thromboembolic — in 3%, neurological — in 6.6%, wound-related — in 1.4% and other types — in 4.8% of the patients. The post-operative chylothorax was developing in 0.2% of the cases. The complications with grade III-b and higher according to the Clavien-Dindo classification were observed in 10.8% of the patients. The post-operative mortality was 1.4%. CONCLUSION: the implementation of the RAPOR program into the practice of the NMRCS has allowed for expanding the operability margins due to the addition of the aged and the comorbid patients, moving away from the criteria for selecting the patients towards the detection of the risk factors and their correction.
Текст научной статьи Результаты эзофагэктомии с одномоментной пластикой пищевода в рамках программы РУПОР: одноцентровой опыт лечения 500 пациентов
Submitted 28.08.2025 Accepted 04.10.2025 Published online 17.12.2025



ОБОСНОВАНИЕ
История эзофагэктомии началась в США в 1913 году, когда F. Torek выполнил первую эзофагэктомию из торакотомного доступа с одномоментным соединением эзофаго- и гастростом наружной резиновой трубкой [1]. Следующая успешная эзофагэктомия с одномоментным формированием эзофагоеюноанастомоза была выполнена T. Oshawa в Японии только в 1933 году [2]. Развитие хирургической методики и периопера-ционного обеспечения эзофагэктомии происходило параллельно, попеременно опережая друг друга. Появление искусственной вентиляции лёг- ких и миорелаксантов «развязало руки» хирургам и позволило максимально усложнить оперативный приём, однако в 80-х годах ХХ века даже в центрах с большим опытом госпитальная летальность пациентов после эзофагэктомии составляла 6,0– 15,4% [3], а в конце 90-х годов — 5–10% [4].
Важной вехой в развитии хирургии в целом и пищеводной хирургии в частности стала разработка «ускоренной реабилитации» (fast-track surgery) Генрихом Кехлетом (Henrik Kehlet). Работы датского профессора о влиянии стресс-ответа организма на послеоперационные осложнения и факторах, снижающих его, способствовали эволюции пе-риоперационного обеспечения [5]. В результате в 2001 году с целью поиска путей оптимизации клинических результатов операций была основана Исследовательская группа европейских хирургов (Enhanced Recovery After Surgery Study Group, ERAS). В 2005 году вышли первые ERAS-протоколы для колоректальной хирургии. В 2010 году было организовано ERAS-сообщество, которое постепенно разработало рекомендации и протоколы для разных областей хирургии [6]. Рекомендации для эзофагэктомии были сформулированы в 2019 году [7]. В основе ERAS-концепции заложен командный мультидисциплинарный подход к пациенту, направленный на скорейшее послеоперационное восстановление и реабилитацию пациента.
Частота осложнений после эзофагэктомии оставалась высокой и варьировала от 17% [8] до 74% [9], однако анализ осложнений долгое время был затруднён из-за отсутствия единой системы учёта осложнений. Эту проблему решили в 2015 году, разработав унифицированный регистр осложнений — Esophagectomy Complications Consensus Group (ECCG) [10].
На основании протоколов ERAS многие специализированные хирургические центры создали соб- ственные протоколы периоперационного ведения пациентов. Так, в ФГБУ «Национальный медицинский исследовательский центр хирургии имени А.В. Вишневского» Минздрава России (ФГБУ НМИЦ хирургии им. А.В. Вишневского) в 2012 году внедрили программу рациональной ускоренной периоперационной реабилитации (РУПОР) пациентов после эзофагэктомии с одномоментной эзофагопластикой.
Цель исследования — изучить результаты лечения пациентов после эзофагэктомии с одномоментной пластикой пищевода в рамках программы рациональной ускоренной периоперационной реабилитации (РУПОР).
МЕТОДЫ
Дизайн исследования
В одноцентровое нерандомизированное ретроспективное исследование включили 500 пациентов после плановой первичной эзофагэктомии с одномоментной пластикой пищевода. На основании полученных данных оценивали летальность, частоту и тяжесть послеоперационных осложнений.
Критерии соответствия
Критерии включения: все пациенты после первичной эзофагэктомии с одномоментной эзофаго-пластикой в рамках программы рациональной ускоренной периоперационной реабилитации (РУПОР), выполненных одним оперирующим хирургом.
Критерии невключения: экстренное вмешательство; смена оперирующего хирурга.
Критерии исключения: эзофагэктомия без реконструктивного этапа.
Условия проведения
Исследование проведено в ФГБУ НМИЦ хирургии им. А.В. Вишневского.
Продолжительность исследования
Продолжительность ретроспекции — с 2012 по 2024 год.
Описание медицинского вмешательства
Лечение всех пациентов проводили в рамках программы РУПОР, включающей обязательный осмотр пациента на догоспитальном этапе междисциплинарной командой с оценкой индекса массы тела, индекса коморбидности Чарльсона (Charlson Comorbidity Index, CCI), степени анестезиологического риска по стандартам Американского общества анестезиологов (American Society иническая
эактика
Том 16 № 4
of Anesthesiologists, ASA), риска кардиальных осложнений по шкале Lee, риска нутритивной недостаточности по шкале NRS-2002 (Nutrition Risk Screening 2002). На основании полученных данных назначали объём предоперационного обследования и подготовки. При необходимости первым этапом проводили нутритивную терапию и коррекцию сопутствующей сердечно-сосудистой патологии.
После коррекции соматического статуса всем больным выполнили трансторакальную (в модификации McKeown) или трансхиатальную суб/то-тальную эзофагэктомию с одномоментной эзофа-гопластикой желудочной трубкой, толстой кишкой или комбинированным желудочно-тонкокишечным трансплантатом (рис. 1). За 2 часа до операции рекомендовали водную нагрузку высокоуглеводными напитками, а интраоперационно поддерживали нор-мотермию, нормоволемию; проводили протектив-ную вентиляцию лёгких, профилактику послеоперационной тошноты и рвоты, тромбоэмболических и инфекционных осложнений. Пациентам после торакального доступа устанавливали плевральный дренаж и дренаж в подпечёночное пространство (от назогастральной декомпрессии и дренирования шейной раны отказались в 2017 году). По окончании вмешательства пациентов в большинстве случаев экстубировали в операционной и переводили под наблюдение в отделение реанимации, где продолжали инфузионную, антибактериальную терапию и профилактику тромбоэмболических осложнений. Для обеспечения мультимодальной анальгезии ин-траперационно устанавливали паравертебральный катетер при торакотомии, эпидуральный катетер/ катетеры во влагалища прямых мышц живота.
Утром первого послеоперационного дня (1 ПОД) пациентов транспортировали в профильное отделение, удаляли мочевой катетер и плевральный дренаж при условии аэростаза и поступления менее 400 мл отделяемого. Подпечёночный дренаж удаляли на 2 ПОД. При классической схеме ведения пациентам назначали полное парентеральное питание до 5 ПОД. Затем выполняли рентгенологический или компьютерный томографический (КТ) контроль и разрешали пероральный приём воды. Приём протёртой пищи был возможен с 7 ПОД, после второго рентген-контроля. Раннее пероральное питание разрешали пациентам при удовлетворительном качестве шейного соустья (положительная интраоперационная оценка жизнеспособности желудочного трансплантата и культи пищевода), отсутствии аспирации и несостоятельности анастомоза при рентгенологическом контроле на 1 ПОД. При раннем начале питания на 1 ПОД назначали пероральный приём воды, с 2 ПОД — сиппинг (от англ. Sipping — питьё мелкими глотками), с 3 ПОД, после удовлетворительного рентген-контроля, — приём протёртой пищи.
Исходы исследования
Основной исход исследования: оценка частоты, качества и тяжести послеоперационных осложнений.
Дополнительные исходы исследования: оценка послеоперационной летальности.
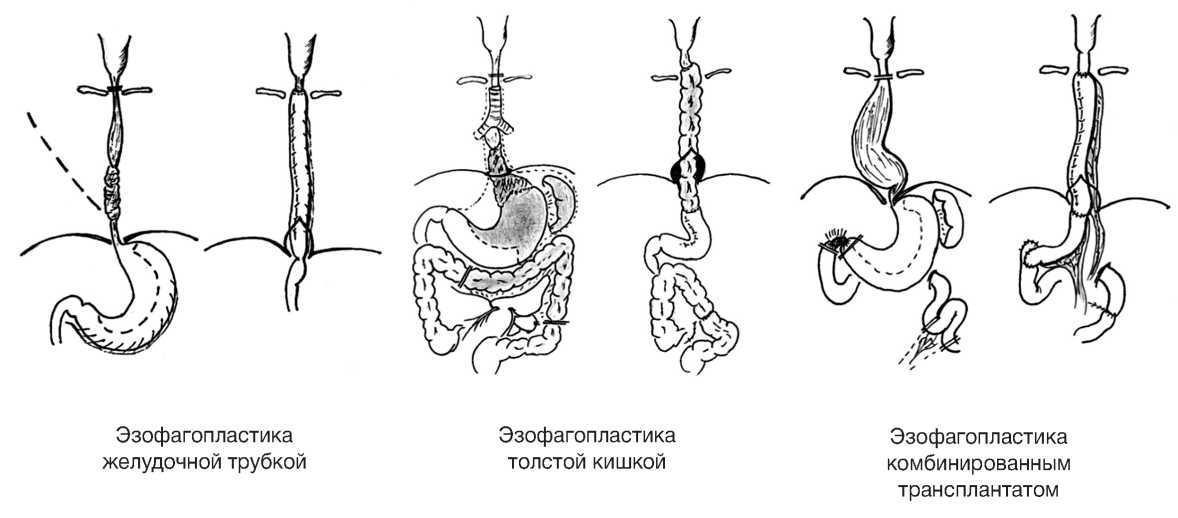
Эзофагопластика желудочной трубкой
Эзофагопластика толстой кишкой
Эзофагопластика комбинированным трансплантатом
Рис. 1. Схематическое изображение вариантов эзофагопластики желудочной трубкой, толстой кишкой, комбинированным желудочно-тонкокишечным трансплантатом.

kV ГА
Методы регистрации исходов
Для верификации осложнений пациентам выполняли рутинное рентген- или КТ-исследование органов грудной клетки и брюшной полости с пероральным контрастированием на 1 ПОД или 5 ПОД и 3 ПОД или 7 ПОД. Лабораторную оценку состояния пациента проводили на 1, 3–5 и 7–10 ПОД. При ухудшении состояния пациента для оценки жизнеспособности трансплантата или исключения кровотечения проводили КТ с внутривенным контрастированием и повторяли лабораторные тесты. Другие осложнения подозревали на основании клинических данных с последующим подтверждением лабораторными и инструментальными методами. Послеоперационные осложнения оценивали по унифицированному регистру ECCG. Тяжесть послеоперационных осложнений оценивали по классификации Clavien-Dindo. Изолированный гидроторакс, связанный с ранним удалением плеврального дренажа на 1 ПОД, за осложнение мы не считали.
Статистический анализ
Статистический анализ данных осуществляли с помощью программы R version 4.3.1 (2023). Описательная статистика представлена в виде абсолютной частоты для категориальной и медианы — для количественных переменных.
РЕЗУЛЬТАТЫ
Объекты (участники) исследования
Медиана индекса массы тела составила 23,5 кг/м2, но у 5,6% пациентов он был ниже 17 кг/м2. При оценке по шкале NRS-2002 17,6% больных набрали 4 балла и более. Медиана по ASA составила 3, а ASA 4 набрали 8,6% пациентов. Медиана индекса коморбидности — 3, но в 34% наблюдений — больше 5 баллов. В зависимости от этих показателей предоперационную подготовку провели 28,8% пациентов; 21,8% выполнили коррекцию нутритивной недостаточности (6,2% — парентеральное питание; 3,8% — назогастральный зонд; 5,2% — гастростома; 3,4% — бужирование пищевода; 0,8% — стентирование пищевода; 6,2% — сиппинг). Инвазивная диагностика и коррекция сопутствующей сердечно-сосудистой патологии потребовалась 7% пациентов (5,8% — коронарография; 1,6% — чрескожное коронарное вмешательство; 0,4% — установка постоянного кардиостимулятора; 0,4% — аортокоронарное шунтирование; 0,2% — аорто-бедренное шунтирование; 0,2% — транскатетерная имплантация аортального клапана; 0,4% — каротидная эндартерэктомия).
С 2017 года 97,4% пациентов экстубировали в операционной и перевели в отделение реанимации для дальнейшего наблюдения. Медиана пребывания в реанимации составила 0,67 суток. По программе раннего перорального питания прошли 96 (19,2%) пациентов. Медиана длительности послеоперационного периода составила 9 ПОД.
Основные результаты исследования
Послеоперационные осложнения развились у 29,2% пациентов. Все осложнения, классифицированные по ECCG, представлены в табл. 1. Чаще всего диагностировали лёгочные осложнения (22,4%). Пневмонию выявили у 50 (10%) пациентов. Вторыми по частоте были желудочно-кишечные осложнения (у 39; 7,8%). Наиболее жизнеугрожающее осложнение — субтотальный некроз трансплантата у 11 (2,2%) пациентов — закончилось его экстирпацией и выведением эзофаго- и гастро-/ еюностом. Апикальный некроз трансплантата у 11 (2,2%) и несостоятельность пищеводного анастомоза у 11 (2,2%) лечили консервативно (зондовое питание, дренирование раны, установка VAC-систем). Урологические осложнения, в основном в виде острой почечной недостаточности, выявили у 35 (7%) больных: большинству из них провели консервативное лечение, но в 10 (2%) случаях потребовалась заместительная почечная терапия. Кардиальные осложнения отметили у 31 (6,2%) больного: чаще осложнения проявлялись впервые выявленной фибрилляцией предсердий, которую лечили консервативно. Инфекционные осложнения выявили у 9,6% больных, тромбоэмболические — у 3%, неврологи- ческие — у 6,6%, раневые — у 1,4%, прочие — у 4,8%. Послеоперационный хилоторакс развился в 0,2% наблюдений.
У 92 (18,4%) пациентов осложнения относились к I, II и IIIa степени по классификации Clavien-Dindo: всем пациентам провели медикаментозное лечение или минимальное хирургическое вмешательство (пункционное лечение гидроторакса или пневмоторакса). Осложнения, вошедшие в эти группы, минимально повлияли на течение послеоперационного периода. Осложнения IIIb степени и тяжелее выявили в 54 (10,8%) случаях.
Летальный исход зафиксирован у 7 (1,4%) пациентов:
-
1) в 2014 году пациент в возрасте 23 лет с протяжённой ожоговой стриктурой пищевода скончался на 14 ПОД после трансхиатальной эзофагэктомии с одномоментной пластикой желудочной трубкой. При аутопсии — острая недостаточность мозгового кровообращения по ишемическому типу в бассейне правой внутренней сонной артерии;
Таблица 1
Эзофагэктомии с одномоментной пластикой: сравнение результатов НМИЦХ и международных исследований
|
Осложнения |
НМИЦХ n =500 (%) |
INC n =219 (%) |
ECCG n =2704 (%) |
DUCA n =1617 (%) |
|
Общее число осложнений |
146 (29,2) |
118 (54) |
1595 (59) |
1046 (65) |
|
Желудочно-кишечные осложнения |
39 (7,8) |
25 (11,4) |
606 (22,4) |
392 (24,2) |
|
Несостоятельность анастомоза / апикальный некроз трансплантата |
22 (4,4) |
12 (5,4) |
307 (11,4) |
307 (19) |
|
Суб-/тотальный некроз трансплантата |
11 (2,2) |
3 (1,3) |
34 (1,3) |
13 (1) |
|
Кишечная непроходимость, требующая вмешательства |
2 (0,4) |
1 (0,4) |
46 (1,7) |
12 (1) |
|
Обструкция тонкой кишки |
0 (0) |
3 (1,3) |
12 (0,4) |
4 (0,3) |
|
Осложнения, связанные с питательной стомой |
0 (0) |
2 (0,9) |
27 (1,0) |
55 (3,4) |
|
Осложнения, связанные с пилоромиотомией / пилоропластикой |
0 (0) |
1 (0,4) |
5 (0,2) |
6 (0,4) |
|
Инфекция, ассрциированная с Clostridium difficile |
0 (0) |
1 (0,4) |
23 (0,9) |
2 (0,1) |
|
Панкреатит |
5 (1) |
2 (0,9) |
8 (0,3) |
3 (0,2) |
|
Желудочно-кишечное кровотечение |
0 (0) |
0 (0) |
21 (0,8) |
1 (0,06) |
|
Нарушение функции печени |
1 (0,2) |
4 (1,8) |
6 (0,2) |
5 (0,3) |
|
Гастростаз, потребовавший назогастральной декомпрессии >7 ПОД или хирургического вмешательства |
0 (0) |
0 (0) |
180 (6,7) |
7 (1,7) |
|
Лёгочные осложнения |
112 (22,4) |
69 (31,5) |
752 (27,8) |
529 (32,7) |
|
Пневмония |
50 (10) |
40 (18,2) |
396 (14,6) |
341 (21,1) |
|
Гидроторакс, требующий дренирования |
83 (16,6) |
33 (15,0) |
267 (9,9) |
124 (7,7) |
|
Пневмоторакс, требующий дренирования |
27 (5,4) |
2 (0,9) |
91 (3,4) |
68 (4,2) |
|
Ателектаз, требующий бронхоскопии |
33 (6,6) |
6 (2,7) |
85 (3,1) |
18 (1,1) |
|
Дыхательная недостаточность, реинтубация |
18 (3,6) |
22 (10) |
189 (7,0) |
84 (5,2) |
|
Острый респираторный дистресс-синдром |
5 (1) |
6 (2,7) |
50 (1,8) |
24 (1,5) |
Таблица 1
kT
Продолжение
|
Осложнения |
НМИЦХ n =500 (%) |
INC n =219 (%) |
ECCG n =2704 (%) |
DUCA n =1617 (%) |
|
Острый аспирационный синдром |
7 (1,4) |
3 (1,3) |
27 (1,0) |
25 (1,6) |
|
Повреждение трахеобронхиального дерева |
0 (0) |
2 (0,9) |
11 (0,4) |
11 (0,7) |
|
Стояние плеврального дренажа >10 ПОД |
0 (0) |
1 (0,4) |
13 (0,5) |
11 (0,7) |
|
Кардиальные осложнения |
31 (6,2) |
51 (23,3) |
455 (16,8) |
276 (17,1) |
|
Остановка сердца (сердечно-лёгочная реанимация) |
2 (0,4) |
2 (0,9) |
28 (1,0) |
9 (0,6) |
|
Инфаркт миокарда |
0 (0) |
1 (0,4) |
15 (0,6) |
5 (0,3) |
|
Предсердная аритмия, потребовавшая лечения |
29 (5,8) |
50 (22,8) |
393 (14,5) |
224 (13,9) |
|
Желудочковая аритмия, потребовавшая лечения |
0 (0) |
0 (0) |
25 (0,9) |
23 (1,4) |
|
Застойная сердечная недостаточность, потребовавшая лечения |
2 (0,4) |
1 (0,4) |
12 (0,4) |
17 (1,1) |
|
Перикардит, потребовавший лечения |
0 (0) |
1 (0,4) |
2 (0,1) |
3 (0,2) |
|
Тромбоэмболические осложнения |
15 (3) |
5 (2,3) |
141 (5,1) |
45 (2,8) |
|
Тромбоз глубоких вен |
6 (1,2) |
2 (0,9) |
25 (0,9) |
4 (0,2) |
|
Тромбоэмболия лёгочной артерии |
6 (1,2) |
2 (0,9) |
33 (1,2) |
35 (2,2) |
|
Инсульт |
3 (0,6) |
1 (0,4) |
4 (0,1) |
1 (0,06) |
|
Тромбофлебит периферических вен |
4 (0,8) |
0 (0) |
79 (2,9) |
4 (0,25) |
|
Урологические осложнения |
35 (7) |
18 (8,2) |
224 (8,3) |
66 (4,1) |
|
Острая почечная недостаточность |
33 (6,6) |
11 (5,0) |
39 (1,4) |
11 (0,7) |
|
Острая почечная недостаточность, потребовавшая заместительную почечную терапию |
10 (2) |
6 (2,7) |
24 (0,9) |
5 (0,3) |
|
Инфекция мочевых путей |
3 (0,6) |
1 (0,4) |
68 (2,5) |
20 (1,2) |
|
Острая задержка мочи, потребовавшая установки катетера |
3 (0,6) |
0 (0) |
104 (3,8) |
32 (2) |
|
Инфекционные осложнения |
48 (9,6) |
28 (12,8) |
383 (14,2) |
120 (7,4) |
|
Раневая инфекция, потребовавшая открытого лечения или антибактериальной терапии |
5 (1) |
9 (4,1) |
20 (0,7) |
37 (2,3) |
|
Инфекция центрального катетера |
6 (1,2) |
6 (2,7) |
55 (2,0) |
10 (0,6) |
|
Внутригрудной/брюшной абсцесс |
10 (2) |
5 (2,3) |
65 (2,4) |
37 (2,3) |
|
Сепсис |
15 (3) |
12 (5) |
52 (1,9) |
17 (1,1) |
|
Другая инфекция, потребовавшая антибактериальной терапии |
20 (4) |
6 (2,7) |
227 (8,4) |
20 (1,2) |
|
Неврологические/психические осложнения |
33 (6,6) |
28 (12,8) |
254 (9,4) |
172 (10,6) |
|
Повреждение возвратного гортанного нерва |
19 (3,8) |
7 (3,1) |
114 (4,2) |
70 (4,3) |
|
Острый делирий |
15 (3) |
11 (5,0) |
105 (3,9) |
97 (6) |
|
Алкогольный делирий |
0 (0) |
3 (1,3) |
16 (0,6) |
2 (0,1) |
|
Прочие неврологические травмы |
6 (1,2) |
0 (0) |
33 (1,2) |
10 (0,6) |
|
Раневые/диафрагмальные осложнения |
7 (1,4) |
3 (1,4) |
78 (2,9) |
30 (1,9) |
|
Расхождение торакотомной раны |
0 (0) |
0 (0) |
40 (1,5) |
16 (1) |
|
Эвентрация |
7 (1,4) |
2 (0,9) |
33 (1,2) |
7 (0,4) |
|
Острая диафрагмальная грыжа |
0 (0) |
1 (0,4) |
8 (0,3) |
7 (0,4) |
|
Прочие осложнения |
24 (4,8) |
24 (11,0) |
185 (6,8) |
138 (8,5) |
|
Хилоторакс |
1 (0,2) |
12 (5,4) |
128 (4,7) |
139 (8,6) |
|
Повторная операция по причинам кроме желудочно-кишечного кровотечения, некроза или несостоятельности кондуита |
18 (3,6) |
7 (3,1) |
39 (1,4) |
17 (1,1) |
|
Полиорганная недостаточность |
8 (1,6) |
4 (1,8) |
27 (1,0) |
2 (0,1) |
|
Летальность |
7(1,4) |
2 (0,9) |
66 (2,4) |
27 (1,7) |
-
2) в 2015 году пациентка в возрасте 69 лет с ахалазией кардии IV стадии умерла на 11-й день после трансхиатальной эзофагэктомии с одномоментной пластикой желудочной трубкой. При аутопсии — некроз трансплантата, тромбоз в бассейне чревного ствола и верхней брыжеечной артерии;
-
3) в 2015 году больной раком пищевода сТ4NxM1 в возрасте 67 лет после трансторакальной эзофагэктомии с одномоментной пластикой желудочной трубкой скончался на 3 ПОД. Причина смерти — печёночная недостаточность на фоне цирроза печени и массивной интраоперационной кровопотери из-за выраженной портальной гипертензии;
-
4) в 2016 году больной раком пищевода сТ2NxM0 в возрасте 69 лет после трансторакальной эзофагэктомии с одномоментной пластикой желудочной трубкой скончался на 6 ПОД: из-за некроза кондуита развились острый респираторный дистресс-синдром и септический шок, повлёкшие летальный исход;
-
5) в 2016 году больной раком пищевода сТ4аNxM0 в возрасте 89 лет после трансхиатальной эзофагэктомии с одномоментной пластикой желудочной трубкой скончался на 12 ПОД вследствие аспирационной пневмонии и декомпенсации сердечной недостаточности;
-
6) в 2019 году пациентка в возрасте 29 лет с протяжённой ожоговой стриктурой пищевода после трансторакальной эзофагогастрэктомии с одномоментной пластикой толстой кишкой умерла на 8 ПОД. При аутопсии — неокклюзионная мезентериальная ишемия;
-
7) в 2020 году больной раком пищевода сТ4аN2M0 в возрасте 85 лет после трансхиатальной эзофагэктомии с одномоментной пластикой желудочной трубкой. На 5 ПОД в профильном отделении у него произошла аритмогенная или гипоксическая остановка сердечной деятельности. Длительные реанимационные мероприятия привели к постреанимационной болезни и вегетативному статусу. Скончался на 55 ПОД от гнойно-септических осложнений.
ОБСУЖДЕНИЕ
ECCG [18], при этом в исследования с низкой частотой осложнений включали только соматически здоровых пациентов (ASA I–II), а плевральный дренаж задерживали до 3 ПОД [15, 16]. Подробный разбор результатов лечения представлен также в многоцентровых датском (Dutch Upper Gastrointestinal Cancer Audit, DUCA, n =1617) [19], общеевропейском (ECCG, n =2704) [20] и американском ( n =9389) [21] исследованиях: частота осложнений по ECCG составила 63%, 59% и 64% соответственно, но об использовании ERAS-принципов авторы не заявляли. Отечественных публикаций, отражающих результаты лечения на большой выборке пациентов, мы не нашли.
После эзофагэктомии наиболее часто развиваются лёгочные осложнения (от 16,7% [22] до 32% [23]), основное место среди них занимает послеоперационная пневмония (от 0,77% [24] до 21,2% [25]). Вторыми по частоте являются предсердные нарушения ритма, входящие в структуру кардиальных осложнений (от 6,8% [20] до 25% [19]). К наиболее опасным относят специфические желудочно-кишечные осложнения, такие как несостоятельность пищеводного анастомоза (от 2,9% [26] до 19% [19]) и некроз трансплантата (0,5–10,4% [27]). Y. Akiyama и соавт. [25] публиковали данные об отсутствии несостоятельности анастомоза в исследовании из 33 человек, однако пациентов выписывали в среднем на 20 ПОД. Зачастую именно послеоперационная пневмония, несостоятельность анастомоза и некроз кондуита определяют длительность послеоперационного периода (от 7 [28] до 19,6 [25] ПОД) и летальность (от 0,8% [29] до 4,5% [20]).
На наш взгляд, наиболее корректным является сравнение результатов ФГБУ НМИЦ хирургии им. А.В. Вишневского с одноцентровым исследованием Ирландского центра (INC), выполненным в рамках ERAS-протокола. В INC включили только больных раком пищевода ASA I–III без дефицита массы тела. Всем пациентам интраоперационно выполнили пилоропластику и вывели еюностому для начала энтерального питания с 1 ПОД. Для сравнения использовали также многоцентровые исследования ECCG и DUCA. Классификацию осложнений во всех работах проводили по единому реестру ECCG (см. табл. 1).
Бросается в глаза, что исследование ERAS-концепции способствует снижению частоты несостоятельности анастомоза и апикального некроза кондуита (4,4% ФГБУ НМИЦ хирургии им. А.В. Вишневского и 5,4% INC против 11,4% ECCG и 19% DUCA). Более высокая частота некроза транс- плантата в ФГБУ НМИЦ хирургии им. А.В. Вишневского (2,2% против 1–1,3% в других исследованиях) связана с формированием более длинного кондуита для субтотального замещения пищевода. Типы операций, выполняемых в ФГБУ НМИЦ хирургии им. А.В. Вишневского, — причина отсутствия послеоперационного гастростаза, характерного для операции Lewis (6,7% ECCG). Благодаря программе РУПОР частота послеоперационной пневмонии в ФГБУ НМИЦ хирургии им. А.В. Вишневского значительно ниже, чем в других центрах (10% против 18,2%, 14,6% и 21,1% в INC, ECCG и DUCA соответственно). Кроме того, шейная локализация соустья, небольшая частота несостоятельности анастомоза и пневмонии способствовали редкости предсердных аритмий в частности (5,8% против 22,8%, 14,5% и 13,9%) и кардиальных осложнений в целом (6,2% против 23,3%, 16,8% и 17,1%). Относительно низкая частота послеоперационной пневмонии, нарушений ритма и несостоятельности анастомоза объясняет низкую частоту острого делирия в ФГБУ НМИЦ хирургии им. А.В. Вишневского (3% против 5%, 3,9% и 6%). Летальность после эзофагэктомии в рамках программы РУПОР была ниже, чем в многоцентровых исследованиях (1,4% ФГБУ НМИЦ хирургии им. А.В. Вишневского и 0,9% INC против 2,4% ECCG и 1,7% DUCA).
Внедрение программы РУПОР начали в 2012 году. Далее в течение 12 лет происходили её эволюция и модификация на основании полученного клинического опыта и новых научных данных. Отказались от дренирования шейной раны, установки 2–3 дренажей в брюшную полость, назогастральной декомпрессии, продлённой искусственной вентиляции лёгких, полипрагмазии, длительного послеоперационного голодания. Интраоперационная инфузионная терапия от либеральной сначала стала ближе к рестриктивной, а затем к цель-ори-ентированной. Сформулировали протоколы нутритивной терапии в пред- и послеоперационных периодах, внедрили раннее пероральное питание. Всё это отразилось на результатах лечения пациентов и отсутствии летальных исходов в период 2021–2024 годов.
Наша программа РУПОР строится на индивидуальном, командном и междисциплинарном подходе к каждому больному. Для пациента разрабатывают персональную программу ведения и подготовки на основании его возраста, физического, соматического, нутритивного и психологического статуса. Благодаря этому в ФГБУ НМИЦ хирургии им. А.В. Вишневского стало возможным безопасное лечение возрастных и коморбидных пациентов. Среди 500 больных индекс Чарльсона более 7 был у 12,2%, физический статус ASA IV — у 8,6%, а 12,8% пациентов были старше 70 лет. Из всего разнообразия элементов периоперационно-го обеспечения в программе РУПОР мы выбираем лишь те из них, которые приемлемы в клинической ситуации конкретного больного. Основное внимание в программе мы уделяем предоперационной подготовке пациента и коррекции всех модифицируемых факторов риска (сердечно-сосудистые заболевания, нутритивный статус и др.), что потребовалось 28,8% больных.
На наш взгляд, основной принцип программы РУПОР — приоритет программы над протоколом. Несмотря на то, что элементы ERAS лежат в основе программы РУПОР в качестве элементов периопе-рационного обеспечения, основное её отличие заключается в гибкости и отсутствии протокольного подхода. Имеются данные, что внедрение ERAS-протокола улучшает результат лечения пациентов только в случае его выполнения более чем на 70%. Но приверженность к нему значительно снижается у коморбидных пациентов и при открытых вмешательствах [30]. Проспективное исследование F. Puccetti и соавт. [28] также выявило, что в первые 48 часов лечения приверженность протоколам сохраняется высокой (82,7%), но затем значимо снижается из-за развития осложнений. В обзорном исследовании S. Salvans и соавт. [31] отмечено, что доля соответствия протоколу в мире в принципе остаётся низкой. Разработать универсальный протокол для крайне разнородной группы пациентов невозможно, поэтому лучше сделать выбор в пользу персонализации лечения и создания гибкой программы периоперационного обеспечения, а не протокола и стандартизации больных. При этом реализация конкретных анестезиологических, реанимационных и реабилитационных элементов происходит в соответствии с протоколом каждого из них, но в рамках гибкой общей программы.
Персонализированное лечение — второй принцип программы РУПОР. Стандартные элементы ПОО (периоперационное обеспечение)/ERAS/РУПОР (отказ от голодания и подготовки кишечника, нор-мотермия, нормоволемия, протективная вентиляция лёгких и др.) применимы в комплексе у среднестатистического пациента. Но у возрастных или коморбидных больных их дополняют специализированными лечебными методиками, исходя из имеющихся факторов риска послеоперационных осложнений и летальности или уже развившихся осложнений, при этом отказ от одного или нескольких стандартных элементов не отменяет следование программе.
Третий принцип программы РУПОР — создание междисциплинарной команды, которая занимается ведением больного в течение всего периопераци-онного периода. В основе ERAS-концепции лежит создание мультидисциплинарной команды, основными участниками которой являются хирурги, анестезиологи, медицинские сёстры, диетологи, физиотерапевты и узкопрофильные специалисты. В расширенных версиях в команду включают социальных работников, клинических фармацевтов, администраторов, статистиков для мониторинга результатов и специалистов по информационным технологиям для ведения электронных протоколов [32]. Мультидисциплинарная команда — большая группа людей, каждый член которой даёт свои рекомендации для лечения пациента. В литературе не найти исследований, критикующих этот вариант команды. Но при мультидисциплинарном подходе каждая дисциплина продолжает оставаться в своих границах, а специалисты работают параллельно и независимо друг от друга на потоке пациентов. При междисциплинарном подходе возможно более тесное взаимодействие меньшего числа специалистов, глубокая интеграция профессиональных знаний членов команды и их активное общение с ежедневным обсуждением плана ведения пациентов. Члены междисциплинарной команды (хирурги, анестезиолог, реаниматолог и медицинские сёстры) работают сообща в одном отделении. Один и тот же хирург и реаниматолог занимаются пациентом в пред- и послеоперационном периодах (в том числе на догоспитальном этапе, в отделении реанимации и интенсивной терапии, в профильном отделении), а в операционной работает один и тот же анестезиолог.
Внедрение программы РУПОР позволило отказаться от критериев отбора пациентов и перейти к оценке рисков осложнений и их коррекции. В итоге уменьшилось количество отказов в хирургическом вмешательстве из-за возраста или тяжести сопутствующих заболеваний.
Ограничения исследования
ЗАКЛЮЧЕНИЕ
Эзофагэктомия с одномоментной пластикой пищевода — операция с высокой частотой осложнений. Отказ от строгого протокола в пользу гибкой программы РУПОР, разработанной в ФГБУ НМИЦ хирургии им. А.В. Вишневского, позволил успешно оперировать даже высокорисковых возрастных и ко-морбидных пациентов, снизив при этом летальность, частоту осложнений в целом и жизнеугрожающих осложнений (пневмонии, некроза кондуита, несостоятельности анастомоза) в частности по сравнению с общемировыми показателями. Индивидуальный, командный, междисциплинарный подход вместе с качественным хирургическим пособием составляют основу обеспечения хирургии высокого риска.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Вклад авторов. Н.Б. Ковалерова — лечение пациентов, сбор данных, написание текста статьи; Д.В. Ручкин — техническое исполнение всех хирургических вмешательств, руководство лечением пациентов, написание текста статьи; О.В. Струнин, В.А. Козлов — поисково-аналитическая работа, обсуждение результатов исследования. Все авторы одобрили рукопись (версию для публикации), а также согласились нести ответственность за все аспекты работы, гарантируя надлежащее рассмотрение и решение вопросов, связанных с точностью и добросовестностью любой её части.
Этическая экспертиза. Организация исследования одобрена локальным этическим комитетом ФГБУ «Национальный медицинский исследовательский центр хирургии имени А.В. Вишневского» Министерства здравоохранения Российской Федерации (протокол № 007-2024 от 25.10.2024). Все участники исследования добровольно подписали форму информированного согласия до включения в исследование.
Источники финансирования . Исследование выполнено без привлечения внешнего финансирования.
Раскрытие интересов. Авторы заявляют об отсутствии конфликта интересов, связанных с данной публикацией.
Оригинальность. При проведении исследования и создании настоящей работы авторы не использовали ранее опубликованные сведения (текст, иллюстрации, данные).
Доступ к данным. Редакционная политика в отношении совместного использования данных к настоящей работе неприменима, данные могут быть опубликованы в открытом доступе.
Генеративный искусственный интеллект. При создании настоящей статьи технологии генеративного искусственного интеллекта не использовали.
ADDITIONAL INFORMATION
Author contributions: N.B. Kovalerova , treatment of patients, data collection, writing the text of the article; D.V. Ruchkin , the operator of all surgical interventions, management of patient treatment and discussion of the results of the study, O.V. Strunin , V.A. Kozlov search and analytical work, discussion of the results of the study. Thereby, all authors provided approval of the version to be published and agree to be accountable for all aspects of the work in ensuring that questions related to the accuracy or integrity of any part of the work are appropriately investigated and resolved.
Ethics approval: The organization of the study was approved by the local Ethics Committee of the Vishnevsky National Medical Research Center for Surgery of the Ministry of Health of the Russian Federation (Protocol No. 007-2024 dated 2024 Oct 25). All study participants signed an informed consent form before being included in the study.
Funding sources: The study was carried out without attracting external funding.
Disclosure of interests: The authors declare no conflict of interests.
Statement of originality: The authors did not utilize previously published information (text, illustrations, data) in conducting the research and creating this paper.
Data availability statement: The editorial policy regarding data sharing does not apply to this work, data can be published as open access.
Generative AI: Generative AI technologies were not used for this article creation.


