Роль адгезивных молекул VCAM-1 и VE-кадгерина в развитии дисфункции эндотелия при геморрагической лихорадке с почечным синдромом
Автор: Байгильдина Асия Ахметовна
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Биохимия
Статья в выпуске: 4 т.5, 2009 года.
Бесплатный доступ
Цель исследования - определение содержания молекул клеточной адгезии (МКА) VCA M-1 и VE-кадгерина в крови больных геморрагической лихорадкой с почечным синдромом (ГЛПС) и оценка их роли в развитии дис- функции эндотелия (ДЭ ). Обследованы 87 больных ГЛПС в возрасте от 15 до 65 лет. Концентрации sVCA M-1 и VE-кадгерина в сыворотке крови определены с помощью наборов компании Bender MedSystems (Австрия). Концентрация sVCA M-1 во все периоды при среднетяжелой и тяжелой неосложненной формах ГЛПС статисти- чески значимо выше контроля с максимумом в периоды олигурии. При осложненной форме уровень данной МКА наиболее высок в лихорадочном периоде с последующим резким, 6-кратным по сравнению с контролем, снижением к периоду олигурии и тенденцией к нормализации к периоду реконвалесценции. Содержание VE- кадгерина преимущественно статистически значимо ниже контроля во всех исследуемых группах больных за исключением периода лихорадки среднетяжелой формы. Между уровнями изучаемых МКА выявлена преи- мущественно отрицательная корреляция средней силы. Усиление экспрессии эндотелиоцитами VCA M-1 при ГЛПС ассоциируется с развитием адгезионной формы ДЭ, снижение экспрессии VE-кадгерина - с развитием ее ангиогенной формы. Изменения в представлении клетками эндотелия данных МКА носят адаптивный характер и преследуют цель ограничения повреждающего действия на него возбудителя ГЛПС.
Ve-кадгерин, дисфункция эндотелия, геморрагическая лихорадка с почечным синдромом
Короткий адрес: https://sciup.org/14916950
IDR: 14916950
Role of adhesion molecules VCAM-1 and VE-cadherin in endothelium dysfunction development at hemorrhagic fever with renal syndrome
The research goal is to determine the changes in concentration of both sVCA M-1 and VE-cadherin in blood serum of patients suffered from hemorrhagic fever with renal syndrome (HF RS). 87 patients aged 15 - 65 were examined. Concentrations of both sVCA M-1 and VE- cadherin in blood serum by means of Bender MedSystems (Austria) EL ISA test were determined. It was shown that in both medium severe and severe forms of HF RS statistically the significant rise of sVCA M-1 concentration in blood with high indices in oliguric period took place. Complicated form was characterized by high indices of sVCA M-1 level in fever period, extremely decreasing in concentration in oliguric period and tendency to normalizing in clinical convalescence period. VE-cadherin level in blood was predominantly lower than control in all the observed groups with the exception of fever period in group with medium severe disease form. Negative correlation of normal intensity between adhesion molecules levels in blood was revealed. In conclusion it is necessary to point out that high VCA M-1 expression by endotheliocytes evidences the development of an adhesion form of endothelial dysfunction, low VE-cadherin production in a base for development of angiogenic form of endothelial dysfunction and changes in expression of these adhesion molecules that have adaptive metabolic response to macroorganism of HF RS pathogenic action.
Текст научной статьи Роль адгезивных молекул VCAM-1 и VE-кадгерина в развитии дисфункции эндотелия при геморрагической лихорадке с почечным синдромом
ежегодной заболеваемости отмечаются в Уральском, Поволжском и Центральном федеральных округах, в том числе и в Республике Башкортостан, определяя 60-90% всей заболеваемости ГЛПС по России. Патогенез ГЛПС к настоящему времени изучен далеко не полностью, что объяснимо, с одной стороны, весьма сложным механизмом развития заболевания, с другой, – отсутствием экспериментальной модели для его изучения. Возбудитель ГЛПС – вирус Hantaan, серотип Puumala, относящийся к сферическим однони-тевым РНК-содержащим вирусам, обладает тропизмом к клеткам эндотелия сосудов [3]. Этот монослой клеток, выстилающих внутреннюю поверхность сосудов и полостей сердца, не только выполняет функцию барьера между кровью и подлежащими тканями, но и является огромной эндокринной железой, секретирующей вазорегуляторы, про- и антикоагулянты, факторы роста, молекулы клеточной адгезии, цитокины, активные формы кислорода и т.д. [4]. Длительное воздействие на эндотелий хантавируса, равно как и других повреждающих агентов (гипоксия, интоксикация, гиперхолестеринемия, гипергликемия, цитокины, малые молекулы), ведет к изменению спектра выделяемых им веществ с усилением синтеза одних и торможением продукции других. Подобные изменения эндотелия, обозначаемые как его дисфункция, наблюдаются при многих патологических состояниях, в частности, при атеросклерозе, сахарном диабете, гипертонической болезни, ИБС и др. [5, 6]. В их патогенезе значительная роль отводится молекулам клеточной адгезии, которые вовлекаются в патогенез заболеваний в самые ранние сроки, обусловливая развитие в ней воспалительной реакции, повышение проницаемости, структурную дезорганизацию и др. [7,8,9].
Целью исследования явилось определение содержания молекул клеточной адгезии VCAM-1 и VE-кадгерина в крови больных ГЛПС в зависимости от периода и тяжести и оценка их роли в развитии дисфункции эндотелия при данном заболевании.
Методы. В исследование включили 87 больных с серологически подтвержденным методом непрямых флюоресцирующих антител диагнозом ГЛПС (69 мужчин и 18 женщин) в возрасте от 15 до 65 лет (средний возраст 38,2±3,6 года), находившихся на стационарном лечении в МУ “Инфекционная клиническая больница № 4” г. Уфы и в отделении гемодиализа Республиканской клинической больницы им. Г.Г. Куватова в 2005-2008 годах. Критериями исключения из исследования явились наличие в анамнезе гипертонической болезни, болезней сердца и сосудов, сахарного диабета, злокачественных заболеваний, заболеваний печени и почек. При определении степени тяжести ГЛПС использовали классификацию Б.З. Сиротина [10]. Среднетяжелая форма выявлена у 47 больных (54,0%), тяжелая без осложнений – у 23 больных (26,4%), тяжелая с осложненным течением – у 17 больных (19,6%). Группу сравнения составили 23 практически здоровых лица, сопоставимых по полу и возрасту. Кровь брали утром натощак в стандартных условиях. Образцы сыворотки хранили при -20є С до момента исследования. Концентрации sVCAM-1 и VE-кадгерина в сыворотке крови определяли с помощью иммуноферментных наборов для количественного определения VCAM-1 и VE-кадгерина соответственно в человеческой сыворотке крови и других биологических жидкостях компании “Bender MedSystems” (Австрия) и выражали в нг/мл. Абсорбцию света регистрировали с помощью ИФА-ридера “Bench mark” компании “Bio-Rad”. Обработку результатов исследования проводили с использованием стандартного статистического пакета программ Statistica 7.0 for Windows: определяли медиану, интерквартильный интервал [25%, 75%], достоверность межгрупповых различий средних величин оценивали при помощи критерия Манна-Уитни, зависимость между отдельными показателями выявляли с помощью корреляционного анализа по Спирмену. Критический уровень достоверности нулевой статистической гипотезы р принимали равным 0,05.
Результаты. Определение в сыворотке крови больных ГЛПС содержания молекул адгезии sV-CAM-1 и VE-кадгерина показало, что они в равной степени зависят как от периода, так и от степени тяжести заболевания. Уровень sVCAM-1 при среднетяжелой форме болезни статистически значимо высок на всем протяжении болезни с плавным подъемом от периода лихорадки к периоду олигурии (2030 [1665; 2345] нг/мл против 963 [915; 1103] нг/мл для группы контроля) и последующим статистически незначимым снижением от периода полиурии к периоду восстановленного диуреза (до 1552 [1240; 1700] нг/ мл) (рис. 1). Тяжелая форма болезни без осложнений также характеризуется статистически значимым подъемом содержания данной МКА, однако обращает на себя внимание статистически значимо более низкий, по сравнению со среднетяжелой формой, ее уровень в лихорадочный период с последующим резким (в 3,3 раза выше контрольных значений) скачком к периоду олигурии и таким же резким, но статистически незначимым спадом к периодам полиурии и восстановления диуреза. Присоединение осложнений (инфекционно-токсического шока Ι-ΙΙ степени, острой почечной недостаточности с переводом на гемодиализ, синдрома диссеминированного внутрисосудистого свертывания крови, острой дыхатель-
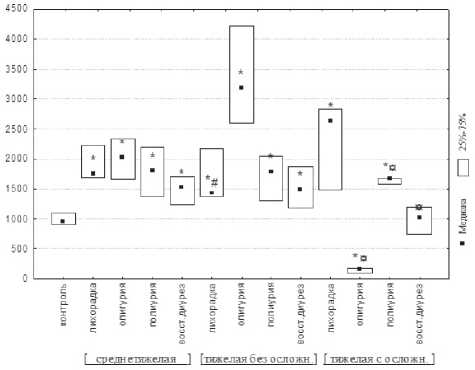
Рис. 1. Концентрация sVCAM-1 в сыворотке крови больных ГЛПС различной степени тяжести на фоне базисной лекарственной терапии (нг/мл); * – статистическая значимость различий с контролем, # – статистическая значимость различий со среднетяжелой формой, ¤ – статистическая значимость различий с тяжелой формой без осложнений
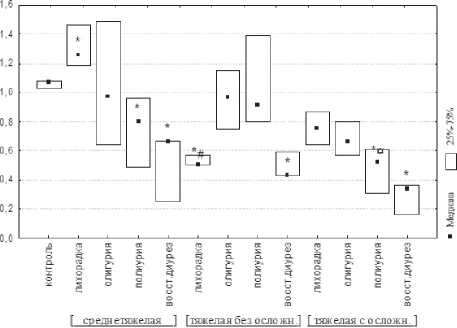
Рис. 2. Концентрация VE-кадгерина в сыворотке крови больных ГЛПС различной степени тяжести на фоне базисной лекарственной терапии (нг/мл); * – статистическая значимость различий с контролем, # – статистическая значимость различий со среднетяжелой формой, ¤ – статистическая значимость различий с тяжелой формой без осложнений ной недостаточности, острого эрозивного гастрита) обусловливает отличную от остальных форм ГЛПС динамику изменения концентрации sVCAM-1 с максимумом уже в лихорадочный период (2625 [1475; 2825] нг/мл), последующим 6-кратным по сравнению с контролем снижением к периоду олигурии, повторным подъемом к периоду полиурии и статистически значимой нормализацией при восстановлении диуреза.
Динамика изменения уровня VE-кадгерина в сыворотке крови больных ГЛПС практически прямо противоположна таковой для молекулы адгезии сосудистого эндотелия: концентрация кадгерина имеет преимущественно тенденцию к снижению вплоть до периода восстановленного диуреза, и наиболее существенные сдвиги наблюдаются у больных с тяжелой формой ГЛПС с осложненным течением (рис. 2). Особенностью среднетяжелой формы является отличная от других форм болезни статистически значимо высокая концентрация данной молекулы в лихорадочный период – 1,26 [1,46; 1,51] нг/мл против 1,07 [1,03; 1,08] нг/мл для группы контроля, однако в последующем наблюдается постепенный спад с минимальным значением в последний период – восстановленного диуреза (в 1, 6 раза ниже контрольных значений). Неосложненная форма заболевания начинается, напротив, со статистически значимо низкой концентрации исследуемой МКА в сыворотке крови – в 2, 15 раз ниже контрольных показателей и, несмотря на тенденцию к нормализации к периодам олигурии и полиурии, при восстановлении диуреза практически возвращается к уровню, имевшему место в лихорадочный период. При осложненной форме ГЛПС имеет место сходная со среднетяжелой формой картина изменения концентрации VE-кадгерина: плавный спад его уровня от периода лихорадки к периоду восстановления диуреза. Нормализации содержания данной адгезивной молекулы на фоне базисной лекарственной терапии к периоду клинического выздоровления не происходит.
Корреляционный анализ между концентрациями в сыворотки крови больных ГЛПС VCAM-1 и VE-кадгерина по Спирмену выявил преимущественно отрицательную связь средней силы, за исключением периода лихорадки при среднетяжелой форме, при которой наблюдается положительная корреляция средней силы (см. таблицу).
Обсуждение. VCAM-1 (vascular cell adhesion molecule), (CD 106) – гликопротеин, экспрессируемый на поверхности только активированного эндотелия; его лигандом является интегрин a-4-b-1 (VLA-1, Very late activating antigen), экспрессируемый лейкоцитами. VCAM-1 обеспечивает привлечение лейкоцитов к активированному эндотелию сосудов с целью ограничения повреждающего действия различного рода факторов. VE-кадгерин (vascular endothelial сadherin) представляет собой кальций-связывающий белок, контролирующий образование межклеточных адгезивных соединений и обеспечивающий взаимодействие между эндотелиальными клетками в слоях, что уменьшает межклеточную проницаемость для молекул с высоким молекулярным весом и степень миграции клеток через повреждённую область. Внутриклеточный домен Е-кадхерина взаимодействует с β-катенином и далее через α-катенин – с цитоскелетом. Таким образом формируется прочный каркас для эндотелия. В результате проведенных исследований у больных ГЛПС выявлены изменения содержания в сыворотке крови изучаемых субстанций, ответственных за включение универсальной защитной реакции организма на повреждение эндотелиальной выстилки сосудов хантавирусом – воспалительной реакции. Антигенная стимуляция вирусом ГЛПС приводит к секреции макрофагами, активированными эндотелиоцитами, натуральными киллерами и другими клетками цитокинов «первого поколения» – ИЛ-1, ИЛ-6 и ФНОα, которые индуцируют синтез цитокинов «второго поколения» – ИЛ-2, ИЛ-4, ИЛ-5 и др.[11] Они, в свою очередь, влияют на синтез ранних цитокинов, что позволяет усиливать иммунный ответ. Усиленно синтезируемые при ГЛПС основные цитокины ИЛ-1β и ФНОα включают сразу несколько механизмов воспалительного ответа, в частности, они вызывают представление на эндоте-лиоцитах молекул клеточной адгезии путем активации митоген-активированных белковых киназ, в последующем фосфорилирующих транскрипционные факторы. Среди адгезивных белков только VCAM-1 экспрессируется активированным эндотелием с целью привлечения лейкоцитов. Лейкоциты с помощью поверхностных белков-интегринов связываются с VCAM-1 на поверхности активированных эндотелио-цитов, при участии хемокинов типа моноцитарных хемотаксических белков МСР-1 и МСР-2 проникают через межэндотелиальные промежутки, движутся в направлении повышения их концентрации, прикрепляются к экстрацеллюлярному матриксу (фибронектину, ламинину, коллагену) и трансформируются в макрофаги [12]. Усиленная экспрессия эндотелиоци-тами VCAM-1 свидетельствует о развитии при ГЛПС адгезионной формы ДЭ, и это способствует эффективной защите организма от действия хантавируса, однако низкий уровень в крови данной МКА в стадию олигоанурии у больных с осложненной формой заболевания ассоциируется с тенденцией к исчерпанию компенсаторных возможностей эндотелия в данный период заболевания и может служить неблагоприятным прогностическим признаком.
Появление растворимой биологически активной формы sVCAM-1 в сыворотке крови может быть результатом не только его усиленной экспрессии на поверхности эндотелиоцита, но и протеолитического отщепления от данной клетки в результате ее повреждения [13], свидетельством чего является обнаруженная нами усиленная десквамация эндотелиоцитов при ГЛПС [14]. Повышенная экспрессии клетками эндотелия VE-кадгерина в лихорадочный период среднетяжелой формы, возможно, является ответной реакцией макроорганизма при незначительной вирусной нагрузке и преследует в данных условиях цель уменьшения
Корреляционная зависимость между концентрациями sVCAM-1 и VE-кадгерина в сыворотке крови больных ГЛПС различной степени тяжести по Спирмену
|
Среднетяжелая |
Тяжелая без осложнений |
Тяжелая с осложнениями |
|||||||||
|
лихорадка |
олигоанурия |
поли урия |
восст. диурез |
лихорадка |
олигоанурия |
полиурия |
восст. диурез |
лихорадка |
олигоанурия |
полиурия |
восст. диурез |
|
R=+0,5 |
R=-0,14 |
R=-0,6 |
R=-0,5 |
R=-0,3 |
R=-0,5 |
R=-0,3 |
R=-0,5 |
R=-0,5 |
R=-0,14 |
R=-0,14 |
R=-0,5 |
|
Р=0,33 |
Р=0,8 |
P=0,15 |
P=0,23 |
P=0,7 |
P=0,3 |
P=0,5 |
P=0,3 |
P=0,7 |
P=0,8 |
P=0,8 |
P=0,3 |
проницаемости эндотелия сосудов для чужеродного агента - хантавируса. При более значительной вирусной атаке, проявляющейся в тяжелой форме ГЛПС более эффективным способом противодействия возбудителю заболевания, вероятнее всего, оказывается снижение синтеза данной адгезивной молекулы. Это ведет к ослаблению межклеточных контактов во внутренней выстилке сосудов целью воспрепятствования персистированию вируса внутри ее клеток [13, 15]. Следовательно, снижение экспрессии эндотелиоцита-ми VE-кадгерина при ГЛПС носит адаптивный характер и свидетельствует о развитии ангиогенной формы ДЭ. В условиях повреждения части клеток интимы сосудов хантавирусом и продуктами метаболизма, обеспечивающими элиминацию возбудителя (активными формами кислорода, окисью азота, пероксинитритом и др.) остающиеся функционально активными эндоте-лиоциты обеспечивают гиперэкспрессию VCAM-1 для поддержания системной воспалительной реакции во внутренней выстилке сосудов.
Выводы :
-
1. У больных ГЛПС при всех формах и периодах заболевания имеет место компенсаторное усиление экспрессии молекулы клеточной адгезии VCAM-1, за исключением периодов олигоанурии и восстановленного диуреза осложненной формы, что свидетельствует о развитии адгезионной формы эндотелиальной дисфункции.
-
2. При ГЛПС наблюдается тенденция к снижению экспрессии эндотелиоцитами VE-кадгерина с развитием ангиогенной формы дисфункции эндотелия.
-
3. Изменения в представлении клетками интимы сосудов данных адгезивных молекул носят адаптивный характер и преследуют цель ограничения повреждающего действия на нее хантавируса - возбудителя ГЛПС.
Список литературы Роль адгезивных молекул VCAM-1 и VE-кадгерина в развитии дисфункции эндотелия при геморрагической лихорадке с почечным синдромом
- Сиротин, Б.З. Геморрагическая лихорадка с почечным синдромом/Б.З. Сиротин. -Хабаровск, 1994. -300 с.
- Онищенко, Г.Г. Заболеваемость зооантропонозными и природно-очаговыми инфекциями и меры по их профилактике/Г.Г. Онищенко, А.А. Монисов, Л.П. Гульченко и др.//Журнал микробиологии. -1999. -№ 4. -С. 14-18.
- Фазлыева, Р.М. Геморрагическая лихорадка с почечным синдромом в Республике Башкортостан/Р.М. Фазлыева, Д.Х. Хунафина, Ф.Х. Камилов. -Уфа, 1995. -343 с.
- Гомазков, О.А. Эндотелин в кардиологии: молекулярный, физиологические и патологические аспекты/О.А. Го-мазков//Кардиология. -2001. -№ 2. -С. 50-58.
- Selwyn, A.P. Cell dysfunction in atherosclerosis and the ischemic manifestation of coronary artery disease/A.P. Selwyn, S. Kinlay, M. Creager et al.//Am. J. Cardiol. -1997. -№ 79. -Р. 17 -23.
- Дисфункция эндотелия у больных сахарным диабетом 1 типа и диабетической кардиомиопатией/Ю.Б. Рыбченко, Л.К. Соколова, О.А. Волошина и др.//Здоровя Украiни. -2007. -№ 15-16. -С. 71.
- Wick, G. Autoimmune and inflammatory mechanisms in atherosclerosis/G. Wick, M. Knoflach, Q. Xu//Annu.Rev.Immunol. -2004. -№ 22. -Р. 361-403.
- Искандарова, Л.Р. Молекулы адгезии и клеточно-цитокиновый комплекс в ремоделировании сосудов при артериальной гипертонии с метаболическими факторами риска/Л.Р. Искандарова, Э.Г. Муталова, Э.Р. Смакаева и др.//Российский кардиологический журнал. -2008. -№ 5. -С. 14-21.
- Hoffmeister, H.M. Soluble adhesion molecules, fibrinogen, leucocytes and activity of coronary heart disease/H.M. Hoffmeister, E. Buttcher, S. Kazmaier//Eur Heart J -1998. -№ 19. -Р. 137.
- Сиротин, Б.З. Геморрагическая лихорадка с почечным синдромом/Б.З. Сиротин. -Хабаровск. -1994. -300 с.
- Байгильдина, А.А. Патогенетическое значение некоторых цитокинов и белка клеточной адгезии VCA M-1 в развитии воспалительных изменений эндотелия сосудов при геморрагической лихорадке с почечным синдромом/А.А. Байгильдина, А.Т. Галиева, Ф.Х. Камилов//Морфологические ведомости. -2008. -№ 3-4. -С. 158-161.
- Игнатов, П.Е. Иммунитет и инфекция/П.Е. Игнатов. -М.: Время, 2002. -352 с.
- Пальцев, М.А. Межклеточные взаимодействия/М.А. Пальцев, А.А. Иванов. -М.: Медицина, 1995. -224 с.
- Камилов, Ф.Х. Состояние целостности эндотелия сосудов при ГЛПС/Ф.Х. Камилов, А.А. Байгильдина, В.Ш. Вагапова//Морфология. -2008. № 4. -С. 72.
- Perez-Moreno, M. Sticky business: orchestrating cellular signals at cadherens junctions/M. Perez-Moreno, C. Jamora, E. Fuchs//Cell. -2003. -№ 112. -Р. 535-548.


