Роль эпикардиальной жировой ткани и автономной нервной системы в патогенезе нарушений ритма сердца
Автор: Лосик Денис Владимирович, Никитин Н.А., Минин С.М., Фишер Е.В., Михеенко И.Л., Чернявский А.М., Романов А.Б.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Обзоры
Статья в выпуске: 3 т.25, 2021 года.
Бесплатный доступ
Обзор посвящен проблемам патогенеза нарушений ритма сердца. Роль эпикардиальной жировой ткани в развитии различных сердечнососудистых заболеваний активно обсуждается. В статье рассмотрены основные механизмы влияния эпикардиальной жировой ткани на патогенез таких нарушений ритма сердца, как фибрилляция предсердий, желудочковые нарушения ритма, а также их взаимосвязь с хронической сердечной недостаточностью. Обозначены перспективы и нерешенные вопросы данной области знаний. Цель обзора - показать роль эпикардиальной жировой ткани и автономной нервной системы в патогенезе нарушений ритма сердца в зависимости от анатомического расположения и нозологии.
Автономная нервная система, желудочковая тахикардия, нарушение ритма сердца, фибрилляция предсердий, хроническая сердечная недостаточность, эпикардиальная жировая ткань
Короткий адрес: https://sciup.org/142230795
IDR: 142230795 | DOI: 10.21688/1681-3472-2021-3-27-33
The role of epicardial adipose tissue and autonomic nervous system in pathophysiology of cardiac arrhythmias
The role of epicardial adipose tissue (EAT) in the pathogenesis and prognosis of cardiovascular diseases has been actively discussed. This review provides information regarding the main mechanisms by which EAT influences the pathophysiology of rhythm disturbances, such as atrial fibrillation and ventricular arrhythmias, as well as their relationship with chronic heart failure. The pathogenesis of cardiac arrhythmias is exceedingly complex. As such, the mechanism by which EAT influences arrhythmias and heart failure can vary according to the anatomy and type of arrhythmia, one of which involves the autonomic nervous system (ANS). Some studies have shown a good treatment effects by targeting EAT in atrial fibrillation, whereas others have found that EAT volume can be used to predict the efficacy of radiofrequency ablation, a method for treating atrial fibrillation and ventricular arrhythmias. However, no standards have yet been established for the use of EAT visualisation. Fundamental, translational and clinical research are needed to study the role of EAT and ANS in the pathogenesis of cardiovascular diseases.
Текст обзорной статьи Роль эпикардиальной жировой ткани и автономной нервной системы в патогенезе нарушений ритма сердца
Д.В. Лосик,
Н.А. Никитин,
С.М. Минин,
Е.В. Фишер,
И.Л. Михеенко,
А.М. Чернявский,
А.Б. Романов,
Патофизиологические механизмы нарушений ритма сердца (НРС) сложны и многогранны. Ключевую роль в патогенезе НРС играет ремоделирование камер сердца, которое напрямую зависит от факторов риска и коморбидных состояний [1]. Концепция повторного входа на фоне зон замедления электрического проведения и гипотезы триггерных очагов аритмии в различных участках миокарда имеют сторонников, однако не объясняют причины возникновения НРС. Радиочастотное воздействие на аритмогенные очаги предотвращает прогрессирование аритмий, но ряд НРС, в первую очередь фибрилляция предсердий (ФП), рецидивирует [2]. В последние годы большой интерес вызывает роль эпикардиальной жировой ткани (ЭЖТ) в патогенезе и поддержании нарушений ритма сердца.
ЭЖТ определяют как жировую клетчатку, расположенную между миокардом и висцеральным листком перикарда [3]. Существует термин «перикардиальный жир» — клетчатка как внутри перикарда (эквивалентно определению эпикардиального жира), так и кнаружи от него. При этом два типа тканей существенно отличаются друг от друга, что определяет влияние ЭЖТ на структуры сердца. Эмбриологически ЭЖТ происходит из спланхноплевральной мезодермы, из которой также формируется клетчатка брыжейки и сальника. ЭЖТ — структура сердца, которая без фасциального разделения плотно прилегает к миокарду, в то время как перикардиальный жир отделен от него перикардом [4]. Кроме того, ЭЖТ кровоснабжается за счет коронарных артерий, а перикардиальный жир — за счет ветвей внутренних грудных артерий. Анатомически ЭЖТ располагается в области правого и левого желудочков, по ходу коронарных артерий и в области левого и правого предсердий [5].
В отличие от висцерального и абдоминального жира, который в первую очередь вызывает ожирение и системно влияет на организм, ЭЖТ, вероятно, действует локально через структурное ремоделирование предсердий и желудочков или посредством паракринных механизмов. Ткань участвует в фиброзе и апоптозе кардиомиоцитов, соответственно, нарушения функций ЭЖТ могут играть ключевую роль в развитии и поддержании НРС, а также при сердечной недостаточности.
С учетом особенностей анатомии и кровоснабжения ЭЖТ может по-разному влиять на патогенез НРС и хронической сердечной недостаточности (ХСН). Для оценки этого влияния при различных нозологиях НРС и ХСН мы выполнили поиск клинических исследований в базе данных PubMed по ключевым словам «эпикардиальный жир», «фибрилляция предсердий», «желудочковые нарушения ритма» и «хроническая сердечная недостаточность». Из более тысячи статей выбрали те, в которых в качестве диагностических инструментов использовали магнитно-резонансную, компьютерную томографию и ультразвуковое исследование сердца для оценки кардиального жира и сравнивали как минимум две группы пациентов. Также учитывали НРС (ФП, желудочковая тахикардия) и ХСН в критериях включения в исследование как основные признаки. В ходе анализа обнаружили похожие механизмы влияния ЭЖТ и автономной нервной системы (АНС) на НРС, выявили обратные зависимости при прогрессировании хронической сердечной недостаточности.
Эпикардиальная жировая ткань и фибрилляция предсердий
В последние годы большое внимание уделяют роли ЭЖТ в патогенезе ФП. Оценку объема ЭЖТ с помощью компьютерной томографии, эхокардиографии или магнитно-резонансной томографии используют в качестве биомаркера в клинических исследованиях. В ФГБУ «НМИЦ им. ак. Е.Н. Ме-шалкина» Минздрава России регулярно применяют анализ объема общей и периатриальной ЭЖТ по данным компьютерной томографии. Методика позволяет визуализировать ЭЖТ ( рисунок ), а также просчитать ее объем и плотность. Установлено, что повышение объема ЭЖТ увеличивает риск ФП независимо от ожирения пациента [6–7]. C.X. Wong и соавт. оценивали ЭЖТ с помощью магнитно-резонансной томографии у 130 пациентов и выявили, что повышенный объем ЭЖТ связан с тяжестью ФП и рецидивами аритмии после радиочастотной аблации [8]. ЭЖТ значимо влияет на поддержание и прогрессирование ФП, в отличие от метаболического ожирения и избыточного содержания висцерального жира [9]. Патогенез, возможно, связан с паракринными эффектами ЭЖТ, приводящими к усилению фиброза и жировой инфильтрации
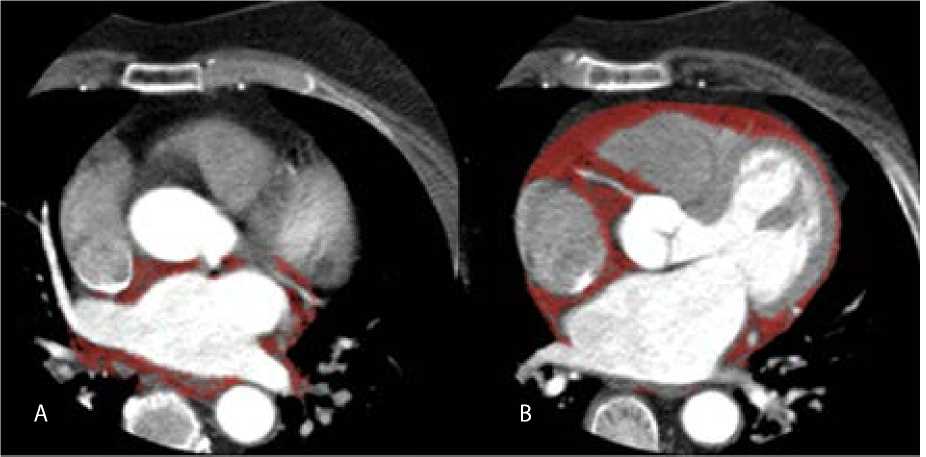
Оценка объема эпикардиальной жировой ткани на компьютерной томографии сердца с внутривенным контрастированием (рентгеноконтрастный препарат — йомепрол): область для оценки объема периатри-альной эпикардиальной жировой ткани (A); область для оценки общего объема эпикардиальной жировой ткани (B). Участки внутри перикарда, соответствующие диапазону компьютерной томографии плотности жировой ткани (от -190 до 0 ед. Хаунсфилда), отмечены красным
в миокарде предсердий, которые, в свою очередь, приводят к электрической гетерогенности структуры миокарда левого предсердия [10].
ЭЖТ может также воздействовать на активность АНС сердца, которая является частью вегетативной нервной системы и влияет на поддержание и развитие ФП [11–12]. АНС сердца состоит из нервных окончаний и ганглиев, которые полностью находятся в области эпикарда и заключены в эпикардиальные жировые подушечки [13]. На моделях животных в экспериментальных исследованиях выявили, что активность парасимпатических нервов в таких жировых подушках приводит к пароксизмам ФП, в первую очередь за счет сокращения рефрактерного периода в левом предсердии. В свою очередь, симпатическая иннервация предсердий более вы-раженна, в отличие от желудочков [14]. Предсердия иннервируются более плотно, и, возможно, дисбаланс между симпатической и парасимпатической АНС является одним из ключевых механизмов НРС. ЭЖТ может локально влиять на эти вегетативные ганглии, повышая тонус блуждающего нерва и ослабляя воздействие симпатической нервной системы, создавая условия для ФП. Так, в клиническом исследовании выявили положительный эффект инъекции ботулотоксина в жировые эпикардиальные подушки на снижение количества послеоперационной ФП в раннем и отдаленном периодах после аортокоронарного шунтирования [15]. Однако стандартный метод оценки функции АНС не выработан.
Существует ряд способов визуализации активности АНС, один из которых — сцинтиграфия сердца с нейротропным радиофармпрепаратом — ме-тайодбензилгуанидином, меченным йодом-123 (123I-МИБГ). Данная методика позволяет оценивать активные зоны симпатической нервной системы и взаимосвязь с объемом ЭЖТ, измеренной по данным компьютерной томографии [16–17]. Растущие доказательства роли ЭЖТ в развитии и поддержании ФП требуют большего количества проспективных исследований. Глубокое изучение ЭЖТ может позволить открыть новые эффективные методы лечения ФП и усовершенствовать существующие.
Эпикардиальная жировая ткань и желудочковые нарушения ритма
ЭЖТ не только участвует в патогенезе ФП, но и влияет на развитие желудочковых нарушений ритма (ЖНР) [18]. Показано, что толщина ЭЖТ связана с такими распространенными патологическими состояниями сердца, как увеличение массы левого желудочка, атеросклероз, жесткость коронарных артерий, артериальная гипертензия и ФП, которые, в свою очередь, являются факторами риска развития ЖНР [19]. Также продемонстрирована значительная связь между увеличением толщины и объема ЭЖТ и развитием желудочковых тахикардий при структурной патологии сердца. В исследование A. Sepehri Shamloo и соавт. включили 61 пациента с показаниями к катетерной аблации желудочковой тахикардии [20]. До процедуры всем больным выполнили магнитно-резонансную томографию сердца для оценки локализации субстрата аритмии и объема ЭЖТ. Выявили, что чем больше был объем ЭЖТ до оперативного лечения желудочковой тахикардии, тем чаще возникали рецидивы аритмии в отдаленном периоде наблюдения. В данном исследовании авторы в числе первых показали подобную взаимосвязь. При этом почти все измеряемые участки толщины ЭЖТ были больше у пациентов с рецидивами желудочковой тахикардии, а увеличение толщины ЭЖТ в области правого и левого желудочков было статистически значимым. Авторы предполагают, что увеличение объема ЭЖТ приводит к повышению уровня воспалительных цитокинов, которые могут впоследствии привести к более серьезному структурному и электрическому ремоделированию сердца и в конечном итоге к более высокой частоте серьезных ЖНР и внезапной сердечной смерти.
S. Kanat и соавт. продемонстрировали взаимосвязь толщины ЭЖТ и рецидива желудочковой экстрасистолии после радиочастотной аблации [21]. Авторы предположили, что несколько механизмов могут отвечать за взаимосвязь ЭЖТ и эффективности радиочастотной аблации арит-могенной зоны частой желудочковой экстрасистолии. Структурное ремоделирование миокарда и такие выраженные изменения, как фиброз, могут привести к нарушениям стабильности потенциала действия кардиомиоцитов, которые вызывают желудочковую экстрасистолию. Другой потенциальный механизм влияния ЭЖТ на развитие ЖНР — содержание холинергических и адренергических нервных волокон АНС в толще
ЭЖТ, которые входят в парасимпатическую и симпатическую нервные системы сердца и являются источником норадреналина и адреналина. При остром инфаркте миокарда симпатические и парасимпатические эфферентные сигналы увеличивают напряжение нейронов в области переин-фарктной зоны, тогда как афферентные сигналы от поврежденной ткани снижаются, что приводит к неоднородности иннервации АНС и является аритмогенным субстратом [22; 23]. Возможно, влияние на уровень активности АНС именно ЭЖТ является ключевым механизмом в патогенезе желудочковых нарушений ритма.
Эпикардиальная жировая ткань и хроническая сердечная недостаточность
Дисбаланс физиологической и патологической роли ЭЖТ может быть причиной сердечной патологии. Вышеописанные исследования продемонстрировали, что ЭЖТ воздействует на морфологию и функцию сердца. Однако о влиянии ЭЖТ на развитие ХСН с систолической дисфункцией левого желудочка известно мало. При этом именно снижение фракции выброса левого желудочка является независимым предиктором внезапной сердечной смерти и желудочковых нарушений ритма.
Однако на риск внезапной сердечной смерти влияют и другие факторы. Есть предположение, что методика стратификации риска внезапной сердечной смерти должна быть модифицирована, и в данном случае изучение ЭЖТ и АНС можно использовать в отборе пациентов для имплантации кардиовертера-дефибриллятора в целях профилактики внезапной сердечной смерти. Кроме того, это поможет улучшить понимание патофизиологии внезапной сердечной смерти, определить предикторы риска и рассмотреть особые группы пациентов, для которых можно оценить риски на более ранних этапах развития систолической дисфункции левого желудочка.
Ch.-K. Wu и соавт. продемонстрировали связь между объемом ЭЖТ и фибрилляцией желудочков или желудочковой тахикардией у 50 пациентов с систолической дисфункцией левого желудочка и ХСН. В отличие от вышеописанных исследований, выявили обратный эффект: чем меньше был объем ЭЖТ, тем чаще регистрировали ЖНР [24]. C. Doesch и соавт. изучали объем ЭЖТ у пациентов с ХСН со сниженной фракцией выброса левого желудочка и подтвердили, что объем ЭЖТ был ниже по сравнению с контрольной группой здоровых людей [25]. Однако у больных ХСН с умеренно сниженной фракцией выброса левого желудочка, а также сохранной фракцией выброса увеличение объема ЭЖТ повышало частоту ФП и биомаркеры, связанные с повреждением миокарда [26]. В исследовании CASTLE-AF катетерная аблация по поводу ФП у пациентов с ХСН и сниженной фракцией выброса левого желудочка продемонстрировала значительное снижение смертности от всех причин или госпитализации по поводу декомпенсации ХСН в сравнении с медикаментозной терапией [27]. В дискуссии N.F. Marrouche и соавт. не отвечают на вопрос, с чем связан значимый эффект катетерной аблации ФП. Можно предположить, что во время катетерной аблации левого предсердия происходит опосредованное воздействие на ЭЖТ и АНС, что, в свою очередь, улучшает прогноз. Однако данное предположение требует подтверждения. С учетом противоречивых данных необходимо изучить влияние ЭЖТ на прогноз у пациентов с различными формами ХСН, что позволит выявить новые точки воздействия для диагностики и лечения данного патологического состояния.
Заключение
ЭЖТ воздействует на различные аспекты работы сердца. Возможность визуализации и оценки влияния объема ЭЖТ на развитие и поддержание НРС может помочь прогнозировать и предотвращать сердечно-сосудистые события у пациентов со структурными изменениями сердца и без них. Не решен вопрос уменьшения объема ЭЖТ у пациентов со сниженной фракцией выброса и доказанным высоким риском ЖНР. Изучение взаимосвязи ЭЖТ и АНС может способствовать поиску новых методик лечения различных заболеваний сердца. Определение ЭЖТ может быть дополнительным критерием отбора пациентов для первичной профилактики внезапной сердечной смерти. Фундаментальные, трансляционные и клинические исследования необходимы для изучения роли ЭЖТ и АНС в патогенезе сердечно-сосудистых заболеваний.
Список литературы Роль эпикардиальной жировой ткани и автономной нервной системы в патогенезе нарушений ритма сердца
- Kirchhof P., Benussi S., Kotecha D., Ahlsson A., Atar D., Casadei B., Castella M., Diener H.-C., Heidbuchel H., Hendriks J., Hindricks G., Manolis A.S., Oldgren J., Popescu B.A., Schotten U., Van Putte B., Vardas P., ESC Scientific Document Group. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur Heart J. 2016;37(38):2893-2962. PMID: 27567408. https://doi. org/10.1093/eurhearti/ehw210
- Лосик Д.В., Романов А.Б., Шабанов В.В., Байрамова С.А., Якубов А.А., Стенин И.Г., Покушалов Е.А. Прогрессирование фибрилляции предсердий после неэффективной первичной процедуры радиочастотной изоляции легочных вен: рандомизированное сравнение повторной катетерной аблации и медикаментозного метода лечения. Патология кровообращения и кардиохирургия. 2015;19(2):84-92. [Losik D.V., Romanov A.B., Shabanov V.V., Bairamova S.A., Yakubov A.A., Stenin I.G., Pokushalov Ye.A. Progression of atrial fibrillation after a failed initial ablation procedure in patients with paroxysmal atrial fibrillation: a randomized comparison of antiarrhythmic drug therapy vs re-ablation. Patologiya krovoobrashcheniya i kardiokhirurgiya = Circulation Pathology and Cardiac Surgery. 2015;19(2):84-92. (In Russ.)] http://doi.org/10.21688/1681-3472-2015-2-84-92
- Sacks H.S., Fain J.N. Human epicardial adipose tissue: a review. Am Heart J. 2007;153(6):907-917. PMID: 17540190. https://doi. org/10.1016/i.ahi.2007.03.019
- lacobellis G. Local and systemic effects of the multifaceted epicardial adipose tissue depot. Nat Rev Endocrinol. 2015;11(6):363-371. PMID: 25850659. https://doi.org/10.1038/ nrendo.2015.58
- Hatem S.N., Sanders P. Epicardial adipose tissue and atrial fibrillation. Cardiovasc Res. 2014;102(2):205-213. PMID: 24648445. https://doi.org/10.1093/cvr/cvu045
- Batal O., Schoenhagen P., Shao M., Ayyad A.E., Van Wagoner D.R., Halliburton S.S., Tchou PJ., Chung M.K. Left atrial epicardial adiposity and atrial fibrillation. Circ Arrhythm Electrophysiol. 2010;3(3):230-236. PMID: 20504944; PMCID: PMC2974566. https://doi.org/10.1161/CIRCEP.110.957241
- Thanassoulis G., Massaro J.M., O'Donnell C.J., Hoffmann U., Levy D., Ellinor P.T., Wang T.J., Schnabel R.B., Vasan R.S., Fox C.S., Beniamin E.J. Pericardial fat is associated with prevalent atrial fibrillation: the Framingham Heart Study. Circ Arrhythm Electrophysiol. 2010;3(4):345-350. PMID: 20558845; PMCID: PMC2953855. https://doi.org/10.1161/CIRCEP.109.912055
- Wong C.X., Abed H.S., Molaee P., Nelson A.J., Brooks A.G., Sharma G., Leong D.P., Lau D.H., Middeldorp M.E., RobertsThomson K.C., Wittert G.A., Abhayaratna W.P., Worthley S.G., Sanders P. Pericardial fat is associated with atrial fibrillation severity and ablation outcome. J Am Coll Cardiol. 2011; 57(17):1745-1751. PMID: 21511110. https://doi.org/10.1016/i. iacc.2010.11.045
- Venteclef N., Guglielmi V., Balse E., Gaborit B., Cotillard A., Atassi F., Amour J., Leprince P., Dutour A., Clément K., Hatem S.N. Human epicardial adipose tissue induces fibrosis of the atrial myocardium through the secretion of adipo-fibrokines. Eur Heart J. 2015;36(13):795-805a. PMID: 23525094. https://doi. org/10.1093/eurhearti/eht099
- Mahaian R., Nelson A., Pathak R.K., Middeldorp M.E., Wong C.X., Twomey D.J., Carbone A., Teo K., Agbaedeng T., Linz D., de Groot J.R., Kalman J.M., Lau D.H., Sanders P. Electroanatomical remodeling of the atria in obesity: impact of adiacent epicardial fat. JACC Clin Electrophysiol. 2018;4(12):1529-1540. PMID: 30573116. https://doi.org/10.1016Aiacep.2018.08.014
- Iwasaki Y.-K., Kato T., Xiong F., Shi Y.-F., Naud P., Maguy A., Mizuno K., Tardif J.-C., Comtois P., Nattel S. Atrial fibrillation promotion with long-term repetitive obstructive sleep apnea in a rat model. J Am Coll Cardiol. 2014;64(19):2013-2023. PMID: 25440097. https://doi.org/10.1016/Uacc.2014.05.077
- Shen MJ., Choi E.-K., Tan A.Y., Lin S.-F., Fishbein M.C., Chen L.S., Chen P.-S. Neural mechanisms of atrial arrhythmias. Nat Rev Cardiol. 2011;9(1):30-39. PMID: 21946776. https://doi. org/10.1038/nrcardio.2011.139
- Kimura K., leda M., Fukuda K. Development, maturation, and transdifferentiation of cardiac sympathetic nerves. Circ Res. 2012;110(2):325-336. PMID: 22267838. https://doi. org/10.1161/CIRCRESAHA.111.257253
- Romanov A., Pokushalov E., Ponomarev D., Bayramova S., Shabanov V., Losik D., Stenin I., Elesin D., Mikheenko I., Strelnikov A., Sergeevichev D., Kozlov B., Po S.S., Steinberg J.S. Long-term suppression of atrial fibrillation by botulinum toxin injection into epicardial fat pads in patients undergoing cardiac surgery: Three-year follow-up of a randomized study. Heart Rhythm. 2019;16(2):172-177. PMID: 30414841. https:// doi.org/10.1016/j.hrthm.2018.08.019
- Minin S.M., Nikitin N.A., Shabanov V.V., Losik D.V., Mikheenko I.L., Ponomarev D.N., Pokushalov E.A., Romanov A.B. Evaluation of CZT SPECT imaging for cardiac sympathetic innervation in healthy individuals and patients with atrial fibrillation. Russian Open Medical Journal. 2018;7(3):e0308. https://doi.org/10.15275/ rusomj.2018.0308
- Nikitin N., Minin S., Romanov A., Shabanov V., Losik D., Elesin D., Stenin I., Mikheenko I., Baavour R., Pokushalov E. Hybrid 123I-mIBG SPECT/CT cardiac imaging for identification of left atrial ganglionated plexi in healthy individuals and patients with atrial fibrillation. Eur Heart J Cardiovasc Imaging. 2019;20(Suppl_3):jez15. https://doi.org/10.1093/ehjci/jez150
- Maan A., Mansour M., Ruskin J.N., Heist E.K. Role of epicardial fat in atrial fibrillation pathophysiology and clinical implications. J Innov Card Rhythm Manag. 2013;4:1077-1082. Available from: https://www.innovationsincrm.com/cardiac-rhythm-management/2013/january/387-epicardial-fat-atrial-fibrillation-pathophysiology
- Dukkipati S.R., Koruth J.S., Choudry S., Miller M.A., Whang W., Reddy V.Y. Catheter ablation of ventricular tachycardia in structural heart disease: indications, strategies, and outcomes — Part II. J Am Coll Cardiol. 2017;70(23):2924-2941. PMID: 29216988. https://doi.org/10.1016Xj.jacc.2017.10.030
- Chistiakov D.A., Grechko A.V., Myasoedova V.A., Melnichenko A.A., Orekhov A.N. Impact of the cardiovascular system-associated adipose tissue on atherosclerotic pathology. Atherosclerosis. 2017;263:361-368. PMID: 28629772. https://doi.org/10.1016/j. atherosclerosis.2017.06.017
- Sepehri Shamloo A., Schoene K., Stauber A., Darma A., Dagres N., Dinov B., Bertagnolli L., Hilbert S., Müssigbrodt A., Husser D., Bollmann A., Hindricks G., Arya A. Epicardial adipose tissue thickness as an independent predictor of ventricular tachycardia recurrence following ablation. Heart Rhythm. 2019;16(10):1492-1498. PMID: 31202898. https://doi. org/10.1016/j.hrthm.2019.06.009
- Kanat S., Duran Karaduman B., Tütüncü A., Tenekecioglu E., Mutluer F.O., Akar Bayram N. Effect of echocardiographic epicardial adipose tissue thickness on success rates of premature ventricular contraction ablation. Balkan Med J. 2019;36(6):324-330. PMID: 31347351; PMCID: PMC6835166. https://doi.org/10.4274/balkanmedj. galenos.2019.2019.4.88
- Rajendran P.S., Nakamura K., Ajijola O.A.,Vaseghi M., Armour J.A., Ardell J.L., Shivkumar K. Myocardial infarction induces structural and functional remodelling of the intrinsic cardiac nervous system. J Physiol. 2016;594(2):321-341. PMID: 26572244; PMCID: PMC4713729. https://doi.org/10.1113/ JP271165
- Ajijola O.A., Lux R.L., Khahera A., Kwon O., Aliotta E., Ennis D.B., Fishbein M.C., Ardell J.L., Shivkumar K. Sympathetic modulation of electrical activation in normal and infarcted myocardium: implications for arrhythmogenesis. Am J Physiol Heart Circ Physiol. 2017;312(3):H608-H621. PMID: 28087519; PMCID: PMC5402014. https://doi.org/10.1152/ ajpheart.00575.2016
- Wu Ch.-K., Tsai H.-Y., Su M.-Y.M., Wu Y.-F., Hwang J.-J., Tseng W.-Y., Lin J.-L., Lin L.-Y. Pericardial fat is associated with ventricular tachyarrhythmia and mortality in patients with systolic heart failure. Atherosclerosis. 2015;241(2):607-614. PMID: 26116961. https://doi.org/10.1016/j.atherosclerosis.2015.05.025
- Doesch C., Haghi D., Flüchter S., Suselbeck T., Schoenberg S.O., Michaely H., Borggrefe M., Papavassiliu T. Epicardial adipose tissue in patients with heart failure. J Cardiovasc Magn Reson. 2010;12(1):40. PMID: 20624277; PMCID: PMC2914772. https:// doi.org/10.1186/1532-429X-12-40
- van Woerden G., Gorter T.M., Westenbrink B.D., Willems T.P., van Veldhuisen D.J., Rienstra M. Epicardial fat in heart failure patients with mid-range and preserved ejection fraction. Eur J Heart Fail. 2018;20(11):1559-1566. PMID: 30070041; PMCID: PMC6607508. https://doi.org/10.1002/ejhf.1283
- Marrouche N.F., Brachmann J., Andresen D., Siebels J., Boersma L., Jordaens L., Merkely B., Pokushalov E., Sanders P., Proff J., Schunkert H., Christ H., Vogt J., Bänsch D., CASTLE-AF Investigators. Catheter ablation for atrial fibrillation with heart failure. N Engl J Med. 2018;378(5):417-427. PMID: 29385358. https://doi.org/10.1056/NEJMoa1707855


