Роль компьютерной томографии и сцинтиграфии в диагностике состояния вилочковой железы у больных генерализованной миастенией
Автор: Ветшев Петр Сергеевич, Кондрашин С.А., Абдалова О.В., Ипполитов Л.И., Фатьянова А.С.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Статья в выпуске: 1 т.4, 2009 года.
Бесплатный доступ
На большом количестве клинических наблюдений изучены возможности методов спиральной компьютерной томографии, мультиспиральной компьютерной томографии до и после внутривенного контрастирования, а также сцинтиграфии в оценке состояния вилочковой железы у больных генерализованной миастенией.
Миастения, компьютерная томография, сцинтиграфия, вилочковая железа
Короткий адрес: https://sciup.org/140187708
IDR: 140187708 | УДК: 616.74-009.17:
Текст научной статьи Роль компьютерной томографии и сцинтиграфии в диагностике состояния вилочковой железы у больных генерализованной миастенией
Диагностика и лечение миастении при опухолевом и неопухолевом поражении вилочковой железы (ВЖ) до настоящего времени представляет серьезную проблему. Известно, что тимомы (органоспецифические опухоли ВЖ) относятся к наиболее частым (до 50%) новообразованиям переднего средостения. Клинические проявления опухолей ВЖ зависят от вида опухоли, характера ее роста и размеров. Среди аутоиммунных заболеваний и синдромов, которые сочетаются с тимомами, наиболее часто встречается генерализованная миастения (ГМ) – примерно в 40% наблюдений, тогда как среди больных миастенией тимомы обнаруживаются приблизительно в 15–20% [1–3, 5]. В свою очередь, миастения является органоспецифическим аутоиммунным заболеванием, характеризующимся нарушением нервно-мышечной передачи, приводящим к слабости и патологической утомляемости различных групп попечно-полосатых мышц, быстро приводящим к нарушению трудоспособности и инвалидизации, что обусловливает высокую медицинскую и социальную значимость проблемы.
Изучение отечественных и зарубежных работ, посвященных методам диагностики ГМ, позволяют заключить, что установление диагноза миастении требует безотлагательного исследования состояния ВЖ, особенно у больных в возрасте старше 30 лет. Особое внимание следует уделять тщательному радиологическому обследованию переднего средостения у пациентов с началом ГМ после 40–45 лет, поскольку именно у таких больных сочетание миастении и тимомы отмечается наиболее часто (40–70%) [16]. Несмотря на широкие возможности компьютерной томографии (КТ) в выявлении опухолевых процессов различной локализации, и наличие работ, посвященных образованиям переднего средостения, состоянию ВЖ и вопросам изучения ГМ, изучения опухолевых и неопухолевых изменений ВЖ при ГМ, а также применения КТ с внутривенным болюсным контрастированием, в нашей стране не проводилось.
Кроме того, в мире все большее практическое значение приобретает использование радионуклидных методов диагностики при поражении ВЖ. Имеются сообщения о сравнительных исследованиях применения различных радиофармпрепаратов (РФП), таких как Tc99mMIBI, Tc99mtetrofosmin, Tc99mDMSA в оценке характера поражения ВЖ [9, 11].
Важно отметить, что характер поражения ВЖ является определяющим в выборе тактики лечения больных ГМ. Если при опухолевом поражении тимуса показания к операции приближаются практически к абсолютным и выполняются по онкологическим показаниям, то при неопухолевом поражении определенной группе больных операция не показана и целесообразно применение консервативной терапии.
Отсутствие единых алгоритмов обследования, поздняя диагностика и несвоевременное начало адекватной патогенетической терапии (в т.ч. оперативного вмешательства) во многом являются неиспользованными резервами в улучшении результатов лечения этой тяжелой категории больных.
Материалы и методы исследования
В исследование включены 102 пациента, находившихся под нашим наблюдением в 2004–2006 гг. Всем больным проводили анализ клинико-анамнестических данных, данных КТ и сцинтиграфии, результатов операции, патоморфологического исследования. Диагноз миастении устанавливали на основании жалоб, анамнеза, оценки не- врологического статуса, результатов прозериновой пробы и стимуляционной электромиографии. Критериями включения пациентов в исследование явились: диагноз ГМ (средней и тяжелой степени тяжести). Все пациенты были прооперированы с последующей морфологической верификацией изменений ВЖ.
Среди 102 больных женщин было 71 (69,3%), мужчин – 31 (30,7%). Средний возраст составил 44,0 ± 12,4 года, (от 15 до 69 лет). Статистически достоверных различий в возрасте между мужчинами и женщинами не выявлено. Средний возраст мужчин составил 43,0 ± 11,3 года (от 25 до 64 лет), женщин – 44,5 ± 13,0 (от 15 до 69 лет). Диагноз ГМ у наших пациентов был установлен через 3-6 месяцев (Мср=4,2 ± 1,2 мес.) после появления первых симптомов миастении.
По результатам морфологического исследования были выявлены следующие формы: тимома – 79 (77,5%) наблюдений, гиперплазия ВЖ – 20 (19,6%), киста ВЖ 3(2,9%). При этом в группе гиперплазии пик заболеваемости для мужчин и женщин пришелся на 25–34 лет; в группе тимом распределение по возрастным группам для мужчин и женщин было следующее: 35–44 лет и 45–54 лет, соответственно.
Спиральная компьютерная томография (СКТ) до и после внутривенного контрастирования была выполнена всем пациентам, мультиспиральная компьютерная томография (МСКТ) до и после внутривенного контрастирования – 84 пациентам. Проводили болюсное контрастирование неионными контрастными препаратами (концентрация йода 300–370 мг/мл) при помощи автоматического инъектора. После окончания исследования оценивали характер контрастирования тканей в изучаемой области во время артериальной фазы (через 20 сек), венозной (через 60 сек) и отсроченной (через 180 сек) от начала введения контрастного препарата. Измерение денситометрической плотности ткани ВЖ (в ед. Хаунсфилда) проводили по разработанной нами схеме в 5 точках: на 3, 6, 9 и 12 часах (по аналогии с циферблатом часов), а также в центре железы. Кроме того, измеряли среднюю плотность ткани железы в зоне интереса.
Сцинтиграфия с «Технетрилом» была выполнена 44 пациентам. 32 больным проведены все вышеперечисленные методы.
Распределение пациентов в зависимости от объема выполненного вмешательства, необходимого для максимально возможного удаления опухоли и /или ткани ВЖ с жировой клетчаткой, у пациентов исследуемой группы выглядело следующим образом: тимомтимэктомия (удаление вместе с опухолью самой ВЖ и жировой клетчатки переднего средостения) выполнена у 78 (76,5%) пациентов, тимэктомия (экстракапсулярное удаление всей ткани ВЖ с окружающей жировой клетчаткой) – у 23 (22,5%), паллиативная резекция – в 1 (1,0%) наблюдении.
Обработку и статистический анализ информации проводили с использованием стандартного пакета прикладных программ SPSS 13.0 for Windows (Chicago, IL).
Достоверность различий показателей в выборке оценивали с помощью непараметрических критериев ^, тесты U Mann-Whitney, Kruskal-Wallis, Freadman), для анализа корреляционной связи между группами применяли коэффициент корреляции Spearman. Минимально достаточный уровень значимости во всех тестах p<0,05.
Результаты
В результате проведенного анализа были выделены КТ-признаки объемных образований ВЖ. Оценивали положение в средостении (уровень и отношение к срединной линии), форму, размеры, контуры, однородность структуры, плотность и характер накопления контрастного вещества. Полученные результаты приведены в табл. 1. Преобладали образования неправильной (в т.ч. двухузловой) и овальной форм – 42% и 33%, соответственно. Округлая форма образований занимала третье место по частоте. В 76% наблюдений структура образований была однородной, в 24% – неоднородной за счет наличия кальцинатов или полостей распада. По отношению к сосудистым структурам средостения образования располагались преимущественно на уровне дуги аорты и ствола легочной артерии.
Признаки гиперплазии, выделенные в результате анализа КТ–картины, представлены в табл. 2. Наиболее частым признаком гиперплазии ВЖ было срединное расположение железы треугольной формы однородной структуры на уровне дуги аорты или ниже. При этом увеличения нормальных размеров ВЖ ни в одном случае не определялось.
В нашем исследовании опирались на данные КТ о нормальных размерах ВЖ у взрослых [14]. Таковыми считали толщину до 1,8 см у людей до 20 лет и 1,3 см у людей старшего возраста.
Оценивая характер накопления контрастного препарата в артериальную, венозную и отсроченную фазы,
Табл. 1. КТ-признаки объемного образования ВЖ
|
Признак |
Результат |
|
|
Плотность образования (в ед. НU) |
47,6±13,1 |
|
|
Форма |
округлая |
25% |
|
овальная |
33% |
|
|
неправильная (в т.ч. двухузловая) |
42% |
|
|
Размеры, см |
ширина |
2,6±1,1 |
|
высота |
2,0±0,9 |
|
|
толщина |
2,5±0,9 |
|
|
Положение в средостении на уровне (частота в %) |
надаортальных сосудов |
8,8% |
|
дуги аорты |
35,4% |
|
|
аорто-пульмонального окна |
16,5% |
|
|
ствола легочной артерии |
39,2% |
|
|
Расположение по отношению к срединной линии (частота в %) |
слева |
65,8% |
|
по центру |
25,3% |
|
|
справа |
8,9% |
|
|
Структура (частота в %) |
однородная |
76% |
|
неоднородная |
24% |
|
Табл. 2. КТ-признаки лимфоидно-фолликулярной гиперплазии ВЖ
|
Признак |
Результат |
|
|
Плотность(в ед. НU) |
29,5±17,6 |
|
|
Форма (частота в %) |
треугольная |
50% |
|
двудольчатая |
20% |
|
|
очаговое уплотнение |
30% |
|
|
Размеры |
не увеличены |
|
|
Положение в средостении на уровне (частота в %) |
надаортальных сосудов |
15% |
|
дуги аорты |
60% |
|
|
аорто-пульмонального окна |
25% |
|
|
Структура (частота в %) |
однородная |
70% |
|
неоднородная |
30% |
|
– данные представлены в таблице 3 – в группе объемных образований увеличение денситометрической плотности (более 20 ед. HU) отмечалось в отсроченную фазу, тогда как в группе гиперплазий накопление контрастного препарата в железе – достоверно выше (p<0,001) в артериальную, венозную и отсроченную фазы.
C учетом того, что стандартное исследование органов грудной клетки выполняется без применения контрастных препаратов, отдельно оценивали данные, полученные при нативном исследовании и после болюсного внутривенного контрастирования.
Чувствительность, специфичность и точность СКТ без контрастирования при объемном образовании ВЖ составили 81,7%; 89,0%; 90,7%, соответственно. При использовании внутривенного контрастирования чувствительность возрастала до 89,3%, специфичность – 93,0%, точность – 92,2%.
При сравнении результатов СКТ и МСКТ в отношении инвазивного роста тимом получили следующие показатели: чувствительность СКТ составила 33,3%, МСКТ – 47,0%; специфичность СКТ – 90,5%, МСКТ – 91,0%; точность СКТ – 76,2%, МСКТ – 82,1%.
Качество полученных мультипланарных реконструкций при МСКТ превосходило таковые при СКТ, что позволяло более точно установить локализацию и распространенность процесса.
Киста ВЖ (рис. 1) выявлена в 2,9% наблюдений. Основным критерием явилось отсутствие накопления контрастного препарата в объемном образовании во все фазы контрастирования. При проведении сцинтиграфии накопления РФП также не отмечалось.
При сцинтиграфии шеи и средостения по характеру накопления РФП в «зоне интереса» выделили следующие типы: 1 – отсутствие накопления препарата, 2 – сомнительное диффузное накопление, 3 – очаг повышенного накопления (рис. 2). 1-й тип встретился в 40,9% наблюдений, 2-й тип – в 27,3%, 3-й – в 31,8% наблюдений. Показатели чувствительности, специфичности и точности сцинтиграфии для опухолевого поражения ВЖ составили 60,8%, 100% и 79,5%, соответственно.
Расчет этих же показателей метода сцинтиграфии для опухолей ВЖ с учетом изменений остаточной ткани органа, сопровождающихся увеличением объема функционирующей ткани: чувствительность – 48,2%, специфичность – 100%, точность – 53%.
Обсуждение
Патологические изменения в ВЖ, согласно данным литературы, при миастении наблюдают у 90–100% больных [1, 5].
Учитывая преимущественно бессимптомное течение тимом, лучевые методы играют ведущую роль в их своевременном обнаружении [4, 6]. Также, анализ литературы не оставляет сомнений в том, что именно КТ является необходимым методом для исследования области ВЖ [7, 8, 10, 15].
По мнению ряда авторов, тимомы являются наиболее частыми образованиями средостения, диагностированными на начальной стадии при помощи КТ [12].
Специалистами часто высказывается мнение, что присоединение ГМ у больных с тимомами в некоторой степени благоприятствует успешному и своевременному лечению опухолевого процесса, благодаря более раннему радиологическому исследованию переднего средостения [4, 15]. Более того, в некоторых работах показано, что наличие ГМ является независимым прогностическим фактором, обусловливающим более благоприятный исход у пациентов с тимомой [10].
По мнению ряда исследователей [7] информативность метода КТ в определении объемных образований
Табл. 3. Характер контрастирования при опухолевом и неопухолевом поражении ВЖ
|
Патоморфологическая форма |
Фаза |
Минимальное значение (ед.HU) |
Максимальное значение (ед.HU) |
Среднее значение (ед. HU) |
Статистическое отклонение (ед. HU) |
|
артериальная |
15,0 |
94,0 |
46,0 |
23,8 |
|
|
Гиперплазия |
венозная |
17,5 |
96,0 |
55,5 |
20,4 |
|
отсроченная |
17,5 |
97,5 |
56,4 |
22,0 |
|
|
артериальная |
42,5 |
95,0 |
65,3 |
17,4 |
|
|
Тимома |
венозная |
37,5 |
117,5 |
74,5 |
21,4 |
|
отсроченная |
37,5 |
122,5 |
81,3 |
23,3 |
Freidman test, р<0,001; Spearman,s rho>0,75
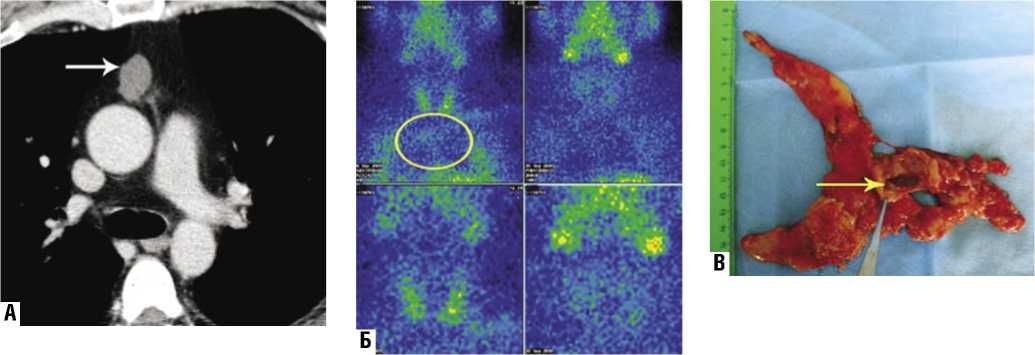
Рис. 1. Комплекс методов обследования пациента К., 45 лет:
А – компьютерная томограмма органов средостения; венозная фаза контрастирования. Выявляется киста ВЖ (указана стрелкой), накопления контрастного вещества в кисте не определяется.
Б – сцинтиграмма средостения с Тс99мМИБИ через 15 мин. (правая вертикальная колонка) и 2 часа (левая вертикальная колонка); аномального очага накопления РФП в проекции ВЖ (область «интереса» выделена овалом) не выявлено;
В – макропрепарат – вскрытая полость кисты ВЖ (указана стрелкой)
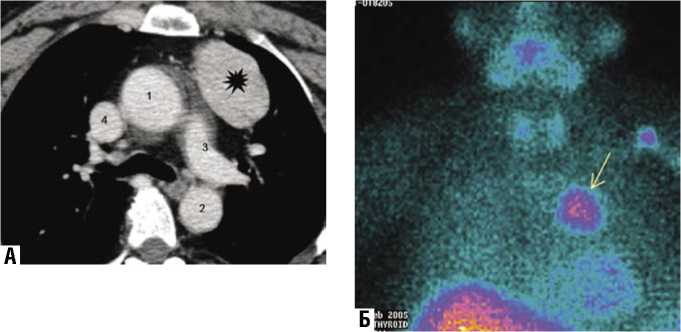
Рис. 2. Комплекс методов обследования пациентки А., 37 лет.
А – компьютерная томограмма органов средостения, венозная фаза контрастирования; выявляется опухоль ВЖ (отмечена звездочкой), накапливающая контрастный препарат; 1 – восходящая аорта, 2 – нисходящая аорта, 3 – левая легочная артерия, 4 – верхняя полая вена
Б – сцинтиграмма средостения с Тс99мМИБИ – выявляется очаг гиперфиксации РФП (указан стрелкой) в опухоли
ВЖ может снижаться за счет существенных изменений, которые развиваются в ткани тимуса с возрастом, и значительных вариаций в размерах и массе ВЖ, в частности, у людей 25–40 лет, когда объем ВЖ может быть увеличен, что затрудняет диагностику тимом. В то время как у больных старше 50 лет, обнаружить тимому легче, поскольку железа замещена жировой тканью, однако ошибки при интерпретации данных КТ случаются во всех возрастных категориях. Гиперплазия ВЖ часто присутствует у пациентов моложе 25 лет, но из-за высокой плотности паренхимы может быть скрытой.
Считается, что наиболее часто тимус имеет треугольную или двудольчатую формы, что подтверждают регистрируемые нами в 50% наблюдений вышеуказанные формы ВЖ в состоянии гиперплазии. Важно отметить, что увеличения размеров железы ни в одном случае верифицированной в дальнейшем лимфоидно-фолликулярной гиперплазии (ЛФГ) не определялось.
Подобные положения подтверждаются литературными данными. В исследовании Nicolaou и соавт. [14] только у 55% больных с ЛФГ на КТ выявлены изменения размеров и структуры тимуса. Более того, Castleman и
Norris [8] показали, что у больных с миастенией масса железы с лимфоидной гиперплазией достоверно не отличался от массы нормального тимуса. Другая литературная ссылка демонстрирует, что до 50% ВЖ, которые по КТ не выглядели измененными, после удаления при гистологическом исследовании содержали ЛФГ [7].
Таким образом, получены результаты, также свидетельствующие о невысокой чувствительности метода КТ в определении ЛФГ. Однако, работ, учитывающих фазовые изменения контрастирования железы, в литературе не представлено. При этом немаловажным результатом нашего исследования явилось значительное увеличение чувствительности метода КТ (до 89,3%) при использовании контрастного усиления. Характер накопления контрастного препарата, начиная с артериальной фазы контрастирования, в отличие от особенностей контрастирования опухолей позволил продемонстрировать большую чувствительность метода.
Среди выделенных нами КТ-признаков тимом чаще встречались образования неправильной формы – 42%, с расположением на уровне ствола легочной артерии – 39,2% или дуги аорты – 35,4%, однородной структуры – 76% наблюдений.
Известно, что на КТ эпителиальные опухоли тимуса обычно представлены гомогенными, овальными, округлыми или дольчатыми (т.е. неправильной формы) мягкотканными структурами, расположенными в переднем средостении. Кроме того, часто опухоль растет асимметрично в одну из сторон переднего средостения, вдаваясь в одну из плевральных полостей. В нашем исследовании подавляющее большинство опухолей (65,8%) располагалось слева по отношению к срединной линии – т.е. в проекции левой доли ВЖ, которая в норме больше правой, что, по-видимому, также объясняет выявленное расположение.
Ряд исследователей, занимающихся проблемами ВЖ, полагают, что контрастирование при выполнении КТ предпочтительно для исключения сосудистой инвазии и наличии кистозного компонента [12]. В нашем исследовании выявлена невысокая чувствительность метода СКТ (33,3%) в выявлении инвазивного характера роста, причем при сравнении СКТ и МСКТ выявлено незначительное преимущество МСКТ (47%). В сравнительных исследованиях методов КТ и МРТ, описанных в литературе [17], МРТ демонстрирует большую чувствительность в обнаружении инвазии. Возможности метода, обусловлены, по-видимому, тем, что при МРТ выявляется более тесная связь между тимусом и прилежащими структурами, благодаря мультипланарности и высокому контрастному разрешению.
Важным результатом проведенного исследования явилось то, что МСКТ является чувствительным методом выявления образований переднего средостения, а при использовании внутривенного контрастирования с учетом артериальной, венозной и отсроченной фаз чувствительность и специфичность метода возрастает. Оценка характера контрастирования позволяет прово- дить дифференциальный диагноз между опухолевым и неопухолевым поражением ВЖ у больных ГМ. Применение методики измерения градиента контрастности в 5-ти разных точках – на 3, 6, 9, 12 часах, и в центре (по аналогии с циферблатом часов), а также в «регионе интереса» позволяет достоверно оценивать характер накопления контрастного препарата. Внутривенное контрастирование в оценке опухолей наиболее информативно в отсроченную (паренхиматозную) фазу, так как тимомы являются слабо васкуляризированными опухолями. В группе гиперплазий накопление контрастного препарата отмечается с артериальной фазы, достигая наибольшей плотности в венозную и отсроченную фазы. Оценка характера контрастирования в артериальную, венозную, отсроченную фазы, не проводимая ранее, позволила достоверно дифференцировать такие изменения ВЖ, как гиперплазия и тимома.
Метод сцинтиграфии является высокоспецифичным в определении опухолей ВЖ. Чувствительность метода снижается за счет сомнительного диффузного накопления РФП в образованиях менее 1,0 см в диаметре, а также при расположении их за рукояткой грудины (рис. 3). В иностранной литературе за последнее время опубликовано немало сообщений о применении неспецифических туморотропных препаратов на основе технеция для исследования пациентов с поражением ВЖ, позволяющих проводить дифференциальный диагноз между опухолевым и неопухолевым ее поражением, у больных ГМ [9,11]. Наше исследование показало, что в группе больных ГМ наличие аномального очага накопления индикатора в проекции ВЖ является специфическим признаком наличия тимомы. Таким образом, в алгоритме обследования больных ГМ высокоспецифичный в отношении опухолевого роста метод сцинтиграфии может быть первым методом исследования. Причем, при отсутствии опухолевого поражения (или наличие опухоли небольших размеров, не выходящей за пределы ВЖ, т.е. не вызывающей подозрений на предмет инвазии) и наличие клинических показаний к проведению оперативного вмешательства, операция может быть выполнена без дополнительного лучевого обследования.
Нельзя не отметить, что диагноз ГМ у наших пациентов был установлен через 3–6 месяцев (Мср=4,2 ± 1,2 мес.) после появления первых симптомов миастении. По данным литературы, в последнее десятилетие с момента появления первых симптомов заболевания до применения одного из специальных методов исследования средостения проходило около 13 месяцев. В предыдущее десятилетие эта цифра достигала 20 месяцев [1, 2]. Соответственно, сократилось время выполнения оперативного вмешательства с 22 до 15 месяцев. По мнению наиболее авторитетных исследователей, безотлагательное исследование ВЖ после установления диагноза миастении создает условия для оперативного вмешательства до развития нерезектабельной опухоли и некорригируемых неврологических расстройств, в связи с чем, проведение
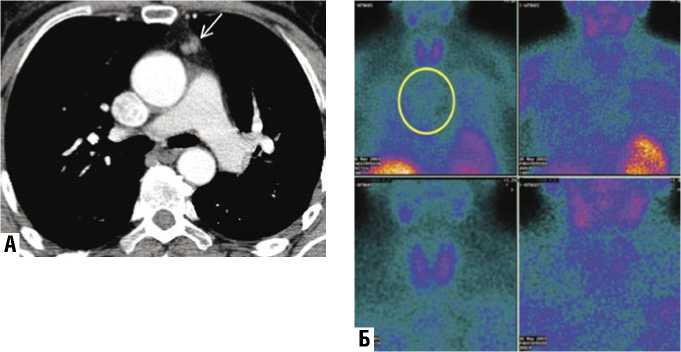
Рис. 3. Комплекс методов обследования пациентки В., 57 лет.
А – компьютерная томограмма органов средостения, артериальная фаза контрастирования, стрелкой указана опухоль ВЖ размерами 1,3х1,0х1,0 см, слабо накапливающая контрастный препарат Б – сцинтиграмма средостения с 99мТс–МИБИ через 15 мин. (правая вертикальная колонка), выделена область «интереса», и через 2 часа (левая вертикальная колонка): очага гиперфиксации РФП в проекции ВЖ не выявлено
КТ или МРТ в максимально короткие сроки после установления диагноза показано всем больным миастенией [3, 6].
Выводы
-
1. МСКТ (СКТ) является информативным методом выявления образований переднего средостения – чувствительность, специфичность и точность метода составили 81,7%, 89,0% и 90,7%, соответственно. Информативность метода возрастает при использовании внутривенного контрастирования, составляя 89,3%, 93,0% и 92,2%.
-
2. Применение внутривенного болюсного контрастирования с оценкой артериальной, венозной и отсроченной фаз оправдано для дифференциальной диагностики поражений ВЖ.
-
3. Чувствительность, специфичность и точность метода МСКТ в отношении инвазии составили 47,0%, 91,0% и 82,1%, а СКТ – 33,3%, 90,5%, 76,2%, соответственно.
-
4. Метод сцинтиграфии является высокоспецифичным – 100% в определении опухолей ВЖ. Чувствительность и точность метода сцинтиграфии при поражении ВЖ несколько ниже и составили 60,8% и 79,5%.
-
5. На первом этапе диагностического алгоритма обследования больных ГМ оптимально проведение МСКТ (СКТ) с внутривенным контрастированием, при невозможности исключения опухолевого роста в ВЖ необходимо проведение сцинтиграфии.


