Роль температурного фактора в морфогенезе генеративных органов лиственницы сибирской (Larix sibirica)
Автор: Иванова А.Н., Голованова Т.И., Новоселова Н.В.
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Экология
Статья в выпуске: 4, 2014 года.
Бесплатный доступ
В ходе исследования выявлено, что на морфогенез генеративных органов лиственницы сибирской оказывают влияние факторы внешней среды: низкие положительные температуры стимулируют воздействие на скорость прохождения материнскими клетками процесса мейоза.
Морфогенез, лиственница сибирская (larix sibirica), низкие положительные температуры, микроспороциты, мейоз
Короткий адрес: https://sciup.org/14083623
IDR: 14083623 | УДК: 57.085.23
The temperature factor role in the morphogenesis of the Siberian larch (Larix sibirica) generative organs
The study revealed that the morphogenesis of the Siberian larch generative organs is influenced by the environmental factors: low positive temperatures stimulate the impact on the rate of mother cell passage of the meiosis process.
Текст научной статьи Роль температурного фактора в морфогенезе генеративных органов лиственницы сибирской (Larix sibirica)
Способность молодых микроспор растений воспроизводить в условиях in vitro целостный организм открывает большие возможности экспериментального получения гаплоидных растений. Гаплоиды являются уникальным и перспективным объектом для клеточной селекции и генетической инженерии растений. Этой проблеме посвящено множество экспериментальных работ и обзорных статей [5, 8, 13, 14].
К настоящему времени накоплен значительный фактический материал по различным аспектам изучения этого явления у представителей различных семейств покрытосеменных растений. Однако не разработана эффективная система массового получения гаплоидов при культивировании мужских генеративных органов, не решены проблемы индукции и регенерации. Остаются неясными механизмы, обусловливающие смену программы развития микроспор с нормального пути созревания на вегетативный путь развития, через эмбриоидо- и каллусогенез в гаплоидное растение. Крайне мало данных по изучению морфогенеза мужских генеративных органов голосеменных.
Ряд исследователей отмечают, что непосредственными причинами морфогенеза являются физиолого-биохимические процессы, происходящие в индивидуальном развитии организма в определенных условиях внешней среды [1– 3, 5– 9, 11, 16, 17].
Одним из важнейших абиотических факторов, определяющих этапность онтогенеза и влияющих на фенотипическое проявление конкретного генотипа растения, являются низкие положительные температуры. Имеются данные о влиянии температурного фактора на становление полярности растительного организма, данный фактор используют как стрессор индукции андроклинии у покрытосеменных растений [8, 14].
Цель работы . Рассмотреть действие низких положительных температур как важный фактор культивирования мужских генеративных органов, при котором происходит высокий выход эмбриоидов.
Объекты и методы. В качестве объектов исследования использовали 30–35-летние деревья лиственницы сибирской, произрастающие на территории экспериментальной базы Института леса «Погорельский бор».
У опытных деревьев Larix sibirica собирали мужские гаметофиты (микростробиллы) с сентября 2003 по май 2004 г. Экспериментальные деревья были разделены на две группы по фенотипическим и морфологическим данным. В первую группу вошли деревья, пораженные лиственничной почковой галлицей, которые отличались от здоровых замедленным ростом и изреженной кроной (рис.1, а). У таких деревьев, как было показано И.Н. Третьяковой [10], идет нарушение мужской сексуализации, то есть превалируют женские шишки. Во вторую группу вошли деревья, не пораженные лиственничной почковой галлицей (рис. 1, б).

а б
Рис. 1. Лиственница сибирская (Larix sibirica Ledeb.): а – не пораженная лиственничной почковой галлицей; б – пораженная лиственничной почковой галлицей
Собранные мужские генеративные органы помещали на модифицированную среду Мурасиге-Скуга [16].
В ходе работы снимали показатели: время прорастания микроспор, размеры пыльцевой трубки; время прохождения мейоза; морфологические особенности материнских клеток микроспор на каждой стадии развития.
Эксперимент проводился в двух вариантах:
-
1. Часть мужских генеративных органов, собранных с поврежденных и неповрежденных деревьев, помещали в холодильник на трое суток, где температура поддерживалась в пределах + 4 Со, после чего переносили на среду MS.
-
2. Другую часть мужских генеративных органов, собранных с поврежденных и неповрежденных деревьев, сразу же помещали на модифицированную среду MS.
Схема проведения эксперимента представлена на рисунке 2.
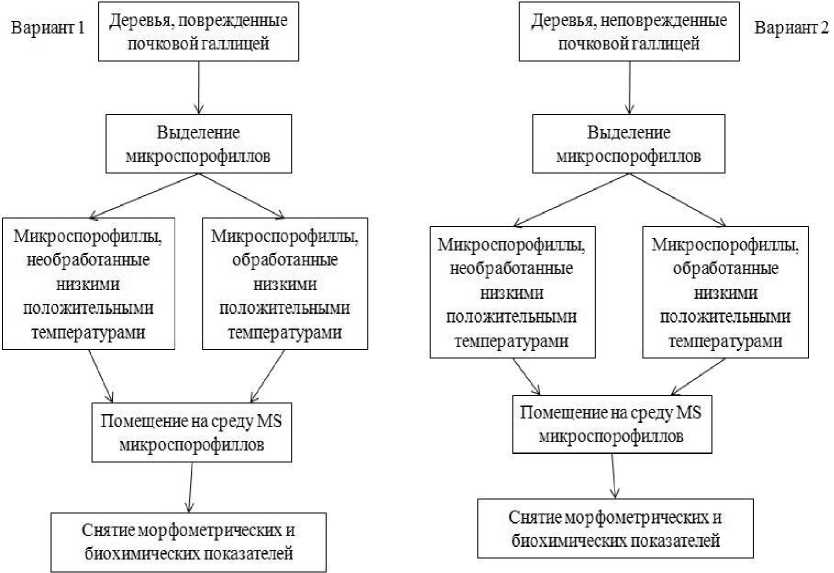
Рис. 2. Схема проведения эксперимента
Результаты и обсуждение. Данные по влиянию температурного фактора на развитие микроспороцитов Larix sibirica in vitro представлены в таблице 1. Необходимо отметить, что для анализа использовали материнские клетки микроспор, которые находились на различных стадиях развития: в осенне-зимний период – на стадии профазы I, в весенний период в микроспороцитах обнаруживалась сильная асинхронность прохождения мейоза (табл. 1), что характерно для хвойных.
Таблица 1
Влияние низких положительных температур на развитие микроспороцитов in vitro , собранных в разные периоды развития микростробил Larix sibirica
|
Дерево |
Месяц |
Сутки |
Метафаза I |
Анафаза I |
Телофаза I |
Интерфаза |
Тетрады |
Микроспоры |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
Микростробилы, не обработанные низкими положительными температурами +4 Сo |
||||||||
|
нП |
Октябрь |
3 |
11,2 |
78,2 |
10,6 |
|||
|
5 |
0,1 |
99,9 |
||||||
|
7 |
0,1 |
10,2 |
89,7 |
|||||
|
Декабрь |
3 |
62,4 |
37,6 |
|||||
|
5 |
0,7 |
52,1 |
47,1 |
0,1 |
||||
|
7 |
0,3 |
21,9 |
77,8 |
|||||
|
14 |
0,1 |
99,9 |
||||||
|
Апрель |
3 |
100 |
||||||
Окончание табл. 1
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
П |
Октябрь |
3 |
35,6 |
64,4 |
||||
|
5 |
0,7 |
52,1 |
47,1 |
0,1 |
||||
|
7 |
0,3 |
21,9 |
77,8 |
|||||
|
14 |
0,1 |
99,9 |
||||||
|
Декабрь |
3 |
78,2 |
11,2 |
10,6 |
||||
|
5 |
0,1 |
75,3 |
24,6 |
|||||
|
7 |
10,3 |
89,7 |
||||||
|
14 |
100 |
|||||||
|
Апрель |
3 |
100 |
||||||
|
Микростробилы, об |
работанные низкими положительными температурами +4 Сo |
|||||||
|
нП |
Октябрь |
3 |
9,6 |
67,3 |
23,1 |
|||
|
5 |
89,2 |
10,8 |
||||||
|
7 |
10,3 |
89,7 |
||||||
|
Декабрь |
3 |
8,4 |
67,3 |
24,3 |
||||
|
5 |
81,3 |
18,7 |
||||||
|
7 |
19,1 |
80,9 |
||||||
|
Апрель |
3 |
100 |
||||||
|
П |
Октябрь |
3 |
9,1 |
67,7 |
23,2 |
|||
|
5 |
99,9 |
0,1 |
||||||
|
7 |
2,9 |
97,1 |
||||||
|
Декабрь |
3 |
7,2 |
92 |
0,8 |
||||
|
5 |
0,2 |
87,7 |
12,1 |
|||||
|
7 |
14,7 |
85,3 |
||||||
|
Апрель |
3 |
100 |
||||||
В культуре in vitro в октябре месяце у непораженных деревьев большое количество материнских клеток микроспор находилось в анафазе I, а на 7-е сутки культивирования появляются тетрады, на долю которых приходится около 90 %. В декабре, когда лиственница сибирская находилась в состоянии физиологического покоя, распределение микроспороцитов по фазам несколько иное. На 3-и сутки большее количество микроспороцитов находилось на стадии метафазы I, однако на 14-е сутки было обнаружено 100 %-е образование микроспор, покрытых тонкой экзиной. У растений, пораженных лиственничной почковой галлицей, было отмечено в осенне-зимний период неравномерное распределение микроспороцитов по отдельным фазам мейоза, и образование микроспор проходило медленнее (табл. 1).
В весенние сроки культивирования у не пораженных и пораженных деревьев лиственничной почковой галлицей у микроспороцитов происходило быстрое завершение мейоза.
Большой интерес представляют данные по обработке микростробил низкими положительными температурами. В литературе встречаются исследования, где низкие положительные температуры способствовали получению высокого выхода андрогенных культур у пшеницы [5]. В.Ю. Горбуновой впервые обнаружено: «… дифференциальная эксперессия транскриптов, накапливающихся в микроспорах в ответ на воздействие пониженных положительных температур на пыльники яровой мягкой пшеницы поздней стадии микроспорогенеза. Эта спорофитная генетическая информация реализуется в перестройке веретена деления первого митоза и появлении микроспор с двумя равными ядрами, что характеризует начало прямого андрогенеза in vitro » [4].
В наших исследованиях показано, что пониженные положительные температуры оказывали стимулирующее воздействие на прохождение клетками процесса мейоза, микростробилы которых были собраны в осенне-зимний и весенний периоды. Следует отметить, что у микростробил, собранных в данный период, уже на 3-е сутки культивирования микроспороциты находились в анафазе I в отличие от клеток, микростробилы которых не были обработаны низкими положительными температурами.
Несмотря на то, что на 7-е сутки образованы микроспоры как у непораженных, так и у пораженных деревьев, в их размерах были отмечены существенные различия (табл. 2).
Таблица 2
|
Дерево Месяцп Сутки in vivo 1 Метафаза I1 Анафаза Iп Телофаза Iп Интерфаза Тетрадып Микроспоры |
|||||||||
|
Микростробилы, не обработанные низкими положительными темпе |
ратурами +4 Сo |
||||||||
|
нП |
Октябрь |
3 |
37,76 ±0,22 |
39,17±0,17 |
56,06 ±0,24 |
76,01±0,21 |
|||
|
5 |
54,01±0,21 |
75,31± 0,18 |
|||||||
|
7 |
76,13±0,19 |
84,21±0,31 |
91,52 ±0,21 |
||||||
|
Декабрь |
3 |
37,92 ±0,20 |
38,19±0,17 |
54,6±0,33 |
|||||
|
5 |
38,92±0,24 |
56,40±0,59 |
75,68±0,18 |
85,53±0,16 |
|||||
|
7 |
85,43±0,19 |
92,01±0,26 |
101,3±0,15 |
||||||
|
Апрель |
3 |
51,27 ±0,16 |
91,59±0,21 |
||||||
|
5 |
101,08±0,15 |
||||||||
|
7 |
115,1±0,31 |
||||||||
|
П |
Октябрь |
3 |
34,48 ±0,17 |
37,76 ± 0,2 |
41,36±0,21 |
52,28±0,33 |
|||
|
5 |
50,21±0,29 |
60,01±0,36 |
75,61±0,23 |
89,75±0,27 |
|||||
|
7 |
76,12±0,12 |
90,20±0,31 |
99,89±0,21 |
||||||
|
Декабрь |
3 |
35,76 ±0,19 |
38,4±0,19 |
39,63±0,25 |
60,3±0,59 |
||||
|
5 |
54,7±0,27 |
73,47±0,18 |
76,09±0,18 |
||||||
|
7 |
90,56±0,26 |
91,60±0,38 |
|||||||
|
Апрель |
3 |
49,92 ±0,12 |
89,79±0,23 |
||||||
|
5 |
98,09±0,38 |
||||||||
|
7 |
102,12±0,26 |
||||||||
|
Микростробилы, обработанные низкими положительными температурами +4 Сo |
|||||||||
|
нП |
Октябрь |
3 |
37,76 ±0,22 |
69,82±0,23 |
85,46±0,36 |
90,06±0,28 |
|||
|
5 |
91,87±0,21 |
95,3 ± 0,12 |
|||||||
|
7 |
96,89±0,27 |
110,63±0,27 |
|||||||
|
Декабрь |
3 |
37,92 ±0,20 |
65,78±0,34 |
78,26±0,18 |
89,61±0,18 |
||||
|
5 |
95,41±0,21 |
109,56±0,31 |
|||||||
|
7 |
19,1 |
120,31±0,15 |
|||||||
|
Апрель |
3 |
51,27 ±0,16 |
93,76±0,28 |
||||||
|
5 |
101,31±0,21 |
||||||||
|
7 |
124,3±0,15 |
||||||||
|
П |
Октябрь |
3 |
34,48 ±0,17 |
50,43±0,19 |
74,89±0,29 |
80,91±0,21 |
|||
|
5 |
76,5±0,31 |
82,84±0,20 |
89,03±0,25 |
||||||
|
7 |
90,95±0,21 |
100,8±0,33 |
|||||||
|
Декабрь |
3 |
35,76 ±0,19 |
60,11±0,33 |
77,23±0,59 |
80,59±0,25 |
||||
|
5 |
80,65±0,21 |
85,36±0.23 |
100,15±0,24 |
||||||
|
7 |
85,95±0,29 |
100,23±0,38 |
|||||||
|
Апрель |
3 |
49,92 ±0,12 |
90,12±0,33 |
||||||
|
5 |
99,89±0,59 |
||||||||
|
7 |
106,39±0,38 |
||||||||
Размеры микроспороцитов и микроспор
Размеры микроспороцитов, образованных от микростробил не обработанных низкими положительными температурами деревьев, не пораженных лиственничной почковой галлицей, в метафазе I на 3-е сутки отличались от размеров микроспороцитов пораженных деревьев. Существенную разницу наблюдали у непораженных и пораженных деревьев на 5-е и 7-е сутки культивирования. Особенно значительные отличия проявились в анафазе I и телофазе I (табл. 2). Образованные микроспоры имели тонкую экзину и к 14-м суткам культивирования образовывали двухклеточное пыльцевое зерно, которое прорастало с образованием пыльцевой трубки.
Наиболее существенную разницу в размерах микроспороцитов наблюдали у деревьев, обработанных низкими положительными температурами: в осенне-зимний и весенний периоды на 3-е сутки культивирования их размеры составили: у деревьев, не пораженных лиственничной почковой, – 69,82 мкм, а у пораженных – 60,11 мкм. Такая же закономерность наблюдается и на 5- и на 7-е сутки культивирования. У микроспор, полученных таким путем, наблюдаются тонкая экзина и деполяризация клетки.
Таким образом, низкие положительные температуры оказывают положительное влияние не только на прохождение мейоза, но и на размер образованных микроспор.
У микроспор, образованных в осенне-зимний период, наблюдается образование одноклеточного пыльцевого зерна, которое образует пыльцевую трубку на 14-е сутки культивирования (рис. 3, а), а в дальнейшем – ценоцит (рис. 3, б).
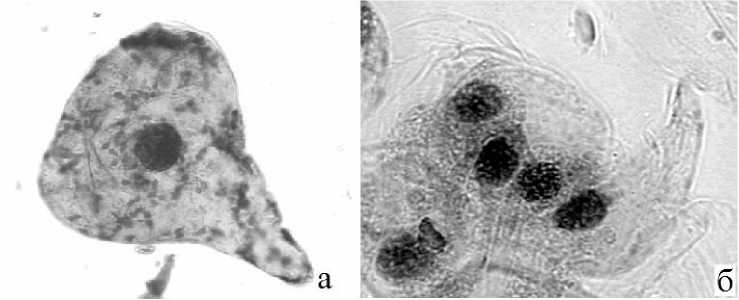
Рис. 3. Образование пыльцевой трубки на 14-е сутки культивирования и на 21-е сутки ценоцита
У микроспор, полученных в апреле месяце, на 14-е сутки от момента инокуляции микроспорофиллов на среду in vitro в образованных микроспорах отмечены равные митотические деления с образованием сначала двух равных ядер, а затем двух равных клеток (рис. 4).
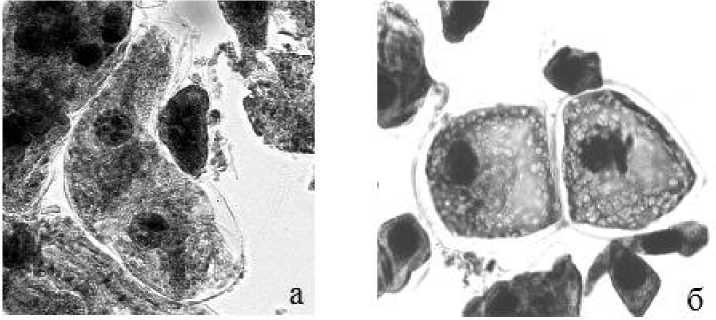
Рис. 4. Митотическое деление микроспоры in vitro
Следовательно, низкие положительные температуры оказывают положительное влияние не только на прохождение мейоза, но и на переход от гаметофитного пути на спорофитный. Это объясняется тем, что в результате действия температур подавляется процесс гаметофитной программы развития и запускается тем самым спорофитная программа.


