Роль воспаления в патогенезе ишемической болезни сердца
Автор: Рохибжонов А.Р.
Журнал: Экономика и социум @ekonomika-socium
Рубрика: Современные науки и образование
Статья в выпуске: 10-1 (101), 2022 года.
Бесплатный доступ
Ишемическая болезнь сердца (ИБС) - важнейшая проблема современной кардиологии. Она приводит к снижению качества жизни, высокой инвалидизации и летальности. Основную роль в патогенезе ИБС играют атерогенез и сопутствующее воспаление сосудов.
Ишемическая болезнь сердца (ибс), медиаторы воспаления, атеросклероз
Короткий адрес: https://sciup.org/140300295
IDR: 140300295
The role of inflammation in the pathogenesis of coronary heart disease
Coronary heart disease (CHD) is the most important problem of modern cardiology. It leads to a decrease in the quality of life, high disability and mortality. The main role in the pathogenesis of coronary heart disease is played by atherogenesis and concomitant vascular inflammation.
Текст научной статьи Роль воспаления в патогенезе ишемической болезни сердца
Воспаление — самый распространенный типовой патологический процесс, лежащий в основе большинства болезней человека. В патогенезе атеросклероза и обострения ИБС роль основного звена отводят воспалительной реакции. Воспалительный процесс развивается на: местном уровне, что определяется базисными механизмами воспалительный ответ (СВО).
воспаления,
и системном —системный
Системное воспаление — это типовой, мультисиндромный, фазоспецифичный патологический процесс, развивающийся на организменном уровне и характеризующийся тотальной воспалительной активностью эндотелиоцитов, плазменных факторов, клеток крови и соединительной ткани, а также микроциркуляторными расстройствами в жизненно важных органах и тканях с развитием полиорганной недостаточности [3].
Воспалительная реакция сопровождается увеличением [Н+] и, соответственно снижением рН в клетках и межклеточной жидкости — развитием ацидоза. Причиной метаболического ацидоза является накопление в очаге воспаления избытка недоокисленных соединений.
Основными механизмами развития метаболического ацидоза являются:
-
• образование большого количества «кислых» продуктов изменённого метаболизма вследствие активации гликолиза (что сопровождается накоплением избытка молочной и пировиноградной кислот), усиления протеолиза и липолиза (с накоплением избытка аминокислот, высших жирных и кетоновых кислот);
-
• нарушение оттока из очага воспаления продуктов как нормального, так и нарушенного обмена веществ. Последнее особенно выражено в связи с замедлением оттока венозной крови и развитием стаза в очаге воспаления; — «истощение» щелочных буферных систем (бикарбонатной, фосфатной, белковой и других) клеток и межклеточной жидкости, которые на начальном этапе воспаления нейтрализуют избыток кислых соединений [10].
Последствия метаболического ацидоза в очаге воспаления приведены на рис. 1.
Хроническое системное воспаление — это мультисиндромный патологический процесс, развивающийся при системном повреждении и характеризующийся тотальной воспалительной реактивностью эндотелиоцитов, плазменных и клеточных факторов крови, соединительной ткани, а на заключительных этапах — и микроциркуляторными расстройствами в жизненно важных органах и тканях [13].
Рис. 1.
Эффекты ацидоза в очаге воспаления [10].
Медиаторы воспаления

Клеточные

Плазменные
-
• Синтезируются в клетках
-
• Высвобождаются в очаге воспаления; как правило, в активированном состоянии
-
• Синтезируются в клетках
-
• Высвобождаются в плазму крови и/или межклеточную жидкость в неактивном состоянии
-
• Активируются непосредственно в очаге воспаления
Медиаторы воспаления представляют собой биологически активные вещества, образующиеся в процессе самого воспаления и обеспечивающие межклеточную коммуникацию. Все медиаторы воспаления и их неактивные предшественники образуются в различных клетках организма.
Тем не менее, условно их подразделяют на клеточные и плазменные (рис. 2).
Рис. 2.
Виды медиаторов воспаления [10].
Клеточные медиаторы высвобождаются в очаге воспаления уже в активированном состоянии непосредственно из клеток, в которых они синтезировались и накопились (обычно из внутриклеточных везикул или гранул). Плазменные медиаторы также образуются в клетках, но выделяются в межклеточную жидкость, лимфу и кровь не в активном состоянии, а в виде предшественников. Эти вещества активируются под действием различных промоторов, преимущественно в плазме крови. После этого они становятся физиологически активными и действуют в тканях [10].
В зависимости от воздействия на воспалительный процесс цитокины подразделяются на две группы — провоспалительные (ИЛ-1, ИЛ-6, ИЛ-8, ФНОа, ИЛ-12) и противовоспалительные (ИЛ-4, ИЛ-10, ТФР-в). Провоспалительные цитокины — важный и хорошо изученный класс биологически активных веществ, оказывающих иммунорегуляторное ипровоспалительное действие [3].
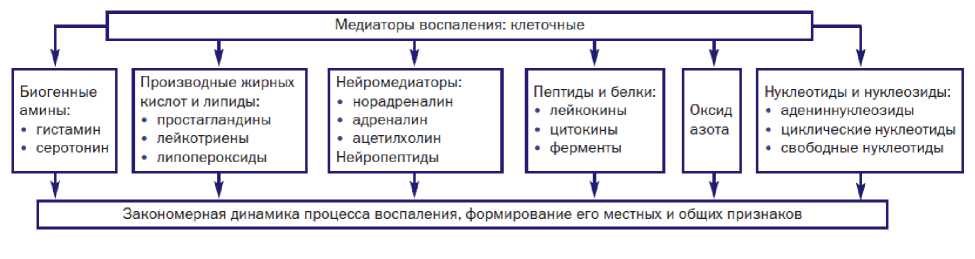
Клеточные медиаторы воспаления. К клеточным медиаторам воспаления относят биогенные амины, нейромедиаторы, нейропептиды, цитокины, лейкокины (факторы, секретируемые лейкоцитами), активные формы кислорода (и вещества их генерирующие, например, оксид азота), производные ВЖК и липидов (липидные медиаторы), нуклеотиды и нуклеозиды (рис. 3).
Рис. 3.
Основные классы клеточных медиаторов воспаления [10].
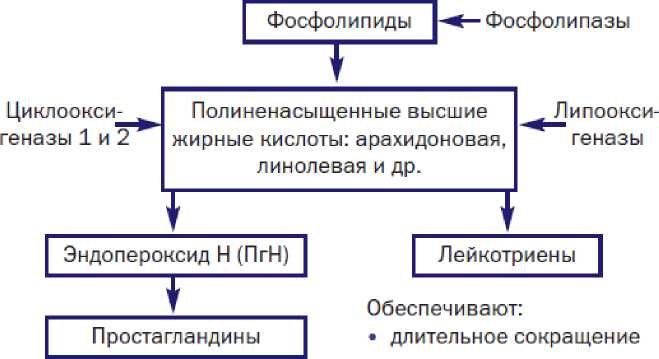
гладкомышечных клеток
Обеспечивают регуляцию:
• тонуса и проницаемости стенок микрососудов
• кровотока в них
• системы гемостаза
• эмиграции лейкоцитов и фагоцитоза
• деления и созревания в стенке микрососудов
• развитие ишемии тканей
• регуляцию эмиграции лейкоцитов и фагоцитоза
• лабилизацию мембран лизосом лейкоцитов клеток
При атеросклерозе отмечается повышение экспрессии молекул адгезии VCAM-1на эндотелиоцитах, что под влиянием провоспалительных хемоаттрактантов приводит к миграции моноцитов винтиму артерий и последующей их трансформации в пенистые клетки. Т-лимфоциты также мигрируют, выделяя цитокины, усиливающие локальное воспаление. После формирования бляшки постоянное взаимодействие лимфоцитов и макрофагов поддерживает воспалительный процесс.
Известно, что цитокины оказывают разнонаправленные регуляторные влияния на атеросклеротический процесс. Так, провоспалительные цитокины (ФНОα, ИЛ-1β, ИЛ-6, ИЛ-8) рассматриваются как атерогенные, а противовоспалительные цитокины (ИЛ-4 и ИЛ-10) — как антиатерогенные медиаторы.
У больных ИБС воспаление представляет собой нелокальный процесс, ограниченный зоной атеросклеротического поражения сосудистой стенки, воспалительные реакции имеют системный характер, сопровождаясь повышением в крови уровня маркеров и медиаторов воспаления [3].
Роль лейкоцитов в патогенезе ИБС и инфаркта миокарда. Многочисленные экспериментальные и клинические исследования показали, что лейкоцитоз является таким же независимым фактором риска ИБС, как увеличение содержания общего холестерола, глюкозы (сахарный диабет), повышенное артериальное давление, курение и избыточная масса тела. Показано, что вызванный спленэктомией лейкоцитоз у мышей с гипергликемией и экспериментальным инфарктом миокарда (ИМ) ассоциируется с увеличением на 43% площади некротизированного участка миокарда в сравнении с животными без удаления органа. В опытах на мышах с экспериментально вызванным ИМ установлено, что ингаляция воздуха, загрязненного твердыми частицами, содержащими ванадий, никель и железо, сопровождается увеличением содержания макрофагов и секреции ими цитокинов. Усугубляется течение заболевания. Так, на фоне трехкратного увеличения в крови содержания клеток площадь ИМ возрастала в 5 раз [2].
Высокая концентрация маркеров системного воспаления ассоциирована с усугублением атеросклероза и развитием его осложнений. Повышенная продукция провоспалительных цитокинов способствует усилению адгезии лейкоцитов сосудистым эндотелием, стимулирует захват липопротеинов низкой плотности макрофагами, обусловливает развитие острого воспаления в основании атеромы, ее дестабилизацию, вазоконстрикцию, тромбообразование и окклюзию коронарных артерий. Все это лежит в основе острого коронарного синдрома (ОКС) [12].
Высокая концентрация маркеров системного воспаления ассоциирована с усугублением атеросклероза и развитием его осложнений. Повышенная продукция провоспалительных цитокинов способствует усилению адгезии лейкоцитов сосудистым эндотелием, стимулирует захват липопротеинов низкой плотности макрофагами, обусловливает развитие острого воспаления в основании атеромы, ее дестабилизацию, вазоконстрикцию, тромбообразование и окклюзию коронарных артерий. Все это лежит в основе острого коронарногосиндрома.
ИЛ-6 играет особую роль в патогенезе атеросклероза. Этот цитокин, по данным современных авторов, имеет значение для раннего прогнозирования высокого риска возникновения серьезных сердечно-сосудистых событий, является показателем тяжести течения заболеваний сердца и маркером высокого риска смерти от инфаркта миокарда.
При воспалении последовательно секретируются ФНО-а, ИЛ-1в и ИЛ-6. Затем ИЛ-6 начинает ингибировать секрецию ФНО-а и ИЛ-ip, активировать продукцию печенью белков острой фазы воспаления и стимулировать гипоталамо-гипофизарно-надпочечниковую систему, что способствует регуляции воспалительного процесса, в связи с чем ИЛ-6 можно рассматривать и как провоспалительный, и как противовоспалительный цитокин. Основное действие ИЛ-6 связано с его участием в качестве кофактора при дифференцировке В-лимфоцитов, их созревании и преобразовании в плазматические клетки, секретирующие иммуноглобулины.
Помимо этого, ИЛ-6 способствует экспрессии рецептора ИЛ-2 на активированных иммуноцитах, а также индуцирует производство ИЛ-2 Т-клетками. Данный цитокин стимулирует пролиферацию Т-лимфоцитов и реакции гемопоэза.
Заключение. Остается до конца не изученным значение провоспалительного цитокина ИЛ-2, продуцируемого Т-лимфоцитами. Имеются данные, указывающие на прямое участие ИЛ-2 в ассоциации с СРБ в провоцирующем механизме развития ОКС. По другим источникам, повышение концентрации растворимых рецепторов ИЛ-2 в крови имеет независимое прогностическое значение агрессивного клинического течения дилатационной кардиомиопатии и превышает их уровень в крови больных ИБС в сравнительном исследовании [12].
Список литературы Роль воспаления в патогенезе ишемической болезни сердца
- Афанасьева О.И., Тмоян Н.А., Клесарева Е.А., Разова О.А., Афанасьева М.И., Бурдейная А.Л., Саидова М.А., Ежов М.В., Покровский С.Н. Маркеры воспаления у больных хронической ишемической болезнью сердца со стенозом аортального клапана // РКЖ. 2018. №9.
- Басалай О. Н., Бушма М. И., Борисенок О. А. Роль воспаления в патогенезе ишемической болезни сердца и инфаркта миокарда //Медицинские новости. - 2020. - №. 6 (309). - С. 13-18.
- Гордеева Е.К., Каде А.Х. Изменение цитокинового статуса при стабильной стенокардии напряжения // Медицинский вестник Юга России. 2016. №1.
- Закирова А. Н., Закирова Н. Э., Николаева И. Е., Хамидуллина Р. М., Фахретдинова Е. Р. Иммуновоспалительные реакции при стабильном течении ишемической болезни сердца // Медицинский вестник Башкортостана. 2012. №4.
- Закирова Аляра Нурмухаметовна, Закирова Нэлли Эриковна Экспрессия провоспалительных цитокинов при стабильной стенокардии // СагёюСоматика. 2013. №1
- Закирова Н. Э. и др. Иммуновоспалительные реакции при ишемической болезни сердца //Рациональная фармакотерапия в кардиологии. - 2007. - Т. 3. - №. 2. - С. 16-19.
- Закирова Нэлли Эриковна, Закирова Аляра Нурмухаметовна Роль иммуновоспалительных реакций и дисфункции эндотелия в ремоделировании миокарда и прогрессировании ишемической болезни сердца // РФК. 2014. №5.
- Зенина Е. А. МЕДИАТОРЫ ВОСПАЛЕНИЯ И ДИСФУНКЦИЯ ЭНДОТЕЛИЯ ПРИ ОСТРОМ КОРОНАРНОМ СИНДРОМЕ //Вестник Российского государственного медицинского университета. - 2006. - №. 2. - С. 24-24.
- Куликов В. А., Гребенников И. Н. Резольвины, протектины и марезины: новые медиаторы воспаления //Вестник Витебского государственного медицинского университета. - 2012. - Т. 11. - №. 1. - С. 25-30.
- Литвицкий П. Ф. Воспаление //Вопросы современной педиатрии. -2006. - Т. 5. - №. 4. - С. 75-81.
- Оганов Р. Г., Закирова Н. Э., Закирова А. Н., Салахова Г. М., Плотникова М. Р. Иммуновоспалительные реакции при остром коронарном синдроме // РФК. 2007. №5.
- Провоторов В. М. и др. Провоспалительные цитокины при сочетании ишемической болезни сердца и хронической обструктивной болезни легких //Клиническая медицина. - 2015. - Т. 93. - №. 2. - С. 5-9.
- Провоторов В. М., Будневский А. В., Семенкова Г. Г., Шишкина Елена Сергеевна Провоспалительные цитокины при сочетании ишемической болезни сердца и хронической обструктивной болезни легких // Клиническая медицина. 2015. №2.
- Сомова Л. М., Плехова Н. Г. Оксид азота как медиатор воспаления //Вестник Дальневосточного отделения Российской академии наук. - 2006. - №. 2. - С. 77-80.
- Татенкулова С. Н. и др. Роль гуморальных воспалительных факторов в патогенезе ишемической болезни сердца //Кардиология. - 2009. - Т. 49. -№. 1. - С. 4-8.
- Хусаинова Л. Н. и др. Медиаторы воспаления в генезе инфаркта миокарда //Евразийский кардиологический журнал. - 2016. - №. 3. - С. 103-104.
- Шальнев В. И. Острый коронарный синдром: как снизить остаточный воспалительный риск? //Российский кардиологический журнал. - 2020. -№. 2. - С. 113-118.
- Шальнев В. И., Мазуров В. И. С-реактивный белок при остром коронарном синдроме: содержание в плазме крови, роль в патогенезе и влияние ранней иммуномодулирующей терапии статинами // Вестник Северо-Западного государственного медицинского университета им. И. И. Мечникова. 2011. №2.


