Роль высокого и низкого уровня тестостерона в развитии сердечно-сосудистой патологии (на примере клинических случаев)
Автор: Тимофеев Е.В., Петрова Е.А., Реева С.В., Парфенова Н.Н.
Журнал: Juvenis scientia @jscientia
Рубрика: Клинические случаи
Статья в выпуске: 3 т.11, 2025 года.
Бесплатный доступ
Снижение и повышение уровня тестостерона у мужчин до андропаузы сопровождается рядом метаболических, функциональных и органических изменений со стороны различных систем, в первую очередь — сердечно-сосудистой. Для таких мужчин характерно развитие дислипидемии и повышение сердечно-сосудистого риска. Гипогонадизм ассоциирован также с ожирением, нарушениями углеводного обмена, развитием атеросклероза. Неконтролируемое введение анаболических стероидных гормонов в отсутствие медицинских показаний для этого приводит к нарушению реологии крови, развитию жизнеугрожащих нарушений сердечного ритма, тяжёлой сердечной недостаточности, внутрисосудистому тромбообразованию. Представлено два клинических случая: мужчина молодого возраста с аритмическим вариантом кардиомиопатии, развившейся вследствие приёма анаболических стероидов, и мужчина среднего возраста с длительно существующим гипогонадизмом. Показаны клинические проявления этих состояний, темпы их развития и прогрессирования, реакция на проводимую специфическую (в случае гипогонадизма — гормонзаместительную) и неспецифическую терапию. Особенностями обоих случаев является недооценка самими пациентами тяжести изменений и своего состояния, отказ от коррекции терапии. Несмотря на очевидность и простоту терапии таких состояний и обратимость большинства изменений, низкая приверженность лечению значительно увеличивает сердечно-сосудистый риск и риск внезапной смерти.
Тестостерон, мужской гипогонадизм, дислипидемия, кардиомиопатия, анаболические стероиды, трепетание предсердий, нарушения ритма сердца, мужчины, сердечно-сосудистый риск
Короткий адрес: https://sciup.org/14133225
IDR: 14133225 | DOI: 10.32415/jscientia_2025_11_3_48-62
The Role of High and Low Testosterone Levels in the Development of Cardiovascular Pathology (on the Example of Clinical Cases)
A decrease and increase in testosterone levels in men before andropause is accompanied by a number of metabolic, functional and organic changes on the part of various systems, primarily the cardiovascular system. Such men are characterized by the development of dyslipidemia and increased cardiovascular risk. Hypogonadism is also associated with obesity, impaired carbohydrate metabolism, and the development of atherosclerosis. Uncontrolled administration of anabolic steroid hormones in the absence of medical indications for this leads to impaired blood rheology, the development of life-threatening cardiac arrhythmias, severe heart failure, and intravascular thrombosis. Two clinical cases are presented: a young man with an arrhythmic variant of cardiomyopathy, which developed as a result of taking anabolic steroids, and a middle-aged man with long-term existing hypogonadism. The clinical manifestations of these conditions, the rate of their development and progression, and the reaction of changes to hormone replacement and non-specific therapy performed in the case of hypogonadism are shown. The peculiarities of both cases are that the patients themselves underestimate the severity of the changes and their condition, and refuse to correct therapy. Despite the obvious and simple treatment of such conditions and the reversibility of most changes, low adherence to therapy significantly increases cardiovascular risk and the risk of sudden death.
Текст научной статьи Роль высокого и низкого уровня тестостерона в развитии сердечно-сосудистой патологии (на примере клинических случаев)
Значительное изменение уровня тестостерона у мужчин до андропаузы сопровождается рядом метаболических, функциональных и органических изменений со стороны различных систем, в первую очередь — сердечно-сосудистой. Для таких мужчин характерно развитие дислипидемии и повышение сердечно-сосудистого риска независимо от характера изменений (снижение или повышение) уровня тестостерона. При этом гипогонадизм (дефицит тестостерона) ассоциирован также с ожирением, нарушениями углеводного обмена, развитием атеросклероза. Гипогонадизм у мужчин — это клинико-биохимический синдром, связанный с низким уровнем тестостерона, а также нечувствительностью рецепторного аппарата к андрогенам, который может оказывать негативное воздействие на различные органы и системы, ухудшая качество жизни и жизненный прогноз [1].
Классифицируют гипогонадизм в зависимости от уровня нарушений — выделяют первичный (на уровне половых желёз), вторичный (патология на уровне гипоталамуса и гипофиза), а также смешанный (при сочетании обоих вариантов) [2].
Основными признаками гипогонадизма считают: снижение либидо и сексуальной активности, снижение числа утренних эрекций, снижение адекватных эрекций [3–5]. Между тем, отмечается, что клинические проявления обычно неспецифичны и без определения уровня тестостерона сыворотки не могут быть идентифицированы. Наиболее частыми поводами для лабораторного обследования являются [из 6 с сокр.]:
— Гипоплазия яичек
— Сексуальная дисфункция
— Бесплодие
— Ожирение
— Гинекомастия
-
— Хронические сердечно-сосудистые заболевания
— Дислипидемия
-
— Метаболический синдром
При гипогонадизме часто развиваются многие из компонентов метаболического синдрома: ожирение, артериальная гипертензия, нарушения углеводного обмена — сахарный диабет 2 типа, нарушение толерантности к глюкозе, инсулино-резистентность и дислипидемия, проявляющаяся повышением уровня триглицеридов и липопротеидов низкой плотности, а также снижением уровня липопротеидов высокой плотности [7]. Сочетание гипогонадизма с ожирением значимо уменьшает продолжительность жизни мужчин [8].
Пути воздействия андрогенов на липидный обмен на сегодняшний день изучены не до конца. Предполагается, что тестостерон реализует свои эффекты на метаболизм липидов через экспрессию двух генов, участвующих в катаболизме липопротеидов, — печёночной липазы и скэвенджер-рецептора SR-B1, активируя их [9]. Печёночная липаза осуществляет гидролиз триглицеридов и фосфолипидов, что ведёт к усиленному распаду ЛПВП. Скэвенджер-рецептор SR-B1 способствует избирательному захвату холестерина гепатоцитами, клетками Сертоли и Лейдига, что обеспечивает стероидогенез, вызывая тем самым отток липидов из периферических тканей. Тестостерон оказывает непосредственное влияние на метаболизм и обладает анаболическим и липолитическим эффектами [10]. Эндогенный тестостерон стимулирует развитие миоцитов, тормозит развитие адипоцитов, снижает синтез свободных жирных кислот, ингибирует ферменты, отвечающие за накопление триглицеридов жировой ткани [11]. Андрогенный дефицит ослабляет данные эффекты, что приводит к нарушению липидного профиля и способствует развитию ожирения [12]. Описанные модели наиболее изучены у мужчин среднего и пожилого возраста в андропаузу [13].
Диагностика гипогонадизма заключается в оценке клинических симптомов, ассоциированных с дефицитом андрогенов, и выявлении стойкого снижения уровня тестостерона (как минимум двукратное подтверждение) надёжным лабораторным методом. Для верификации первичного гипогонадизма оценивают размер тестикул [2].
Первичный гипергонадотропный, вторичный гипогонадотропный, а также смешанный гипогонадизм являются необратимыми, таким пациентам в случае отсутствия необходимости в сохранении репродуктивной функции рекомендуется назначение препаратов тестостерона (уровень доказа- тельности 1А). Рекомендуется назначение трансдермального препарата тестостерона мужчинам с гипогонадизмом, обусловленным нарушением отрицательной обратной связи гипофиз–гонады, при невозможности добиться целевых показателей терапии основного заболевания с целью повышения эффективности лечения основного заболевания и минимизации негативного воздействия на гонадотропную функцию гипофиза (уровень доказательности 5С) [14].
С другой стороны, известно, что тестостерон и его синтетические аналоги или анаболические стероиды (АС) обладают одновременно анаболическим и андрогенизирующим действием. Основной эффект применения АС заключается в стимуляции синтеза белка за счёт воздействия на рецепторы к андрогенам, что в результате приводит к росту всех органов, потенциально способных увеличиваться [15]. АС назначаются не только для коррекции андрогенного дефицита, о чем уже говорилось, но и для стимуляции эритропоэза при недостаточности костного мозга; также АС широко используются для увеличения мышечной массы и достижения спортивных результатов. Описаны и другие положительные эффекты заместительной гормонотерапии [16, 17]. Однако за последние несколько десятилетий использование АС значительно возросло не только среди спортсменов, но и среди населения в целом. Такая тенденция к немедицинскому применению АС является серьёзной проблемой здравоохранения из-за рисков развития побочных эффектов. Такими нежелательными эффектами являются бесплодие, гепатотоксичность, психические нарушения и гинекомастия, а также различные сердечно-сосудистые осложнения, одним из которых является кардиомиопатия [18].
Кардиомиопатия, вызванная АС, характеризуется структурными и функциональными изменениями в сердце, которые проявляются гипертрофией левого желудочка, нарушением систолической и диастолической функции и в тяжёлых случаях сердечной недостаточностью. При этом кардио-токсические эффекты, особенно вследствие неправильного использования АС, включают прямое повреждение миокарда, фиброз и дисфункцию эндотелия. Эти механизмы способствуют развитию структурных изменений, выявляемых при визуализации, таких как диффузная гипокинезия миокарда и кардиомегалия. Симптомы кардиомиопатии, вызванной АС, часто неспецифичны и варьируют от одышки до серьёзных сердечных осложнений, таких как желудочковая тахикардия и кардиогенный шок.
По мнению многих исследователей, применение АС связано со значительным повышением риска сердечно-сосудистых заболеваний в целом. Так, по результатам 11-летнего наблюдения установлено, что у лиц, получавших АС (n = 1189), регистрировалась значительно более высокая частота сердечно-сосудистых осложнений по сравнению с контрольной группой (n = 59450) [19]. Авторами показано, что применение АС связано с повышенным риском острого инфаркта миокарда, чрескожного коронарного вмешательства или аортокоронарного шунтирования, венозной тромбоэмболии, аритмии, кардиомиопатии и сердечной недостаточности.
Несмотря на имеющиеся доказательства связи АС с неблагоприятными сердечно-сосудистыми исходами, распространённость кардиомиопатии, вызванной АС, остаётся неизвестной. Это обусловлено с одной стороны сложностью диагностики этого состояния, поскольку оно может не иметь чётких клинических проявлений и протекать ма-лосимптомно, а с другой — трудностью получения данных о применении АС, поскольку пациенты зачастую скрывают этот факт или дают неполную информацию о продолжительности приёма и дозах используемых препаратов [20]. В настоящее время в литературе встречаются в основном описания отдельных клинических случаев повреждения сердечно-сосудистой системы при применении АС [21, 22].
В метаанализе 2025 года обобщены результаты 29 исследований, в ходе которых были изучены 32 клинических случая применения АС — преимущественно мужчины (n = 31) в возрасте от 22 до 73 лет (средний возраст 38,3 года) [23]. Наиболее частым симптомом среди пациентов была одышка, также были выявлены отёки нижних конечностей, ортопноэ и учащенное сердцебие- ние. Тахикардия была наиболее частым физикальным проявлением (56,3%), синусовая тахикардия — наиболее частой ЭКГ-находкой. У четверых обследованных выявлена фибрилляция предсердий, также были зарегистрированы эпизоды предсердной и желудочковой тахикардии. Рентгенография грудной клетки выявила кардиомегалию в 15 случаях, у 8 пациентов были отмечены признаки застоя в лёгких и двусторонний плевральный выпот. ЭхоКГ в большинстве случаев продемонстрировала диффузную гипокинезию и дилатацию левого желудочка, при этом фракция выброса левого желудочка определялась в диапазоне от менее 10% до 45%. Тяжёлая митральная регургитация была выявлена у шести пациентов, трикуспидальная регургитация — в двух случаях. У 11 пациентов была проведена коронарография, которая выявила нормальные коронарные артерии, что позволяет расценивать клинические проявления именно как признак АС-индуцированной кардиомиопатии [23]. Следует отметить, что в литературе описаны также и противоположные изменения коронарных артерий у лиц, получающих АС, — применение нефизиологических доз ассоциировано с ускоренным развитием коронарного атеросклероза. Потенциальным механизмом развития ишемии миокарда, связанной с применением АС, также является полицитемия и увеличение образования тромбоксана А2 и снижение синтеза простациклина [20]. Применение АС предположительно связано с развитием дислипидемии, проявляющейся снижением концентрации липопротеинов высокой плотности и увеличением концентрации липопротеинов низкой плотности, что также может способствовать прогрессированию коронарного атеросклероза [19, 24, 25]. Таким образом, нерациональное использование АС создаёт условия для развития нежелательных эффектов их применения со стороны сердечно-сосудистой системы, которые могут проявляться самой разнообразной патологией.
КЛИНИЧЕСКИЙ СЛУЧАЙ ПАЦИЕНТАС ГИПОГОНАДИЗМОМ
На плановый профосмотр явился мужчина 47 лет, жалоб при осмотре не предъявляет. Работает инженером; не курит; отягощённую наслед- ственность по сердечно-сосудистой и эндокринной патологии отрицает; имеет двух детей школьного возраста; с детства отмечает избыточную массу тела, с периода пубертата диагностировалась гинекомастия, по поводу которой проведено оперативное лечение. Объективно состояние удовлетворительное, питание избыточное. Рост 179 см, масса тела 135 кг, ИМТ 41 кг/м2. Пульс симметричный, ритмичный, ЧСС 67 в мин., АД — 140/90 мм рт. ст. Живот увеличен за счёт подкожной жировой клетчатки, печень не увеличена. Окружность талии 133 см, окружность бёдер 123 см, индекс талия/ бедра 1,08.
С 2017 г. знает о гиперхолестеринемии: общий холестерин (ОХ) до 16,3 ммоль/л. Тогда же был выявлен первичный гипогонадизм: значительно
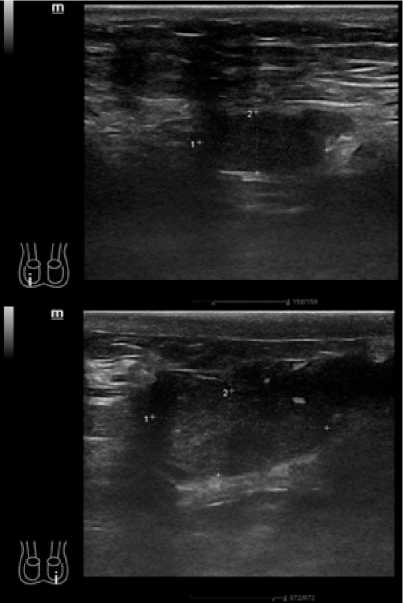
Рисунок 1. УЗИ яичек мужчины с гипогонадизмом — уменьшение обеих тестикул
Figure 1. Testicular ultrasound of a man with hypogonadism—reduction in size of both testicles
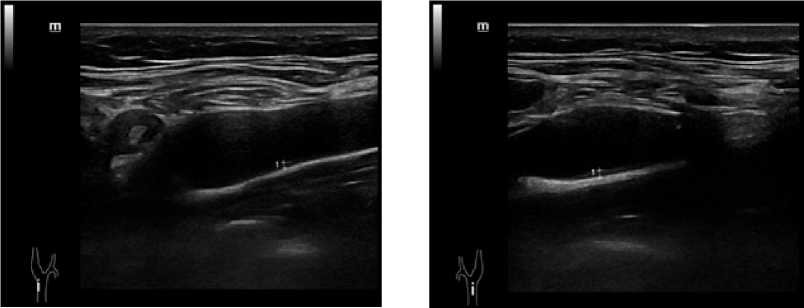
Рисунок 2. УЗДГ брахиоцефальных сосудов — отсутствие признаков атеросклеротического поражения сонных артерий
Figure 2. Doppler ultrasound of the brachiocephalic vessels—no signs of atherosclerotic lesions in the carotid arteries
снижен уровень тестостерона крови, уровень эстрадиола — на нижней границе нормы, в 3,5 раза повышен уровень фолликулостимулирующего гормона (ФСГ), несколько повышен лютеинизирующий гормон (ЛГ), пролактин — на верхней границе нормы (табл. 1). Для оценки состояния половых желёз выполнено УЗИ, согласно заключению — оба яичка в мошонке, отмечается гипоплазия обоих яичек: правое 1,5 × 0,8 см, левое 2,1 × 1,1 см (рис. 1). Выявлена также пограничная гипергликемия натощак (6,31 ммоль/л), при нормальном уровне гликированного гемоглобина (5,6%). На УЗДГ брахиоцефальных и бедренных артерий признаков атеросклеротического поражения не выявлено, толщина КИМ в пределах нормы — до 0,9 мм (рис. 2). Риск по шкале SCORE2 — 15%.
По результатам обследования назначена терапия: «Омнадрен» по 250 мг 1 раз в две недели, фе-нофибрат, розувастатин. На фоне терапии отмечена положительная лабораторная динамика в виде
Таблица 1 / Table 1
Исходный уровень половых гормонов пациента с гипогонадизмом /
Baseline levels of sex hormones in a patient with hypogonadism
|
Гормон / Hormone |
Уровень до начала заместительной гормональной терапии (2017) / Level before the start of hormone replacement therapy (2017) |
|
ЛГ, мМе/мл (0,57–12,07) LH, mIU/mL (0.57–12.07) |
13,47 |
|
ФСГ, мМе/мл (1,5–12,4) FSH, mIU/mL (1.5–12.4) |
42,23 |
|
Пролактин, мМЕ/л (72,66–407,4) Prolactin, mIU/L (72.66–407.4) |
401,28 |
|
Эстрадиол, нг/мл (11–44) Estradiol, ng/mL (11–44) |
11 |
|
Тестостерон, нг/мл (2,4–8,7) Testosterone, ng/mL (2.4–8.7) |
1,36 |
Таблица 2 / Table 2
Динамика липидного спектра, уровня глюкозы и тестостерона у пациента с гипогонадизмом Dynamics of the lipid profile, glucose, and testosterone levels in a patient with hypogonadism
|
Показатель |
2017 |
2018 |
2019 |
2022 |
2024 |
2025 |
|
Тестостерон, нг/мл (2,4–8,7) |
1,36 |
2,34 |
3,01 |
1,0 |
0,228 |
1,08 |
|
Testosterone, ng/mL (2.4–8.7) |
||||||
|
ОХ, ммоль/л (3,91–6,94) |
16,3 |
11,3 |
3,97 |
5,18 |
7,8 |
11,8 |
|
Total cholesterol, mmol/L (3.91–6.94) |
||||||
|
ТГ, ммоль/л (0,62–3,61) |
13,38 |
13,43 |
1,77 |
5,41 |
10,6 |
16,8 |
|
Triglycerides, mmol/L (0.62–3.61) |
||||||
|
ЛПНП, ммоль/л (2,25–4,82) |
9,11 |
4,34 |
2,12 |
2,54 |
3,9 |
5,4 |
|
LDL, mmol/L (2.25–4.82) |
||||||
|
ЛПОНП, ммоль/л (0,26–1,04), |
6,14 |
6,16 |
0,81 |
1,48 |
4,8 |
7,7 |
|
VLDL, mmol/L (0.26–1.04) |
||||||
|
ЛПВП, ммоль/л (0,7–1,73) |
1,11 |
0,8 |
1,04 |
0,86 |
0,87 |
1,7 |
|
HDL, mmol/L (0.7–1.73) |
||||||
|
Глюкоза натощак, ммоль/л (3,4–6,1) |
6,31 |
не определялась / not measured |
7,8 |
4,73 |
6,8 |
не определялась / not measured |
|
Fasting glucose, mmol/L (3.4–6.1) |
Примечание: / Note:
2017 — До терапии / Before therapy
2018 — Инициация ГЗТ и гиполипидемической терапии / Initiation of TRT and lipid-lowering therapy
2019 — Регулярная ГЗТ и гиполипидемическая терапия / On regular TRT and lipid-lowering therapy
2022 — Нерегулярная ГЗТ + гиполипидемическая терапия / On lipid-lowering therapy and irregular TRT
2024 — Отмена ГЗТ, гиполипидемическая терапия* / On lipid-lowering therapy only, after TRT withdrawal*
2025 — Отмена ГЗТ, гиполипидемическая терапия* / On lipid-lowering therapy only, after TRT withdrawal*
* розувастатин 40 мг + эзетимиб 10 мг. ГЗТ — гормонозаместительная терапия, ОХ — общий холестерин, ТГ — триглицериды, ЛПНП — липопротеиды низкой плотности, ЛПОНП — липопротеиды очень низкой плотности, ЛПВП — липопротеиды высокой плотности.
* rosuvastatin 40 mg + ezetimibe 10 mg. TRT – testosterone replacement therapy, TC – total cholesterol, TG – triglycerides, LDL – low-density lipoproteins, VLDL – very-low-density lipoproteins, HDL – high-density lipoproteins.
снижения уровня общего холестерина, тенденция к повышению тестостерона. Затем несколько лет в связи с длительными командировками «Омнад-рен» вводил нерегулярно, но приём гиполипиде-мических препаратов не прекращал. Несмотря на приём статинов, отмечается рост уровня липидов при сохранении выраженного андрогенного дефицита (табл. 2). На момент визита получал метформин 1000 мг в сутки, розувастатин 40 мг + эзетимиб 10 мг в сутки, инъекции препарата тестостерона прекратил.
Несмотря на значительные изменения лабораторных показателей и отсутствие эффекта от гипо-липидемической терапии, пациент считает себя практически здоровым, в связи с чем нацеленности на повышение приверженности терапии у мужчины нет.
КЛИНИЧЕСКИЙ СЛУЧАЙ ПАЦИЕНТА
С РАЗВИТИЕМ КАРДИОМИОПАТИИ ВСЛЕДСТВИЕ ДЛИТЕЛЬНОГО ПРИМЕНЕНИЯ АНАБОЛИЧЕСКИХ СТЕРОИДОВ
Мужчина 38 лет, поступил в кардиологическое отделение городского стационара с жалобами на боль в области сердца, ощущение сердцебиения и перебоев в работе сердца, повышение АД до 150/80 мм рт. ст. в течение 2 дней.
Из анамнеза: ранее считал себя здоровым; занимался фитнесом много лет, избыточной массы тела не было никогда, имеет двух детей дошкольного возраста. Актёр, блогер. Последние 2 года интенсивно занимался пауэрлифтингом (5 раз в неделю) и, по рекомендации спортивного тренера, получал в/м тестостерон («Сустанон») 500 мг и нандроло-на фенилпропионат; кроме того, в больших дозах принимал аминокислоты, витамины группы B и D, предпочитал высокоуглеводную диету для набора массы тела.
В 2024 г. в связи с жалобами на периодические сердцебиения выполнено холтеровское мониторирование (ХМ) ЭКГ: выявлена желудочковая экстрасистолия 5-й градации по Ryan, эпизоды неустойчивых пароксизмов желудочковой тахикардии.
На ЭКГ — выраженное отклонение электрической оси влево, блокада передне-верхнего разветвления левой ножки пучка Гиса, признаки увеличения правого желудочка (рис. 3).
При поступлении на ЭКГ пароксизм трепетания предсердий с нерегулярным проведением с частотой желудочковых сокращений 160 в 1 мин. При ХМ ЭКГ — выраженная тахикардия в течение всего времени наблюдения за счёт трепетания предсердий с АВ-проведением 2:1 (ЧСС днём средняя 114, мин. 89, макс. 181 в 1 минуту; ЧСС ночью средняя 94, мин. 90, макс. 137 в 1 минуту) (рис. 4, 5); циркадный индекс в пределах нормы (121%). На фоне трепетания предсердий регистрируется полиморфная желудочковая эктопическая активность (рис. 6–8), длительные паузы за счёт замедления АВ-проведения (рис. 9); удлинения QT-интервала не зарегистрировано.
При проведении эхокардиографии (ЭхоКГ): аорта на уровне синусов Вальсальвы 32 мм, восходящая аорта 30 мм; левое предсердие 34 мм; левый желудочек: КДР 49 мм, КСР 40 мм, КДО 133 мл, КСО 73 мл, МЖП 12 мм, ЗС 10 мм, ФВ по Симпсону 45% (оценена на фоне тахисистолии); локальная сократимость не нарушена; правый желудочек не расширен (в 4-камерной позиции 32 мм), правое
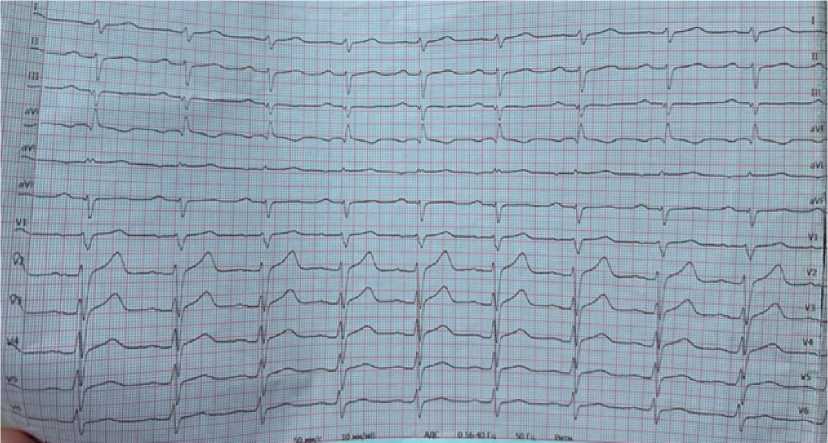
Рисунок 3. ЭКГ пациента, снятая в 2024 году
Figure 3. Patient’s ECG recorded in 2024
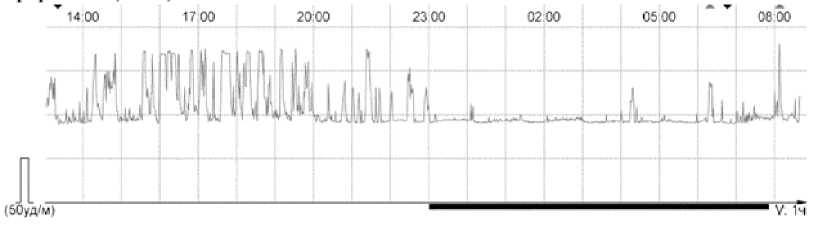
Рисунок 4. Фрагмент ХМ. График ЧСС (оценка за 1 мин.)
Figure 4. Fragment of Holter monitoring. Heart rate graph (per-minute assessment)
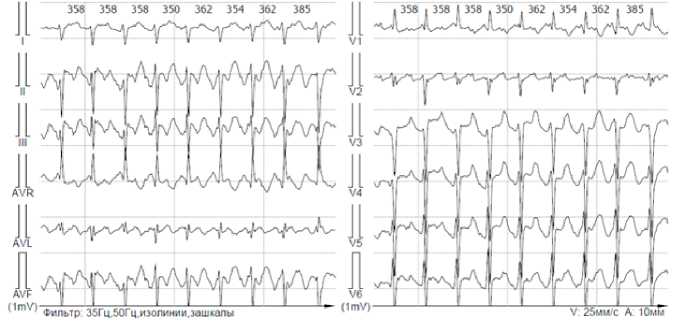
Рисунок 5. Фрагмент ХМ. Трепетание предсердий 2:1
Figure 5. Fragment of Holter monitoring. Atrial flutter 2:1
а^фгй|^й₽^^
(Я>ий “1~“ * * '“
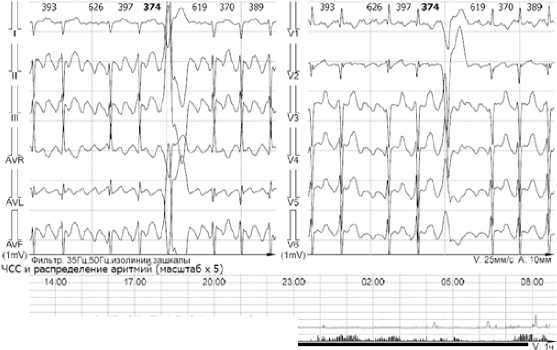
Рисунок 6. Фрагмент ХМ. Одиночная желудочковая экстрасистолия 1-го типа на фоне трепетания предсердий, всего 1257 (63 в час), днём: 279 (25 в час), ночью: 978 (111 в час)
Figure 6. Fragment of Holter monitoring. Single type 1 ventricular extrasystole against the background of atrial flutter, total: 1257 (63 per hour), daytime: 279 (25 per hour), nighttime: 978 (111 per hour)
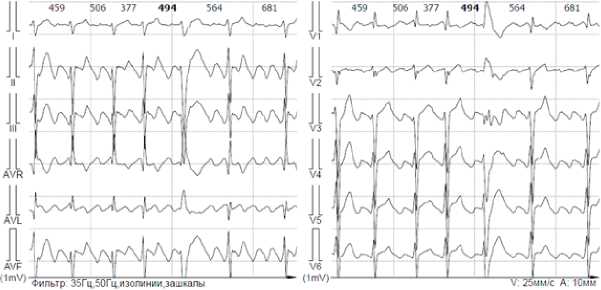
Рисунок 7. Фрагмент ХМ. Одиночная желудочковая экстрасистолия 2-го типа на фоне трепетания предсердий, всего: 10 (1 в час), днём: 8 (1 в час). ночью: 2 (менее 1 в час)
Figure 7. Fragment of Holter monitoring. Single type 2 ventricular extrasystole against the background of atrial flutter, total: 10 (1 per hour), daytime: 8 (1 per hour), nighttime: 2 (less than 1 per hour)
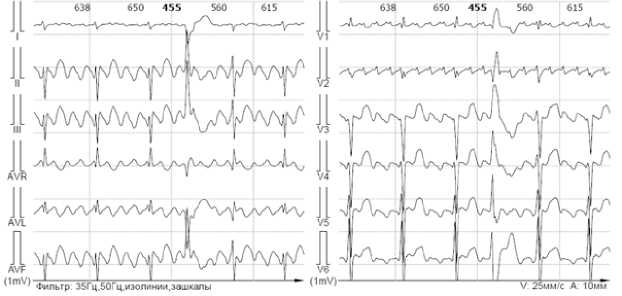
Рисунок 8. Фрагмент ХМ. Одиночная желудочковая экстрасистолия 3-го типа на фоне трепетания предсердий, всего: 1, днем: 1
Figure 8. Fragment of Holter monitoring. Single type 3 ventricular extrasystole against the background of atrial flutter, total: 1, daytime: 1

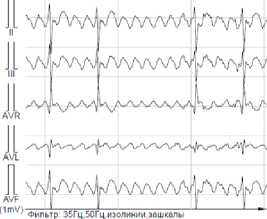
Рисунок 9. Фрагмент ХМ. Длительные паузы на фоне трепетания предсердий
Figure 9. Fragment of Holter monitoring. Prolonged pauses against the background of atrial flutter
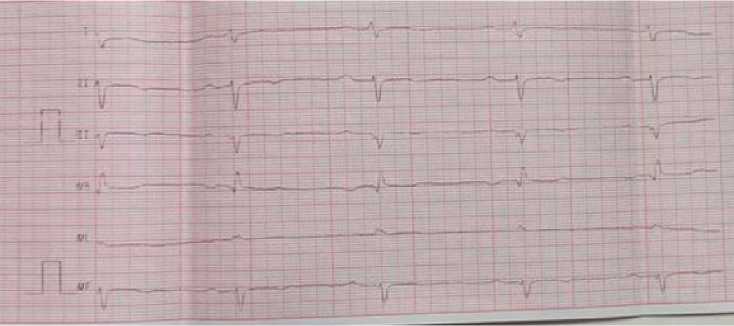
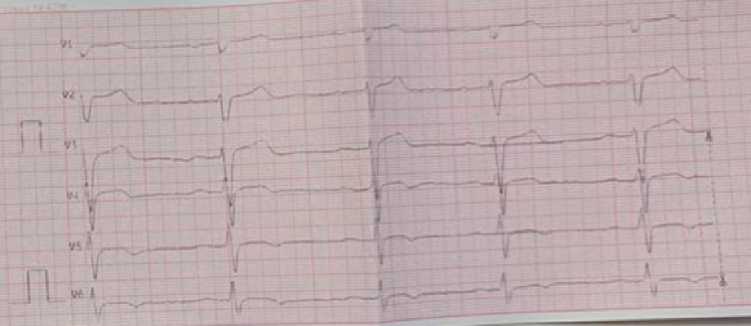
Рисунок 10. ЭКГ пациента с восстановленным синусовым ритмом (2025 г.) Figure 10. Patient’s ECG with restored sinus rhythm (2025)
предсердие не расширено (объем 56 мл); лёгочная артерия не расширена (22 мм), расчётное давление в лёгочной артерии 23 мм рт. ст.; изменений со стороны клапанного аппарата не выявлено. Выполнена чреспищеводная ЭхоКГ — в полости левого предсердия отмечается эффект спонтанного контрастирования, в полости ушка лоцируется гиперэхогенное включение без УЗ-признаков флотации, размером 6 мм; прокрашивание в режиме цветного допплеровского картирования ушка неполное.
Лабораторно в клиническом анализе крови выявлен абсолютный эритроцитоз 7,44 × 1012/л и гипергемоглобинемия до 204 г/л. В биохимическом анализе — повышение уровня общего холестерина до 5,59 ммоль/л, ЛПВП 0,69 ммоль/л, ЛПНП 3,8 ммоль/л, ЛПОНП 1,1 ммоль/л, триглице- ридов 2,43 ммоль/л, при этом кардиоспецифичные маркеры (тропонин, КФК-МВ, трансаминазы) без виража. Выписан с трепетанием предсердий, нор-мосистолией (ЧСС 88 в мин.), с рекомендациями приёма ривароксабана, бисопролола, комбинаций периндоприла с индапамидом и розувастатина с эзетимибом.
Через 10 дней на контрольной ЭКГ: восстановление (спонтанное) синусового ритма с ЧСС 67 в мин., блокада передне-верхнего разветвления левой ножки пучка Гиса (те же изменения были в 2024 году), появились нарушения процессов реполяризации (рис. 10). Чреспищеводная ЭхоКГ в динамике — тромб не лоцируется, прокрашивание в режиме цветного допплеровского картирования ушка полное.
Пациент несколько снизил интенсивность физических нагрузок, однако продолжает вводить тестостерон в/м, спустя 3 месяца после госпитализации чувствует себя хорошо.
ОБСУЖДЕНИЕ
Первичный гипогонадизм у представленного мужчины среднего возраста существует, вероятно, в течение всей жизни. Особенностью случая является сохранение репродуктивной функции с возможностью зачатия двух детей. Основным проявлением гипогонадизма является тяжёлая дислипидемия, не корригируемая приёмом интенсивной гиполипидемической терапии. Улучшение и нормализацию липидограммы удалось достичь только при адекватной гормонзаместительной терапии, после прекращении которой уровень общего холестерина вновь превышает норму в 2 раза. В то же время изменений сосудов, характерных для атеросклеротического их поражения, у пациента в настоящее время не обнаружено. Пациенту показана длительная заместительная терапия препаратами тестостерона, с контролем уровня гормонов, липидов, гликированного гемоглобина. При отсутствии эффективной гиполипидемической терапии и отказе пациента от гормонотерапии прогноз серьёзный.
Второй случай представляет развитие комплекса нежелательных эффектов у изначально здорового мужчины молодого возраста с бесконтрольным и немотивированным с клинической точки зрения применением анаболических стероидов с целью увеличения скелетной мышечной массы. Неполные два года введения препаратов тестостерона привели к развитию изменений периферической крови, изменению липидного статуса и кардиомиопатии, проявляющейся полиморфной желудочковой экстрасистолией и трепетанием предсердий, осложнённым образованием внутрисердечного тромба. Кроме того, создаётся реальная угроза сохранению репродуктивной функции — вполне вероятна атрофия яичек и снижение эндогенного синтеза тестостерона. Можно ожидать, что отмена АС у такого пациента может привести к снижению сердечно-сосудистого риска, однако пациент воспринимает себя практически здоровым и прекращать введение препарата тестостерона не намерен. Кроме того, в силу своей профессиональной деятельности (актёр и блогер) пациент формирует сомнительное представление о здоровье и цели физических тренировок не только у себя, но и у своих возможных последователей. Таким образом, проблема имеет не только медицинские, но и социальные последствия.
ЗАКЛЮЧЕНИЕ
Известно, что роль половых гормонов не сводится только к сохранению репродуктивной функции мужчины, а проявляется во влиянии на все виды обмена — жировой, углеводный, белковый. Длительно существующий низкий, как и высокий уровень тестостерона оказывает патологическое влияние на здоровье мужчины в целом, вызывая ряд изменений со стороны различных органов и систем, обратимость которых в настоящее время не доказана. В качестве иллюстрации приведено два клинических случая, показывающих роль эндогенного дефицита половых гормонов и их экзогенного избытка в развитии функциональных и структурных изменений со стороны сердечнососудистой системы. Несмотря на полярность гормонального статуса и существенные различия фенотипов у обоих пациентов формируются в чем-то схожие лабораторные изменения липидного статуса, повышающие риск сердечно-сосудистых катастроф, развития ишемической болезни сердца, цереброваскулярной патологии, а также риск снижения качества жизни, в том числе угнетение половой функции и либидо.
Финансирование: Авторы заявляют об отсутствии финансирования.


