Синтез 1,3,5-триазинтионов(онов) и возможность их практического применения
Автор: Головина А.В., Рыбакова А.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 1 т.18, 2026 года.
Бесплатный доступ
Настоящий обзор посвящён различным производным 1,3,5триазинонов и 1,3,5триазинтионов. Наиболее полно рассмотрены вопросы синтетических подходов к синтезу симмтриазинонов(тионов) и их O(S)производных, а также возможности их практического приме нения. В настоящее время 1,3,5триазиноны(тионы) и их производные находят широкое применение в различных областях: в сельском хозяйстве, промышленности, фармацевтическом производстве, в органическом синтезе, а также в производстве высокопористых ковалентных триазиновых каркасов с различными свойствами. В связи с высоким интересом к данным гетероциклическим системам, обусловленным высокой биологической активностью и широким применением соединений с 1,3,5 триазиновым каркасом, нами проведён поиск, анализ и систематизация имеющихся литературных данных с 1952 по 2025 год, в том числе патентных документов.
1, 3, 5-триазин-оны, 1, 3, 5-триазин-тионы, 2, 4, 6-тризамещённые-1, 3, 5-триазины, мочевина, тиомочевина, гуанидины, амидины
Короткий адрес: https://sciup.org/147253375
IDR: 147253375 | УДК: 547.874.1+ 547.874.15 | DOI: 10.14529/chem260109
Synthesis of 1,3,5-triazinethiones(ones) and their potential for practical application
The present review deals with various derivatives of 1,3,5-triazinones and 1,3,5- triazinethiones. The review provides comprehensive discussion of synthetic approaches to the synthesis of s-triazinones(thiones) and their O-(S-)derivatives, as well as the potential for their practical application. Currently, 1,3,5-triazinones(thiones) and their derivatives are widely used in various fields: agriculture, industry, pharmaceutical production, organic synthesis, and production of highly porous covalent triazine frameworks with various properties. Due to the strong interest in these heterocyclic systems, driven by their high biological activity and widespread use of compounds with the 1,3,5-triazine framework, we have searched, analyzed, and systematized available literature sources from 1952 to 2025, including patent documents.
Текст научной статьи Синтез 1,3,5-триазинтионов(онов) и возможность их практического применения
-
1,3,5- Триазины ( симм -триазины или симметричные триазины) наиболее хорошо изучены, их первые представители были получены и описаны ещё в первой половине XIX века: так, в 1829 г. Фридрих Вёлер пиролизом мочевины синтезировал циануровую кислоту (1,3,5-тригидрокси- симм -триазин).
Симм -Триазины с одной или несколькими оксо- или тио-группами у атомов углерода представляют собой симм -триазиноны и симм - триазинтионы соответственно.
Многие производные симм -триазинона(тиона) нашли применение в качестве гербицидов и пестицидов. В частности гексазинон (3-циклогексил-6-(диметиламино)-1-метил-1,3,5-триазин-2,4(1 Н ,3 Н )-дион, рис. 1) и прочие его аналоги-гербициды являются крупнотоннажными продуктами, производимыми на предприятиях и используемыми в сельском хозяйстве в ряде стран. При этом данный гербицид был подробно исследован на изменение его концентрации в почве, воде и тканях растений. Так, после его внесения осуществляли контроль за скоростью его рассеивания и выщелачивания из почвы на меньшую глубину [1]. Известно, что риск загрязнения грунтовых вод в результате быстрого выщелачивания высокорастворимых пестицидов можно минимизировать путем применения пестицида, адсорбированного на матрице или носителе, что ограничивает количество пестицида, немедленно доступного для нежелательных потерь. Аналогичный подход к адсорбации был применен и для гексазинона [2].
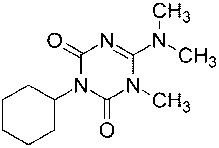
Гексазинон
Рис. 1. Гербициды 1,3,5-триазинового ряда
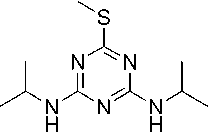
Прометрин
Широкое использование симм -триазинов в качестве пестицидов началось ещё с середины 1950-х годов. Один из производных 1,3,5-триазинтиона – прометрин (6-метилсульфанил-2-N,4-N-ди(пропан-2-ил)-1,3,5-триазин-2,4-диамин, см. рис. 1) – начали применять в 1964 г. в США. В настоящее время работы по поиску аналогичных по строению, но более эффективных и селективных пестицидов, фунгицидов, инсектицидов и гербицидов по прежнему ведутся.
Некоторые 1,3,5-триазиноны также важны в качестве фармацевтических препаратов и заявлены в качестве антибактериальных и противоопухолевых агентов. Примером последнего могут служить 5-азацитидин (международное непатентованное название) или 4-амино-1- β -D-рибофуранозил-1,3,5-триазин-2(1 H )-он (рис. 2) и его 2'(3')-фторсодержащие аналоги [3].
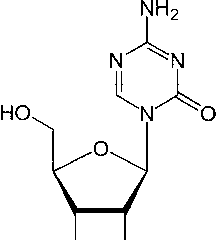
он он
Рис. 2. Структура 5-азацитидина (4-амино-1-β-D-рибофуранозил-1,3,5-триазин-2(1 H )-она)
Кроме того, соединения, содержащие в своей структуре скелет 3,4-дигидро-1,3,5-триазин-2(1 H )-она, продемонстрировали интересные свойства в предварительном исследовании на нейропротектор-ную и нейрогенную активность и отсутствие нейротоксичности в клеточных анализах [4].
Важным стоматологическим материалом является 6-(N-(4-винилбензил)пропиламино)-1,3,5-триазин-2,4-дитион (рис. 3), применяемым в качестве адгезивного мономера [5–8]. Представленные в работах [5, 6] результаты приводят к выводу, что для данного мономера существуют некоторые специфические взаимодействия между его атомами серы и поверхностью Au с образованием химических связей, которые эффективны для улучшения прочности связи между драгоценными металлами для зубов и смолой.
Толтразурил (1-метил-3-[3-метил-4-[4-(трифторметилсульфанил)фенокси]фенил]-1,3,5-триазин-2,4,6-трион, рис. 4) – ветеринарный препарат, используемый при борьбе с патологиями, вызываемыми простейшими паразитами [9, 10].
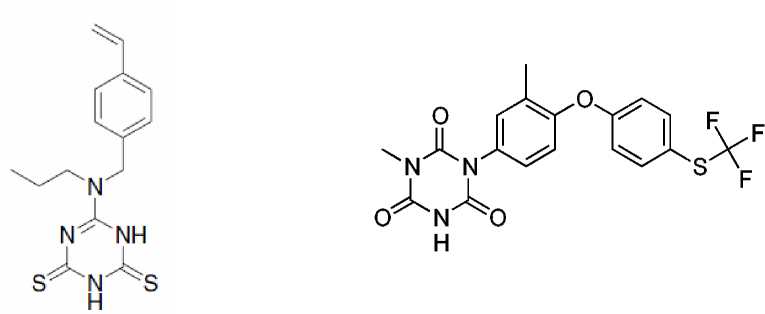
Рис. 3. Структура 6-(N-(4-винилбензил)пропиламино)- Рис. 4. Структура толтразурила (1-метил-3-[3-метил-4-
1,3,5-триазин-2,4-дитиона [4-(трифторметилсульфанил)фенокси]фенил]-1,3,5- триазин-2,4,6-триона)
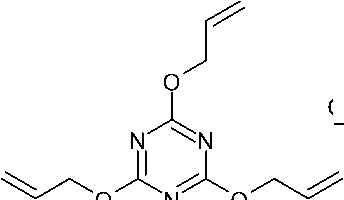
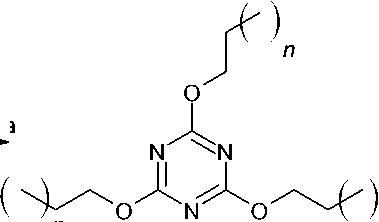
Стоит отметить и способность производных s -триазинонов(тионов) к полимеризации, некоторые стратегии синтеза C3-симметричных полимерных материалов, содержащих триазиновые ядра, и их биомедицинское применение отражены в обзоре [11]. Новый функционализированный мезопористый полимер был синтезирован посредством радикальной полимеризации 2,4,6-триаллилокси-1,3,5-триазина (ТАТ) в водной среде в присутствии анионного поверхностноактивного вещества (додецилсульфата натрия) [12] (схема 1).
HCI
(NH4)2S2O8/
CH,(CH2)11OSO,Na
n
Схема 1. Полимеризация 2,4,6-триаллилокси-1,3,5-триазина
Получаемые на основе 1,3,5-триазина полимеры находят широкое применение в химии. Например, при использовании двухстадийного гидротермального метода и тритиоциануровой кислоты (TTCA), 2,4,6-тригидразино-1,3,5-триазина (THT) и Fe 3 O 4 в качестве исходных материалов, был синтезирован сферический магнитный адсорбционный полимер (TTCA/THT@Fe 3 O 4 ) (рис. 5) для эффективного удаления Cr(VI) из сточных вод. В оптимальных условиях адсорбции максимальная адсорбционная емкость TTCA/THT@Fe 3 O 4 по Cr(VI) может достигать 1340 мг·г-1 . Примечательно, что эффективность удаления может приближаться к 98,9 % даже при более низкой концентрации 20 мг·л-1 Cr(VI). Для реальных сточных вод, содержащих Cr(VI), концентрация Cr(VI) была снижена с 25,8 до 0,4 мг·л-1, что на 20 % ниже действующего стандарта сброса в промышленность [13].
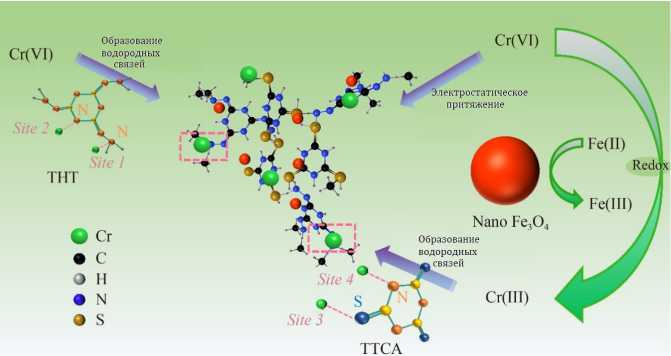
Рис. 5. Полимер TTCA/THT@Fe 3 O 4
Также производные симм -триазина, содержащие в своей структуре полимерные звенья могут быть использованы в качестве скавенджера (вещество, добавляемое в смесь для удаления или дезактивации примесей и нежелательных продуктов реакции). Одним их таких примеров является полиэтиленгликоль-дихлортриазин (PEG-DCT), который использовался в качестве растворимого электрофильного поглотителя. Он был получен по реакции MeO-PEG-OH (Mw = 5000) с 5 эквивалентами 2,4,6-трихлор-1,3,5-триазина в хлороформе в присутствии N,N-диизопропилэтиламина (DIPEA). PEG-DCT добавляли в конце реакции для полного удаления нуклеофильных реагентов или побочных продуктов. Растворимый полимер связывал спирты, тиолы, трифенилфосфин и трифенилфосфиноксид (схема 2) [14].
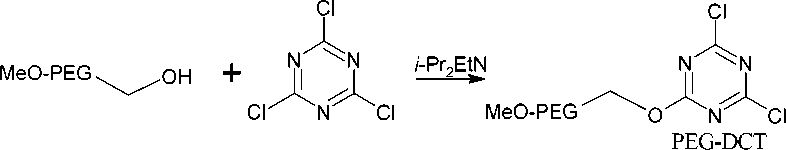
Схема 2. Получение полиэтиленгликоль-дихлортриазина
Пористые углеродные композиты с привитыми дисульфидными полимерами выступают в качестве сорбентов для удаления тяжелых металлов из ливневых стоков. Процессы модификации поверхности проводились в четыре этапа: окисление гранулированного активированного углерода (ГАУ, GAC), ацилхлорирование, присоединение линейного тиола и прививка дисульфидной связи полимера к поверхности подложки. Последний этап осуществляли действием сильного окислителя, содержащего избыточное количество йода и йодида калия, на смесь обработанного цистеамином ГАУ в 150 мл раствора гидроксида натрия с 3 ммоль тритиоциануровой кислоты, в следствие чего был получен поверхностно-модифицированный композит (DiS-AC) (схема 3). Характеристика материала показала, что полимер был успешно привит и выращен на поверхности углеродного субстрата. Коэффициент распределения связывания Cd2+ составил 89·103 л/кг при концентрации раствора 0,35 мг/л, что заметно выше, чем сродство к сорбции Cd2+, наблюдаемое у обычных сорбентов [15].
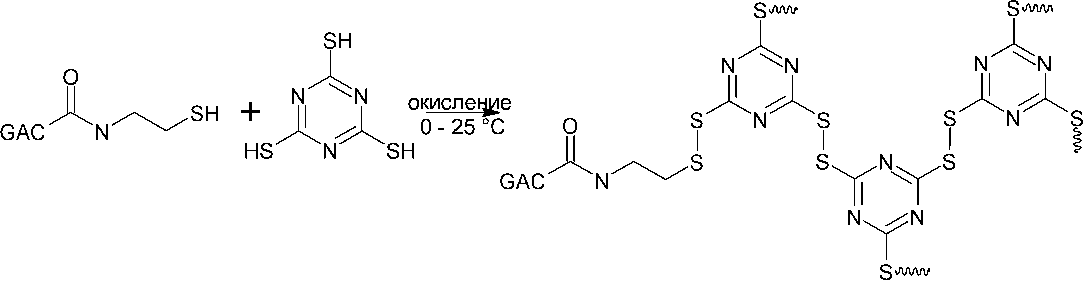
DiS-AC
Схема 3. Синтез сорбентов для удаления тяжелых металлов из ливневых стоков
Предложены и сконструированы ковалентные триазиновые каркасы с тритиоциануровой кислотой (TTC-CTF) для эффективного извлечения драгоценных металлов (рис. 6). Как и ожидалось, предлагаемые TTC-CTF обеспечивают сверхвысокую поглощающую способность 3365 мг/г для Au(III) и 1125 мг/г для Pt(IV) при облучении светом. Важно отметить, что TTC-CTF также способны избирательно и эффективно извлекать золото из продуктов выщелачивания вычислительного блока, обеспечивая эффективность извлечения 99 % [16].
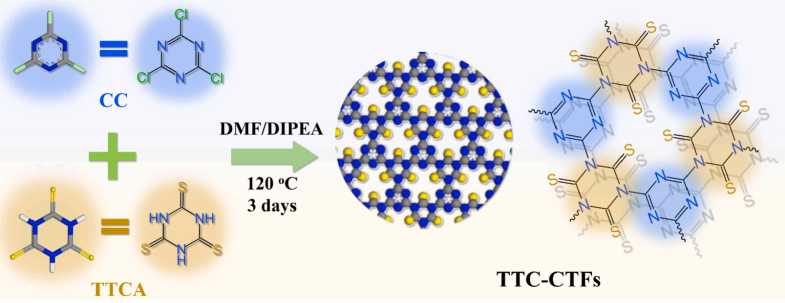
Рис. 6. КТК для извлечения драгоценных металлов из электронных отходов [16]
Таким образом, различные производные 1,3,5-триазинонов и 1,3,5-триазинтионов нашли применение во многих различных областях – это и сельское хозяйство, и промышленность, а также фармацевтическое производство. В связи с чем интерес к их дальнейшему изучению очевидно заключается в том, что 1,3,5-триазиноны(тионы) являются перспективными компонентами для их функционализации. С точки зрения поиска последующих научно-практических решений по исследованию обсуждаемых гетероциклических систем представляется актуальным и необходимым иметь научную базу об их синтезе и свойствах.
В настоящее время нам удалось найти ряд обзорных статей, посвященных 1,3,5-триазинам. Например, 1,3,5-триазины нашли широкое применение в качестве строительных блоков для создания олигомеров, важных для супрамолекулярной химии, химической биологии и полимерной науки, что легло в основу обзора [17] «Супрамолекулярная химия монодисперсных 1,3,5-триазиновых олигомеров». Получаемые на основе симм-триазина пористые ковалентные триазиновые каркасы [18] потенциально применимы для адсорбции СО2 [19], для создания фото- и электрокатализаторов [20,21], катодных материалов для аккумуляторов, не относящихся к литий-ионным [22] и в качестве электродных материалов для суперконденсаторов [23]. Также имеются обзоры о синтезе дендримеров [24] и антипиренов [25], о достижениях в области фотокатализаторов на основе полигептазинимида/политриазинимида [26] и свойствах материалов на основе три-s-триазинов (графитоподобного нитрида углерода) [27]. Кроме того в литературе представлены синтетические и фармакологические разработки гибридного s-триазинового фрагмента [28], разработки терапевтических средств против рака молочной железы [29] и краткий обзор эффективности s-триазинов в борьбе с раком молочной железы [30]. В прочих обзорах отражены общие сведения о синтезе и применении производных имидазолов, триазинов и изатинов и доступных лекарственных препаратов на их основе [31], возможности применения 2,4,6-трихлор-1,3,5-триазинов и их производных в органическом синтезе [32]. В обзоре [33] обобщены и систематизированы опубликованные данные о нитропроизводных 1,3,5-триазинов, которые представляют особый интерес как высокоэнергетические соединения, особое внимание уделяется их взрывчатым свойствам. В другом обзоре [34] рассматриваются иммунохимические методы анализа гербицидов группы симм-1,3,5-триазинов, в том числе возможности их применения для определения симм-1,3,5-триазинов в различных объектах (вода, почва, продукты питания и др.). Более ранние обзорные статьи посвящены синтезу триалкил(арил-, гетарил)- [35], триамино-, триал-кил(арил)окси-, тригалоген-1,3,5-триазинов [36], синтезу и свойствам кремний-, германий-, олово- и свинецсодержащих симм-триазинов [37] и реакциям 1,3,5-триазинов с нуклеофилами [38]. Возможности синтеза 1,3,5-триазин-2-онов, 2,4-дионов, 2,4,6-трионов, а также 1,3,5-триазинтионов кратко представлены в работе 1996 г. [39], в обзоре 2004 года изложены основные подходы к сборке симм-триазинового цикла и его функционализации [40], однако более поздних и более подробных аналогичных обзорных статей, посвящённых способам синтеза симм-триазинонов(тионов) и возможности их практического применения, нам найти не удалось. В связи с чем систематизация имеющихся в настоящий момент литературных данных и составление на их основе аналитического обзора о синтезе и свойствах 1,3,5-триазинонов(тионов) на наш взгляд является актуальным.
1. Синтез 1,3,5-триазинонов, 1,3,5-триазинтионов и их производных
Несмотря на то, что 1,3,5-триазины являются одним из старейших известных классов органических молекул, в настоящее время существуют некоторые проблемы при их практическом получении, связанные с выделением продукта из реакционной смеси, получением побочных соединений и улучшением выхода целевого продукта.
Среди общеизвестных способов синтеза 1,3,5-триазинонов(тионов) и их производных можно выделить несколько подходов в зависимости от используемых субстратов:
-
• Синтез из галоген замещенных 1,3,5-триазинов;
-
• Синтез на основе мочевины, тиомочевины и их производных;
-
• Синтезы на основе амидинов;
-
• Синтезы на основе производных гуанидина;
-
• Синтезы на основе изо(тио)цианатов
-
• Синтезы на основе нитрилов и их производных
-
1.1. Синтез из галоген замещенных 1,3,5-триазинов
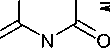
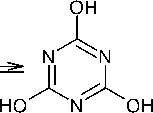
Одним из способов синтеза некоторых производных s -триазина является синтез из дешевого, легкодоступного хлорида циануровой кислоты, то есть из 2,4,6-трихлор-1,3,5-триазина ( 1 ). Последний гидролизуется водой в присутствии гидроксида натрия с получением 1,3,5-триазин-2,4,6-(1 Н ,3 Н ,5 Н )-триона ( 2 ). Кроме того, имеются данные о достаточно большом разнообразии превращений 2,4,6-трихлор-1,3,5-триазина 1 в различные 1,3,5-триазиноны(трионы) 2 и их О-производные ( 3–6) (схема 4) [41].
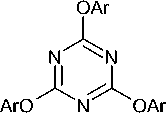
^ArOH -3HCI
Cl
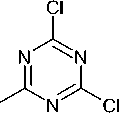
NaOH_ H2O*
O
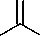
MeO
NaHCO: 35°C
Cl

NN
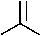

MeOH
VH2°
N OMe MeO
OMe
97% 3%
OMe
Схема 4. Получение 1,3,-триазинонов(трионов) и их О-производных
Взаимодействие хлорида циануровой кислоты 1 с фенолами приводит к образованию 2,4,6- трис (арилокси)- s -триазинов 4 (схема 5), реакция протекает в присутствии основания (Na или NaOH) в различных растворителях, таких как: ацетон, этанол, 1,4-диоксан, ДМФА/ДМСО [42].
Cl OAr
+ ЗАГОН J J
CI^N^CI -3HCI ArO^N^OAr
Схема 5. Синтез 2,4,6-трис(арилокси)-s-триазинов
Гидролиз ряда 2,4,6- трис (арилокси)- s -триазинов 4 с использованием палладия на углероде позволил наряду с 1,3,5-триазинотрионом 2 получить соответствующие арены с превосходными выходами (схема 6). При этом электронный характер заместителей не влияет на скорость гидролиза, а вот увеличение размера заместителей замедляет реакцию [43].
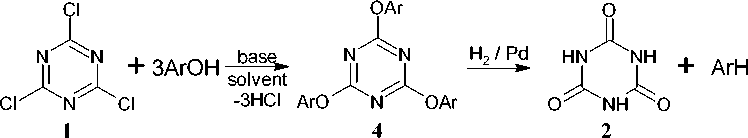
Схема 6. Получение триазинтриона и аренов
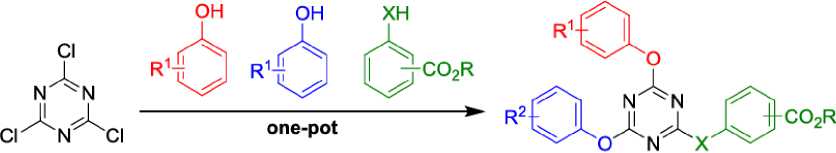
Разработан однореакторный синтез для быстрой функционализации 1,3,5-триазинового ядра без необходимости выделения промежуточных соединений. Путь начинается с легкодоступного 2,4,6-трихлор-1,3,5-триазина 1 , на первой стадии замещение атома хлора арилокси-группой протекает при пониженной температуре (–35 °С) для повышения селективности, дальнейшее последовательное замещение арилокс-, ариламино- или арилтиогруппами протекает при комнатной температуре (схема 7), что обеспечивает доступ к молекулам с тремя различными заместителями этого типа ( 7 ) с хорошими выходами [44].
1 7
R = H, Me, tert -Bu X = NH, S
Схема 7. Однореакторный синтез тризамещённых триазинов
Было показано [45], что 2-хлор-4,6-диметокси-1,3,5-триазин 5 может использоваться для активации фенольных соединений в реакции Сузуки-Мияуры для получения биарилов. В трёхэтапном синтезе исходный 2,4,6-трихлор-1,3,5-триазина 1 переводят в соединение 5 , которое затем реагирует с фенолами с образованием 2-арилокси-4,6-диметокси-1,3,5-триазина ( 8 ), строение одного из полученных соединений 8 было установлено методом РСА (рис. 7).
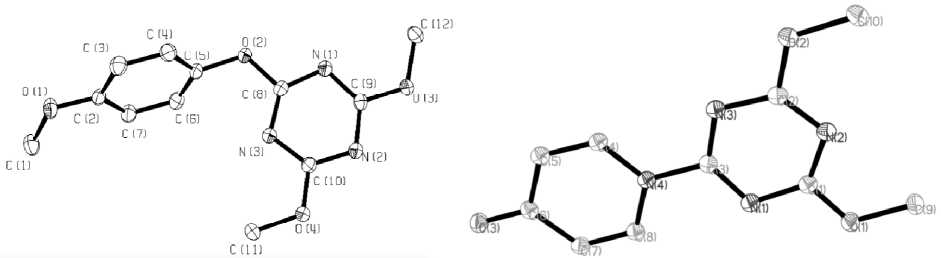
8 10
Рис. 7. Строение соединений 9 и 11 установленное методом РСА
При последующем действии арилборной кислоты в присутствии NiCl2(dppf) в качестве катализатора происходит образование биарилов, а триазиновая компонента переходит в 2-гидрокси-4,6-диметокси-1,3,5-триазин ( 9 ) (схема 8).
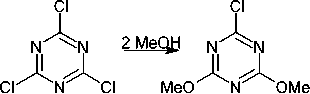
АЮЦ R[
1 5
ОМе
N^N
ArB(OH)2
О N ОМе NiCI2(dppf), К3РО4 toluene, 110 °C
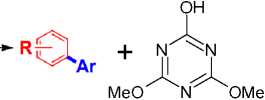
Схема 8. Реакция кросс-сочетания Сузуки – Мияура
В случае 4-гидроксипиридина реакция с 2-хлорид-4,6-диметокси-1,3,5-триазином 5 не привела к образованию соответствующего эфира 4-пиридинил-O-DMT, и был выделен неожиданный изомер – N-(4,6-диметокси-1,3,5-триазин-2-ил)-пиридин-4-он ( 10 ), структура которого была установлена методом РСА (см. рис. 7) [45].
Позднее был разработан прямой вариант реакции, в котором происходит активация сразу трёх моль производных фенола через образование 2,4,6- трис (арилокси)-1,3,5-триазина 4 [46]. Также было показано, что при использовании 1,3,5- трис ( п -толилокси)бензола ( 11 ) вместо 2,4,6- трис ( п -толилокси)-1,3,5-триазина ( 12 ) продукт не был получен (схема 9). Этот эксперимент проясняет, что орто -атом азота в структуре 1 играет важную роль в активации связи C–O [46].
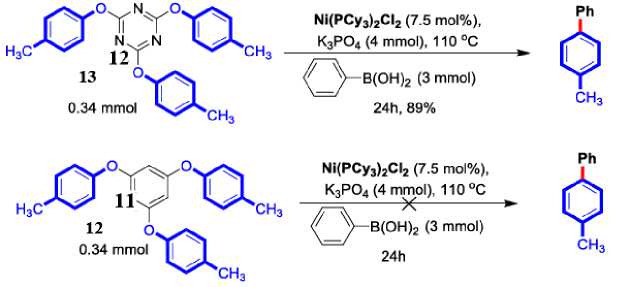
Схема 9. Прямая реакция кросс-сочетания
Схожим образом 2,4,6-Трихлор-1,3,5-триазин 1 может быть использован в качестве эффективного и мягкого реагента для прямого никель-катализируемого аминирования фенолов. В данном случае in situ генерируемый арильный электрофил C–O (Ar-O-ТХТ) реагирует с желаемым амином с образованием соответствующего ариламина (рис. 8) [47].
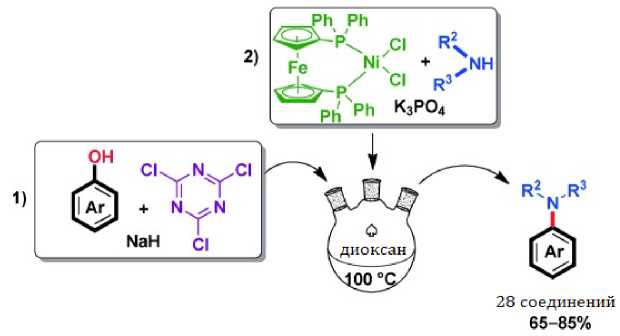
Рис. 8. Синтез ариламинов в присутствии ТСТ
Другое производное 1,3,5-триазина – 2,4,6- трис -(2,2,2-трифторэтокси)-[1,3,5]триазин (TriT-FET, 13 ), полученное из трихлортриазина – может служить эффективным фторирующим агентом (например, спиртов) превращаясь при этом в 1,3,5-триазин-2,4,6-трион 2 [48]. Данная процедура является привлекательной альтернативой для синтеза фторированных компонентов, которые содержатся в различных биологически активных молекулах. Кроме того, предложенный фторирующий агент является нетоксичным (схема 10).
Cl
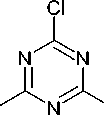
NaOH (3.5 eq) TFE^gq) 50°C, 6h
Cl F3CH2CO
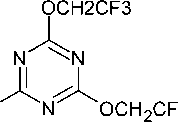
1 13, TriTFET zCH2^ zCH? TriTFET CH2 ZCH2 CH, +
H3C CH2 OH TsOH н3С 'CH2 ЯО 2'CF3 J 1
O^NH^O
Схема 10. Получение 2,4,6- трис -(2,2,2-трифторэтокси)-[1,3,5]триазена и его применение
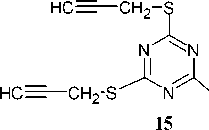
О-пропаргильные производные 1,3,5-триазин-2,4,6-триона (14) также могут быть получены по реакции трихлор-1,3,5-триазина 1 с пропаргиловым спиртом, тогда как для получения S-пропаргильных производных (15) исходят из 1,3,5-триазин-2,4,6-тритиола (16) и пропаргилбромида (схема 11) [49, 50].
X HC^^CH2-O
X = SH X _X = C1 I
ЗНС=—CH2-Br N 4N Зн с= CH2-OH N xN
-3HBr X -3HC1 __ __
S-CH,-^CH X^N^X HC^CH2-O O—CH2=CH
l:x = cl 16: X = SH 14
Схема 11. Получение О-(S-)пропаргильных производных 1,3,5-триазина
Проведение подобных превращений трихлор-1,3,5-триазина с различными спиртами и аминами может быть осуществлено и при микроволновом облучении, что способствует увеличению выходов соответствующих тризамещённых триазинов ( 17 ) (схема 12) [51].
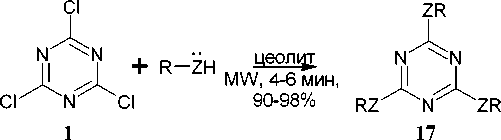
R = Ar, Alk, Ac; Z = O, NH
Схема 12. Синтез симметричных тризамещённых триазинов при MW
Последовательное замещение атомов хлора в 2,4,6-трихлор-1,3,5-триазине 1 можно осуществлять с использованием аминов, гидроксида натрия и гидразингидрата, что приводит к синтезу 4-аминозамещенных 6-гидразинил-1,3,5-триазин-2-онов ( 18 ) (схема 13) [52].
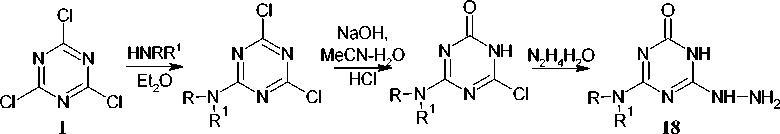
R = R1 = Alk
Схема 13. Синтез 4-аминозамещённый-6-гидразинил-1,3,5-триазин-2-она
Аналогичным образом могут быть получены 2-алкилокси-4,6-диаминозамещённые-1,3,5-триазины ( 19 ). Например, при последовательной обработке триазина 1 4-аминобензонитрилом, бензилиден тиазолидендионом и 2-(морфолин-4-ил)этанолом приводит к замещенным 4-[4-(5-бензоил-2,4-диоксотиазолидин-3-ил)-6-(2-морфолин-4-ил-этокси)-[1,3,5]триазин-2-иламино]-бен-зонитрилам 19 (схема 14) [53]. Полученные соединения 19 продемонстрировали высокую ингибирующую способность против ВИЧ, SARS-CoV-2 и бактериальных микроорганизмов.
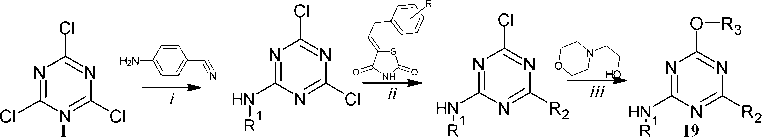
R1 =
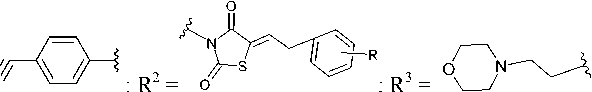
R = 2-OH, 4-OH, 4-Cl, 3-NO 2 , 4-F
Условия: i : EtOH, пиперидин; ii : Na 2 CO 3 , 45-50 T ; iii : DMF, NaOH, нагревание 65-70 °С
Схема 14. Получение 2-алкилокси-4,6-диаминозамещённые-1,3,5-триазины
Изучены реакции трихлор-1,3,5-триазина 1 с солями тринитрометана. В зависимости от условий, используемых солей тринитрометана и специальных добавок, авторами было выявлено шесть типов реакций тринитрометилирования 2,4,6-трихлор-1,3,5-триазина, в результате которых образуется и 1,3,5-триазин-2,4,6-трион 2 или, в случае третьего компонента реакции – спиртов, О-производные 1,3,5-триазин-2,4,6-триона ( 20 ) (схема 15) [54].
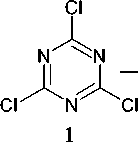
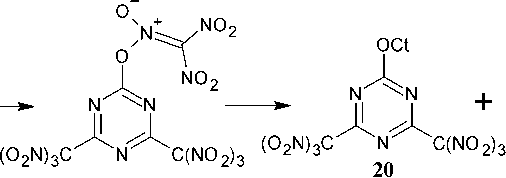
н7 7H + C(NOACI
Oz NH XO
Ct+ = K+ , Na+ , Ag+ , третичный амин, четвертичный аммоний
Схема 15. Взаимодействие трихлор-1,3,5-триазина с солями тринитрометана
Реакция ароматических карбоновых кислот с трихлортриазином (ТСТ) в присутствии N-формилпирролидина, который является мощным катализатором Льюиса, протекает через активацию карбоновых кислот посредством хлорирования (схема 16). Таким образом были синтезированы четыре различных хлорида кислоты в многограммовом масштабе и выделены после дистилляции с выходом 79–90 % [55].
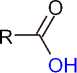
OH
TCI (40 mol %) F Pyr( 10-15 mol% )
MeCN( 3-4 M) 40-80°C, 4-5h
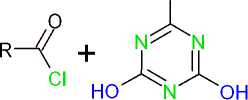
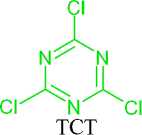
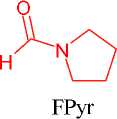
Схема 16. Синтез хлорангидридов ароматических карбоновых кислот
Разработан простой и эффективный подход к синтезу первичных амидов из ароматических
карбоновых кислот через образование 2,4,6-трихлор-1,3,5-триазина 1 (схема 17). Условия проведения реакции были оптимизированы на модельном субстрате – бензойной кислоте. Наибольших выходов (от 71 до 99 %) удалось достичь при использовании тиоцианата аммония и карбоната калия, что приводит к быстрому превращению карбоновых кислот в соответствующие амиды в течение пяти минут при измельчении при комнатной температуре [56].
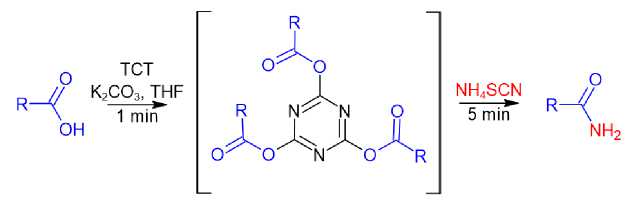
Схема 17. Синтез амидов из ароматических карбоновых кислот
Интересным способом получения 1,3,5-триазин-2,4-дионов являетя взаимодействие цианур хлорида 1 с β -дикетонами в растворе щёлочи. В зависимости от соотношения реагентов могут быть получены производные триазина, содержащие в положении 6 фрагмент β -дикетона ( 21 ) или монокетона ( 22 ). Соединения 21 переходят в 22 после их нагревания в метаноле в присутствии соляной кислоты, при этом R1 более сильный электроно-донор, чем R2 (схема 18) [57].
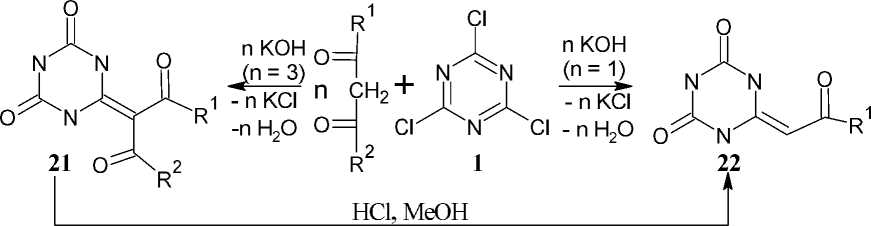
-R2COOMe
R1,R2 = Alk, OAlk
Схема 18. Взаимодействие цианурхлорида с β -дикетонами
Строение полученных соединений установлено с использованием методов ИК-, ЯМР 1Н и 13С, а также методом РСА для некоторых представителей соединений 21 и 22 (рис. 9) [57].
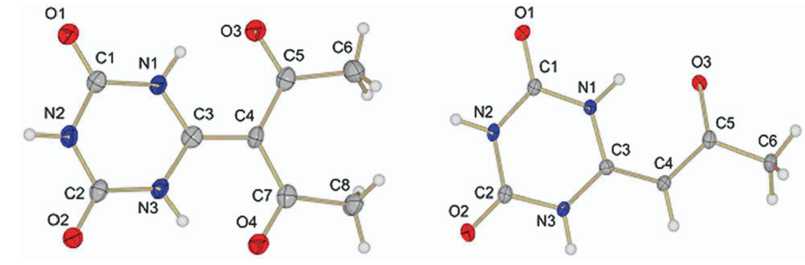
21 22
Рис. 9. Строение соединений 22 и 23, установленное методом РСА
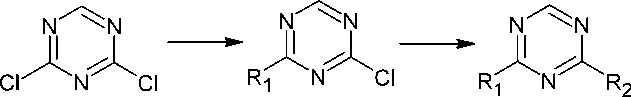
Дизамещённые триазины также могут быть получены на основе дихлортриазина ( 23 ) при его взаимодействии с аминами при пониженной температуре и гетероароматическими спиртами при умеренном нагревании, что приводит к (4-(аминозамещённым)-1,3,5-триазин-2-ил)окси-хромен-2-онам ( 24 ) [58] или (4-(аминозамещённым)-1,3,5-триазин-2-ил)окси-хромен-4-онам ( 25 ) (схема 19) [59].
23 24,25
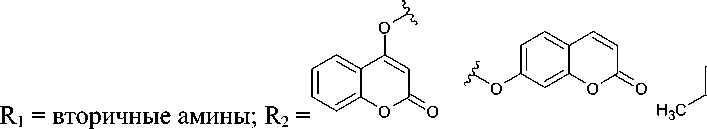
Схема 19. Синтез 2,4-дизамещённых триазинов
Для серии новых производных кумарин-1,3,5-триазина 24 была проведена оценка биологической активности на предмет их потенциального ингибирующего действия на ацетилхолинэстеразу и бутирилхолинэстеразу. Ингибирующее действие этих соединений 24 на АХЭ было относительно сильным: тринадцать соединений продемонстрировали ингибирование >50 % при концентрации 300 мкМ [58]. Для соединения 25 была исследована активность против MDA-MB-231 (клетки рака молочной железы), HeLa (клетки рака шейки матки), HCCLM3 (клетки рака печени) и HCT116 (клетки рака толстой кишки). Результаты показывают, что некоторые производные хризина-1,3,5-триазина обладают большей противораковой активностью, чем цисплатин и хризин [59]. Все соединения 24 и 25 были структурно подтверждены методами ЯМР, ИК и HRMS, в случае одного из сединений 24 и одного из соединений 25 удалось установить структуры методом РСА (рис. 10).
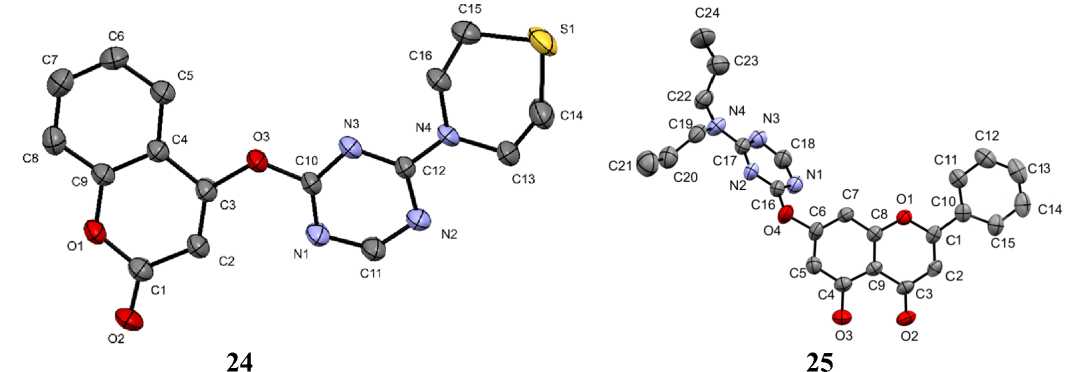
Рис. 10. Строение соединений 24 и 25, установленнное методом РСА
При обработке дихлортриазина 23 метилатом натрия и метиламином был получен 2-метил-4-метиламино-6-метокси-1,3,5-триазин ( 26 ). Данный способ получения O,N-замещенного 1,3,5-триазина в качестве промежуточного продукта был разработан при производстве гербицидов на основе сульфонилмочевины (схема 20) [40].
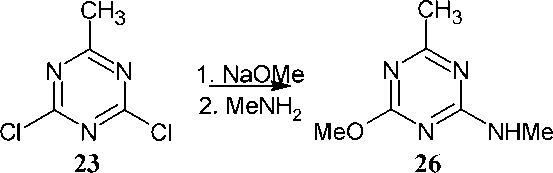
Схема 20. получения O,N-замещенного 1,3,5-триазина
2,4-Дихлор-1,3,5-триазин 23 также как и трихлортриазин 1 может подвергаться ступенчатому гидролизу. Сначала в присутствии основания в ацетонитриле при комнатной температуре заменяется только один хлор с получением 1,3,5-триазин-2(1 Н )-она ( 27 ), тогда как второй хлор гидролизуется при дальнейшем нагревании первичного продукта в водном растворе щелочи с получением диона ( 28 ) (схема 21) [60].
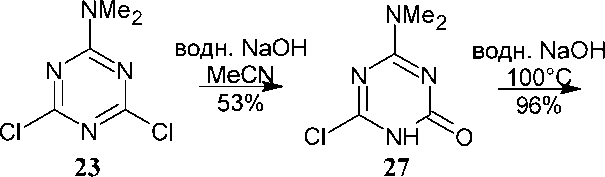
Схема 21. Ступенчатый гидролиз 2,4-дихлор-6-(диметиламино)-1,3,5-триазина
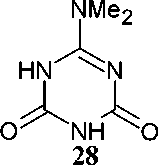
Кроме того, 2,4-дихлор-1,3,5-триазин 23 может быть переведён с хорошими выходами и высокой чистотой в 2,4-диарилокси-1,3,5-триазин ( 29) при его обработке двумя эквивалентами производных 4-гидроксибензальдегида (схема 22) [61].
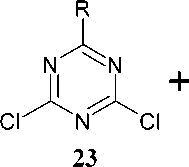
он
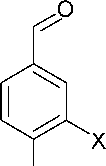
Na2CO3 бенздр △, 24 ч
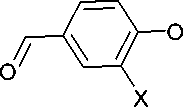
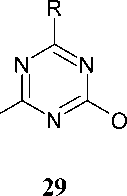
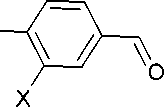
R = морфолин, пиперидин, диэтиламин; X = H, OCH 3
Схема 22. Получение 2,4-диарилокси-1,3,5-триазинов
Моногалогензамещенный 2-хлор-4,6-диметокси-1,3,5-триазин 5 при действии уксусной кислоты и силикагеля, функционализированного диметиламином, путем взбалтывания в этаноле превращается в 4,6-диметокси-1,3,5-триазин-2(1 Н )-он ( 30 ). Авторы [62] отмечают, что силикагель можно повторно использовать, промыв его разбавленным водным раствором аммиака (схема 23).
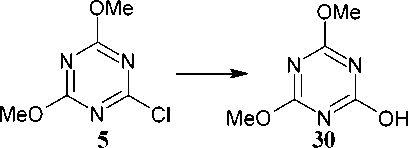
Схема 23. Получение 4,6-диметокси-1,3,5-триазин-2(1 Н )-она
О синтезе 1,3,5-триазин-2,4,6-тритиона ( 31 ) из хлорида циануровой кислоты в литературе гораздо меньше сведений. Впервые 1,3,5-триазин-2,4,6-тритион 31 был получен в 1880-х годах путем взаимодействия метилтиоцианата и сульфида натрия с образованием тиоцианата натрия и выделен после обработки кислотой. Его также можно легко и недорого приготовить, смешав 1-но молярный эквивалент хлорида циануровой кислоты с 3-мя молярными эквивалентами гидросульфида натрия (NaHS) и затем понизив рН до уровня ниже 4,96 [63]. Аналогично при добавлении гидросульфида натрия к хлориду циануровой кислоты 1 в метаноле была сначала получена тритиоциануровая кислота 31 , которая далее без предварительной очистки подвергалась действию йодистого метила при перемешивании и приводила к получению 2,4,6-триметилсульфанил- s -триазина ( 32 ) (схема 24) [64].
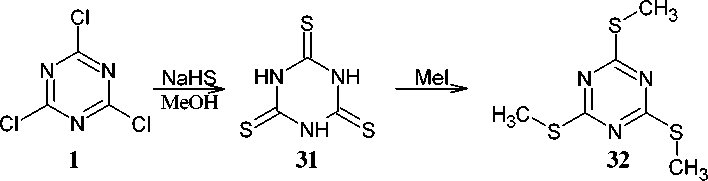
Схема 24. Образование 2,4,6-триметилсульфанил- s -триазина
Кроме того, запатентован способ получения водного раствора динатриевой соли 2,4,6-тримеркапто- s -триазина как агента активно связывающего тяжелые металлы. Способ получения включает несколько стадий. На первом этапе предполагается добавление водного раствора хлорида циануровой кислоты и сульфида натрия к водному раствору гидросульфида натрия при температуре 0–20 °С для получения смеси с рН 10~12. Далее необходимо нагревание полученной смеси и после завершения реакции охлаждение и фильтрование целевого продукта. Отмечается, что настоящее изобретение позволяет избежать использования щелочи для регулирования значения рН реакционной системы за счет изменения молярного соотношения гидросульфида натрия и сульфида натрия. Реакция гидролиза подавляется в наибольшей степени, чтобы обеспечить чистоту и выход 2,4,6-тримеркапто-динатриевой соли s -триазина [65].
Получить натриевую соль триазинтиона можно и при действии на хлорид циануровой кислоты 1 дитиокарбоната. Для осуществления реакции в колбу ввели цианурхлорид 1 и метилизобутиловый эфир, затем при перемешивании к смеси при температуре 5 °C добавили изопропилксантогенат в воде, смесь перемешивали в течение 3 часов при 30 °C и отделили органическую фазу. Затем в органическую фазу при температуре 5 °C медленно добавляли растворы бутиламина и NaOH. После перемешивания смеси в течение 2 часов при 40 °C образовавшийся твердый продукт отфильтровали и перекристаллизовали из воды, получив белое твердое вещество 6-бутиламино-1,3,5-триазин-2(1 H )-тион-4-тиолят натрия ( 33 ) (схема 25) [66].
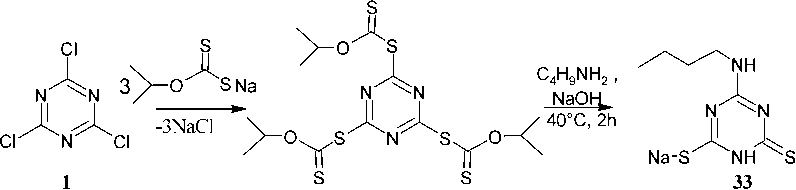
Схема 25. Получение 6-бутиламино-1,3,5-триазин-2(1 H )-тион-4-тиолята натрия
Придти к производным 1,3,5-триазин-2,4,6-тритиона ( 34 ) можно также подействовав пентасульфидом фосфора на исходные триазинтрионы ( 35 ). При этом желаемые тритионы удаётся выделить с достаточно высокими выходами 70–99 %, однако для достижения полного превращения в тритионы необходим избыток P4S10 (схема 26) [67].
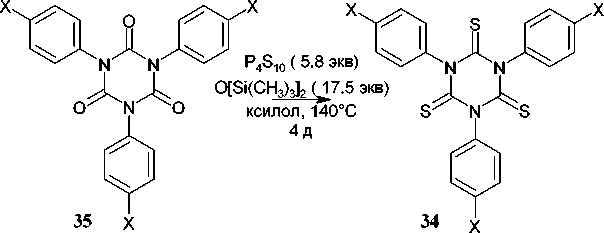
X = Br, I, H, Me
Схема 26. Образование 1,3,5-триазин-2,4,6-тритиона под действием P 2 S 10
В случае недостатка P 2 S 10 образуется смесь триазинов, состоящая из моно- 34’ , бис - 34’’ и трис -тиоизоциануратов 34 , которые после разделения на селикагеле были выделены в виде индивидуальных соединений с выходами 20, 24 и 6 % соответственно [67]. Для моно- и трис -тио-производных изоциануратов структура была подтверждена методом РСА (рис. 11).
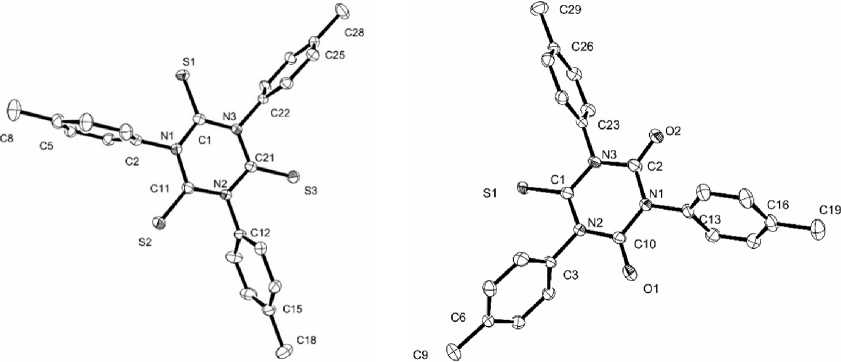
34 34’
Рис. 11. Структуры соединений 34’ и 34 по данным РСА
Таким образом, цианурхлорид является активным субстратом в реакциях с О-, S- и другими нуклеофилами, а при контроле температуры возможны реакции селективного нуклеофильного замещения атомов хлора цианурхлорида. Так, первый атом хлора замещается легко уже при температуре 0–5 °С, а второй атом хлора – при более высокой температуре (35–45 °С). Замещение третьего атома хлора затруднено и для его осуществления требуется нагревание до 80–100 °С (схема 27) [68].
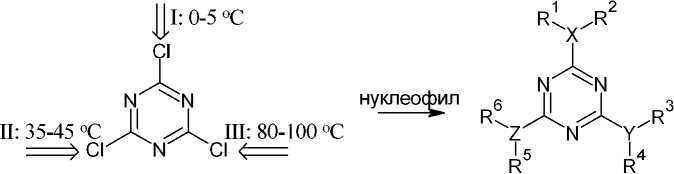
X, Y, Z = N, O, S, C; R1 – R6 = алкил, алкенил, арил
Схема 27. Последовательное замещение хлора в цианурхлориде
Однако, по причине того, что многие из рассмотренных выше превращений приводят к образованию нескольких продуктов, либо являются многостадийными, подобный подход к синтезу 1,3,5-триазинонов(тионов) из циануровой кислоты не имеет особого практического значения и предполагает дополнительную очистку целевого продукта.
-
1.2. Синтез на основе мочевины, тиомочевины и их производных
Одним из простейших методов прямого синтеза 1,3,5-триазинонов является термолиз мочевины. Однако, в зависимости от температуры в результате таких реакций образуется сразу несколько различных продуктов [69], что в ряде случаев затрудняет использование этого синтеза в практических целях.
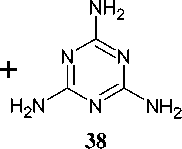
Так, мочевина разлагается при повышенной температуре с образованием 1,3,5-триазин-2,4,6-(1 Н ,3 Н ,5 Н )-триона 2 , 6-амино-1,3,5-триазин-2,4(1 H ,3 H )-диона ( 36 ), 4,6-диамино-1,3,5-триазин-2(1 H )-она ( 37 ) и 1,3,5-триазин-2,4,6-триамина ( 38 ) (схема 28) [40].
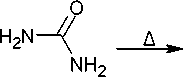
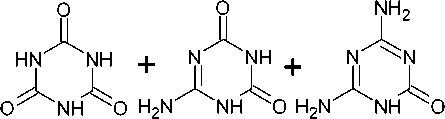
Схема 28. Термолиз мочевины
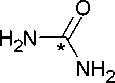
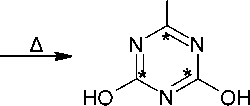
Процесс термического превращения мочевины в вакууме был исследован с применением изотопной метки. (2,4,6-14С)-циануровую кислоту 2’ получали из 14С-мочевины путем гетероциклизации последней в присутствии хлорида аммония без растворителя в стеклянной пробирке с вакуумной герметизацией. Продукт был очищен методом ионообменной хроматографии, а радиохимический выход на основе 14С-мочевины составил 60,5 % (схема 29) [71].
он
2'
Схема 29. Получение (2,4,6-14С)-циануровой кислоты
Оптимальные условия были определены путем варьирования количества хлорида аммония и проведения реакции в вакууме в течение различного времени. Таким образом, было установлено, что использование эквимолярных количеств хлорида аммония и мочевины и температура плавления 250 °С в течение 20 мин в вакууме (1 мм) являются наилучшими для максимизации выхода. Этот новый подход к получению (2,4,6-14С)-циануровой кислоты позволил получить более высокий выход.
Другим способом получения циануровой кислоты 2 является тримеризация мочевины в растворителе с или без катализатора (схема 30). В сравнении с термолизом мочевины, этот метод является экологически безопасным, недорогим, и продукт можно использовать в неочищенном виде. Но есть и недостаток: растворитель с высокой температурой кипения необходимо регенерировать после нескольких использований, а некоторые из потенциально дорогостоящих растворителей, таких как сульфолан, тетраэтиленгликольдиметиловый эфир, бутилкарбитол и циклогексанол, могут быть потрачены впустую [72]. Авторами [72] была опробована методика триме-ризации мочевины в более дешёвых растворителях, таких как дизельное топливо или керосин, при этом добавление катализаторов (солей аммония, кальция, цинка, калия и натрия) не привело к существенному изменению выхода циануровой кислоты. Наилучших результатов удалось достичь при проведении реакции в керосине при 190 °С (88,9 %). Иные результаты были изложены Shinichi Kawahara и Takahiro Tejima [73], где циануровая кислота 2 была получена нагреванием мочевины в присутствии гидридов, амидов и солей щелочных металлов в органических растворителях. Например, мочевину обрабатывали NaH в метиловом эфире тетраэтиленгликоля при 150 °C в течение 5 часов, что дало 99 % циануровой кислоты 2 , тогда как без NaH образования циануровой кислоты 2 не наблюдалось.
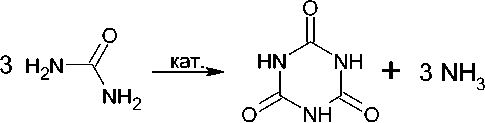
Схема 30. Тримеризация мочевины
Предложен и экспериментально проверен новый способ получения высокочистой циануровой кислоты из мочевины. Способ основан на силилировании мочевины в смеси ксилолов в присутствии гексаметилдисилазана (HMDS), что приводит к образованию нестабильной в условиях синтеза N-триметилсилилмочевины ( 39 ), которая отщепляя амиак переходит в триме-тилсилилизоцианат ( 40 ). Он был выделен в чистом виде перегонкой из реакционной смеси с использованием ректификационной колонки. На следующей стадии процесса триметилсилилизо-цианат 40 был подвергнут мягкому гидролизу при низких температурах в присутствии третичных аминов с получением циануровой кислоты 2 . Циануровую кислоту выделяли простой фильтрацией, промывкой и последующей сушкой. В девяти из десяти синтезов продукт содержал 99 % основного вещества (схема 31) [74].
О
-
2 H2N

NH2
ксилол, .NH 70- 100 °C
MeoSi SiMoo □ ел if 2
-
3 HMDS 3 tW
-NH3
Q
H2N 39 NH—SiMes
-NH.
* 2 Me3Si-N=C=O
3 о 40
Me3Si-N=C=O 40
H,0 ■
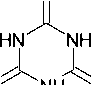
О НП О
Схема 31. Получение высокочистой циануровой кислоты
Сложность выше описанных превращений мочевины делает более предпочтительной реакцию её социклизации с другими реагентами, приводящую, как правило, к одному целевому про- дукту.
Мочевина в таких реакциях является источником N-C-N фрагмента. В её реакции с бензо- нитрилами два других фрагмента, необходимых для образования триазинового кольца, образу- ются из нитрила. Нагревание смеси обоих компонентов в присутствии гидрида натрия дает 4,6- диарил-1,3,5-триазин-2(1H)-оны (41) с выходом ~50 % (схема 32) [75].
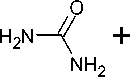
2 Ar1CN
1. NaH, ДМСО, 25°C, 2ч
2. 100 °C, 32 ч
HCI „
~ 50 % .
Ar
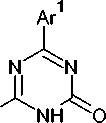
Ar1 = Ph, 4-Cl-C 6 H 5 , 4-Tol
Схема 32. Синтез 4,6-диарил-1,3,5-триазин-2(1 H )-она
Получить тиоаналог соединения 41 (4,6-диарил-1,3,5-триазин-2-тионы, 41 ) можно при конденсации тиомочевины с N-(1-хлорбензил)бензимидоилхлоридом в присутствии Et 3 N с хорошими выходами (80–86 %). При этом в отсутствии основания реакция приводит к образованию хлорида 2-тиоксо-1,3,5-триазиния ( 42 ) (схема 33) [76].
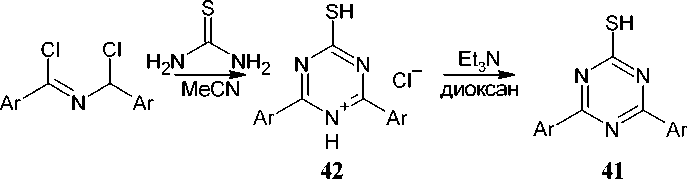
Ar = Ph, 4-FC 6 H 4
Схема 33. Конденсация тиомочевины с имидоилхлоридом
Кипячение фуран-2-карбонил изотиоцианата с мочевиной в обезвоженном ацетоне приводит к получению производного тиомочевины, которое подвергается внутримолекулярной циклизации при катализе основанием в растворе этилата натрия при комнатной температуре и образуется 4-(фуран-2-ил)-6-тиоксо-5,6-дигидро-1,3,5-триазин-2(1 H )-он ( 43 ) (схема 34) [77].
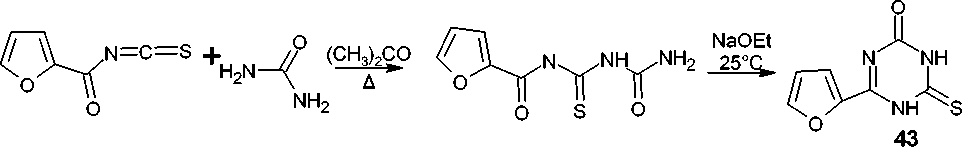
Схема 34. Взаимодействие фуран-2-карбонил изотиоцианата с мочевиной
Плавление смеси перхлората 2,4,6-трифенил-1,3,5-оксадиазиния и мочевины дает 4,6-дифенил-1,3,5-триазин-2(1 Н )-он, (X = O) ( 44 ) с разумным выходом путем формального обмена бензамида на мочевину. Аналогично протекает реакция перхлората 2,4,6-трифенил-1,3,5-оксадиазиния с N-метилтиомочевиной с образованием 3-N-метил-4,6-дифенил-1,3,5-триазин-
2(1 Н )-она ( 45 ), а вот в случае незамещенной тиомечевины выделяется не только 4,6-дифенил-1,3,5-триазин-2(1 Н )-тион (X = S) ( 46 ) , но и побочный продукт – бисульфид ( 47 ) (схема 35) [78].
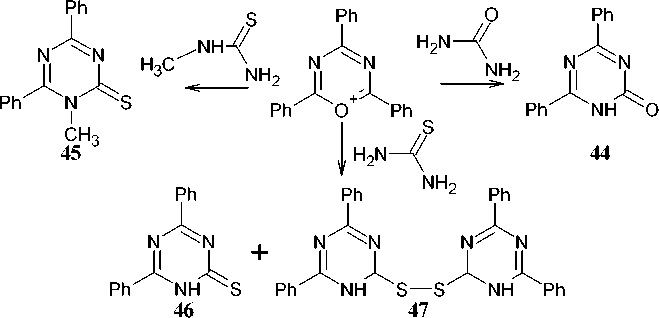
Схема 35. Превращения перхлората 2,4,6-трифенил-1,3,5-оксадиазиния
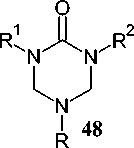
Различные 5-N-замещённые гексагидро-1,3,5-триазин-2-тионы ( 48 ) могут быть получены исходя из диметилолмочевины (производное мочевины, которое образуется при реакции мочевины с формальдегидом) и первичных аминов, однако, выходы по данной реакции не высоки и составляют 7–32 % (схема 36) [79]. Аналогичная реакция 1,3-дизамещённой-диметилолмочевины с аминами приводит к образованию 1,3,5-N-тризамещённых-1,3,5-триазин-2-тионов [80].
R NH2
H20
A .
O
HO CH2 N N CH2 OH
R1 R2
R = Me, Et, i -Pr, tert -Bu, Bn, CH 2 CH 2 N(C 2 H 5 ) 2 , CH 2 CH 2 OH R1, R2 = H, n -Bu, CH 3 C 6 H 4 SO 2
Схема 36. Взаимодействие диметилолмочевины и первичных аминов
Для синтезированного 5-(2-гидроксиэтил)-1,3,5-триазин-2-тиона 48 (HOTAT) была проведена оценка ингибирующего действия на коррозию для углеродистой стали марки 10# в 2 % растворе NH 4 Cl, изучение проводилось методами потери веса, поляризации и электрохимической импедансной спектроскопии. Результаты показали, что HOTAT является хорошим ингибитором коррозии. Эффективность ингибирования HOTAT увеличивается с увеличением концентрации ингибитора и уменьшается с ростом температуры [81].
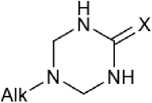
Реакция мочевины с эквимолярным количеством N,N- бис (метоксиметил)циклогексил-1-амина была использована в качестве модельного процесса для оценки каталитической активности различных катализаторов на основе d- и f-элементов (Fe, Co, Pd, Ti, Zr, Cu, Sm, Yb). Установлено, что 5 мол. % SmCl 3 · H 2 O (CHCl 3 –EtOH, 1:2 по объёму, 60 °C, 6 ч) обеспечивает наилучший выход 5-циклогексил-1,3,5-триазин-2-она ( 49 , 52 %). В данных условиях реакции мочевины и тиомочевины с N,N- бис (метоксиметил)алкиламинами в присутствии 5 мол. % SmCl3 · 6H2O селективно давали 5-алкил-1,3,5-триазинан-2-оны 49 и 5-алкил-1,3,5-триазинан-2-тионы ( 50 ) с выходом 30–58 % (схема 37) [82].
49, 50
Aik * [Sm]
MeO. ,N. zOMe + u -2MeOH
[Sm] = SmCl 3 ·6H 2 O; 49 , X = O; 50 , X = S; Alk = cyclo -C 6 H 11 , t -Bu, HO(CH 2 ) 2 , i -Pr
Схема 37. Получение гексагидро-1,3,5-триазин-2-(ти)онов, катализируемое SmCl 3 · H 2 O
Ряд новых производных гексагидро-1,3,5-триазин-2-тиона был получен путем аминометилирования тиомочевины формальдегидом и первичными аминами. При использовании анилина в качестве аминного компонента образуется аномальный продукт аминометилирования - 5-фенил-1-фениламинометилгексагидро-1,3,5-триазин-2-тион [83]. 3-N-алкил-гексагидро-1,3,5-триазин-2-тионы ( 51 ) могут быть получены с высокими выходами (96–98 %) путем взаимодействия тиомочевин не только с формальдегидом, но и с ароматическими/гетероциклическими аминами при микроволновом облучении (схема 38) [84].
s
1эквАгЫН2Д
§ 5 экв НСНО R—NNH
MW? IJ
R-NH NH2 0.5 - 2 минN
Ar
N-N
UeANASH
Ar = 2-(CF 3 )-C 6 H 4 , 3-F-C 6 H 4 , Tol, 4-MeOC 6 H 4 ,
R = Ph, 2-(CF 3 )-C 6 H 4 , H
Схема 38. Образование гексагидро-1,3,5-триазин-2-тионов
При реакции глицилглицина с двумя эквивалентами безводного параформальдегида и одним эквивалентом N,N'-диметил- или N,N'-диэтилмочевины был выделен 1,3-диметил- или 1,3-диэтилгексагидро-1,3,5-триазин-2-он ( 52 или 53 ) соответственно. Реакция глицилглицина с N,N'-диэтилтиомочевиной дала 1,3-диэтилгексагидро-1,3,5-триазин-2-тион ( 54 ). Конденсацию целесообразно проводить в диметилформамиде, обеспечивающем полное растворение исходных соединений. Выходы соединений 52–54 в этих условиях составляют 88, 62 и 41 % соответственно (схема 39) [85].
x о 9 о R,N^\ if /9
Д + 1+ H^-C^C-NH-ChX ^ X=( \-CH2C-NH CH2-C
R-NH ^NH-R H^H 4OH RN-7 52_54 OH
-
52 : R = Me, X = O; 53 : R = Et, X = O; 54 : R = Me, X = S
Схема 39. Взаимодействие N,N'-диалкил(тио)мочевины с формальдегидом и глицилглицином
Pазработан простой и эффективный метод синтеза 4-арил-6-(алкилсульфанил)-3,4-дигидро-1,3,5-триазин-2(1 H )-тионов ( 55 ) в ДМФА при 80 °С посредством многокомпонентной реакции замещенных альдегидов, тиомочевины и триалкилортоформиатов без катализатора с выходами от умеренных до хороших (схема 40) [86].
h2n
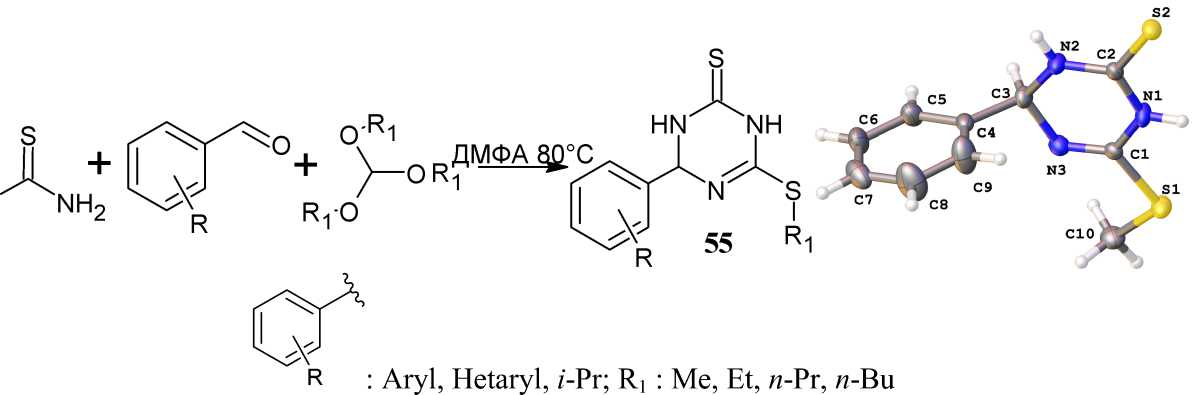
Схема 40. Однореакторный синтез 4-арил-6-(алкилсульфанил)-3,4-дигидро-1,3,5-триазин-2(1 H )-тионов
Ряд 4-фенил-6(замещенный фенил)-[1,3,5]триазин-2-иламин/-ол/-тиолов (56) был синтезирован путем трёхкомпонентной реакции между ароматическими эфирами или кислотой, мочевиной (или гуанидином, или тиомочевинной) и бензонитрилом путем воздействия микроволн (280 Вт) (схема 41). Ход реакции контролировали методом ТСХ. Кроме того, авторами проведен биологический скрининг некоторых производных [1,3,5]триазин-2-иламин/-ол/-тиолов 56, который пока- зал наличие хорошей активности в отношении ингибитора фосфодиэстеразы, ингибитора убихи-нол-цитохром-с-редуктазы и ингибитора птериндеаминазы [87].
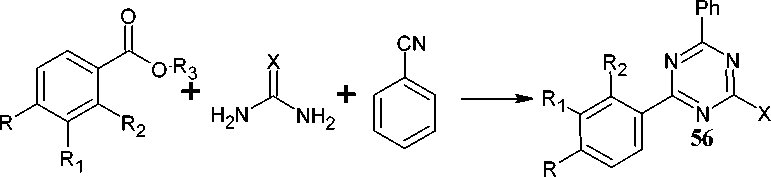
X = Nh, S, O; R, R 1 , R 2 , R 3 = Alk, H
Схема 41. Синтез 4-фенил-6(замещенный фенил)-[1,3,5]триазин-2-иламин/-ол/-тиолов
В результате трёхкомпонентной реакции конденсации мочевины с формальдегидом и бутан-1,4-диамина в соотношении 2:4:1 был получен 5,5'-бутан-1,4-диил- бис (1,3,5-триазинан-2-он) ( 57 ) (схема 42) [88].
NH2(CH2)4NH2, HCHO H
О N—\/—N и А 2ч, EtOH : H2O = 1:1 / \ / \__
U n-ch2ch2ch2ch2n
H2N^NH2 27 /o V^N
H 57
Схема 42. Получение 5,5'-бутан-1,4-диил- бис (1,3,5-триазинан-2-она)
Аналогичным образом при кипячении в водно-этанольной смеси пропан-1,3-диамина с тиомочевиной и 37%-ным раствором формальдегида (мольное соотношение 1:2:4) был получен 5,5'-пропан-1,3-диил- бис (1,3,5-триазинан-2-тион) ( 58 , ПБТ) с выходом 75 % (схема 43) [89].
NH2(CH2)3NH2, HCHO
А 2ч, EtOH : H2O = 1.1
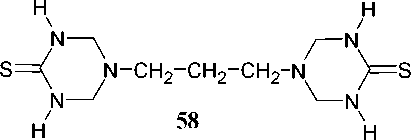
Схема 43. Конденсация тиомочевины, пропан-1,3-диамина и формальдегида
Ингибирующие свойства ПБТ в растворе 1,0 моль/л HCl были исследованы с помощью гравиметрического измерения, электрохимического анализа, анализа поверхности и квантово- химических методов. Результаты показали, что ингибирующая эффективность ПБТ близка к 90 % при 298,15 К в диапазоне концентраций 0,005–1,0 ммоль/л, при этом максимальная ингибирующая эффективность ПБТ составляет 92,1 % при концентрации 1,0 ммоль/л. Кроме того, адсорбция ПБТ на поверхности углеродистой стали согласуется с изотермической моделью Ленгмюра [89].
Известны и другие системы бис (1,3,5-триазин-2-тионов) ( 59 ), имеющие различное число метиленовых звеньев между триазинами. Их получают конденсацией тиомочевины с формальдегидом и различными диаминами (этан-1,2-диамин, бутан-1,4-диамин и пропан-1,2-диамин), для проведения реакции также используют смесь вода-этанол или вода-пропанол-2 (схема 44) [90].
NH2RNH2, HCHO
EtOH-H2O/ * /-РЮН-Н20
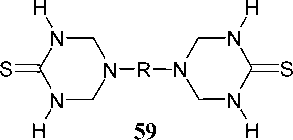
R = -CH 2 CH 2 -, -(CH 2 ) 4 -, -CH 2 CH(CH 3 )-
Схема 44. Взаимодействие тиомочевины, формальдегида и диаминов
Для получения O-/S-производных 1,3,5-триазина в качестве исходного реагента используют О-метилизомочевину, S-метилизотиомочевину и их соли. При нагревании сульфата 2-метилизотиурония в формамиде образуется 4-(метилсульфанил)-1,3,5-триазин-2-амин (60) с выходом 51 % (схема 45). В этой реакции циклоконденсации соль изотиурония образует как
N-C-N, так и N-C-фрагмент с отщеплением тиольной-группы и элемент =С- получают из формамида. В этой реакции формамид может быть заменен его диэтилацеталем [40].
h2n
SMe
NH. 0,5H2SO4
nh2
1 30°С,ж1 ч
51 %
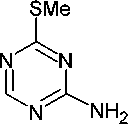
Схема 45. Образование 4-(метилсульфанил)-1,3,5-триазин-2-амин
В модификации этого способа различные соли изотиурония взаимодействуют с диметилформамидом в присутствии оксалилхлорида в качестве активирующего агента и
N,N-диизопропилэтиламина в качестве основания с получением 4-(алкилсульфанил)-1,3,5- триазин-2-аминов 60 с умеренным выходом (схема 46). Алкилсульфанильная группа в триазин-2-амине может быть окислена 3-хлорпероксибензойной кислотой и легко заменена первичными и вторичными аминами [40].
h2n
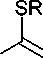
NH. HX
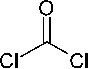
ДМФА, /- Pr2NEt 0-25 °Ct R = f-Bu, 61 %
R = Bn, 73 %
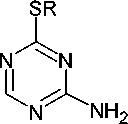
Схема 46. Получение 4-(алкилсульфанил)-1,3,5-триазин-2-аминов
При аналогичном взаимодействии тиоурониевой соли, связанной со смолой, с диметилцианодитиоимидокарбонатом может быть получен триазин (61), содержащий две серосодержащие функциональные группы (схема 47) [40].
SMe
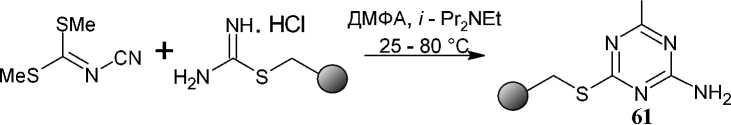
Схема 47. Взаимодействие тиоурониевой соли с диметилцианодитиоимидокарбонатом
Тризамещённые-1,3,5-триазины образуются с умеренными и хорошими выходами в ходе реакции между имидатами и O-метилизомочевинами или S-метилизотиомочевинам (схема 48). Такое взаимодействие приводит к 2-метокси или 2-метилсульфанил-4,6-диалкил-1,3,5-триазинам ( 62 ). Триалкил- s -триазины получают при замене производных мочевины на амидины или гуанидины [91].
R1
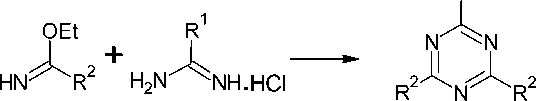
R1 = OMe, SMe;
R2 = Me, Et
Схема 48. Получение 4,6-диалкил-2-метокси(метилсульфанил)-1,3,5-триазинов
N-Ацилимидаты при конденсации с производными мочевины и тиомочевины образуют переходное соединение, которое дегидратируется при комнатной температуре в соответствующие тризамещённые-1,3,5-триазины. 2-Метокси(метилсульфанил)-4,6-диалкил-1,3,5-триазины ( 63 ) могут быть получены исходя из O-метилизомочевины или S-метилизотиомочевины соответственно (схема 49) [92].
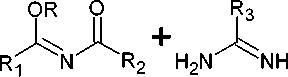
Me OHfr^u OH 25 °C, 3 - 5 д.
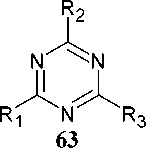
R 1 = Et, Ph ;
R 2 = Me, Et, Ph, CH=CHPh;
R 3 = OMe, SMe
Схема 49. Конденсация ацилимидатов с амидинами
Гуанилтиомочевина и её N-производные в реакциях с карбонильными соединениями приводят к формированию замещенного 4-амино-1,3,5-триазинтионового цикла. Так, 4-амино-6- сульфанил-1,3,5-триазин-2(5Н)-он (64) может быть синтезирован при кипячении амидинотиомо- чевины с 1,1-карбонил-бис-1Н-имидазолом в ДМФА (схема 50) [93].
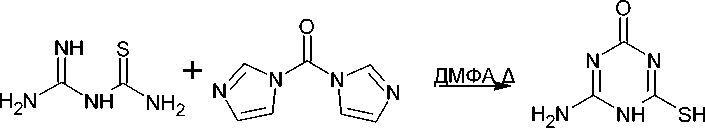
Схема 50. Синтез 4-амино-6-сульфанил-1,3,5-триазин-2(5 Н )-она
Ряд 6-замещенных производных 4-амино-1,3,5-триазин-2-тиона ( 65 или 65’ ) получен взаимодействием гуанилтиомочевины и её N-производных с альдегидами и кетонами, как показано на схеме 51 [94].
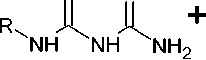
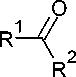
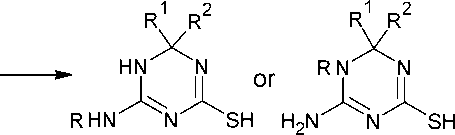
65’
R = H, Ph, p -CH 3 OC 6 H 4 , p -ClC 6 H 4 ; R1, R2 = H, Me, i -Pr, Ph
Схема 51. Превращение амидинотиомочевины при действии кетонов и альдегидов
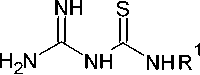
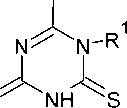
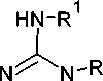
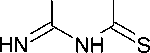
Другим вариантом получения замещённых триазинтионов является реакция N-производных гуанилтиомочевины и арилизотиоцианатов, приводящая к 4-имино-1-арил-6-(ариламино)-3,4-дигидро-1,3,5-триазин-2(1 H )-тионам ( 66 , 66’ ) с умеренными выходами (схема 52) [95].
HN-R
+ R-N^C-S -NaOU.
-H2S
HN
or
66’
R, R1 = Ar
Схема 52. Получение 4-имино-1-арил-6-(ариламино)-3,4-дигидро-1,3,5-триазин-2(1H)-тионов
Авторами [96] предполагается, что реакция может протекать по двум путям: исходный продукт конденсации (A) циклизуется до тиадиазина (B), который изомеризуется до 1,3,5-триазин-2-тиона ( 67 ). Или конденсация изотиоцианата с амидинотиомочевиной может дать структуру 67 через промежуточное соединение (C) (схема 53). Поскольку промежуточные соединения (В) или (С) не удалось выделить, нельзя сказать, какой из механизмов является предпочтительным.
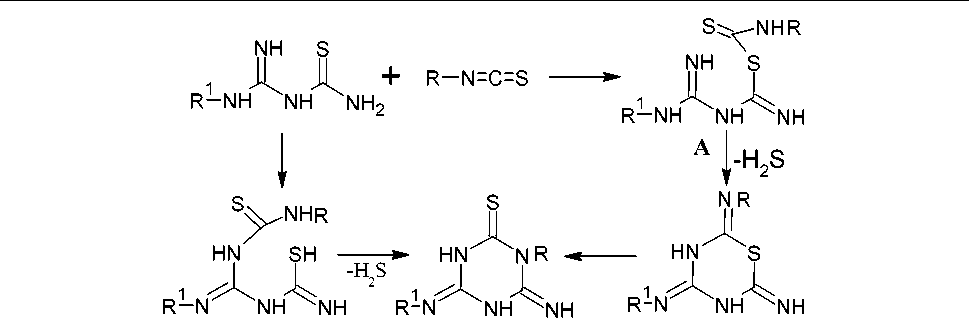
С 67 В
Схема 53. Возможные пути реакции изотиоцианата с амидинотиомочевиной
S-производные 1,3,5-триазина ( 68 ) можно получить исходя из S-замещённых гуанилтиомочевин и хлорангидридов алифатических галогенкарбоновых кислот (схема 54) [97].
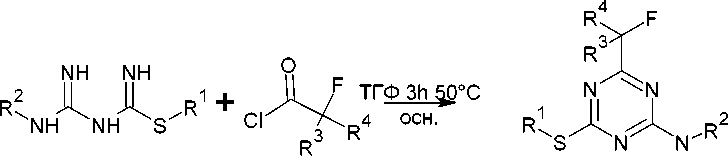
R1: Ph, i -Pr, Et; R2: Me, Ph, 3-MeC 6 H 4 ;
R3: Me, Et, t -Bu, F; R4: Me, Et, F
Схема 54. Взаимодействие S-замещённых амидинотиомочевин с хлорангидридами карбоновых кислот
Для получения 6-R1-4-амино-1,3,5-триазин-2-тиона ( 69 ) осуществляют циклизацию гуанилмочевины или тиомочевины с ортоэфирами в ДМФА при нагревании до 150 °С в течение 30 минут с выходом 72–86 % (схема 55) [98–101].
NH2
NN
S NH R1
NH S
HN S R1C(OR)3 ?50°С
H 2 N NH NH2 3
R1: H, Alk
Схема 55. Получение 6-R1-4-амино-1,3,5-триазин-2-тиона
Для 6-незамещенного 4-амино-1,3,5-триазин-2-тиона (70) предложен альтернативный метод синтеза, заключающийся в кипячении гуанилтиомочевины диметилформамида в диоксане в течение 30-ти минут. При выходом 85 % (схема 56) [102].
и диметилацеталя N,N-этом образуется продукт с
NH S
H2N NH NH2
MeO. диоксан, 2—OMe A 30 m^h H3C-N
CH3
N XN
H2N N xS
Схема 56. Альтернативный метод синтеза 6-незамещенного 4-амино-1,3,5-триазин-2-тиона
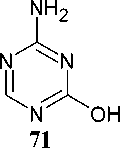
Циклизация формиата гуанилмочевины путем нагревания при 150 °С представляет собой ещё один метод синтеза кольца s -триазина. Поскольку эта реакция приводит к включению углерода формиата в кольцо s -триазина [103], она может стать основой для синтеза нескольких дизамещенных s -триазинов ( 71 ) из различных формиатных солей гуанилмочевины или из её солей, образованных другими карбоновыми кислотами (схема 57).
о-сн=о
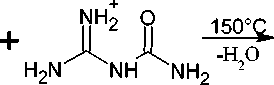
Схема 57. Циклизация формиата гуанилмочевины
Разработан новый эффективный метод синтеза 4(6)-амино-1,6(4)-дизамещенных 1,3,5-триазин-2-онов ( 72 ), а также 4(6)-амино-1,6(4)-дизамещенных-1,3,5-триазин-2-тионов ( 73 ) [104]. В присутствии трет -бутоксида калия N2-ацил-1 H -бензотриазол-1-карбоксимидамиды ( 74 ) реагируют с мочевиной или тиомочевиной, давая 4-амино-1,3,5-триазин-2(1 H )-оны 72 или
4-амино-1,3,5-триазин-2(1 H )-тионы 73 с высоким выходом (схема 58).
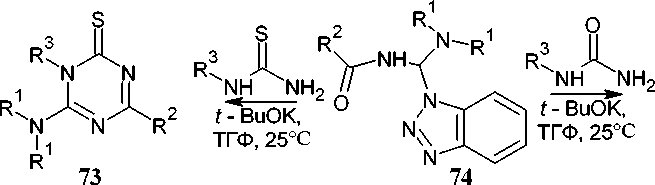
R1 = (CH 2 ) 2 O(CH 2 ) 2 , Et, Allyl;
R2 = Et, t -Bu, Ph, замещённый-Ph, тиофен-2-ил;
R3 = H, Alk, Ph
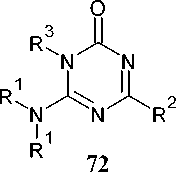
Схема 58. Синтез триазинонов(тионов) из N2-ацил-1 H -бензотриазол-1-карбоксимидов
То есть бензотриазол является подходящей уходящей группой в реакции циклоконденсации с мочевиной или ее тиоаналогом. Замещенные мочевины превращаются в N-замещенные триазины.
2-Алкилизомочевино-1-карбоксимидамиды ( 75 ) могут подвергаться циклизации с эфирами карбоновых кислот с получением 6-замещенных 4-алкокси-1,3,5-триазин-2-аминов ( 76 ) с переменным выходом. При использовании ортоэфиров выход увеличивается [105]. Другим методом, который облегчает реакцию замыкания триазинового кольца, является использование хелатов меди(II) имидоилгуанидинов (схема 59).
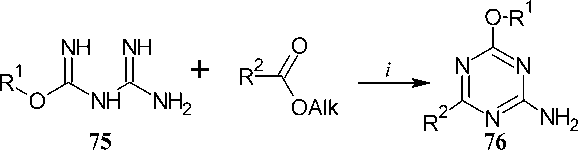
i : MeOH, 4д; EtOH, Д 24ч/ 25 °C 5д/ охлаждение 14ч; DMF 50оС 1ч, 90оС 5ч R1 = Me, Et; R2 = H, CO 2 Et, 2-пиридил, CH 2 Cl, CH 2 CN, CF 3
Схема 59. Получение 6-замещенных 4-алкокси-1,3,5-триазин-2-аминов
Эту реакцию циклоконденсации можно также провести с аналогичным 2-алкилизотиомочевино-1-карбоксимидамидом ( 77 ). Взаимодействие гидриодида 2-метилизо-тиомочевины-1-карбоксимидамида в качестве аддукта 1-метилпирролидин-2-она c метилтрифторацетатом в присутствии метоксида натрия дает 4-(метилсульфанил)-6-(трифторметил)-1,3,5-триазин-2-амин ( 78 ) с выходом 94 % [40]. Дальнейшая обработка метоксидом натрия приводит к замене метилсульфанильной группы на метоксильную группу (схема 60).
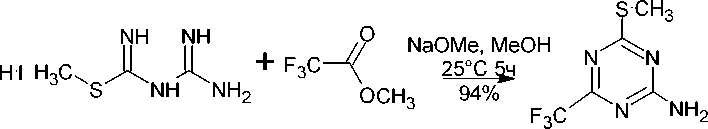
77 78
Схема 60. Циклоконденсация 2-алкилизотиомочевино-1-карбоксимидамида с метилтрифторацетатом
Циклизация N-ацил-N'-карбамоил-S-метилизотиомочевин ( 79 ) при кипячении в метаноле дает соответствующие S-метилпроизводные 1,3,5-триазин-2(1 Н )-она(тиона) ( 80 ) [106]. Исходные S-метилизотиомочевины 79 образуются из S,S'-диметил-N-цианокарбонимидодитиоата ( 81 ) при взаимодействии с амидами в присутствии гидрида натрия в смеси бензола и N,N-диметилацетамида (схема 61).
MeS
>= N
MeS CN

X
NH2, NaH нз°+ R
NH2
81 79
S CH3
NN
R NH X
R = Me, Ph, 4MeC 6 H 4 , 4-MeOC 6 H 4 ; X = O, S
Схема 61. Циклизация N-ацил-N'-карбамоил-S-метилизотиомочевин
В общем случае производные гексагидро-1,3,5-триазин-2,4-диона могут быть получены не из самой тиомочевины, а из биуретов. Например, при взаимодействии биурета с этилформиатом в присутствии этоксида натрия с последующей обработкой хлористым водородом образуется 1,3,5-триазин-2,4-(1 Н ,3 Н )-дион ( 82 ,5-азаурацил) с выходом 59 % [40]. Эту реакцию циклоконденсации также можно провести с использованием гидрохлорида N,N-диметилхлорформамида (схема 62).
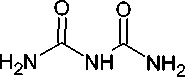
+
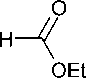
1. NaOEt, EtOH, △ , 3ч 2. HCI, EtOH, A, 15 мин
59 %
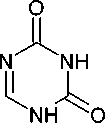
Схема 62. Синтез 1,3,5-триазин-2,4(1 Н ,3 Н )-диона
Серия 6-арил-2,4-диоксопергидро-1,3,5-триазинов ( 83 ) (схема 63) была получена из ароматических альдегидов и биурета. Смесь соответствующего альдегида и биурета в трифторуксусной кислоте при длительном кипячении приводит к триазину. Все реакции протекали гладко и, как правило, с выходами от умеренных до превосходных (45–90 %) [107]. Для получения 6-фенил- s -триазин-2,4-диона 83 также применимо перемешивание биурета с бензальдегидом в соляной кислоте в течение суток при комнатной температуре [108].
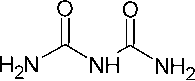
ArCHO
F 3CCOOH
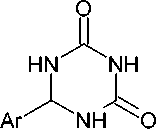
Схема 63. Конденсация биурета и ароматических альдегидов
Реакции индол-2,3-дионов с биуретом привели к образованию 1,3-дигидро-3-уреидоформимидо-2 H -индол-2-онов ( 84 ) и спиро[3 H -индол-3,2′(1′ H )-(1,3,5)триазин]-2,4′,6′(1 H ,3′ H ,5′ H )-трионов ( 85 ), что свидетельствует о зависимости направления реакции от растворителя. Были исследованы различные органические растворители, такие как метанол, этанол (нейтральный/кислый) и ледяная уксусная кислота, и было обнаружено, что ледяная уксусная кислота является хорошим растворителем для получения целевых продуктов, а именно спи-ро[3 H -индол-3,2′(1′ H )-(1,3,5)триазин]-2,4′,6′(1 H , 3′ H ,5′ H )-трионов 85 , с хорошими выходами (схема 64) [109].
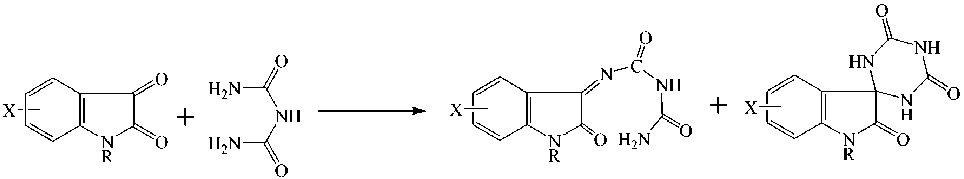
R = H, Me, COMe,
X = H, 5-F, 5-CF 3
Схема 64. Получение спиро[3 H -индол-3,2′(1′ H )-(1,3,5)триазин]-2,4′,6′(1 H ,3′ H ,5′ H )-трионов
Циклизацию 1-(2-Х-4-йодфенил)биурета проводили нагреванием с EtONa в обезвоженном
EtOH с (EtO)2C=O в атмосфере аргона (схема 65), в следствие чего были получены N-(2-Х-4-йодфенил)изоциануровые кислоты (86). При этом первоначально была получена натриевая соль целевого соединения, которая затем была переведена в кето форму подкислением HCl [110].
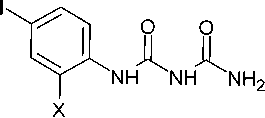
1. (EtO)2C=O безв EtOH, NaOEt Ar
2. HCI, H2O
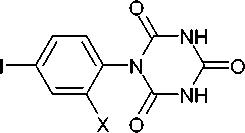
X = H (55 %), Cl (34 %)
Схема 65. Синтез N-(2-Х-4-йодфенил)изоциануровых кислот
Образование 3,5-диарил-4-фенилимино-6-оксогексагидро-1,3,5-триазин-2-тионов (87) воз- можно при взаимодействии 1,5-дизамещённого тиобиурета с фенилизоцианодихлоридом в бензоле при кипячение в течение 5 часов, первоначально образуется 1,3,5-тиадиазин (88), который после изомеризации переходит в конечный продукт 87 (схема 66) [111].
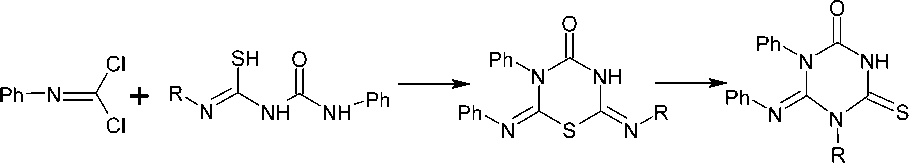
R = Ph, m -Tol, p -Tol, m -ClC 6 H 4 , p -ClC 6 H 4
Схема 66. Взаимодействие 1,5-дизамещённоготиобиурета с фенилизоцианодихлоридом
Циклизацией ацилбиуретов ( 89 ), которые могут быть получены из 3-ацилгуанидин-1-карбоксамидов ( 90 ) путем кислотного гидролиза, в присутствии NaOH получен гуанамид (2-замещенный-4,6-дигидрокси- s -триазин, 91 ) (схема 67). В 1929–1930 гг. эта реакция была изучена Остроговичем [112].
R
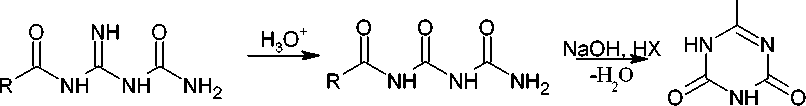
90 89 91
Схема 67. Синтез гуанамида
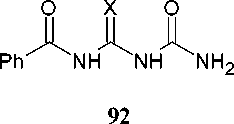
В то время как бензоильное производное ( 92 ) дает соответствующий 1,3,5-триазин-
2,4(1H,3H)-дион (93, X = O) с почти количественным выходом, ацетильное производное цикли- зуется лишь частично [40]. 1-Бензоил-2-тиобиурет подвергается той же реакции циклоконденсации при обработке гидроксидом натрия, давая 6-фенил-4-сульфанил-1,3,5-триазин-2(1H)-он (94, X = S) с аналогичным выходом. При обработке соединения 94 пероксидом водорода образуется триазин-2,4-дион (93) (схема 68) [113].
х = о, кон, 25°C, 5ч
X = S, NaOH, 25°C, 10 ми^
X = О 98%
X = S 99%
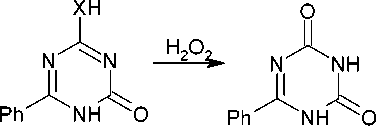
93,94 93
Схема 68. Циклоконденсация 1-бензоил-2-тиобиурета
В аналогичной реакции 3-ацил-2-метилизотиомочевина-1-карбоксамиды ( 95 ) при нагревании в метаноле циклизуются до соответствующих 4-(метилсульфанил)-1,3,5-триазин-2(1 Н )-онов ( 96 ) (схема 69) [40].
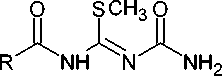
Me OH, 2^ 244 R = Ph 75%
R = p-Tol 60%
R = p-MeOTol 54%
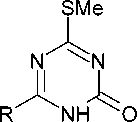
Схема 69. Циклоконденсация с образованием 4-(метилсульфанил)-1,3,5-триазин-2(1 Н )-онов
Среди аналогичных рассмотренным выше исходных соединений можно отметить, например, формилбиурет ( 97 ), который получают из амидиниевой соли биурета, а затем циклизуют в дигидрокситриазин ( 98 ) (схема 70) [114].
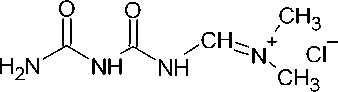
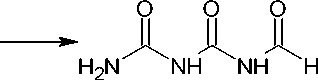
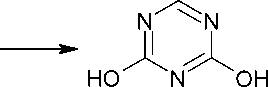
Схема 70. Получение дигидрокситриазина
N1,N2-Дикарбамоилформимидамид ( 99 ) количественно превращается в 1,3,5-триазин-
2,4(1H,3H)-дион (100) при нагревании до 175 °C. Циклизация также может быть достигнута с помощью этилата натрия в кипящем этаноле, однако выход продукта по такой методике существенно ниже и составляет 62 % (схема 71) [40].
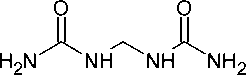
A: 175°C, 15ч
В: N aOEt, EtO^ А. 2ч
A: 100%
B: 62%
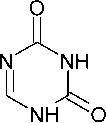
Схема 71. Превращение N1,N2-дикарбамоилформимидамида в 1,3,5-триазин-2,4(1 H ,3 H )-дион
Обработкой диарил имидодикарбонимидатов ( 101 ) (О,О-диарилизобиуретов, полученных взаимодействием арилцианатов с аммиаком) арилцианатами дает 4,6- бис (арилокси)-1,3,5-триазин-2-амины ( 102 ) с хорошим выходом (схема 72) [40].
NH NH
2 ArOCN NH3

ArO NH OAr
ArQCJS -ArOH
ArO
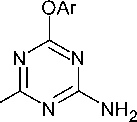
Схема 72. Взаимодействие диарил имидодикарбонимидатов с арилцианатами
Пути получения триазинтионов циклизацией дитиобиуретана с основанием получили меньшее распространение [40]. 1-Алкилиден-2,4-дитиобиуреты ( 103 ) при нагревании в водном гидроксиде натрия претерпевают циклизацию в 1-алкил/арил-6,6-диалкил-дигидро-l,3,5-триазин-2,4-дитионы ( 104 ) (схема 73).
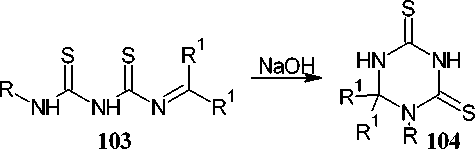
Схема 73. Синтез 1-алкил/арил-6,6-диалкил-дигидро-1,3,5-триазин-2,4-дитионов
Получить триазин-дитион можно исходя из дитиобирута ( 105 ) и ацетона. Так, взаимодействие дитиобиурета 105 с ацетоном в этаноле при барботировании HCl привело к образованию 6,6-диметил-1,3,5-триазин-2,4(1 H ,3 H )-дитиона ( 106 ) с выходом 88 %, который был выделен последовательным добавлением сначала избытка 1M NaOH и затем уксусной кислоты. Дальнейшее прикапывание пероксида водорода к дитиону 106 в 2,5М NaOH при 40-45 °C и последующем нагреве до 80 °C приводит к диметил-1,3,5-триазин-2,4(1 H ,3 H )-диону ( 107 ) с выходом 85 %, выделение дикетона осуществляют подкислением 2н серной кислотой (Схема 74) [108].
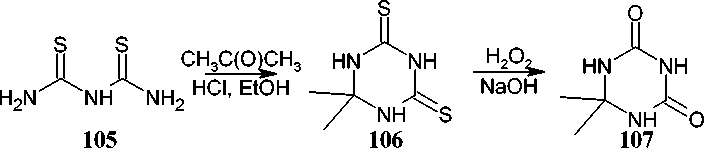
Схема 74. Взаимодействие дитиобиурета с ацетоном и перевод в форму дикетона
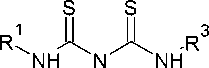
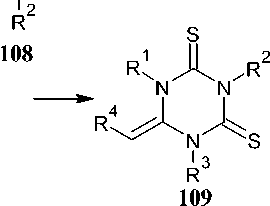
Реакция изотиоцианатов с 1,3,5-тризамещенным 2,4-дитиобиуретом (108) в присутствии порошкообразного гидроксида натрия или калия в полярном растворителе дала 1,3,5- тризамещенные 6-(алкилимино)-1,3,5-триазин-2,4-дитионы (109). Конденсация изотиоцианата не происходила в случае арильного заместителя у атома азота. Триазины 109 были чувствительны к присутствию кислоты и легко гидролизовались до 4,6-дитиоксотетрагидрол,3,5-триазин-2-онов (110) (схема 75) [40].
R4NCS MeCN
R1
Н3СГ 85-9?%
S
SS
NH N N NH
R2
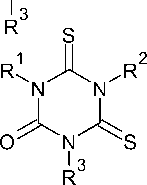
Схема 75. Получение 4,6-дитиоксотетрагидро-1,3,5-триазин-2-онов
Реакция бензоилацетилена с 1,5-дифенил-2,4-дитиобиуретом ( 111 ) в растворителях MeOH, C6H6 или MeCN протекает неселективно с образованием смеси продуктов (схема 76), таких как
2-(бензоилметил)-4,6-ди(фенилимино)дигидро-4 H -1,3,5-дитиазин ( 112 ), 2-(бензоилметил)-4-(бензоилвинил)сульфанил-3-фенил-6-(фенилимино)-3,6-дигидро-2 H -1,3,5-тиадиазин ( 113 ) и 2-(бензоилметил)-1,3-дифенилгексагидро-1,3,5-триазин-4,6-дитион ( 114 ) [115, 116]. Кипячение 1,3,5-дитиазина 108 приводит к увеличению содержания 1,3,5-триазина 114 .
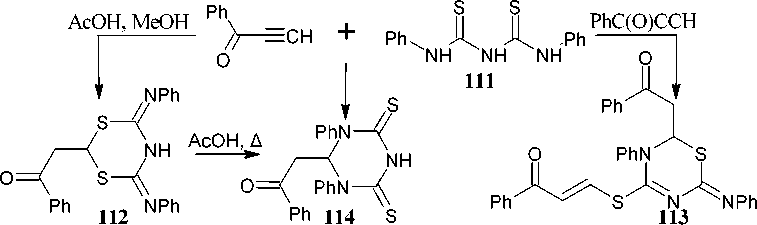
Схема 76. Реакция бензоилацетилена с 1,5-дифенил-2,4-дитиобиуретом
При кипячении бензальдегида с дитиобиуретом в ледяной уксусной кислоте был получен 6-фенилдигидро-1,3,5-триазин-2,4-дитиол ( 115 ), его окисление до 6-фенил-1,3,5-триазин-2,4-дитиола ( 116 ) проводили в среде 5%-ного гидроксида калия с гексацианоферратом (II) калия. Альтернативный путь получения соединения 116 состоит в циклизации 1-бензоилбиурета при действии щёлочи c дальнейшим замещением гидроксогрупп в 6-фенил-1,3,5-триазин-2,4-диоле 93 на группы -SH последовательной обработкой POCl 3 и KSH (схема 77) [117].
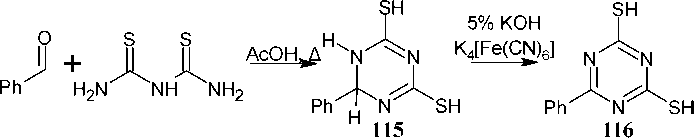
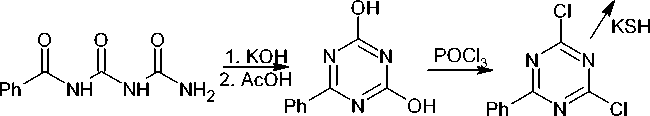
Схема 77. Получение 6-фенил-1,3,5-триазин-2,4-дитиола
В исследовании [118] ряд 1-R-(2 H )-4-(3-R1тиокарбамидо-1-ил)-6-(2-имино-4-тио-5-R1биурето-1-ил)-1,2-дигидро- s -триазин-2-тионов ( 117 ) был получен путем изомеризации 2-(2-имино-4-тио-5-R1биурето-1-ил)-4-(3-R-тиокарбамидо-1-ил)-6-R-имино-1,3,5-тиадиазина ( 118 ) в присутствии этанольного раствора бикарбоната натрия (схема 78). Производные тиадиазина 118 были синтезированы взаимодействием 1,3- бис -(N-фениламидинотиокарбамидо) тиокарбамида ( 119 ) и арил/алкилизоцианодихлоридов. Все синтезированные s -триазины были проверены на антимикробную активность в отношении грамположительных и грамотрицательных бактериальных организмов, а именно: S. aureus, B. subtilis, A. aerogenes, E. coli и S. typhi [118].
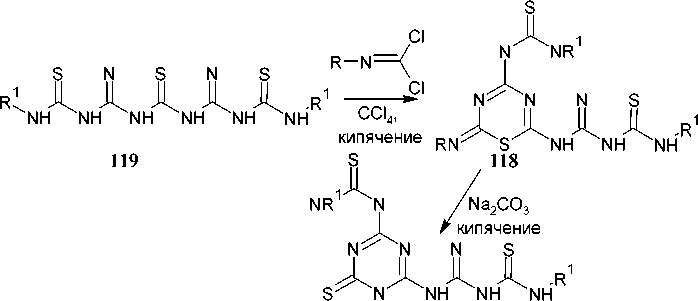
R 117
Схема 78. С-интез замещённого 1,3,5-триазин-2-тиона
Таким образом, различные синтезы на основе мочевины, тиомочевины и их производных являются практичными и эффективными для получения различных 1,3,5-триазинонов и -тионов. Выходы продуктов при этом достаточно высоки, а исходные вещества – доступны, осуществление синтезов не требует особых условий их проведения.
-
1.3. Синтезы на основе амидинов
Амидины являются полезными исходными материалами для синтеза диалкил- и диарилзамещенных 1,3,5-триазинов, поскольку они могут создавать как N-C-N, так и N-C-фрагмент. Синтез 2-гидрокси-4,6-диарил- s -триазинов ( 120 ) из двух молей ариламидина и одного моля фосгена был описан Пиннером и соавторами более века назад. На первом этапе этой реакции образуется N,N'- бис -имидилмочевина ( 121 ), которая при нагревании выше своей точки плавления подвергается замыканию цикла в желаемый гидрокси- s -триазин с выделением аммиака (схема 79) [119, 120].
OH
Ar
O
Ar O Ar
\ A -2 HCI А л A NH Cl Cl HN NH NH NH
NN
Схема 79. Синтез Пиннера
Ar N Ar
Этот метод также использовался для получения различных 4,6- бис (хлоралкил)-замещенных 1,3,5-триазин-2(1 H )онов ( 122 ) (схема 80) [40] Из-за своей кислотности полученные триазиноны кристаллизуются в виде солей 1:1 с амидиновым реагентом.
/R 0
NH СГ С1
NaOH, H2O, толуол, 5-10 ° C
R = CCl 3 – 75 %; R = CHCl 2 – 40 %; R = CH 3 Cl – 63 %
Схема 80. Синтез 4,6- бис (хлоралкил)-замещенных 1,3,5-триазин-2(1 H )онов
Такой синтез на основе амидинов хотя и может считаться простым и дающим удовлетворительные выходы продуктов, однако при своем проведении требует особой техники безопасности, поскольку тот же фосген является крайне активным газообразным ядовитым веществом.
-
1,3,5- Триазин-2(1 H )-оны ( 123 ) с двумя различными заместителями в 4-ом и 6-ом положениях получены с высоким выходом из реакции N-(1-хлоралкилиден)карбамоилхлоридов с амидинами в присутствии щелочи [40]. При использовании тиомочевины в качестве фрагмента N-C-N в реакции с N-(1-хлорбензил)бензимидоилхлоридом образуется соответствующий 3,4-дигидро-1,3,5-триазин-2(1 H )-тион 123 (схема 81).
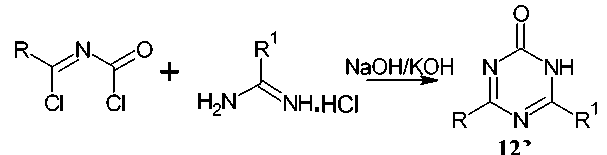
NaOH/KOH N NH
Cl Cl
R = Ph, CCl 3 ;
R1 = Me, SMe, Ph, Bn
Схема 81. Реакция N-(1-хлоралкилиден)карбамоилхлоридов с амидинами
Реакция N-ацилтиоамидов или N-(этоксикарбонил)тиоамидов с различными амидинами позволяет получать 1,3,5-триазины с двумя или тремя различными заместителями. Таким образом, N-(этоксикарбонил)тиоамиды реагируют с гидрохлоридом бензимидамида или хлоридом S-бензилизотиоурония в присутствии алкоголята натрия с получением дизамещенных 1,3,5-триазин-2(1 H )-онов ( 124 ) (схема 82) [121].
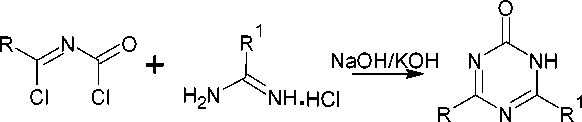
R = 4-Tol, 4-ClC 6 H 4 , 1 H -пиррол-2-ил; R1 = Ph, SBn
Схема 82. Синтез дизамещенных 1,3,5-триазин-2(1 H )-онов
Данный метод синтеза также может приводить к синтезу 1,3,5-триазин-2,4-дионов. Реакция дифенилимидодикарбоната ( 125 ) с N1- трет -бутилбензимидамидами дает 6-арил-1,3,5-триазин-2,4(1 H ,2 H) -дионы ( 126 ) при 120-130 °C почти с количественным выходом [122]. Предполагается, что трет -бутильная группа отщепляется в виде изобутена в ходе реакции (схема 83).
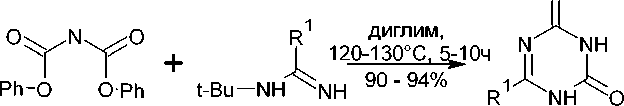
125 126
R1 = Ph, 4-Tol, 4-BrC 6 H 4 Схема 83. Реакция дифенилимидодикарбоната с N1- трет -бутилбензимидамидами
Аналогичным образом были получены производные триазин-2,4-диона 126, содержащие в своей структуре остатки а-аминокислот. Для этого раствор дифенилимидодикарбоната 125 перемешивали с различными имидамидами в дихлорметане при комнатной температуре с добавлением диазабициклоундецена, что привело к образованию соответствующих 6-замещённых-1,3,5- триазин-2,4-дитионов 126 с выходами 62–67 % (схема 84) [123].
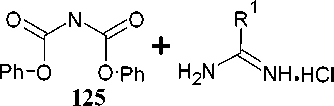
ДБУ, СН2С12 25 °C, 2ч
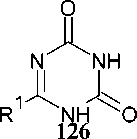
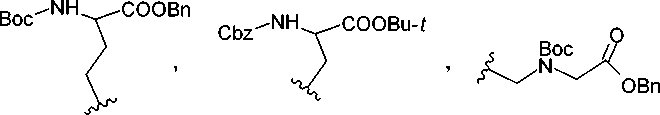
Схема 84. Синтез замещённых 1,3,5-триазин-2,4-дионов
Удобным способом получения s -триазинонов и тионов является синтез из амидинов и изо(тио)цианатов. Взаимодействие гликозил изотиоцианата с фармамидином или ацетоамидином в ацетонитриле приводит к замещённым амидинотиомочевинам ( 127 ) (ранее нами уже были рассмотрены способы синтеза триазинов из гуанидинотиомочевин и ортоформиата (схема 54) и другие способы получения триазинов из гуанилмочевиновых систем, что представлено на схемах 49–59). Амидинотиомочевины также реагируя с этил ортоформиатом образуют соответствующие 1,3,5-триазин-2-тионы ( 128 ) (схема 85) [124].
R1
R1 R1 S
N^ N
S^ N
128 R
rncs+ x w ЛА H®
R = гликозил; R1 = H, Me
Схема 85. Образование триазин-2-тионов из амидинов и изотиоцианатов
Исследован ряд структурно разнообразных изотиоцианатов и ариламидинов в синтезе новых 6-ариламино-1,3,5-триазин-2(1H)-тионов (129) с хорошими выходами. Для их получения изотио- цианаты нагревают при 80 °C с арил(гетарил)амидинами в присутствии NaOH в ДМФА, подвергая микроволновому облучению в течение 15–25 минут (схема 86) [125].
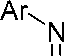
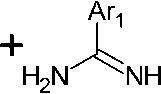
NaOH Д МФА, 80 °C MW*
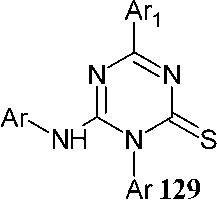
Схема 86. Домино [3+2+1] гетероциклизация
Структуры полученных соединений 129 установлены с использованием спектральных методов анализа и в случае двух триазинов с помощью РСА (рис. 12) [125].
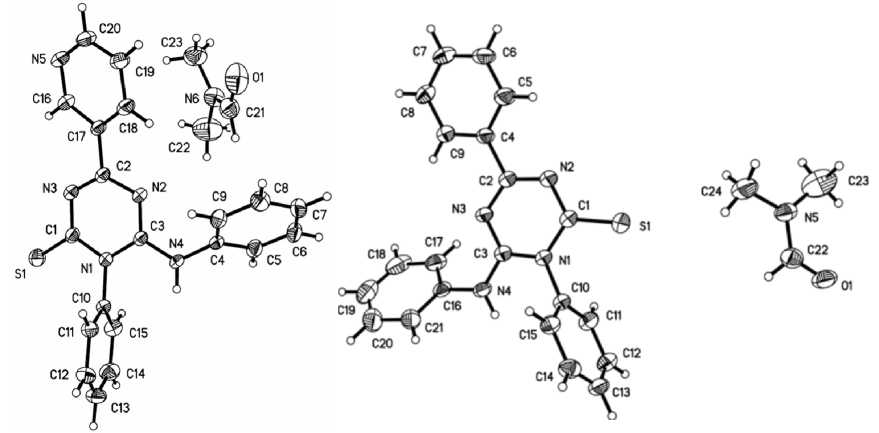
Рис. 12. Структуры соединений 129 по данным РСА
Взаимодействие ароилизо(тио)цианатов ( 130 ) или ацилизо(тио)цианатов 130 с ал-кил/ариламидинами используется для получения несимметрично замещённых триазинов. Данный метод прост в исполнении и позволяет получать триазин-2-оны высокой чистоты с хорошими и отличными выходами [126–128]. Кроме того, исходные ароил/алкилизоцианаты 130 могут быть получены при взаимодействии амидов с оксалил хлоридом (COCl 2 ), далее они не подвергаются выделению из реакционной смеси и происходит дальнейшая конденсация до 4,6-дизамещённых-1,3,5-триазин-2-онов ( 131 ) (схема 87) [128].
Ri о R<1
П с^Х । I раст ворител ь, △ n^^N
R^N^ H^^NHI
~ R NH^X
R, R 1 = Alk, Ar, HetAr
Схема 87. Конденсация амидинов с изо(тио)цианатами
Для некоторых полученных триазинов 131 удалось установить строение методом рентгеноструктурного анализа монокристального образца, общий вид молекул представлен на рис. 13, эллипсоиды тепловых колебаний атомов показаны на уровне 50 % вероятности [128].
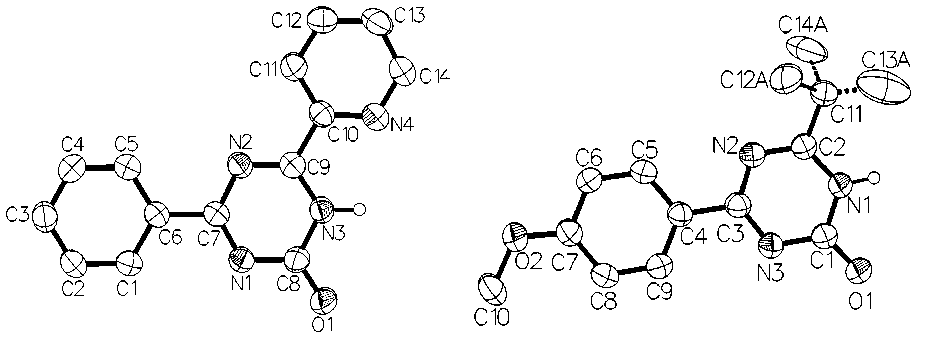
Рис. 13. Общий вид молекул 131 по данным РСА
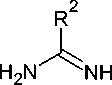
1,3,5-Триазин-2(1H)-тионы 131 с хорошим выходом могут быть получены циклоконденсаци- ей ароил- или этоксикарбонилизотиоцианатов 130 не только с амидинами, но и с изо(тио)моче-винами или гуанидинами (схема 88) [40]. Добавление гидроксида натрия к двухфазной реакци- онной смеси генерирует свободное основание из соли амидиния и катализирует циклизацию. N-Арилимидоилизотиоцианаты подвергаются той же реакции в аналогичных условиях, что и ацилизотиоцианаты. Однако, использование другой уходящей группы не имеет преимуществ.
O
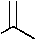
R NCS
NaOH, H2O бенздр 25 °C 1ч
R
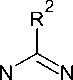
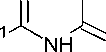
R1 = Ph, 4-MeOC 6 H 4 , 4-NO 2 C 6 H 4 , OEt;
R2 = Me, Bn, OMe, SMe, SEt, NMe 2 , OPh, OBn
Схема 88. Циклоконденсация ароил- или этоксикарбонилизотиоцианатов с амидинами
Вышеописанный метод сборки триазинового цикла удобен, в частности тем, что целевые несимметрично замещённые триазины могут быть получены двумя путями. Так бензоилизоцианат при циклизации с различными гидрохлоридами амидина и затем одностадийным хлорированием образует 2-хлор-4-R 1 -6-R 2 -1,3,5-триазин ( 132 ). Альтернативно, те же соединений 132 были получены циклизацией различных замещенных диизоцианатов с гидрохлоридом бензамидина и затем одностадийным хлорированием (схема 89) [129].
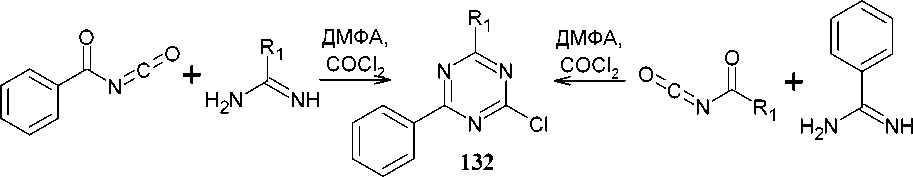
Схема 89. Синтез различных замещённых триазинов 132
Независимо от природы заместителя амидина, реакции этоксикарбонилизотиоцианата 130 с 1-ним эквивалентом амидинов в присутствии 2 М NaOH протекали с образованием целевых 6-R-4-тиоксо-3,4-дигидро-1,3,5-триазин-2(1 H )-онов ( 133 ) с хорошими выходами в толуоле или бензоле при комнатной температуре (схема 90) [130–131].
R
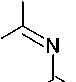
О R бензол/ толуол HN NaOH J
д + Д
ЕЮ N^ HNZ NH3CI
Oz 'NH 4S
130 133
Схема 90. Реакция этоксикарбонилизотиоцианата с амидинами
При реакции цианодитиоимидокарбонатов ( 134 ) с производными амидина образуются S-метилзамещенные 1,3,5-триазин-2-амины ( 135 ). Когда диметилцианодитиоимидокарбонат 134 реагирует с замещенными бензимидамидами или гидрохлоридами 2-бензилизотиомочевины в присутствии N,N-диизопропилэтиламина, соответствующие 4-(метилсульфанил)-1,3,5-триазин-2-амины 135 получаются с хорошим выходом [40]. Соли 2-метилизотиомочевины и тиобисформи-мидамида подвергаются той же реакции с диметилцианодитиоимидокарбонатом 134 с образованием соответствующих триазинов 135 в присутствии разных оснований. Когда в дитиоимидокар-бонате одна из двух метилсульфанильных групп заменяется цианоаминогруппой, а нитрильная функциональная группа преобразуется в сложный эфир, соответствующие 1,3,5-триазины получаются с умеренным выходом (схема 91) [40].
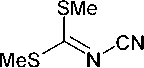
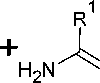
основание ,
-MeSH
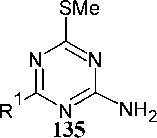
Схема 91. Синтез S-метилзамещенных 1,3,5-триазин-2-аминов
Аналогично цианодитиоимидокарбонатам 134 диметилацилдитиоимидокарбонаты ( 136 ), как фрагмент C—N—C, реагируют с производными амидина с образованием 2-(метилсульфанил)-
Необычным способом синтеза диарилзамещенного-1,3,5-триазинона ( 138 ) является реакция термолиза 3-фенил-1,2,4-оксадиазол-5-ил-метилгидразинов ( 139 ) [132]. Термическое превращение соединений 139 можно объяснить так, как показано на схеме 93. Первой стадией процесса, по-видимому, является разрыв N-О связи в исходных циклических соединениях, который протекает даже при комнатной температуре.
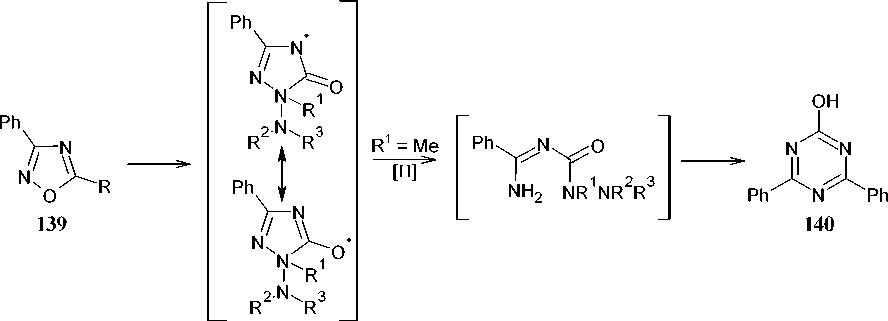
R = NMeNH 2 , NMeNHMe, NMeNMe 2
Схема 93. Термическое разложение 3-фенил-1,2,4-оксадиазол-5-ил-метилгидразинов
1,3,5-триазинов ( 137 ) с умеренным выходом (схема 92) [40].
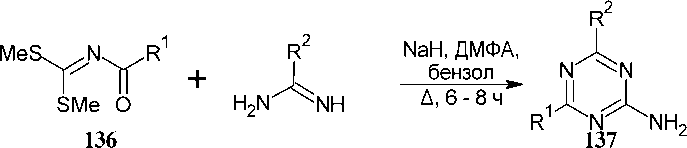
Схема 92. образование 2-(метилсульфанил)-1,3,5-триазинов
Триазадиеновые иодиды ( 141 ) содержат амидиновый фрагмент и также, как аналогичные гуанил(тио)мочевины (см. схемы 50–60), являются эффективными промежуточными продуктами в гетероциклическом синтезе. Они реагируют с фенилизоцианатом, давая соответствующие триазиноны ( 142 ) или триазинтионы ( 143 ) (схема 94) [133].
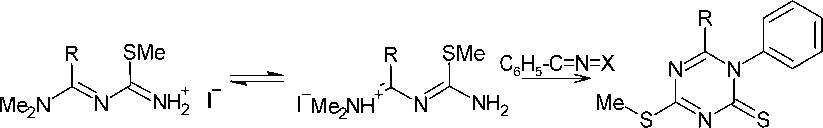
142 X = О
143 X = S
Схема 94. Триазадиеновые иодиды в синтезе триазинонов(тионов)
Схожим образом замещённые триазинтионы могут быть получены из производных амидинотиомочевины. Так, региоселективная гетероциклизация производного амидинотиомочевины ( 144 ) с метилатом натрия дала дигидротриазинтион ( 145 ). Если заместитель R был отличен от водорода, то образовывались тиадиазины (схема 95) [40].
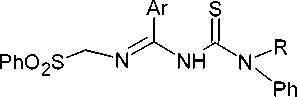
NaOI\^e R = H
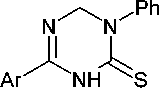
144 145
Ar = Ph, 4-MeC 6 H 4
Схема 95. Получение дигидротриазинтиона
1,3,5-Триазин-4,6-дитион-2-амин ( 146 ) или его S-калиевое ( 147 ) и S-метил производное ( 148 ) может быть получено из N-цианоформамидинодитиокарбимата калия при его кипячении в метаноле с последующим подкислением или реакцией с метилирующим агентом для выделения S-метильного производного 148 (схема 96) [134].
K2[S2C=NC(NH2)=NCN]
CH3OH, △
-коснз
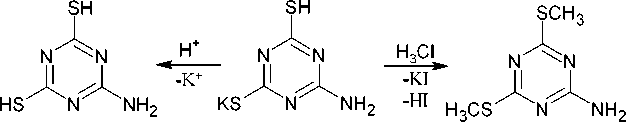
147 146 148
Схема 96. Синтез триазин-дитиона и его производных
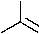
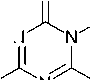
Диметил N-(N -цианоамидино)карбонимидодитиоат ( 149 ) при взаимодействии с аминами в ацетоне или диоксане при температуре ниже комнатной образуются промежуточные N-R-N1-(N -цианоамидино)-S-метилизотиомочевины ( 150 ), которые при нагревании до 30 °C циклизуются в соответствующие 2-метилсульфанил-1,3,5-триазины ( 151 ) (схема 97) [135].
SMe NH 2
MeS N
N
NHR NH 2
MeS N N
NH
N зо °с
H 2 N N SMe
Схема 97. Получение 2-метилсульфанил-1,3,5-триазина
Подводя небольшой итог, можно отметить, что амидины и их производные являются удобным исходным соединением для синтеза ди- и тризамещённых 1,3,5-триазинов, содержащих различные алкильные и арильные заместители в положениях 4,6 или 2,4,6. Однако, для введения оксо или тиок-согруппы необходимо использовать дополнительные реагенты, содержащие данные функции.
-
1.4. Синтезы на основе производных гуанидина
Для получения амино-замещенных 1,3,5-триазинонов(тионов) используют не мочевины (тиомочевины) и их производные, а производные гуанидина. Известно несколько подходов к синтезу 4(6)-амино-1,3,5-триазин-2-онов и 2-тионов из производных гуанидина. Приведем ниже некоторые из них.
Во-первых, реакция замещённых гуанидинов с ароилизотиоцианатами 130 аналогично реакциям амидинов с ароилизотиоцианатами (см. схемы 87–90) приводит к образованию соответствующих 1,3,5-триазин-2-тионов ( 152 ), замена амидинов на гуанидин приводит к появлению амино- или диалкиламиногруппы в 4-ом положении триазина-2-тиона (схема 98) [126, 127 ,136].
S
O
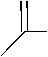
NH
N NH
Ar N X
N C S H2N X
Ar
X = NH 2 , NR 2
Схема 98. Синтез 4-амино/диалкиламино-1,3,5-триазин-2-тиона
Во-вторых, получить N2,N2-диметил-6-метилсульфанил-1,3,5-триазин-2,4-диамин ( 153 ) можно обработкой сульфата N,N-диметиламиногуанидина ( 154 ) диметил-N-цианодитиоимино-карбонатом в присутствии карбоната калия при кипячении (схема 99) [137].
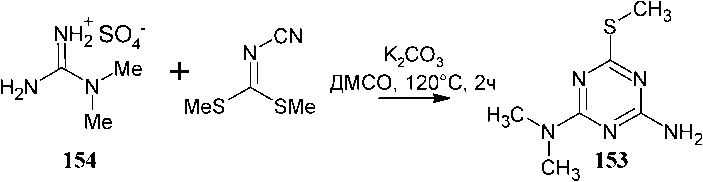
Схема 99. Получение N2,N2-диметил-6-метилсульфанил-1,3,5-триазин-2,4-диамина
В-третьих, известен ряд реакций с использованием гуанидиннитрилов, приводящих к формированию триазинового цикла. Так гуанидин-1-карбонитрил реагирует с метилтрифторацетатом после активации метоксидом натрия и хлоридом цинка(II) с образованием 4-метокси-6-(трифторметил)-1,3,5-триазин-2-амина ( 155 ) с высоким выходом (схема 100) [40].
NaOMe, ZnCI2 (cat.)
MeOH, 50 °C, 8 h
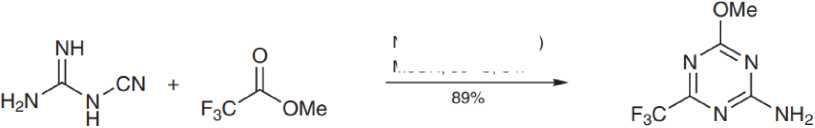
Схема 100. Реакция гуанидин-1-карбонитрила с метилтрифторацетатом
Схожим образом гуанидин-1-карбонитрил подвергается конденсации с мочевиной в мольном соотношении 1:1 тигельным методом без растворителя, что приводит к замыканию 1,3,5-триазинового цикла с высоким выходом и чистотой (схема 101). Очистку полученного 4,6-диамино-1,3,5-триазин-2-она (аммелина, 156 ) проводят перекристаллизацией из водного раствора Na 2 CO 3 . Монокристаллы, пригодные для РСА, были получены медленным испарением раствора соединения 156 в водном NH 3 (25 мас. %) [138].
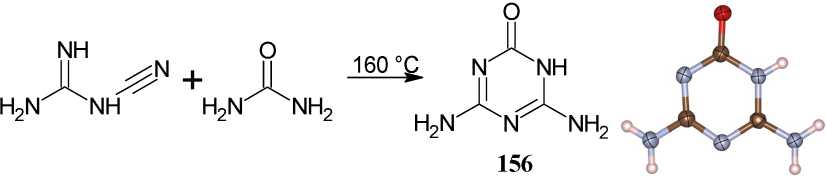
Схема 101. Образование аммелина
Реакции 1,2-дицианогуанидиновых солей с концентрированными галогенводородами приводит к гидрогалогенидам диамино-1,3,5-триазин-4-она ( 156 ) с высокими выходами >95 % (схема 102) [40].
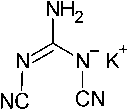
H2O, HX 6QJ0^C, 15 мин
H2N
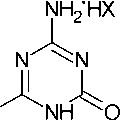
X = Cl, Br
Схема 102. Взаимодействие 1,2- дицианогуанидиновых солей с конц. галогенводородами
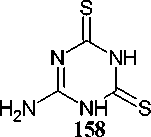
Калиевая соль гуанидин-1,2-дикарбонитрила в водном растворе реагирует с сероводородом в автоклаве при повышенных температурах, образуя смесь 4,6-диамино1,3,5-триазин-2(1 H )-тиона ( 157 ) и 6-амино-1,3,5-триазин-2,4(1 H ,2 H )-дитиона ( 158 ) в равных количествах, которая легко разделяется, поскольку дитиоаммелид калия хорошо растворим в кипящей воде, а тиоам-мелин остаётся нерастворённым (схема 103) [40].
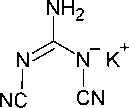
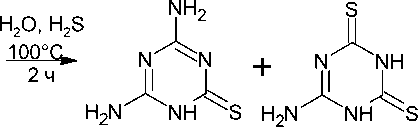
157 158
Схема 103. Реакция соли гуанидин-1,2-дикарбонитрила с сероводородом
Аналогичное соединение 157 можно получить при конденсации дициандиамида с изотиоцианатом в ацетоне в присутствии щёлочи (схема 104) [96].
NH
NH NH
-CN
RNCS ацетон
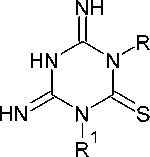
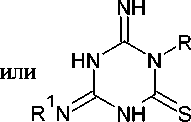
R = Me, Et, Ar; R1 = H, Ph
Схема 104. Конденсация дициандиамида с изотиоцианатом
Цианозамещенный дитиоимидокарбонат дикалия (159) можно считать формальным тиоаналогом 3-ацилгуанидин-1-карбонитрила. Его циклизация в нейтральных или щелочных условиях [40] приводит к 6-амино-1,3,5-триазин-2,4(1H,3H)-дитиону (158) с выходом 63 % после подкисления (схема 105).
NH
JI 1)МеОНДили
NH N Na OH. H^ O, Д
NC 2) H+ , H2O
KS SK
Схема 105. Циклизация цианозамещенного дитиоимидокарбонат дикалия
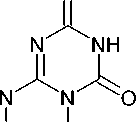
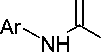
Получить аналогичный триазиндитиону 158 6-амино-1,3,5-триазин-2,4-дион ( 160 ) можно взаимодействием 1,3-замещённого гуанидина с хлоркарбонилизоцианатом в ТГФ при взбалтывании в течение 2 часов (схема 106) [139].
О
NH CIC(O)NCO
ТГФ, 2 ч
Ri Rn Ar 160
R1, R2 = Alk, Bn; R1 = R2 = циклический амин
Схема 106. Получение 6-амино-1,3,5-триазин-2,4-диона
1-Ацилгуанидины образуют N-C-N-C фрагмент в реакции с нитрилами с образованием 1,3,5-триазинов. По этой реакции различные 1,3,5-триазин-2-амины ( 161 ) с различными заместителями в 4 - и 6-положениях получаются с хорошим выходом (схема 107) [40].
О NH JI + MeSCN
Ri NH NH2
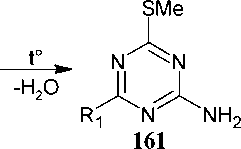
Схема 107. Ацилгуанидины в реакции с нитрилами
Реакция N-карбамимидоил-2-формамидоацетамида с двумя эквивалентами трихлорацетонитрилом в ДМФА приводит к образованию 6-трихлорметил-1,3,5-триазин-4-амина ( 162 ), который после гидролиза переходит в 4-амино-6-[(формиламино)метил]-1 H -[1,3,5]триазин-2-он ( 163 ) (схема 108) [140].
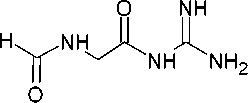
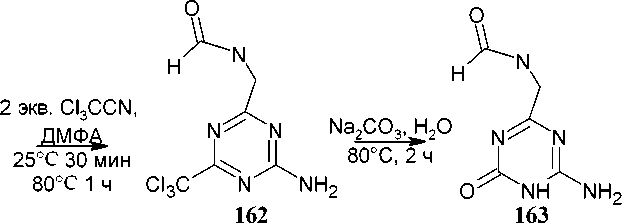
Схема 108. Образование триазинона 163
Молекулярная перегруппировка ацилдициандиамидов, содержащих в своей структуре фрагмент амидина NH 2 -C=NR, при нагревании приводит к 2-замещенным-4-гидрокси-6-амино- s -триазинам ( 164 ). Нагревание само по себе вызывает данную перегруппировку, но соли аминов могут катализировать данную реакцию [112]. Важно отметить, что добавление сероводорода к ацилдициандиамидам приводит к соответствующим ацилгуанилтиомочевинам. Однако, последние, в свою очередь, при обработке едким натром превращаются в гуанид, а не в ожидаемый тио-гуазид, поэтому подобный способ не удаётся использовать для синтеза 2-замещенных-6-амино- s -триазин-4-тиолов (схема 109).
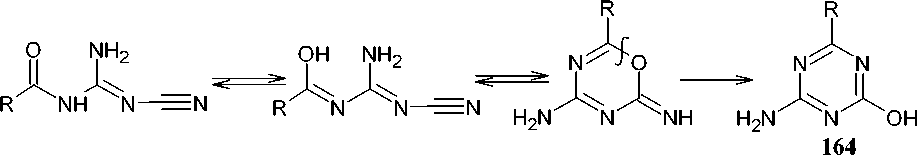
Схема 109. Молекулярная перегруппировка ацилдициандиамидов
Исходные соединения были получены путем нагревания дициандиамида, в отсутствие основания с ацилхлоридом в высококипящем растворителе, таким как хлорбензол.
4-Амино-1,3,5-триазин2(1 H )-оны ( 165 ) легко образуются при циклизации 3-ацилгуанидин-1-карбоксамидов ( 166 ) при обработке основанием. 3-Ацилгуанидин-1-карбоксамиды 166 являются изолируемыми промежуточными продуктами в реакции замыкания кольца 3-ацилгуанидин-1-карбонитрилов ( 167 ) и образуются путем присоединения воды к цианогруппе (схема 110) [40].
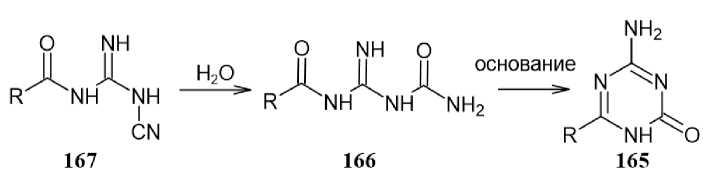
Схема 110. Циклизация 3-ацилгуанидин-1-карбоксамидов
Ацилдициандиамиды также можно гидролизовать кислотами до ацилгуанилмочевины 166 . Эквивалент щелочи или избыток аммиака осаждают менее растворимое свободное основание ( 168 ), которое также можно циклизовать до 2-замещенного 4-гидрокси-6-амино- s -триазина 164 путем обработки раствора вторым эквивалентом щелочи с последующим подкислением (схема 111) [112].
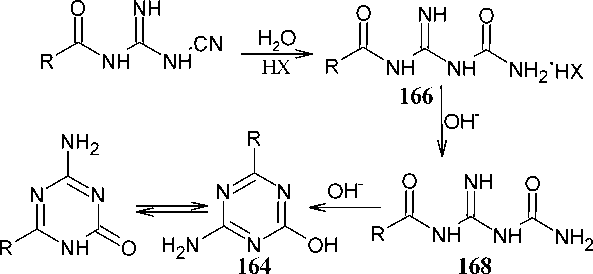
Схема 111. Получение 2-замещенного 4-гидрокси-6-амино- s -триазина 164 из ацилдициандиамидов
Также удобным прекурсором для синтеза триазинов является гуанилмочевина и её производ- ные. Например, 6-замещенные 4-амино-1,3,5-триазин-2(1H)-оны 165 получают путем циклоконденсации гидрохлорида N-карбамоилгуанидина с ортоэфиром в ДМФА при 100 °C (схема 112).
Триазиноны 165 также доступны (51–93 %) из бигуанидов и диэтилазодикарбоксилата с улучше- нием выхода по сравнению с использованием этиленкарбоната (47 %) [39].
h2n
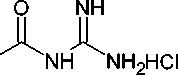
R(COR1)3, ДМФА
R
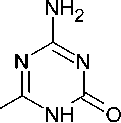
Схема 112. Циклоконденсация гидрохлорида N-карбамоилгуанидина с ортоэфиром
Использование ацилцианогуанидинов способствует введению разнообразия в 4(6)-положение, но не позволяет одновременно вводить заместитель в аминогруппу. Удобным методом синтеза 1,3,5-триазинонов, который позволяет вводить различные заместители по аминогруппам, что невозможно или ограничено также и при прямых реакциях, например, с цианогуанидинами, является циклизация соединений (169) при кипячении в присутствии гексаметилдисилазана (ГМДС). Предлагаемый авторами [104] метод не требует строгого контроля условий реакции по сравнению с методами конденсации, например, цианурового хлорида с аминами, а желаемые конечные продукты (170) образуются с высоким выходом (схема 113).
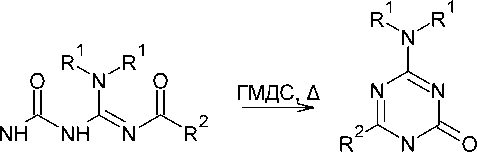
169 170 ph
R1 = Et, All, (CH 2 ) 2 O(CH 2 ) 2 ; R2 = Et, Ar, HetAr
Схема 113. Циклизация соединений 169
S-Бензильное производное ацилгуанилмочевины (171) циклизуется в пиридине до триази- на (172) (схема 114) [39].
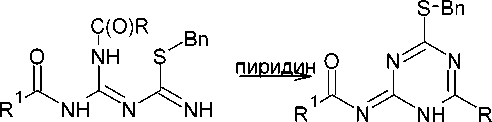
Схема 114. Получение бензилсульфанил-1,3,5-триазина 172
N-карбамимидоил(трихлор)этанимидамид (173) также может быть использован в синтезе симм-триазинов. Взаимодействие 173 с аминокислотой в присутствии 1,3-дициклогексил-карбодиимида (DCC) и N-гидроксисукцинимида (N-Hosu) приводит к образованию трихлорме- тил-1,3,5-триазина (174), который переводят с 75%-ным выходом в триазинон (175) щелочным гидролизом (схема 115) [123].
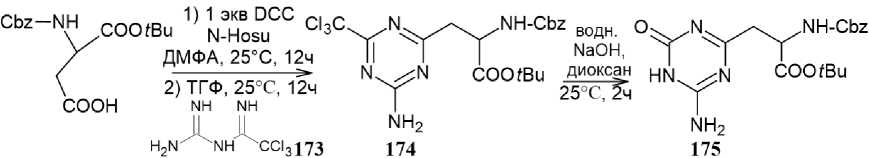
Схема 115. Синтез триазинона 175
В качестве пятиатомных фрагментов для построения 1,3,5-триазинового цикла могут выступать бигуаниды. γ-Бутиролактам и этилхлордитиоформиат используются в качестве одноатомных фрагментов для введения аминопропильной и меркаптогрупп в 1,3,5-триазиновое кольцо соответственно (схема 116) [39].
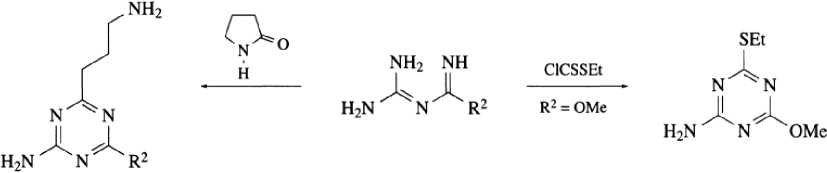
Схема 116. Использование бигуанида в синтезе триазинов
Конденсация 1-арилбигуанидов с изотиоцианатами приводит к различным 1,3,5-триазин-2- тионам в зависимости от условий реакции (Схема 117). Так при проведении реакции в ДМФА при 15 °С был получен 3-NR1-триазинтион (176), а в пиридине при 100 °С 6-NR1- триазинтион (177) [96].
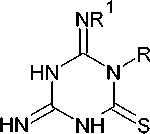
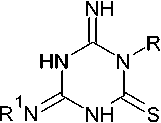
J^NCS
ДМФА, 15°C
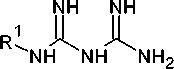
RNC£ пиридин 15 °C
R = Me, Et, Ar; R1 = H, Ph
Схема 117. Взаимодействие бигуанида с изотиоцианатом
При циклизации Boc-гуанида ( 178 ), полученного реакцией между Boc-защищённым гуанидином и диметилцианамидом при нагревании при 90 °C в течение 6 часов наблюдается образование 4-амино-6-диметиламино[1,3,5]триазин-2-ола ( 179 ) (схема 118) [141].
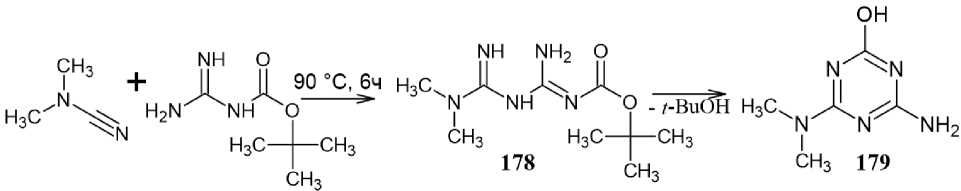
Схема 118. Циклизация Boc-бигуанида
Таким образом, гуанидины, бигуаниды и их производные могут быть использованы для синтеза триазинонов(тионов), дополнительно содержащих в своей структуре одну или две аминогруппы, в отличие от методов синтеза, описанных в разделах 1.1–1.3.
-
1.5. Синтез на основе изо(тио)цианатов
Следующими немаловажными исходными соединениями, подходящими для сборки симм-триазинонов(тионов) являются изо(тио)цианаты. На данный момент довольно подробно изучена одна из наиболее характерных реакций для данных соединений – их тримеризация с образовани- ем различных триазинов.
Авторы [142] подробно представили историю исследования самоконденсации фенилизоцианата с получением тримера, которая известна достаточно давно (Saunders & Slocombe, 1948). Так, реакция мономера с образованием циклического тримера катализируется комплексными гидратами металлов (Ellzey & Mack, 1963), третичными аминами (Beitchman, 1966) и N-метилморфолином (Kogan, 1956). В 1960 Shashoua, Sweeny & Tietz сообщили о самоконденсации мономера в полимер при низких температурах (195 К) и в тример при высоких температурах (398 К) с помощью анионных катализаторов. В исследованиях Natta, DiPietro & Cambini (1962) сообщается, что при низкой температуре с использованием металлоорганических катализаторов можно получить высококристаллический полимер. В работе [142] показано, что трифенил-1,3,5-триазинтрион ( 180 ) может быть получен с высоким выходом при низкой температуре с подходящей концентрацией катализатора (схема 119).
О
Ph^ /Ph
„ кат. N N
3 PhN=C=O ----► I I
О N
Ph
Схема 119. Тримеризация фенизизоцианата
Установлено [143], что соединение 180 , кристаллизуется в двух полиморфных формах. В ромбическом полиморфе (I), в пространственной группе Fdd 2 с Zʹ = 1, молекулы лежат в общих положениях, в то время как в моноклинном полиморфе (II), в пространственной группе C 2/ c с Zʹ = 1. В каждом полиморфе молекулы связаны водородной связью C-H…π(арен), образуя цепочки в полиморфе (I) и слои в полиморфе (II).
Ряд N-гетероциклических карбенов (NHC) [144] был оценен в качестве потенциальных катализаторов для циклотримеризации изоцианатов с получением изоциануратов ( 181 ). Было обнаружено, что 1,3- бис -(2,6-диизопропилфенил)-4,5-дигидроимидазол-2-илиден (SIPr) является высокоэффективным катализатором для циклотримеризации различных изоцианатов (схема 120).
О
„ SIPr N N
3 RN-C-0 ТГфУ25°^ 1ч J
R
R = All, Ph, o- Me-C 6 H 4 , p -MeO-C 6 H 4 , (-CH 2 -) 5 CH
Схема 120. Тримеризация изоцианатов в присутствии SIPr
Использованные в исследовании N-гетероциклические карбены приведены на рис. 14.
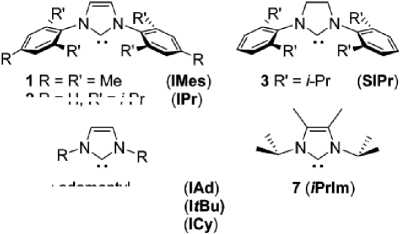
2 R = H. R' = /-Pr
4 R = adamantyi
5 R = f-Butyl
6 R = cyclohexyl
Рис. 14. N-гетероциклические карбены
Необычные циклические тетрасульфидные комплексы олова
{(CyNC(R)NCy)[N(SiMe3)2]}SnS4 (Cy = циклогексил; R = Me, tBu) являются превосходными катализаторами циклотримеризации арилизоцианатов в пергидро-1,3,5-триазин-2,4,6-трионы (изоцианураты, 182) при комнатной температуре (схема 121) [145].
3 ArN=C=O
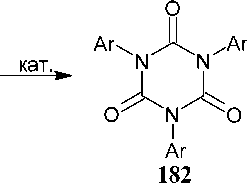
Ar = Ph, p -MeOC 6 H 4
Схема 121. Тримеризация изоцианатов
Смешанные амидинато-амидокомплексы [Me 3 SiNC( t Bu)NSiMe 3 ]M[N(SiMe 3 ) 2 ] (M = Sn, Ge) заявлены как отличные катализаторы циклотримеризации фенилизоцианатов в пергидро-1,3,5-триазин-2,4,6-трионы (изоцианураты) при комнатной температуре [146].
Было обнаружено, что при нагревании фенилизоцианата с 2 мол. % п -толуолсульфината натрия при 140 °C 1,3,5-трифенил-1,3,5-триазин-2,4,6(1 H ,3 H ,5 H )-трион (трифенилизоцианурат) появляется в виде белого осадка через 12 мин с выходом 90 %. Арил- и алкилизоцианаты были эффективно преобразованы в симметричные трехзамещенные арил- и алкилизоцианураты ( 183 ), катализируемые пара -толуолсульфинатом натрия как таковым или в присутствии тетрабутиламмониййодида (TBAI), в условиях, не содержащих растворителей. Было показано, что последний обладает более высокой каталитической активностью [147]. Процесс тримеризации происходит путем первоначальной атаки п -толуолсульфината натрия ( 184 ) на первую молекулу изоцианата, за которой следуют атаки полученных промежуточных продуктов на две молекулы изоцианата, что приводит к образованию изоцианурата, поскольку структура 184 восстанавливается (Схема 122).
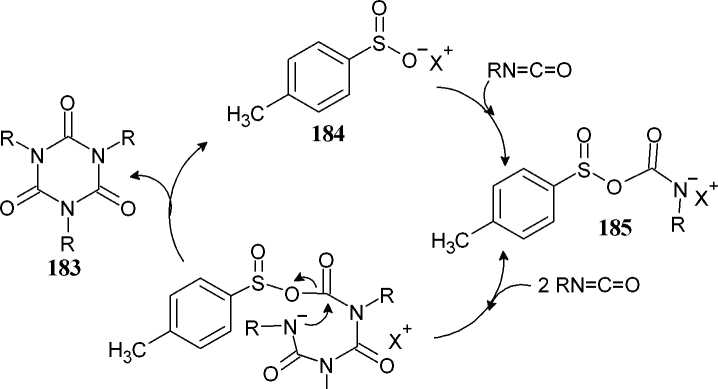
R
X+ = Na+, Bu 4 N+
Схема 122. Тримеризация изоцианатов при катализе пара -толуолсульфинатом
Карбоксилаты, аналогично вышеописанному тиосульфинату, обладают каталитической способностью по отношению к реакциям тремирезации изоцианатов, они также являются наиболее часто используемыми катализаторами в промышленном получении полиуретанов. Авторы [148] считают, что карбоксилаты являются лишь прекатализаторами в этой реакции. Реакция карбоксилатов с избытком ароматических изоцианатов приводит к необратимому образованию соответствующих депротонированных амидных соединений (аналогичных соединению 185 на схеме 121), обладающих сильными нуклеофильными и основными свойствами. В результате они являются активными катализаторами в процессе нуклеофильной анионной тримеризации с образованием изоциануратов ( 186 ) (схема 123) [148].
N N
CH 3COONB u4
толуол/ ТГФ
R = H, CH 3
Схема 123. Тримеризация изоцианатов при катализе тетрабутиламмоний ацетатом
Обнаружено, что нейтральные соли, CsF и фторид тетрабутиламмония (TBAF), очень эффективно действуют в качестве катализаторов тримеризации арил- и алкилизоцианатов. Новые ароматические изоцианураты ( 187 ) с различными функциональными группами были синтезированы путем катализируемой CsF селективной тримеризации реакционноспособных изоцианатов и химической трансформации продуктов (схема 124) [149].
3 ArN=C=O
Аг\ кат._ N
Аг
Ar = p -Me 3 SiOC 6 H 4 , p -Me 3 SiOCOC 6 H 4 , p -Me 3 OCOC 6 H 4 , p -AllOC 6 H 4
Схема 124. Тримеризация ароматических изоцианатов
При концентрациях фосфотранов ZP(MeNCH 2 CH 2 ) 3 N (Z = одиночная пара) всего 0,0033 мол. % изоцианаты каталитически тримеризуются до пергидро-1,3,5-триазин-2,4,6-трионов (изоциануратов) при комнатной температуре. Эта реакция легко протекает в присутствии или в отсутствие растворителя, и катализатор можно повторно использовать по меньшей мере шесть раз без заметного ухудшения его каталитической способности [150].
Кроме того, описан не содержащий растворителей способ эффективного получения симметрично тризамещенных арил- или алкилизоциануратов ( 188 ) из изоцианатов, катализируемый пиперидиндитиокарбаматом натрия или калия или легкодоступным нитритом натрия или калия при обычном или микроволновом нагревании (схема 125) [151].
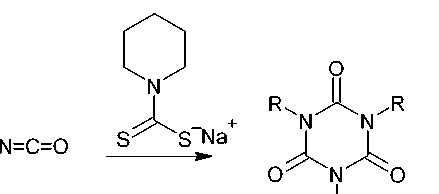
R 188
R = Ph, p -ClC 6 H 4 , p -MeOC 6 H 4 , нафтил, Et, c -C 6 H 11
Схема 125. Образование ариловых или алкилизоциануратов
Для тримеризации изотиоцианатов требуется высокое давление, обычно в присутствии триэтиламина, но выход триазинтритионов, как правило, высок (76 %). Когда давление увеличивают в десять раз, наблюдается образование неожиданного продукта – триазина ( 189 ) (схема 126) [39].
3 RN=C=S
Et3N, ДМФА 41^404 8000 кг/см2
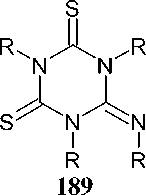
Схема 126. Тримеризация изотиоцианатов
Помимо тримеризации известны и другие реакции изо(тио)цианатов, приводящие к симм -триазинам. Например, при их взаимодействии с мочевинами и тиомочевинами в зависимости от использованных реагентов могут быть получены 1,3,5-триазин-дионы, тиоксо-1,3,5-триазиноны и 1,3,5-триазин-дитионы.
Так при конденсации ароилизотиоцианатов с замещёнными (тио)мочевинами образуются различные замещённые 1,3,5-триазин-2-тионы (190) (схема 127) [126, 127]. Данная реакция ана- логична ранее описанным конденсациям ароилизотиоцианатов с мочевинами, амидинами и гуа- нидинами (см. схемы 33, 86–89, 98).
ArN=C=S

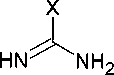
-н2о
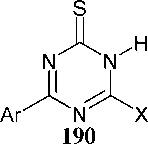
X = OR, SR
Схема 127. Взаимодействие ароилизотиоцианатов с мочевинами и тиомочевинами
Для получения 6-бензилсульфанил-4-(4-метоксифенил)-1,3,5-триазин-2-тиона (191) раствор 4-метоксибензоилизотиоцианата в бензоле постепенно добавляли при интенсивном перемешивании к S-бензилизотиомочевине в течение 15 мин. При этом происходило образование золотисто- жёлтого осадка триазинтиона 191 (схема 128) [152].
S
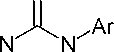
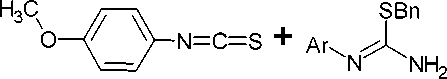
бенздл 15 мин.
р-МеОС^Нд N SBn
Схема 128. Синтез триазин-2-тиона 191
l,3,5-Триазин-2,4-дионы ( 192 ) представляют особый интерес в качестве потенциальных гербицидов. Стандартный метод их синтеза заключается во взаимодействии изоцианата с
Известно, что N-этоксикарбонилы-S-ДМФА при комнатной температуре с
производными мочевины или тиомочевины [39]. метилизотиомочевины реагируют с изоцианатами в образованием триазиндионов 192 (схема 129).
SMe
ЕЮ2С^
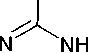
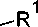
R2NCO ДМФА
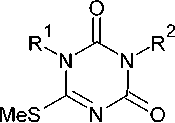
Схема 129. Получение триазиндионов 192
Взаимодействие N-этоксикарбонил-N,S-диметилизотиомочевины с циклогексилизоцианатом при комнатной температуре даёт l,3,5-триазин-2,4-дион ( 193 ) с выходом 78 % (схема 130) [39].
I FTNCO
EtOoCk ^Mp ----►
2 N^NH M ДМФА
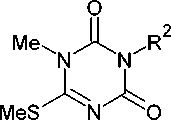
R2 = циклогексил
Схема 130. Реакция N-этоксикарбонил-N,S-диметилизотиомочевины с циклогексилизоцианатом
N-метоксикарбонилы-О-метилизомочевины также вступают в реакцию с изоцианатами, и промежуточное соединение (194) может быть циклизовано действием метоксида натрия при кипячении до 1,3,5-триазин-2,4-диона (195) (схема 131) [39].
SMe
M6O2C
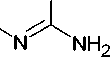
RNC9
SMe О
MeC^C
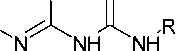
H NaOI\^
MeO
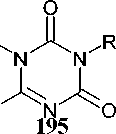
Схема 131. Взаимодействие N-метоксикарбонилы-О-метилизомочевины с изоцианатами
Производные иминов могут быть использованы вместо изоцианатов для взаимодействия с N-алкоксикарбонилизомочевинами и изотиомочевинами (схема 132). Таким образом, были получены производные 1,3,5-триазин-2-оны ( 196 ), которые используются в качестве диуретиков, антибактериальных и противовоспалительных средств, а также в качестве анальгетиков [39].
XMe
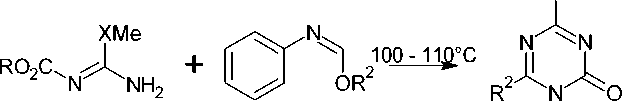
I
Ph
X = O, S
Схема 132. Производные иминов в синтезе 1,3,5-триазин-2-онов
Berluenga J. с соавторами опубликовали метод [153] получения производных дигидротриазин-2,4-диона ( 197 ) посредством последовательной реакции N-триметил-силилиминов ( 198 ) с двумя различными изоцианатами, что позволяет получать продукты с отличными выходами 84–96 % (схема 133).
R1 198
SiMe3 R NZ 4- \
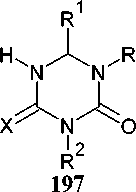
CH2CL, X = O, 25 °C X = S, А, 8 ч
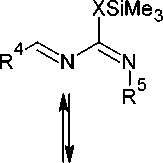
RNCO 2 £°C, 12ч MeOH 1ч
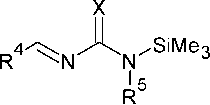
X = O, S
Схема 133. Получение несимметричных производных дигидротриазин-2,4-диона
Описаны реакции циклоприсоединения 1- п -толил- ( 199 ) и 1-бензил-2,4-дифенил-1,3-диазабута-1,3-диенов ( 200 ) с различными арил - и алкилизоцианатами и изотиоцианатами [154]. В случае соединения 199 реакция протекает с образованием не только триазина ( 201 ), но и с получением побочных бициклических продуктов – бензпиримидинов ( 202 ) и ( 203 ) (схема 134).
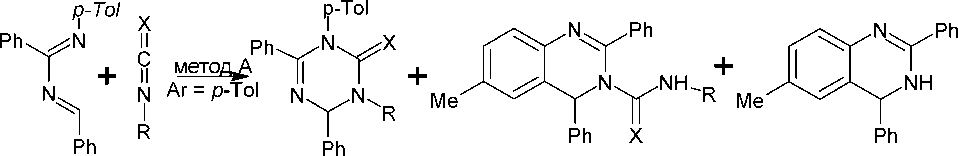
199 201 202 203
|
R |
X |
Выход, % |
||
|
Ph |
O |
68 |
– |
– |
|
m -Cl-C 6 H 4 |
O |
84 |
– |
– |
|
p -CH 3 -C 6 H 4 -SO 2 |
O |
91 |
– |
– |
|
Bn |
O |
39 |
60 |
– |
|
c -C 6 H 11 |
O |
– |
78 |
– |
|
CH 3 CH 2 CH 2 |
O |
– |
63 |
– |
|
p -NO 2 -C 6 H 4 |
S |
– |
– |
77 |
|
Ph |
S |
– |
– |
82 |
Схема 134. Циклоприсоединение диазабутадиена 199 и RN=C=X
При проведении реакции 1-бензил-2,4-дифенил-1,3-диазабута-1,3-диенов 200 с арил- и алкилизоцианатами и изотиоцианатами наблюдается образование лишь двух продуктов – триа-зин(ти)она ( 204 ) и трифенилтриазина ( 205 ) (схема 135).
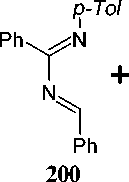
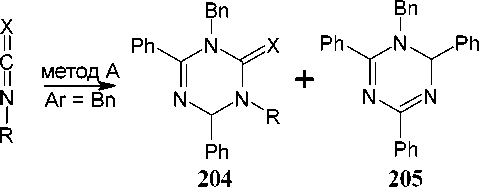
X = O; R = Ph, m -Cl-C 6 H 4 , p -CH 3 -C 6 H 4 -SO 2 , Bn, c -C 6 H 11 , CH 3 CH 2 CH 2
X = S; R = p -NO 2 -C 6 H 4 , Ph, Bn
Схема 135. Циклоприсоединение диазабутадиена 200 и RN=C=X
Для осуществления данного синтеза используются два метода. Метод A [154] заключается в проведении реакции в запаянной пробирке в атмосфере азота. Соответствующий гетероаллен добавляли к раствору соединений 199 или 200 в сухом бензоле в присутствии нескольких кристаллов гидрохинона. Реакционную смесь перемешивали при 25–110 °C в течение 1–120 ч до тех пор, пока исходный азадиен не переставал обнаруживаться с помощью ТСХ. Затем растворитель удаляли в вакууме. Сырой продукт очищали кристаллизацией или флэш-хроматографией на колонке с силикагелем.
Метод Б [154] также представляет собой реакцию в запаянной пробирке в атмосфере азота. Соединения 199 или 200 добавляли к соответствующему гетероалену в присутствии нескольких кристаллов гидрохинона (схема 136). Реакционную смесь перемешивали при 25–122 °C в течение 44–72 ч до тех пор, пока исходный азадиен не переставал обнаруживаться с помощью ТСХ. Когда он становился жидким, избыток гетероаллена удаляли перегонкой при пониженном давлении. Неочищенный продукт очищали с помощью флэш-хроматографии на колонке с силикагелем.
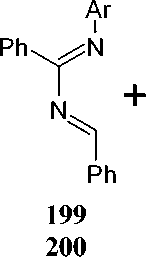
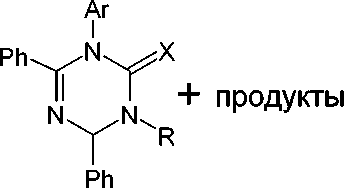
Схема 136. Циклоприсоединение диазабутадиенов и RN=C=X, метод Б
Авторами также обсуждается возможный механизм реакции, показанный на схеме 137 [154].
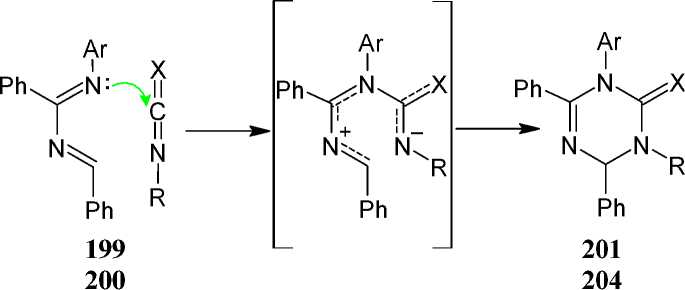
Схема 137. Механизм циклоприсоединения
Схожие реакции циклоприсоединения возможны и при участии иминов с двумя эквивалентами изоцианата. Обработка несколько затрудненного алифатического иминоэфира ( 206 ) двумя эквивалентами п -толуолсульфонилизоцианата приводит к 1,3-ди- п -толуолсульфонил-5- трет -бутил-6-метокситриазин-2,4-диону ( 207 ) c выходом 86 % (схема 138) [155].
Ts
N
H 3 C
CH 3
CH 3
Схема 138. Циклоприсоединение имина и изоцианата
Комплекс ( 208 ) реагирует с двумя эквивалентами алкилизоцианатов, как показано на схеме 139. Продукты ( 209 ) были охарактеризованы спектроскопически и в случае одного из соединений рентгеновской дифракцией. Шестичленные циклические лиганды, присутствующие в соединении 209 , должны быть результатом реакции [4+2]циклоприсоединения второй молекулы RN=C=O к 1,3-диаза-1,3-бутадиеновому фрагменту, образованному на предыдущем этапе формального введения RN=C=O в связь Re–N [156].
—
O
[ Re – н N ..
ч RN=C= O
CPh 2
Ph Ph
/ R
HN Njion
ONO
R
O
RNCO
Ph Ph
/ R NN
[Re–-N + N – R CPh 2
CPh 2
+ NR
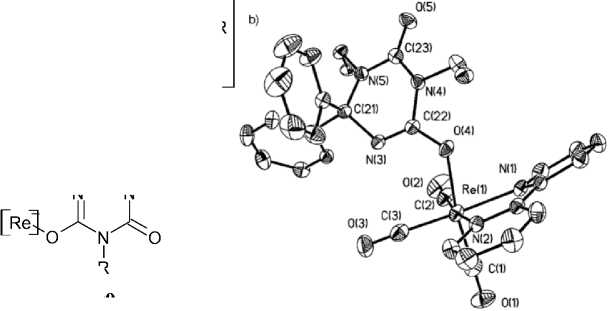
R
I 209
Схема 139. Циклоприсоединение комплекса рения к изоцианату
Реакции соединения 209 с трифторметансульфокислотой (HOTf) полностью деметаллируют 1,3,5-триазин-2,4-дионы ( 210 ) и позволяют эффективно рециркулировать металлический вспомогательный элемент в виде трифлатокомплекса [Re(OTf)(CO) 3 (bpy)] (см. схему 138) [156].
Реакция эквимолярных количеств иминоэфира бензойной кислоты и N-фенилбензимидоилизотиоцианата в бензоле при 20 °С дает нестабильный аддукт ( 211 ), который подвергается циклизации в 1,2,6-трифенил-1,4-дигидро-1,3,5-триазин-4-тион ( 212 ) с небольшим выходом (26,4 %) в условиях реакции (схема 140) [40].
s
NH
N—Ph
Ph OEt
N=C=S
N—Ph Ph
Ph—^ N=^
NH^ OEt
S
N N
Ph N Ph
Ph
Схема 140. Реакция иминоэфира бензойной кислоты и N-фенилбензимидоилизотиоцианата
Склонность изотиоцианатов к 1,4-циклоприсоединениям с образованием различных симм- триазин(ти)онов ярко выражена и наблюдалась в ряде реакций (с фенилизоцианатом, 1,3-дициклогексилкарбодиимидом и роданистоводородной кислотой), представленных на схеме 141. В результате данных превращений были получены триазины, содержащие одну (соединения 213, 214) и две тиоксо группы (соединение 215) [157].
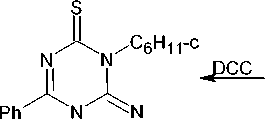
213 R С6Н1Гс
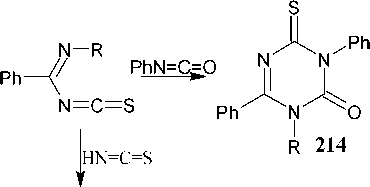
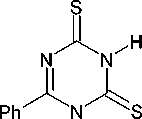
R215
213 : R = Ph, p -MeO-C 6 H 4 , 214 : R = p -Cl-C 6 H 4 , 2,6-(CH 3 ) 2 C 6 H 3
215 : Ph, p -Cl-C 6 H 4 , p -MeO-C 6 H 4 , 2,6-(CH 3 ) 2 C 6 H 3
Схема 141. Реакции 1,4-циклоприсоединения
Было показано [158], что имидоилизотиоцианаты аналогично ароилизотиоцианатам реаги- руют с амидиносоединениями по реакции присоединения-циклоконденсации, что приводит к образованию s-триазинтионов (216). При этом можно использовать два типа реакций. Первый представляет собой реакции [3+3] циклоприсоединения (схема 142).
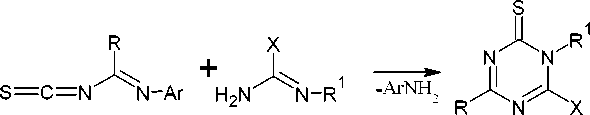
R = Alk, Ar; R1 = H, Ph; X = Alk, Ar, Alk 2 N, Ar 2 N, AlkO Схема 142. Циклоприсоединение по типу [3+3]
Второй тип реакций представляет собой [4+2] циклоприсоединение, в ходе которого образуются диарилзамещённые триазин-2-тионы ( 217 ) (схема 143).
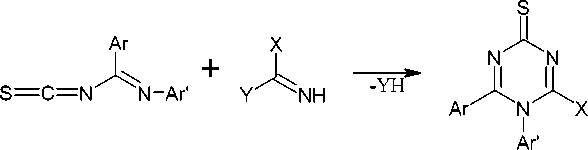
Y = EtO, PhO, MeS; X = Ph, EtO, Et 2 N Схема 143. Циклоприсоединение по типу [4+2]
Добавление гидроксида натрия в двухфазную реакционную смесь генерирует из соли амидиния свободное основание и катализирует циклизацию (схема 144). При этом наблюдается перегруппировка менее стабильных соединений ( 218 ) в стабильные триазинтионы ( 219 ) [159].
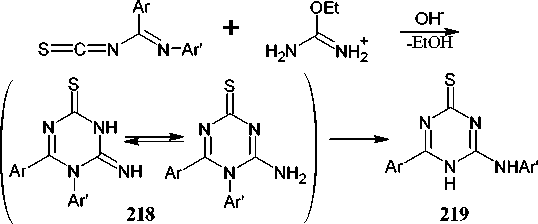
Схема 144. Процесс катализа циклизации
Cерусодержащие производные 1,3,5-триазинов можно получить тримеризацией тиоциановой кислоты HSCN в органических растворителях (например, i-PrOH, AcOH, диоксан) в присутствии серной кислоты. При этом образуется 1,3,5-триазин-2,4,6-тритион с выходом 29 % [160]. Нестандартный подход к синтезу N-арильных производных 1,3,5-триазин-2-тиона (220) на основе домино-реакции [3+2+1]-гетероциклизации изотиоцианатов с ариламидинами предложен в работе (схема 145) [161].
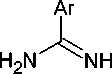
2 Ar1NCS
MW *
20 мол% NaOH ДМФА 110 °C
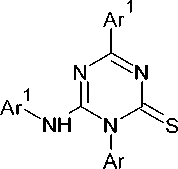
Ar, Ar1 = Ph, Tol, Py, p -Br-C 6 H 4 , p -Cl-C 6 H 4
Схема 145. Синтез N-арильных производных 1,3,5-триазин-2-тиона
В попытке синтеза пиридо[2,3-d]пиримидинов была обнаружена более неожиданная реакция фенилизоцианата с производным пиридина, приводящая к образованию соединений (221) (схе- ма 146). Предполагается, что реакция протекает через аза-реакцию Виттига, [4+2] гетероциклоприсоединение и нуклеофильное расщепление пиридинового кольца с последующей геометрической изомеризацией и образованием амида. Структура одного из соединений 221 (Ar=Ph, R= All) подтверждена рентгеноструктурным анализом [162].
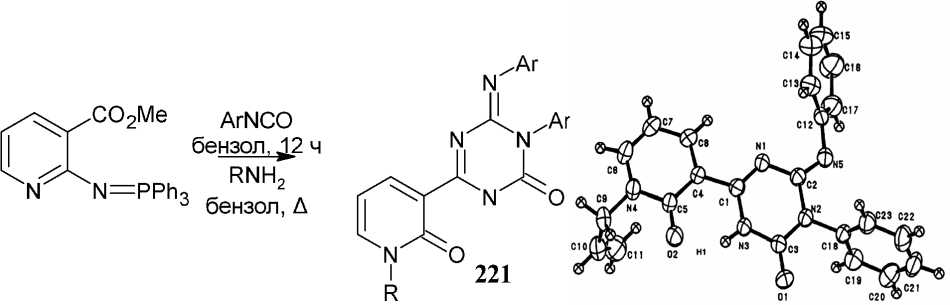
Ar = Ph, p -Cl-C 6 H 4 , p -MeO-C 6 H 4 ; R = All, i -Pr
Схема 146. Реакция фенилизоцианата с производным пиридина
При взаимодействии изофталоилхлорида с тиоцианатом калия и дифениламином в ацетоне ожидалось образование симметричного диподального производного бензоилтиомочевины, однако в реальности наблюдалось образование производного триазинтиона ( 222 ) (схема 147) [163].
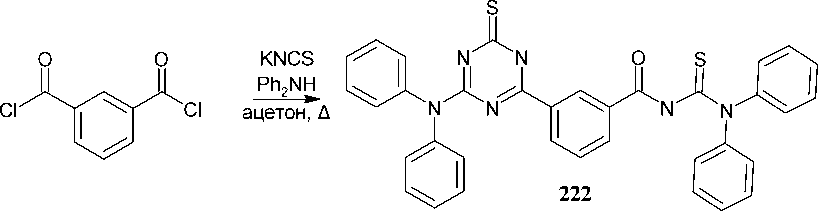
Схема 147. Получение триазинтиона
Для полученного соединения 222 был исследован способ координации с органометаллическим ядром fac -[Re(CO) 3 ]+ путем реакции лиганда 222 с [Re(CO) 5 Br] в толуоле. Реакция привела к образованию димерного комплекса [(μ- 222 ) 2 (Re(CO) 3 Br) 2 ], в котором 222 координируется с каждой из единиц fac -[Re(CO) 3 ]+ в виде нейтрального монодентатного и S-донорного хелата. Димер [(μ- 222 ) 2 (Re(CO) 3 Br) 2 ] был проанализирован с помощью ЯМР 1H, инфракрасной спектроскопии (ИК), масс-спектрометрии высокого разрешения (HR-ESI-MS) и рентгеноструктурного анализа монокристаллов (рис. 15) [163].
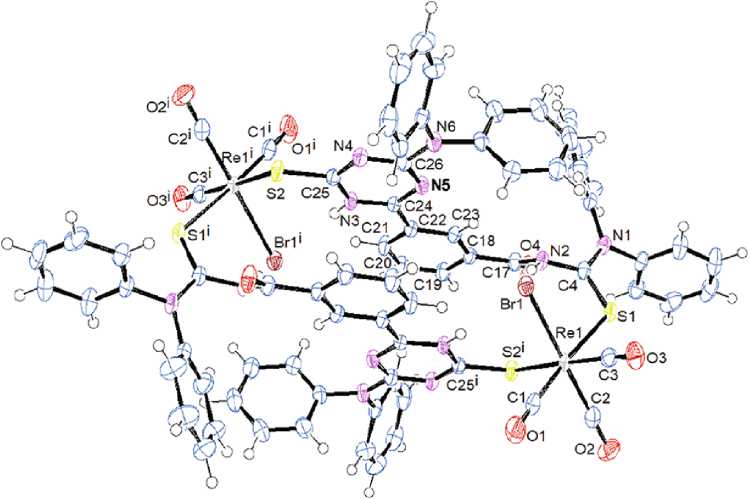
Рис. 15. Строение димерного комплекса [(μ-222) 2 (Re(CO) 3 Br) 2 ] по данным РСА
-
1.6. Синтезы на основе нитрилов и их производных
Наиболее распространенным методом синтеза 1,3,5-триазинов является циклотримеризация нитрилов, протекающая в присутствии HCl и кислот Льюиса [40]. В обзоре [164] представлены работы по циклотримеризации замещенных монофункциональных цианидов XC≡N, различающихся строением заместителя X = H, R, Ar, >N, HO, RO, ArO, HS, RS, Hal. Внимание уделено выяснению влияния заместителей X на реакционную способность соединений, содержащих N≡C-группу; обсуждаются различные механизмы циклотримеризации, а также влияние катализаторов, давления и других факторов. Рассмотрена не только гомоциклотримеризация, но и смешанная циклотримеризация производных цианидов и влияние условий реакции на структуру образующихся 1,3,5-триазинов.
Протекание реакции облегчается в случае наличия в структуре нитрила электроноакцепторных заместителей. Для алкилнитрилов тримеризация протекает в жестких условиях (давление до 100 МПа). В реакцию циклотримеризации вступают и другие соединения, содержащие группу -C≡N.
1,3,5-Триазинон(тион) (223) получается путем сотримеризации 4 толилцианата или
тиоциановой кислоты и нитрила (схема 148) [40].
2 R1CN + R2CN -^
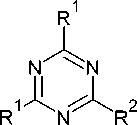
R1 = 4-TolO, SH; R2 = OH, Ph Схема 148. Сотримеризания нитрилов
Ранее мы уже упоминали ряд реакций с участием CN-функционализированных соединений (см. схемы 32, 41, 46, 61, 72, 85, 99, 118), а также реакции производных изомочевины, амидина и гуанидина, содержащих функцию CN (см. схемы 91, 97, 100–105, 109–111) [40]. Кроме того, стоит упомянуть синтез S-производных 1,3,5-триазин-2-тиона, который можно осуществить конденсацией 2-алкил- или 2-арилизотиомочевины с двумя эквивалентами арилцианата (схема 149). Как правило, реакция протекает спонтанно с получением триазина ( 224 ) с хорошим выходом. При использовании солей изотиурония (например, сульфата 2-метилизотиурония) требуется добавление основания, такого как карбонат натрия или гидроксид натрия [40].
OR1
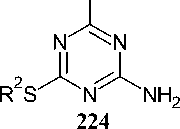
SR2
2 R1OCN + Д R1 = 4-Tol, R2* Ph H2N NH R1 = 3-CIC6H4, R2 = Me
Схема 149. Конденсация изотиомочеины с нитрилами
Также арилцианиды вступают в реакции с незамещёнными (тио)мочевинами и гуанидинами в соотношении 2:1, что приводит к соответствующим диарилтриазинам (225) (схема 150). Реакция протекает в присутствии гидрида натрия в ДМСО, при этом в случае о-хлорбензонитрила, был получен о-хлорбензамид, а не желаемый триазин. По-видимому, атом хлора в орто-положении к цианогруппе стерически препятствует циклизации. В случае с 2,6-дихлорбензонитрилом из реакционной смеси был выделен только непрореагировавший нитрил. Стерический эффект двух орто-атомов хлора препятствует любой реакции [165, 166].
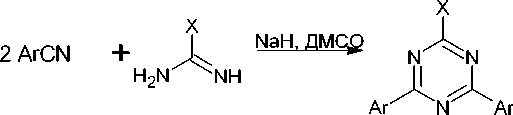
X = OH, SH, NH 2 Схема 150. Взаимодействие арилцианидоа с (тио)мочевинами, гуанидинами
При замене мочевин и гуанидина на биуреты или бигуаниды по вышеописанному методу удаётся получить триазиндиолы или триазиндиамины (226) (схема 151) [165].
X
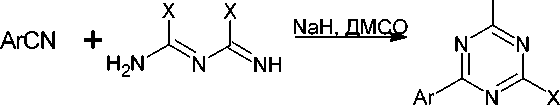
X = OH, NH 2
Схема 151. Получение триазиндиолов и триазиндиаминов
Авторами [167] предложен многокомпонентный однореакторный подход к синтезу триазин-дионов ( 227 ), основанный на взаимодействии фосфонатов, нитрилов, альдегидов и изоцианатов, однако выходы существенно колеблются от 13 до 91 % (схема 152).
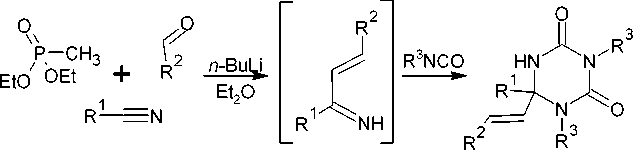
Схема 152. Многокомпонентный синтез триазиндионов 227
В качестве альтернативных способов синтеза триазиндионов были опробованы две методики [167]. В первой реакции α,β-ненасыщенный нитрил обрабатывали MeLi с последующим добавлением фенилизоцианата, что привело к желаемому триазину ( 228 ) с выходом 30 % (схема 153).
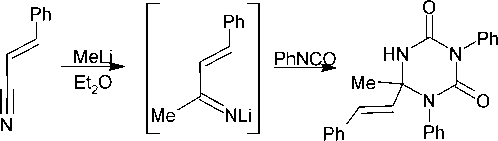
Схема 153. Синтез с использованием а,в -ненасыщенного нитрила
Во втором случае взаимодействию с MeLi подвергался трет -бутилцианид, который впоследствии так же реагировал с фенилизоцианатом с образованием триазиндиона ( 229 ) с невысоким выходом всего 20 % (схема 154) [167].
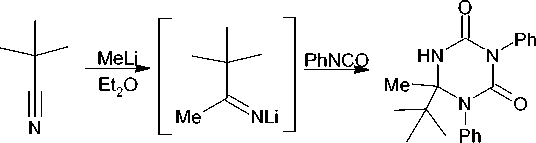
Схема 154. Синтез с использованием нитрила
О-производные 1,3,5-триазинонов также могут быть получены реакцией N-цианоимидатов с цианамидом и метоксидом натрия в виде 6-замещенных 4-метокси-1,3,5-триазин-2-аминов ( 230 ) с умеренными выходами как показано на схеме 155 [40].
R1
RO
NaOMe R
N MeO^ N^=\ ' R0H NC N Na
NC
R = Me, Et; R1 = Me, Ph
ОН
А 5 ^ n \N
R N NH2
Схема 155. Реакция N-цианоимидатов с цианамидом и метоксидом натрия
В завершении раздела, посвященного синтезу различных производных 1,3,5-триазинонов(тионов), в качестве отличных от приведенной классификации методов хотелось бы упомянуть ещё несколько подходов.
Один из них связан с возможностью замещения аммонийных групп с получением 2-оксо-1,2-дигидро- сим -триазинов ( 231 ) (схема 156) [168].
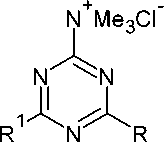
он
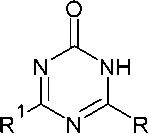
Схема 156. Замещение аммонийной группы
Стереоструктура некоторых 2-оксо-1,2-дигидро- сим -триазинов была исследована с помощью рентгеноструктурного анализа, и было показано, что они существуют в виде димеров в кристаллическом состоянии (рис. 16) [168].
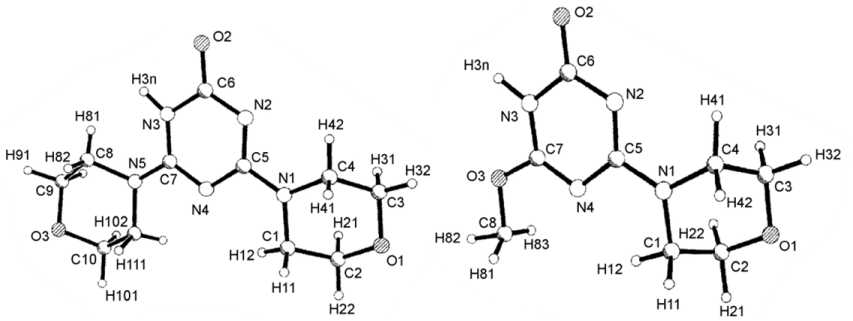
Рис. 16. Строение соединений 231 по данным РСА
Ранее нами упоминалась способность тиадиазинов подвергаться перегруппировке до триа-зинтионов (см. схемы 52, 65, 75, 77). Схожим образом, замещённый 1,3,5-оксодиазин-2,4-диимин ( 232 ) подвергается перециклизации до триазин-2-она ( 233 ) при действии щёлочи (схема 157) [169].
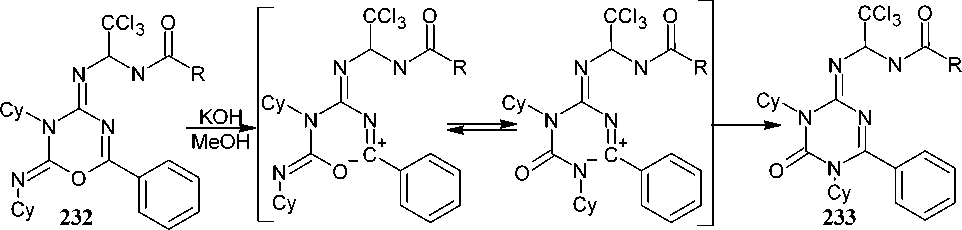
Cy = циклогексил, R = Me, Ph
Схема 157. Перегруппировка 1,3,5-оксадиазин-2,4-диимина в 1,3,5-триазин
Строение исходного оксадиазин-диимина (R = Ph), а также полученного триазинона (R = Me) было установлено по данным рентгено-структурного анализа (рис. 17) [169].
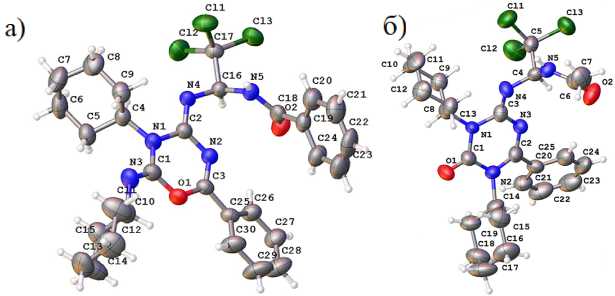
Рис. 17. Строение оксадиазина (а) и триазинона (б) по данным РСА
Ещё один довольно необычный подход к синтезу 1,3,5-триазина, содержащего в своей структуре как оксо-, так и тиоксо-группу, был обнаружен в рамках изучения серии 1,2,4-тиадиазолидинонов [170]. Авторами отмечено интересное восстановительное расщепление тиадиазолидиноновой системы (схема 158), которое приводит к образованию нового пиперидинового спиротриазинового гетероцикла наряду с N’-этил-N’-[2-(4-диметиламинопропил)-1,3-тиазолил]-N-пропилмочевиной. Структура 5-этил-1’-метил-4-оксо-пергидро-3-пропил-6-тиоксо-1,3,5-триазин-2-спиро-3’-пиперидина ( 234 ) однозначно подтверждается с помощью ЯМР-экспериментов COSY, HMQC, HMBC и РСА [170].
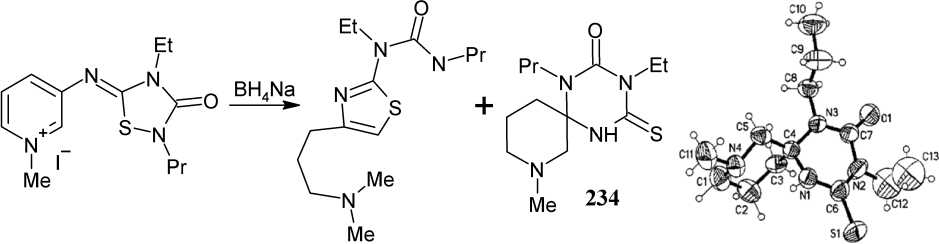
Схема 158. Восстановительное расщепление 1,2,4-тиадиазолидинонов
Интересный подход фрагментации-циклизации был описан Гонгом и др. (Yong Gong et. al.), где расщепление связи N–N триазолидиндионов с участием 9-бромфлуорена приводит к образованию соответствующего флуоренилуразола ( 235 ) наряду с продуктом перегруппировки триази-нандионом ( 236 ), как показано на схеме 159. Соединение 235 может быть превращено в триазин-дион 236 при обработке первого трет -бутилатом калия [171].
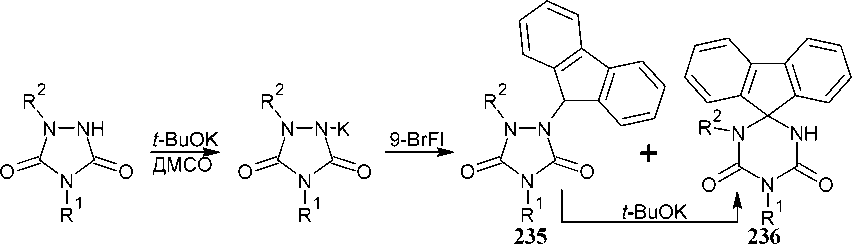
R1 = Me, Ph; R2 = Me, Ph, 4-NO 2 C 6 H 4
Схема 159. Фрагментация-циклизация уразола при действии 9-бромфлуорена
Позднее аналогичная реакция фрагментации N–N уразольного цикла, но уже во внутримолекулярном варианте, была использована для построения шестичленного дигидро-1,3,5-триазин-2,4-дионного кольца ( 237 ) (схема 160) [172]. Для двух соединений структуры были установлены с использованием метода РСА (рис. 18).
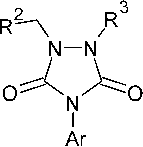
LDA толудр 78 до 25 °C, 3 ч
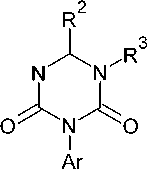
Схема 160. Реакция фрагментации-циклизации во внутримолекулярном варианте
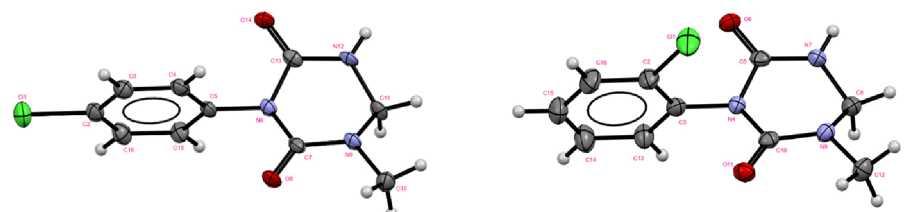
Рис. 18. Строение триазиндионов 237 по данным РСА
Другим вариантом расширения пятичленного цикла триазола до симм -триазина является реакция 1,2,4-триазолин-3,5-дионов с алкилдиазаацетатом в дихлорметане при 0 °C. При этом изначально образуются 6-алкоксикарбонил-3-арил-1,3,5-триазабицикло[3.1.0]гексан-2,4-дионы ( 238 ). При кипячении последних в хлорбензоле в течение двух недель происходит раскрытие цикла с образованием 2-алкоксикарбонил-5-арил-1,3,5-триазин-4,6(1 H ,5 H )-дионов ( 239 ) (схема 161) [173].
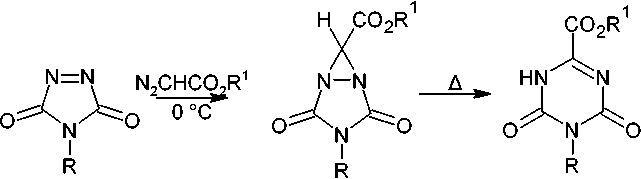
238 239
R = Ph, 4-ClC 6 H 4 ; R1 = Me, Et
Схема 161. Присоединение карбена по связи N=N с раскрытием цикла
Заключение
Таким образом, данный аналитический обзор литературы показывает, что на данный момент известен достаточно широкий ряд синтетических подходов к созданию 1,3,5-триазинового каркаса. При этом некоторые методы являются более удобными при создании алкил- или арилзамещённых триазинов, в то время как другие приводят к созданию триазин(ти)онов, триазин-ди(ти)онов и даже триазинтри(ти)онов. Такое разнообразие синтетических подходов позволяет выбрать наиболее удобную и эфективную методику синтеза для каждого отдельного случая. Среди симм -триазин(ти)онов имеется немало соединений, нашедших своё практическое применение. Например, способы их получения [65, 73, 174] и применения в качестве гербецидов [97], полимерных стоматологических композитов [175], материалов для трубных соединений, снижающих уровень шума в автомобиле [176], антиозонантов [177], предшественников децитабина [178, 179], для изготовления фотоматериалов на основе галогенида серебра литологического типа, содержащий производное тетрагидро-1,3,5-триазин-2-тиона и производное поли-алкиленоксида [180] отражены в соответствующих патентах: CN 111377875 A, JP 04364173 A, JP 6086797 B2, WO 2014064094 A1, CN 105367912 A, US 5019611 A, WO 2009086687 A1, CN 107011399 A, US 4724196 A.


