Синтез 3-фторфенилацетата тетрафенилсурьмы из пентафенилсурьмы и бис(3-фторфенилацетато)трифенилсурьмы
Автор: Шарутин В.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Краткие сообщения
Статья в выпуске: 1 т.17, 2025 года.
Бесплатный доступ
Взаимодействием эквимолярных количеств пентафенилсурьмы и бис (3-фторфенилацетато)трифенилсурьмы в бензоле получен с выходом 92 % 3-фторфенилацетат тетрафенилсурьмы (1), который был идентифицирован методами ИК-спектроскопии и рентгеноструктурного анализа. РСА проводили на дифрактометре D8 QUEST фирмы Bruker, кристаллографические характеристики элементарной ячейки соединения следующие: пространственная группа моноклинная С с, а = 10,2427(6), b = 17,7825(7), c = 14,6472(5) Å, β = 95,260(4), V = 2656,60(17) Å3, Z = 4, ρвыч = 1,458 г/см3, m = 1,072 мм-1, F (000) = 1176,0, размер кристалла 0,32 ´ 0,2 ´ 0,09 мм, диапазон сбора данных по 2θ, град: 6,952-56,992, диапазон индексов -13 ≤ h ≤ 12, -19 ≤ k ≤ 23, -19 ≤ l ≤ 19, число измеренных рефлексов 9906, число независимых рефлексов 4334, R int = 0,0228, GOOF = 1,139, число параметров 330, R 1 = 0,0350, wR 2 = 0,1042. По данным РСА, атомы сурьмы в соединении имеют искаженную тригонально-бипирамидальную координацию с атомом кислорода карбоксилатной группы в аксиальном положении. Аксиальный угол СSbO составляет 175,9(2)º. Сумма экваториальных углов CSbC равна 357,1(9)º, расстояния Sb-Сэкв [2,109(7), 2,117(5), 2,146(5) Å] значительно короче длин связей Sb-Сакс [2,194(7) Å] и Sb-O [2,244(4) Å]. Организация молекул в кристалле соединения 1 обусловлена водородными связями и СН××× π -взаимодействиями колец арильных и карбоксильных лигандов. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2055555; deposit@ccdc.cam.ac.uk или http://www.ccdc.cam.ac.uk/data_request/cif).
Пентафенилсурьма, бис(3-фторфенилацетато)трифенилсурьма, 3-фторфенилацетат тетрафенилсурьмы, синтез, реакция перераспределения лигандов, строение
Короткий адрес: https://sciup.org/147248059
IDR: 147248059 | УДК: 546.865 | DOI: 10.14529/chem250119
Synthesis of tetraphenylantimony 3-fluorophenylacetate from pentaphenylantimony and triphenylantimony bis(3-fluorophenyl acetate)
The interaction of equimolar amounts of pentaphenylantimony and bis (3-fluorophenylacetato)triphenylantimony in benzene yielded 92% tetraphenylantimony 3-fluorophenylacetate (1), which was identified by IR spectroscopy and X-ray structural analysis. X-ray diffraction analysis was performed on a D8 QUEST diffractometer from Bruker. The crystallographic characteristics of the unit cell of the compound are as follows: monoclinic space group C c, a = 10,2427(6), b = 17,7825(7), c = 14,6472(5) Å, β = 95,260(4), V = 2656,60(17) Å3, Z = 4, ρcalc = 1,458 g/cm3, m = 1,072 mm-1, F(000) = 1176,0, crystal size 0,32´0,2´0,09 mm, data collection range for 2θ, deg: 6,952-56,992, index range -13 ≤ h ≤ 12, -19 ≤ k ≤ 23, -19 ≤ l ≤ 19, number of measured reflections 9906, number of independent reflections 4334, R int = 0,0228, GOOF = 1,139, number of parameters 330, R 1 = 0,0350, wR 2 = 0,1042. According to X-ray diffraction data, the antimony atoms in the compound have a distorted trigonal-bipyramidal coordination with the oxygen atom of the carboxylate group in the axial position. The axial angle CSbO is 175,9(2)º. The sum of the equatorial angles CSbC is 357,1(9)°, the Sb-Ceq distances [2,109(7), 2,117(5), 2,146(5) Å] are significantly shorter than the Sb-Cax [2,194(7) Å] and Sb-O [2,244(4) Å] bond lengths. The organization of molecules in the crystal of compound 1 is due to hydrogen bonds and CH∙∙∙π-interactions of the rings of the aryl and carboxyl ligands. Complete tables of atomic coordinates, bond lengths, and bond angles have been deposited with the Cambridge Crystallographic Data Center (No. 2055555; deposit@ccdc.cam.ac.uk or http://www.ccdc.cam.ac.uk/data_request/cif).
Текст краткого сообщения Синтез 3-фторфенилацетата тетрафенилсурьмы из пентафенилсурьмы и бис(3-фторфенилацетато)трифенилсурьмы
Аннотация. Взаимодействием эквимолярных количеств пентафенилсурьмы и бис(3-фторфенилацетато)трифенилсурьмы в бензоле получен с выходом 92 % 3-фторфенилацетат тет-рафенилсурьмы (1), который был идентифицирован методами ИК-спектроскопии и рентгеноструктурного анализа. РСА проводили на дифрактометре D8 QUEST фирмы Bruker, кристаллографические характеристики элементарной ячейки соединения следующие: пространственная группа моноклинная Сс, а = 10,2427(6), b = 17,7825(7), c = 14,6472(5) Å, β = 95,260(4), V = 2656,60(17) Å3, Z = 4, Рвыч = 1,458 г/см3, ц = 1,072 мм-1, F(000) = 1176,0, размер кристалла 0,32 х 0,2 х 0,09 мм, диапазон сбора данных по 20, град: 6,952-56,992, диапазон индексов -13 < h < 12, -19 < k < 23, –19 ≤ l ≤ 19, число измеренных рефлексов 9906, число независимых рефлексов 4334, Rint = 0,0228, GOOF = 1,139, число параметров 330, R1 = 0,0350, wR2 = 0,1042. По данным РСА, атомы сурьмы в соединении имеют искаженную тригонально-бипирамидальную координацию с атомом кислорода карбоксилатной группы в аксиальном положении. Аксиальный угол СSbO составляет 175,9(2)º. Сумма экваториальных углов CSbC равна 357,1(9)º, расстояния Sb–Сэкв [2,109(7), 2,117(5), 2,146(5) Å] значительно короче длин связей Sb–Сакс [2,194(7) Å] и Sb–O [2,244(4) Å]. Организация молекул в кристалле соединения 1 обусловлена водородными связями и СН--- п -взаимодействиями колец арильных и карбоксильных лигандов. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2055555; или .
Начало изучения реакций перераспределения лигандов в ряду арильных соединений пятивалентной сурьмы относится к 1974 г., когда Фергюсон и Хавли при перекристаллизации дигидроксида трифенилсурьмы из хлороформа в атмосфере воздуха наблюдали образование карбоната бис (тетрафенилсурьмы) [1]. Очевидно, что формирование фрагмента Ph 4 Sb можно объяснить только обменом фенильных заместителей между атомами сурьмы. Изучая строение производного сурьмы, полученного из дихлорида трифенилсурьмы и оксалата серебра, Соверби с Миллин-гоном показали, что данное соединение имеет солеобразное строение [Ph 4 Sb][Ph 2 Sb(Ox) 2 ] (Ох = О 2 ССО 2 ) и предположили, что оно может быть получено из дихлорида трифенилсурьмы [2].
Решив исследовать взаимодействие пентаарилсурьмы с производными общей формулы Ar3SbX2 (Х - электроотрицательный лиганд) авторы [3] полагали, что будет иметь место либо образование комплексов ионного типа, либо перераспределение органических радикалов и синтез производных несимметричного строения. Действительно обнаружено, что пентафенилсурьма реагирует с дигалогенидами, дибензоатом и дироданидом трифенилсурьмы с образованием продуктов несимметричного строения – галогенида, бензоата и роданида тетрафенилсурьмы соответственно, с выходом до 99 %. С помощью этого эффективного способа синтеза производных сурьмы общей формулы Ar 4 SbX (Х – электроотрицательный лиганд) были получены роданиды, нитраты, карбоксилаты, сульфонаты, оксиматы и ароксиды тетраарилсурьмы [4–27]. Преимуществом данного метода синтеза соединений Ar 4 SbX является высокий выход и легкость выделения целевого продукта, а также мягкие условия проведения реакции.
С целью продолжения изучения реакции перераспределения лигандов в ряду арильных соединений пятивалентной сурьмы изучено взаимодействие эквимолярных количеств пентафенилсурьмы с бис (3-фторфенилацетато)трифенилсурьмой в бензоле.
Экспериментальная часть
Синтез 3-фторфенилацетата тетрафенилсурьмы ( 1 ) осуществляли по методике реакции перераспределения лигандов, описанной в работах [27,28].
3-Фторфенилацетат тетрафенилсурьмы (C 6 H 5 ) 4 SbOC(O)CH 2 C 6 H 4 F-3 (1): бледно-желтые кристаллы, выход 92 %, Т пл = 146 °С. ИК-спектр ( ν , см–1): 3107, 3061, 2974, 2927, 1639, 1612, 1587, 1477, 1436, 1311, 1298, 1276, 1269, 1247, 1186, 1159, 1145, 1136, 1064, 1020, 997, 962, 929, 918, 875, 781, 742, 732, 721, 702, 690, 642, 578, 522, 470, 457, 445, 424. Найдено (%): C 65,75; H 4,52. Для C 32 H 26 FO 2 Sb вычислено (%): C 65,89; H 4,50.
ИК-спектр соединения 1 записывали на ИК-спектрометре Shimadzu IRAffinity-1S в таблетке KBr в области 4000–400 см–1.
РСА кристалла 1 проведен на дифрактометре D8 Quest фирмы Bruker (Mo K α-излучение, λ = 0,71073 Å, графитовый монохроматор) при 296(2) К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT- Plus [29]. Все расчеты по определению и уточнению структуры выполнены по программам SHELXL/PC [30] и OLEX2 [31]. Структура определена прямым методом и уточнена методом наименьших квадратов в анизотропном приближении для неводородных атомов.
Кристаллографические данные и результаты уточнения структуры приведены в табл. 1, основные длины связей и валентные углы - в табл. 2. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2055555; или .
Кристаллографические данные, параметры эксперимента и уточнения структуры 1
Длины связей и валентные углы в структуре 1
Таблица 1
|
Параметр |
1 |
|
Стехиометрическая формула |
C 32 H 26 FO 2 Sb |
|
М |
583,28 |
|
Сингония |
Моноклинная |
|
Пространственная группа |
С с |
|
a , Å |
10,2427(4) |
|
b , Å |
17,7825(7) |
|
c, Å |
14,6472(5) |
|
α , град. |
90,00 |
|
β, град. |
95,260(4) |
|
γ , град. |
90,00 |
|
V , Å3 |
2656,60(17) |
|
Z |
4 |
|
ρ выч, г/см |
1,458 |
|
µ , мм–1 |
1,072 |
|
F (000) |
1176,0 |
|
Размер кристалла, мм |
0,32 × 0,2 × 0,09 |
|
Диапазон сбора данных по 2 θ , град. |
6,952–56,992 |
|
Диапазон индексов |
–13 ≤ h ≤ 12, –19 ≤ k ≤ 23, –19 ≤ l ≤ 19 |
|
Число измеренных рефлексов |
9906 |
|
Чисто независимых рефлексов |
4334 |
|
R int |
0,0228 |
|
GOOF |
1,139 |
|
Число параметров |
330 |
|
R -факторы по I > 2 σ ( I ) |
R 1 = 0,0350, wR 2 = 0,1042 |
|
R -факторы по всем рефлексам |
R 1 = 0,0374, wR 2 = 0,1078 |
|
Остаточная электронная плотность (max/min), e/A3 |
0,80/–0,91 |
Таблица 2
|
Связь |
d , Å |
Угол |
ω, град. |
|
Sb(1)–O(1) |
2,244(4) |
C(31)‒Sb(1)‒O(1) |
175,9(2) |
|
Sb(1)–C(11) |
2,146(5) |
C(21)‒Sb(1)‒C(11) |
121,7(3) |
|
Sb(1)–C(31) |
2,194(7) |
C(1)‒Sb(1)‒C(11) |
116,5(3) |
|
Sb(1)–C(21) |
2,117(5) |
C(1)‒Sb(1)‒C(21) |
118,9(3) |
|
Sb(1)–C(1) |
2,109(7) |
С(48)‒O(1)‒Sb(1) |
122,3(4) |
|
O(1)–C(48) |
1,280(8) |
O(1)‒C(48)‒C(47) |
113,7(6) |
|
O(2)–C(48) |
1,218(9) |
O(2)‒C(48)‒O(1) |
126,1(6) |
|
С(48)–C(47) |
1,558(10) |
O(2)‒C(48)‒C(47) |
120,2(6) |
|
F(1)–C(43) |
1,355(13) |
C(41)‒C(47)‒C(48) |
111,6(5) |
|
Sb(1)∙∙∙O(2) |
3,371(11) |
F(1)‒C(43)‒C(42) |
118,3(10) |
Обсуждение результатов
Известно, что реакции перераспределения лигандов с участием пентафенилсурьмы и дикарбоксилата трифенилсурьмы, независимо от соотношения исходных реагентов протекают с образованием ониевых производных сурьмы Ph 4 SbOC(O)R [3–8]. В продолжение настоящей работы исследовано взаимодействие эквимолярных количеств пентафенилсурьмы и бис (3-фторфенилацетато)трифенилсурьмы, единственным продуктом которого являлcя 3-фторфенилацетат тетрафенилсурьмы ( 1 ), выделенный из реакционной смеси с выходом 92 %.
PhH
Ph 5 Sb + Ph 3 Sb[OC(O)CH 2 C 6 H 4 F-3] 2 ^ 2 Ph 4 SbOC(O)CH 2 C 6 H 4 F-3
Наличие в ИК-спектре полученного комплекса интенсивной полосы поглощения в области валентных колебаний карбонильных групп (1639 см–1), свидетельствует о присутствии в нем карбонильной группы [32]. В ИК-спектре 1 также присутствуют полосы поглощения валентных колебаний фрагмента SbC4 при 457, 445 см–1 и полосы валентных колебаний углеродного скелета арильных групп (1477, 1436 см–1). Валентным колебаниям связей CAr–H отвечают полосы поглощения средней интенсивности при 3107 и 3061 см–1, а внеплоскостным деформационным колебаниям этих же связей – интенсивные полосы при 732 и 702 см–1.
С целью подтверждения строения комплекса 1 было проведено его рентгеноструктурное исследование. По данным РСА атом сурьмы в соединении 1 имеет тригонально-бипирамидальную координацию (см. рисунок).
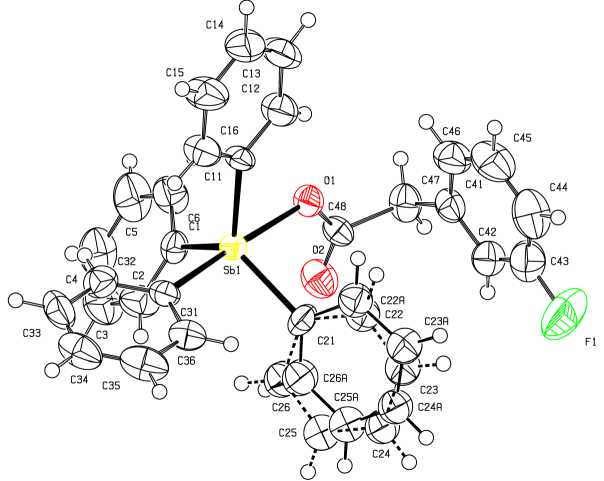
Строение 3-фторфенилацетата тетрафенилсурьмы (1)
В аксиальном положении находится атом кислорода ацилатного заместителя, угол OSbС акс равен 175,9(2) ° (табл. 2). Интервал валентных углов ОSbСэкB составляет 82,25(19)-87,1(2)°, атом сурьмы выходит из экваториальной плоскости на 0,211 Å в сторону аксиального атома углерода. Сумма углов CSbC в экваториальной плоскости равна 357,1 ° , при этом углы между экваториальными арильными заместителями неравноценны и составляют 116,5(3), 118,9(3), 121,7(3) ° . Длины связей Sb–C экв [2,109(7)–2,146(5) Å] меньше расстояния Sb–C акс [2,194(7) Å]. Расстояние Sb–O составляет 2,244(4) Å и близко к подобным расстояниям в карбоксилатах тетраарилсурьмы [33]. В молекуле соединения 1 , как и в других ацилатах тетраарилсурьмы, расстояние между атомом сурьмы и атомом кислорода карбонильной группы Sb --- O=C [3,371(9) А] меньше суммы ван-дер-ваальсовых радиусов соответствующих атомов (3,7 Å [34]). Отметим, что в отличие от большинства карбоксилатов тетраарилсурьмы, в которых контакт центрального атома металла с карбонильным атомом кислорода располагается внутри наибольшего угла CSbC [33], контакт Sb --- O=C располагается внутри угла C(1)Sb(1)C(21), составляющего 118,9(3) ° .
Выводы
Таким образом, взаимодействием пентафенилсурьмы с бис (3-фторфенилацетато)трифенилсурьмой в бензоле с выходом 92 % получен 3-фторфенилацетат тетрафенилсурьмы ( 1 ), который был идентифицирован методами ИК-спектроскопии и рентгеноструктурного анализа. По данным РСА, атомы сурьмы в соединении 1 имеют искаженную тригонально-бипирамидальную координацию с атомом кислорода в аксиальном положении, при этом наличие внутримолекулярного контакта между атомом сурьмы и атомом кислорода карбонильной группы Sb ⋅⋅⋅ О=С [3,371(9) Å] позволяет говорить об увеличении координационного числа атома сурьмы до 6.


