Синтез борсодержащих производных трис (2-гидроксиэтил) аммония и их влияние на рост и развитие растений
Автор: Даин И.А., Логинов С.В., Лебедев А.В., Стороженко П.А.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Химическая технология
Статья в выпуске: 4 (74), 2017 года.
Бесплатный доступ
Для создания композиционных препаратов по предотвращению дефицита бора для важнейших сельскохозяйственных культур были синтезированы и охарактеризованы спектрографическими методами трис (2-гидроксиэтил) аммониевые комплексы с анионами бора и низших дикарбоновых кислот (С2-С4). Показано, что формирование и стабилизация комплексов, содержащих дикарбоновые кислоты с большим числом углеродных атомов или имеющих внутримолекулярное ?-сопряжение (малеиновая кислота), связана с большими стерическими или электростатическими затруднениями, соответственно. В случае винной кислоты наблюдалось связывание по вицинальным гидроксильным группам кислоты, согласно данным ЯМР спектроскопии и элементного анализа. Проведено усовершенствование существовавшего прежде способа получения боратрана методом азеотропной отгонки воды: а именно, осуществлён выбор оптимального соотношения исходных компонентов в реакционной смеси и выбор оптимальной реакционной смеси. Были испробованы различные среды для взаимодействия борной кислоты и ТЭА: неполярные (толуол) и полярные апротонные (ДМСО) растворители, спирты (изопропанол, 2-бутанол) и их смеси. В результате был выработан оптимальный метод синтеза с применением смеси изопропанол/2-бутанол в соотношении 3:1, в котором выход был увеличен на 12.08%, по сравнению со стандартной отгонкой азеотропной смеси изопропанола и воды (с 82.70% до 94.78%) и при этом было показано низкое содержание примесей в продукте. Также разработан лабораторный альтернативный метод синтеза боратрана без применения растворителей на стадии химического взаимодействия, проведён выбор оптимального состава промывных жидкостей. В ходе сельскохозяйственных экспериментов исследовано влияние отобранных композиций на всхожесть и энергию прорастания свеклы столовой и урожайность свеклы сахарной. Установлено, что боратран оказывает незначительный положительный эффект по стимуляции всхожести семян. В ходе полевых испытаний композиция, содержащая боратран, о-крезоксиацетат трис (2-гидроксиэтил) аммония и 1-хлорметилсилатран, продемонстрировала наилучший результат по длине корневой апикальной части растения, среднему весу растения и корнеплода по сравнению с контролем.
Атраны, боратран, триэтаноламин, дефицит бора, сахарная свекла
Короткий адрес: https://sciup.org/140229898
IDR: 140229898 | DOI: 10.20914/2310-1202-2017-4-165-174
Synthesis and plant growth modulation of tris (2-hydroxyethyl)ammonium boron-containing compounds
To develop boron deficiency treatment composite preparations for significant agricultural crops tris(2-hydroxyethyl)ammonium complexes containing boron and lower dicarboxylic acid (C2-C4) anions were synthesized and characterized. It was shown, that formation and stabilization of complexes containing a greater number of carbon atoms or intermolecular ?- conjugation (e.g. maleic acid) is related to space and electrostatical hurdles, respectively. According to NMR spectroscopy, in case of tartaric acid complex vicinal hydroxyl bounding with boron was found. The preexisted boratrane azeotropic water distillation synthetic method was modernized (videlicet optimal solvent mixture and raw materials ratio were chosen). Various triethanolamine and boric acid reaction mediums, i.e. nonpolar (toluene), polar aprotic (dimethylsulphoxide), protic (isopropanol, 2-butanol) solvents and their mixtures, were tested. In the issue optimal synthetic method, utilizing isopropanol/2-butanol mixture in ratio 3 to 1, was elaborated. In comparison to standard azeotropic water-isopropanol distillation the yield of the process was exceeded to 12.08% (from 82.70% to 94.78%) and low impurity concentrations in product was committed. Besides alternative laboratory solvent-free boratrane synthetic method was developed and optimal rinsing fluid composition was found. During agricultural experiments substance effectiveness in germination power and germinability of beet seeds and productivity of sugar beet was studied. Boratrane was found to be slightly effective for seed germinability stimulation. Boratrane-containing composition (i.e. boratrane + tris(2-hydroxyethyl)ammonium o-cresoxyacetate + 1-chloromethylsilatrane) was shown to have the best results in apical root length, average root-crop and average plant weigth increasing in comparison with the control.
Текст научной статьи Синтез борсодержащих производных трис (2-гидроксиэтил) аммония и их влияние на рост и развитие растений
Начиная с двадцатых годов прошлого века, многие биологи неоднократно высказывали предположение о возможности рассмотрения бора как одного из важнейших микроэлементов высших растений [1]. Однако первые свидетельства его биологических функций как участника основных физиологических процессов были обнаружены у диатомовых водорослей и цианобактерий [1]. Лишь к началу XXI века было установлено, что этот элемент принимает участие в формировании и нормальном функционировании клеточной стенки. Фактически, он выступает стабилизатором стенок пектиновых каналов, и, таким образом, регулирует проницаемость клеточной мембраны [2]. Высказываются также предположения, что бор занимает граничное место в биологии, поскольку у ряда видов животных и грибов также доказана его физиологическая значимость [2], что говорит о его применимости, не ограничивающейся богатой целлюлозой клеточной стенкой растений, которая не свойственна двум другим вышеупомянутым царствам.
Текущий уровень знания в этой области обусловлен в первую очередь интересом исследователей к проблеме дефицита данного элемента у сельскохозяйственных культур [3]. Симптомами этого явления у высших растений служат прекращения роста апикальных меристем (как корневых, так и стеблевых) и появление эффекта «прозрачности» листьев, который приписывают нарушению целостности клеточной стенки [3]. Тщательные наблюдения за ней в данном процессе выявили её утончение, структурную деформацию, хрупкость и слияние примыкающих везикул с наружной мембраной клетки [4], причём, все эти явления обнаруживались сравнительно быстро после установления условий дефицита бора [5]. Также установлено, что бор является инициатором процессов ферментативной гидратации с участием ауксиновых фитогормонов [3]. Было выявлено, что характер зависимостей химического состава отдельных органов от количества потребляемого бора схож у различных видов растений, несмотря на существенные отличия в нормах потребления данного элемента [6]. Это доказывает значимость бора как растительного микроэлемента, присутствие которого в агрохимических препаратах и композициях способно улучшать продуктивность сельскохозяйственных культур.
В рамках данной работы было принято решение о необходимости ввода в композиции, содержащие синтетические аналоги гетероауксина (как например, показавший ранее эффективность на различных биологических объектах трис
(2-гидроксиэтил) аммония о-крезоксиаце-тат [7]), источников бора с расчётом на пролонгированную доставку препарата до областей апикальных меристем для эффективного воздействия на процессы формирования плодов и корнеплодов, в особенности в условиях обеднённых микроэлементом почв полупустынной, степной и лесостепной зон южных регионов. Для решения подобной задачи наиболее подходящими группами соединений были выбраны 2, 8, 9-триокса-5-аза-1-боробицикло [3.3.3] ундекан (более известный под тривиальным названием «боратран»), как бициклическое производные триэтаноламина, содержащее связанный ковалентно бор, и ионные комплексы бора с дикарбоновыми кислотами, способными предохранять некоторое время борный компонент от перехода в водной среде в полиборатное состояние, затрудняющее депонирование микроэлемента в целевых органах растения [8].
Экспериментальная часть
Синтез борсодержащих соединений
Все полученные соединения были исследованы методами ИК и ЯМР1 Н, 11 B спектроскопии и элементного анализа. Спектры ЯМР1 Н и11 B регистрировали на спектрометре Bruker AM-360 с рабочей частотой 360.13 и 115.56 МГц, соответственно. Спектр записывали при комнатной температуре в DMSO-d6 и СDСl 3 . Химические сдвиги в спектре ЯМР1 Н приведены в δ-шкале. ИК спектры регистрировали на ИК-Фурье спектрометре Nicolet 6700 с детектором DTGS-КВr в таблетках бромида калия.
Трис (2-гидроксиэтил) аммония бис (оксалато) борат (1) . К раствору 5.04 г. щавелевой кислоты моногидрата (0.040 моль кислоты) и 1.24 г. борной кислоты (0.020 моль) в 70 мл изопропанола при 70 °С приливали по каплям 2.98 г. Триэтаноламина (0.020 моль) в течение 20 минут. По окончании прикапывания капельную воронку промывали 20 мл изопропанола, сливали промывные жидкости в реакционную массу и отгоняли азеотропную смесь изопропанол-вода. По окончании отгонки азеотропа реакционную массу охлаждали и упаривали на роторном испарителе под вакуумом без нагревания. Кубовый остаток промывали 30 мл изопропилового спирта с прокаленным бикарбонатом магния, фильтровали, нижний слой (вязкая прозрачная жидкость цвета чайной розы) отделяли на делительной воронке и помещали на 12 часов в эксикатор с хлоридом кальция. Аналогично были получены трис (2-гидрокси-этил) аммония бис(малонато)борат (2) и бис (сукцинато)борат (3). Сведения об аналитических данных полученных соединений представлены в таблице 1.
Трис (2-гидроксиэтил) аммония бис (тартрато) борат (4) . К раствору 13.45 г. виноградной кислоты моногидрата (0.040 моль кислоты) и 1.24 г. борной кислоты (0.020 моль) в 100 мл дистиллированной воды при 55 °С приливали по каплям 2.98 г. триэтаноламина (0.020 моль). По окончании прикапывания капельную воронку промывали 20 мл воды, сливали промывные жидкости в реакционную массу и перемешивали при неизменной температуре в течение 30 минут. По истечению указанного срока раствор упаривали на роторном испарителе под вакуумом без нагревания. Кубовый остаток промывали 30 мл изопропилового спирта с прокаленным бикарбонатом магния, фильтровали, нижний слой (вязкая прозрачная жидкость цвета чайной розы) отделяли на делительной воронке и помещали на 12 часов в эксикатор с хлоридом кальция. Выход (1): 38.59 г. (91.5%).
Боратран (5) . В ходе испытаний были предложены два способа получения продукта:
-
1. К прозрачному раствору 12.37 г. борной кислоты (0.200 моль) в 200 мл органического растворителя при нагревании и интенсивном перемешивании в течение 10 минут прикапывания 29.85 г. триэтаноламина (0.200 моль). По окончании прикапывания капельную воронку промывали 30 мл растворителя сливали промывные жидкости в реакционную массу, доводили реакционную смесь до кипения и проводили азеотропную отгонку смеси растворителя и 10,8 г воды (0.600 моль), выделившейся в ходе реакции. По прекращению отгонки азеотропной смеси реакционную массу охлаждали до комнатной температуры при сохранении перемешивания и оставляли в тёмном прохладном месте на 1 сутки. Образовавшийся белый осадок отфильтровывали и промывали смесью изопропанол-гексан (3:1). Продукт сушили при температуре 80 °С в течение 3 часов в сушильном шкафу. Выходы продуктов и схема проведённых опытов представлены в таблицах 2 и 3.
-
2. К 32.84 г. триэтаноламина (0.220 моль) порционно добавляли 12.37 г. борной кислоты (0.200 моль) при интенсивном перемешивании и температуре 55–75 °С. Полученную пастообразную массу перемешивали в течение 30 минут, после чего приливали в колбу 10 мл изопропанола и охлаждали при перемешивании до комнатной температуры. Реакционную массу отфильтровывали и сушили при температуре 80 °С в течение 3 часов в сушильном шкафу. Выходы продуктов и схема проведённых опытов представлены в таблице 4.
Испытания на сельскохозяйственных культурах
Испытания проводились согласно «Методическим указаниям по регистрационным испытаниям фунгицидов в сельском хозяйстве».
Влияние на энергию прорастания и всхожесть свеклы столовой . Исследования проведены на кафедре генетики и биотехнологии РГАУ-МСХА имени К.А. Тимирязева, совместно с к.б.н. Карсункиной Н.П., на свекле столовой сорта «Двусемянная ТСХА» согласно ГОСТ 12038–84. Семена опрыскивали водными растворами биологически активных веществ. Проращивание семян проводили в климат камере в факторостатичных условиях (температуре 24 °C и темноте). В каждую чашку Петри раскладывали по 50 семян, повторность опытов – пятикратная. На пятый день определяли энергию прорастания, а на десятый день – всхожесть семян. Были использованы индивидуальные препараты трис (2-гидроксиэтил) аммония сукцината (р-р, 1 г/л), янтарной кислоты (р-р, 1 г/л), боратрана (р-р, 1 г/л), борной кислоты, трис (2-гидроксиэтил) аммония о-крезоксиацетат (р-р, 1 г/л) и смесь трис (2-гидроксиэтил) аммония сукцината с боратраном в соотношении 1:2 (р-р, 0.5 + 1 г/л). Норма расхода рабочего раствора – 10 л/т семян.
Влияние на показатели качества свеклы сахарной . Исследования проведены в 2014 году на открытом грунте на территории с. Лебеди-новка (Чуйская область, Киргизия) на культуре свеклы сахарной сорта «Киргизская односемянная 70», совместно с ООО «Бекпр». В качестве стандартного образца использовался южнокорейский борсодержащий препарат «Сенгын-сенгын»©. Опрыскивание препаратами производилось на фазе формирования 3–4 настоящих листьев, сбор урожая – спустя 5 месяцев после посадки. Боратран вводился в виде композиционного препарата с трис (2-гидроксиэтил) аммония о-крезоксиацетатом и 1-хлорметилси-латраном в соотношении 5:5:1, соответственно (р-р, 0.5 + 0.5 + 0.1 г./л).
Синтез борсодержащих соединений
Синтез трис (2-гидроксиэтил) аммониевых комплексов с анионами бора
Модификация борной кислоты способна приводить не только к образованию боратных эфиров, но также к появлению ионных комплексов с двумя органическими молекулами, сшитыми воедино при помощи мостикового боратного аниона [9]. Это связывание происходит благодаря реакции борной кислоты в среде щелочей или органических оснований, в которых существует борат-анион, с гидроксильными группами органической молекулы, находящихся в вицинальном положении, или же с карбоксильными группами низших дикарбоновых кислот [10]. Для связывания с гидроксильными группами наиболее часто используются многоатомные спирты или моносахариды [9], к незамещенным группам которых присоединяют дополнительные фрагменты молекул, изменяющие их поверхностно-активные свойства. Основным применением данной группы соединений является использование бис-оксалатоборатов щелочных металлов в смеси с сульфоланом в качестве компонентов литий-ионных батарей, обладающих меньшей токсичностью к окружающей среде и сходной электрической проводимостью с традиционными компонентами [10]. В данном направлении сосредоточено большинство исследований в данной области, посему до настоящего момента не проводилось синтеза подобных анионных комплексов бора с органическими противоионами.
Поскольку получение ионных комплексов с щелочными металлами осуществляется в ходе прямой реакции между кислородсодержащим комплексообразователем, борной кислотой и щелочами [9] было решено использовать аналогичный подход и к синтезу комплексов триэтаноламина. В случае комплексов с низшими дикарбоновыми кислотами для удаления образующейся в ходе реакции воды нами было решено использовать в ходе процесса отгонку азеотропной смеси (Рисунок 1). По окончанию процесса реакционная масса упаривалась в роторном испарителе. В случае производного винной кислоты была использована водная среда реакции по причине низкой растворимости кислоты в спиртах (Рисунок 2) .
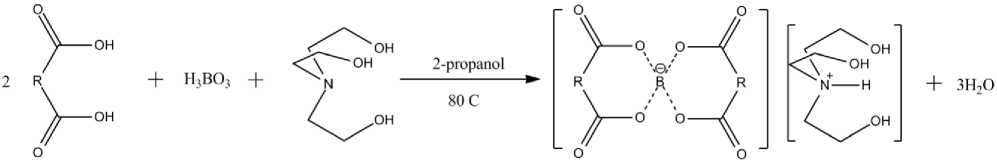
Рисунок 1. Синтез трис (2-гидроксиэтил) аммониевых комплексов дикарборновых кислот с анионами бора (1–3) R = (СН 2 ) n ; n = 0–2 (0–1, 1–2, 2–3)
Figure 1. Synthesis of tris(2-hydroxyethyl) ammonium complexes with boron and dicarboxylic acids anions (1–3) R = (СН 2 ) n ; n = 0–2 (0–1, 1–2, 2–3)
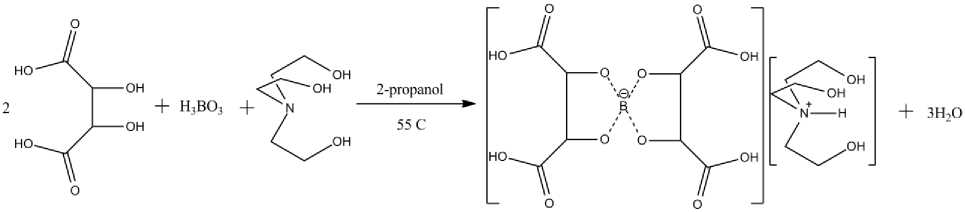
Рисунок 2. Синтез бис(тартрато)бората трис (2-гидроксиэтил) аммония (4)
Figure 2. Synthesis of tris(2-hydroxyethyl) ammonium bis(tartrato)borate
В результате были получены комплексы трис (2-гидроксиэтил) аммония с анионами бис (оксалато)бората (1), бис(малонато)бората (2) и бис (сукцинато)бората (3), являющиеся прозрачными вязкими жидкостями светло-жёлтой или бесцветной окраски. Стоит оговориться, что исследования не ограничивались лишь данными анионами – были произведены попытки синтеза с использованием малеиновой, глутаровой и адипиновой кислот, которые не привели к получению продукта. Во всех этих попытках была отмечена неустойчивость полученной жидкости, из которой в процессе охлаждения выкристаллизовывались нецелевые продукты: в случае малеиновой кислоты – гидромалеинат трис (2-гидроксиэтил) аммония, глутаровой и адипиновой – боратран, а оставшаяся субстанция представляла собой загрязнённый триэтаноламин. Подобное поведение в случае малеиновой кислоты объясняется образованием более устойчивого нежели боратный комплекс стабилизированного внутримолекулярной водородной связью гидромалеинат-аниона. Предположительно выпадение боратрана при реакциях с дикарбоновыми кислотами с большей длиной углеродной цепи объясняется большим потенциальным барьером к переходу большего количества атомов в заслонённую конформацию.
Также был проведён опыт с винной кислотой, как содержащей две гидроксильные группы в вицинальном положении по отношению друг к другу. В отличие от реакции с карбоксиль- ными группами в ходе процесса была использована меньшая температура и не использовалась отгонка воды, поскольку предполагалось также, что борат-анион обладает большим сродством к гидроксильным группам нежели к карбоксильным. Таким образом, была получена вязкая жидкость цвета чайной розы (4).
Таблица 1.
Физико-химические свойства полученных трис (2-гидроксиэтил) аммониевых комплексов дикарбоновых кислот с анионами бора (1–4)
Table 1.
Physicochemical properties of tris(2-hydroxyethyl) ammonium complexes with boron and dicarboxylic acids anions (1–4)
|
Соединение Compound |
25 n D |
ИК-спектр (ν В-О ), см-1 IR spectrum (ν В-О ), cm-1 |
11 B ЯМР-спектр, δ, м.д. 11 B NMR spectrum, δ |
1 H ЯМР-спектр, δ, м.д. 1 H NMR spectrum, δ |
|
|
NСН 2 |
ОСН 2 |
||||
|
1 |
1.4921 |
1363 |
19.036 |
2.984 |
3.563 |
|
2 |
1.5064 |
1355 |
18.932 |
3.127 |
3.622 |
|
3 |
1.5107 |
1346 |
18.811 |
2.786 |
3.493 |
|
4 |
1.5286 |
1350 |
18.743 |
3.214 |
3.505 |
Синтез боратрана
Существует несколько способов получения 2, 8, 9-триокса-5-аза-1-боробицикло [3.3.3] ундеканов, отличающихся как используемым сырьём, так и условиями проведения химической реакции [11]. Для получения замещённых в бициклическом кольце боробицикло [3.3.3] ундеканов преимущественно используются реакции с алкильными эфирами борной кислоты и галогенидов бора [12]. Однако с точки зрения принципов «зелёной химии» наиболее перспективным для получения незамещённого 2, 8, 9-триокса-5-аза-1-боробицикло [3.3.3] ундекана (боратрана) представляется прямое взаимодействие триэтаноламина с борной кислотой, благодаря малой токсичности исходных компонентов и возможности проведения реакции в мягких условиях (рисунок 3).
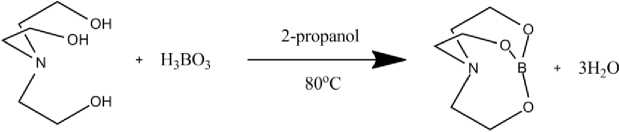
Рисунок 3. Синтез 2, 8, 9-триокса-5-аза-1-боробицикло [3.3.3] ундекана (боратрана)
Figure 3. Synthesis of 2, 8, 9-trioxa-5-aza-1-borobicyclo[3.3.3] undecane (boratrane)
Поскольку в ходе реакции выделяется вода, а само соединение чувствительно к действию кислого гидролиза, то чаще всего синтез проводят в спиртовой среде при непрерывной отгонке азеотропной смеси воды со спиртами [11]. Этот способ является достаточно затратным, поскольку требует больших количеств растворителя (низших одноатомных спиртов) для удаления воды, смещающий равновесие реакции в сторону исходных веществ, а также не позволяет производить единовременно большие объёмы продукта. Существует и иной способ, предложенный в 2013 году, отличительной особенностью, которого является протекание реакции в водной среде с последующей отгонкой растворителя на роторном испарителе без проведения дополнительных стадий очистки [13]. Однако, из-за протекания обратной реакции гидролиза, перехода борной кислоты в среде в полиборатное состояние ухудшается качество продукта (происходит загрязнение исходными компонентами, что отражается на изменении температуры плавления продукта с необходимых 232–234 °C до 239– 240 °C [13]). Кроме того ранее было показано, что увеличение количества отогнанной воды в азеотропной смеси приводит к увеличению выхода боратрана [13].
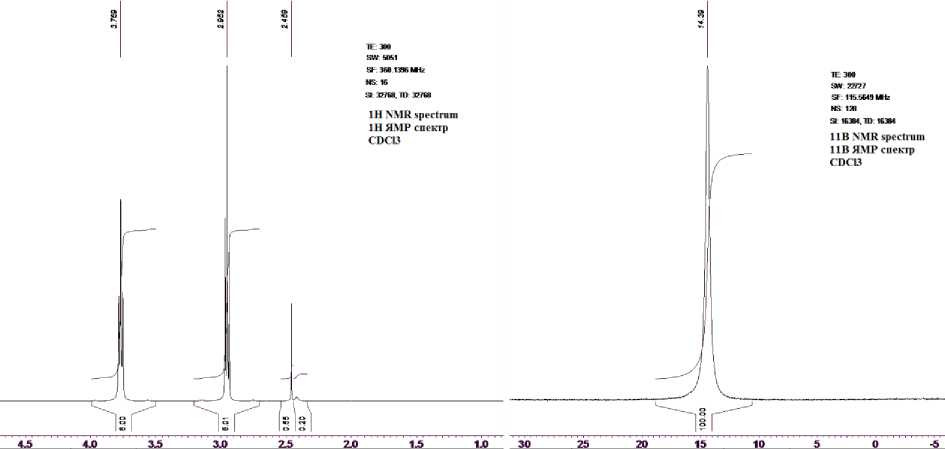
Рисунок 4.1 H (слева) и11 B (справа) ЯМР спектры полученных образцов боратрана
Figure 4.1 H (left) аnd11 B (right) spectra of synthesized boratrane samples
В этой связи было решено провести работу по разработке нового способа синтеза, способного преодолеть недостатки предшественников и сочетать в себе принципы «зелёной химии», требующие минимального использования растворителей. Было выбрано два основных направления: улучшение уже существующего метода с азеотропной отгонкой растворителей (с целью нахождения азеотропных смесей с наибольшим возможным содержанием воды и максимальными выходами) и разработка способа синтеза без использования растворителей.
По модификации азеотропного способа нами были испробованы различные среды для взаимодействия борной кислоты и ТЭА:
Условия проведения реакции борной кислоты и триэтаноламина (TEA) с отгонкой азеотропной смеси (серия опытов по поиску оптимального соотношения компонентов)
неполярные (толуол) и полярные апротонные (ДМСО) растворители, спирты (изопропанол, 2-бутанол) и их смеси. Подбор растворителей в смесях проводился таким образом, чтобы помимо увеличения количества воды в азеотропной смеси могло быть достигнуто осаждение целевого продукта в чистом более высококипящем компоненте. В результате был выработан оптимальный метод синтеза, в котором выход был увеличен на 12.08%, по сравнению со стандартной отгонкой азеотропной смеси изопропанола и воды (с 82.70% до 94.78%) и при этом было показано низкое содержание примесей в продукте (по результатам ИК,1 H и11 B ЯМР спектроскопии (рисунок 4) ).
Таблица 2.
Table 2.
Boric acid and triethanolamine (TEA) reaction with azeotropic distillation conditions (optimal raw materials ratio research series)
|
№ |
Избыток (компонент) Exceeding component |
Растворитель | Solvent |
Выход, % Yield, % |
t плав , °C t mеlt , °C |
|
1 |
20% (Н 3 ВО 3 ) |
Изопропанол | Isopropanol |
75.83 |
236–238 |
|
2 |
10% (Н 3 ВО 3 ) |
78.21 |
234–236 |
|
|
3 |
Стехиометрично Stoichiometrically |
82.70 |
232–235 |
|
|
4 |
10% (TEA) |
91.16 |
230–232 |
|
|
5 |
20% (TEA) |
84.03 |
224–227 |
|
|
6 |
20% (Н 3 ВО 3 ) |
Изопропанол : 2-бутанол (3:1) Isopropanol : 2-butanol (3:1) |
85.11 |
236–238 |
|
7 |
10% (Н 3 ВО 3 ) |
88.65 |
235–237 |
|
|
8 |
Стехиометрично Stoichiometrically |
93.21 |
232–234 |
|
|
9 |
5% (TEA) |
93.54 |
232–234 |
|
|
10 |
10% (TEA) |
94.78 |
231–233 |
|
|
11 |
15% (TEA) |
89.64 |
228–230 |
|
|
12 |
20% (TEA) |
86.92 |
226–228 |
После поиска оптимального растворителя было проведено уточнение по соотношениям исходных компонентов реакции, в ходе которой было выяснено, что наибольший выход (по наименьшему взятому прекурсору) достигается при использовании 10% избытка триэтаноламина. Дальнейшее увеличение концентрации амина в смеси приводило к загрязнению продукта в ходе выделения (продукт приобретал жёлтую окраску, и снижалась температура его плавления до 224–227 °C, что требует дополнительной перекристаллизации) и снижению выхода. Использование избытка борной кислоты также приводило к уменьшению выхода, что предположительно объяснялось возможностью взаимодействия с другими молекулами борной кислоты и образованием полиборатных ионов. Схемы всех проведённых экспериментов представлены в Таблицах 2 и 3.
Наилучшие результаты были продемонстрированы смесью 2-бутанол / изопропанол, причём стоит отметить, что использование смесей растворителей не оправдало себя на примере системы толуол / изопропанол, где было отмечено снижение выхода во всём диапазоне концентраций по сравнению с индивидуальными компонентами.
Таблица 3.
Условия проведения реакции борной кислоты и триэтаноламина с отгонкой азеотропной смеси
Предположительно это связано с меньшим сродством веществ в данной системе по сравнению со смесью спиртов. Кроме того азеотропная смесь изобутанол/вода обладала близкой температурой кипения к смеси изопропанол /вода (87.3 °C и 80.3 °C, соответственно), чем позволило снизить общую температуру в реакционной массе по сравнению с системами включавшими толуол.
В ходе реакций в системах с ДМСО азеотропной смеси не образовывалось, однако её исследование было оправдано свойствами самого продукта, малорастворимого в данном растворителе в отличие от обоих исходных реагентов, что могло бы позволить улучшить стадию выделения продукта. Хотя результаты применения смеси ДМСО/изопропанол превзошли по выходам индивидуальные растворители, но последние оказались меньшими по сравнению с системой 2-бутанол / изопропанол (87.02% и 93.21%, соответственно), в которой отгонка образовавшийся воды производилась эффективнее, что ещё раз подтверждает тезис об увеличении выхода боратрана с увеличением количества отогнанной влаги из реакционной смеси [13].
(серия опытов по поиску оптимального растворителя)
Table 3.
Boric acid and triethanolamine reaction with azeotropic distillation conditions (optimal solvent mixture research series)
|
№ |
Растворитель 1 (Р1) Solvent 2 (S2) |
Растворитель 2 (Р2) Solvent 1 (S1) |
Соотношение растворителей (Р1 : Р2) Solvent ratio (S1 : S2) |
t реакции , °C t rеасtiоn , °C |
Выход,% Yield,% |
t плав , °C t mеlt , °C |
|
1 |
Изопропанол (Isopropanol) |
– |
82 |
82.70 |
232…235 |
|
|
2 |
Толуол (Toluene) |
– |
110 |
82.31 |
233…235 |
|
|
3 |
ДМСО (DMSO) |
– |
70 |
69.95 |
231…233 |
|
|
4 |
2-бутанол (2-butanol) |
– |
100 |
54.17 |
234…236 |
|
|
5 |
Изопропанол Isopropanol |
2-бутанол 2-butanol |
1:4 |
85 |
62.48 |
232–234 |
|
6 |
3:7 |
85 |
68.55 |
233–235 |
||
|
7 |
2:3 |
85 |
76.07 |
233–235 |
||
|
8 |
1:1 |
85 |
81.88 |
230–233 |
||
|
9 |
3:2 |
85 |
87.95 |
231–233 |
||
|
10 |
7:3 |
85 |
91.63 |
232–235 |
||
|
11 |
3:1 |
85 |
93.21 |
232–234 |
||
|
12 |
4:1 |
85 |
92.42 |
232–234 |
||
|
13 |
9:1 |
85 |
89.91 |
233–235 |
||
|
14 |
Этанол (Ethanole) |
1:1 |
80 |
62.64 |
228–230 |
|
|
15 |
Толуол Toluene |
Изопропанол Isopropanol |
1:3 |
90 |
69.58 |
233–235 |
|
16 |
1:1 |
90 |
77.13 |
232–234 |
||
|
17 |
3:1 |
90 |
79.46 |
233–235 |
||
|
18 |
ДМСО DMSO |
1:3 |
80 |
79.31 |
230–232 |
|
|
19 |
1:1 |
80 |
86.31 |
231–233 |
||
|
20 |
3:1 |
80 |
87.02 |
229–232 |
||
Разработка второго способа синтеза проводилась в рамках концепции «зелёной химии» без использования растворителей в ходе реакции. Схема проведённых экспериментов и выход целевого продукта представлена в таблице 4.
Образовывавшаяся в ходе реакции вода в данном случае удалялась в ходе промывки реакционной смеси растворителем. Несмотря на присутствие воды в реакторе в ходе процесса, проведение отгонки под вакуумом серьёзно осложняло бы воспроизведение манипуляций по перемешиванию, промывке и выгрузке продукта, требовало бы увеличения затрат энергии и оборудования, что стало причиной нашего отказа от контроля за смещением равновесия в сторону образования продуктов.
Было принято во внимание, что боратран имеет высокую скорость гидролиза в водной среде, что исключало возможность использования каких бы то ни было водных растворов в качестве
Таблица 4.
Условия проведения реакции борной кислоты и триэтаноламина без использования растворителей Table 4.
Boric acid and triethanolamine solvent-free reaction conditions
|
№ |
Промывная жидкость Rinsing fluid |
t реакции , °C t rеасtiоn , °C |
Выход,% Yield,% |
t плав , °C t mеlt , °C |
|
1 |
Вода дист. (0.1 мМ р-р NН 3 ) Distilled water (0.01mМ NН 3 solution) |
65 |
57.90 |
228–230 |
|
2 |
Изопропанол | Isopropanol |
50 |
76.53 |
230–233 |
|
3 |
55 |
81.93 |
230–232 |
|
|
4 |
60 |
84.77 |
232–234 |
|
|
5 |
65 |
87.43 |
232–234 |
|
|
6 |
70 |
87.52 |
231–234 |
|
|
7 |
75 |
87.62 |
232–235 |
|
|
8 |
Изопропанол (0.01 мМ р-р NН 3 ) Isopropanol (0.01mМ NН 3 solution) |
65 |
88.23 |
233–235 |
|
9 |
Изопропанол (0.1 мМ р-р NН 3 ) Isopropanol (0.1mМ NН 3 solution) |
65 |
88.68 |
232–234 |
|
10 |
Изопропанол (1 мМ р-р NН 3 ) Isopropanol (1mМ NН 3 solution) |
65 |
88.46 |
233–235 |
Было установлено, что присутствие оснований в составе промывных жидкостей оказывает существенно меньшее влияние при сходных температурных условиях – разность выходов наилучших опытов при 65 °C составила 1.23%. Кроме того, при температурах реакции не превышающих 40–45 °C выпадение осадка происходило крайне медленно (от двух до пяти суток), что позволило отбросить данную температурную область как потенциально нетехнологичную. Увеличение температуры реакции свыше 65 °C не приводило к дальнейшему увеличению выхода по реакции. Таким образом, в данном случае именно проведение реакции при 65 °C без введения оснований в промывную жидкость представляются нам оптимальными условиями данного процесса.
Испытания борсодержащих соединений на сельскохозяйственных культурах
В результате испытаний было исследование влияние отобранных композиций на всхожесть промывных жидкостей. По этой причине в ходе выделения преимущественно исследовалось влияние растворов на основе изопропанола, а также действие фактора температуры в ходе процесса на выход боратрана. В данном случае реакционная масса после окончания ожидаемого времени химической реакции подвергалась принудительному охлаждению до комнатной температуры, после чего производилась промывка. В ходе процесса использовался 10% избыток триэтаноламина, который по нашему предположению мог связывать часть образующейся влаги благодаря образованию разветвлённой сети водородных связей в собственной структуре, а также для увеличения растворимости борной кислоты в гетерогенной реакции (как и в случае способа с азеотропной отгонкой воды, использование большего количества триэтаноламина приводит к загрязнению продукта).
и энергию прорастания свеклы столовой (Beta vulgaris) и урожайность свеклы сахарной. Выбор компонентов и их соотношение в композициях производился с учётом индивидуальных особенностей объектов обработки, принимая во внимание установленные дозировки родственных или сходных по цели применения соединений, представленные в «Государственном Каталоге пестицидов и агрохимикатов, разрешенных к применению на территории Российской Федерации».
Влияние на энергию прорастания и всхожесть свеклы столовой
Обработка янтарной кислотой, взятой за стандарт, не повлияла на этот показатель, который остался на уровне контроля. Увеличение энергии прорастания было в вариантах с обработкой сукцинатом трис (2-гидроксиэтил) аммония (сукцината TEA) и смесью сукцината с боратраном (таблица 5).
Таблица 5.
Влияние препаратов на энергию прорастания и всхожесть свеклы столовой (Beta vulgaris)
Table 5.
Substance effectiveness in germination power and germinability of beet (Beta vulgaris) seeds
|
Препарат Substance |
Энергия прорастания, % Germination power, % |
Всхожесть, % Germinability, % |
|
Сукцинат TEA TEA Succinate |
39 |
51.3 |
|
Янтарная кислота Succinic acid |
29 |
45.3 |
|
Боратран Boratrane |
31 |
39.0 |
|
Борная кислота Boric acid |
31 |
42.0 |
|
О-крезоксиацетат TEA TEA o-cresoxyacetate |
32 |
33.0 |
|
Боратран + Сукцинат TEA Boratrane + TEA Succinate |
35 |
37.0 |
|
Вода (контроль) Water (control) |
28 |
31.3 |
В остальных вариантах этот показатель был на уровне 31–33%, что выше контрольного варианта на 3–5%. Обработка семян всеми препаратами, за исключением о-крезоксиацетата трис (2-гидроксиэтил) аммония и смеси боратрана с сукцинатом, способствовала повышению этого важного показателя качества семян. Наибольший эффект получен при обработке сукцинатом трис (2-гидроксиэтил) аммония (51.3%).
Важно отметить, что по сравнению с проростками вариантов борной и янтарных кислот и из трис (2-гидроксиэтил) аммониевых производных, имевших развитую корневую систему длиной 11–14 см, в варианте с о-крезоксиацетатом трис (2-гидроксиэтил) аммония, наблюдалось ингибирование длины роста корней (на 2–3 см по сравнению с контролем и составляла 3.5–4.5 см). Таким образом, лучшие результаты по обработке семян столовой свеклы получены при обработке их сукцинатом трис (2-гидроксиэтил) аммония: по сравнению с обработкой контролем и янтарной кислотой (стандарт) у семян повысилась энергия прорастания на 11 и 10%, всхожесть –
Влияние препаратов на морфобиологические показатели свеклы сахарной
на 20 и 6%, соответственно. Кроме того, проростки отличались развитой корневой системой.
Влияние на урожайность и качество свеклы столовой
Проведение испытаний на территории Киргизии было обусловлено фиксированием случаев симптомов дефицита бора на культуре сахарной свеклы (поражения листовой пластины, образование пустот в корнеплодах, нарушения вертикального роста культуры на второй год жизни) в условиях местных почв Чуйской долины. Композиция боратран + о -крезоксиацетат трис (2-гидроксиэтил) аммония + 1-хлорметилсила-тран продемонстрировала наилучший результат по длине корневой апикальной части растения, среднему весу растения и корнеплода (таблиц а 6) , увеличив их по сравнению с контролем на 9.58, 42.85 и 77.46%, соответственно. Контроль качества корнеплодов подтвердил наличие наименьшего числа свекл с повреждениями, вызванных условиями дефицита бора.
Таблица 6.
Table 6.
Composition effectiveness in morphobiology of sugar beet
|
Препарат | Composition |
Длина корня, см Root length, cm |
Средний вес растения, кг Average plant weight, kg |
Средний вес корнеплода, кг Average root-crop weight, kg |
|
Вода | Water |
31.3 |
2.266 |
1.433 |
|
«Сенгын-сенгын»© | Sengeun-sengeun© |
30.6 |
2.600 |
2.063 |
|
Боратран + TEA о-крезоксиацетат + 1-хлор-метилсилатран Boratrane + TEA o-cresoxyacetate + 1-chloromethylsilatrane |
34.3 |
3.237 |
2.543 |
Н.П. Карсункиной (РГАУ-МСХА имени К.А. Тимирязева) за проведение опытов по измерению всхожести и энергии прорастания семян свеклы столовой, а также помощь в интерпретации полученных результатов.
Список литературы Синтез борсодержащих производных трис (2-гидроксиэтил) аммония и их влияние на рост и развитие растений
- Chen M., Mishra S., Heckathorn S.A., Frantz J.M. et al. Proteomic analysis of Arabidopsis thaliana leaves in response to acute boron deficiency and toxicity reveals effects on photosynthesis, carbohydrate metabolism, and protein synthesis//Journal of Plant Physiology. 2014. V. 171. № 3. P. 235-242.
- Brown P.H., Bellaloui N., Wimmer M.A., Bassil E.S. et al. Boron in Plant Biology//Plant Biology. 2002. V. 4. P. 205-223.
- Abreu I., Poza L., Bonilla I., Bola?os L. Boron deficiency results in early repression of a cytokinin receptor gene and abnormal cell differentiation in the apical root meristem of Arabidopsis thaliana//Plant Physiology and Biochemistry. 2014. V. 77. P. 117-121.
- Koshiba T., Kobayashi M., Ishihara A., Matoh T. Boron nutrition of cultured tobacco BY2 cells. VI. Calcium is involved in early responses to boron deprivation//Plant and Cell Physiology. 2010. V. 51. № 2. P. 323-327.
- Goldbach H.E., Wimmer M.A. Boron in plants and animals: Is there a role beyond cell-wall structure?//Zeitschrift f?r Pflanzenern?hrung und Bodenkunde. 2007. V. 170. P. 39-48.
- Cong X., Jiang X., Huang M. -J., Zhong M. et al. Mechanism of cell wall loosening of cherry radish by the method of immunochemistry//Journal of South China Agricultural University. 2015. V. 46. № 3. P. 397-400.
- Pernak J., Syguda A., Janiszewska D., Materna K. et al. Ionic liquids with herbicidal anions//Tetrahedron. 2011. V. 67. P. 4838-4844.
- Herrera-Rodr?guez M.B., Gonz?lez-Fontes A., Rexach J., Camacho-Crist?bal J.J. et al. Role of Boron in Vascular Plants and Response Mechanisms to Boron Stresses//Plant Stress. 2010. V. 4 (2). P. 115-122.
- D?az-?lvarez A.E., Francos J., Lastra-Barreira B., Crochet P. et al. Glycerol and derived solvents: new sustainable reaction media for organic synthesis//Chemical Communications. 2011. V. 47. P. 6208-6227.
- Xiang H., Shi P., Bhattacharya P., Chen X. et al. Enhanced charging capability of lithium metal batteries based on lithium bis(trifluoromethanesulfonyl)imide-lithium bis(oxalato)borate dual-salt electrolytes//Journal of Power Sources. 2016. V. 318. P. 170-177.
- Wang Ch., Liang T., Wei Ch. Synthesis and characterization of triethanolamine borate//Advanced Materials Research. 2013. V. 709. P. 28-31.
- Karlov S.S., Selina A.A., Chernyshova E.S., Oprunenko Y.F. et al. Synthesis and characterization of metallatranes with phenyl substituents in atrane cage//Inorganica Chimica Acta. 2007. V. 360. P. 563-578.
- Bolgova Y.I., Kuznetsova G.A., Trofimova O.M., Voronkov M.G. Convenient and Fast Synthesis of Boratrane in Water Medium//Chemistry of Heterocyclic Compounds. 2013. V. 49 (8). P. 1246-1248.


