Синтез и гетероциклизация 4-метил-3-циннамил-сульфанил-1,2,4-триазола
Автор: Ильиных Е.С., Васильева А.Е.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 2 т.17, 2025 года.
Бесплатный доступ
В настоящей работе нами впервые исследовано взаимодействие 4-метил-1,2,4-триазол-3-тиола (1) с транс-циннамилхлоридом (2) в различных системах (i-PrOH-КOH, i-PrOH-Na, MeOH-Na, Me2CO-K2CO3), в результате чего синтезирован индивидуальный 4-метил-3-циннамилсульфанил-1,2,4-триазол (3). Установлено, что селективность реакций алкилирования соединения 1 не зависит от условий проведения реакций (растворитель, основание), однако с наибольшим выходом (89 %) целевой продукт 3 был получен в системе MeOH-Na. Строение синтезированного соединения 3 исследовано и доказано методами масс-спектрометрии (ГХ-МС) и спектроскопии ЯМР ¹Н и ¹³С. Выявлены основные закономерные направления фрагментации молекулярного иона S-производного 3, сопровождающиеся отщеплением метильного, бензильного и триазолилсульфидного радикалов. Доказательством протекания реакции алкилирования по атому серы является наличие в спектре ЯМР 1Н соединения 3 сигналов протонов группы -SCH2- при δ 4,06 м. д. Впервые исследована гетероциклизация 4-метил-3-циннамилсульфанил-1,2,4-триазола 3 под действием йода и брома в различных растворителях (иодирование - в хлороформе, ацетоне, дихлорметане, этаноле; бромирование - в хлороформе, дихлорметане) при соотношениях субстрат : йод (1 : 2) и субстрат : бром (1 : 1,5). Найдено, что независимо от условий реакций взаимодействие с йодом соединения 3 протекает региоселективно, сопровождается линеарным аннелированием тиазиниевого цикла и образованием бициклической конденсированной гетероциклической системы. В результате синтезированы новые иодсодержащие [1,2,4]триазоло[5,1-b][1,3]тиазиниевые системы - полииодид и иодид 6-иод-3-метил-7-фенил-6,7-дигидро-5Н-[1,2,4]триазоло[5,1-b][1,3]тиазиния (4, 5). В отличие от реакций иодирования, взаимодействие циннамилсульфида 3 с бромом в указанных условиях протекает нерегиоселективно: кроме продукта бромциклизации, бромида 6-бром-3-метил-7-фенил-6,7-дигидро-5Н-[1,2,4]триазоло[5,1-b][1,3]тиазиния (6), получен продукт присоединения брома, 3-[(2,3-дибром-3-фенилпропил)сульфанил]-4-метил-1,2,4-триазол (7). Доказательством протекания реакций гетероциклизации соединения 3 является отсутствие в спектрах ЯМР 1Н продуктов гетероциклизации 4, 5 и 6 сигналов протонов циннамильного фрагмента и наличие более сложной картины расщепления сигналов протонов тиазиниевого цикла.
4-метил-1, 2, 4-триазол-3-тиол, алкилирование, 4-метил-3-циннамилсульфа-нил-1, 2, 4-триазол, гетероциклизация, иод- и бромциклизация, иод- и бромсодержащие [1, 2, 4]-триазоло[5, 1-b][1, 3]тиазиниевые системы, хромато-масс-спектрометрия, спектроскопия ямр 1н и 13с, «эффект тяжелого атома»
Короткий адрес: https://sciup.org/147248069
IDR: 147248069 | УДК: 547.792.3+547.792.9 | DOI: 10.14529/chem250210
Synthesis and heterocyclization of 3-cinnamyl-sulfanyl-4-methyl-1,2,4-triazole
In the present paper the interaction between 4-methyl-1,2,4-triazole-3-thiol (1) and trans-cinnamyl chloride (2) under various conditions (i-PrOH-КOH, i-PrOH-Na, MeOH-Na, Me2CO-K2CO3) has been studied for the first time. As a result, individual 4-methyl-3-cinnamylsulfanyl-1,2,4-triazole (3) has been synthesized. It has been found that selectivity of the alkylation reactions of compound 1 does not depend on the reaction conditions (solvent, base), however, target product 3 has been obtained in the highest yield (89 %) in the MeOH-Na system. The structure of synthesized compound 3 has been studied and proved by mass spectrometry (GC-MS), as well as ¹H, ¹³C NMR spectroscopy. General predictable directions for fragmentation of the molecular ion of S-derivative 3, which are accompanied by elimination of methyl, benzyl, and triazolylsulfide radicals, have been revealed. The evidence that alkylation reaction occurs at the sulfur atom is the presence of signals for the -SCH2- protons at δ 4.06 ppm in the 1Н NMR spectra of compound 3. Heterocyclization of 4-methyl-3-cinnamylsulfanyl-1,2,4-triazole 3 has been studied for the first time under the action of iodine and bromine in various solvents (iodination in chloroform, acetone, dichloromethane, ethanol; bromination in chloroform, dichloromethane), and at different ratios substrate : iodine (1 : 2) and substrate : bromine (1 : 1.5). It has been found that the interaction of compound 3 with iodine proceeds regioselectively, regardless of the reaction conditions, and it is accompanied by the linear annelation of the thiazinium ring and formation of a bicyclic fused heterocyclic system. As a result, new iodine-containing [1,2,4]triazolo[5,1-b][1,3]thiazinium systems have been synthesized: 6-iodo-3-methyl-7-phenyl-6,7-dihydro-5H-[1,2,4]triazolo[5,1-b][1,3]thiazinium polyiodide and iodide (4, 5). In contrast to iodination reactions, the interaction of cinnamyl sulfide 3 with bromine proceeds non-regioselectively under the indicated conditions: in addition to the bromocyclization product, 6-bromo-3-methyl-7-phenyl-6,7-dihydro-5Н-[1,2,4]triazolo[5,1-b][1,3]thiazinium bromide (6), the bromine addition product, 3-[(2,3-dibromo-3-phenylpropyl)sulfanyl]-4-methyl-1,2,4-triazole (7), has been obtained. The evidence for heterocyclization reactions of compound 3 is the absence of signals for the cinnamyl protons and the presence of a more complicated splitting pattern of signals for the thiazinium ring protons in the 1H NMR spectra of heterocyclization products 4, 5, and 6. Keywords: 4-methyl-1,2,4-triazole-3-thiol, alkylation, 3-cinnamylsulfanyl-4-methyl-1,2,4-triazole, heterocyclization, iodo- and bromocyclization, iodine- and bromine-containing [1,2,4]triazolo[5,1-b]-[1,3]thiazinium systems, chromatography-mass spectrometry, 1H and 13C NMR spectroscopy, “heavy atom effect”
Текст научной статьи Синтез и гетероциклизация 4-метил-3-циннамил-сульфанил-1,2,4-триазола
Азотсодержащие гетероциклические соединения в настоящее время составляют большинство всех синтезируемых лекарственных веществ [1]. Это является одной из причин устойчивого синтетического и биологического интереса к химии таких классов соединений, как триазолы. 1,2,4-Триазолы, 1,2,4-триазолтиолы и их производные используются в медицине, проявляя бактерицидную, анальгетическую, нейролептическую, гипотензивную, спазмолитическую, противовоспалительную, фунгицидную и другие виды активности [2–7]. Соединения данного класса также нашли применение в качестве ингибиторов коррозии, в сельском хозяйстве (фунгициды, пестициды), электронике и производстве пластификаторов и клеев [8–11].
Наличие атома серы в структуре 1,2,4-триазол-3-тиолов дает возможность использовать эти соединения в органическом синтезе путем их дальнейшей S-функционализации [7, 12–14], в ча- стности, алкилированием алкенил- и алкинилгалогенидами [15–17]. В целом, различные S-непредельные производные азол- и азинтиолов служат удобным синтоном для синтеза конденсированных гетероциклических систем на их основе. В обзоре [18] обобщены данные по электрофильной гетероциклизации ненасыщенных серо- и фосфорсодержащих соединений. Ранее нами исследована электрофильная гетероциклизация ряда S-непредельных производных 4-метил-1,2,4-триазол-3-тиола [15], 5-трифторметил-1,2,4-триазол-3-тиола [16], 1-метилимидазол-2-тиола [19] и бензимидазол-2-тиола [20] под действием галогенов и показано, что региоселектив-ность реакций зависит от структуры исходного субстрата и условий реакций.
Введение в структуру производных азолов и других гетероциклических соединений атомов галогенов является перспективным направлением их модификации. Широкий спектр действия и высокий терапевтический эффект иодсодержащих лекарственных препаратов определяют актуальность физико-химических исследований органических соединений йода и прогнозирования их фармакологической активности [21].
Однако в литературе отсутствуют данные о синтезе 4-метил-3-циннамилсульфанил-1,2,4-триазола и исследовании его гетероциклизации под действием галогенов. Целью настоящей работы является разработка методов синтеза и исследование строения данного соединения и ранее неизвестных иод- и бромсодержащих [1,2,4]триазоло[5,1- b ][1,3]тиазиниевых систем, полученных на его основе.
Экспериментальная часть
Исходные соединения 4-метил-1,2,4-триазол-3-тиол 1 , транс -циннамилхлорид 2 являются коммерческими препаратами фирмы Alfa Aesar. A Johnson Matthey Company.
Синтез 4-метил-3-циннамилсульфанил-1,2,4-триазола (3) ( общая методика для систем (А) i-PrOH–КOH, (В) i-PrOH–Na, (С) MeOH–Na и (D) Me2CO–K2CO3 ). В плоскодонную колбу помещали 0,280 г (5 ммоль) КОН ( метод А ), 0,115 г (5 ммоль) Na ( методы В и С ), 0,690 г (5 ммоль) K 2 CO 3 ( метод D ), приливали 20 мл изопропилового спирта ( методы А и В ), метанола ( метод С ) или ацетона ( метод D ). Далее к полученным растворам ( методы А, В и С ) или суспензии ( метод D ) добавляли 0,575 г (5 ммоль) 4-метил-1,2,4-триазол-3-тиола 1 и 0,70 мл (5 ммоль) транс -циннамилхлорида 2 . Реакционную смесь перемешивали на магнитной мешалке. Через 7 суток отфильтровывали белый осадок, отгоняли растворитель, остаток обрабатывали хлороформом и фильтровали. Получали соединение 3 в виде светло-желтого масла, которое частично кристаллизовалось, выход 0,797 г (69 %) ( метод А ), 0,751 г (65 %) ( метод В ), 1,028 г (89 %) ( метод С ), 0,566 г (49 %) ( метод D ), R f 0,65. Масс-спектр (ЭИ, 70 эВ), m/z ( I отн ., %): 231 [M]+• (45), 117 [M – C 3 H 4 N 3 S]+ (100), 140 [M – C 6 H 5 CH 2 ]+ (30), 91 [M – C 3 H 4 N 3 S – C 2 H 2 ]+ (25). Спектр ЯМР 1Н, δ , м. д. ( J , Гц), СDCl 3 : 3,64 (3Н, с, 4-CH 3 ); 4,06 (2H, д, 3J = 7,5, –SCH 2 –); 6,33 (1Н, м, –СН=); 6,56 (1Н, д, 3J trans = 15,7, =CHPh); 7,23–7,36 (5Н, м, H Ar ); 8,58 (1Н, с, Н-5). Спектр ЯМР 13С, δ , м.д., СDCl 3 : 31,46 (–SСН 2 –); 36,52 (4-CH 3 ); 123,21 (–CH=); 126,49 (C Ar -2, C Ar -6); 128,05 (C Ar -4); 128,63 (=СНPh, C Ar -1, C Ar -3, C Ar -5); 134,43 (С-5); 136,16 (С-3).
Синтез полииодида 6-иод-3-метил-7-фенил-6,7-дигидро-5 Н -[1,2,4]триазоло[5,1- b ][1,3]-тиазиния ( 4 ) ( методы А и В ). К раствору 1,016 г (4 ммоль) йода в 5 мл CH 2 Cl 2 ( метод А ) или этанола ( метод В ) добавляли раствор 0,462 г (2 ммоль) 4-метил-3-циннамилсульфанил-1,2,4-триазола 3 в 5 мл CH 2 Cl 2 ( метод А ) или этанола ( метод В ). Через 7 суток получали полииодид 4 в виде темно-коричневых кристаллов, которые отфильтровывали и сушили. Выход 1,164 г ( метод А ), 1,028 г ( метод В ), т. пл. 105 °С. Спектр ЯМР 1Н, δ , м. д. ( J , Гц), ДМСО- d 6 : 3,71 (1H, дд, 2J = 13,6, 3J = 2,7, –SС H А H B –); 3,78 (3Н, с, 3-CH 3 ); 3,92 (1H, дд, 2J = 13,6, 3J = 7,8, –SСH А H B –); 5,21 (1Н, м, Н-6); 6,11 (1Н, д, 3J = 6,3, Н-7); 7,32–7,45 (5Н, м, H Ar ); 9,11 (1Н, с, Н-2). Спектр ЯМР 13С, δ , м.д., ДМСО- d 6 : 20,07 (С-6); 32,92 (С-5); 33,07 (3-CН 3 ); 69,12 (С-7); 127,45 (C Ar -1, C Ar -3, C Ar -5); 128,85 (C Ar -2, C Ar -6); 136,27 (C Ar -4); 144,97 (С-2); 150,15 (С-3а).
Синтез иодида 6-иод-3-метил-7-фенил-6,7-дигидро-5 Н -[1,2,4]триазоло[5,1- b ][1,3]тиази-ния ( 5 ) ( методы C и D ). К раствору 1,016 г (4 ммоль) йода в 5 мл CHCl 3 ( метод С ) или ацетона ( метод D ) добавляли раствор 0,462 г (2 ммоль) 4-метил-3-циннамилсульфанил-1,2,4-триазола 3 в 5 мл CHCl 3 ( метод С ) или ацетона ( метод D ). Через 7 суток отгоняли растворитель, получали масло темно-коричневого цвета, растворяли его в 10 мл ацетона и добавляли иодид натрия. Образовавшийся осадок отфильтровывали, промывали ацетоном и сушили. Получали иодид 5 в виде желтого порошка, выход 0,155 г (16 %) ( метод С ), 0,243 г (25 %) ( метод D ), т. пл. 153 °С. Данные ЯМР 1Н и 13С иодида 5 идентичны соответствующим данным ЯМР полииодида 4 .
Синтез бромида 6-бром-3-метил-7-фенил-6,7-дигидро-5 Н -[1,2,4]триазоло[5,1- b ][1,3]ти-азиния ( 6 ) ( методы А и В ). К раствору 0,462 г (2 ммоль) 4-метил-3-циннамилсульфанил-1,2,4-триазола 3 в 5 мл CHCl 3 ( метод А ) или CH 2 Cl 2 ( метод В ) добавляли по каплям при температуре 0–5 °С раствор 0,15 мл (3 ммоль) брома. Через 7 суток отгоняли растворитель, остаток обрабатывали ацетоном, отфильтровывали белый порошок бромида 6 , выход 0,219 г (28 %) ( метод А ), 0,258 г (33 %) ( метод В ), т. пл. 143 °С. Спектр ЯМР 1Н, δ , м. д. ( J , Гц), ДМСО- d 6 : 3,66 (1H, дд, 2J = 14,0, 3J = 2,4, –SС H А H B –); 3,83 (3Н, с, 3-CH 3 ); 3,93 (1H, дд, 2J = 14,0, 3J = 7,5, –SСH А H B –); 5,45 (1Н, м, Н-6); 6,26 (1Н, д, 3J = 4,6, Н-7); 7,33–7,46 (5Н, м, H Ar ); 9,29 (1Н, с, Н-2). Спектр ЯМР 13С, δ , м.д., ДМСО- d 6 : 31,10 (С-5); 33,05 (3-CН 3 ); 44,25 (С-6); 67,71 (С-7); 127,08 (C Ar -1, C Ar -3, C Ar -5); 128,98 (C Ar -2, C Ar -6); 135,56 (C Ar -4); 145,42 (С-2); 150,14 (С-3а).
Индивидуальность синтезированных соединений контролировали методом ТСХ на пластинах SilufolUV-254 в системе 2-пропанол-гексан (3 : 1), обнаружение в УФ-свете (254 нм) облучателя хроматографического УФС 254/365.
Температуры плавления установлены на аппарате для определения температуры плавления «ПТП ТУ-25-11-1144-76» и не корректировались.
Масс-спектры (ЭИ, 70 эВ) сняты на хромато-масс-спектрометре фирмы Shimadzu QGMS QP-2010 Ultra.
Спектры ЯМР 1H, 13C записаны на приборе Bruker DRX-400 в ДМСО- d 6 и СDCl 3 , внутренний стандарт ‒ ТМС.
Обсуждение результатов
Теоретически, реакции алкилирования 4-метил-1,2,4-триазол-3-тиола ( 1 ) вследствие его ти-он-тиольной таутомерии могут протекать как по атому серы, так и по атому азота. Согласно литературным данным, использование основания в реакциях данного типа смещает равновесие в сторону более устойчивой тиольной формы, что положительно сказывается на селективности процесса.
В настоящей работе с целью расширения ряда S-алкенильных производных соединения 1 нами впервые осуществлено его алкилирование транс -циннамилхлоридом ( 2 ) с использованием разных основных систем (( А ) i -PrOH–КOH, ( В ) i -PrOH–Na, ( С ) MeOH–Na и ( D ) Me 2 CO–K 2 CO 3 ). В результате во всех системах нами синтезирован индивидуальный продукт S-алкилирования, 4-метил-3-циннамилсульфанил-1,2,4-триазол ( 3 ), в виде закристаллизованного масла светложелтого цвета с выходами 69 % (метод А ), 65 % (метод В ), 89 % (метод С ) и 49 % (метод D ) (схема 1). Варьирование условий реакции позволило определить наиболее эффективную методику (метод С ) для селективного синтеза целевого продукта.
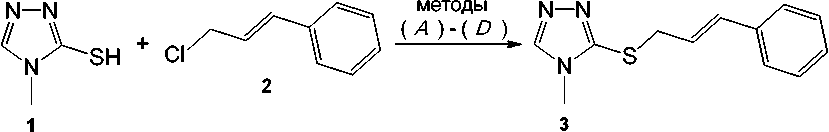
И) /-PrOH-KOH, (S) /-PrOH-Na, (C) MeOH-Na, (D) Me2CO-K2CO3 Выходы 69 % И), 65 % (S), 89 % (C), 49 % (D)
Схема 1. Синтез 4-метил-3-циннамилсульфанил-1,2,4-триазола (3)
Индивидуальность и чистота синтезированного соединения 3 контролировались с помощью тонкослойной хроматографии (ТСХ) ( R f 0,65), а его строение было исследовано и доказано методами масс-спектрометрии (ГХ–МС) и спектроскопии ЯМР ¹Н и ¹³С.
В масс-спектре соединения 3 пик молекулярного иона М+ ˙ с m/z 231 имеет среднюю интенсивность (45 %) и претерпевает различные направления фрагментации (схема 2). Наиболее интенсивный пик иона с m/z 117 принадлежит фрагментному циннамильному катиону, образующемуся в результате фрагментации по связи S–C. Менее интенсивные пики ионов с m/z 140 и 91 принадлежат фрагментным ионам, образующимся в результате выброса бензильного радикала из молекулярного иона и молекулы ацетилена из циннамильного катиона, соответственно.
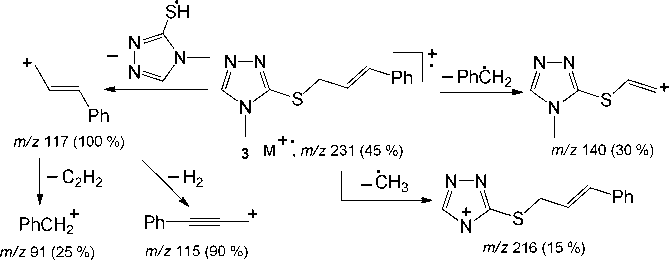
Схема 2. Фрагментация молекулярного иона соединения 3 при ГХ–МС анализе
О протекании алкилирования по атому серы и образовании сульфида 3 свидетельствует наличие в спектре ЯМР 1Н дублета протонов –SCH 2 – при δ 4,06 м. д. Кроме того, при δ 6,33 и 6,56 м. д. наблюдаются мультиплет и дублет протонов –СH= и =СHPh, соответственно. Большое значение КССВ этих двух протонов (3 J trans = 15,7 Гц) свидетельствует о транс -расположении заместителей относительно двойной связи.
В спектре ЯМР 13С соединения 3 сигналы при δ 31,46 и 36,52 м. д. относятся к сигналам атомов углерода групп –SCH2– и –NCH3, соответственно. Самый слабопольный сигнал (при δ 136,16 м.д.) закономерно дает углерод С-3 триазольного цикла, связанный с двумя атомами азота (N-2, N-4) и атомом серы.
Полученный 4-метил-3-циннамилсульфанил-1,2,4-триазол 3 в дальнейшем был использован для исследования его реакций электрофильной гетероциклизации под действием йода и брома с целью синтеза новых представителей [1,2,4]триазоло[5,1-b][1,3]тиазиниевых систем. Ранее [15] нами было показано, что региоселективность реакций гетероциклизации других различных S-непредельных производных 4-метил-1,2,4-триазол-3-тиола 1 зависит от характера заместителя при атоме серы и условий реакций: в разных случаях реакции сопровождались линеарным замы- канием тиазолиевого или тиазиниевого циклов.
Иодирование соединения 3 исследовано нами в различных растворителях (( А ) CH2Cl2, ( В ) EtOH, ( С ) CHCl 3 , ( D ) Me 2 CO) при соотношении субстрат : йод, равном 1 : 2. Установлено, что взаимодействие соединения 3 с двукратным избытком йода в указанных растворителях сопровождается гетероциклизацией искомого циннамилсульфида, замыканием шестичленного цикла и образованием индивидуального продукта гетероциклизации, полииодида 6-иод-3-метил-7-фенил-6,7-дигидро-5 Н -[1,2,4]триазоло[5,1- b ][1,3]тиазиния ( 4 ).
В результате реакций, проведенных по методам (А) и (В) , полииодид 4 был выделен в виде блестящих темно-коричневых кристаллов. Полученный в методах (С) и ( D ) полииодид 4 представлял собой темно-коричневое масло, действием на которое NaI в ацетоне был выделен иодид 6-иод-3-метил-7-фенил-6,7-дигидро-5 Н -[1,2,4]триазоло[5,1- b ][1,3]тиазиния ( 5 ) в виде желтого порошка с выходами 16 % (метод С ) и 25 % (метод D ) (схема 3).
Строение полииодида 4 (в виде кристаллов) и иодида 5 исследовано и доказано методами ЯМР 1Н и 13С спектроскопии. Спектры ЯМР 1Н и 13С полииодида 4 идентичны соответствующим спектрам иодида 5 . Спектр ЯМР 1Н иодида 5 приведен на рис. 1.
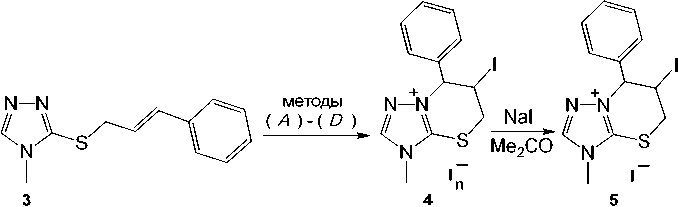
(A) 2I2, CH2CI2, 20-25 °C; (B) 2I2. EtOH, 20-25 °C; (C) 2I2. CHCI3i 20-25 °C; (D) 2I2i Me2CO, 20-25 °C Выходы иодида 5 16 % (С), 25 % (D)
Схема 3. Иодциклизация 4-метил-3-циннамилсульфанил-1,2,4-триазола (3)
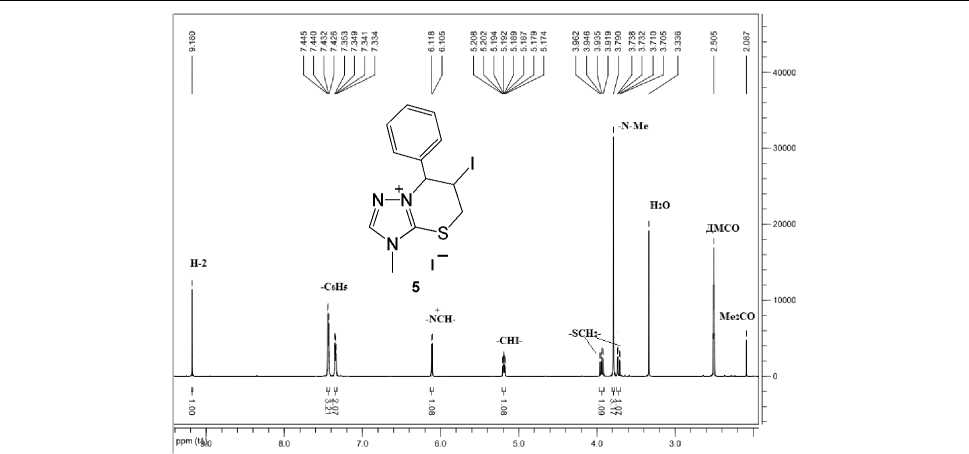
Рис. 1. Спектр ЯМР 1Н иодида 6-иод-3-метил-7-фенил-6,7-дигидро-5 Н -[1,2,4]триазоло[5,1- b ][1,3]тиазиния (5)
Док а за т е ль с тв ом п роте к ания реакции гетероциклизации циннамилсульфи д а 3 является отсутствие в спектрах ЯМР 1Н пол и и од и д а 4 и иодида 5 сигналов протонов циннамильного фрагмента и н али чи е б олее с л ожн ой картины расщепления сигналов протонов тиа зи н иевого ц и к л а .
К роме т ого, н аб л ю д ае тс я с мещение сигнала гетероароматического протон а Н -2 триазольного ц и к л а в с п ек тра х п родук тов и од ц и к л иза ц и и в более слабое поле на δ 0,53–0,60 м. д. по сравнению с с оотв е тс тв у ю щ и м с и гна лом п ротона в с п ек тре ис ход н ог о с о е д и н е н и я 3 , что обусловлено образов а н и е м за ряже н н ой к онд е н с и ров а н н ой ге те р оц и кли че с к ой с и с те м ы.
В спектрах ЯМР 13С п ол и и од и д а 4 и иодида 5 самый слабопольный сигнал ( δ 150,15 м. д.) соответс тв уе т уз л ов ом у а тому у гл е род а С-3a, связанному с электроотрицательными атомом серы и двумя атомами азота (N-3, N-8). Несмотря на выраженную электроотрицательность атома йода, сигнал атома углерода С- 6, н епосредственно связанного с йодом, расположен в области достаточно сильного поля ( δ 2 0, 06 м. д.), что обусловлено «эффектом тяжелого атома» [22]. Данный э ф фек т встре ча е т с я в с п ек тра х Я МР 13С различных галогенпроизводных ароматических и гете-роароматических сое д и нен ий [23–27].
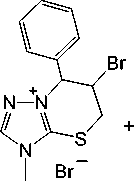
Бромирование 4-метил-3-ц и н н а ми лс у ль фа н и л-1,2,4-триазола 3 полуторакратным избытком брома исследовано нами в C HC l 3 (метод (А) ) и CH 2 Cl 2 (метод (В) ) при охлаждении льдом до 0– 5 о С. У с та н ов лено, что в за и мод е й с тв и е сое ди нен ия 3 с бромом в указанных условиях, аналогично его ге те роц ик ли за ц и и п о д д е йствием йода, протекает по пути аннелировани я ти а зи н и е в ого ц и кл а и при в од и т к о б раз ов ани ю б роми да 6-бром-3-метил-7-фенил-6,7-дигидро-5 Н -[1,2,4]-триазоло[5,1- b ][1,3]тиазиния ( 6 ) в виде белого порошка, не растворимого в ацетоне, с выходами 28 % (метод А ) и 33 % (метод В ) (схема 4).
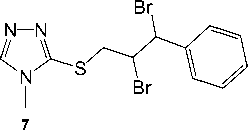
Однак о в отли чи е от ре ак ции с йодом, бромирование циннамилсульф и да 3 является менее се лек ти в н ым п роц ес с ом : п об очн ым п ро д у к том реак ц и й, п о -видимому, является продукт присоеди н е н ия б рома п о д в ой ной с в язи ц и н н а ми льн ого фра гм е н та – 3-[(2,3-дибром-3-фенилпропил)-сульфанил]-4-метил-1,2,4-т ри аз ол (7 ). Соединение 7 , в отличие от бромида 6 , представляет собой мас ло же лто го ц в е та , к от орое хор ош о р а с тв оряе тся в а ц е тон е .
Строение бромида 6 и ссле дов а н о и д о к а за н о ме т о д а ми Я МР 1Н и 13С спектроскопии. Налич ие б оле е с ло жн ой к арт и н ы расщепления сигналов протонов в спектре Я МР 1Н бромида 6 (рис. 2) и о т сутст в и е сигн алов п ротонов циннамильного фрагмента является доказательством протекания реак ц и и ге тероц и к ли за ц и и циннамилсульфида 3 . В частности, сигналы протонов – SСH 2 – ти аз и н и е в ого ц и к ла ра с ще п ляю т с я н а д в а д у б ле та д у б ле тов п ри δ 3,66 и 3,93 м.д., тогда как сигнал протонов –SCH 2 – и сход н ого соед и н е н ия 3 представляет собой дублет при δ 4,06 м. д.
К роме т ого, н аб л ю д ае тс я с ме щ е н ие с и гн ала гетероароматического протона Н-2 триазольного цикла в спектре продукта бром циклизации 6 в более слабое поле на δ 0,71 м. д. по сравнению с соответствующим сигналом п ротон а в спектре исходного соединения 3 , что обусловлено образов ани е м за ряженн ой к он ден с и ров а н н ой ге т е роц и к личе с к ой с ист ем ы .
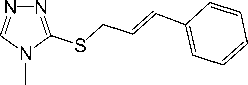
1. методы
( А ) , ( B )
2. Me 2 CO
( A ) 1,5Br 2, CHCl 3, 0-5 o C; ( B ) 1,5Br 2, CH 2 Cl 2, 0-5 oC; выходы бромида 6 28 % ( A ), 33 % ( B )
Схема 4. Бромирование 4-метил-3-циннамилсульфанил-1,2,4-триазола (3)
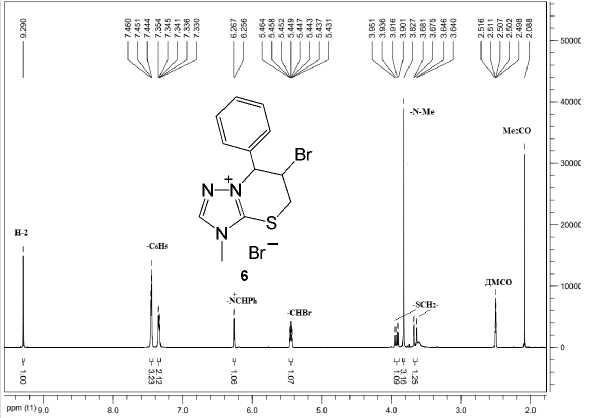
Рис. 2. Спектр ЯМР 1Н бромида 6-бром-3-метил-7-фенил-6,7-дигидро-5 Н -[1,2,4]триазоло[5,1- b ][1,3]тиазиния (6)
В отл и чи е от а то ма й од а, а том брома не дает «эффект тяжелого атома», поэто м у в сп е к тре Я М Р 13С бромида 6 си гн а л ато ма у гле род а С -6, связанного с бромом, расположен закономерно в слабом поле при δ 44,25 м. д . Са м ый с ла б оп оль н ый с и гн а л при δ 150,14 м. д. дает углерод С-3а триазольного ц и к ла , св я за нн ый с э ле кт р оотриц а те ль н ыми а то м ом с е ры и дву м я а то ма м и а з от а (N-3, N-8).
Заключение
У ст ан овл е н о, что на и б ол е е э ффективная методика для селективного синте з а ранее неизвестного 4-метил-3- ци н н а ми лс у ль фа н и л-1,2,4-триазола с выходом 89 % основана на взаимодействии 4-метил-1,2,4-триазол-3-т и ола с транс -циннамилхлоридом в системе MeOH–Na. Гетероциклизация 4-метил-3-ц и н н а ми лс у ль фа н и л-1,2,4-триазола под действием йода (иодциклизация) протека ет ре ги о с е лек ти в н о с а нн е ли рованием исключительно тиазиниевого цикла н е за в и с и мо от у с л овий реакции. В от л и чие от ре ак ций иодирования, взаимодействие синтезированного циннамил-сульфида с б р омом п ротек а е т нерегиоселективно: кроме продукта бромц и к ли за ц и и , п олу че н продукт присоединения брома. Строение новых иод- и бромсодержащих [1,2,4]триазоло[5,1- b ]-[1,3]тиазиниевых систем под роб н о и с с ле д о в а н о и док а за н о методами спектроскопии ЯМР ¹Н и ¹³С, в ыя в ле н ы об щ и е за к он о мер н ос т и и сп е ци фи че с ки е о с об е н н ос ти сп е к тро в полученных соединений.


