Синтез и гетероциклизация 8-R-транс-3-циннамилсульфанил-5H-[1,2,4]триазино[5,6-b]индолов и метил 4-(8-R-5H-[1,2,4]триазин[5,6-b]индол-3-сульфанил)бут-2-еноатов
Автор: Рыбакова Анастасия Владимировна, Старцева Анна Андреевна, Ким Дмитрий Гымнанович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 3 т.14, 2022 года.
Бесплатный доступ
Конденсацией водного раствора изатина и 5-бромизатина с тиосемикарбазидом получены β-тиосемикарбазон изатина и β-тиосемикарбазон 5-бромизатина, соответственно. Последующей циклизацией полученных тиосемикарбазонов в растворе гидроксида натрия при нагревании осуществлен синтез 5 Н -[1,2,4]триазино[5,6- b ]индол-3-тиона (1а) и 8-бром-5 Н -[1,2,4]триазино[5,6- b ]индол-3-тиона (1b). Соединения 1а и 1b были изучены нами в реакциях алкилирования транс -циннамилхлоридом и метиловым эфиром 4-бромкротоновой кислоты. При этом из соединения 1а были синтезированы неизвестные ранее транс -3-циннамилсульфанил-5 H -[1,2,4]триазино[5,6- b ]индол (2a), метил 4-(8-бром-5 H -[1,2,4]триазин[5,6- b ]индол-3-сульфанил)бут-2-еноат (3a), из соединения 1b - 8 - бром -транс -3-циннамилсульфанил-5 H -[1,2,4]триазино[5,6- b ]индол (2b) и метил 4-(8-бром-5 H -[1,2,4]триазин[5,6- b ]индол-3-сульфанил)бут-2-еноат (3b). В спектрах ЯМР 1Н соединений 2а и 2b протоны S-CH2-группы образуют дублет в области 4,13 и 4,15 м. д. соответственно, в спектрах соединений 3а и 3b аналогичные протоны резонируют при 4,09 и 4,12 м.д. соответственно. Наличие электроноакцепторного атома брома в 8-м положении в структурах 2b и 3b приводит к незначительному смещению сигналов ароматических протонов индольного кольца и сигнала протона NH-группы в область более слабого поля по сравнению с аналогичными сигналами протонов в спектре ЯМР 1Н соединений 2a, 3a, не содержащих атом брома в индольном фрагменте. Реакции гетероциклизации S-производных триазино[5,6- b ]индол-3-тионов под действием иода и брома привели к аннелированию шестичленного тиазинового цикла и образованию новых поликонденсированных систем в виде тригалогенидов 8-R-3-галоген-4-R1-2,3,4,11-тетрагидро[1,3]тиазино[3׀,2׀:2, 3][1,2,4]триазин[5,6- b ]индолия. В структурах синтезированных нами тригалогенидов протоны группы SCH2 находятся рядом с асимметрическим атомом углерода, являются диастереотопными и в спектрах ЯМР 1Н образуют дублеты дублетов в области 3,35-5,36 м.д.
5н-[1, 2, 4]триазино[5, 6-b]индол-3-тион, 8-бром-5н-[1, 2, 4]триазино[5, 6-b]индол-3-тион, транс-3-циннамилсульфанил-5h-[1, 2, 4]триазин[5, 6-b]индол, метил 4-(8-бром-5h-[1, 2, 4]триазин[5, 6-b]индол-3-сульфанил)бут-2-еноат, 8-бром-транс-3-циннамилсульфанил-5h-[1, 2, 4]триазино[5, 6-b]индол и метил 4-(8-бром-5h-[1, 2, 4]триазин[5, 6-b]индол-3-сульфанил)бут-2-еноат, тригалогениды 8-r-3-галоген-4- r1-2, 3, 4, 11-тетрагидро[1, 3]тиазино[3׀, 2׀:2, 3][1, 2, 4]триазин[5, 6-b]индолия
Короткий адрес: https://sciup.org/147238625
IDR: 147238625 | УДК: 547.873 | DOI: 10.14529/chem220310
Synthesis and heterocyclization of 8-R-trans-3-cinnamylsulfanyl-5H-[1,2,4]triazino[5,6-b]indoles and methyl 4-(8-R-5H-[1,2,4]triazine[5,6-b]indole-3-sulfanyl)but-2-enoates
Isatin β-thiosemicarbazone and 5-bromoisatin β-thiosemicarbazone were obtained by condensation of aqueous solutions of thiosemicarbazide with isatin and 5-bromoisatin, respectively. Then 5 H -[1,2,4]triazino[5,6- b ]indole-3-thione (1a) and 8-bromo-5 H -[1,2,4]triazino[5,6- b ]indole-3-thione (1b) were synthesized by subsequent cyclization of obtained thiosemicarbazones in heated sodium hydroxide solution. Compounds 1a and 1b were studied in alkylation by trans -cinnamyl chloride and methyl ester of 4-bromocrotonic acid. At that, previously unknown trans -3-cinnamylsulfanyl-5 H -[1,2,4]triazino[5,6- b ]indole (2a) and methyl 4-(8-bromo-5 H -[1,2,4]triazine[5,6- b ]indole-3-sulfanyl)but-2-enoate (3a) were synthesized from compound 1a, 8-bromo- trans -3-cinnamylsulfanyl-5 H -[1,2,4]triazino[5,6- b ]indole (2b) and methyl 4-(8-bromo-5 H -[1,2,4]triazine[5,6- b ]indole-3-sulfanyl)but-2-enoate (3b) were synthesized from compound 1b. The protons of the S-CH2 group form a doublet band in the region of 4.13 and 4.15 p.p.m. in the 1H NMR spectra of compounds 2a and 2b, respectively. Similar protons in the 1H NMR spectra of compounds 3a and 3b resonate at 4.09 and 4.12 p.p.m., respectively. The presence of the bromine atom, which is an electron acceptor, at locant 8 in structures 2b and 3b leads to a slight shift of the signals of aromatic protons of the indole ring, as well as the signal of the NH group proton, to a weaker field in comparison to similar proton signals in the 1H NMR spectra of compounds 2a and 3a that do not contain bromine atoms in the indole fragment. Heterocyclization of S-derivatives of triazino[5,6- b ]indole-3-thiones by iodine and bromine leads to annelation of the six-membered thiazine cycle and formation of new polycondensation systems in the form of 8-R-3-halo-4-R1-2,3,4,11-tetrahydro[1,3]thiazino[3׀,2׀:2,3][1,2,4]triazine[5,6- b ]indolium trihalides. The protons of the SCH2 group in structures of the synthesized trihalides are located next to the asymmetric carbon atom, they are diastereotopic and form doublets of doublets in the region of 3.35-5.36 p.p.m. in the 1H NMR spectra.
Текст научной статьи Синтез и гетероциклизация 8-R-транс-3-циннамилсульфанил-5H-[1,2,4]триазино[5,6-b]индолов и метил 4-(8-R-5H-[1,2,4]триазин[5,6-b]индол-3-сульфанил)бут-2-еноатов
Известно, что многие соединения, построенные на 5H-[1,2,4]триазин[5,6-b]индол-3-тионном каркасе, являются фармакологически активными [1–3]. В частности в литературе описывается, что 5H-[1,2,4]триазин[5,6-b]индол-3-тион и его производные обладают широким спектром биологической активности, включая противовоспалительное, противомикробное, обезболивающее, гипотензивное, противоопухолевое, кардиотоническое, нейролептическое, ноотропное, туберкулостатическое, противовирусное, противомалярийное и противопаразитарное действия [3-10]. Некоторые производные 1,2,4-триазиноиндол-3-тиона активны по отношению к кишечным паразитам, а также вызывают нормализацию нейроэндокринных реакций в условиях стресса и гипертермии [11, 12]. Также они могут выступать в качестве модуляторов эстрогеновых рецепторов и ингибиторов циклинзависимых киназ [13-16]. В целом несимметрические триазины применяют в синтезе различных красителей, полимеров, химических покрытий, фотографических материалов и полупродуктов синтеза пластмасс [17-22].
Изучение производных 1,2,4-триазин-3-тиона привело к открытию гиперактивности обонятельных систем крыс. Действие триазиновых гербицидов на животных приводит к дисфункции массы и температуры тела, спаривания и активности. В больших дозах данные вещества могут служить ядами для нежелательных грызунов [23-25].
При анализе активности триазинов было выявлено, что наибольшая активность соединения проявляется в роли ингибитора ферментов, при этом при добавлении алкильных фрагментов в структуру соединения данная биологическая активность уменьшается [25].
Таким образом, производные 1,2,4-триазин-3-тиона являются важнейшим классом органических соединений, применяемых в медицине [1-8], электрохимии [17], в качестве катализаторов [15] и хемосенсоров [18].
Одна из наиболее значимых областей исследования 5 H -[1,2,4]триазин[5,6- b ]индол-3-тиона -это изучение их реакций с различными бифункциональными электрофильными реагентами. Подобные превращения дают возможность получить новые аннелированные поликонденсирован-ные гетероциклические системы [12, 15, 17-20].
В литературе [3–5] имеются данные о синтезе и свойствах некоторых S-алкенильных(алкильных) производных 5 Н -[1,2,4]триазино[5,6- b ]индол-3-тиона (1a) , но бромзамещённый 8-бром-5 Н -[1,2,4]триазино[5,6- b ]индол-3-тион (1b) и его S-производные практически не описаны в литературе.
В настоящей работе осуществлен синтез 5 Н -[1,2,4]триазино[5,6- b ]индол-3-тиона 1a и 8-бром - 5 Н -[1,2,4]триазино[5,6- b ]индол-3-тиона 1b и на их основе получены неизвестные ранее S-производные, для которых изучено дальнейшее взаимодействие с бромом и йодом.
Экспериментальная часть
Спектры ЯМР 1 Н соединений записаны на спектрометре Bruker DRX-400 (400 МГц), внутренний стандарт ТМС.
5 H -[1,2,4]Триазино[5,6- b ]индол-3-тион 1а и 8-бром-5 Н -[1,2,4]триазино[5,6- b ]индол-3-тион 1b получены конденсацией 1 H -индол-2,3-диона и его бромзамещенного производного с солянокислым тиосемикарбазидом по известной методике [3] с выходом 89 и 71 % соответственно.
Общая методика синтеза 8-R-транс-3-циннамилсульфанил-5H-[1,2,4]триазино[5,6- b]индолов (2а, 2b)
К раствору 1,000 ммоль индолтриазина в 30 мл ДМСО добавляли концентрированный раствор 0,040 г (1 ммоль) NaOH в 0,120 мл воды и 0,140 мл (1 ммоль) транс -циннамилхлорида. Реакционную смесь перемешивали в течение суток. После чего для выделения продукта к реакционной смеси добавляли избыток воды (50 мл), отфильтровывали образующийся осадок и сушили.
Для синтеза транс -3-циннамилсульфанил-5 H -[1,2,4]триазино[5,6- b ]индола 2а брали 0,202 г (1 ммоль) индолтриазина 1а . Выход 0,192 г (69 %). Т пл 235 °С с разложением.
Спектр ЯМР 1 Н (400 МГц, DMSO-d6) 5, м. д. / J , Гц: 4,12 (2H, д, J = 7,1, SCH 2 ); 6,41-6,47 (1H, м, -CH=CHPh); 6,71-6,75 (1H, м, -CH=CHPh); 7,17-7,40 (6H, м, Н-8, С 6 Н 5 ); 7,54-7,56 (1H, м, H-6), 7,61-7,64 (1H, м, H-7); 8,27-8,29 (1H, м, H-9); 12,52 (1Н, уш. с., NH).
Для синтеза 8 - бром -транс -3-циннамилсульфанил-5 H -[1,2,4]триазино[5,6- b ]индола 2b брали 0,281 г (1 ммоль) 8-броминдолтриазина 1b . Жёлтый осадок перекристаллизовывали из смеси ДМСО:вода (1:2). Выход 0,185 г (58 %). Тпл 263-265 °С с разложением.
Спектр ЯМР 1 Н (400 МГц, DMSO-d6) 5, м. д. / J , Гц: 4,15 (2H, д, J = 7,2, SCH 2 ); 6,42-6,46 (1H, м, -CH=CHPh); 6,75-6,79 (1H, м, -CH=CHPh); 7,23-7,45 (6H, м, Н-8, С 6 Н 5 ); 7,55-7,58 (1H, м, H-6), 7,80-7,83 (1H, м, H-7); 8,47-8,49 (1H, м, H-9); 12,83 (1Н, уш. с., NH).
Общая методика синтеза метил 4-(5 H -[1,2,4]триазин[5,6- b ]индол-3-сульфанил)бут-2-еноатов (3а, 3b)
К раствору 1,310 ммоль индолтриазина в 30 мл ДМСО добавляли концентрированный раствор 0,052 г (1,3 ммоль) NaOH в 0,120 мл воды и 0,154 мл (1,310 ммоль) метилового эфира 4-бромкротоновой кислоты. Реакционную смесь перемешивали в течение суток. После чего для выделения продукта к реакционной смеси добавляли избыток воды (50 мл), отфильтровывали и сушили осадок.
Для синтеза метил 4-(5 H -[1,2,4]триазин[5,6- b ]индол-3-сульфанил)бут-2-еноата (3а) брали 0,265 г (1,3 ммоль) индолтриазина 1а. Выход: 0,215 г (76 %). Т пл 242–244 °С с разложением.
Спектр ЯМР 1Н (400 MГц, DMSO-d6) δ, м. д. / J , Гц: 3,65 (3H, c, ОCH 3 ); 4,12 (2H, д, J =7,0, SCH 2 ); 6,20 (1H, д, J = 15,5, C H -CООМе); 7,05 (1H, м, -CH=); 7,45 (1H, м, H-8); 7,58–7,60 (1H, м, H-6), 7,68–7,70 (1H, м, H-7); 8,30–8,32 (1H, м, H-9); 12,69 (1Н, уш. с., NH).
Для синтеза метил 4-(8-бром-5 H -[1,2,4]триазин[5,6- b ]индол-3-сульфанил)бут-2-еноата (3b) брали 0,240 г (1,2 ммоль) 8-броминдолтриазина 1b . Выход 0,214 (60 %). Тпл 241-243 °С с разложением.
Спектр ЯМР 1Н (400 MГц, DMSO-d6) δ, м. д. / J , Гц: 3,70 (3H, c, ОCH 3 ); 4,12 (2H, д, J = 6,9, SCH 2 ); 5,73 (1H, д, J = 15,1, C H -CООМе); 7,03 (1H, м, -CH=); 7,54–7,57 (1H, м, H-6), 7,83–7,85 (1H, м, H-7); 8,46–8,48 (1H, м, H-9); 12,85 (1Н, уш. с., NH).
Трииодид 3-иод-4-фенил-2,3,4,11-тетрагидро[1,3]тиазин[3|,2|:2,3] [1,2,4]триазино[5,6- b ]индолия 4a
К раствору 0,100 г (0,3 ммоль) транс -3-циннамилсульфанил-5 H -[1,2,4]триазин[5,6- b ]индола в 40 мл хлороформа добавляли раствор 0,159 г (0,6 ммоль) йода в 10 мл хлороформа. Реакционную смесь оставляли до образования темно-бурых кристаллов. Полученные кристаллы отфильтровывали и сушили. Выход 0,112 г (79 %). Т пл 182–184 °С.
Спектр ЯМР 1Н (400 MГц, DMSO-d6) δ, м. д.: 3,35 (1H, д.д, 2J = 14,5; 3J = 3,1; SCH 2 ); 3,54 (1H, д.д, 2J = 14,5; 3J = 2,2; SCH 2 ), 5,74 (1H, м, CHI); 6,51 (1H, м., -CHPh); 7,32–7,43 (5H, м, С 6 Н 5 ); 7,54–7,58 (1H, м, H-8); 7,73–7,75 (1H, м, H-10); 7,88–7,92 (1H, м, H-9); 8,20–8,23 (1H, H-7).
Трибромид 3-бром-4-фенил-2,3,4,11-тетрагидро[1,3]тиазино[3|,2|:2,3][1,2,4]триазин[5,6- b]индолия 4b
К раствору 0,180 г (0,5 ммоль) транс -3-циннамилсульфанил-5 H -[1,2,4]триазин[5,6- b ]индола в 40 мл ледяной уксусной кислоты добавляли по каплям 0,058 мл (1 ммоль) брома в 10 мл ледяной уксусной кислоты при постоянном охлаждении льдом. Реакционную смесь оставляли на сутки при комнатной температуре, затем полностью испаряли растворитель. Остаток собирают, выход 0,089 г (65 %). Т пл больше 250 °С.
Спектр ЯМР 1Н (400 MГц, DMSO-d6) δ, м. д.: 3,48 (1H, д. д, 2J = 14,4; 3J = 2,6; SCH 2 ); 3,68 (1H, д. д, 2J = 14,4; 3J = 1,2; SCH 2 ); 5,82 (1H, м, CHBr); 6,56 (1H, м, -CHPh); 7,36–7,43 (5H, м, С 6 Н 5 ); 7,54– 7,56 (1H, м, H-8); 7,78–7,80 (1H, м, H-10); 7,88–7,92 (1H, м, H-9); 8,20–8,22 (1H, м, H-7).
Трииодид 8-бром-3-иод-4-фенил-2,3,4,11-тетрагидро[1,3]тиазин[3|,2|:2,3]
-
[1,2,4] триазино[5,6- b ]индолия (4c)
К раствору 0,218 г (0,5 ммоль) 8-бром- транс -3-циннамилсульфанил-5 H -[1,2,4]триазин[5,6- b ]индола в 40 мл хлороформа добавляли раствор 0,171 г (1 ммоль) иода в 10 мл хлороформа. Реакционную смесь оставляли до образования темно-бурых кристаллов. Полученные кристаллы отфильтровали и сушили. Выход 0,209 г (81%). Т пл 198–201 °С.
Спектр ЯМР 1Н (400 MГц, DMSO-d6) δ, м. д.: 3,35 (1H, д. д, 2J = 14,5; 3J = 2,0; SCH 2 ); 3,60 (1H, д. д, 2J = 14,5; 3J = 1,8; SCH 2 ), 5,70 (1H, м, CHI); 6,50 (1H, м., -CHPh); 7,34–7,46 (5H, м, С 6 Н 5 ); 7,68-7,72 (1H, м, H-10); 8,95–9,10 (1H, м, H-9); 8,50–8,52 (1H, м, H-7).
Трибромид 8,3-дибром-4-фенил-2,3,4,11-тетрагидро[1,3]тиазин[3|,2|:2,3]
-
[1,2,4] триазино[5,6- b ]индолия (4d)
К раствору 0,062 г (0,15 ммоль) 8-бром- транс -3-циннамилсульфанил-5 H -[1,2,4]триазин[5,6- b ]индола в 40 мл ледяной уксусной кислоты добавляли по каплям 0,016 мл (0,3 ммоль) брома в 10 мл ледяной уксусной кислоты при постоянном охлаждении льдом. Реакционную смесь оставляли на сутки при комнатной температуре, образовавшийся отсадок отфильтровали и сушили. Выход 0,071 г (68 %). Т пл больше 250 °С.
Спектр ЯМР 1Н (400 MГц, DMSO-d6) δ, м. д.: 3,44 (1H, д. д, 2J = 14,6; 3J = 2,9; SCH 2 ); 3,69 (1H, д. д, 2J = 14,6; 3J = 2,6; SCH 2 ), 5,80 (1H, м, CHI); 6,60 (1H, м., -CHPh); 7,35–7,56 (5H, м, С 6 Н 5 ); 7,70–7,75 (1H, м, H-10); 8,05-8,07 (1H, м, H-9); 8,52–8,54 (1H, м, H-7).
Трииодид 3-иод-4-метилкарбокси-2,3,4,11-тетрагидро[1,3]тиазин[3|,2|:2,3][1,2,4]триазин[5,6-b]индолия (5а)
К раствору 0,030 г (0,1 ммоль) метил 4-(5 H -[1,2,4]триазин[5,6- b ]индол-3-сульфанил)бут-2-еноата в 40 мл хлороформа добавляли раствор 0,040 г (0,2 ммоль) иода в 10 мл хлороформа. Реакционную смесь оставляли на сутки. Затем из реакционной смеси испарили растворитель. Остаток - чёрный кристаллический порошок. Выход 0,115 г (52 %). Тпл больше 250 °С.
Спектр ЯМР 1Н (400 MГц, DMSO-d6) δ, м. д.: 3,87 (3H, c, ОCH 3 ); 4,28 (1H, д. д, 2J = 11,9; 3J = 8,9; SCH 2 ); 5,28 (1H, д. д, 2J = 11,9; 3J = 8,0; SCH 2 ); 5,59–5,64 (2H, м, CHI, С Н СООМе); 7,61 (1H, м, H-8); 7,73 (м, H-10); 7,90 (1H, м, H-9); 8,22 (1H, H-7).
Трибромид 3-бром-4-метилкарбокси-2,3,4,11- тетрагидро[1,3]тиазин[3|,2|:2,3][1,2,4]триазин5,6-b]индолия (5b)
К раствору 0,100 г (0,3 ммоль) метил 4-(5 H -[1,2,4]триазин[5,6- b ]индол-3-сульфанил)бут-2-еноата в 40 мл ледяной уксусной кислоты добавляли по каплям 0,034 мл (0,6 ммоль) брома в 10 мл ледяной уксусной кислоты при постоянном охлаждении льдом. Реакционную смесь оставляли на сутки при комнатной температуре. Затем из реакционной смеси испарили растворитель. Остаток – жёлтый порошок. Выход 0,213 г (77 %). Т пл 245–246 °С с разложением.
Спектр ЯМР 1Н (400 MГц, DMSO-d6) δ, м. д.: 3,73 (3H, c, ОCH 3 ); 3,84 (1H, д. д, 2J = 11,4; 3J = 8,9; SCH 2 ); 4,20 (1H, д. д, 2J = 11,4; 3J = 8,5; SCH 2 ); 5,59–5,67 (2H, м, CHBr, С Н СООМе); 7,61 (1H, м, H-8); 7,77 (м, H-10); 7,92 (1H, м, H-9); 8,27 (1H, H-7).
Трииодид 8-бром-3-иод-4-метилкарбокси-2,3,4,11- тетрагидро[1,3]тиазин[3|,2|:2,3][1,2,4]триазин[5,6-b]индолия (5c)
К раствору 0,045 г (0,1 ммоль) метил 4-(8-бром-5 H -[1,2,4]триазин[5,6- b ]индол-3-сульфанил)бут-2-еноата в 40 мл хлороформа добавляли раствор 0,045 г (0,2 ммоль) иода в 10 мл хлороформа. Реакционную смесь оставляли на сутки. Затем из реакционной смеси испарили растворитель. Остаток – чёрный кристаллический порошок. Выход 0,202 г (58 %).
Спектр ЯМР 1Н (400 MГц, DMSO-d6) δ, м. д.: 3,83 (3H, c, ОCH 3 ); 4,30 (1H, д.д, 2J = 11,6; 3J = 9,4; SCH 2 ); 5,27 (1H, д.д, 2J = 11,6; 3J = 9,0; SCH 2 ); 5,60–5,64 (2H, м, CHI, С Н СООМе); 7,70– 7,73 (1H, м, H-10); 8,04–8,07 (1H, м, H-9); 8,50–8,52 (1H, м, H-7).
Трибромид 3,8-дибром-4-метилкарбокси-2,3,4,11-тетрагидро[1,3]тиазин[3|,2|:2,3][1,2, 4]триазин[5,6- b ]индолия (5d)
К раствору 0,115 г (0,3 ммоль) метил 4-(8-бром-5 H -[1,2,4]триазин[5,6- b ]индол-3-сульфанил)бут-2-еноата в 40 мл ледяной уксусной кислоты добавляли по каплям 0,08 мл (0,6 ммоль) брома в 10 мл ледяной уксусной кислоты при постоянном охлаждении льдом. Реакционную смесь оставляли на сутки при комнатной температуре. Затем из реакционной смеси испарили растворитель. Остаток – коричневый порошок. Выход 0,231 г (80 %).
Спектр ЯМР 1Н (400 MГц, DMSO-d6) δ, м. д.: 3,73 (3H, c, ОCH 3 ); 4,20 (1H, д.д, 2J = 11,3; 3J = 8,6; SCH 2 ); 5,36 (1H, д.д, 2J = 11,3; 3J = 8,2; SCH 2 ); 5,60–5,64 (2H, м, CHI, С Н СООМе); 7,70– 7,73 (1H, м, H-10); 8,04–8,07 (1H, м, H-9); 8,48–8,50 (1H, м, H-7).
Обсуждение результатов
С целью получения новых гетероциклических систем, содержащих индолтриазиниевый фрагмент, нами впервые было осуществлено взаимодействие 5 Н -[1,2,4]триазин[5,6- b ]индол-3-тиона 1a и 8-бром-5 Н -[1,2,4]триазино[5,6- b ]индол-3-тиона 1b с транс -циннамилхлоридом в системе ДМСО-Н 2 О-NaOH и метиловым эфиром 4-бромкротоновой кислоты в системе ДМФА-H2O-NaOH при перемешивании при комнатной температуре в течение суток (схема 1).
По указанной методике выход транс -3-циннамилсульфанил-5 H -[1,2,4]триазин[5,6- b ]индола ( 2а ) и 8 - бром -транс -3-циннамилсульфанил-5 H -[1,2,4]триа-зин[5,6- b ]индола ( 2b ) составляет 69 и 58 % соответственно.
II
————
III
-
1: a: R=H; b: R=Br;
2a, 4a, 4b: R=H, R1= Ph; 2b, 4c, 4d: R=Br, R1=Ph;
3a, 5a, 5b: R=H, R1=COOMe; 3b, 5c, 5d: R=Br, R1=COOMe;
4a, 4c, 5a, 5c: Hal=I; 4b, 4d, 5b, 5d: Hal=Br.
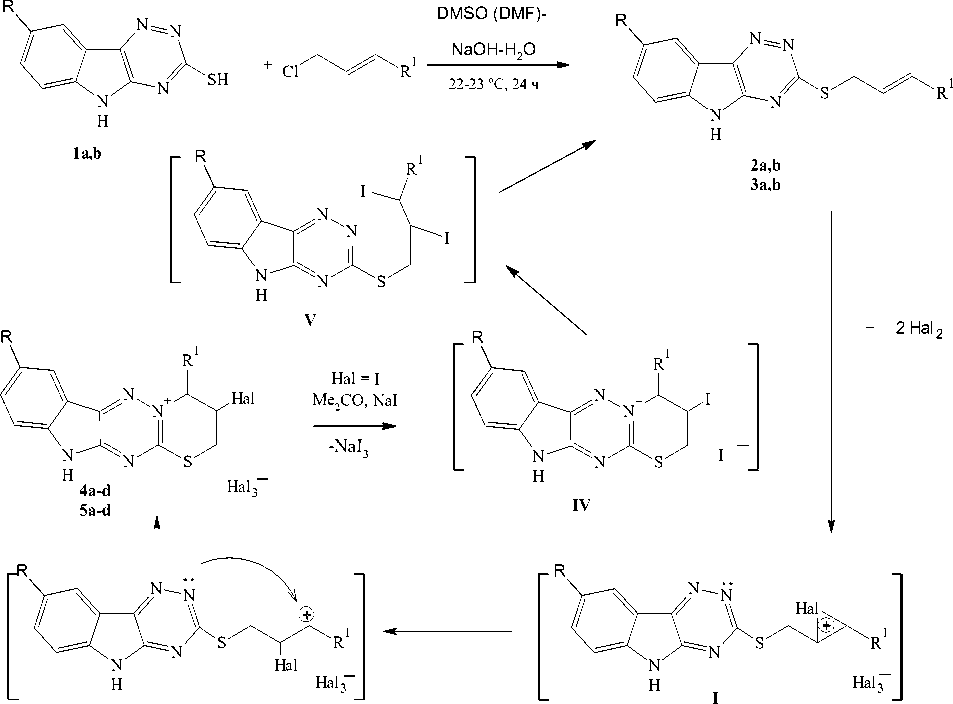
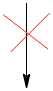
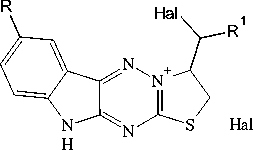
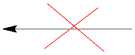
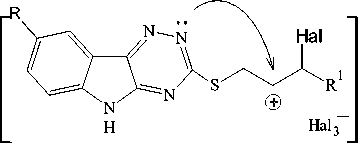
Схема 1. Взаимодействие соединений 1a,b с транс -циннамилхлоридом и метиловым эфиром 4-бромкротоновой кислоты и последующая гетероциклизация соединений 2a,b и 3a,b под действием галогенов
Метил 4-(8-бром-5 H -[1,2,4]триазин[5,6- b ]индол-3-сульфанил)бут-2-еноат ( 3а) и метил 4-(8-бром-5 H -[1,2,4]триазин[5,6- b ]индол-3-сульфанил)бут-2-еноат (3b) также были получены нами с достаточно высокими выходами (76 и 60 % соответственно).
Впервые синтезированные соединения 2a,b и 3a,b были исследованы нами методом ЯМР 1Н. Отметим, что в спектрах ЯМР 1Н структур 2а и 2b протоны S-CH2-группы образуют дублет в области 4,13 и 4,15 м. д. соответственно, в то время как S-CH2 протоны в спектрах ЯМР 1Н соединений 3а и 3b резонируют при 4,09 и 4,12 м. д. соответственно. Также можно наблюдать неболь- шое смещение сигналов ароматических протонов индольного кольца и сигнала протона NH-группы в область более слабого поля при наличии электроноакцепторного атома брома в 8-м положении для структур 2b и 3b по сравнению с аналогичными сигналами в спектрах структур 2a,3a, не содержащих атом брома в индольном фрагменте.
В различных источниках [14, 17] имеется противоречивая информация о гетероциклизации триазинов, так как возможно образование как пяти-, так и шестичленного цикла или протекание реакции как по атому азота N-2, так и по атому азота N-4. В то же время нами ранее на основе рентгеноструктурного анализа было установлено, что внутримолекулярная гетероциклизация 5-фенил- транс -3-циннамилсульфанил[1,2,4]триазина под действием галогенов протекает с анне-лированием шестичленного цикла по атому N-2 [12]. Таким образом, мы предполагаем, что электрофильная внутримолекулярная гетероциклизация соединений 2а, b и 3а, b под действием двукратного избытка брома в ледяной уксусной кислоте при охлаждении льдом или йода в хлороформе при комнатной температуре протекает аналогично с аннелированием шестичленного тиазинового цикла с образованием тригалогенидов 3-галоген-4-R1-8-R-2,3,4,11-тетрагидро[1,3]тиазино[31,2,4][2,3: ׀ 2, ׀ ]триазино[5,6- b ]индолия ( 4, 5 ) (см. схему 1). При этом выходы продуктов 4а–d и 5а–d достаточно высоки и колеблются в интервале от 52 до 81 %.
По-видимому, из-за стерических препятствий протекание реакции через образование галоге-нониевого иона I не выгодно, и гетероциклизация осуществляется по карбкатионному механизму через ион II . Атака атомом азота на положительно заряженный углерод в карбкатионе III также будет стерически затрудненной, поэтому соединение 6 не образуется.
В спектрах ЯМР 1Н соединений 4а–d и 5а–d протоны группы SCH2 являются диастереотоп-ными, так как находятся рядом с асимметрическим атомом углерода и образуют два дублета дублетов. Мультиплетность сигналов обусловлена спин-спиновым взаимодействием каждого из SCH2 протонов между собой ( 2J ) и с соседним протоном группы СНHal ( 3J ).
В литературе известно, что трииодиды органических катионов могут быть переведены в соответствующие моноиодиды при действии на них иодида натрия [26] или сульфита натрия [14] в ацетоне. Однако в нашем случае трииодиды 4а, 4с и 5а, 5с при действии на них NaI в ацетоне переходят в исходные сульфиды 2а, 2b и 3a, 3c соответственно, что было установлено нами на основе данных ЯМР 1Н – спектроскопии. По-видимому, моноиодиды IV являются неустойчивыми и разлагаются до продуктов присоединения V , которые в свою очередь могут легко распадаться до исходных соединений.
Заключение
Таким образом, алкилированием 5 Н -[1,2,4]триазин[5,6- b ]индол-3-тиона и 8-бром-5 Н -[1,2,4]триазин[5,6- b ]индол-3-тиона в системе NaOH-ДМСО(ДМФА)-H 2 O нами синтезированы неизвестные ранее S-производные [1,2,4]триазино[5,6- b ]индол-3-тионов. Установлено, что гало-генциклизация полученных соединений 2a, b и 3a, b под действием йода и брома осуществляется с аннелированием шестичленного цикла с участием атома азота N-2 и образованием тригалогенидов 4а–d и 5а–d . Доказано, что полученные трииодиды 4а, 4с, 5а, 5с могут быть обратно переведены в соответствующие исходные S-алкенильные производные под действием NaI в ацетоне.
Список литературы Синтез и гетероциклизация 8-R-транс-3-циннамилсульфанил-5H-[1,2,4]триазино[5,6-b]индолов и метил 4-(8-R-5H-[1,2,4]триазин[5,6-b]индол-3-сульфанил)бут-2-еноатов
- Ligand-Based Virtual Screening Identifies a Family of Selective Cannabinoid Receptor 2 Agonists / M. Gianella-Borradori, I. Christou, C.J.R. Bataille et al. // Bioorganic & Medicinal Chemistry. 2015. Vol. 23, iss. 1. P. 241-26. DOI: 10.1016/j.bmc.2014.11.002.
- Microwave Irradiation for Accelerating each Step for the Synthesis of 1,2,4-Triazino[5,6-b]indole-3-thiolsand their Derivatives from Isatin and 5-Chloroisatin / E.S.H. El Ashry, E.S. Ramadan, H M. Hamid, M. Hagar // Synlett. 2004. Iss. 4. P. 723-725. DOI: 10.1055/s-2004-815437.
- Ким Д.Г., Журавлёва А.В. Синтез [1,3]тиaзоло[3',2':2,3][1,2,4]триaзино[5,6-b]индолиевых систем // Химия гетероциклических соединений. 2009. Т. 45, № 10. С. 1590-1592.
- Gomha S., Abdel-Aziz H. Synthesis of New Functionalized Derivatives of Indo-lo[2,3-ß][1,2,4]triazolo[4,5-b]-1,2,4-triazine / J. of the Serb. Chem. Soc. 2016. Vol. 78, no. 8. P. 11191125. DOI: 10.2298/jsc120914013g.
- Производные тиомочевины и тиосемикарбазида. строение, превращения и фармакологическая активность. 10. Синтез, фармакологические и фармакокинетические свойства нового анти-гипоксанта и антисурдитанта томпаслина / А.Б. Томчин, Л.В. Пастушенков, А.Л. Пастушенков и др. // Химико-фармацевтический журнал. 2008. Т. 42, № 5. С. 14-19.
- Triazino Indole-Quinoline Hybrid: A Novel Approach to Antileishmanial Agents / R. Sharma, A.K. Pandey, R. Shivahare et al. // Bioorganic & Medicinal Chemistry Letters. 2014. Vol. 24, no. 1. P. 298-301. DOI: 10.1016/j.bmcl.2013.11.018.
- Novel Multitarget Directed Triazinoindole Derivatives as Anti-Alzheimer Agents / D.V. Patel, NR. Patel, A.M. Kanhed et al. // ACS Chemical Neuroscience. 2019. Vol. 10, no. 8. P. 36353661. DOI: 10.1021/acschemneuro.9b00226.
- Синтез гетарилсульфанил- и гетарилоксифуроксанов нуклеофильным замещением нитрогруппы в нитрофуроксанах под действием гетероциклических тиолов и спиртов / Л.Л. Ферштат, M.A. Епишина, A.C. Куликов и др. // Химия гетероциклических соединений. 2015. Т. 51, № 2. С. 176-186.
- Li H., Zhou H., Krieger S. Triazine-Based Tool Box for Developing Peptidic PET Imaging Probes: Syntheses, Microfluidic Radiolabeling, and Structureeactivity Evaluation // Bioconjug. Chem. 2014. Vol. 25. P. 761-772. DOI: 10.1021/bc500034n.
- Prokhorov A.M., Kozhevnikov D.N. Triazines, Tetrazines, and Fused Ring Polyaza Systems // Progress in Heterocyclic Chemistry. 2011. Vol. 23. P. 403-425. DOI: 10.1016/B978-0-08-096805-6.00014-0.
- Neunhoeffer H. 1,2,4-Triazines and Their Benzo Derivatives // Compr. Heterocycl. Chem. II. 1996. P. 507-573. DOI: 10.1016/b978-008096518-5.00127-1.
- Halo-heterocyclization of Tra«s-5-phenyl-3-cinnamylsulfanyl[1,2,4]triazine into [1,3]Thiazino[3,2-6][1,2,4]triazine-9-ium Systems / D.G. Kim, A.V. Rybakova, V.V. Sharutin, E.I. Danilina, O.V. Sazhayeva // Mendeleev Communications. 2019. Vol. 73, no. 29. P. 59-60. DOI: 10.14529/chem210107.
- Effect of Newly Synthesized 1,2,4-Triazino[5,6-6]indole-3-thione Derivatives on Olfactory Bulbect-omy Induced Depression in Rats / U.M. Aswar, P.P. Kalshetti, S.M. Shelke et al. // Asian Pacific Journal of Tropical Biomedicine. 2012. Vol. 2, no. 12. Р. 992-998. DOI: 10.1016/S2221-1691(13)60012-X.
- Региоселективная циклизация 3-аллил(пропаргил)сульфанил-5Н-[1,2,4]триазино[5,6-6]индолов / Р.И. Васькевич, А.И. Васькевич, А.В. Туров и др. // Химия гетероциклических соединений. 2011. Т.47, № 8. С. 1258-1263.
- 1,2,4-Triazole-based Palladium Pincer Complexes. A New Type of Catalyst for the Heck Reaction / E. Diez-Barra, J. Guerra, V. Hornillos et al. // Organometallics. 2003. Vol. 22, № 22. Р. 46104612. DOI: 10.1021/om0340600.
- Synthesis of Some Nitrogen Heterocycles under Microwave Irradiation in Solventless System. / H.A. Oskooie, M.M. Heravi, N. Nami, A. Nazari // Heterocyclic Communications. 2005. Vol. 11, no. 1. Р. 101-104. DOI: 10.1515/hc.2005.11.1.101.
- Синтез производных 5Н-тиазоло[2,3-с|[1,2,4]триазина и замещенных 3-(2-ацилвинилтио)-I,2,4-триазин-5-онов из 6-метил-3-тиоксо-1,2,4-триазин-5-она, 1-ацил-2-бромацетиленов и ацетиленовых кетонов. Рентгеноструктурный анализ 3-бензол-6-метил-5Н-тиазоло[2,3-с][1,2,4]триазин-5-она / B.Н. Елохина, А.С. Нахманович, Т.Н. Комарова и др. // Известия академии наук. Серия химическая. 1996. Т.45, № 12. С. 2971-2975.
- Heteropoly Acid Catalyzed Selective Cyclization of 6-Alkyl-3-propargylmercapto-1,2,4-triazin-5(2H)-one / F. Hakim, M.M. Tabatabaee, M. Hheravi et al. // E-Journal of Chemistry. 2011. Vol. 8, № 2. Р. 798-802. DOI: 10.1155/2011/103913.
- Hassan S. Synthesis, Antibacterial and Antifungal Activity of Some New Pyrazoline and Pyra-zole Derivatives // Molecules. 2013. Vol. 18. P. 2683-2711. DOI: 10.3390/molecules18032683.
- Synthesis of Novel Triazinoindole-Based Thiourea Hybrid: A Study on a-Glucosidase Inhibitors and Their Molecular Docking. / M. Taha, F.J. Alshamrani, F. Rahim et al. // Molecules. 2019. Vol. 24. P. 3819-3843. DOI: 10.3390/molecules24213819.
- Saad H.A., Moustafa A.H. Synthesis and Anticancer Activity of Some New Sglycosyl and S-Alkyl 1,2,4-Triazinone Derivatives Agents. // Molecules. 2011. Vol. 16, no. 7. Р. 5682-5700. DOI: 10.3390/molecules16075682.
- Synthesis, Chemical Reactivity and Fungicidal Activity of Pyrido[1,2-b][1,2,4]triazine Derivatives. / M.A. Ibrahim, R.M. Abdel-Rahman, A.M. Abdel-Halim et al. // J. Braz. Chem. Soc. 2009. Vol. 20, no. 7. Р. 1275-1286. DOI: 10.1590/s0103-50532009000700012.
- Cyclocondensation Reaction of Heterocyclic Carbonyl Compounds, Part XIII: Synthesis and Cytotoxic Activity of Some 3,7-Diaryl-5-(3,4,5-Trime-thoxyphenyl)pyrazolo[4,3-e][1,2,4]triazines / T. Gucky, I. Frysova, J. Slouka et al. // Eur. J. Med. Chem. 2009. Vol. 44, no. 2. Р. 891-900. DOI: 10.1016/j.ejmech.2008.05.026.
- Rezaei D., Fazlollahi M. Synthesis, Solvatochromism and Crystal Structure of 5-Methoxy-5,6-diphenyl-4,5-dihydro-2# - 1,2,4-Triazine-3-thione // Chemistry Central Journal. 2015. Vol. 7, no. 1. ID 130. DOI: 10.1186/1752-153X-7-130.
- Condensed 1,2,4-Triazines: I. Fused to Heterocycles with Three-, Four-, and Five-Membered Rings / E.S.H. El Ashry, N. Rashed, M. Taha, E. Ramadan // Advances In Heterocyclic Chemistry. 1994. Vol. 59. P. 39-177. DOI: 10.1016/S0065-2725(08)60007-0.
- Heterocyclization of 3-Propargylsulfanyl-5-phenyl-1,2,4-triazine: Tandem Reactions with Bromine Leading to New Derivatives of 7-Phenyl[1,3]thiazolo[3,2-6][1,2,4]triazinium / A.V. Rybako-va, D.G. Kim et al. // Izvestiya Vysshikh Uchebnykh Zavedeniy Khimiya Khimicheskaya Tekhnolo-giya. 2020. Vol. 63, no. 6. Р. 19-24. DOI: 10.6060/ivkkt.20206306.6102.

![Синтез и гетероциклизация 8-R-транс-3-циннамилсульфанил-5H-[1,2,4]триазино[5,6-b]индолов и метил 4-(8-R-5H-[1,2,4]триазин[5,6-b]индол-3-сульфанил)бут-2-еноатов Синтез и гетероциклизация 8-R-транс-3-циннамилсульфанил-5H-[1,2,4]триазино[5,6-b]индолов и метил 4-(8-R-5H-[1,2,4]триазин[5,6-b]индол-3-сульфанил)бут-2-еноатов](/file/cover/147238625/sintez-i-geterociklizacija-8-r-trans-3-cinnamilsulfanil-5h124-triazino-56-b.png)
