Синтез и гетероциклизация неизвестного ранее S-аллилтиосемикарбазона 11Н-индено[1,2-B]хиноксалин-11-она
Автор: Рыбакова А.В., Ейник А.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 4 т.16, 2024 года.
Бесплатный доступ
Известно, что некоторые производные инденохиноксалина проявляют себя как биологически активные соединения. О синтезе 11 H -индено[1,2- b ]хиноксалин-11-она известно примерно с 1910 г, и с тех пор имеется немало сведений об одном наиболее практически значимом его производном - тиосемикарбазоне индено[1,2- b ]хиноксалин-11-она. Последний был исследован нами в реакции с бромистым аллилом в среде ДМФА-KOH-Н2О при комнатной температуре, что вызывает большой интерес с точки зрения возможности получения S-производных тиосемикарбазона индено[1,2- b ]хиноксалин-11-она, сведения о которых в литературе отсутствуют. Этот факт объясняется тем, что тиосемикарбазон инденохиноксалина ранее изучен в основном в реакциях с бифункциональными соединениями, которые сопровождаются процессом молекулярной циклизации и, минуя S-замещенные продукты, сразу приводят к синтезу (индено[1,2- b ]хиноксалин-11-илиден)гидразин)тиазольных систем. Так, впервые полученный нами S-аллилтиосемикарбазон 11 H -индено[1,2- b ]хиноксалин-11-он в результате дальнейшей электрофильной гетероциклизации под действием галогенов был превращен в галогениды 11 H -индено[1,2- b ]хиноксалин-11-илиден-гидразин-4-(иодметил)-4,5-дигидро-1,3-тиазолия. В спектрах ЯМР 1Н галогенидов индено[1,2- b ]хиноксалинилиден-гидразин-4-(галогенметил)-1,3-тиазолия наблюдаются сигналы протонов SCH2 и CH2X групп (X=I, Br) в области 3,60-4,24 м. д., сигналы протонов -NH- и =N+H- групп при 9,69-10,47 м. д. и мультиплеты ароматических протонов гетероциклического фрагмента - при 7,73-7,76; 7,83-7,84;7,89-7,91; 7,97-7,99; 8,18-8,20; 8,20-8,22; 8,30-8,32 м. д. Однопротонный сигнал =СНN+- группы в случае трииодида образует сигнал при 5,83 м. д., тогда как в случае трибромида аналогичный сигнал протона проявляется при 6,05 м. д.
11h-индено[1, 2-b]хиноксалин-11-он, тиосемикарбазон индено[1, 2-b]хиноксалин-11-она, бромистый аллил, гетероциклизация
Короткий адрес: https://sciup.org/147246057
IDR: 147246057 | УДК: 547.863.11+ | DOI: 10.14529/chem240413
Synthesis and heterocyclization of a previously unknown S-allylthiosemicarbazone of 11H-indeno[1,2-B]quinoxaline-11-one
It is known that some derivatives of indenoquinoxaline prove to be biologically active compounds. Synthesis of 11 H -indeno[1,2- b ]quinoxalin-11-one has been known since about 1910, and since then considerable information has been accumulated about one of its most practically significant derivatives: thiosemicarbazone of indeno[1,2- b ]quinoxalin-11-one. We studied the latter in the reaction with allyl bromide in a DMF-KOH-H2O medium at room temperature, which is of great interest from the point of view of obtaining S-derivatives of thiosemicarbazone of indeno[1,2- b ]quinoxalin-11-one, information about which is not available in the literature. This is explained by the fact that thiosemicarbazone of indenoquinoxaline has been previously studied mainly in reactions with bifunctional compounds, which are accompanied by molecular cyclization and, bypassing the S-substituted products, immediately lead to synthesis of (indeno[1,2- b ]quinoxalin-11-ylidene)hydrazine)thiazole systems. Thus, the S-allylthiosemicarbazone of 11 H -indeno[1,2- b ]quinoxalin-11-one obtained by us for the first time as a result of further electrophilic heterocyclization under the action of halogens has been converted into halides of 11 H -indeno[1,2- b ]quinoxalin-11-ylidene-hydrazine-4-(iodomethyl)-4,5-dihydro-1,3-thiazolium. In the 1H NMR spectra of indeno[1,2- b ]quinoxalinylidenehydrazine-4-(halomethyl)-1,3-thiazolium halides, the signals of the protons of the SCH2 and CH2X groups (X=I, Br) are observed in the region of 3.60-4.24 ppm, the signals of the protons of the -NH- and =N+H- groups are at 9.69-10.47 ppm and multiplets of the aromatic protons of the heterocyclic fragment are observed at 7.73-7.76; 7.83-7.84; 7.89-7.91; 7.97-7.99; 8.18-8.20; 8.20-8.22; 8.30-8.32 ppm. The single-proton signal of the =СНN+- group in the case of triiodide forms a signal at 5.83 ppm, whereas in the case of tribromide a similar proton signal appears at 6.05 ppm.
Текст научной статьи Синтез и гетероциклизация неизвестного ранее S-аллилтиосемикарбазона 11Н-индено[1,2-B]хиноксалин-11-она
Производные хиноксалина имеют довольно широкий спектр полезных свойств, таких как: антибактериальные (производные хиноксалин-1,4-диоксида применяются в медицине и ветеринарии в качестве антибактериальных агентов для лечения тяжелых форм инфекционных заболеваний [1]), противораковые (производные 2-(1-алкилбензимидазол-2-ил)хиноксалинов были использованы в разработке многоцелевых подходов к ингибированию клеток рака шейки матки in vitro для создания новых терапевтических целевых агентов [2]) и противогрибковые (проявляют активность в отношении фитопатогенных грибов [1]).
Кроме того, различные антибиотики, такие как эхиномицин, левомицин и актинолеутин, содержат хиноксалиновые циклы в структуре активного соединения, и используются для подавления грамположительных бактерий [3]. Механизм действия хиноксалинов принципиально отличается от других антимикробных лекарственных средств. Хиноксалины характеризуются высокой реакционной активностью и способностью активировать в организме в анаэробных условиях свободнорадикальные процессы. Бактерицидное действие хиноксалинов обусловлено повреждением ДНК микробной клетки, нарушением процесса ее деления и развитием необратимых структурных изменений в ядре и цитоплазме [4]. Некоторые производные инденохиноксалина проявляют себя как ингибиторы N-концевой киназы [5].
Первые упоминания о реакции о -фенилендиамина ( 1 ) с нингидрином ( 2 ), приводящей к синтезу 11 H -индено-[1,2- b ]-хиноксалин-11-она ( 3 ) встречаются в работе [6]. При этом соединение 3 было получено в разбавленной уксусной кислоте при 120°С с выходом 77 %. Аналогичным способом, но в этаноле, был получен 2,3,8-тризамещенный 11 H -индено-[1,2- b ]-хиноксалин-11-он с выходом в 83 % [6] и 3,4,5-тризамещенные 11 H -индено-[1,2- b ]-хиноксалин-11-оны с выходами 35–90 % [7].
При проведении реакции конденсации нингидрина с о -фенилендиамином и его нитропроизводным в смеси этанола и ледяной уксусной кислоты при кипячении в течении 3ч выход соединения 3 и 4-нитро-11 H -индено[1,2- b ]хиноксалин-11-она составил 87 и 82 % соответственно [8]. Кроме того, соединение 3 можно получить при взаимодействии соединений 1 и 2 , но при комнатной температуре в дистиллированной воде [9] или в этаноле в присутствии ацетата натрия (при этом выход продукта незначительно снижается 79 %) [10], а также при кипячении в течение 1 ч в ТГФ в присутствии HCl [9]. Более подробно влияние растворителя, присутствия катализатора и температуры на реакцию конденсации соединений 1 и 2 описано в современной работе [11].
Кроме того, реакцией о -фенилендиамина с 1,2-индандионом в метаноле может быть сначала получен 11 H -индено-[1,2- b ]-хиноксалин, дальнейшее окисление которого бихроматом калия приводит к синтезу соединения 3 [12].
Интересно, что с выходом 55 % можно получить инденохиноксалин-11-он 3 при окислительном дегидрировании 2-инданона и орто -фенилендиамина с использованием молекулярного кислорода в качестве окислителя и триэтиламина в качестве катализатора. Однако в ходе реакции наравне с соединением 3 образуется индено[1,2- b ]хиноксалин с выходом 40 %. При этом увеличение времени реакции не влияет на соотношение продуктов реакции [13].
В литературе также описан метод получения соединения 3 из этилового эфира 3-фенилхиноксалин-2-карбоновой кислоты в две стадии. На первой стадии происходит гидролиз исходного соединения в этаноле в присутствии KOH с образованием 3-фенилхиноксалин-2-карбоновой кислоты с выходом 97 %. На второй стадии по реакции внутримолекулярной циклизации образуется инденохиноксалинон 3 с выходом 46 % [14].
Более специфичным способом получения инденохиноксалиновых систем является превращение бензо[ « ]феназин-5,6-дион-7-оксидов при их обработке метанольным гидроксидом калия при 20-25 °C. При этом реакция сопровождается выделением CO2, сжатием орто -хиноидного кольца, восстановлением N -оксидного фрагмента и приводит к синтезу 3,5-дизамещенных инде-но[1,2- b ]хиноксалин-11-онов с выходом 58-83 % [15].
Химические свойства соединения 3 представлены в литературе различными превращениями, в ходе которых тетрациклическая конденсированная система остается устойчивой даже в случае нарушения ароматичности отдельных циклов [6]. Однако, наиболее характеристичными для соединения 3 являются реакции функционализации по карбонильной группе [16]. Например, его конденсация с тиокарбогидразидом [17], метил К-(4-ацетилфенил)карбаматом [18], гидроксиламином [19, 20], бензогидразонамдами [21] и др. [11]. Кроме того, описываются реакции синтеза спиросоединений на основе 11 H -индено-[1,2- b ]-хиноксалин-11-она [22].
Аналогично по карбонильной группе протекает реакция конденсации инденохиноксалин-11-она 3 с тиосемикарбазидом (4) в смеси этанола и хлороформа при кипячении в течении 8 ч в присутствии безводного сульфата магния. Выход конечного продукта реакции - тиосемикарбазона индено[1,2- b ]хиноксалин-11-она (5) - составляет 74 % [23].
Данная реакция может так же протекать в этаноле при кипячении в присутствии каталитического количества ледяной уксусной кислоты [24], либо в метаноле в присутствии концентрированной H2SO4 [25].
Для тиосемикарбазона 5 характерными являются реакции комплексообразования с ионами металлов [23, 26, 27]. Однако, наиболее часто встречаются в литературе реакции тиосемикарбазона 5 с бифункциональными соединениями, сопровождающиеся, по-видимому, образованием промежуточных S-производных соединения 5 , претерпевающих молекулярную циклизацию [28]. Например, в статье [29] описывается взаимодействие тиосемикарбазона 5 с этилхлорацетатом в кипящем диоксане в присутствии триметиламина, приводящее к образованию 2-(2-(11 H -индено[1,2- b ]хиноксалин-11-илиден)гидразин)тиазол-4(5 H) -она с выходом 78 %. Так же к аннелированию тиазольного цикла приводит взаимодействие тиосемикарбазона 5 с диметилацетилендикарбок-силатом в абсолютном метаноле. В этой реакции атом серы атакует тройные связи и образуется тиолактам, последующий аммонолиз сложноэфирной группы приводит к образованию метил-2-(2-(2-(-11 H -индено[1,2- b ]хиноксалин-11-илиден)гидразинил)-4-оксотиазол-5(4 H) -илиден) ацетата с выходом 86 %. Еще одним примером получения тиазольного кольца является взаимодействие соединения 5 с 3-хлорпентан-2,4-дионом. При этом выделяется 1-(2-(2-(11 H -индено[1,2- b ]хиноксалин-11-илиден)гидразинил)-4-метилтиазол-5-ил)этан-1-он с выходом 79 % [29].
Практически значимым является возможность использования тиосемикарбазона 5 в качестве хемосенсора для быстрого и точного определения содержания ионов F- в среде ацетонитрила (предел обнаружения 6 мкм) [30].
Экспериментальная часть
Спектры ЯМР 1Н и 13С записывали на спектрометрах Bruker DRX-400 (рабочая частота 400 ( ' Н) МГц) и AVANCE-500 (рабочая частота 500 ( ' Н) и 126 (13С) МГц) в ДМСО-d6, внутренний стандарт - ТМС (для ядер 1Н) и сигнал растворителя (для ядер 13С, 39,5 м. д.).
Температуры плавления измерены с помощью прибора для определения температуры плавления ПТП (М) (V ~ 220 В, W = 500 BA).
ИК-спектры соединения 1 записывали на ИК-спектрометре Shimadzu IRAffmity-1S в таблетках KBr в области 4000–400 см–1.
Масс-спектр сняты на хромато-масс-спектрометре фирмы SHIMADZU GCMS-QP2010 Ultra, режим электронной ионизации ЭИ (70 эВ).
Синтез 11 Н -индено[1,2- b ]хиноксалин-11-она (3) . Раствор 0,899 г (5 ммоль) нингидрина в 50 мл этилового спирта смешивают с 2 мл AcOH и 0,541 г (5 ммоль) орто -фенилендиамина. Реакционную смесь нагревают в течение 3 ч. Через 24 ч образовавшийся осадок жёлтооранжевого цвета отфильтровывают и сушат. Выход 11 Н -индено[1,2- b ]хиноксалин-11-она составляет 1,077 г (92 %), Т пл 218–220 °С (Лит. 214–216 °С [11]). ИК-спектр ( ν , см - 1): 422, 462, 484,
526, 542, 552, 571, 609, 633, 648, 702, 731, 756, 766, 868, 887, 939, 957, 1165, 1184, 1199, 1236, 1248, 1308, 1337, 1368, 1396, 1464, 1508, 1549, 1681, 1709, 1722, 1809, 1844, 1911, 1942, 1977, 3023, 3048, 3069, 3424.
1005, 1568,
1044, 1109, 1123,
1605, 1616, 1653,
Синтез тиосемикарбазона 11 Н -индено[1,2- b ]хиноксалин-11-она
Раствор 0,054 г
(0,6 ммоль) тиосемикарбазида в 50 мл метилового спирта смешивают с 0,132 г (0,6 ммоль) 11 Н -индено[1,2- b ]хиноксалин-11-она. Реакционную смесь нагревают в течение 5 ч. Через 24 ч образовавшийся осадок жёлтого цвета отфильтровывают и сушат. Выход тиосемикарбазона 11 Н -индено[1,2- b ]хиноксалин-11-она составляет 0,148 г (82 %), Т пл 265 °С (Лит. 263–265°С [29]).
Синтез S-аллилтиосемикарбазона 11 Н -индено[1,2- b ]хиноксалин-11-она (6a) . К раствору 0,408 г (1,3 ммоль) тиосемикарбазона 11 Н -индено[1,2- b ]хиноксалин-11-она в 10 мл ДМФА добавляют раствор 0,073 г (1,3 ммоль) КОН в 1 мкл воды и 0,11 мл аллилбромида (1,3 ммоль) и перемешивают при комнатной температуре. Через 24 ч реакционную смесь отфильтровывают, к фильтрату добавляют раствор 15 мг хлорида кальция в 100 мл воды. Образовавшийся осадок оранжево-коричневого цвета отфильтровывают и сушат. Выход осадка составляет 0,116 г (25 %), Т с разл 190 °С.
Синтез S-металлилтиосемикарбазона 11 Н -индено[1,2- b ]хиноксалин-11-она (6b) . К раствору 0,408 г (1,3 ммоль) тиосемикарбазона 11 Н -индено[1,2- b ]хиноксалин-11-она в 30 мл ДМСО добавляют раствор 0,07 г (1,3 ммоль) КОН в 1 мкл воды и 0,13 мл (1,3 ммоль) хлористого металлила. Через 24 ч реакционную смесь отфильтровывают, к фильтрату добавляют 70 мл воды. Образующийся осадок оранжевого цвета отфильтровывают и сушат. Выход осадка составляет 0,144г (30 %), Т пл 197 °С.
Синтез трииодида 11 H -индено[1,2- b ]хиноксалин-11-илиден)гидразин-2-амино-4-(иодметил)-4,5-дигидро-1,3-тиазолия (10a) . К раствору 0,020 г (0,058 ммоль) S-аллилтиосемикарбазона 11 Н -индено[1,2- b ]хиноксалин-11-она в 30 мл CH3Cl приливают раствор 0,030 г I 2 (0,12 ммоль) в 15 мл CH 3 Cl. Через 48 ч растворитель испаряют. Механическим путём коричневый осадок отделяют от красно-коричневого масла. Выход осадка составляет 0,342 г (70 %). Т пл 140 °С.
Синтез моноиодида 11 H -индено[1,2- b ]хиноксалин-11-илиден)гидразин-2-амино-4-(иодметил)-4,5-дигидро-1,3-тиазолия (13a) . 0,300 г (0,36 ммоль) Полученного осадка 7a растворяют в ацетоне и добавляют 15 мг (0,08 ммоль) NaI·2H 2 O. Образовавшийся осадок красного цвета отфильтровывают и сушат. Выход осадка составляет 0,063 г (30 %). Т пл 150 °С.
Синтез трибромида 11 H -индено[1,2- b ]хиноксалин-11-илиден)гидразин-2-амино-4-(бромметил)-4,5-дигидро-1,3-тиазолия (10b) . К раствору 0,020 г (0,058 ммоль) S-аллилтиосемикарбазона 11 Н -индено[1,2- b ]хиноксалин-11-она в 30 мл CH3Cl добавляют по каплям раствор 0,01 мл Br2 (0,12 ммоль) в 10 мл CH3Cl при внешнем охлаждении льдом. Реакционную смесь оставляют стоять в течение 24 ч при 7 °С. Через 24 ч осадок бурого цвета отфильтровывают и сушат. Выход осадка составляет 0,020 г (53 %). Т с разл 135 °С.
Синтез монобромида 11 H -индено[1,2- b ]хиноксалин-11-илиден)гидразин-2-амино-4-(бромметил)-4,5-дигидро-1,3-тиазолия (13b) . 0,018 г (0,02 ммоль) Трибромида 7b растворяют в 15 мл ацетона, образующийся осадок серо-коричневого цвета отфильтровывают и сушат. Выход осадка составляет 4 мг (29 %). Т пл 160 °С.
Обсуждение результатов
Взаимодействием орто -фенилендиамина 1 с нингидрином 2 с в системе C2H5OH/AcOH при 80 °С нами был осуществлён синтез 11 Н -индено[1,2- b ]хиноксалин-11-она 3 с выходом 84 %:
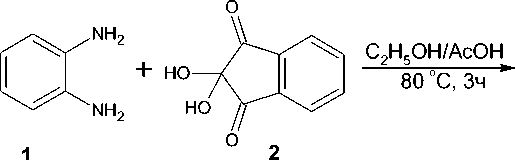
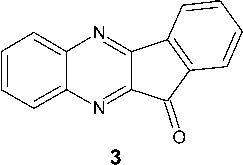
В ИК-спектре соединения 3 наблюдается интенсивная полоса поглощения С=О группы при 1722 см-1. В масс-спектре, полученном при прямом вводе пробы, (рис. 1) 11 Н -индено[1,2- b ]хиноксалин-11-она имеется максимально интенсивный (100 %) пик молекулярного иона с m/z 232, что соответствует молекулярной массе соединения 3 .
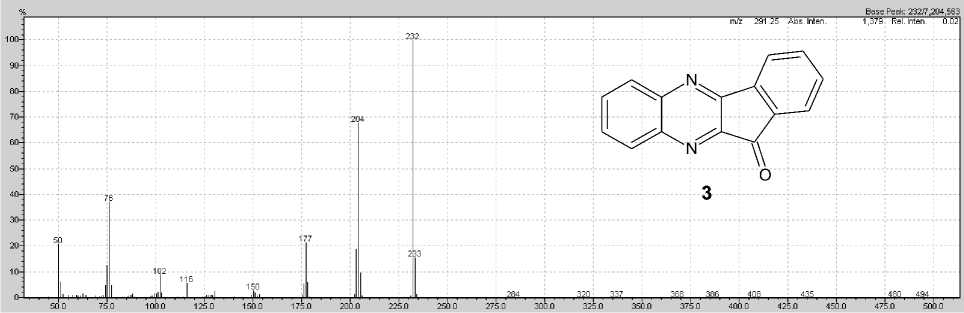
Рис. 1. Масс-спектр (прямой ввод пробы) 11 Н -индено[1,2- b ]хиноксалин-11-она (3)
Фрагментация молекулярного иона (схема 1) в первую очередь связана с отщеплением молекулы СО и образованием катион-радикала бензо[3,4]циклобута[1,2- b ]хиноксалина, которому соответствует пик с m/z 204 и интенсивностью 68 %. Далее катион-радикал бен-зо[3,4]циклобута[1,2- b ]хиноксалина претерпевает отщепление 2,3-дидегидрохиноксалина, что может быть связано с появлением в масс-спектре пика с m/z 76 (интенсивность 38 %), соответствующего катион-радикалу циклогекса-1,3-диен-5-ина.
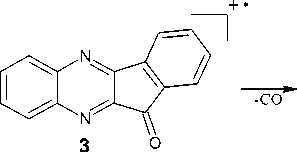
m/z 232 (100%)
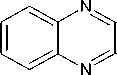
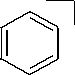
+ .
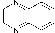
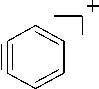
m/z 76 (38%)
m/z 204 (68%)
Схема 1. Фрагментация 11 Н -индено[1,2- b ]хиноксалин-11-она (3) при съёмке масс-спектра
Далее реакцией 11 Н -индено[1,2- b ]хиноксалин-11-она 3 с эквимолярным количеством тиосемикарбазида ( 4 ) в метаноле при 50 °С нами был осуществлён синтез тиосемикарбазона 11 Н -индено[1,2- b ]хиноксалин-11-она ( 5 ) с выходом 82 %. В спектре ЯМР 1 Н тиосемикарбазона 5 (рис. 2) ароматические протоны резонируют при 7,67; 7,91; 8,10 и 8,17 м. д., а уширенные сигналы при 8,84 и 9,08 м.д можно отнести к сигналам протонов -NH2 группы, уширенный синглет при 12,61 м. д., по-видимому, соответсвует протону -NH-N= группы.
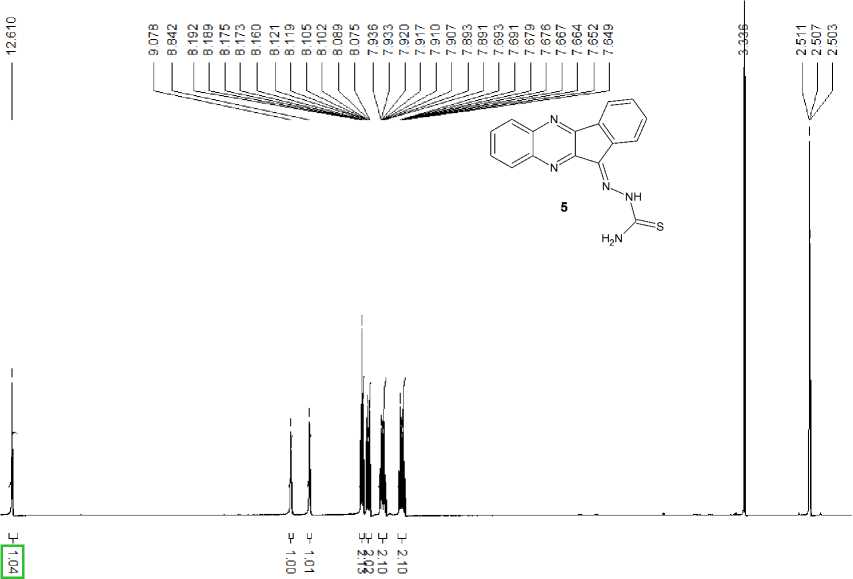
Рис. 2. Спектр ЯМР 1Н тиосемикарбазона 11 Н -индено[1,2- b ]хиноксалин-11-она (5)
Тиосемикарбазон 5 был исследован в реакции S-алкенилирования под действием эквимолярного количества бромистого аллила и хлористого металлила в системе ДМФА-KOH-Н 2 О при комнатной температуре. При этом из реакционной смеси были выделены S-аллилтиосемикарбазоны 11 H -индено[1,2- b ]хиноксалин-11-она ( 6a,b ) с выходом 25 %:
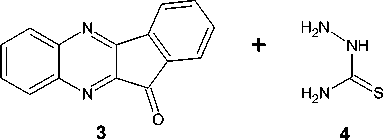
X=Br, R=H; X=Cl, R=CH
ДМФА-КОН-Н О 23-25 °C, 224ч
6a : R=H; 6b : R=CH
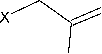
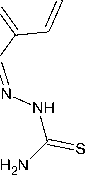
Стоит отметить, что небольшой выход аллилтиосемикарбазонов 6a,b может быть связан с трудностью выделения продукта реакции из реакционной смеси.
В ЯМР 1Н спектре соединения 6а наблюдаются сигнал протонов SCH2 группы при 3,97 м. д., однопротонные сигналы =СН 2 группы – при 5,21 и 5,43 м. д. и мультиплет протона –СН= при 6,03–6,05 м. д. Ароматические протоны гетероциклического фрагмента образуют мультиплеты в характерной для них области слабого поля: 7,64–7,68; 7,82–7,91 и 8,15–8,19 м. д. При 8,90 и 9,06 м. д. проявляются уширенные сигналы, которые, вероятнее всего, можно отнести к протонам амино-группы.
Идентификациию соединения 6b осуществляли методом масс-спектрометрии (прямой ввод пробы). В масс-спектре (рис. 3) наблюдается сигнал молекулярного иона с m/z 359 с небольшой интенсивностью (38 %).
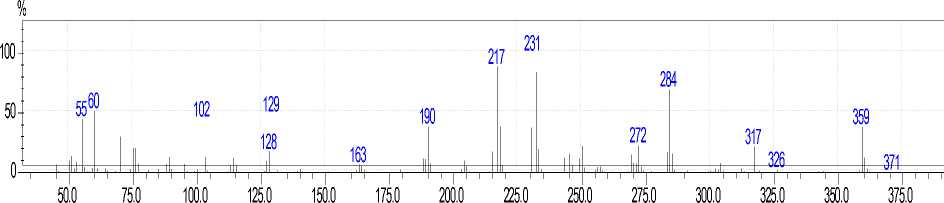
Рис. 3. Масс-спектр (прямой ввод пробы) S-металлилтиосемикарбазона 11 H -индено[1,2- b ]хиноксалин-11-она (6b)
Фрагментация соединения 6b заключается в характеристичном для аллилсульфидов гетероциклического ряда элиминировании радикала ’ SH [31], что подтверждается наличием в масс-спектре соединения 6b соответствующего малоинтенсивного пика с m/z 326 [M-SH]+. Максимально интенсивный пик в масс-спектре можно отнести к катион-радикалу индено[1,2- b ]хиноксалин-11-имина с m/z 231. Имин образуется при отщеплении от молекулярного иона 3-[2-метилпропенилсульфанил]-1 H -диазирена, причем процесс отщепления сопровождается миграцией атома Н:
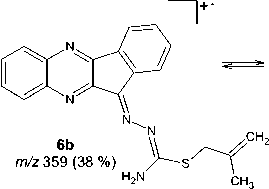
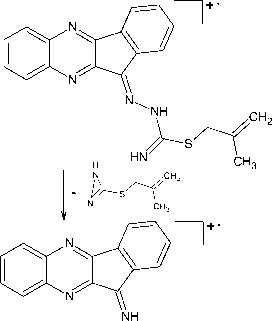
m/z 231 (100 %)
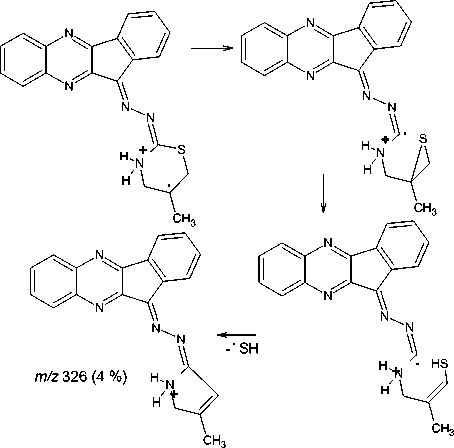
Химические свойства S-аллилтиосемикарбазона 11 H -индено[1,2- b ]хиноксалин-11-она 6а были изучены нами в реакциях с двукратным избытком галогенов, которые были осуществлены в хлороформе при комнатной температуре в случае йода и при охлаждении льдом в случае брома. Теоретически данное взаимодействие может протекать с образованием продуктов присоединения галогенов по кратной связи ( 7a,b ), продуктов аннелирования тиазольного цикла ( 8a,b–11a,b ) или молекулярных комплексов соединения 6а с галогенами ( 12a,b ):
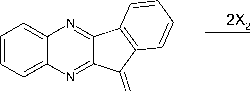
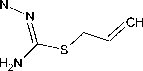
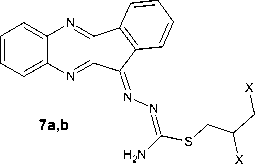
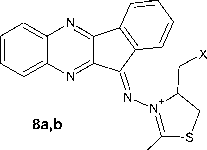
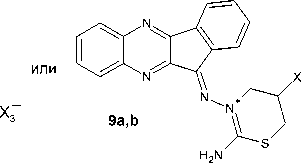
X 3
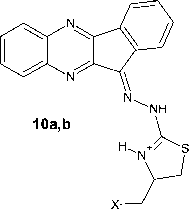
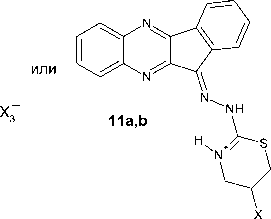
X 3
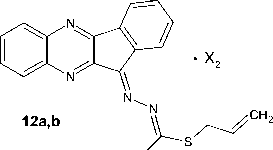
HN
7-12a : X= I; 7-12b : X= Br
Аналогично известным в литературе данным о синтезе 2-(2-(11 H -индено[1,2- b ]хиноксалин-11-илиден)гидразин)тиазол-4(5 H )–ониевых систем [29] и на основании согласующихся с ними данных спектров ЯМР 1Н для сигнала протона =N-NH- группы (в области 9,43–9,97 м. д.) нами показано, что при взаимодействии S-аллилтиосемикарбазона 6а с галогенами происходит образование продуктов циклизации с участием атома азота –NH2 группы. При этом аннелирование тиазольного цикла приводит к синтезу тригалогенидов 11 H -индено[1,2- b ]хиноксалин-11-илиден-гидразин-4-(галогенметил)-4,5-дигидро-1,3-тиазолия ( 10a , b ) с выходом 70 и 53 % соответственно для соединений 10a , b . В спектре ЯМР 1Н соединения 10a (рис. 4) наблюдается наложение сигнала протонов SCH 2 и CH 2 I групп и образование трёхпротонного мультиплета при 3,60–3,62 м. д., при этом ещё один сигнал при 4,19 м. д. может быть отнесен к одному из протонов SCH 2 группы. В то же время в спектре ЯМР 1Н соединения 10b подобного наложения сигналов не наблюдается и протоны группы SCH 2 образуют два мультиплета при 3,67–3,70 м. д. и 4,19–4,24 м. д., а протоны группы СH 2 Br – два мультиплета при 3,85–3,88 м. д. и при 3,94–3,99 м. д. (рис. 5). Различное расположение данных сигналов связано, прежде всего, с различным влиянием (экранированием), создаваемым электронами разных атомов галогена. Однопротонный сигнал =СНN+– группы в случае трииодида 10а образует сигнал при 5,83 м. д., тогда как в случае трибромида 10b аналогичный сигнал протона проявляется при 6,05 м. д. Протоны –NH- и =N+H- групп резонируют при 9,69 и 10,41 м. д. соответственно для соединения 10а и при 9,74 и 10,47 м. д. – для соединения 10b . Ароматические протоны гетероциклического фрагмента образуют сложные мультиплеты в области 7,74–7,76; 7,83–7,84;7,89–7,91; 7,97–7,99; 8,18–8,20; 8,20–8,22; 8,30–8,32 м. д. в спектре соединения
10а и в области 7,73–7,75; 7,83–7,84; 7,89–7,91; 7,97–7,99; 8,17–8,19; 8,20–8,22; 8,29–8,30 в спектре соединения 10b.
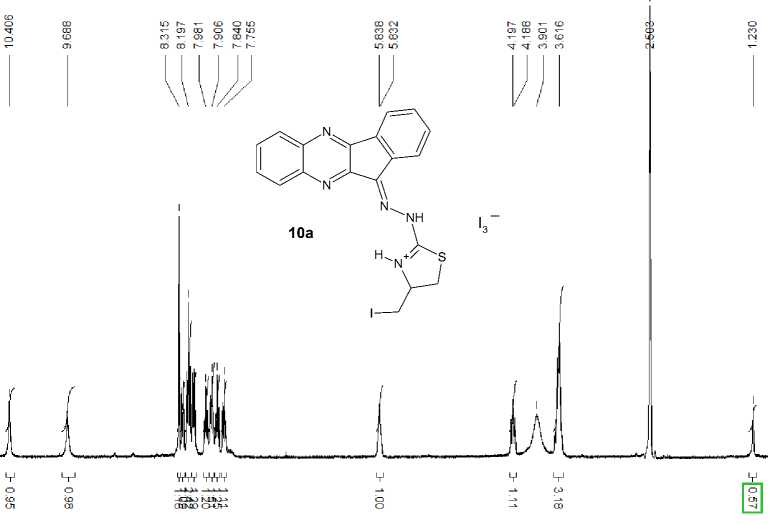
Рис. 4. Спектр ЯМР 1Н трииодида 11 H -индено[1,2- b ]хиноксалин-11-илиден-гидразин-4-(иодметил)-4,5-дигидро-1,3-тиазолия (10a)
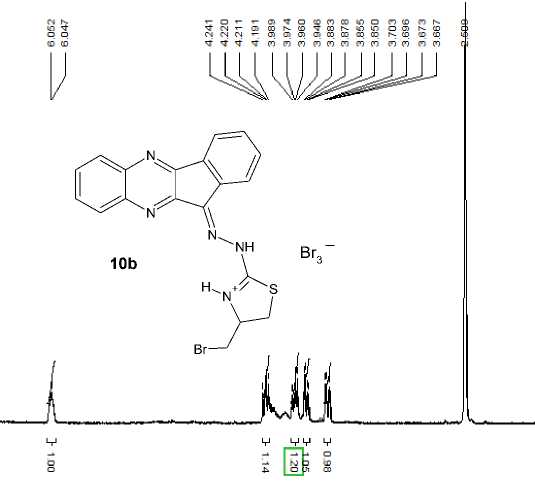
Рис. 5. Фрагмент спектра ЯМР 1Н трибромида 11 H -индено[1,2- b ]хиноксалин-11-илиден-гидразин-4-(бромметил)-4,5-дигидро-1,3-тиазолия (10b) (область сигналов протонов SCH 2 , СH 2 Br и СНN+Н– групп)
Следует отметить, что ввиду отсутствия монокристаллов, подходящих для проведения РСА, образование соединений 10a,b в виде тригалогенидов предложено нами на основе существующих литературных данных аналогичных реакций гетероциклизации при действии двукратного избытка галогенов на различные аллилсульфиды гетероциклического ряда [31, 32]. Однако, в данной работе нами также обнаружено, что трииодид 10a при дальнейшем действии на него NaI·2H2O в ацетоне переходит в соответствующий монойодид 11H-индено[1,2-b]хиноксалин-11-илиден)гидразин-2-амино-4-(галогенметил)-4,5-дигидро-1,3-тиазолия (13a), а трибромид 10b превращается в соответствующий монобромид (13b) при действии на него ацетона, что также является характерным для подобных полигалогенидов [32–34]:
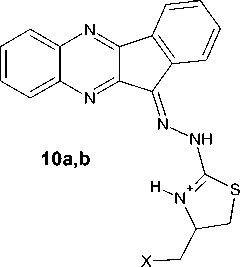
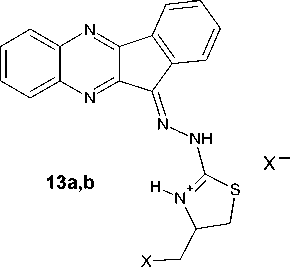
10a, 13a : X=I; 10b,13b : X=Br. 10a : i = Me CO, NaI*2 H O;
10b : i = Me CO
Заключение
Таким образом, в ходе настоящего исследования нами при взаимодействии тиосемикарбазона 11 Н -индено[1,2- b ]хиноксалин-11-она 5 с эквимолярным количеством бромистого аллила и хлористого металлила в системе ДМФА-KOH-Н 2 О при комнатной температуре впервые были получены S-аллил(металлил)тиосемикарбазоны 11 H -индено[1,2- b ]хиноксалин-11-она 6a,b . Также установлено, что дальнейшая гетероциклизация соединения 6a под действием двукратного избытка йода или брома приводит к аннелированию тиазольного цикла и образованию неизвестных ранее внутримолекулярных солей 10a,b, строение которых было установлено методом ЯМР 1Н.
Список литературы Синтез и гетероциклизация неизвестного ранее S-аллилтиосемикарбазона 11Н-индено[1,2-B]хиноксалин-11-она
- Javidi J., Esmaeilpour M. // Materials Research Bulletin. 2016. V. 73. P. 409. D01:10.1016/j.materresbull.2015.10.002
- Pashirova T.N., Zhukova N.A., Lukashenko S.S. et al. // Colloids. Surf., B. 2019. V. 178. P. 317. DOI: 10.1016/j.colsurfb.2019.03.021
- Varma R.R., Pandya J.G., Vaidya F.U. et al. // Journal of Molecular Structure. 2021. V. 1240. № 130529. DOI: 10.1016/j.molstruc.2021.130529
- Desai V., Desai S., Gaonkar S.N. et al. // Bioorganic & Medicinal Chemistry Letter. 2017. V. 27. P. 2174. DOI: 10.1016/j.bmcl.2017.03.059
- Schepetkin I.A., Kirpotina L.N., Khlebnikov A.I. et al. // Mol. Pharmacol. 2012. V. 81, No. 6. P. 832. DOI: 10.1124/mol.111.077446
- Ruhemann S. // J. Chem. Soc. Trans. 1910. V. 97. P. 1438. DOI:10.1039/CT9109701438
- Liakhov S.A., Schepetkin I.A., Karpenko O.S. et al. // Molecules. 2021. V. 26. P. 5688. DOI: 10.3390/molecules26185688
- Tantawy E.S., Amer A.M., Mohamed E.K. et al. // Journal of Molecular Structure. 2020. V. 1210. №128013. DOI: 10.1016/j.molstruc.2020.128013
- Ghalib R.M., Hashim R., Sulaiman O. et al. // Acta Cryst. 2010. E66. o1494. DOI: 10.1107/S1600536810019252
- Alizadeh A., Mohammadi R., Bayat F. et al. // Tetrahedron. 2017. V. 73, No. 30. P. 4433. DOI:10.1016/j.tet.2017.06.010
- Sharma A., Kaur G., Singh D. et al. // Current Organocatalysis. 2022. V. 9. P. 53. DOI: 10.2174/2213337208666210825112301
- Pearson B.D., Mitsch R.A., Cromwell N.H. // J. Org. Chem. 1962. V. 27, No. 5. P. 1674. DOI: 10.1021/JO01052A046
- Zhang C, Xu Z., Zhang L. et al. // Tetrahedron. 2012. V. 68, No. 26. P. 5258. DOI: 10.1016/j.tet.2012.03.020
- Jiao Y.-X., Wei L.-S., Zhao Ch.-Y. et al. // Advanced Synthesis & Catalysis. 2018. V. 360. P. 4446. DOI: 10.1002/adsc.201800928
- Gornostaev L.M., Rukovets T.A., Arnold E.V. et al. // Chemistry of Heterocyclic Compounds. 2015. V. 51. P. 166. DOI: 10.1007/s10593-015-1676-7
- Кутлалиева Э.Н., Шустова Е.А., Великородов А.В. // Прикаспийский вестник медицины и фармации. 2022. Т. 3, № 2. С. 6. DOI: 10.48612/agmu/2022.3.2.6.19
- Selvam P., Clercq E., Pannecouque C. // Int. J. Drug Des. Dis. 2013. V. 4. P. 1017.
- Velikorodov A.V., Stepkina N.N., Shustova E.A. et al. // Russian Journal of Organic Chemistry. 2015. V. 51. P. 674. DOI: 10.1134/S1070428015050164
- Tseng C.-H., Chen Y.-R., Tzeng C.-C. et. al. // European Journal of Medicinal Chemistry. 2016. V. 108. P. 258. DOI: 10.1016/j.ejmech.2015.11.031
- Матвеевская В.В. ^нтез производных ПН-индено[1,2-0]хиноксалин-11-она и индазола как биологически активных соединений и лигандов в арен-рутениевых комплексах: автореф. дис.... канд. хим. наук. Томск. 2021 г. 23 c.
- Gomaa M.A.-M., El-Katatny M.H., and Alia H.A. // Synthetic Communications. 2020. V. 50, No. 18. P. 2819. DOI: 10.1080/00397911.2020.1786122
- Barkov A.Yu., Zimnitskiy N.S., Korotaev V.Yu. et al. // Chemistry of Heterocyclic Compounds. 2017. V. 53, No. 4. P. 451. DOI: 10.1007/s10593-017-2074-0
- Babgia B.A., Bawazeer M., Alzaidi N.A. et al. // Journal of Molecular Structure. 2021. V. 1238. № 130309. DOI: 10.1016/j.molstruc.2021.130309
- Hameed S., Khan K.M., Salar U. et al. // International Journal of Biological Macromolecules. 2022. V. 221. P. 1294. DOI: 10.1016/j.ijbiomac.2022.09.102
- Kumar A., Kumar V., Diwan U. et al. // Sensors and Actuators B: Chemical. 2013. V. 176. P. 420. DOI: 10.1016/j.snb.2012.09.089
- CheX.-Q., WangLi-B. // Wuji Huaxue Xuebao. 2006. V. 22, No. 10. P 1857.
- Che X.-Q., Gao Y.-X. and Wang J.-W. // Acta Crystallographica. Section C: Crystal Structure Communications. 2006. C62. P. m440. DOI: 10.1107/S0108270106027582
- Abdallah A.M., Gomha S.M., Zaki M.E.A. et al. // Journal of Molecular Structure. 2023. 1292. № 136044. DOI: 10.1016/j.molstruc.2023.136044
- Fayed E.A., Ammar Y.A., Ragab A. et al. // Bioorganic Chemistry. 2020. V. 100. № 103951. DOI: 10.1016/j.bioorg.2020.103951
- Sahu S., Sikdar Y., Bag R. et al. // Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy. 2019. V. 213. P. 354. DOI: 10.1016/j.saa.2019.01.073
- Рыбакова А.В., Ким Д.Г., Столповская Н.В. // Вестник ЮУрГУ. Серия «Химия». 2024. Т. 16, № 1. С. 93. DOI: 10.14529/chem240107
- Рыбакова А.В. // Журнал органической химии. 2016. Т. 52, № 1. С. 106. EDN: VHTGLP.
- Рыбакова А.В., Ким Д.Г., Шарутин В.В., Слепухин П.А. // Вестник ЮУрГУ. Серия «Химия». 2023. Т. 15, № 1. С. 93. DOI 10.14529/chem230110.
- Ким Д.Г., Рыбакова А.В., Шарутин В.В. и др. Mendeleev Commun. 2019. V. 29. P. 59. DOI: 10.1016/j.mencom.2019.01.019

![Синтез и гетероциклизация неизвестного ранее S-аллилтиосемикарбазона 11Н-индено[1,2-B]хиноксалин-11-она Синтез и гетероциклизация неизвестного ранее S-аллилтиосемикарбазона 11Н-индено[1,2-B]хиноксалин-11-она](/file/cover/147246057/sintez-i-geterociklizacija-neizvestnogo-ranee-s-alliltiosemikarbazona-11n-indeno.png)
