Синтез и исследование структуры Nʹ-ацетил-N-(2,4-динитрофенил)гидразина
Автор: Анастасия Владимировна Рыбакова, Дмитрий Сергеевич Копчук, Василий Семёнович Гавико, Маргарита Александровна Еремеева, Алина Андреевна Юртаева, Наталья Валерьевна Словеснова, Татьяна Александровна Поспелова
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 4 т.17, 2025 года.
Бесплатный доступ
Nʹ-ацетил-N-(2,4-динитрофенил)гидразин 2 получен нами действием на 2,4 динитрофенилгидразин ледяной уксусной кислоты при нагревании в отсутствии катализаторов (например, концентрированной серной кислоты, предложенной в литературе) и в качестве основного продукта реакции, а не минорного, как известно в литературе. Различными физико-химическими методами (ИК-, ЯМР 1Н, 13С, хромато-масс-спектрометрия и РСА) было подробно изучено его строение в сравнении с имеющимися в литературе сведениями. Данные спектров ИК-, ЯМР 1Н и 13С хорошо согласуются с уже известными данными, результаты хромато-масс-спектрометрии дополнены предложенной схемой фрагментации. Супрамолеклярная структура соединения 2 впервые изучена в сравнении с аналогичными ему соединениями, а именно с данными РСА гидрата Nʹ ацетил-N-(2,4-динитрофенил)гидразина 2∙Н2О, N'-(2,4-динитрофенил)формилгидразида 3, N'-(2,4-динитрофенил)бензогидразида 4 и N'-(2,4-динитрофенил)-2-фторбензогидразида 5. Для всех пяти соединений молекулярная конформация определяется внутримолекулярной водородной связью N-H…O, являющейся более сильной в случае соединения 2 и его гидрата (dN-H…O 1,95 Å) по сравнению с гидразидами 3–5 (dN-H…O в диапозоне 2,01(7)–2,02(9) Å). Формирование упаковки молекул во всех кристаллах обусловлено межмолекулярными водородными связями типа N H…O. Для указанной в заголовке структуры 2 также отмечено, что она является одним из немногочисленных примеров соединений с межмолекулярными ONO…NO2, NO2…π взаимодействиями в кристалле.
2, 4-динитрофенилгидразин, ацилирование, Nʹ-ацетил-N-(2, 4-динитрофенил)гидразин, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147252523
IDR: 147252523 | УДК: 547.566 | DOI: 10.14529/chem250411
Synthesis and structural study of Nʹ-acetyl-N-(2,4-dinitrophenyl)hydrazine
Nʹ-acetyl-N-(2,4-dinitrophenyl)hydrazine 2 was obtained by the action of glacial acetic acid on 2,4-dinitrophenylhydrazine upon heating without catalysts (for example, concentrated sulfuric acid, suggested previously) and as the main reaction product, not the minor one, as was known in the literature. Its structure was studied in detail by various physicochemical methods (IR, 1H, 13C NMR, gas chromatography– mass spectrometry and X-ray structural analysis) in comparison with the information available in the literature. The IR, 1H, and 13C NMR spectra are in good agreement with the published data, the gas chromatography– mass spectrometry results are supplemented by the proposed fragmentation scheme. The supramolecular structure of compound 2 was studied for the first time in comparison with similar compounds, namely, with the X-ray analysis data of Nʹ-acetyl-N-(2,4-dinitrophenyl)hydrazine hydrate 2∙H2O, N'-(2,4- dinitrophenyl)formylhydrazide 3, N'-(2,4-dinitrophenyl)benzohydrazide 4, and N'-(2,4-dinitrophenyl)-2- fluorobenzohydrazide 5. For all five compounds, the molecular conformation is determined by the intramolecular N–H…O hydrogen bond, which is stronger in the case of compound 2 and its hydrate (dN–H…O 1.95 Å) compared to hydrazides 3–5 (dN–H…O in the range of 2.01(7)–2.02(9) Å). Formation of molecular packing in all crystals is due to intermolecular hydrogen bonds of the N H…O type. For structure 2, indicated in the title, it has also been noted that it is one of the few examples of compounds with intermolecular ONO…NO2, NO2…π interactions in a crystal.
Текст научной статьи Синтез и исследование структуры Nʹ-ацетил-N-(2,4-динитрофенил)гидразина
Химия гидразонов в последнее время вызывает значительный интерес в связи с их биологической активностью. Гидразоны демонстрируют универсальную координационную способность, что позволяет образовывать стабильные комплексы с такими металлами, как медь, серебро и золото. В обзорной статье [1] представлена универсальность и эффективность соединений на основе гидразонового фрагмента и их комплексов c металлами, о которых сообщалось за последние пять лет. При этом подчеркивается их потенциал в качестве диагностических и терапевтических агентов следующего поколения. Из-за разнообразного фармакологического потенциала гидразонов и простоты синтеза эти соединения стали предметом существенных исследований, отраженных в ряде обзорных статей. Например, известно, что медные комплексы на основе лигандов, в качестве которых выступают различные гидразоны – основания Шиффа, показывают противораковые свойства [2]. В литературе, опубликованной за последние несколько лет (2013–2023), описана антипролифера-тивная активность и механизмы действия подобных комплексов с другими ионами металлов, включая Ru, Pt, Pd, V, другие d-блоки, лантаноиды, а также ионы Ga и Sn [3]. Кроме того, широкий ряд гидразид-гидразонов проявляет сильную антибактериальную, антимикобактериальную и противогрибковую активности [4]. В обзоре 2023 г. [5] проведена оценка соединений, содержащих фрагменты гидразид-гидразона и тиадиазола, обладающих антимикобактериальным эффектом, и представлены механизмы действия имеющихся в настоящее время противотуберкулезных препаратов, включая агенты и молекулы, недавно одобренные в клинических испытаниях.
Помимо уже описанных полезных свойств гидразоны также используются в качестве прекурсоров для эффективного синтеза различных конденсированных гетероциклов в органической химии. Например, новые серии замещенных тиазолов и тиадиазолов были получены, исходя из N′-(3,4-дигидронафталин-1(2 H )-илиден)гидразинкарботиогидразида путем взаимодействия с различными типами гидразоноилхлоридов [6].
В аналитической химии гидразоны могут быть применены как высокоселективные поглотители металлов. С использованием модификации гидразида получен новый потенциальный адсорбент для разделения и удаления ионов тяжелых металлов, который имеет большой потенциал в практической очистке загрязнений воды [7].
Основным объектом нашего исследования является Nʹ-ацетил-N-(2,4-динитрофенил)гидразин. Данные о его синтезе реакцией ацилирования 2,4-динитрофенилгидразина почти двукратным избытком уксусного ангидрида в этаноле при кипячении в течение 1-ого часа были опубликованы в 1982 г. [8]. Немного позже были опубликованы данные о синтезе других Nʹ-алканоил-N-(2,4-динитрофенил)гидразинов [9].
В работе [10] описан синтез Nʹ-ацетил-N-(2,4-динитрофенил)гидразина путем реакции 2,4-динитрофенилгидразина с уксусным ангидридом в соотношении 2:1 при комнатной температуре без растворителя, что позволило увеличить выход с 64 % [8] до 82 %.
Гидрат Nʹ-ацетил-N-(2,4-динитрофенил)гидразина был получен при перемешивании водного раствора, содержащего 2,4-динитрофенилгидразин и уксусную кислоту, при 333 К в течение 30 мин [11].
Ацилирование 2,4-динитрофенилгидразина с целью получения Nʹ-ацетил-N-(2,4-динитрофенил)гидразина можно осуществить действием ацилхлорида в системе NEt 3 / Et 2 O при 0°C, либо при кипячении в системе пиридин-этилацетат [12]. Полученный Nʹ-ацетил-N-(2,4-динитрофенил)гидразин был подвержен реакции с PCl5 в диэтиловом эфире при комнатной температуре в течение 16 ч, что привело к замещению карбонильного атома кислорода на хлор и дегидрогалогенированию с образованием 2-(хлор(метил)метилен)-1-(2,4-динитрофенил)гидразина.
В исследовании [13] было обнаружено, что карбоновые кислоты (в том числе уксусная кислота) реагируют с 2,4-динитрофенилгидразином в присутствии серной кислоты с образованием соответствующих производных гидразида. Авторами было также отмечено, что образующиеся соединения термически стабильны и демонстрируют возможность применения картриджей, содержащих силикагель и 2,4-динитрофенилгидразин, в одновременном обнаружении карбоновых кислот и альдегидов в воздухе.
Интересно отметить, что при взаимодействии 3-ацетил-4-гидрокси-6-метил-2 H -пиран-2-она с 2,4-динитрофенилгидразином в уксусной кислоте образуются два соединения, которые представляют собой ( E )-3-(1-(2-(2,4-динитрофенил)гидразоно)этил)-6-метил-2-оксо-2 H -пиран-4-илацетат и исследуемый нами Nʹ-ацетил-N-(2,4-динитрофенил)гидразин в качестве минорного продукта [14].
Было обнаружено[15], что ацетат цинка, безопасный и недорогой реагент, сам по себе может действовать как селективный N-ацетилирующий агент в отсутствие растворителя при микроволновом облучении в закрытом сосуде. При таком подходе к синтезу конечные продукты образуются с умеренными выходами, в том числе Nʹ-ацетил-N-(2,4-динитрофенил)гидразин получен с выходом 95 % [15]. Одновременно другими авторами [16] предложено использование каталитического количества не только ацетата цинка, но и ацетатов других металлов (натрия, кальция, магния, марганца, меди), а также их оксидов, в уксусной кислоте в качестве высокоэффективной ацетилирующей системы для хемоселективного N-ацетилирования первичных и вторичных аминов с отличными выходами в условиях кипячения. При этом растворитель не требуется, а отмеченные особенности этого метода включают мягкие условия реакции, использование безвредных реагентов, отличные выходы, удобную обработку и повторное использование катализатора. Следует отметить, что наибольший выход (99 %) для синтеза Nʹ-ацетил-N-(2,4-динитрофенил)гидразина получен в присутствии ацетата магния.
Среди химических свойств Nʹ-ацетил-N-(2,4-динитрофенил)гидразина следует отметить описанный в литературе синтез азосоединений [17] и дальнейшее ацетилирование Nʹ-ацетил-N-(2,4-динитрофенил)гидразина с образованием N,Nʹ-диацетил-N-(2,4-динитрофенил)гидразина [18].
Целью настоящей работы является синтез и изучение Nʹ-ацетил-N-(2,4-динитрофенил)гидразина различными физико-химическими методами, включая РСА, в сравнении с имеющимися в литературе сведениями о его ренгеноструктурных данных и о структуре аналогичных динитрофенилгидразонов.
Экспериментальная часть
Спектры ЯМР записывали на спектрометрах Bruker DRX-400 (рабочая частота 400 (1Н) МГц) и AVANCE-500 (рабочая частота 500 (1Н) и 126 (13С) МГц) в ДМСО-d6, внутренний стандарт – ТМС (для ядер 1Н) и сигнал растворителя (для ядер 13С, 39,5 м. д.).
Температуру плавления измеряли с помощью прибора для определения температуры плавления ПТП (М) (V ~ 220 В, W = 500 BA).
ИК-спектр записывали на ИК-спектрометре Shimadzu IRAffinity-1S в таблетках KBr в области 4000–400 см–1.
Рентгеноструктурный анализ (РСА) проведен на автоматическом четырехкружном дифрактометре Rigaku XtaLAB Synergy с CCD-детектором HyPix-6000HE и источником рентгеновского излучения PhotonJet по стандартной процедуре (MoKα-излучение, графитовый монохроматор, ω-сканирование с шагом 1°) при T = 295(2) K. Была применена эмпирическая поправка на поглощение. Данные измеренных отражений проиндексированы, интегрированы и масштабированы с использованием пакета программ CrysAlisPro [19]. Структуры расшифрованы методом внутренней фазировки по программе SHELXT [20] и уточнены методом наименьших квадратов по F2 с использованием программы SHELXL [21]. Расшифровка и уточнение структуры проведены в программной оболочке Olex2 [22]. Неводородные атомы уточнены в анизотропном приближении. Атомы водорода при атомах кислорода выявлены из разностных рядов Фурье. Все остальные атомы водорода помещены в вычисленные положения в соответствии со стереохимическими критериями и уточнены по «схеме наездника». Результаты рентгеноструктурного анализа зарегистрированы в Кембриджской базе структурных данных под номером CCDC 2445219. Эти данные находятся в свободном доступе и могут быть запрошены по адресу
Основные кристаллографические данные и результаты уточнения структуры Nʹ-ацетил-N-(2,4-динитрофенил)гидразина приведены в табл. 1.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры Nʹ-ацетил-N-(2,4-динитрофенил)гидразина
|
Параметр |
Значение |
Параметр |
Значение |
|
Формула |
C 8 H 8 N 4 O 5 |
ρ (выч.), г/см3 |
1,554 |
|
М |
240,177 |
µ , мм–1 |
0,132 |
|
Сингония |
orthorhombic |
F (000) |
496,3 |
|
Пр. группа |
P 2 1 2 1 2 1 |
Размер кристалла (мм) |
0,42 × 0,1 × 0,06 |
|
a , Å |
4,8464(1) |
Область сбора данных по 2 θ , град. |
5,62–59,02 |
|
b, Å |
10,8110(3) |
Интервалы индексов отражений |
–6 ≤ h ≤ 6, –14 ≤ k ≤ 14, –26 ≤ l ≤ 26 |
|
c, Å |
19,5933(6) |
Измерено отражений |
45086 |
|
α, град. |
90 |
Независимых отражений |
2685 [ R int = 0,0935, R sigma = 0,0454] |
|
β, град. |
90 |
Переменных уточнения |
163 |
|
γ, град. |
90 |
GOOF |
1,047 |
|
V , Å3 |
1026,58(5) |
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0464, wR 2 = 0,1051 |
|
Z |
4 |
R -факторы по всем отражениям |
R 1 = 0,1062, wR 2 = 0,1329 |
|
Остаточная электронная плотность (min/max), e /Å3 |
0,25/–0,23 |
Синтез Nʹ-ацетил-N-(2,4-динитрофенил)гидразина (2) . Смесь 0,396 г (1,7 ммоль) 2,4-динитрофенилгидразина в 60 мл уксусной кислоты кипятили 3,5 часа. Спустя сутки из реакционной смеси испаряют растворитель, остаток перекристаллизовали из этанола. Выход желтых игольчатых кристаллов составил 0,253 г, Тпл = 195–197 °С (Лит. 196–198 °С [14], 471 K [10]). ИК-спектр: 424, 447, 466, 478, 501, 574, 594, 615, 644, 657, 667, 682, 725, 742, 790, 833, 912, 927, 1004, 1033, 1060, 1120, 1147, 1174, 1238, 1273, 1300, 1338, 1361, 1377, 1388, 1419, 1439, 1456, 1490, 1508 ( v as NO 2 ), 1521, 1543, 1558 ( v as NO 2 ), 1579, 1620, 1637, 1653 (С=О), 1683, 3120 (NH), 3344 (NH) (Лит. 3338 (NH), 3182 (NH), 1661 (C=O) [14]). ЯМР 1H (DMSO-d6, 500 МГц): δ (м.д.) 2,00 (с, 3H, CH 3 ); 7,23 (д, J =9,6, 1H, CH); 8,31 (дд, J =2,6, J =9,6, 1H, CH); 8,86 (д, J =2,6, 1H, CH); 10,06 (с, 1H, NH); 10,42 (с, 1H, NH). ЯМР 13C (DMSO-d6, 125 МГц): δ (м.д.): 21,09 (CH 3 ); 115,92 (C-6); 123,66 (C-3); 130,03 (C-5); 130,53 (C-1); 137,08 (C-2); 149,02 (C-4); 169,39 (C=O).
Обсуждение результатов
В настоящей работе нами предложен простой способ ацилирования 2,4-динитрофенилгидразина ( 1 ) уксусной кислотой при нагревании. При этом Nʹ-ацетил-N-(2,4-динитрофенил)гидразин ( 2 ) получен без использования серной кислоты в качестве катализатора, как описывалось ранее [13], и с выходом 53 %:
O^CH 3
. NH 2 NH
HNZ O HNZO
1 N t, AcOH, △ , 3ч 1
O
+
N\/N\
O'"' O O""O’
-
(1)(
Об аналогичных условиях синтеза соединения 2 было отмечено в работе [14], однако в ней соединение было побочным минорным продуктом (выход 35 %).
Nʹ-Ацетил-N-(2,4-динитрофенил)гидразин 2 исследован нами методами ИК-, ЯМР 1Н, 13С, хромато-масс-спектрометрии и РСА. В ИК-спектре соединения 2 наблюдаются полосы колебаний нитрогрупп при 1508 и 1558 см–1. В литературе [23] на основе анализа данных колебательных частот нитрогрупп в несимметричных замещенных динитробензолах показано, что в более высокочастотной составляющей антисимметричных колебаниях принимают участие атомы нитрогруппы, находящейся в орто -положении к заместителю, а в низкочастотной – атомы нитрогруппы, находящейся в пара -положении. Кроме того, можно отметить присутствие полосы колебаний карбонильной группы при 1653 см–1 и NH при 3120 и 3344 см–1.
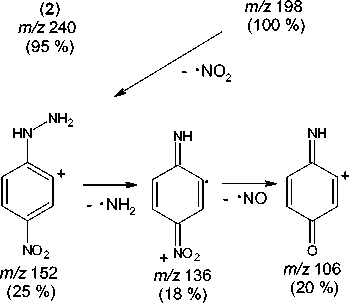
В масс-спектре соединения 2 (рис. 1) пик молекулярного иона соответствует значению его молекулярной массы ( m/z 240) и не является максимально интенсивным, что, по-видимому, связано с образованием стабильного катион-радикала 2,4-динитрофенилгидразина ( m/z 198) при отщеплении CH2CO от молекулярного иона. Подобная фрагментация является характерной для Nʹ-ацетил-фенилгидразинов [24]. Дальнейшая фрагментация катион-радикала 2,4-динитрофенилгидразина протекает согласно описанному в литературе механизму [25] с миграцией двух атомов H из гидразиновой группы в о -нитрогруппу, а последующая потеря воды приводит к образованию фраг-ментного иона с m/z 180, который далее диссоциирует посредством последовательных потерь N2 и NO. Образование пика с m/z 79 может быть связано с последовательным отщеплением радикалов NO 2 , NH 2 , NO и молекулы HCN:
Данные ЯМР 1Н и 13С согласуются с представленными в литературе данными [14]. В спектре ЯМР 1Н Nʹ-ацетил-N-(2,4-динитрофенил)гидразина 2 в сильном поле при 2,00 м.д. наблюдается синглет протонов метильной группы, ароматические протоны резонируют в области 7,23–8,86 м.д. В слабом поле при 10,06 и 10,42 м.д. имеются сигналы протонов гидразинового фрагмента. Спектр ЯМР 13С характеризуется соответствующим строению соединения 2 набором сигналов углеродных атомов, из которых метильный углерод является самым сильнопольным (δ 21,09 м.д.), а углерод карбонильной группы С=О – самым слабопольным (δ 169,39).
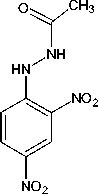
- CH2CO

+ .
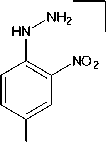
- H2O
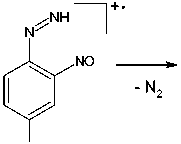
NO 2
m/z 180
(68 %)
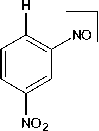
+ m/z 152
(25 %)
NO 2
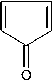
m/z 79
(70 %)
- . NO
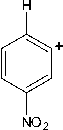
m/z 122
(38 %)
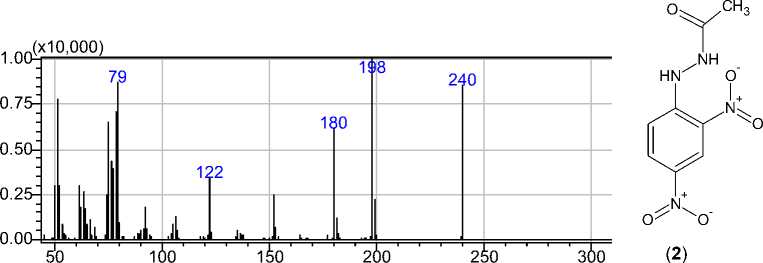
Рис. 1. Масс-спектр Nʹ-ацетил-N-(2,4-динитрофенил)гидразина 2
Структура Nʹ-ацетил-N-(2,4-динитрофенил)гидразина ранее уже была исследована методом РСА [10]. Авторами отмечено, что большинство длин связей и углов аналогичны таковым в родственных молекулах и что более сильное скручивание орто -нитрогруппы по отношению к группе гидразона (на 10,0(2) °) возникает из-за внутримолекулярной водородной связи. В нашем случае данный угол составляет 9,84 °, а длина внутримолекулярной водородной связи 1,95 Å (2,001 Å [10]) (рис. 2).
Каждая молекула также образует межмолекулярную водородную связь N(3)-H…O(5)=C (2,03(8) Å), что приводит к образованию стопок молекул вдоль оси a . Авторы [10] отмечают и более слабые взаимодействия, связывающие стопки в трехмерную сеть, C-H…O-N с участием нитрогрупп и метильных/арильных атомов водорода. Следует отметить, что для упомянутых слабых контактов ONO…NO 2 (O1···N1i = 2,944(2) Å) не обозначена их роль в формировании паркетно-стопочной («елочной») упаковки (рис. 3, CCDC 2218907). Природа таких ONO…NO 2 взаимодействий между нитробензольными фрагментами была изучена в работе [26], причём наиболее благоприятный межплоскостной угол взаимодействующих нитро-групп получается, когда обе NO 2 -группы параллельны друг другу и расположены вокруг центра инверсии, то есть параллельная форма вычисляется как более стабильная, чем перпендикулярная. Однако, что интересно, расстояние N…O немного короче в перпендикулярной геометрии, которая, к слову, и наблюдается в кристалле соединения 2 (см. рис. 3), по сравнению с параллельной геометрией.
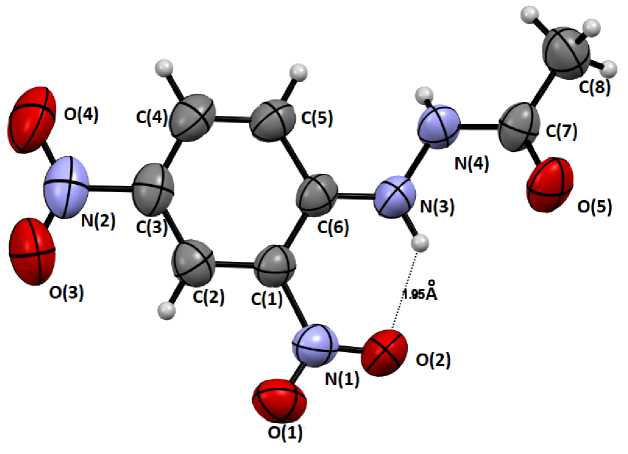
Рис. 2. Данные РСА соединения 2 и принятая в структурном эксперименте нумерация атомов (пунктирными линиями показана внутримолекулярная водородная связь). Эллипсоиды смещения нарисованы на уровне вероятности 50 %, а атомы H – в виде небольших сфер произвольного размера
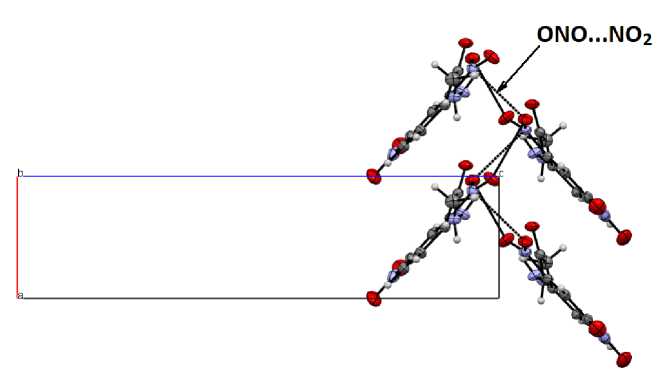
Рис. 3. Паркетно-стопочная («елочная») упаковка молекул по данным кристалла CCDC 2218907
Кроме того, как для полученных нами кристаллографических данных, так и для известных в литературе примеров [10] стопки молекул поддерживаются межмолекулярными NO2…π-взаимодействиями с участием нитро-групп в орто -положении и электронодефицитного динитробензольного цикла. При этом расстояние ONO(1)…C(3) Ar составляет 3,20(9) Å (рис. 4) (3,13(3) Å [10]), что меньше суммы ван-дер-ваальсовых радиусов соответствующих атомов [27], расстояние от атома кислорода О(1) до центра ароматической системы динитробензола составляет 3,54(8) Å (3,49(5) Å [10]). Теоретический анализ (расчет DFT) для кристалла бис (малеонитрилдитиолато)никелата(III) 1-(4′-нитробензил)пиразиния (dONO…C Ar 3,17(3) Å, расстояние от атома кислорода О до центра ароматической системы пиразина составляет 3,32(5) Å, CCDC 707088) показал, что такие межмолекулярные взаимодействия можно отнести к кулоновскому взаимодействию [28]. Если взаимодействия O…π (поделенная пара…π) наблюдались, например, в электронодефицитном триазиновом кольце и атоме O фрагментов воды, эфира или карбонила [28], то примеры взаимодействия NO 2 …π действительно редки.
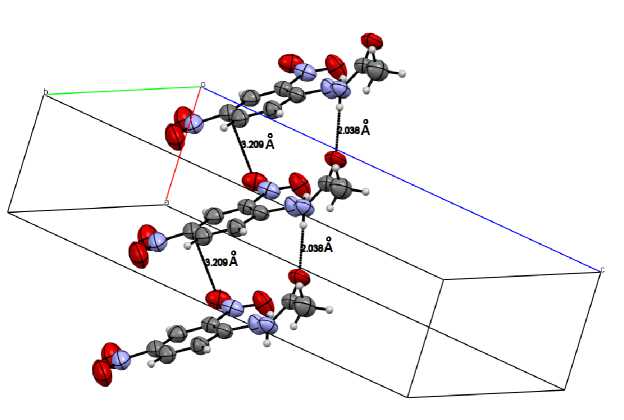
Рис. 4. Участие NO 2 …π- взаимодействий (3,20(9) Å)
и контактов N(3)-H…O(5)=C (2,03(8) Å) в образовании стопок вдоль оси а
В Кембриджской Структурной Базе Данных (Cambridge Structural Database нами были найдены структуры, близкие по строению соединению 2: гидрат Nʹ-ацетил-N-(2,4-динитрофенил)гидразина (2∙Н2О, CCDC 961991 [11]), N'-(2,4-динитрофенил)формилгидразид (3, CCDC 2063756 [29]), N'-(2,4-динитрофенил)бензогидразид (4, CCDC 896359 [30]), N'-(2,4-динитрофенил)-2-фторбензогидразид (5, CCDC 942588 [31]). Анализ выбранных структур показал, что внутримолекулярная водородная связь N-H…O присутствует во всех гидразидах 3–5, однако по сравнению с соединением 2 и его гидратом 2∙Н2О (dN-H…O 1,95(4) Å не отличается от аналогичного расстояния в молекуле 2) она слабее и характеризуется большим расстоянием dN-H…O (в диапозоне 2,01(7)–2,02(9) Å). Следует отметить, что стабилизация структуры фторбензогидразида 5 также обусловлена дополнительной внутримолекулярной связью N–H…F (dH…F 2,10 Å). Упаковка молекул во всех описываемых соединениях 2–5 обусловлена межмолекулярными водородными связями типа N-H…O=С, которые в случае соединений 4 и 5 связывают молекулы в зигзагообразные цепи, вытянутые вдоль оси а и b соответственно, а в случае соединений 2 и 3 – в стопки вдоль оси а и b соответственно. В случае гидрата 2∙Н2О упаковка молекул в кристалле является более сложной за счёт участия молекулы воды в формировании множественных межмолекулярных водородных связей типа O-H…O и N-H…O. При этом молекула воды окружена тремя органическими группами посредством этих связей, что приводит к образованию трехмерной сети. Также интересно, что межмолекулярных ONO…NO2, NO2…π взаимодействий в структурах гидрата 2∙Н2О и гидразидов 3–5 нами не обнаружено.
Заключение
Таким образом, Nʹ-ацетил-N-(2,4-динитрофенил)гидразин 2 получен нами действием на 2,4-динитрофенилгидразин ледяной уксусной кислоты при нагревании в отсутствии катализаторов. Различными физико-химическими методами (ИК-, ЯМР 1Н, 13С, хромато-масс-спектрометрия и РСА) детально изучено его строение в сравнении с имеющимися в литературе сведениями. Описаны особенности супрамолеклярной структуры соединения 2 и аналогичных ему структур: гидрат Nʹ-ацетил-N-(2,4-динитрофенил)гидразина ( 2∙Н 2 О ), N'-(2,4-динитрофенил)формилгидразид ( 3 ), N'-(2,4-динитрофенил)бензогидразид ( 4 ), N'-(2,4-динитрофенил)-2-фторбензогидразид ( 5 ). При этом общей концепцией в стабилизации молекул является образование внутримолекулярной водородной связи N-H…O. Формирование упаковки молекул во всех кристаллах обусловлено межмолекулярными водородными связями типа N-H…O. Для структуры 2 также отмечено, что она является одним из немногочисленных примеров соединений с межмолекулярными ONO…NO2, NO2…π взаимодействиями в кристалле.


