Синтез и исследование свойств 7-замещенных теофиллинов
Автор: Петрова Ксения Юрьевна, Ким Дмитрий Гымнанович, Шарутин Владимир Викторович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 1 т.12, 2020 года.
Бесплатный доступ
В настоящей работе впервые алкилированием теофиллина алкенилгалогенидами в ДМФА в присутствии K2CO3 при нагревании на водяной бане (100 ºС) получены 7-(2-бромаллил)- и 7-циннамилтеофиллины. Методом масс-спектрометрии на газовых хромато-масс-спектрометрах GCMS-QP2010 UltraShimadzu и Agilent 6890 N проведен анализ спектров полученных алкенилтеофиллинов и изучено поведение при электронной ионизации, выявлены закономерности фрагментации молекул. Максимальной интенсивностью в масс-спектре 7-циннамилтеофиллина обладает пик, принадлежащий циннамил-катиону, пик с m/z 91 свидетельствует об образовании тропилий-катиона. В случае 7-(2-бромаллил)теофиллина максимальной интенсивностью обладает катион, обусловленный элиминированием бром-радикала. 7-(2,2,3-Трибромпропил)теофиллин и 7-(2,3-дибром-3-фенилпропил)теофиллин получены присоединением брома по двойной связи 7-(2-бромаллил)- и 7-циннамилтеофиллина в CHCl3 при комнатной температуре. Структуры продуктов реакции подтверждены методами протонного магнитного резонанса и масс-спектрометрии. Структура 7-(2,2,3-трибромпропил)теофиллина подтверждена методом РСА, в кристалле присутствуют по два типа кристаллографически независимых молекул, геометрические параметры которых незначительно отличаются. В масс-спектрах галогенсодержащих соединений проявляется характерное распределение изотопных пиков молекулярного иона: дублет с соотношением интенсивностей приблизительно 1:1 для соединения с одним атомом брома, триплет пиков в случае наличия двух атомов брома, а также квартет в соотношении 1:3:3:1 для трибромсодержащих производных. Взаимодействие 7-пропаргилтеофиллина с бромом в CHCl3 при комнатной температуре останавливается на стадии присоединения одной молекулы, в результате получен 2,3-дибромаллилтеофиллин, что доказано методами протонного магнитного резонанса и масс-спектрометрии. Взаимодействие 7-(2,3-дибромпропил)теофиллина с о -фенилендиамином в ацетонитриле при комнатной температуре приводит к аннелированию хиноксалинового кольца. В спектре ЯМР 1Н характерным является появление сигналов ароматического кольца при 6,85-7,05 м.д.
Теофиллин, 7-(2-бромаллил)теофиллин, 7-циннамилтеофиллин, 7-(2, 2, 3-трибромпропил)теофиллин, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147233162
IDR: 147233162 | УДК: 546.865 | DOI: 10.14529/chem200111
Synthesis and some transformations of 7-substituted theophyllines
In the present study 7-(2-bromoallyl)- and 7-cinnamyltheophylline have been obtained by the interaction of alkenylhalides with theophylline in DMF in the presence of anhydrous potassium carbonate at 100 ºС in water bath. Fragmentation under electron ionization of the obtained 7-alkenyltheophyllines has been investigated by gas chromatography-mass spectrometry analysis, the main molecule fragmentation ways have been revealed. The mass spectra have been obtained on an UltraShimadzu GCMS-QP2010 and an Agilent 6890 N. The cinnamyl cation peak has the maximum intensity in the 7-cinnamylteophylline mass spectrum. The formation of tropylium cation ( m/z 91) is characteristic for the 7-cinnamylteophylline mass spectrum. In the case of 7-(2-bromoallyl)theophylline the elimination of bromine radical leads to formation of the peak with the maximum intensity. 7-(2,2,3-Tribromopropyl)theophylline and 7-(2,3-dibromo-3-phenylpropyl)theophylline have been synthesized by the addition of bromine to the double bonds of 7-(2-bromoallyl)- and 7-cinnamyltheophylline in CHCl3 at room temperature. The structures of reaction products have been confirmed by 1H NMR spectroscopy and gas chromatography-mass spectrometry. The structure of 7-(2,2,3-tribromopropyl)theophylline has been confirmed by X-ray analysis. The crystal contains two types of crystallographically independent molecules, the geometric parameters of which slightly differ. There is characteristic distribution of the molecular ion isotope peaks in the mass spectra of halogen-containing compounds: a doublet with an intensity ratio of approximately 1:1 for compounds with one bromine atom, a triplet of peaks in the case of two bromine atoms, and a quartet with an intensity ratio 1:3:3:1 for tribromoderivatives. In the case of 7-propargyltheophylline the reaction with bromine stops at the addition of one bromine molecule, which is proved by the formation of 7-(2,3-dibromoallyl)theophylline. It has been confirmed by 1H NMR and chromatography-mass spectrometry. Interaction of 7-(2,3-dibromopropyl)theophylline with o -phenylenediamine in acetonitrile at room temperature leads to the formation of quinoxaline ring. The 1H NMR spectrum contains characteristic signals of aromaticprotons at δ 6.85-7.05 ppm.
Текст научной статьи Синтез и исследование свойств 7-замещенных теофиллинов
Известно, что производные ксантина обладают широким спектром биологической активности, в частности среди них найдены вещества, обладающие антибактериальной, противоаллергической, противовоспалительной, противогрибковой, антиокислительной и инсектицидной активностью [1–6]. Ранее в литературе алкилированием теофиллина ( 1 ) получены различные N7-замещенные производные, в том числе 7-аллил- ( 2a ) [7–11] и 7-пропаргилтеофиллин ( 2d ) [9, 12– 16]. Нами ранее в работе [17] проведен анализ масс-спектров и изучено поведение при электронной ионизации теофиллинов 2a и 2d .
Обсуждение результатов
В настоящей работе алкилированием теофиллина 1 в ДМФА в присутствии K 2 CO 3 при нагревании на водяной бане (100 ºС) впервые получены 7-(2-бромаллил)теофиллин ( 2b ) и 7-циннамилтеофиллин ( 2c ) (схема 1).
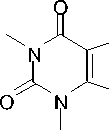
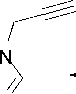
N
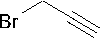
2d
K 2 CO 3 , DMF
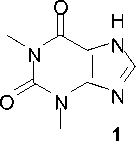

R 1
K2CO3, DMF
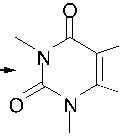
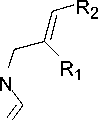
N
2a-c
Схема 1
a R 1 = H, R 2 = H; b R 1 = Br, R 2 = H, c R 1 = H, R 2 = Ph
В масс-спектрах соединений 2b , c присутствуют пики молекулярных ионов. В случае бро-маллилтеофиллина 2b он обладает характерной мультиплетностью. Максимальной интенсивностью в масс-спектре циннамилтеофиллина 2c обладает пик с m/z 117, принадлежащий цин-намил-катиону A , при этом пик с m/z 91 свидетельствует об образовании тропилий-катиона B (схема 2).
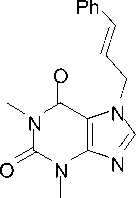
- C 7 H 7 N 4 O 2
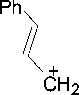
- C 2 H 2
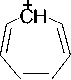
2c m/z 296
A m/z 117
B m/z 91
Схема 2
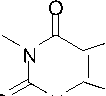
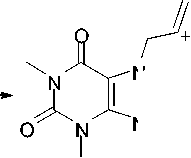
В случае бромаллилтеофиллина 2b максимальной интенсивностью обладает катион C , обусловленный элиминированием бром-радикала. Пики с m/z 162 ( D ) и 134 ( E ) свидетельствуют о дальнейшем элиминировании метилизоцианата и СО (схема 3).
NN
N
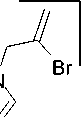
+
.
- Br
N
N - CH 3 NCO
C m/z 219
Схема 3
O< C
N
2b
m/z 298
N
N N - CO N N
D m/z 162
E m/z 134
Ранее нами в работах [17, 18] было показано, что взаимодействие 7-алкенил-8-хлортеофиллинов и 7-аллилтеофиллина с бромом протекает с образованием продуктов присоединения по двойной связи – 7-(2,3-дибромалкил)теофиллинов. В частности реакция теофиллина 2a с бромом приводит к образованию 7-(2,3-дибромпропил)теофиллина ( 3a ). В работе [19] показано, что бром реагирует с 1-аллилтебромином с образованием продукта присоединения по двойной связи, а с 1-металлилтеобромином – смеси оксазолопуринов линеарного и ангулярного строения и 1-(2,3-дибром-2-метилпропил)теобромина.
В настоящей работе нами взаимодействием аллилтеофиллинов 2b , c с бромом получены 7-(2,2,3-трибромпропил)теофиллин ( 3b ) и 7-(2,3-дибром-3-фенилпропил)теофиллин ( 3с ) (схема 4). Структура соединения 3b подтверждена методом РСА (см. рисунок).
2a-c
Br2
CHCl3
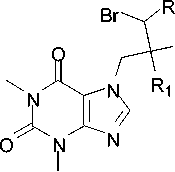
3a-c
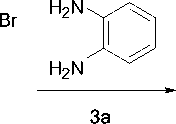
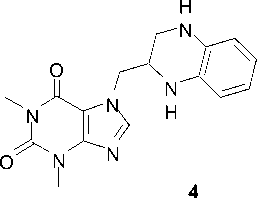
Схема 4
a R 1 = R 2 = H, b R 1 = Br, R 2 = H, c R 1 = H, R 2 = Ph
В кристалле соединения 3b присутствуют по два типа кристаллографически независимых молекул, геометрические параметры которых незначительно отличаются.
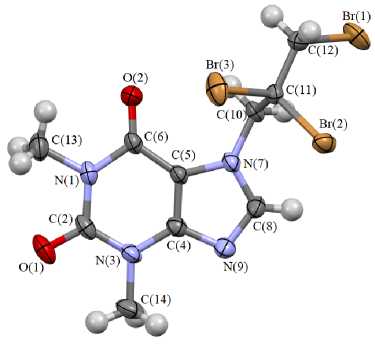
Строение соединения 3b
Строение дибромпропилтеофиллина 3а подтверждается превращением в 7-((1,2,3,4-тетрагидрохиноксалин-2-ил)метил)теофиллин ( 4 ) при его взаимодействии с о -фенилендиамином в ацетонитриле при комнатной температуре (схема 4). В спектре ЯМР 1Н характерным является появление сигналов ароматического кольца при 6,85–7,05 м.д.
Теоретически взаимодействие пропаргилтеофиллина 2d с бромом может приводить к образованию как 2,3-дибромаллилтеофиллина ( 3d ), так и 2,2,3,3-тетрабромпропилтеофиллина ( F ). Методами ЯМР 1Н и ХМС нами доказано, что реакция останавливается на образовании соединения 3d (схема 5), в спектре ЯМР характерным является однопротонный триплет =СHBr при 7,24 м.д.
2d
Br 2
CHCl 3
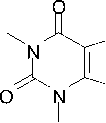
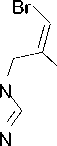
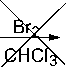
3d
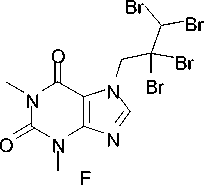
Схема 5
Экспериментальная часть
Спектры ЯМР 1Н (500 МГц) соединений 3b , 3d записаны на приборе Bruker AVANCE-500. Спектры ЯМР 1Н (400 МГц) соединений 2b , c , 3c , 4 записаны на приборе Bruker DRX-400. Внутренний стандарт – ТМС, растворитель – ДМСО-d6.
Масс-спектры соединений 2b , c , 3c сняты на газовом хромато-масс-спектрометре Agilent 6890 N (ЭУ, 70 эВ). Масс-спектры электронного удара соединений 3b сняты на газовом хро-мато-масс-спектрометре GCMS-QP2010 UltraShimadzu (ЭУ, 70 эВ).
Рентгеноструктурное исследование соединения 3b проведено на автоматическом четырехкружном дифрактометре D8 QUEST фирмы Bruker (Mo K α -излучение, λ = 0,71073 Å, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [20]. Все расчеты по определению и уточнению структуры выполнены по программам SHELXL/PC [21]. Структура соединения определена прямым методом и уточнена методом наименьших квадратов в анизотропном приближении для неводородных атомов. Полный набор рентгеноструктурных данных депонирован в Кембриджском банке структурных данных (CCDC 1905740).
Синтез соединений 2b, c. Общая методика
К раствору 276 мг (2 ммоль) безводного карбоната калия в 10 мл ДМФА добавляли 360 мг (2 ммоль) теофиллина, смесь нагревали на водяной бане с обратным холодильником в течение 30 минут. К полученному раствору добавили раствор 2 ммоль алкилирующего агента в 1 мл ДМФА. Полученную смесь нагревали на водяной бане с обратным холодильником в течение 6 ч. Полученный осадок отфильтровывали, фильтрат испаряли. Продукт экстрагировали хлороформом, растворитель испаряли.
7-(2-Бромаллил)теофиллин (2b). Выход 514 мг (86 %), белый порошок, т. пл. 95–97 °С. Спектр ЯМР 1Н (ДМСО- d 6 ), δ, м.д.: 3,21 с (3Н, N1CH 3 ), 3,43 с (3Н, N3CH 3 ), 5,19 c (2Н, NCH 2 ), 5,70 д (1H, =CHH, 2 J 1,9 Гц), 5,85 д (1Н, =CHH, 2 J 1,9 Гц), 8,14 c (1Н, Н 8 ). Масс-спектр, m/z ( I отн. , %): 300 [M+2]+ (6,8), 298 [M]+• (7,5), 220 (12,6), 219 [M–Br]+ (100), 162 [M–Br–CH 3 NCO]+ (17,7), 135 (7,0), 134 [M–Br–CH 3 NCO–CO]+ (24,6), 107 [M–Br–CH 3 NCO–CO–HCN]+ (23,1), 95 (9,2), 94 [C 4 H 4 N 3 ]+ (17,0), 81 [C 5 H 7 N]+• (5,7), 68 (10,1), 67 (24,4), 66 (7,4), 53 [C 2 HN 2 ]+ (6,2), 42 (10,8), 41 [C 2 H 3 N]+• (6,2), 40 (8,3), 39 (20,2).
7-Циннамилтеофиллин (2c). Выход 440 мг (74 %), белый порошок, т. пл. 94–95 °С. Спектр ЯМР 1Н (ДМСО- d 6 ), δ, м.д.: 3,23 с (3Н, N1CH 3 ), 3,43 с (3Н, N3CH 3 ), 5,07 д (2H, NCH 2 , 3 J 5,6 Гц), 6,49 дт (1H, =СН, 3 J 15,9 Гц, 3 J 5,6 Гц), 6,58 д (1H, =СНC 6 H 5 , 3 J 15,9 Гц), 7,21–7,42 м (5H, C 6 H 5 ), 8,14 с (1H, Н8). Масс-спектр, m/z ( I отн. , %): 296 [M]+• (28,0), 117 [C 9 H 9 ]+ (100), 91 [C 7 H 7 ]+ (14,3). ИК-спектр, ν, см - 1: 3099 (=CH 2 ), 1705 (C=O), 1666 (C=O), 1598 (С-С ар ), 1475 (С-С ар ), 923 (=CH).
Синтез соединений 3b-d . Общая методика . К раствору 0,5 ммоль 7-органилтеофиллина в 4 мл хлороформа добавляли раствор 0,052 мл (1 ммоль) Br 2 в 2 мл хлороформа. Полученную смесь перемешивали на магнитной мешалке в течение 1 ч и оставляли на сутки. Полученный осадок отфильтровывали и сушили.
7-(2,2,3-Трибромпропил)теофиллин (3b). Выход 93 мг (62 %), желтые кристаллы, т. пл. 160–162 °С. Спектр ЯМР 1Н (ДМСО- d 6 ), δ, м.д.: 3,26 с (3Н, N1CH 3 ), 3,50 с (3Н, N3CH 3 ), 4,40 с (2H, СН 2 Br), 5,35 с (3H, NСH 2 ), 8,18 c (1Н, Н 8 ). Масс-спектр, m/z ( I отн. , %): 462 (10,8), 460 (27,0), 458 (29,8), 456 [ M ]+• (10,9), 381 (49,7), 379 (100), 377 [ M -Br]+ (50,0), 299 (8,1), 297 [ M -Br 2 ]+• (8,2), 219 [ M -Br 3 ]+ (77,0), 218 [ M -Br 2 -HBr]+• (29,7), 193 [ M -Br 3 -HCN]+ (52,7), 180 [C 7 H 8 N 4 O 2 ]+• (27,0), 162 (18,9), 152 (16,2), 134 (28,4), 128 (32,4), 109 (28,4), 107 (29,7), 95 (43,2), 94 (54,0), 81 (25,0), 67 (62,1), 53 (12,2), 42 (24,5), 39 (39,2).
7-(2,3-Дибром-3-фенилпропил)теофиллин (3с). Выход 96 мг (70 %), белый порошок, т. пл. 146–148 °С. Спектр ЯМР 1Н (ДМСО- d 6 ), δ, м.д: 3,27 с (3Н, N1CH 3 ), 3,44 с (3Н, N3CH 3 ), 4,66 дд (1H, NCHH, 3 J 10,7 Гц, 2 J 14,4 Гц), 5,25 дд (1H, NCHH, 3 J 3,0 Гц, 2 J 14,4 Гц), 5,38 тд (1H, СНBr, 3 J 10,7 Гц, 3 J 3,0 Гц, 3 J 10,0 Гц), 5,72 д (1H, СНBrC 6 H 5 , 3 J 10,0 Гц), 7,34 д (1Н, пара -Ph, 3 J 7,3 Гц), 7,41 т (2Н, мета -Ph, 3 J 7,3 Гц), 7,51 д (2Н, орто -Ph, 3 J 7,3 Гц), 8,14 c (1Н, Н 8 ). Масс-спектр, m/z ( I отн. , %): 456 [M]+• (4,9), 378 (6,7), 377 [M–Br]+ (31,6), 376 (6,7), 375 (35,3), 296 [M–Br 2 ]+• (6,6), 193 (34,8), 118 (10,6), 117 [C 9 H 9 ]+ (100), 116 (41,3), 115 (88,8), 109 (6,2), 94 (5,0), 91 [C 7 H 7 ]+ (23,1), 81 (7,3), 67 (5,1), 32 (13,3), 28 (37,9).
7-(2,3-Дибромаллил)теофиллин (3d). Выход 132 мг (70 %), оранжевые кристаллы, т. пл. 176–177 °С. Спектр ЯМР 1Н (ДМСО- d 6 ), δ, м.д: 3,22 с (3Н, N1CH 3 ), 3,44 с (3Н, N3CH 3 ), 5,36 д (2Н, NСH 2 , 4 J 1,2 Гц) , 4,88 т (1Н, =CHBr, 4 J 1,2 Гц), 8,16 c (1Н, Н 8 ).
7-((1,2,3,4-Тетрагидрохиноксалин-2-ил)метил)теофиллин (4). К раствору 300 мг (0,79 ммоль) 7-(2,3-дибромпропил)теофиллина в 10 мл ацетонитрила добавить раствор 85 мг (0,79 ммоль) о -фенилендиамина в 5 мл ацетонитрила. Полученную смесь перемешивали на магнитной мешалке в течение 4 ч. Растворитель испаряли и экстрагировали продукт этиловым спиртом. Вещество выделяют в виде коричневого масла. Выход 50 мг (20 %). Спектр ЯМР 1Н (400 МГц, ДМСО- d 6 ): 3,21 с (3Н, N1CH 3 ), 3,42 с (3H, N3CH 3 ), 3,99 д (2Н, NCH 2 , 3 J 5,4 Гц), 4,59 дд (1Н, NHCHH, 2 J 14,3 Гц, 3 J 9,1 Гц), 4,79 дд (1Н, NHCHH, 2 J 14,3 Гц, 3 J 4,7 Гц), 4,87 м (1Н, NHCH, 3 J 5,4 Гц, 3 J 9,1 Гц, 3 J 4,7 Гц), 6,89–7,01 м (4Н, C 6 H 4 ), 8,14 с (1Н, Н 8 ).
Выводы
Таким образом, алкилирование теофиллина алкенил(пропаргил)галогенидами протекает с образованием 7-алкенил(пропаргил)теофиллинов. Взаимодействие 7-алкенил(пропаргил)теофил-линов с бромом протекает с образованием дибромалкилтеофиллинов, а реакция 7-(2,3-дибромпропил)теофиллина с о-фенилендиамином приводит к аннелированию хиноксалинового кольца.
Список литературы Синтез и исследование свойств 7-замещенных теофиллинов
- Synthesis and Biological Activities of Novel Methyl Xanthine Derivatives / Y. Chen, B. Wang, Y. Guo et al. // Chem. Res. Chin. Univ. - 2014. - V. 30, № 1. - P. 98-102. DOI: 10.1007/s40242-014-3173-4
- Synthesis and Antiaggregant Activity of 8-Substituted 1-Alkyl-3-Methyl-7-(1-Oxothietan-3-yl)Xanthines / Yu.V. Shabalina, F.A. Khaliullin, A.A. Spasov et al. // Pharm. Chem. J. - 2013. - V. 47, № 3. - P. 151-153. DOI: 10.1007/s11094-013-0915-4
- The Synthesis and the Biological Evaluation of New Thiazolidin-4-one Derivatives Containing a Xanthine Moiety / F.G. Lupascu, O.M. Dragostin, L. Foia et al. // Molecules. - 2013. - V. 8, № 18. - P. 9684-9703. DOI: 10.3390/molecules18089684
- Synthesis and Antiallergic Activity of 7-Substituted Theophylline Derivatives / R.G. Glushkov, I.M. Ovcharova, V.B. Nikitin et al. // Pharm. Chem. J. - 1989. - V. 23, № 10. - P. 849-852. DOI: 10.1007/bf00764818
- Design and Synthesis of Some New Theophylline Derivatives with Bronchodilator and Antibacterial Activities / A.M. Hayallah, W.A. Elgaher, O.I. Salem et al. // Arch. Pharmacal Res. - 2011. - V. 34, № 1. - P. 3-21. DOI: 10.1007/s12272-011-0101-8
- Hayallah, A.M. Design and Synthesis of New 8-Anilide Theophylline Derivatives as Bronchodilators and Antibacterial Agents / A.M. Hayallah, A.A. Talhouni, M.A. Alim // Arch. Pharmacal Res. - 2012. - V. 35, № 8. - P. 1355-1368.
- DOI: 10.1007/s12272-012-0805-4
- Tanabe, T. The N-Alkylation of Xanthine Derivatives with Trialkyl Phosphates / T. Tanabe, K. Yamauchi, M. Kinoshita // Bull. Chem. Soc. Jpn. - 1976. - № 49. - P. 3224-3226.
- DOI: 10.1246/bcsj.49.3224
- Solid Liquid Phase Transfer Catalysis: Alkylation of Theophylline / G. Bram, Y. Bensaid, C. Combet-Farnoux et al. // Pharmazie. - 1986. - V. 41, № 6. - P. 431-432.
- Daly, J.W. Analogs of Caffeine and Theophylline: Effect of Structural Alterations on Affinity at Adenosine Receptors / J.W. Daly, W.L. Padgett, M.T. Shamim // J. Med. Chem. - 1986. - V. 29, № 7. - P. 1305-1308.
- DOI: 10.1021/jm00157a035
- Caffeine-Based Gold(I) N-Heterocyclic Carbenes as Possible Anticancer Agents: Synthesis and Biological Properties / B. Bertrand, L. Stefan, M. Pirrotta et al. // Inorg. Chem. - 2014. - V. 53, № 4. - P. 2296-2303.
- DOI: 10.1021/ic403011h
- Lysakowska, M. Design, Synthesis, Antiviral, and Cytostatic Evaluation of Novel Isoxazolidine Analogs of Homonucleotides / M. Lysakowska, J. Balzarini, D.G. Piotrowska // Arch. Pharm. - 2014. -V. 347, № 5. - P. 341-353.
- DOI: 10.1002/ardp.201300382
- Design, Synthesis, Anticancer, Antimicrobial Activities and Molecular Docking Studies of Theophylline Containing Acetylenes and Theophylline Containing 1,2,3-Triazoles with Variant Nucleoside Derivatives / R.R. Ruddarraju, A.Ch. Murugulla, R. Kotla et al. // Eur. J. Med. Chem. - 2016. - V. 123. - P. 379-396.
- DOI: 10.1016/j.ejmech.2016.07.024
- ‘Click Synthesis' of 1H-1,2,3-Triazolyl-Based Oxiconazole (=(1Z)-1-(2,4-Dichlorophenyl)-2-(1H-imidazol-1-yl)ethanone O-[(2,4-Dichlorophenyl)methyl]oxime) Analogs / M.N. Soltani Rad, M. Navid, A. Zeinab et al. // Helv. Chim. Acta. - 2011. - V. 94, № 12. - P. 2194-2206.
- DOI: 10.1002/hlca.201100189
- Click Reaction Based Synthesis, Antimicrobial, and Cytotoxic Activities of New 1,2,3-Triazoles / M.R. Sayed Aly, S. Hosam Ali, M. Mosselhi et al. // Bioorg. Med. Chem. Lett. - 2015. - V. 25, № 14. - P. 2824-2830.
- DOI: 10.1016/j.bmcl.2015.04.096
- 1,4-Dihydroxyanthraquinone-copper(II) Nanoparticles Immobilized on Silica Gel: a Highly Efficient, Copper Scavenger and Recyclable Heterogeneous Nanocatalyst for a Click Approach to the Three-Component Synthesis of 1,2,3-Triazole Derivatives in Water / H. Sharghi, A. Khoshnood, M.M. Doroodmand et al. // J. Iran. Chem. Soc. - 2012. - V. 9, № 2. - P. 231-250.
- DOI: 10.1007/s13738-011-0046-3
- Copper/Graphene/Clay Nanohybrid: A Highly Efficient Heterogeneous Nanocatalyst for the Synthesis of Novel 1,2,3-Triazolyl Carboacyclic Nucleosidesvia‘Click'Huisgen1,3-Dipolar Cycloaddition / M.N. Soltani Rad, S. Behrouz, J. Hoseini et al. // Helv. Chim. Acta. - 2015. - V. 98, № 9. - P. 1210-1224.
- DOI: 10.1002/hlca.201500149
- Исследование N-алкильных производных теофиллина методом хроматомасс-спектрометрии / К.Ю. Ошеко, Д.Г. Ким, А.Ф. Алзамили, Т.Д. Еременко // Вестник ЮУрГУ. Серия "Химия". - 2018. - Т. 10, № 4. - С. 12-24.
- Синтез и исследование свойств 7-алкенил(пропаргил)-8-хлортеофиллинов / К.Ю. Петрова, Д.Г. Ким, В.В. Шарутин и др. // ЖОХ. - 2019. - Т. 89, № 11. - С. 1679-1685.
- Взаимодействие 1-аллил(металлил)теобромина с галогенами / К.Ю. Ошеко, Д.Г. Ким, О.С. Ельцов, Т.Д. Еременко // ЖОХ. - 2019. - Т. 89, № 4. - С. 561-565.
- Bruker (2000) SMART. Bruker Molecular Analysis Research Tool, Versions 5.625, Bruker AXS, Madison, Wisconsin, USA.
- Bruker (2000) SAINTPlus Data Reduction and Correction Program Versions 6.02a, Bruker AXS, Madison, Wisconsin, USA.


