Синтез и кристаллическая структура аренсульфонатов алкилтрифенилфосфония [Ph3PR][OSO2Ar]
Автор: Механошина Евгения Сергеевна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 2 т.15, 2023 года.
Бесплатный доступ
Реакцией эквимолярных количеств бромидов алкилтрифенилфосфония с мезитиленсульфоновой, 1-окси-2,4-динитро-7-нафталинсульфоновой, 2-карбоксибензолсульфоновой и сульфосалициловой кислотами в воде получены ионные аренсульфонаты алкилтрифенилфосфония [Ph3PR][OSO2Ar], R = CH2Ph, Ar = С6H2Me3-2,4,6 (1), R = CH2ОMe, Ar = C10H4(OH-1)(NO2)2-2,4 (2), R = (CH2)4Br, Ar = C6H4(COOH-2) (3), R = CH2ОН, Ar = C6H3(COOH-3)(OH-4) (4). Особенности строения комплексов 1-4 установлены методом РСА. Кристаллы 1 [C34H35O4PS, M 570,65; сингония моноклинная, группа симметрии P21/c ; параметры ячейки: a = 11,083(12), b = 21,520(16), c = 12,768(10) Å; a = 90,00, β = 92,62(4), g = 90,00 град., V = 3042(5) Å3, Z = 4; rвыч = 1,246 г/см3], 2 [C30H25N2O9PS, M 620,55; сингония триклинная, группа симметрии P- 1; параметры ячейки: a = 8,998(5), b = 12,347(5), c = 13,204(6) Å; a = 82,92(2), β = 81,90(3), g = 83,92(2) град., V = 1435,2(12) Å3, Z = 2; rвыч = 1,436 г/см3], 3 [C29H28O5PSBr, M 599,45; сингония моноклинная, группа симметрии P21/n ; параметры ячейки: a = 12,685(11), b = 16,178(13), c = 13,743(13) Å; a = 90,00, β = 90,39(3), g = 90,00 град., V = 2820(4) Å3, Z = 4; rвыч = 1,412 г/см3], 4 [C26H27O9PS, M 546,50; сингония моноклинная, группа симметрии P21/n ; параметры ячейки: a = 9,201(4), b = 10,113(15), c = 28,77(4) Å; a = 90,00, β = 90,51(6), g = 90,00 град., V = 2677(7) Å3, Z = 4; rвыч = 1,356 г/см3] состоят из тетраэдрических алкилтрифенилфосфониевых катионов и аренсульфонатных анионов с тетраэдрическим атомом серы. Длины связей P-C варьируют в интервале 1,717(3)-1,931(3) Å. Валентные углы СРС принимают значения 101,87(14)°-122,99(13)°. Расстояния S-C близки между собой и изменяются в пределах 1,752(5)-1,798(6) Å; длины связей S-O: 1,303(2)-1,53(2) Å. Соединения 1 и 4 кристаллизуются в виде гидратов. Катионы и анионы в комплексах 1-4 связаны слабыми водородными связями типа S=O∙∙∙Н(Рh) [2,25-2,67 Å] и S=O∙∙∙Н(C) [2,23-2,63 Å]. В кристаллических структурах 1, 2, 4 присутствуют CH∙∙∙π взаимодействия. В формировании пространственной структуры кристаллов соединений 1, 2 также принимают участие π-π взаимодействия. Полные таблицы координат атомов, длин связей и валентных углов для структур депонированы в Кембриджском банке структурных данных (№ 2164931 (1), № 2168826 (2), № 2163921 (3), № 2168621 (4), deposit@ccdc.cam.ac.uk; http://www.ccdc. cam.ac.uk).
Мезитиленсульфоновая, 1-окси-2, 4-динитро-7-нафталинсульфоновая, 2-карбоксибензолсульфоновая, сульфосалициловая, кислота, аренсульфонат алкилтрифенилфосфония, синтез, строение, рентгеноструктурные исследования
Короткий адрес: https://sciup.org/147240929
IDR: 147240929 | УДК: 546.87+547.29+548.312.5 | DOI: 10.14529/chem230204
Synthesis and crystal structure of alkyltriphenylphosphonium arenesulfonates [Ph3PR][OSO2Ar]
The reaction of equimolar amounts of alkyltriphenylphosphonium bromides with mesitylenesulfonic, 1-hydroxy-2,4-dinitro-7-naphthalenesulfonic, 2-carboxybenzenesulfonic and sulfosalicylic acids in water leads to the formation of ionic alkyltriphenylphosphonium arenesulfonates [Ph3PR][OSO2Ar], R = CH2Ph, Ar = С6H2Me3-2,4,6 (1), R = CH2ОMe, Ar = C10H4(OH-1)(NO2)2-2,4 (2), R = (CH2)4Br, Ar = C6H4(COOH-2) (3), R = CH2ОН, Ar = C6H3(COOH-3)(OH-4) (4). Structures of complexes 1-4 have been established by X-ray diffraction analysis. Crystals 1 [C34H35O4PS, M 570.65; monoclinic syngony, space group P 21/ c ; сell parameters: a = 11.083(12), b = 21.520(16), c = 12.768(10) Å; a = 90.00, β = 92.62(4), g = 90.00 deg.; V = 3042(5) Å3, Z = 4; rcalc = 1.246 g/cm3], 2 [C30H25N2O9PS, M 620.55; triclinic syngony, space group P- 1; сell parameters: a = 8.998(5), b = 12.347(5), c = 13.204(6) Å; a = 82.92(2), β = 81.90(3), g = 83.92(2) deg.; V = 1435.2(12) Å3, Z = 2; rcalc = 1.436 g/cm3], 3 [C29H28O5PSBr, M 599.45; monoclinic syngony, space group P21/n ; сell parameters: a = 12.685(11), b = 16.178(13), c = 13.743(13) Å; a = 90.00, β = 90.39(3), g = 90.00 deg.; V = 2820(4) Å3, Z = 4; rcalc = 1.412 g/cm3], and 4 [C26H27O9PS, M 546.50; monoclinic syngony, space group P 21/ n ; сell parameters: a = 9.201(4), b = 10.113(15), c = 28.77(4) Å; a = 90.00, β = 90.51(6), g = 90.00 deg.; V = 2677(7) Å3, Z = 4; rcalc = 1.356 g/cm3] consist of tetrahedral alkyltriphenylphosphonium cations and arenesulfonate anions with a tetrahedral sulfur atom. The P-C bond lengths vary within the range 1.717(3)-1.931(3) Å. The СРС valence angles take values 101.87(14)-122.99(13) deg. The S-C distances are close to each other and vary in range of values 1.752(5)-1.798(6) Å; the S-O bond lengths are 1.303(2)-1.53(2) Å. Compounds 1 and 4 crystallize as hydrates. Cations and anions in complexes 1-4 are linked by weak hydrogen bonds of the S=O∙∙∙Н(Рh) [2.25-2.67 Å] and S=O∙∙∙Н(C) [2.23-2.63 Å] type. Crystal structures 1, 2, 4 contain the CH∙∙∙π interactions. The spatial structure of crystals 1, 2 is formed with the participation of the π-π interactions. Complete tables of atomic coordinates, bond lengths and bond angles for structures have been deposited at the Cambridge Crystallographic Data Centre (no. 2164931 (1), no. 2168826 (2), no. 2163921 (3), no. 2168621 (4), deposit@ccdc.cam.ac.uk; https://www.ccdc.cam.ac.uk).
Текст научной статьи Синтез и кристаллическая структура аренсульфонатов алкилтрифенилфосфония [Ph3PR][OSO2Ar]
Органические соединения фосфора (ОФС) активно исследуются во всех научных центрах мира, что связано с их химическими достоинствами и широкими возможностями практического применения. Так, фосфорорганические соединения используются в качестве пластификаторов, инсектицидов, фунгицидов, дефолиантов и гербицидов [1]. ОФС ‒ важнейшие промежуточные продукты в синтетической химии, в частности в реакции Виттига [2]. Фосфониевые соли также являются органокатализаторами в асимметрическом межфазном катализе [3], реагентами для транс -металлирования [4] и метатезиса σ -связей [5]. В нефтехимической промышленности ОФС используют как присадки к маслам и бензинам с целью улучшения их качества [6]. Следует отметить огромное значение солей фосфония в создании новых материалов, каталитических систем, ионных жидкостей, проявляющих уникальные свойства [7‒9]. Кроме того, ОФС применяются в качестве антимикробных, антигрибковых соединений, которые обладают высокой биологической активностью и низкой токсичностью [10‒12].
Наиболее распространенным способом синтеза фосфониевых солей является кватернизация соответствующего фосфина в результате реакции с электрофилом или кислотой Бренстеда [13‒16]. Иной способ получения основан на реакции пентафенилфосфора с кислотами [17‒20]. Однако данные методики имеют определенные недостатки: длительность, достаточно жесткие условия и сравнительно невысокие выходы целевого продукта. Таким образом, разработка новых простых методик получения солей фосфония, содержащих разнообразные функциональные группы, является актуальным направлением современной органической химии.
В работах [21 - 23] нами был синтезирован и структурно охарактеризован ряд органосульфонатов тетраорганилфосфония. Кристаллы соединений были получены в результате реакции водных растворов галогенидов тетраорганилфосфония и аренсульфоновых кислот. Достоинствами данного одностадийного способа являются мягкие условия, быстрота и высокие выходы комплексов.
В настоящей работе представлен синтез новых ионных аренсульфонатов алкилтрифенилфосфония [Ph3PR][OSO2Ar], R = CH2Ph, Ar = С6H2Me3-2,4,6 ( 1 ), R = CH2OMe, Ar = C10H4(OH-1)(NO2)2-2,4 ( 2 ), R = (CH2)4Br, Ar = C 6 H4(COOH-2) ( 3 ), R = CH 2 OH, Ar = C 6 H3(COOH-3)(OH-4) ( 4 ), особенности строения которых установлены методом РСА.
Экспериментальная часть
В работе использовали бромиды алкилтрифенилфосфония производства фирмы Alfa Aesar.
Гидрат 2,4,6-триметилбензолсульфоната бензилтрифенилфосфония (1). К раствору бромида бензилтрифенилфосфония (0,108 г, 0,250 ммоль) в 10 мл воды добавляли 10 мл водного раствора мезитиленсульфоновой кислоты (0,050 г, 0,250 ммоль). По мере испарения растворителя выделялись бесцветные кристаллы, которые сушили на воздухе. Выход 0,131 г (95 %), Т пл = 104 ° С. ИК-спектр ( у , см - 1): 3375, 3051, 2999, 2984, 2849, 2772, 1601, 1585, 1483, 1456, 1437, 1408, 1333, 1315, 1250, 1188, 1165, 1111, 1072, 1032, 995, 922, 874, 849, 824, 791, 748, 719, 691, 615, 582, 530, 496, 449. Найдено, %: C 71,49; Н 6,13. C 34 H 35 O 4 PS. Вычислено, %: С 71,56; Н 6,18.
Соединения 2 - 4 синтезировали аналогично.
1-Окси-2,4-динитро-7-нафталинсульфонат (метоксиметил)трифенилфосфония (2). Оранжевые кристаллы. Выход 0,146 г (94 %), Т = 173 ° С. ИК-спектр ( у , см - 1): 3206, 3096, 3044, 3024, 2905, 2837, 1601, 1576, 1541, 1520, 1481, 1437, 1406, 1343, 1323, 1292, 1271, 1234, 1202, 1161, 1126, 1115, 1092, 1076, 1036, 995, 935, 901, 860, 847, 814, 795, 781, 746, 721, 704, 691, 638, 621, 588, 530, 500, 449, 417. Найдено, %: С 58,00; Н 4,12. C 30 H 25 N 2 O 9 PS. Вычислено, %: С 58,07; Н 4,06.
2-Карбоксибензолсульфонат (4-бромбутил)трифенилфосфония (3). Бесцветные кристаллы. Выход 0,139 г (93 %), Т пл = 99 ° С. ИК-спектр ( у , см - 1): 3193, 3059, 3003, 2980, 2934, 2886, 2793, 1705, 1587, 1560, 1485, 1437, 1296, 1279, 1248, 1173, 1159, 1136, 1111, 1076, 1022, 1007, 995, 984, 918, 877, 854, 799, 754, 733, 723, 691, 621, 569, 528, 503, 457, 419. Найдено, %: С 58,06; Н 4,80. C 29 H 28 O 5 PSBr. Вычислено, %: С 58,11; Н 4,71.
Гидрат 3-карбокси-4-гидроксибензолсульфоната (гидроксиметил)трифенилфосфония (4). Бесцветные кристаллы. Выход 0,121 г (96 %), Тпл = 106 ° С. ИК-спектр ( у , см - 1): 3424, 3169, 3073, 2940, 2905, 2866, 1670, 1609, 1587, 1476, 1439, 1319, 1290, 1242, 1171, 1157, 1148, 1115, 1076, 1057, 1030, 997, 959, 934, 916, 885, 870, 833, 799, 743, 721, 689, 665, 598, 581, 532, 501, 478, 440. Найдено, %: C 57,07; Н 5,02. C 26 H 27 O 9 PS. Вычислено, %: С 57,14; Н 4,98.
Элементный анализ выполнен на элементном анализаторе Carlo Erba CHNS-O EA 1108. Температуры плавления измерены на синхронном термоанализаторе Netzsch 449C Jupiter.
ИК-спектры соединений 1-4 записывали на ИК-Фурье спектрометре Shimadzu IR Affinity-1S в таблетке KBr в области 4000 - 400 см - 1.
Рентгеноструктурный анализ (РСА) проводили на автоматическом четырехкружном дифрактометре D8 QUEST фирмы Bruker (Mo Ka-излучение, X = 0,71073 А, графитовый монохроматор) при 293 K. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены с помощью программ SMART и SAINT-Plus. Все расчеты по определению и уточнению структур выполнены с помощью программ SHELXL/PC и OLEX2 [24‒26]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Положение атомов водорода уточняли по модели наездника (Uизо(H) = 1,2Uэкв(C)). Кристаллографические данные и результаты уточнения структур приведены в табл. 1, длины связей и валентные углы – в табл. 2.
Кристаллографические данные, параметры эксперимента и уточнения структур 1 ‒ 4
Длины связей и валентные углы в структурах 1 ‒ 4
Таблица 1
|
Параметр |
1 |
2 |
3 |
4 |
|
Формула |
C 34 H 35 O 4 PS |
C 30 H 25 N 2 O 9 PS |
C 29 H 28 O 5 PSBr |
C 26 H 27 O 9 PS |
|
М |
570,65 |
620,55 |
599,45 |
546,50 |
|
Сингония |
Моноклинная |
Триклинная |
Моноклинная |
Моноклинная |
|
Пр. группа |
P2 1 / c |
P -1 |
P2 1 / n |
P2 1 / n |
|
a , Å |
11,083(12) |
8,998(5) |
12,685(11) |
9,201(4) |
|
b, Å |
21,520(16) |
12,347(5) |
16,178(13) |
10,113(15) |
|
c, Å |
12,768(10) |
13,204(6) |
13,743(13) |
28,77(4) |
|
α , град. |
90,00 |
82,92(2) |
90,00 |
90,00 |
|
β , град. |
92,62(4) |
81,90(3) |
90,39(3) |
90,51(6) |
|
γ , град. |
90,00 |
83,92(2) |
90,00 |
90,00 |
|
V , Å3 |
3042(5) |
1435,2(12) |
2820(4) |
2677(7) |
|
Z |
4 |
2 |
4 |
4 |
|
Двыч.), г/см 3 |
1,246 |
1,436 |
1,412 |
1,356 |
|
ц , мм-1 |
0,195 |
0,228 |
1,625 |
0,232 |
|
F (000) |
1208,0 |
644,0 |
1232,0 |
1144,0 |
|
Размер кристалла, мм |
0,37 × 0,23 × 0,15 |
0,5 × 0,27 × 0,05 |
0,3 × 0,25 × 0,2 |
0,35 × 0,17 × 0,02 |
|
Область сбора данных по 9 , град. |
6,08–64,9 |
5,76‒71,58 |
5,84–56,56 |
5,986–56,948 |
|
Интервалы индексов отражений |
–16 ≤ h ≤ 16, –28 ≤ k ≤ 28, –14 ≤ l ≤ 14 |
–14 ≤ h ≤ 14, –20 ≤ k ≤ 20, –21 ≤ l ≤ 21 |
–16 ≤ h ≤ 16, –21 ≤ k ≤ 21, –18 ≤ l ≤ 18 |
–12 ≤ h ≤ 12, –13 ≤ k ≤ 13, –38 ≤ l ≤ 38 |
|
Измерено отражений |
64557 |
74248 |
90194 |
76873 |
|
Независимых отражений |
7518 |
12433 |
6963 |
6640 |
|
R int |
0,1069 |
0,0598 |
0,0622 |
0,2321 |
|
Переменных уточнения |
367 |
392 |
335 |
372 |
|
GOOF |
1,020 |
1,088 |
1,847 |
1,085 |
|
R -факторы по F 2 > 2 с ( F 2 ) |
R 1 = 0,0687, wR 2 = 0,1745 |
R 1 = 0,1039, wR 2 = 0,1559 |
R 1 = 0,1338, wR 2 = 0,4344 |
R 1 = 0,0973, wR 2 = 0,1767 |
|
R -факторы по всем отражениям |
R 1 = 0,1294, wR 2 = 0,2069 |
R 1 = 0,1686, wR 2 = 0,1782 |
R 1 = 0,1715, wR 2 = 0,4654 |
R 1 = 0,2243, wR 2 = 0,2150 |
|
Остаточная электронная плотность (min/max), e/A3 |
0,38/–0,59 |
0,48/–0,54 |
2,17/–2,79 |
0,42/–0,30 |
Таблица 2
|
Связь d , Å |
Угол ю, ° |
||
|
1 |
|||
|
S(1)–O(1) |
1,303(2) |
O(1)S(1)O(2) |
110,46(18) |
|
S(1)–O(2) |
1,494(3) |
O(1)S(1)O(3) |
107,10(19) |
|
S(1)–O(3) |
1,611(3) |
O(2)S(1)O(3) |
120,81(19) |
|
S(1)–C(41) |
1,788(3) |
O(1)S(1)C(41) |
97,84(16) |
|
P(1)–C(1) |
1,744(3) |
C(1)P(1)C(11) |
102,91(13) |
|
P(1)–C(11) |
1,897(3) |
C(11)P(1)C(21) |
122,99(13) |
|
P(1)–C(21) |
1,931(3) |
C(21)P(1)C(37) |
106,44(14) |
|
P(1)–C(37) |
1,717(3) |
C(1)P(1)C(21) |
105,22(13) |
|
C(47)‒C(42) |
1,605(5) |
C(41)C(42)C(47) |
126,3(3) |
Окончание табл. 2
|
Связь d , Å |
Угол ю, ° |
||
|
2 |
|||
|
S(1)–O(2) |
1,437(2) |
O(2)S(1)O(3) |
113,26(16) |
|
S(1)–O(3) |
1,440(2) |
O(2)S(1)O(4) |
113,45(17) |
|
S(1)–O(4) |
1,444(2) |
O(3)S(1)O(4) |
113,22(15) |
|
S(1)–C(31) |
1,791(2) |
O(2)S(1)C(31) |
105,67(13) |
|
P(1)–C(1) |
1,791(2) |
C(1)P(1)C(7) |
107,15(10) |
|
P(1)–C(7) |
1,818(2) |
C(7)P(1)C(11) |
111,19(11) |
|
P(1)–C(11) |
1,792(2) |
C(11)P(1)C(21) |
110,49(11) |
|
P(1)–C(21) |
1,791(2) |
C(1)P(1)C(21) |
108,54(10) |
|
O(1)–C(7) |
1,408(3) |
C(7)O(1)C(8) |
110,71(19) |
|
O(1)–C(8) |
1,426(3) |
O(1)C(7)P(1) |
107,60(14) |
|
O(5)–C(38) |
1,333(3) |
O(5)C(38)C(39) |
116,4(2) |
|
N(1)–O(6) |
1,240(3) |
O(6)N(1)O(7) |
122,4(2) |
|
N(2)–O(8) |
1,222(4) |
O(8)N(2)O(9) |
121,62(17) |
|
3 |
|||
|
S(1)–O(1) |
1,447(6) |
O(1)S(1)O(2) |
116,4(4) |
|
S(1)–O(2) |
1,439(6) |
O(1)S(1)O(3) |
111,0(4) |
|
S(1)–O(3) |
1,456(5) |
O(2)S(1)O(3) |
111,6(4) |
|
S(1)–C(31) |
1,798(6) |
O(1)S(1)C(31) |
105,6(3) |
|
P(1)–C(1) |
1,785(6) |
C(1)P(1)C(7) |
110,1(3) |
|
P(1)–C(7) |
1,814(7) |
C(7)P(1)C(11) |
108,8(4) |
|
P(1)–C(11) |
1,798(6) |
C(11)P(1)C(21) |
106,2(3) |
|
P(1)–C(21) |
1,814(6) |
C(1)P(1)C(21) |
108,9(3) |
|
O(4)–C(37) |
1,185(8) |
C(7)P(1)C(21) |
112,3(3) |
|
O(5)–C(37) |
1,315(9) |
O(4)C(37)O(5) |
118,4(6) |
|
Br(1)–C(10) |
1,923(15) |
Br(1)C(10)C(9) |
114,0(10) |
|
4 |
|||
|
S(1)–O(1A) |
1,453(5) |
O(1A)S(1)O(2A) |
111,4(4) |
|
S(1)–O(1B) |
1,53(2) |
O(1A)S(1)O(3A) |
111,6(4) |
|
S(1)–O(2A) |
1,451(5) |
O(2A)S(1)O(3A) |
112,4(4) |
|
S(1)–O(2B) |
1,35(2) |
O(1B)S(1)O(2B) |
111,5(14) |
|
S(1)–O(3A) |
1,442(5) |
O(1B)S(1)O(3B) |
108,5(13) |
|
S(1)–O(3B) |
1,43(2) |
O(2B)S(1)O(3B) |
123,1(15) |
|
S(1)–C(31) |
1,752(5) |
O(1A)S(1)C(31) |
106,9(3) |
|
P(1)–C(1) |
1,801(5) |
C(1)P(1)C(7) |
111,0(3) |
|
P(1)–C(7) |
1,822(6) |
C(7)P(1)C(11) |
107,2(3) |
|
P(1)–C(11) |
1,783(5) |
C(11)P(1)C(21) |
111,4(2) |
|
P(1)–C(21) |
1,781(5) |
C(1)P(1)C(11) |
110,3(2) |
|
O(4)–C(37) |
1,297(6) |
C(1)P(1)C(21) |
109,0(2) |
|
O(5)–C(37) |
1,214(6) |
O(4)C(37)O(5) |
122,5(5) |
|
O(6)–C(34) |
1,337(6) |
O(6)C(34)C(35) |
117,8(5) |
|
O(8)–C(7) |
1,398(6) |
O(8)C(7)P(1) |
112,1(4) |
Полные таблицы координат атомов, длин связей и валентных углов для структур депонированы в Кембриджском банке структурных данных (№ 2164931 (1), № 2168826 (2), № 2163921 (3), № 2168621 (4), ; .
Обсуждение результатов
Взаимодействие водных растворов бромидов алкилтрифенилфосфония и соответствующей аренсульфоновой кислоты приводит к образованию целевых комплексов 1 ‒ 4 . Устойчивые на воздухе прозрачные кристаллы аренсульфонатов алкилтрифенилфосфония хорошо растворимы в хлороформе, диэтиловом эфире, этаноле, аренах, ацетонитриле, тетрагидрофуране, четыреххлористом углероде и плохо - в воде при комнатной температуре.
[Ph3PR]Br + HOSO2Ar ⎯⎯⎯-> [Ph3PR][OSO2Ar] R = CH2Ph, Ar = С-6H2rMe3-2,4,6 (1), он
R = CH2ОMe, Ar = и Л Л (2), no2
R = (CH 2 ) 4 Br, Ar = C 6 H 4 (COOH-2) ( 3 ), R = CH 2 ОН, Ar = C 6 H 3 (COOH-3)(OH-4) ( 4 )
В ИК-спектрах комплексов 1 - 4 наблюдаются полосы поглощения средней интенсивности при 3096‒3003 см–1, отвечающие валентным колебаниям связей C Ar –H. Полосы при 1126‒984 и 885‒781 см–1 относятся соответственно к плоскостным и внеплоскостным деформационным колебаниям этих же связей. Также присутствуют характерные полосы валентных колебаний углеродного скелета ароматических фрагментов в области 1609‒1456 см–1. Валентным колебаниям метиленовых групп соответствуют полосы при 2999‒2837 см–1, деформационным колебаниям ‒ при 1485‒1456 см–1.
Полосы поглощения сильной интенсивности при 1439-1437 и 1115-1111 см-1 отвечают асимметричным и симметричным валентным колебаниям сульфонатной группы SO 3 . Интенсивные полосы в области 719‒689 см–1 соответствуют валентным колебаниям связи S‒O. Валентным колебаниям связей CAr–S и CAr–P отвечают полосы сильной интенсивности при 532‒528 и 754‒721 см–1 соответственно [27].
В структурах комплексов 2–4 присутствуют связанные гидроксильные группы, валентным колебаниям которых соответствуют широкие полосы при 3206, 3193 и 3169 см–1. Интенсивные полосы поглощения валентных колебаний карбонильной группы в комплексах 3 , 4 расположены при 1705 и 1670 см–1. Валентным колебаниям связей C‒O в спектрах 3 , 4 отвечают полосы в области 1319‒1279 см–1. Присутствие метоксигруппы в соединении 2 подтверждается наличием полосы при 2837 см–1. В ИК-спектре комплекса 2 также наблюдается широкая полоса при 1202 см–1, соответствующая валентным колебаниям связи C‒O‒C. Широкие полосы в спектрах 2 , 3 , 4 при 691, 934, 916 см–1 отвечают деформационным колебаниям гидроксильных групп.
В спектре соединения 2 асимметричным колебаниям NO2-групп соответствует интенсивная полоса поглощения при 1520 см–1, симметричным колебаниям – при 1343 см–1. Полоса валентных колебаний связи C - Br в спектре комплекса 3 расположена при 569 см–1. Наличие молекул воды в кристаллах гидратов 1 , 4 подтверждается полосами при 3375 и 3424 см–1 [28].
По данным РСА, кристаллы комплексов 1 ‒ 4 образованы катионами алкилтрифенилфосфония и аренсульфонатными анионами (рис. 1 - 3).
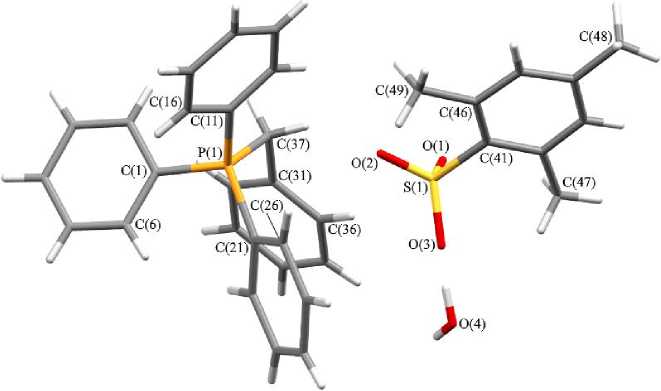
Рис. 1. Общий вид гидрата 2,4,6-триметилбензолсульфоната бензилтрифенилфосфония
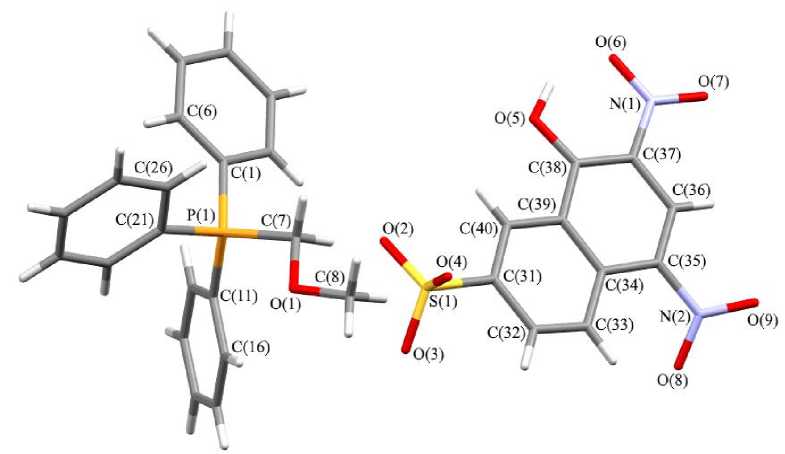
Рис. 2. Общий вид 1-окси-2,4-динитро-7-нафталинсульфоната (метоксиметил)трифенилфосфония
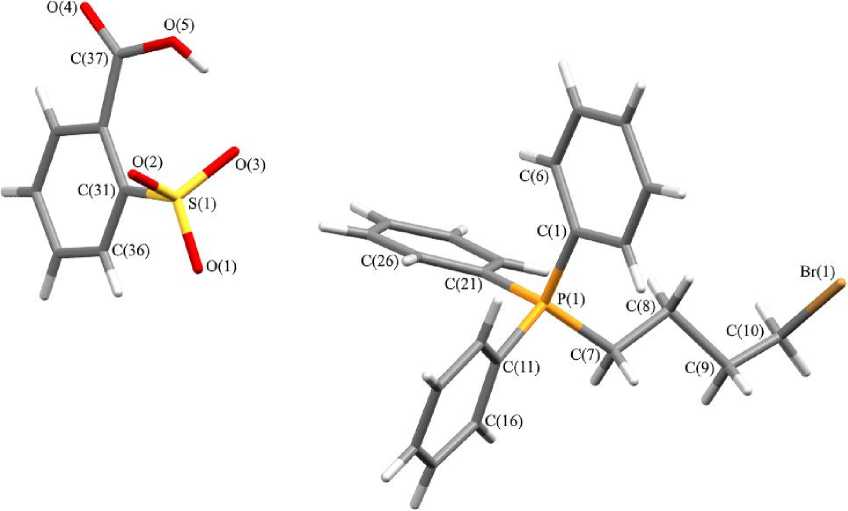
Рис. 3. Общий вид 2-карбоксибензолсульфоната (4-бромбутил)трифенилфосфония
Комплексы 1 и 4 кристаллизуются в виде гидратов состава [Ph 3 PCH 2 Ph][OSO 2 С 6 H 2 Me 3 -2,4,6] ∙ H 2 O и [Ph 3 PCH 2 ОН][OSO 2 C 6 H 3 (COOH-3)(OH-4)] ∙ 2H 2 O.
В соединении 4 атомы кислорода в аренсульфонат-анионе [O(1)‒O(3)] разупорядочены по двум положениям (рис. 4). Уточненное соотношение вкладов положений в разупорядоченный фрагмент составляет 0,82/0,18.
Атомы фосфора в катионах алкилтрифенилфосфония 1 ‒ 4 имеют незначительно искаженную тетраэдрическую координацию. Длины связей P-С варьируют в интервалах 1,717(3)-1,931(3) Å [1,717(3)-1,931(3) Å ( 1 ); 1,791(2)–1,818(2) Å ( 2 ); 1,785(6)–1,814(7) Å ( 3 ); 1,781(5)–1,822(6) Å ( 4 )], что в основном меньше суммы ковалентных радиусов атомов-партнеров (1,83 Å) [29]. Валентные углы СРС принимают значения 101,87(14)-122,99(13)°: 101,87(14)-122,99(13)°; 107,15(10)-111,19(11)°; 106,2(3)-112,3(3)°; 107,2(3)-111,4(2)° в 1 , 2 , 3 , 4 соответственно.
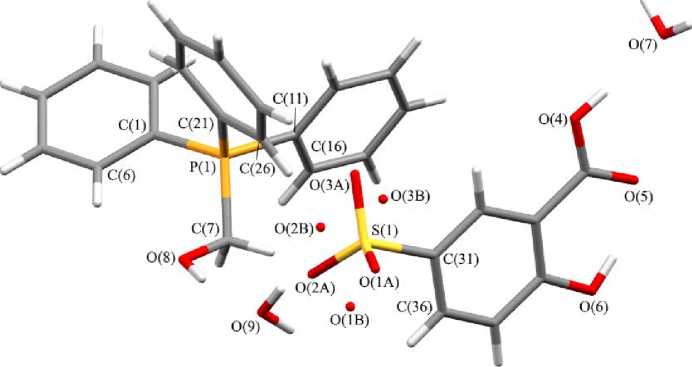
Рис. 4. Общий вид гидрата 3-карбокси-4-гидроксибензолсульфоната (гидроксиметил)трифенилфосфония
[для разупорядоченных атомов показаны два положения: O(A) и O(B)]
Расстояния S-C в аренсульфонатных анионах соединений 1 - 4 близки между собой и изменяются в интервале 1,752(5)-1,798(6) А. Длины связей S-О варьируют в пределах 1,303(2)-1,53(2) А: 1,303(2)-1,611(3) А ( 1 ), 1,437(2)-1,444(2) А ( 2 ), 1,439(6)-1,456(5) А ( 3 ), 1,35(2)-1,53(2) А ( 4 ). Валентные углы oSC в сульфонатных группах (97,84(16)-114,90(15)°) в среднем меньше, чем углы OSO (107,10(19)-123,1(15)°), что полностью согласуется с теорией отталкивания электронных пар валентных оболочек [30].
В сульфонат-анионе комплекса 2 плоскость ^О2-2)-группы незначительно отклоняется от средней плоскости нафталинового цикла (соответствующий двугранный угол 8,46°), нитрогруппа NO 2 -4 развернута относительно плоскости кольца на угол 35,88°. Связи N-O практически выровнены и принимают значения 1,218(3)-1,240(3) А.
В структуре 4 молекулы воды формируют пространственную сетку сульфосалицилат-анионов посредством прочных водородных связей (Н∙∙∙O 1,82‒1,97 Å), кроме того, имеют место водородные связи между карбоксильной и гидроксильной группами в орто -положении (1,89 А) (рис. 5).
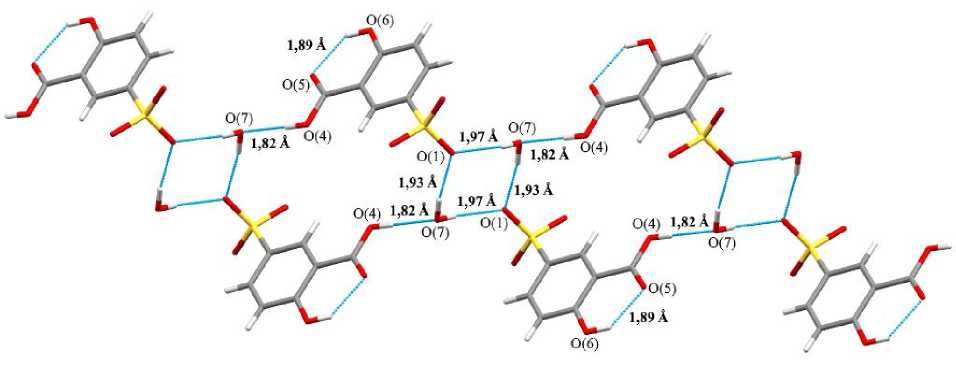
Рис. 5. Пространственная организация аренсульфонатных анионов в кристалле соединения 4
Катионы и анионы в комплексах 1 - 4 связаны слабыми водородными связями типа S=O—H(Ph) [2,56-2,67 А ( 1 ), 2,25-2,56 А ( 2 ), 2,43-2,63А ( 3 ), 2,47-2,67 А ( 4 )]. Также имеют место водородные связи между атомами водорода алкильных групп в катионах и атомами кислорода в аренсульфонатных анионах S=O-R(C) [2,23-2,61 А ( 1 ), 2,31-2,63 А ( 2 ), 2,36-2,39 А ( 3 ), 2,31 А ( 4 )].
В структуре 2 присутствуют короткие контакты типа N - O∙∙∙H(Ph) [2,678–2,710 Å] (сумма ван-дер-ваальсовых атомов-партнеров O···Н 2,62 Å [31]). В кристалле соединения 3 наблюдаются короткие контакты типа Br∙∙∙H(Ph) (2,875 Å), а в кристаллических структурах 1 , 2, 4 ‒ короткие контакты типа С Ar ∙∙∙H(C) (CH∙∙∙π взаимодействия) [2,617; 2,857 Å ( 1 ), 2,827; 2,882 Å ( 2 ), 2,873‒2,893 Å ( 4 )]. Более того, в формировании пространственной структуры кристаллов комплексов 1 , 2 принимают участие π‒π взаимодействия [3,360 Å ( 1 ), 3,374; 3,385 Å ( 2 )]. Так, множественные межмолекулярные контакты типа O···Н, CH∙∙∙π и π‒π взаимодействия структурируют молекулы кристалла 2 в катионный и анионный слои, чередующиеся вдоль кристаллографической оси c (рис. 6).
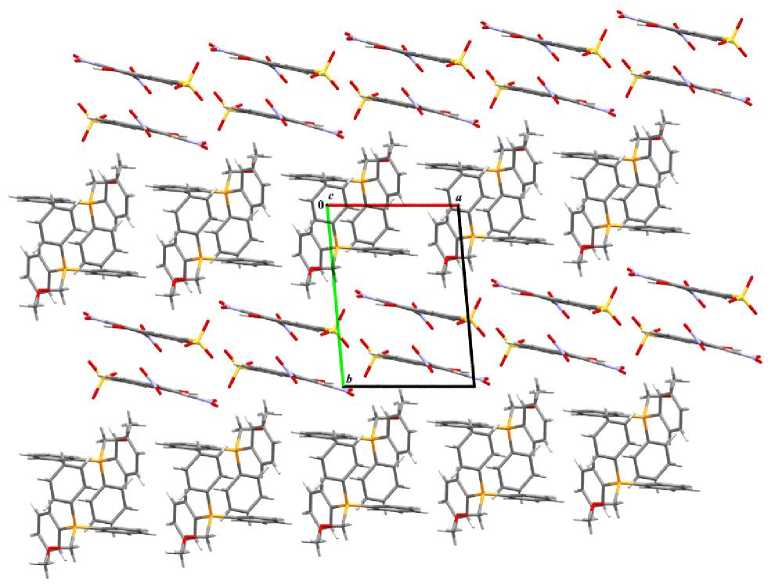
Рис. 6. Упаковка ионов комплекса 2 в кристалле
Выводы
Реакцией замещения доступных бромидов алкилтрифенилфосфония с аренсульфоновыми кислотами в воде синтезированы новые ионные комплексы аренсульфонатов алкилтрифенилфосфония, особенности строения которых установлены методом РСА.
Выражаю признательность профессору В.В. Шарутину за рентгеноструктурный анализ кристаллов соединений 1‒4 и помощь при работе над статьей.
Список литературы Синтез и кристаллическая структура аренсульфонатов алкилтрифенилфосфония [Ph3PR][OSO2Ar]
- Hartley F.R. The Chemistry of Organophosphorus Compounds. Vol. 3. Phosphonium Salts, Ylides and Phosphoranes / F.R. Hartley. John Wiley & Sons, Ltd., 1983. 458 p.
- Hydrophobic encapsulated phosphonium salts-synthesis of weakly coordinating cations and their application in Wittig reactions / R. Moritz, M. Wagner, D. Schollmeyer et al. // Chem. Eur. J. 2015. Vol. 21. P. 9119–9125. DOI: 10.1002/chem.201406370.
- Werner T. Phosphonium salt organocatalysis / T. Werner // Adv. Synth. Catal. 2009. Vol. 351. P. 1469‒1481. DOI: 10.1002/adsc.200900211.
- The Stille reaction, 38 years later / C. Cordovilla, C. Bartolome, J.M. Martinez-Ilarduya et al. // ACS Catal. 2015. Vol. 5. P. 3040‒3053. DOI: 10.1021/acscatal.5b00448.
- Chong C.C. Metal-free 𝜎-bond metathesis in 1,3,2-diazaphospholene-catalyzed hydroboration of carbonyl compounds / C.C. Chong, H. Hirao, R. Kinjo // Angew. Chem. Int. Ed. 2015. Vol. 127. P. 192‒196. DOI: 10.1002/ange.201408760.
- Luiz J.F. Tribofilm formation, friction and wear-reducing properties of some phosphorus-containing antiwear additives / J.F. Luiz, H. Spikes // Tribology Letters. 2020. Vol. 68. P. 75‒99. DOI: 10.1007/s11249-020-01315-8.
- Enantioselective base-free electrophilic amination of benzofuran-2(3H)-ones: catalysis by binol-derived P-spiro quaternary phosphonium salts / Ch.-L. Zhu, F.-G. Zhang, W. Meng et al. // Angew. Chem. Int. Ed. 2011. Vol. 50. P. 5869‒5872. DOI: 10.1002/anie.201100283.
- Ionic liquids of superior thermal stability / C.G. Cassity, A. Mirjafari, N. Mobarrez et al. // Chem. Commun. 2013. Vol. 49, no. 69. P. 7590‒7592. DOI: 10.1039/c3cc44118k.
- Canac Y. A diaminocarbene-phosphonium ylide: direct access to C,C chelating ligands / Y. Canac, C. Duhayon, R. Chauvin // Angew. Chem. Int. Ed. 2007. Vol. 46. P. 6313‒6315. DOI: 10.1002/anie.200701490.
- Synthesis, spectral and solid state characterization of a new bioactive hydrazine bridged cyclic diphosphonium compound / M. Milenkovic, B. Warzajtis, U. Rychlewska et al. // Molecules. 2012. Vol. 17, no. 3. P. 2567‒2578. DOI: 10.3390/molecules17032567.
- Triphenilphosphonium analogs of chloramphenicol as dual-acting antimicrobial and antiprolife-rating agents / J.A. Pavlova, Z.Z. Khairullina, A.G. Tereshchenkov et al. // Antibiotics. 2021. Vol. 10. P. 489‒511. DOI: 10.3390/antibiotics10050489.
- Synthesis and in vitro evaluation of triphenylphosphonium derivatives of acetylsalicylic and salicylic acids: structure-dependent interactions with cancer cells, bacteria, and mitochondria / O.V. Tsepaeva, T.I. Salikhova, L.R. Grigor’eva et al. // Med. Chem. Res. 2021. Vol. 30. P. 925‒939. DOI: 10.1007/s00044-020-02674-6.
- Tuning the hydrophobicity of a mitochondria-targeted NO photodonor / F. Sodano, B. Rolando, F. Spyrakis et al. // ChemMedChem. 2018. Vol. 13. P. 1238‒1245. DOI: 10.1002/cmdc.201800088.
- Rational design 2-hydroxypropylphosphonium salts as cancer cell mitochondria-targeted vec-tors: synthesis, structure, and biological properties / V.F. Mironov, A.V. Nemtarev, O.V. Tsepaeva et al. // Molecules. 2021. Vol. 26. P. 6350‒6384. DOI: 10.3390/molecules26216350.
- New bisphosphonium salt containing a 1,4-dihydroxynaphthalene moiety: molecular and supramolecular structure / N.R. Khasiyatullina, A.T. Gubaidullin, A.M. Shinkareva et al. // Russ. Chem. Bull., Int. Ed. 2020. Vol. 69. P. 2140‒2146. DOI: 10.1007/s11172-020-3012-3.
- Tertiary phosphines in reactions with substituted cinnamic acids / S. Romanov, A. Aksunova, Y. Bakhtiyarova et al. // J. Organomet. Chem. 2020. Vol. 910. P. 121130. DOI: 10.1016/j.jorganchem.2020.121130.
- Карбоксилаты и сульфонаты тетрафенилфосфора. Синтез и строение / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина и др. // Журн. общей химии. 2009. Т. 79. С. 80‒89. DOI: 10.1134/S1070363209010125.
- Синтез и строение карбоксилатов тетрафенилфосфония / В.В. Шарутин, О.К. Шарутина, А.В. Рыбакова и др. // Журн. общей химии. 2018. Т. 88, № 8. С. 1308‒1313. DOI: 10.1134/S0044460X18080139.
- Шарутин В.В., Мукушева Н., Уржумова А.В. Синтез и строение 2,4-динитробензолсульфоната тетрафенилфосфония // Вестник ЮУрГУ. Серия «Химия». 2018. Т. 10, № 2. С. 48‒54. DOI: 10.14529/chem180206.
- Шарутин В.В., Шарутина О.К., Губанова Ю.О. Синтез и строение аренсульфонатов тет-рафенилфосфония // Изв. вузов. Химия и хим. технология. 2019. Т. 62, № 2. С. 4‒10. DOI: 10.6060/ivkkt.20196202.5823.
- Шарутин В.В., Шарутина О.К., Механошина Е.С. Синтез и строение органосульфонатов органилтрифенилфосфония [Ph3PR][OSO2R’], R = Ph, R’ = C6H3Cl2-2,5; R = C6H11-cyclo, R’ = C6H3Cl2-2,5; R = CH2OMe, R’ = C6H3(NO2)2-2,4; R = CH2OMe, R’ = C6H4(COOH-2) // Вестник ЮУрГУ. Серия «Химия». 2022. Т. 14, № 2. С. 41–51. DOI: 10.14529/chem220205.
- Шарутин В.В., Шарутина О.К., Механошина Е.С. Новый способ синтеза аренсульфонатов тетраорганилфосфония [Ph3PR1][OSO2R2] // Журн. общей химии. 2022. Т. 92, № 6. С. 885–893. DOI: 10.31857/S0044460X22060087.
- Шарутин В.В., Шарутина О.К., Механошина Е.С. Исследование кристаллических струк-тур 2,4-динитробензолсульфонатов органилтрифенилфосфония [Ph3PR][OSO2C6H3(NO2)2-2,4], R = CH2OMe, CH2CN, CH2CH=CHCH2PPh3 // Журн. структурной химии. 2022. Т. 63, № 10. С. 99532. DOI: 10.26902/JSC_id99532.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Display-ing Crystal Structures from Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: a complete structure solution, refinement and analysis program / O.V. Dolomanov, L.J. Bourhis, R.J. Gildea et al. // J. Appl. Cryst. 2009. Vol. 42. P. 339–341. DOI: 10.1107/S0021889808042726.
- Тарасевич Б.Н. ИК-спектры основных классов органических соединений / Б.Н. Тарасевич. М.: МГУ, 2012. 54 с.
- Инфракрасная спектроскопия органических и природных соединений: учебное пособие / А.В. Васильев, Е.В. Гриненко, А.О. Щукин и др. СПб.: СПбГЛТА, 2007. 54 с.
- Covalent radii revisited / B. Cordero, V. Gómez, A.E. Platero-Prats et al. // Dalton Trans. 2008. Vol. 21. P. 2832–2838. DOI: 10.1039/B801115J.
- Гиллеспи Р., Харгиттаи И. Модель отталкивания электронных пар валентной оболочки и строение молекул. М.: Мир, 1992. 75 c.
- Consistent Van der Waals radii for the whole main group / M. Mantina, A.C. Chamberlin, R. Valero et al. // J. Phys. Chem. A. 2009. Vol. 113, no. 19. P. 5806–5812. DOI: 10.1021/jp8111556.

![Синтез и кристаллическая структура аренсульфонатов алкилтрифенилфосфония [Ph3PR][OSO2Ar] Синтез и кристаллическая структура аренсульфонатов алкилтрифенилфосфония [Ph3PR][OSO2Ar]](/file/cover/147240929/sintez-i-kristallicheskaja-struktura-arensulfonatov-alkiltrifenilfosfonija-ph3pr.png)
