Синтез и строение 2-гидрокси-4-тетрафенилстибоксибензоата тетрафенилсурьмы
Автор: Шарутин Владимир Викторович, Шарутина Ольга Константиновна, Губанова Юлия Олеговна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 4 т.9, 2017 года.
Бесплатный доступ
Взаимодействием пентафенилсурьмы с 2,4-диоксибензойной кислотой в толуоле синтезирован 2-гидрокси-4-тетрафенилстибоксибензоат тетрафенилсурьмы. По данным РСА, атомы сурьмы имеют искаженную тригонально-бипирамидальную координацию. Аксиальные углы CSb(1,2)O равны 169,28(16)° и 166,45(15)°, экваториальные углы CSb(1,2)C варьируют в интервалах 116,6(3)°-120,1(3)° и 117,6(3)°-120,5(3)°. Длины связей Sb(1,2)-O и Sb(1,2)-Cакс составляют 2,245(3), 2,254(3) Å и 2,150(7), 2,193(5) Å соответственно.
Пентафенилсурьма, 4-диоксибензойная кислота, 2-гидрокси-4-тетрафенилстибоксибензоат тетрафенилсурьмы, строение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147160410
IDR: 147160410 | УДК: 546.865+547.47+548.312.5 | DOI: 10.14529/chem170409
Synthesis and structure of tetraphenylantimony 2-hydroxy-4-tetraphenylstiboxybenzoate
By interaction between pentaphenylantimony and 2,4-dyhydroxybenzoic acid in toluene tetraphenylantimony 2-hydroxy-4-tetraphenylstiboxybenzoate was obtained. According to X-ray analysis the atoms of antimony have a distorted trigonal bypiramidal coordination. The axial angles CSb(1,2)O equal 169.28(16)° and 166.45(15)°, equatorial angles CSb(1,2)C range within 116.6(3)°-120.1(3)° and 117.6(3)°-120.5(3)°. The bond lengths Sb(1,2)-O and Sb(1,2)-Cax equal 2.245(3), 2.254(3) Å and 2.150(7), 2.193(5) Å, respectively.
Текст научной статьи Синтез и строение 2-гидрокси-4-тетрафенилстибоксибензоата тетрафенилсурьмы
Особенности взаимодействия пентафенилсурьмы с органическими соединениями, содержащими несколько подвижных атомов водорода, представляют определенный интерес, поскольку могут приводить к продуктам различного строения. Так, было установлено, что в реакциях пентафенилсурьмы с салициловой кислотой (1:1 или 2:1 мольн.) происходит замещение атома водорода только в карбоксильной группе и образуется салицилат тетрафенилсурьмы [1]. Не удалось заместить атом водорода гидроксильной группы в 5-бромсалициловой кислоте при взаимодействии с бромидом тетрафенилсурьмы в присутствии этилата натрия [2]. Однако реакция с 4-гидроксибензойной кислотой в аналогичных условиях привела к образованию биядерного сурьмаорганического продукта [3]. Другие сурьмаорганические производные гидроксикислот в литературе не описаны.
В настоящей работе изучено взаимодействие пентафенилсурьмы с 2,4-диоксибензойной кислотой и установлено строение продукта реакции.
Экспериментальная часть
Синтез 2-гидрокси-4-тетрафенилстибоксибензоата тетрафенилсурьмы (1). Смесь 300 мг (0,6 ммоль) пентафенилсурьмы и 45 мг (0,3 ммоль) 2,4-диоксибензойной кислоты в 5 мл толуола помещали в стеклянную ампулу и запаивали, смесь выдерживали при комнатной температуре в течение 24 часов. Раствор концентрировали, твердый продукт перекристаллизовывали из диме-тилформамида. Получили 555 мг (93 %) бесцветных кристаллов с т. пл. 231 °С (с разл). ИК-спектр ( ν , см-1): 3062, 1670, 1618, 1562, 1477, 1435, 1418, 1381, 1344, 1307, 1291,1257, 1225, 1170, 1151 1088 1065 1020, 995, 966, 877, 852, 783, 756, 732, 694, 636, 443.
ИК-спектр соединения 1 записывали на ИК-Фурье спектрометре Shimadzu IRAffinity-1S в таблетке KBr в области 4000–400 см–1.
Рентгеноструктурный анализ ( РСА ) кристалла 1 проведен на автоматическом четырехкружном дифрактометре D8 QUEST фирмы Bruker (Mo K α -излучение, λ = 0,71073 Å, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены с помощью программ SMART и SAINT-Plus [4]. Все расчеты по определению и уточнению структуры выполнены с помощью программ SHELXL/PC [5] и OLEX [6]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Положение атомов водорода уточняли по модели наездника ( U изо (H) = 1,2 U экв (C)). Кристаллографические данные и результаты уточнения структур приведены в табл. 1, геометрические характеристики координационного полиэдра атома сурьмы – в табл. 2.
Taблица 1
Кристаллографические данные, параметры эксперимента и уточнения структур соединения 1
|
Параметр |
C 55 H 44 O 4 Sb 2 |
|
M |
1012,40 |
|
Сингония |
триклинная |
|
T, K |
273,15 |
|
Пр. группа |
P 1 |
|
a , Å |
9,5138(4) |
|
b , Å |
10,4541(3) |
|
c , Å |
12,5441(5) |
|
α, ° |
80,8950(10) |
|
β, ° |
69,486(2) |
|
γ, ° |
72,4460(10) |
|
V , Å3 |
1112,15(7) |
|
Z |
1 |
|
ρ (выч.), г/см3 |
1,512 |
|
- 1 μ, mm |
1,262 |
|
F (000) |
508 |
|
Размер кристалла, мм |
0,48 × 0,43 × 0,21 |
|
Область сбора данных по 2θ, град |
4,1 - 71,62 |
|
Интервалы индексов отражений |
–15 ≤ h ≤ 15; –17 ≤ k ≤ 17; –20 ≤ l ≤ 20 |
|
Измерено отражений |
111219 |
|
Независимых отражений |
20583 |
|
R int |
0,0297 |
|
Число уточняемых параметров |
551 |
|
GOOF |
1,051 |
|
R -факторы по F 2> 2 σ ( F 2) |
R 1 = 0,0414; wR 2 = 0,0971 |
|
R -факторы по всем отражениям |
R 1 = 0,0629; wR 2 = 0,1108 |
|
Остаточная электронная плотность (min/max), е /Å3 |
–1,30 / 1,66 |
Таблица 2
Основные длины связей ( d ) и валентные углы ( ω ) в структуре соединения 1
|
Связь |
d , Å |
Угол |
ω, град. |
Угол |
ω, град. |
|
Sb(1) – C(1) |
2,091(7) |
C(31)Sb(1)O(1) |
169,28(16) |
C(81)Sb(2)O(2) |
166,45 (15) |
|
Sb(1) – C(11) |
2,101(7) |
C(1)Sb(1)C(11) |
116,6(3) |
C(71)Sb(2)C(61) |
118,5(3) |
|
Sb(1) – C(21) |
2,120(7) |
C(1)Sb(1)C(21) |
120,1(3) |
C(71)Sb(2)C(51) |
120,5(3) |
|
Sb(1) – C(31) |
2,150(7) |
C(11)Sb(1)C(21) |
119,9(3) |
C(61)Sb(2)C(51) |
117,6(3) |
|
Sb(1) – O(1) |
2,245(3) |
C(31)Sb(1)C(1) |
97,5(3) |
C(51)Sb(2)C(81) |
98,4(2) |
|
Sb(2) – C(51) |
2,135(6) |
C(31)Sb(1)C(11) |
98,5(3) |
C(61)Sb(2)C(81) |
91,5(2) |
|
Sb(2) – C(61) |
2,139(8) |
C(31)Sb(1)C(21) |
92,5(2) |
C(71)Sb(2)C(81) |
98,4(2) |
|
Sb(2) – C(71) |
2,108(7) |
C(1)Sb(1)O(1) |
84,4(2) |
C(51)Sb(2)O(2) |
80,9(2) |
|
Sb(2) – C(81) |
2,193(5) |
C(11)Sb(1)O(1) |
90,0(3) |
C(61)Sb(2)O(2) |
77,1(2) |
|
Sb(2) – O(2) |
2,254(3) |
C(21)Sb(1)O(1) |
77,5(2) |
C(71)Sb(2)O(2) |
93,5(2) |
|
О(1) – C(41) |
1,339(5) |
Sb(1)O(1)С(41) |
122,3(3) |
Sb(2)O(2)С(47) |
118,4(3) |
|
О(2) – C(47) |
1,272(5) |
О(2)С(47)О(3) |
121,3(4) |
||
|
О(3) – C(47) |
1,254(6) |
Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1566931, .
Обсуждение результатов
Выявлено, что в результате реакции пентафенилсурьмы с 2,4-диоксибензойной кислотой в толуоле, проходящей при комнатной температуре в течение суток, происходит замещение двух подвижных атомов водорода в кислоте и образуется биядерное соединение 1 с высоким выходом:
Химия элементоорганических соединений
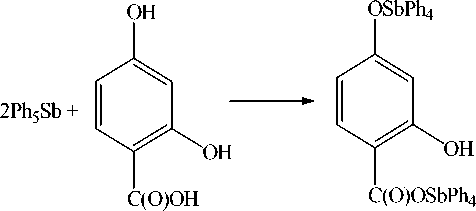
+ 2PhH.
Следует отметить, что строение продукта не зависело от мольного соотношения реагентов, и даже при избытке пентафенилсурьмы (3:1 мольн.) не происходило замещения атома водорода на фрагмент Ph4Sb в гидроксильной группе, находящейся в орто- положении. Вероятно, это обусловлено наличием внутримолекулярной водородной связи между гидроксильной группой и карбонильным атомом кислорода, а так же стерическими затруднениями.
По данным РСА, атомы сурьмы Sb(1) и Sb(2) имеют искаженную тригонально-бипирамидальную координацию (см. рисунок). В эваториальных положениях находятся три фенильных лиганда, в аксиальных - четвертый фенильный и мостиковый карбоксилатный лиганд, координированный через гидроксильный (на Sb(1)) или карбоксильный (на Sb(2)) атомы кислорода. Атомы Sb(1) и Sb(2) выходят из соответствующих экваториальных плоскостей в сторону аксиально расположенных фенильных лигандов на 0,224 и 0,227 Å. Аксиальные углы O(1,2)Sb(1,2)C акс равны 169,28(16)° и 166,45(15)°. Суммы углов в экваториальных плоскостях Sb(1) и Sb(2) составляют 356,3(3)° (116,6(3)° - 120,1(3)° и 356,6(3)° (117,6(3)° - 120,5(3)°). Углы C акс Sb(1,2)C экв изменяются в интервалах 92,5(2)° – 98,5(3)° и 91,5(2)° – 98,4(2) ° соответственно. Аксиальная связь Sb(1)–C акс , равная 2,150(7) Å, намного короче соответствующей связи Sb(2)–C акс , составляющей 2,193(5) Å. Значение длин экваториальных связей Sb(1,2)–C экв также существенно различаются и составляют 2,091(7) – 2,120(7) Å и 2,108(8) – 2,139(8) Å.
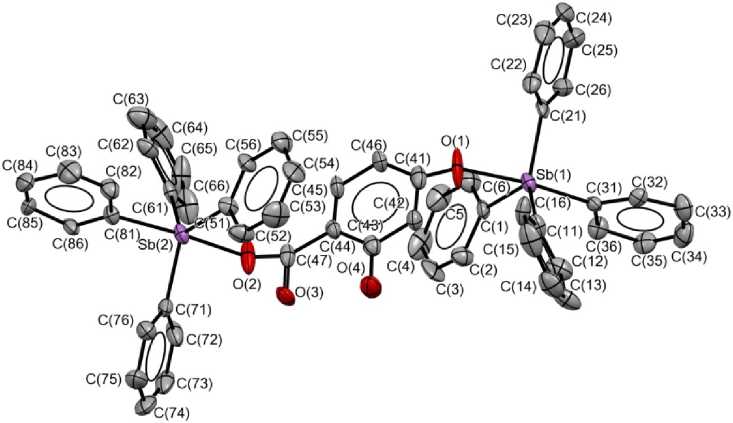
Строение соединения 1 (атомы водорода не показаны)
Длины связей Sb(1,2)–O(1,2) несмотря на различную природу функциональных групп, в которые входят атомы кислорода, имеют близкие значения (2,245(3) и 2,254(3) Å). Отметим, что в молекуле салицилата тетрафенилсурьмы расстояние Sb–O составляет 2,329(2) Å [1], а в 3-гидроксифенокиде тетрафенилсурьмы значительно меньше - 2,205(1) Å [7]. В молекуле (μ2-4-оксибензоато-O,O’,O’’)-бис(тетрафенилсурьме) расстояние между атомом сурьмы и атомом кислорода гидроксильной группы равно 2,185(4) Å [3]. Молекула этого соединения отличается также от соединения 1 координацией карбоксилатного лиганда на атом сурьмы, который прояв- ляет выраженные бидентатные свойства. Длина связи Sb–O составляет 2,277(4) Å, а расстояние между атомом сурьмы и атомом кислорода карбонильной группы Sb∙∙∙O=C – 2,574() Å. Отношение расстояний Sb∙∙∙O к Sb–O, которое характеризует асимметрию координации лиганда, равно 1,13, т. е. близко к 1, что приводит к переходу тригонально-бипирамидальной координации атома сурьмы в октаэдрическую. В 1 внутримолекулярный контакт атома сурьмы с карбонильной группой проявляется слабо (соответствующее расстояние 3,373(4) Å), асимметрия координации лиганда характеризуется значением 1,50.
В молекуле 1 наблюдается выравнивание ординарной С(47) - О(2) и двойной С(47) - О(3) связей в карбоксильной группе (1,273(5) и 1,254(6) Å соответственно), что можно объяснить наличием внутримолекулярной водородной связи О(3)∙∙∙Н - О(4) с параметрами: O(4)–H 0,82 Å, H∙∙∙O(3) 1,81 Å O(4)∙∙∙O(3) 2,522(5) Å, угол O(4)HO(3) cоставляет 144°. Наличие этой связи, возможно, является причиной удлинения расстояния С(47) - О(3) и большой асимметрией координации карбоксилатного лиганда. Для сравнения: в молекуле салицилата тетрафенилсурьмы аналогичные параметры внутримолекулярной водородной связи составляют 0,77 Å; 1,82 Å; 2,546 Å и 157°, при этом связи в карбоксильной группе также выровнены, и асимметрия координации лиганда 1,36 [1].
Вывод
Таким образом, 2,4-диоксибензойная кислота при взаимодействии с пентафенилсурьмой проявляет себя как бифункциональное соединение, поскольку гидроксильная группа в орто положении участия в реакции не принимает. По данным РСА, в молекуле 2-гидрокси-4-тетрафенилстибоксибензоата тетрафенилсурьмы лиганд выполняет мостиковую функцию. Особенностью строения молекулы являются близкие значения геометрических параметров координационных узлов атомов сурьмы, связанных с лигандом через разные функциональные группы.
Список литературы Синтез и строение 2-гидрокси-4-тетрафенилстибоксибензоата тетрафенилсурьмы
- Реакции пентаарилсурьмы с диацилатами триарилсурьмы/В.В. Шарутин, О.К. Шарутина, А.П. Пакусина и др.//Журн. общ. химии. -1997. -Т. 67, вып. 9. -С. 1536-1541.
- Synthesis, Characterization and Crystal Structures of Tri-and Tetraphenylantimony(V) Compounds Containing Arylcarbonyloxy Moiety/L. Quan, H. Yin, J. Cui et al.//J. Organometal. Chem. -2009. -V. 694, № 23. -P. 3708-3717.
- Synthesis and Crystal Structure of Dinuclear Tetraphenylantimony Carboxylate Derivatives Based on Different Coordination Modes/L. Quan, H. Yin, J. Cui et al.//J. Organometal. Chem. -2009. -V. 694, № 23. -P. 3683-3687.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures From Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: Complete Structure Solution, Refinement and Analysis Program/O.V. Dolomanov, L.J. Bourhis, R.J. Gildea et al.//J. Appl. Cryst. -2009. -V. 42. -P. 339-341.
- Синтез и строение Sb-содержащих производных биядерных фенолов/В.В. Шарутин, А.П. Пакусина, О.К. Шарутина и др.//Коорд. химия. -2002. -Т. 28, № 11. -С. 812-817.


