Синтез и строение аренсульфонатов алкилтрифенилфосфония
Автор: Шарутин Владимир Викторович, Шарутина Ольга Константиновна, Механошина Евгения Сергеевна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 4 т.14, 2022 года.
Бесплатный доступ
Взаимодействием эквимолярных количеств галогенида алкилтрифенилфосфония с мезитиленсульфоновой, 2,5-дихлорбензолсульфоновой и сульфосалициловой кислотами в воде синтезированы аренсульфонаты алкилтрифенилфосфония [Ph3PR][OSO2Ar], R = CH2OMe, Ar = C6H2Me3-2,4,6 (1); R = CH2C(O)Me, Ar = C6H2Me3-2,4,6 (2); R = (CH2)2Br, Ar = C6H3Cl2-2,5 (3); R = (CH2)4COOH, Ar = C6H3(COOH-3)(OH-4) (4), особенности строения которых установлены методом РСА. Кристаллы 1 [С29H31O4PS, M 506,57; сингония моноклинная, группа симметрии P21/c; параметры ячейки: a = 13,228(9), b = 14,530(12), c = 14,192(10) Å; a = 90,00, β = 101,46(3), g = 90,00 град., V = 2673(3) Å3, Z = 4; rвыч = 1,259 г/см3], 2 [С30H31O4PS, M 518,58; сингония моноклинная, группа симметрии P21/c; параметры ячейки: a = 12,569(8), b = 15,888(12), c = 13,819(10) Å; a = 90,00, β = 100,16(2), g = 90,00 град., V = 2716(3) Å3, Z = 4; rвыч = 1,268 г/см3], 3 [С26H22BrCl2O3PS, M 596,28; сингония моноклинная, группа симметрии Cc; параметры ячейки: a = 21,731(15), b = 8,974(6), c = 14,794(9) Å; a = 90,00, β = 117,928(19), g = 90,00 град., V = 2549(3) Å3, Z = 4; rвыч = 1,554 г/см3], 4 [С60H59O16.5P2S2, M 1170,12; сингония триклинная, группа симметрии P-1; параметры ячейки: a = 10,678(7), b = 11,025(5), c = 13,250(7) Å; a = 104,117(19), β = 104,13(2), g = 91,23(3) град., V = 1461,5(14) Å3, Z = 2; rвыч = 1,330 г/см3] состоят из катионов алкилтрифенилфосфония и аренсульфонатных анионов. Атомы фосфора в катионах 1-4 имеют тетраэдрическую координацию [углы CРС варьируют в интервале 104,50(8)°-115,41(9)°]. Длины связей P-C составляют 1,7890(16)-1,823(3) Å, что несколько меньше суммы их ковалентных радиусов (1,88 Å). Расстояния S-O в аренсульфонатных анионах незначительно отличаются и равны 1,441(3)-1,454(2) Å; длины связей S-C составляют 1,7706(15)-1,807(3) Å. Структурная организация кристаллов 1-4 формируется за счет множества слабых водородных связей между катионами и анионами. Аренсульфонатные анионы в комплексе 4 посредством прочных водородных связей структурированы в димеры. Полные таблицы координат атомов, длин связей и валентных углов для структур депонированы в Кембриджском банке структурных данных (№ 2161982 (1), 2162500 (2), 2162502 (3), 2167983 (4), deposit@ccdc.cam.ac.uk; http://www.ccdc. cam.ac.uk).
Аренсульфонат алкилтрифенилфосфония, синтез, строение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147239552
IDR: 147239552 | УДК: 546.865+547.53.024+548.312.5 | DOI: 10.14529/chem220404
Synthesis and structure of alkyltriphenylphosphonium arenesulfonates
The interaction of equimolar amounts of alkyltriphenylphosphonium halide with mesitylene sulfonic, 2,5-dichlorobenzene sulfonic, and sulfosalicylic acids in water leads to the formation of alkyltriphenylphosphonium arenesulfonates [Ph3PR][OSO2Ar], R = CH2OMe, Ar = C6H2Me3-2,4,6 (1); R = CH2C(O)Me, Ar = C6H2Me3-2,4,6 (2); R = (CH2)2Br, Ar = C6H3Cl2-2,5 (3); R = (CH2)4COOH, Ar = C6H3(COOH-3)(OH-4) (4). Structures of complexes 1-4 have been established by X-ray diffraction analysis. Crystals 1 [С29H31O4PS, M 506.57; monoclinic syngony, space group P21/c; cell parameters: a = 13.228(9), b = 14.530(12), c = 14.192(10) Å; a = 90.00, β = 101.46(3), g = 90.00 deg.; V = 2673(3) Å3, Z = 4; rcalc = 1.259 g/cm3], 2 [С30H31O4PS, M 518.58; monoclinic syngony, space group P21/c; сell parameters: a = 12.569(8), b = 15.888(12), c = 13.819(10) Å; a = 90.00, β = 100.16(2), g = 90.00 deg.; V = 2716(3) Å3, Z = 4; rcalc = 1.268 g/cm3], 3 [С26H22BrCl2O3PS, M 596.28; monoclinic syngony, space group Cc; cell parameters: a = 21.731(15), b = 8.974(6), c = 14.794(9) Å; a = 90.00, β = 117.928(19), g = 90.00 deg.; V = 2549(3) Å3, Z = 4; rcalc = 1.554 g/cm3], 4 [С60H59O16.5P2S2, M 1170.12; triclinic syngony, space group P-1; cell parameters: a = 10.678(7), b = 11.025(5), c = 13.250(7) Å; a = 104.117(19), β = 104.13(2), g = 91.23(3) deg.; V = 1461.5(14) Å3, Z = 2; rcalc = 1.330 g/cm3] consist of alkyltriphenylphosphonium cations and arenesulfonate anions. Phosphorus atoms in cations 1-4 have a tetrahedral coordination [the CРС angles vary in the range 104.50(8)-115.41(9) deg.]. The P-C bond lengths are 1.7890(16)-1.823(3) Å, which is slightly less than the sum of their covalent radii (1.88 Å). The S-O distances in arenesulfonate anions differ insignificantly and take values of 1.441(3)-1.454(2) Å; the S-C bond lengths are 1.7706(15)-1.807(3) Å. The structural organization of crystals 1-4 is due to weak hydrogen bonds between cations and anions. Arenesulfonate anions in complex 4 are structured into dimers via strong hydrogen bonds. Complete tables of atomic coordinates, bond lengths and bond angles for structures have been deposited at the Cambridge Crystallographic Data Centre (No. 2161982 (1), No. 2162500 (2), No. 2162502 (3), No. 2167983 (4), deposit@ccdc.cam.ac.uk; http://www.ccdc. cam.ac.uk).
Текст научной статьи Синтез и строение аренсульфонатов алкилтрифенилфосфония
Известно, что органические соединения фосфора (ОСФ) применяются в самых разнообразных областях практической деятельности: в качестве инсектицидов, фунгицидов, дефолиантов, гербицидов, пластификаторов, ионитов, присадок к бензинам и смазочным маслам [1]. ОСФ нашли применение и в синтетической органической химии, например, при получении олефинов по Виттигу [2] или синтезе элементоорганических соединений [3]. Сообщалось также о перспективах практического применения некоторых фосфорорганических соединений в качестве катализаторов гидрофункционализации непредельных субстратов [4], реагентов для транс металлирования [5] и метатезиса σ-связей [6]. Из всех производных пятивалентного фосфора наиболее изучены соли тетрафенилфосфония, которые обычно получают по реакции пентафе-нилфосфора с кислотами [7 - 10]. Синтез структурно охарактеризованных органосульфонатов тетрафенилфосфония описан в работах [11 - 17], однако в литературе неизвестны примеры получения аренсульфонатов органилтрифенилфосфония.
Экспериментальная часть
В работе использовали галогениды алкилтрифенилфосфония производства фирмы Alfa Aesar.
2,4,6-Триметилбензолсульфонат (метоксиметил)трифенилфосфония (1). Раствор хлорида (метоксиметил)трифенилфосфония (0,103 г, 0,300 ммоль) в 8 мл воды смешивали с 8 мл водного раствора 2,4,6-триметилбензолсульфоновой кислоты (0,060 г, 0,300 ммоль). При медленном испарении растворителя выделялись бесцветные кристаллы, которые сушили на воздухе. Выход 0,147 г (97 %), т. пл. 101 ° С. ИК-спектр ( v , см - 1): 3078, 3053, 2972, 2934, 2914, 1585, 1481, 1435, 1246, 1217, 1206, 1179, 1159, 1109, 1084, 1043, 1016, 995, 853, 758, 725, 691, 675, 579, 535, 427. Найдено, %: С 68,68; H 6,19. С 29 H 31 O 4 PS. Вычислено, %: С 68,70; H 6,12.
2,4,6-Триметилбензолсульфонат (ацетонил)трифенилфосфония (2). Раствор бромида (ацетонил)трифенилфосфония (0,120 г, 0,300 ммоль) в 8 мл воды смешивали с 8 мл водного раствора 2,4,6-триметилбензолсульфоновой кислоты (0,060 г, 0,300 ммоль). При медленном испарении растворителя выделялись бесцветные кристаллы, которые сушили на воздухе. Выход 0,148 г (95 %), т. пл. 127 ° С. ИК-спектр ( v , см - 1): 3088, 3073, 3051, 2988, 2968, 2895, 1983, 1929, 1603, 1587, 1564, 1485, 1470, 1437, 1377, 1362, 1319, 1308, 1243, 1217, 1198, 1169, 1109, 1082, 1039, 1011, 995, 982, 856, 800, 748, 721, 692, 675, 581, 548, 509, 496, 451, 411. Найдено, %: С 69,39; H 6,01. С 30 H 31 O 4 PS. Вычислено, %: С 69,42; H 5,98.
2,5-Дихлорбензолсульфонат (2-бромэтил)трифенилфосфония (3). Раствор бромида (2-бромэтил)трифенилфосфония (0,135 г, 0,300 ммоль) в 8 мл воды смешивали с 8 мл водного раствора 2,5-дихлорбензолсульфоновой кислоты (0,068 г, 0,300 ммоль). При медленном испарении растворителя выделялись бесцветные кристаллы, которые сушили на воздухе. Выход 0,170 г (95 %), т. пл. 92 ° С. ИК-спектр ( v , см - 1): 3080, 3049, 2994, 2934, 2897, 1612, 1585, 1557, 1485, 1437, 1406, 1373, 1339, 1319, 1231, 1217, 1169, 1148, 1107, 1096, 1051, 1015, 995, 899, 835, 810, 741, 733, 714, 692, 619, 567, 535, 523, 482, 469, 457, 428. Найдено, %: С 52,28; H 3,71. С 26 H 22 BrCl 2 O 3 PS. Вычислено, %: С 52,33; H 3,69.
Гидрат 3-карбокси-4-гидроксибензолсульфоната (4-карбоксибутил)трифенилфосфония (4). Раствор бромида (4-карбоксибутил)трифенилфосфония (0,133 г, 0,300 ммоль) в 8 мл воды смешивали с 8 мл водного раствора 3-карбокси-4-гидроксибензолсульфоновой кислоты (0,066 г, 0,300 ммоль). При медленном испарении растворителя выделялись бесцветные кристаллы, которые сушили на воздухе. Выход 0,157 г (90 %), т. пл. 165 ° С. ИК-спектр ( v , см - 1): 3084, 3063, 2995, 2887, 1989, 1938, 1670, 1612, 1587, 1474, 1439, 1400, 1344, 1317, 1281, 1238, 1217, 1171, 1150, 1108, 1086, 1040, 1013, 835, 800, 779, 745, 714, 691, 660, 565, 550, 496, 467, 444. Найдено, %: С 61,50; H 5,11. С 60 H 59 O 16.5 P 2 S 2 . Вычислено, %: С 61,53; H 5,04.
Элементный анализ выполнен на элементном анализаторе Carlo Erba CHNS-O EA 1108. Температуры плавления измерены на синхронном термоанализаторе Netzsch 449C Jupiter.
ИК-спектры соединений 1-4 записывали на ИК-Фурье спектрометре Shimadzu IR Affinity-1S в таблетке KBr в области 4000 - 400 см - 1.
Рентгеноструктурный анализ ( РСА ) проведен на автоматическом четырехкружном дифрактометре D8 QUEST фирмы Bruker (Mo K „ -излучение, X = 0,71073 А, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [18]. Все расчеты по определению и уточнению структур выполнены по программам SHELXL/PC [19] и OLEX-2 [20]. Структуры соединений определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Кристаллографические данные и результаты уточнения структур приведены в табл. 1, длины связей и валентные углы – в табл. 2.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структур 1 ‒ 4
|
Параметр |
1 |
2 |
3 |
4 |
|
Формула |
С 29 H 31 O 4 PS |
С 30 H 31 O 4 PS |
С 26 H 22 BrCl 2 O 3 PS |
С 60 H 59 O 16.5 P 2 S 2 |
|
М |
506,57 |
518,58 |
596,28 |
1170,12 |
|
Сингония |
Моноклинная |
Моноклинная |
Моноклинная |
Триклинная |
|
Пр. группа |
P 2 1 /c |
P 2 1 /c |
Cc |
P– 1 |
|
a , Å |
13,228(9) |
12,569(8) |
21,731(15) |
10,678(7) |
|
b, Å |
14,530(12) |
15,888(12) |
8,974(6) |
11,025(5) |
|
c, Å |
14,192(10) |
13,819(10) |
14,794(9) |
13,250(7) |
|
α, град. |
90,00 |
90,00 |
90,00 |
104,117(19) |
Окончание табл. 1
|
Параметр |
1 |
2 |
3 |
4 |
|
β, град. |
101,46(3) |
100,16(2) |
117,928(19) |
104,13(2) |
|
γ, град. |
90,00 |
90,00 |
90,00 |
91,23(3) |
|
V , Å3 |
2673(3) |
2716(3) |
2549(3) |
1461,5(14) |
|
Z |
4 |
4 |
4 |
2 |
|
ρ (выч.), г/см3 |
1,259 |
1,268 |
1,554 |
1,330 |
|
µ , мм–1 |
0,213 |
0,212 |
1,994 |
0,215 |
|
F (000) |
1072,0 |
1096,0 |
1208,0 |
613,0 |
|
Размер кристалла, мм |
0,34×0,32×0,08 |
0,5×0,26×0,19 |
0,45×0,32×0,1 |
0,5×0,5×0,3 |
|
Область сбора данных по θ , град. |
5,48–56,64 |
5,94‒65,3 |
6,4–60,24 |
5,746–57 |
|
Интервалы индексов отражений |
–17 ≤ h ≤ 17, –19 ≤ k ≤ 19, –18 ≤ l ≤ 18 |
–19 ≤ h ≤ 19, –24 ≤ k ≤ 24, –20 ≤ l ≤ 20 |
–30 ≤ h ≤ 28, –12 ≤ k ≤ 11, –20 ≤ l ≤ 20 |
–14 ≤ h ≤ 14, –14 ≤ k ≤ 14, –17 ≤ l ≤ 17 |
|
Измерено отражений |
109903 |
82287 |
17067 |
64488 |
|
Независимых отражений |
6632 |
9896 |
6290 |
7406 |
|
R int |
0,0585 |
0,0634 |
0,0330 |
0,0285 |
|
Переменных уточнения |
320 |
329 |
307 |
406 |
|
GOOF |
1,054 |
1,008 |
1,026 |
1,044 |
|
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0432, wR 2 = 0,1115 |
R 1 = 0,0571, wR 2 = 0,1268 |
R 1 = 0,0340, wR 2 = 0,0715 |
R 1 = 0,0373, wR 2 = 0,0992 |
|
R -факторы по всем отражениям |
R 1 = 0,0632, wR 2 = 0,1240 |
R 1 = 0,1193, wR 2 = 0,1532 |
R 1 = 0,0531, wR 2 = 0,0779 |
R 1 = 0,0461, wR 2 = 0,1067 |
|
Остаточная электронная плотность (min/max), e/A3 |
0,22/–0,38 |
0,27/–0,49 |
0,23/–0,65 |
0,29/–0,22 |
Таблица 2
|
Связь d , Å |
Угол ω, град. |
||
|
1 |
|||
|
S(1)–O(2) |
1,4512(17) |
O(2)S(1)O(3) |
111,67(11) |
|
S(1)–O(3) |
1,4417(17) |
O(2)S(1)O(4) |
112,01(10) |
|
S(1)–O(4) |
1,4502(18) |
O(3)S(1)O(4) |
113,71(11) |
|
S(1)–C(31) |
1,800(2) |
O(2)S(1)C(31) |
105,83(9) |
|
P(1)–C(1) |
1,7932(19) |
C(1)P(1)C(7) |
111,04(9) |
|
P(1)–C(7) |
1,8048(17) |
C(7)P(1)C(11) |
109,21(8) |
|
P(1)–C(11) |
1,793(2) |
C(11)P(1)C(21) |
110,59(8) |
|
P(1)–C(21) |
1,7910(18) |
C(1)P(1)C(21) |
110,57(8) |
|
C(7)‒O(1) |
1,415(2) |
C(7)O(1)C(8) |
111,27(16) |
|
2 |
|||
|
S(1)–O(2) |
1,442(2) |
O(2)S(1)O(3) |
111,97(11) |
|
S(1)–O(3) |
1,4423(17) |
O(2)S(1)O(4) |
114,68(12) |
|
S(1)–O(4) |
1,4459(16) |
O(3)S(1)O(4) |
110,44(11) |
|
S(1)–C(31) |
1,798(2) |
O(2)S(1)C(31) |
104,34(9) |
|
P(1)–C(1) |
1,797(2) |
C(1)P(1)C(7) |
110,36(9) |
|
P(1)–C(7) |
1,7999(18) |
C(7)P(1)C(11) |
115,41(9) |
|
P(1)–C(11) |
1,796(2) |
C(11)P(1)C(21) |
109,34(9) |
|
P(1)–C(21) |
1,7983(18) |
C(1)P(1)C(21) |
109,26(8) |
|
O(1)‒C(8) |
1,206(2) |
O(1)C(8)C(7) |
121,57(16) |
|
3 |
|||
|
S(1)–O(1) |
1,441(3) 1 |
O(1)S(1)O(2) |
115,01(17) |
Окончание табл. 1
|
Связь d , Å |
Угол ω, град. |
||
|
S(1)–O(2) |
1,454(2) |
O(1)S(1)O(3) |
113,51(18) |
|
S(1)–O(3) |
1,452(3) |
O(2)S(1)O(3) |
112,38(15) |
|
S(1)–C(31) |
1,807(3) |
O(1)S(1)C(31) |
105,72(15) |
|
P(1)–C(1) |
1,797(3) |
C(1)P(1)C(7) |
109,29(14) |
|
P(1)–C(7) |
1,823(3) |
C(7)P(1)C(11) |
113,48(13) |
|
P(1)–C(11) |
1,808(3) |
C(11)P(1)C(21) |
105,22(12) |
|
P(1)–C(21) |
1,797(3) |
C(1)P(1)C(11) |
111,33(13) |
|
Br(1)–C(8) |
1,939(3) |
C(1)P(1)C(21) |
110,56(13) |
|
Cl(1)–C(32) |
1,748(3) |
C(7)P(1)C(21) |
106,79(13) |
|
Cl(2)–C(35) |
1,740(3) |
Br(1)C(8)C(7) |
112,9(2) |
|
4 |
|||
|
S(1)–O(3) |
1,4505(15) |
O(3)S(1)O(4) |
113,56(9) |
|
S(1)–O(4) |
1,4438(13) |
O(3)S(1)O(5) |
111,04(9) |
|
S(1)–O(5) |
1,4497(13) |
O(4)S(1)O(5) |
112,23(9) |
|
S(1)–C(31) |
1,7706(15) |
O(3)S(1)C(31) |
106,13(8) |
|
P(1)–C(1) |
1,8004(16) |
C(1)P(1)C(7) |
111,52(7) |
|
P(1)–C(7) |
1,8004(17) |
C(7)P(1)C(11) |
110,67(7) |
|
P(1)–C(11) |
1,7890(16) |
C(11)P(1)C(21) |
107,79(7) |
|
P(1)–C(21) |
1,7924(15) |
O(1A)C(17B)O(1B) |
123,1(5) |
|
O(1A)–C(17B) |
1,195(6) |
O(1A)C(17B)C(10) |
125,2(4) |
|
O(1B)–C(17B) |
1,326(6) |
O(1B)C(17B)C(10) |
111,7(4) |
|
O(2A)–C(17A) |
1,194(4) |
O(2A)C(17A)O(2B) |
122,8(3) |
|
O(2B)–C(17A) |
1,318(4) |
O(2A)C(17A)C(10) |
126,8(4) |
|
C(10)–C(17A) |
1,383(4) |
O(2B)C(17A)C(10) |
110,3(3) |
|
C(10)–C(17B) |
1,688(5) |
C(17A)C(10)C(9) |
120,82(18) |
|
O(6)–C(37) |
1,2209(19) |
C(17B)C(10)C(9) |
103,7(2) |
|
O(7)–C(37) |
1,310(2) |
O(6)C(37)O(7) |
122,79(15) |
|
O(8)–C(34) |
1,355(2) |
O(8)C(34)C(35) |
118,50(15) |
Полные таблицы координат атомов, длин связей и валентных углов для структур депонированы в Кембриджском банке структурных данных (№ 2161982 (1), № 2162500 (2), № 2162502 (3), № 2167983 (4), ; .
Обсуждение результатов
Нами найдено, что реакции галогенидов алкилтрифенилфосфония с аренсульфоновыми кислотами в воде приводят к образованию аренсульфонатов алкилтрифенилфосфония, выделенных из реакционной смеси с выходом до 97 %.
[Ph3PR]Hal + HOSO2Ar н20124^' 14 [Ph3PR][OSO2Ar]
—HHal
Hal = Cl, Br;
R = CH 2 OMe, Ar = C 6 H 2 Me 3 -2,4,6 ( 1 ); R = CH 2 C(O)Me, Ar = C 6 H 2 Me 3 -2,4,6 ( 2 );
R = (CH 2 ) 2 Br, Ar = C 6 H 3 Cl 2 -2,5 ( 3 ); R = (CH 2 ) 4 COOH, Ar = C 6 H 3 (COOH-3)(OH-4) ( 4 )
При испарении воды имело место образование устойчивых на воздухе бесцветных прозрачных кристаллов, хорошо растворимых в хлороформе, аренах и дихлорметане, плохо - в воде и ацетонитриле при комнатной температуре.
В ИК-спектрах соединений 1-4 наблюдаются полосы поглощения средней интенсивности валентных и деформационных колебаний связей CAr–H при 3088‒3049 см–1 и 1171‒1107 см–1; внеплоскостные деформационные колебания характеризуются полосами при 872‒810 см–1. Колебания связей C-Н в алкильных заместителях проявляются в области 2995-2934 см–1 (СН3), 2914-2887 см–1 (СН2). Полосы поглощения при 1246-1217 см-1 и 1109-1082 см-1 относятся к асимметричным и симметричным валентным колебаниям сульфонатной группы SO3. Интенсивные полосы поглощения при 692‒691 см–1 и 581‒535 см‒1 можно отнести к валентным колебаниям связей S‒O и C–S. Валентные и деформационные колебания связей CAr–P характеризуются полосами поглощения в областях 1439‒1435 см–1 и 1051‒1011 см–1 соответственно. Колебаниям связей CAr–Cl в спектре структуры 3 отвечают полосы высокой интенсивности при 741 и 733 см–1, полоса при 523 см–1 подтверждает присутствие в комплексе связи C-Br. Также в ИК-спектре комплекса 4 присутствуют три интенсивные полосы валентных колебаний карбонильной группы в области 1670-1587 см–1, свидетельствующие о наличии в нем двух типов карбоксильных групп [21, 22].
По данным РСА, кристаллы 1 - 4 состоят из катионов алкилтрифенилфосфония и аренсульфонатных анионов (рис. 1 - 4).
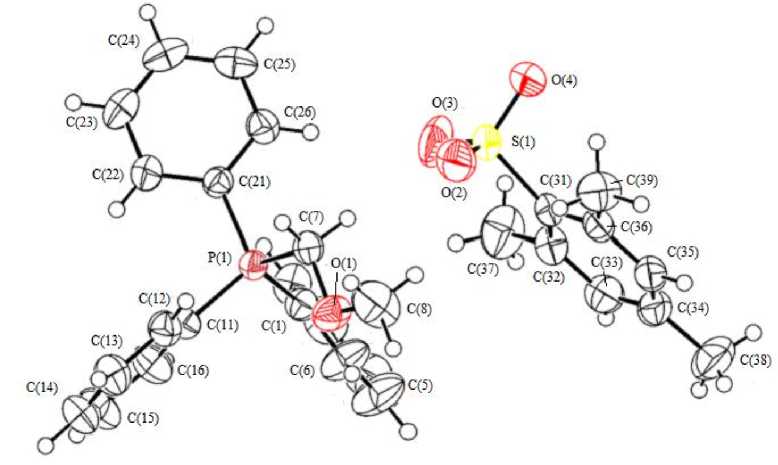
Рис. 1. Строение комплекса 1 в представлении атомов эллипсоидами тепловых колебаний с 50%-ной вероятностью
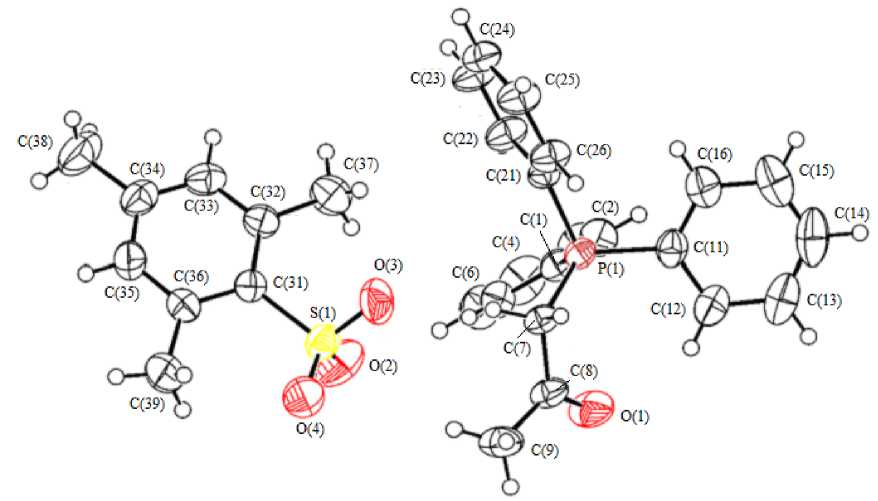
Рис. 2. Строение комплекса 2 в представлении атомов эллипсоидами тепловых колебаний с 50%-ной вероятностью
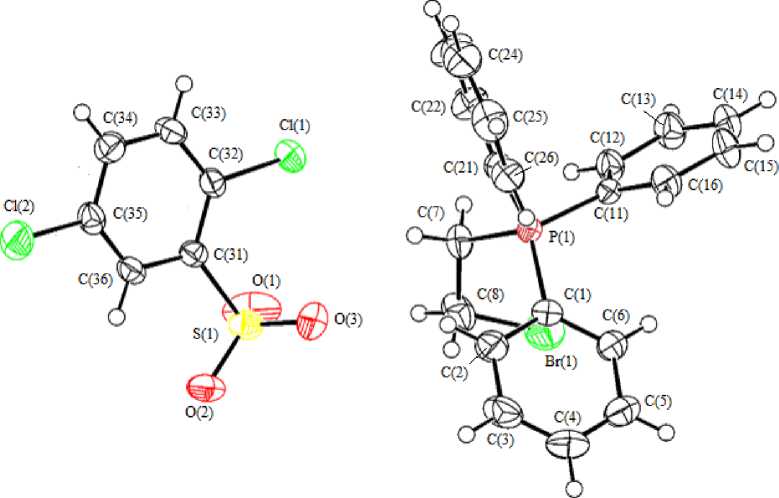
Рис. 3. Строение комплекса 3 в представлении атомов эллипсоидамитепловых колебаний с 50%-ной вероятностью
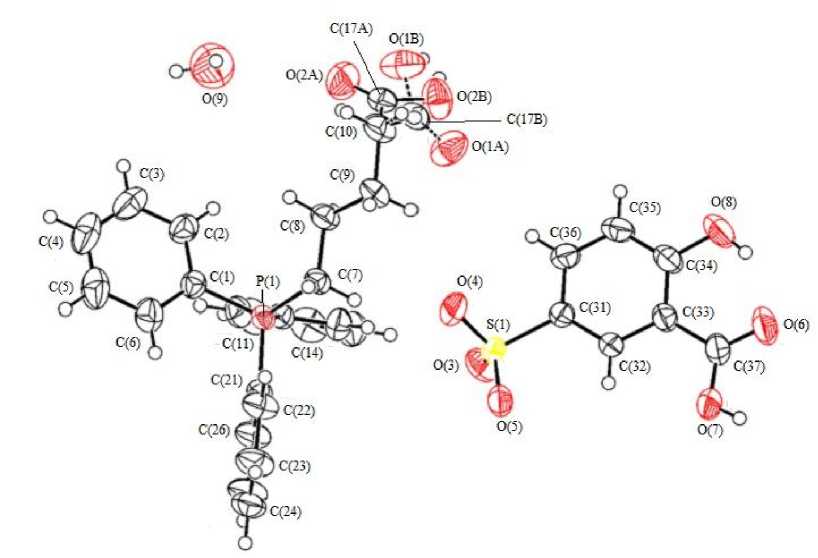
Рис. 4. Строение гидрата комплекса 4 в представлении атомов эллипсоидами тепловых колебаний с 50%-ной вероятностью
Атомы фосфора в катионах 1-4 имеют тетраэдрическую координацию (углы СРС варьируют в интервале 107,18(8)°-111,04(9)° для 1, 104,50(8)°-115,41(9)° для 2, 105,22(12)°-113,48(13)° для 3, 107,79(7)°-111,52(7)° для 4). Длины связей P-C составляют 1,7910(18)-1,8048(17), 1,796(2)-1,7999(18), 1,797(3)-1,823(3), 1,7890(16)-1,8004(17) А соответственно, что несколько меньше суммы их ковалентных радиусов (1,88 А [23]). Расстояния S-O в аренсульфонатных анионах незначительно отличаются [1,4417(17)-1,4512(17), 1,442(2)-1,4459(16), 1,441(3)-1,454(2), 1,4438(13)-1,4505(15) А], однако в первом приближении можно говорить о равномерном распределении электронной плотности в группах SO3. Длины связей S-C состав- ляют 1,800(2), 1,798(2), 1,807(3), 1,7706(15) Å, что сопоставимо с суммой ковалентных радиусов атомов-партнеров [1,81 Å].
Структурная организация кристаллов 1 - 4 формируется за счет множества слабых водородных связей между катионами и анионами, например, S=O···H - CAr (2,33 - 2,58, 2,34 - 2,62, 2,47 - 2,65, 2,56 - 2,62 Å). В кристалле 4 наблюдаются наиболее прочные водородные связи (S=O···H - OC(O) (1,83 Å)), посредством которых аренсульфонатные анионы структурируются в димеры (рис. 5).
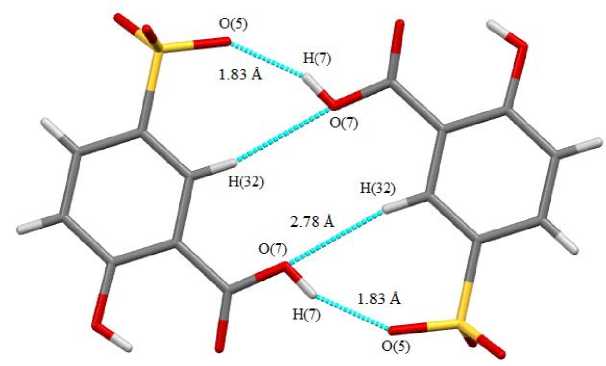
Рис. 5. Димерная организация аренсульфонатных анионов в кристалле соединения 4
Выводы
Таким образом, взаимодействием эквимолярных количеств галогенида алкилтрифенилфосфония с мезитиленсульфоновой, 2,5-дихлорбензолсульфоновой и сульфосалициловой кислотами в воде получены аренсульфонаты алкилтрифенилфосфония [Ph 3 PR][OSO 2 Ar], R = CH 2 OMe, Ar = C 6 H 2 Me 3 -2,4,6 ( 1 ); R = CH 2 C(O)Me, Ar = C 6 H 2 Me 3 -2,4,6 ( 2 ); R = (CH 2 ) 2 Br, Ar = C 6 H 3 Cl 2 -2,5 ( 3 ); R = (CH 2 ) 4 COOH, Ar = C 6 H 3 (COOH-3)(OH-4) ( 4 ), особенности строения которых установлены методом РСА. Кристаллы 1 - 4 состоят из тетраэдрических алкилтрифенилфосфониевых катионов и аренсульфонатных анионов с тетраэдрическим атомом серы. Аренсульфонатные анионы в комплексе 4 посредством водородных связей структурированы в димеры.
Список литературы Синтез и строение аренсульфонатов алкилтрифенилфосфония
- Пурдела Д., Вылчану Р. Химия органических соединений фосфора. М.: Химия, 1972. 752 с.
- Бартон Д. Общая органическая химия. Т. 5. Соединения фосфора и серы / Д. Бартон, У.Д. Оллис. М.: Химия, 1983. 720 с.
- Alkyloxy- and silyloxy-derivatives of P(V) and Sb(V) / G.A. Razuvaev, N.A. Osanova, T.G. Brilkina et al. // J. Organomet. Chem. 1975. Vol. 99, no. 1. P. 93-106. DOI: 10.1016/S0022-328X(00)86365-2.
- Wang D., Astruc D. The golden age of transfer hydrogenation // Chem. Rev. 2015. Vol. 115. P. 6621-6686. DOI: 10.1021/acs.chemrev.5b00203.
- The Stille reaction, 38 years later / C. Cordovilla, C. Bartolome, J.M. Martinez-Ilarduya et al. // ACS Catal. 2015. Vol. 5. P. 3040-3053. DOI: 10.1021/acscatal.5b00448.
- Chong C.C., Kinjo R. Metal-free ст-bond metathesis in 1,3,2-diazaphospholene-catalyzed hydro-boration of carbonyl compounds // Angew. Chem. Int. Ed. 2015. Vol. 127. P. 192-196. DOI: 10.1002/ange.201408760.
- Карбоксилаты и сульфонаты тетрафенилфосфора. Синтез и строение / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина и др. // Журн. общей химии. 2009. Т. 79. С. 80-89. DOI: 10.1134/S1070363209010125.
- Синтез и строение карбоксилатов тетрафенилфосфония / В.В. Шарутин, О.К. Шарутина, А.В. Рыбакова и др. // Журн. общей химии. 2018. Т. 88, № 8. С. 1308-1313. DOI: 10.1134/S0044460X18080139.
- Шарутин В.В., Мукушева Н., Уржумова А.В. Синтез и строение 2,4-динитробензолсульфоната тетрафенилфосфония // Вестник ЮУрГУ. Серия «Химия». 2018. Т. 10, № 2. С. 48-54. DOI: 10.14529/chem180206.
- Шарутин В.В., Шарутина О.К., Губанова Ю.О. Синтез и строение аренсульфонатов тетрафенилфосфония // Изв. вузов. Химия и хим. технология. 2019. Т. 62, № 2. С. 4-10. DOI: 10.6060/ivkkt.20196202.5823.
- New organic free radical anions TEMPO-A-CO-(o-; m-; ^СбН^Оз- (A = NH; NCH3; O) and their TTF and/or BEDT-TTF salts / H. Akutsu, K. Masaki, K. Mori et al. // Polyhedron. 2005. Vol. 24. P. 2126-2132. DOI: 10.1016/j.poly.2005.03.023.
- Tunable GUMBOS-based sensor array for label-free detection and discrimination of proteins / W.I.S. Galpothdeniya, F.R. Fronczek, M. Cong et al. // J. Mater. Chem. B. 2016. Vol. 4, no. 8. P. 1414-1422. DOI: 10.1039/C5TB02038G.
- A new anionic acceptor, 2-sulfo-3,5,6-trichloro-1,4-benzoquinone and its charge-transfer salts / H. Akutsu, J. Yamada, S. Nakatsuji et al. // CrystEngComm. 2009. Vol. 11, no. 12. P. 2588-2592. DOI: 10.1039/b909519e.
- Dinuclear calcium complex with weakly NH-0 hydrogen-bonded sulfonate ligands / A. Onoda, Y. Yamada, M. Doi et al. // Inorg. Chem. 2001. Vol. 40, no. 3. P. 516-521. DOI: 10.1021/ic0003067.
- Anion polarity-induced self-doping in a purely organic paramagnetic conductor, a-a'-(BEDT-TTF)2(PO-CONH-m-C6H4SO3-H2O where BEDT-TTF is te(ethylenedithio)tetrathiafulvalene and PO is the radical 2,2,5,5-tetramethyl-3-pyrrolin-1-oxyl / H. Akutsu, K. Ishihara, S. Ito et al. // Polyhedron. 2017. Vol. 136. P. 23-29. DOI: 10.1016/j.poly.2017.02.001.
- Correlation between metal-insulator transition and hydrogen-bonding network in the organic metal á-(BEDT-TTF)4[2,6-anthracene-67s(sulfonate)](H2O)4 / F. Camerel, G. Le Helloco, T. Guizouarn et al. // Cryst. Growth Des. 2013. Vol. 13, no. 11. P. 5135-5145. DOI: 10.1021/cg401416h.
- Ferrer E.G., Williams P.A.M., Castellano E.E. On a novel synthesis of 2-sulfonatobenzoic acid by oxidation of thiosalicylic acid catalyzed by copper(II): a structural study // Z. Anorg. Allg. Chem. 2002. Vol. 628. P. 1979-1984. DOI: 10.1002/1521-3749(200209)628:9/10<1979::AID-ZAAC1979-3.0.CO;2-V.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures from Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: a complete structure solution, refinement and analysis program / O.V. Dolomanov, L.J. Bourhis, R.J. Gildea et al. // J. Appl. Cryst. 2009. Vol. 42. P. 339-341. DOI: 10.1107/S0021889808042726.
- Тарасевич Б.Н. ИК-спектры основных классов органических соединений. М.: МГУ, 2012. 54 с.
- Инфракрасная спектроскопия органических и природных соединений: учебное пособие / А.В. Васильев, Е.В. Гриненко, А.О. Щукин и др. СПб.: СПбГЛТА, 2007. 54 с.
- Covalent radii revisited / B. Cordero, V. Gómez, A.E. Platero-Prats et al. // Dalton Trans. 2008. Vol. 21. P. 2832-2838. DOI: 10.1039/B801115J.


