Синтез и строение аренсульфонатов тетра(пара-толил)сурьмы p-Tol4SbOSO2C6H3(NO2)-2,4 и [p-Tol4Sb] [p-Tol4SbOC(O)C6H3(OH-4)SO3] ∙ H2O
Автор: Шарутин В.В., Морозова К.Д.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 3 т.16, 2024 года.
Бесплатный доступ
Взаимодействием бромида тетра( пара -толил)стибония p- Tol4SbBr с дигидратом 2,4-динитробензолсульфоновой кислоты в воде синтезирован 2,4-динитробензолсульфонат тетра( пара -толил)стибония p -Tol4SbOSO2С6H3(NO2)2-2,4 (1), который также синтезировали из пента( пара -толил)сурьмы и 2,4-динитробензолсульфоновой кислоты в бензоле. Продуктом реакции пента( пара -толил)сурьмы с сульфосалициловой кислотой (мольное соотношение 2:1 соответственно) в бензоле с последующей перекристаллизацией целевого продукта из воды является гидрат сульфосалицилата тетра( пара -толил)стибония [ p -Tol4Sb][ p -Tol4SbOC(O)C6H3(OH-4)SO3]∙H2O (2). По данным рентгеноструктурного анализа, атомы сурьмы в комплексе 1 имеют координацию искаженной тетрагональной пирамиды, а с учетом координационной связи Sb∙∙∙OSO2С6H3(NO2)2-2,4 (2,877(3) Å) - искаженной тригональной бипирамиды, при этом аксиальный угол CSbО составлял 170,53(9)°. В состав комплекса 2 входят тетраэдрические катионы тетра( пара -толил)стибония, молекулы гидратной воды и тригонально-бипирамидальные сульфосалицилатные анионы, в которых толильные заместители занимают экваториальные положения, а атом кислорода связан с центральным атомом полярной ковалентной связью Sb-O (2,279(3) Å). Кроме того, карбонильный атом кислорода координирован на атом металла (расстояние Sb∙∙∙O=С составляет 3,323(6) Å), что превышает сумму ковалентных радиусов атомов партнеров (2,14 Å), но короче суммы ван-дер-ваальсовых радиусов атомов-партнеров (3,7 Å). В катионе 2 атом сурьмы координирован на один из атомов кислорода сульфонатной группы сульфосалицилатного заместителя, причем расстояние Sb∙∙∙OSO2 (2,651(3) Å) короче аналогичного расстояния в комплексе 1, а угол CSbО составляет 176,51(13)°, поэтому можно говорить о тригонально-бипирамидальной координации обоих атомов сурьмы в комплексе 2. Приведены кристаллографические характеристики: 1 (C34H31N2O7SSb, M = 733,42; триклинная сингония, пр. гр. P- 1; параметры ячейки: a = 9,819(3) Å, b = 11,531(4) Å, c = 15,778(6) Å; a = 93,631(18)°, β = 102,62(2)°, g = 110,333(13)°, V = 1615,7(10) Å3, Z = 2; r(выч.) = 1,508 г/см3; m = 0,969 мм-1; F (000) = 744,0; обл. сбора по 2q: 5,86-58,38°; -13 ≤ h ≤ 13, -15 ≤ k ≤ 15, -21 ≤ l ≤ 21; всего отражений 67524; независимых отражений 8685 ( R int = 0,0445); GOOF = 1,046; R -фактор = 0,0308) и 2 (C63H62O7SSb2, M = 1206,69; моноклинная сингония, пр. гр. P 21/ c ; параметры ячейки: a = 21,132(15) Å, b = 13,644(9) Å, c = 21,796(19) Å; a = 90,00°, β = 111,52(3)°, g = 90,00°, V = 5846(8) Å3, Z = 4; r(выч.) = 1,371 г/см3; m = 1,010 мм-1; F (000) = 2456,0; обл. сбора по 2q: 5,98-47,76°; -24 ≤ h ≤ 24, -15 ≤ k ≤ 15, -24 ≤ l ≤ 24; всего отражений 59879; независимых отражений 8986 ( R int = 0,0621); GOOF = 1,028; R -фактор = 0,0355). Полные таблицы координат атомов, длин связей и валентных углов соединений 1 и 2 депонированы в Кембриджском банке структурных данных (CCDC 2216049 и 2233523; deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
2, 4-динитробензолсульфонат, сульфосалицилат, тетра(пара-толил)стибоний, синтез, строение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147244642
IDR: 147244642 | УДК: 546.865+547.53.024+548.312.4 | DOI: 10.14529/chem240305
Synthesis and structure of tetra(para-tolyl)antimony arenesulfonates p-Tol4SbOSO2C6H3(NO2)-2,4 and [p-Tol4Sb] [p-Tol4SbOC(O)C6H3(OH-4)SO3] ∙ H2O
Reaction of tetra( para -tolyl)stibonium bromide p -Tol4SbBr with 2,4-dinitrobenzenesulfonic acid in water synthesized tetra( para -tolyl)stibonium 2,4-dinitrobenzenesulfonate p -Tol4SbOSO2С6H3(NO2)2-2,4 (1), which was also synthesized from penta( para -tolyl)antimony and 2,4-dinitrobenzenesulfonic acid in benzene. The product of the reaction of penta( para -tolyl)antimony with sulfosalicylic acid (mole ratio 2:1, respectively) in benzene, followed by recrystallization of the target product from water, was tetra( para -tolyl)stibonium sulfosalicylate hydrate [ p -Tol4Sb][ p -Tol4SbOC(O)C6H3(OH-4)SO3]∙H2O (2). According to X-ray diffraction analysis, the antimony atoms in complex 1 have the coordination of a distorted tetragonal pyramid, and taking into account the coordination bond Sb∙∙∙OSO2С6H3(NO2)2-2,4 (2.877(3) Å), they form a distorted trigonal bipyramid, while the CSbО axial angle is 170.53(9)°. Complex 2 includes tetrahedral tetra( para -tolyl)stibonium cations, hydration water molecules and trigonal-bipyramidal sulfosalicylate anions, in which tolyl substituents occupy equatorial positions and the oxygen atom is linked to the central atom by a polar covalent bond Sb-O (2.279(3) Å). In addition, the carbonyl oxygen atom is coordinated to the metal atom (the Sb∙∙∙O=C distance is 3.323(6) Å), which exceeds the sum of the covalent radii of the partner atoms (2.14 Å), but is shorter than the sum of Van der Waals radii of partner atoms (3.7 Å). In cation 2, the antimony atom is coordinated to one of the oxygen atoms of the sulfonate group of the sulfosalicylate substituent, and the Sb∙∙∙OSO2 distance (2.651(3) Å) is shorter than the similar distance in complex 1, and the CSbО angle is 176.51(13)°, therefore we can talk about trigonal bipyramidal coordination of both antimony atoms in complex 2. The crystallographic characteristics: 1 [C34H31N2O7SSb, M = 733.42; triclinic system, sp. gr. P-1; cell parameters: a = 9.819(3) Å, b = 11.531(4) Å, c = 15.778(6) Å; a = 93.631(18)°, β = 102.62(2)°, g = 110.333(13)°, V = 1615.7(10) Å3, Z = 2; rcalc = 1.508 g/cm3; m = 0.969 mm-1; F(000) = 744.0; region collection at 2q 5.86-58.38°; -13 ≤ h ≤ 13, -15 ≤ k ≤ 15, -21 ≤ l ≤ 21; total reflections 67524; independent reflections 8685 ( R int = 0.0445); GOOF = 1.046; R -factor = 0.0308] and 2 [C63H62O7SSb2, M = 1206,69; monoclinic system, sp. gr. P 21/c; cell parameters: a = 21.132(15) Å, b = 13.644(9) Å, c = 21.796(19) Å; β = 111.52(3)°, V = 5846(8) Å3, Z = 4; rcalc = 1.371 g/cm3; m = 1.010 mm-1; F(000) = 2456.0; region collection by 2q 5.98-47.76; -24 ≤ h ≤ 24, -15 ≤ k ≤ 15, -24 ≤ l ≤ 24; total reflections 59879; independent reflections 8986 ( R int = 0.0621); GOOF = 1.028; R -factor = 0.0355]. Complete tables of atomic coordinates, bond lengths, and bond angles of compounds 1 and 2 have been deposited in the Cambridge Structural Data Center (CCDC 2216049 and 2233523; deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac. uk).
Текст научной статьи Синтез и строение аренсульфонатов тетра(пара-толил)сурьмы p-Tol4SbOSO2C6H3(NO2)-2,4 и [p-Tol4Sb] [p-Tol4SbOC(O)C6H3(OH-4)SO3] ∙ H2O
Известно, что органические соединения сурьмы применяются в качестве лекарственных препаратов, биоцидов, фунгицидов, в тонком органическом синтезе и др. [1]. Одними из наиболее исследованных сурьмаорганических соединений являются фенильные производные пятивалентной сурьмы общей формулы Ph 4 Sb]X (Х – электроотрицательная группа) [2]. В меньшей степени изучены подобные толильные производные [3 - 24]. С целью расширения экспериментального материала по данному направлению в настоящей работе изучены синтез и особенности строения
2,4-динитробензолсульфоната тетра( пара -толил)стибония ( 1 ) и сульфосалицилата тетра( пара -толил)стибония ( 2 ). Для комплексов 1 и 2 приведены результаты рентгеноструктурного исследования.
Экспериментальная часть
ИК-спектры соединений записывали на ИК-Фурье спектрометре Shimadzu IR Affinity-1S в таблетке KBr в области 4000 - 400 см - 1.
Элементный анализ выполнен на элементном анализаторе Carlo Erba CHNS-O EA 1108. Температуры плавления измерены на синхронном термоанализаторе Netzsch 449C Jupiter.
В работе использовали дигидрат 2,4-динитробензолсульфоновой кислоты и сульфосалициловую кислоту производства фирмы Alfa Aesar. Пента( пара -толил) сурьму и бромид тетра( пара -толил)сурьмы получали по методикам, описанным в [1].
Синтез 2,4-динитробензолсульфоната тетра( пара -толил) сурьмы (1). К водному раствору 566 мг (1,0 ммоль) бромида тетра( пара -толил)сурьмы приливали раствор 284 мг (1,0 ммоль) 2,4-динитробензолсульфоновой кислоты в 10 мл воды. После удаления растворителя получили 594 мг (81%) бесцветных кристаллов 1 с t пл = 213 °С. ИК-спектр ( v , см-1): 3102 сл, 3055 сл, 2918 ср, 2868 сл, 1603 ср, 1593 ср, 1533 оч. с, 1493 ср, 1449 ср, 1396 с, 1350 оч.с, 1261 оч.с, 1242 сл, 1211 оч. с, 1194 сл, 1132 ср, 1107 с, 1063 с, 1040 сл, 1022 оч. с, 916 сл, 895 ср, 847 ср, 833 ср, 799оч. с., 745 с, 737 ср, 714 ср, 664 ср, 631 оч. с, 600 сл, 582 ср, 555 с, 480 оч.с, 420 сл. Найдено: C 55,58; H 4,33 %. Для C 34 H 31 N 2 O 7 SSb вычислено: C 55,63; H 4,23 %.
Реакция эквимолярных количеств пента( пара -толил)сурьмы и 2,4-динитробензолсульфоновой кислоты в бензоле, с последующей перекристаллизацией целевого продукта из воды приводила к образованию 1 с выходом 82 %.
Из пента( пара -толил)сурьмы и сульфосалициловой кислоты в бензоле при мольном соотношении исходных реагентов 2:1 получали 2 с выходом 88 %.
Рентгеноструктурный анализ проводили на автоматическом четырехкружном дифрактометре Bruker D8 QUEST (Mo K α -излучение, λ = 0,71073 Å, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [25]. Все расчеты по определению и уточнению структур выполнены по программам SHELXL/PC [26] и OLEX2 [27]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Кристаллографические данные и результаты уточнения структур приведены в таблице.
Таблица
Кристаллографические данные, параметры эксперимента и уточнения структур 1 и 2
|
Параметр |
1 |
2 |
|
Формула |
C 34 H 31 N 2 O 7 SSb |
C 63 H 62 O 7 SSb 2 |
|
М |
733,42 |
1206,69 |
|
Сингония |
Триклинная |
Моноклиная |
|
Пространственная группа |
P -1 |
P 2 1 / c |
|
a , Å |
9,819(3) |
21,132(15) |
|
b, Å |
11,531(4) |
13,644(9) |
|
c, Å |
15,778(6) |
21,796(19) |
|
α, град. |
93,631(18) |
90,00 |
|
β, град. |
102,62(2) |
111,52(3) |
|
γ, град. |
110,333(13) |
90,00 |
|
V , Å3 |
1615,7(10) |
5846(8) |
|
Z |
2 |
4 |
|
ρ (выч.), г/см3 |
1,508 |
1,371 |
|
–1 µ , мм– |
0,969 |
1,010 |
|
F (000) |
744,0 |
2456,0 |
|
Форма кристалла (размер, мм) |
0,35 × 0,3 × 0,15 |
0,45 × 0,2 × 0,09 |
Окончание табл. 1
|
Параметр |
1 |
2 |
|
Область сбора данных по 2 0 , град. |
5,86–58,38 |
5,98–47,76 |
|
Интервалы индексов отражений |
–13 ≤ h ≤ 13, –15 ≤ k ≤ 15, –21 ≤ l ≤ 21 |
–24 ≤ h ≤ 24, –15 ≤ k ≤ 15, –24 ≤ l ≤ 24 |
|
Измерено отражений |
67524 |
59879 |
|
Независимых отражений ( R int ) |
8685 (0,0445) |
8986 (0,0621) |
|
Переменных уточнения |
410 |
670 |
|
GOOF |
1,046 |
1,028 |
|
R -факторы по F 2 > 2 а ( F 2 ) |
R 1 = 0,0308, wR 2 = 0,0644 |
R 1 = 0,0355, wR 2 = 0,0644 |
|
R -факторы по всем отражениям |
R 1 = 0,0487, wR 2 = 0,0705 |
R 1 = 0,0614, wR 2 = 0,0726 |
|
Остаточная электронная плотность (min/max), e /Å3 |
0,33/ - 0,49 |
0,34/ - 0,43 |
Полные таблицы координат атомов, длин связей и валентных углов соединения 1 и 2 депонированы в Кембриджском банке структурных данных (№ 2216049 и 2233523; ; .
Обсуждение результатов
Известно, что реакции обмена галогенид-аниона в галогенидах тетраарилстибония используются для получения различных комплексов металлов [2]. Интересный случай замещения гало-генид-аниона на остаток более сильной кислоты описан авторами работы [28], в которой представлена реакция хлорида тетра( пара -толил)стибония с бензолсульфоновой кислотой, приводящая к синтезу бензолсульфоната тетра( пара -толил)стибония.
Мы предположили, что подобным образом может протекать реакция 2,4-динитробензолсульфоновой кислоты с бромидом тетра( пара -толил)сурьмы. Действительно, нами показано, что взаимодействие эквимолярных количеств указанных реагентов в воде приводит к образованию 2,4-динитробензолсульфоната тетра( пара -толил)сурьмы ( 1 ), выделенного из реакционной среды с выходом 81 %.
p -Tol 4 SbBr + HOSO 2 C 6 H 3 (NO 2 ) 2 -2,4 p -Tol 4 SbOSO 2 C 6 H 3 (NO 2 ) 2 -2,4 + HBr
Нами найдено, что продуктом реакции пента( пара -толил)сурьмы с 2,4-динитробензолсульфоновой кислотой в бензоле является комплекс 1 , выделенный из реакционной среды с выходом 82 %.
p -Tol 5 Sb + HOSO 2 C 6 H 3 (NO 2 ) 2 -2,4 p -Tol 4 SbOSO 2 C 6 H 3 (NO 2 ) 2 -2,4 + TolH
В литературе описано строение моно- и биядерных сурьмаорганических производных тет-раарилсурьмы, которые получали из пентаарилсурьмы и сульфосалициловой кислоты [29 - 31]. В настоящей работе уточнена структура биядерного производного тетра( пара -толил)сурьмы ( 2 ), полученного нами из пента( пара -толил)сурьмы и сульфосалициловой кислоты с выходом 88 %.
2 p -Tol 5 Sb + HOSO 2 C 6 H 3 (OH-4)(COOH-3) [ p -Tol 4 Sb][OSO 2 C 6 H 3 (OH-4)(COOSbTol 4 -3)]
По данным рентгеноструктурного анализа, атомы сурьмы в комплексе 1 имеют координацию искаженной тетрагональной пирамиды (рис. 1), а с учетом координационной связи Sb∙∙∙OSO 2 С 6 H 3 (NO 2 ) 2 -2,4 (2,877(3) Å) – искаженной тригональной бипирамиды, при этом аксиальный угол CSbO составлял 170,53(9) ° .
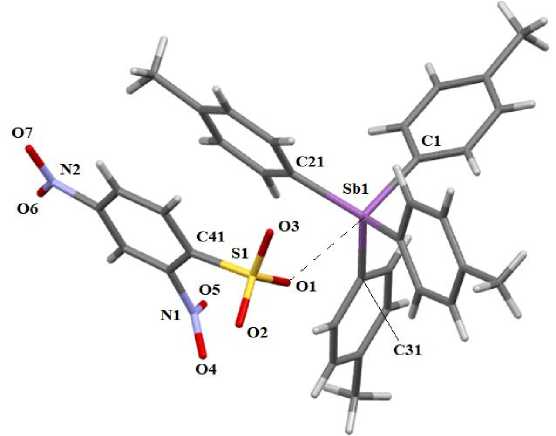
Рис. 1. Строение 2,4-динитробензолсульфоната тетра( пара -толил)сурьмы (1)
В состав комплекса 2 (рис. 2) входят тетраэдрические катионы тетра( пара -толил)стибония, молекулы гидратной воды и тригонально-бипирамидальные сульфосалицилатные анионы, в которых толильные заместители занимают экваториальные положения, а атом кислорода связан с центральным атомом полярной ковалентной связью Sb - O (2,279(3) А).
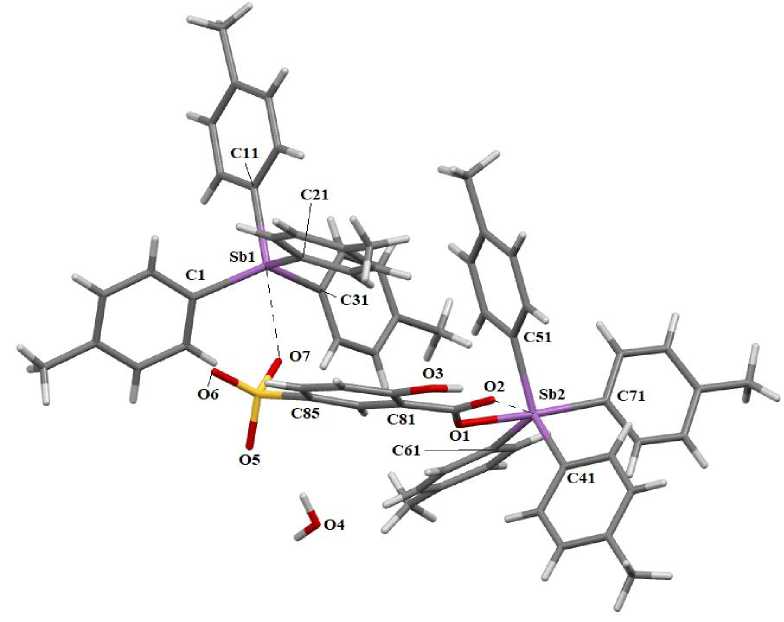
Рис. 2. Строение гидрата сульфосалицилата тетра( пара -толил)стибония (2)
Кроме того, карбонильный атом кислорода координирован на атом металла (расстояние Sb—O=C составляет 3,323(6) А), что превышает сумму ковалентных радиусов атомов партнеров (2,14 А [32]), но короче суммы ван-дер-ваальсовых радиусов атомов-партнеров (3,7 А [33]). В катионе 2 атом сурьмы координирован на один из атомов кислорода сульфонатной группы суль- фосалицилатного заместителя, причем расстояние Sb∙∙∙OSO2 (2,651(3) Å) короче аналогичного расстояния в комплексе 1, а угол CSbO составляет 176,51(13)°, поэтому можно говорить о триго-нально-бипирамидальной координации обоих атомов сурьмы в комплексе 2.
Заключение
Впервые синтезирован с выходом 81 % из бромида тетра(пара-толил)стибония и 2,4-динитробензолсульфоновой кислоты 2,4-динитробензолсульфонат тетра(пара- толил)стибония (1). Комплекс 1 синтезирован также из пента(пара-толил)сурьмы и 2,4-динитробензолсульфоновой кислоты в бензоле с выходом 82 %. Сульфосалицилат тет-ра(пара-толил)сурьмы получен аналогично и после перекристаллизации из воды целевой продукт выделен в виде гидрата (2). Строение комплексов 1 и 2 доказано методом рентгеноструктурного анализа.
Список литературы Синтез и строение аренсульфонатов тетра(пара-толил)сурьмы p-Tol4SbOSO2C6H3(NO2)-2,4 и [p-Tol4Sb] [p-Tol4SbOC(O)C6H3(OH-4)SO3] ∙ H2O
- Кочешков К.А., Сколдинов А.П., Землянский Н.Н. Методы элементоорганической химии. Сурьма, висмут. М.: Наука, 1976. 483 с.
- Шарутин В.В., Поддельский А.И., Шарутина О.К. // Коорд. химия. 2020. Т. 46, № 10. С. 579. DOI: 10.31857/S0132344X20100011
- Акатова К.Н., Бочкова Р.И., Лебедев В.А. и др. // Докл. АН СССР. 1983. Т. 268, № 6. С. 1389.
- Шарутин В.В., Шарутина О.К., Пакусина А.П. и др. // Коорд. химия. 2005. Т. 31, № 2. С. 117. EDN: HRZYJR
- Шарутин В.В., Шарутина О.К., Платонова Т.П. и др. // Коорд. химия. 2003. Т. 29, № 1. С. 13. EDN: OOFNKD
- Шарутин В.В., Шарутина О.К., Панова Л.П., Бельский В.К. // Журн. общ. химии. 1997. Т. 67, №. 9. С. 1531.
- Шарутин В.В., Пакусина А.П., Егорова И.В. и др. // Коорд. химия. 2003. Т. 29, № 5. С. 336. EDN: OOFOOD
- Шарутин В.В., Шарутина О.К., Пакусина А.П., Бельский В.К. // Журн. общ. химии. 1997. Т. 67, № 9. С. 1536. EDN: PFLFSA 9. Шарутин В.В., Шарутина О.К., Тарасова Т.А. и др. // Журн. общ. химии. 1999. Т. 69, № 12. С. 1979.
- Шарутин В.В., Шарутина О.К., Платонова Т.П. и др. // Журн. общ. химии. 2000. Т. 70, № 11. С. 1932. EDN: BAWNYU
- Шарутин В.В., Шарутина О.К., Молокова О.В. и др. // Коорд. химия. 2002. Т. 28, № 8. С. 581. EDN: QEXAWC
- Шарутин В.В., Шарутина О.К., Молокова О.В. и др. // Журн. общ. химии. 2001. Т. 71, № 8. С. 1317.
- Шарутин В.В., Шарутина О.К., Осипов П.Е. и др. // Журн. общ. химии. 2000. Т. 70, № 6. С. 931.
- Сопшина Д.М. // Вестник ЮУрГУ. Сер. «Химия». 2022. Т. 14, № 1. С. 50. DOI: 10.14529/chem220106
- Ефремов А.Н., Шарутин В.В. // Вестник ЮУрГУ. Сер. «Химия». 2021. Т. 13, № 1. С. 47. DOI: 10.14529/chem210105
- Шарутина О.К. // Вестник ЮУрГУ. Сер. «Химия». 2021. Т. 13, № 4. С. 63. DOI: 10.14529/chem210404
- Сенчурин В.С., Орленко Е.Д. // Вестник ЮУрГУ. Сер. «Химия». 2019. Т. 11, № 2. С. 66. DOI: 10.14529/chem190207
- Шарутин В.В., Шарутина О.К., Бондарь Е.А. и др. // Коорд. химия. 2002. Т. 28, № 5. С. 356. EDN: EOICYB
- Шарутин В.В., Шарутина О.К., Ефремов А.Н., Андреев П.В. // Журн. неорг. химии. 2017. Т. 62, № 10. С. 1330. DOI: 10.7868/S0044457X17100075
- Шарутин В.В., Шарутина О.К. // Журн. неорг. химии. 2017. Т. 62, № 7. С. 925. DOI: 10.7868/S0044457X17070224
- Шарутин В.В., Шарутина О.К., Сенчурин В.С., Сомов Н.В. // Журн. неорг. химии. 2016. Т. 61, № 8. С. 1017. DOI: 10.7868/S0044457X16080146
- Шарутин В.В., Шарутина О.К., Ефремов А.Н. // Журн. структ. химии. 2020. Т. 61, № 9. С. 1490. DOI: 10.26902/JSC_id60682
- Шарутин В.В., Шарутина О.К., Ефремов А.Н. // Журн. неорг. химии. 2020. Т. 65, № 1. С. 49. DOI: 10.31857/S0044457X20010158
- Шарутин В.В., Шарутина О.К., Ефремов А.Н., Артемьева Е.В. // Журн. неорг. химии. 2020. Т. 65, № 4. С. 482. DOI: 10.31857/S0044457X20040170
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Dis-playing Crystal Structures from Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Cryst. 2009. V. 42. P. 339. DOI: 10.1107/S0021889808042726
- Шарутин В.В. // Вестник ЮУрГУ. Серия «Химия». 2022. Т. 14, № 4. С. 64. DOI: 10.14529/chem220406
- Шарутин В.В., Шарутина О.К., Панова Л.П., Бельский В.К. // Коорд. химия. 1997. Т. 23, № 7. С. 513.
- Шарутин В.В., Шарутина О.К., Тарасова Т.А. и др. // Журн. общ. химии. 1999. Т. 69, № 12. С. 1979.
- Панова Л.П. Аренсульфонаты тетра- и триарилсурьмы. Синтез и строение: дис. … канд. хим. наук. Иркутск. 1998. 105 с.
- Cordero B., Gómez V., Platero-Prats A.E. // Dalton Trans. 2008. P. 2832. DOI: 10.1039/B801115J
- Бацанов С.С. // Журн. неорган. химии. 1991. Т. 36, № 12. С. 3015.

![Синтез и строение аренсульфонатов тетра(пара-толил)сурьмы p-Tol4SbOSO2C6H3(NO2)-2,4 и [p-Tol4Sb] [p-Tol4SbOC(O)C6H3(OH-4)SO3] ∙ H2O Синтез и строение аренсульфонатов тетра(пара-толил)сурьмы p-Tol4SbOSO2C6H3(NO2)-2,4 и [p-Tol4Sb] [p-Tol4SbOC(O)C6H3(OH-4)SO3] ∙ H2O](/file/cover/147244642/sintez-i-stroenie-arensulfonatov-tetra-para-tolil-surmy-p-tol4sboso2c6h3-no224.png)
