Синтез и строение Бис(2-карбоксибензолсульфоната) три(пара-толил)сурьмы p-tol3Sb[OSO2C6H4(COOH)-2]2
Автор: Шарутин В.В., Морозова К.Д.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 1 т.17, 2025 года.
Бесплатный доступ
Взаимодействием три( пара -толил)сурьмы с 2-сульфобензойной кислотой в эфире в присутствии пероксида водорода в эфире синтезирован бис (2-карбоксибензолсульфонат) три( пара -толил)сурьмы p -Tol3Sb[OSO2С6H4(COOH)-2]2 (1). По данным рентгеноструктурного анализа атомы сурьмы в комплексе 1 имеют координацию искаженной тригональной бипирамиды с толильными заместителями в экваториальной плоскости и аренсульфонатными лигандами в аксиальных положениях, при этом аксиальный угол CSbО составлял 177,96(12)°. Молекулы 1 в кристалле имеют собственную (некристаллографическую) симметрию С2. Ось второго порядка может быть проведена через атомы Sb(1)C(11)C(14)С(15). Аренсульфонатные заместители находятся по одну сторону от аксиальной оси О(1)Sb(1)O(1’), и их арильные группы образуют «стопку» с толильным заместителем С(11)-С(17). В кристалле 1 присутствуют контакты центрального атома с атомами кислорода аренсульфонатных групп (3,639(9) Å), что несколько меньше суммы ван-дер-ваальсовых радиусов атомов Sb и S (3,7 Å). В кристалле молекулы 1 объединяются в димеры при помощи водородных связей между карбонильными атомами кислорода и атомами водорода соседних карбоксильных групп (расстояния С=O∙∙∙HOC(O) составляют 1,85 Å). По данным РСА кристаллографические характеристики 1 [C35H31O10S2Sb, M = 797,47; моноклинная сингония, пр. гр. C 2/ c ; параметры ячейки: a = 14,819(9) Å, b = 15,728(11) Å, c = 14,707(9) Å; β = 93,00(2)°, V = 3423(4) Å3, Z = 4; r(выч.) = 1,547 г/см3; m = 0,985 мм-1; F (000) = 1616,0; обл. сбора по 2q: 6,84-53,34°; -18 ≤ h ≤ 16, -16 ≤ k ≤ 19, -17 ≤ l ≤ 18; всего отражений 6622; независимых отражений 3221 ( R int = 0,0433); GOOF = 1,021; R -фактор = 0,0381]. Полные таблицы координат атомов, длин связей и валентных углов соединения 1 депонированы в Кембриджском банке структурных данных (CCDC 2336248; deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
Бис(2-карбоксибензолсульфонат) три(пара-толил)сурьмы, синтез, строение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147248065
IDR: 147248065 | УДК: 546.865+547.53.024+548.312.4 | DOI: 10.14529/chem250106
Synthesis and structure of tri(para-tolyl)antimony bis(2-carboxybenzenesulfonate) P-Tol3Sb[OSO2C6H4(COOH)-2]2
Reaction of tri( p -tolyl)antimony with 2-sulfobenzoic acid in ether in the presence of hydrogen peroxide in ether leads to tri( para -tolyl)antimony bis (2-carboxybenzenesulfonate) p -Tol3Sb[OSO2С6H4(COOH)-2]2 (1). According to X-ray diffraction analysis, the antimony atoms in centrosymmetric complex 1 have a distorted trigonal bipyramidal coordination with tolyl substituents in the equatorial plane and arenesulfonate ligands in axial positions, while the CSbО axial angle equals 177.96(12)°. Molecules 1 in the crystal have their own (non-crystallographic) C2 symmetry. The second order axis can be drawn through the Sb(1)C(11)C(14)C(15) atoms. The arenesulfonate substituents are located on one side of the axial axis O(1)Sb(1)O(1’), and their aryl groups form a “stack” with the tolyl substituent C(11)-C(17). In crystal 1 there are contacts of the central atom with the oxygen atoms of the arenesulfonate groups (3.639(9) Å), which are slightly less than the sum of the van der Waals radii of the Sb and S atoms (3.7 Å). In the crystal, molecules 1 are combined into dimers using hydrogen bonds between the carbonyl oxygen atoms and the hydrogen atoms of neighboring carboxyl groups (C=O∙∙∙HOC(O) is 1,85 Å). According to the X-ray diffraction data, the crystallographic characteristics of 1 [C35H31O10S2Sb, M = 797.47; monoclinic system, sp. gr. C 2/c; cell parameters: a = 14.819(9) Å, b = 15.728(11) Å, c = 14.707(9) Å; β = 93.00(2)°, V = 3423(4) Å3, Z = 4; rcalc = 1.547 g/cm3; m = 0.985 mm-1; F(000) = 1616.0; collection region by 2q: 6.84-53.34°; -18 ≤ h ≤ 16, -16 ≤ k ≤ 19, -17 ≤ l ≤ 18; total reflections 6622; independent reflections 3221 ( R int = 0.0433); GOOF = 1.021; R -factor = 0.0381]. Complete tables of atomic coordinates, bond lengths, and bond angles of compound 1 have been deposited in the Cambridge Structural Data Center (CCDC 2336248; deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk). Keywords: tri( para -tolyl)antimony bis (2-carboxybenzenesulfonate), synthesis, structure, X-ray diffraction analysis
Текст научной статьи Синтез и строение Бис(2-карбоксибензолсульфоната) три(пара-толил)сурьмы p-tol3Sb[OSO2C6H4(COOH)-2]2
Аннотация. Взаимодействием три(пара-толил)сурьмы с 2-сульфобензойной кислотой в эфире в присутствии пероксида водорода в эфире синтезирован бис(2-карбоксибензолсульфонат) три(пара-толил)сурьмы p-Tol3Sb[OSO2С6H4(COOH)-2]2 (1). По данным рентгеноструктурного анализа атомы сурьмы в комплексе 1 имеют координацию искаженной тригональной бипирамиды с толильными заместителями в экваториальной плоскости и аренсульфонатными лигандами в аксиальных положениях, при этом аксиальный угол CSbO составлял 177,96(12)°. Молекулы 1 в кристалле имеют собственную (некристаллографическую) симметрию С2. Ось второго порядка может быть проведена через атомы Sb(1)C(11)C(14)С(15). Аренсульфонатные заместители находятся по одну сторону от аксиальной оси О(1)Sb(1)O(1’), и их арильные группы образуют «стопку» с толильным заместителем С(11)-С(17). В кристалле 1 присутствуют контакты центрального атома с атомами кислорода аренсульфонатных групп (3,639(9) Å), что несколько меньше суммы ван-дер-ваальсовых радиусов атомов Sb и S (3,7 Å). В кристалле молекулы 1 объединяются в димеры при помощи водородных связей между карбонильными атомами кислорода и атомами водорода соседних карбоксильных групп (расстояния С=O∙∙∙HOC(O) составляют 1,85 Å). По данным РСА кристаллографические характеристики 1 [C35H31O10S2Sb, M = 797,47; моноклинная сингония, пр. гр. C2/c; параметры ячейки: a = 14,819(9) Å, b = 15,728(11) Å, c = 14,707(9) Å; в = 93,00(2)°, V = 3423(4) A3, Z = 4; р(выч.) = 1,547 г/см3; ц = 0,985 мм-1; F(000) = 1616,0; обл. сбора по 20: 6,84-53,34°; -18 < h < 16, -16 < k < 19, -17 < l < 18; всего отражений 6622; независимых отражений 3221 (Rint = 0,0433); GOOF = 1,021; R-фактор = 0,0381]. Полные таблицы координат атомов, длин связей и валентных углов соединения 1 депонированы в Кембриджском банке структурных данных (CCDC 2336248; ; .
Известно, что органические соединения сурьмы применяются в качестве лекарственных препаратов, биоцидов, фунгицидов, в тонком органическом синтезе и др. [1]. Одними из наиболее исследованных сурьмаорганических соединений являются арильные производные пятивалентной сурьмы общей формулы Ar 3 SbX 2 (X – электроотрицательный лиганд), которые получают, как правило, по схеме реакции окислительного присоединения из триарилсурьмы, кислоты HX и пероксида [2]. Эффективное получение дисульфонатов триарилсурьмы этим способом впервые осуществлено и для простейших органосульфоновых кислот. Показано, что из триарилсурьмы, аренсульфоновой кислоты и пероксида водорода (мольное соотношение 1:2:1) в растворе эфира образуются с высоким выходом дисульфонаты триарилсурьмы [3].
Ar3Sb + 2 Ar’OSO 2 H + H 2 O 2 ^ Ar3Sb(OSO 2 Ar') 2 + 2 H 2 O
Полученные бис (аренсульфонаты) триарилсурьмы являются кристаллическими веществами с четкими температурами плавления, хорошо растворимыми в полярных растворителях. Однако увеличение объема аренсульфонатного лиганда приводило к значительному понижению выхода целевого продукта [4, 5]. В меньшей степени изучены подобные реакции окислительного присоединения с участием аренсульфоновых кислот и триарилсурьмы, содержащей различные функциональные группы в арильных заместителях [6 - 11].
По аналогичной реакции не удалось получить из трифенилстибина, пероксида водорода и фенилметансульфоновой кислоты бис (фенилметансульфонат) трифенилсурьмы [12]. В этом случае из реакционной смеси было выделено, независимо от соотношения исходных реагентов, сурьмаорганическое соединение, хорошо растворимое в ароматических углеводородах. Было установлено, что наибольший выход этого комплекса наблюдался при мольном соотношении исходных реагентов 1:1:1. По данным РСА полученный комплекс имеет структуру цвиттер-иона.
-O-SO 2
+
Ph 3 Sb + HOSO 2 CH 2 Ph + H 2 O 2 Ph 3 Sb CH + 2 H 2 O
Ph
Очевидно, что схема реакции окислительного присоединения изменялась из-за наличия в молекуле фенилметансульфоновой кислоты двух подвижных атомов водорода вместо одного, присутствующего в молекулах аренсульфоновых кислот. Органические кислоты иного строения в присутствии окислителя реагируют с трифенилсурьмой с образованием весьма неожиданных соединений.
Так, взаимодействие трифенилсурьмы с 6,6,6-трифтор-2,2-диметилгександионом-3,5 в присутствии пероксида водорода в эфире приводит к образованию (6,6,6-трифтор-3-гексанон-5,5-диолато)трифенилсурьмы [13].
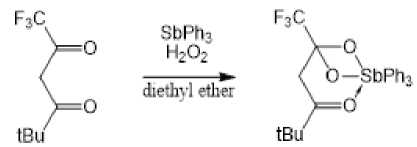
По данным рентгеноструктурного анализа, атом Sb в комплексе имеет искаженную октаэдрическую координацию.
Показано, что полифункциональная 3,4-дигидроксибензойная кислота реагирует с трифенил-сурьмой в присутствии пероксида водорода в растворе диэтилового эфира как дигидроксибензол, при этом продуктом реакции являлся тетраядерный макроцикл: тетракис ( μ 2-4-карбоксипирокатехолато-О,О’O’’)- тетракис [трифенилсурьма(V)] [14].
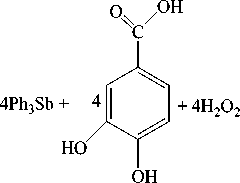
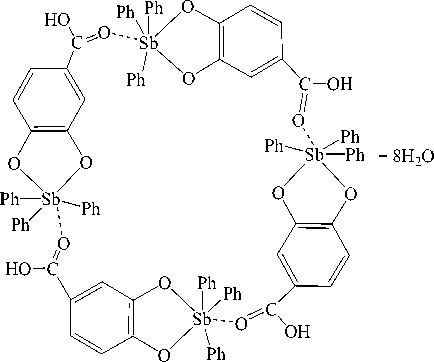
В макроцикле органический лиганд связан с атомом сурьмы двумя гидроксильными атомами кислорода, образуя хелатный цикл, а на соседний атом сурьмы координирует атомом кислорода карбонильной группы.
С целью расширения экспериментального материала по данному направлению в настоящей работе изучены синтез и особенности строения бис (2-карбоксибензолсульфоната) три( пара -толил)сурьмы p -Tol 3 Sb[OSO 2 С 6 H 4 (COOH)-2] 2 ( 1 ), строение которого доказано методом РСА.
Экспериментальная часть
ИК-спектры соединений записывали на ИК-Фурье спектрометре Shimadzu IR Affinity-1S в таблетке KBr в области 4000 - 400 см - 1.
Элементный анализ выполнен на элементном анализаторе Carlo Erba CHNS-O EA 1108. Температуры плавления измерены на синхронном термоанализаторе Netzsch 449C Jupiter.
В работе использовали 2-карбоксибензолсульфоновую кислоту производства фирмы «Alfa Aesar». Три( пара -толил)сурьму получали по методике, описанной в [15].
Синтез бис (2-карбоксибензолсульфоната) три( пара -толил)сурьмы (1) . Смесь 0,15 г (0,38 ммоль) три( пара- толил)сурьмы, 0,15 г (0,76 ммоль) 2-карбоксибензолсульфоновой кислоты и 0,043 г 30%-ного пероксида водорода в 15 мл диэтилового эфира выдерживали 18 ч. После испарения растворителя получили 0,24 г (80 %) бесцветных кристаллов с Т разл = 185 °С. Найдено (%): C 52,47; Н 4,00; для C 35 H 31 O 10 S 2 Sb рассчитано (%): С 52,67; Н 3,89.
Рентгеноструктурный анализ проводили на автоматическом четырехкружном дифрактометре Bruker D8 QUEST (Mo K α -излучение, λ = 0,71073 Å, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [16]. Все расчеты по определению и уточнению структуры выполнены по программам SHELXL/PC [17] и OLEX2 [18]. Структура определена прямым методом и уточнена методом наименьших квадратов в анизотропном приближении для неводородных атомов. Кристаллографические данные и результаты уточнения структуры 1 приведены в таблице.
Кристаллографические данные, параметры эксперимента и уточнения структуры 1
|
Параметр |
1 |
|
Формула |
C 35 H 31 O 10 S 2 Sb |
|
М |
797,47 |
|
Сингония |
Моноклинная |
|
Пространственная группа |
С 2/ с |
|
a , Å |
14,819(9) |
|
b, Å |
15,728(11) |
|
c, Å |
14,707(9) |
|
α, град. |
90,00 |
|
β, град. |
93,00(2) |
|
γ, град. |
90,00 |
|
V , Å3 |
3423(4) |
|
Z |
4 |
|
ρ (выч.), г/см3 |
1,547 |
|
µ , мм–1 |
0,985 |
|
F (000) |
1616,0 |
|
Форма кристалла (размер, мм) |
0,34 × 0,18 × 0,17 |
|
Область сбора данных по 2 θ , град. |
6,84–53,34 |
|
Интервалы индексов отражений |
–18 ≤ h ≤ 16, –16 ≤ k ≤ 19, –17 ≤ l ≤ 18 |
|
Измерено отражений |
6622 |
|
Независимых отражений ( R int ) |
3221 (0,0433) |
|
Переменных уточнения |
222 |
|
GOOF |
1,021 |
|
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0381, wR 2 = 0,0635 |
|
R -факторы по всем отражениям |
R 1 = 0,0605, wR 2 = 0,0703 |
|
Остаточная электронная плотность (min/max), e /Å3 |
0,39/ - 0,53 |
Полные таблицы координат атомов, длин связей и валентных углов соединения 1 депонированы в Кембриджском банке структурных данных (№ 2336248; ; .
Обсуждение результатов
В начале статьи были приведены примеры влияния природы кислоты на структуру продукта в реакциях окислительного присоединения с участием триарилсурьмы. При определении наиболее вероятного строения продукта реакции, несомненно, следует также учитывать роль стерических эффектов [19] в образовании молекул производных пятивалентной сурьмы. Действительно, из рассмотрения возможности существования молекул пентаарильных соединений фосфора, мышьяка, сурьмы и висмута в производных висмута, согласно расчетам [20, 21], не имело места пространственных напряжений, в то время как в аналогичных соединениях сурьмы увеличение объема одного или двух лигандов при центральном атоме металла могло изменить схему реакции, поскольку вызывало в молекуле сурьмаорганического производного стерические затруднения, поэтому мы выбрали в качестве двух большеобъемных лигандов остатки 2-карбоксибензолсульфоновой кислоты. Нами показано, что реакция окислительного присоединения с участием три(пара-толил)сурьмы, пероксида водорода и 2-карбоксибензолсульфоновой кислоты, содержащей в органическом ядре две функциональные группы, протекала по обычной схеме.
p -Tol 3 Sb + 2 HOSO 2 C 6 H 4 (COOH-2) + H 2 O 2 p -Tol 3 Sb[OSO 2 C 6 H 4 (COOH-2] 2 + H 2 O
В ИК-спектре дисульфоната три( пара -толил) сурьмы 1 присутствуют интенсивные полосы поглощения при 1020 и 1186 см-1, относящиеся к валентным колебаниям SO 2 -групп и полоса при 1722 см-1 (С=О), кроме других полос поглощения, характерных для дисульфонатов триарилсурь-мы [5, 24, 25].
По данным рентгеноструктурного анализа, атом сурьмы в соединении 1 имеет искаженную тригонально-бипирамидальную координацию (см. рисунок) с аксиально расположенными аренсульфонатными лигандами (аксиальный угол CSbO составляет 177,96(12) ° ).
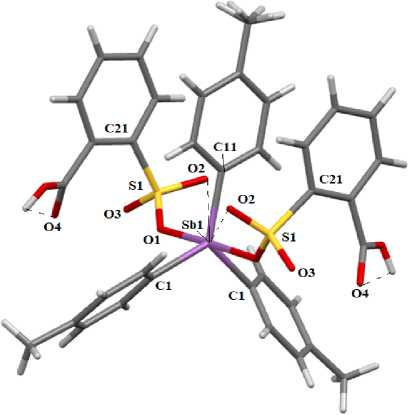
Строение бис (2-карбоксибензолсульфоната) три( пара -толил)сурьмы (1)
Расстояния Sb - C (2,087(5), 2,103(3) А) значительно короче длин связей Sb - О (2,160(3) А), что характерно для тригонально-бипирамидальных комплексов такого типа. Молекула 1 обладает симметрией C2v и имеет ось симметрии 2-го порядка, проходящую через атом металла и атом углерода С(11) одного из арильных лигандов. В кристалле 1 присутствуют контакты центрального атома с атомами кислорода аренсульфонатных групп (Sb∙∙∙OSO 2 С 6 H 4 (COOH-2) 2 3,639(9) Å), что несколько меньше суммы ван-дер-ваальсовых радиусов атомов Sb и S (3,7 Å), поэтому можно говорить о пентагонально-бипирамидальном окружении центрального атома. В кристалле молекулы 1 объединяются в димеры при помощи водородных связей между карбонильными атомами кислорода и атомами водорода соседних карбоксильных групп (расстояния С= O∙∙∙H OC(O) составляют 1,85 Å).
Заключение
Впервые синтезирован с выходом 80 % из три( пара -толил)сурьмы, 2-карбоксибензолсульфоновой кислоты и пероксида водорода в эфире бис (2-карбоксибензолсульфонат) три( пара -толил)сурьмы ( 1 ). Строение комплекса 1 доказано методом рентгеноструктурного анализа. Показано, что схема реакции окислительного присоединения не зависит от наличия карбоксильных групп в кислотных остатках и увеличения объема аренсульфонатных лигандов.

![Синтез и строение Бис(2-карбоксибензолсульфоната) три(пара-толил)сурьмы p-tol3Sb[OSO2C6H4(COOH)-2]2 Синтез и строение Бис(2-карбоксибензолсульфоната) три(пара-толил)сурьмы p-tol3Sb[OSO2C6H4(COOH)-2]2](/file/cover/147248065/sintez-i-stroenie-bis-2-karboksibenzolsulfonata-tri-para-tolil-surmy-p-tol3sb.png)
