Синтез и строение бис(бромдифторацетата) трис(5-бром-2-метоксифенил)висмута
Автор: Ермакова Валентина Андреевна, Шарутина Ольга Константиновна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 2 т.10, 2018 года.
Бесплатный доступ
Взаимодействием трис (5-бром-2-метоксифенил)висмута с бромдифторуксусной кислотой в присутствии пероксида водорода в диэтиловом эфире (мольное соотношение 1:2:1) синтезирован бис (бромдифторацетат) трис (5-бром-2-метоксифенил)висмута (5-Br-2-MeOC6H3)3Bi[OC(O)CBrF2]2 (1), выход которого после перекристаллизации из смеси бензол-петролейный эфир составил 80 %. Использование в качестве окислителя трет -бутилгидропероксида не приводит к образованию целевого продукта. Соединение 1 охарактеризовано методом ИК-спектроскопии и рентгеноструктурного анализа. По данным РСА, в кристалле присутствуют два типа кристаллографически независимых молекул, геометрические характеристики которых незначительно отличаются. Атом висмута в молекуле имеет искаженную тригонально-бипирамидальную координацию с атомами кислорода карбоксилатных заместителей в аксиальных и атомами углерода арильных групп в экваториальных положениях. Углы между аксиальными и экваториальными заместителями ОBi(1,2)O и CBi(1,2)C равны 169,3(5)°, 170,6(7)° и 113,1(8)°-123,5(8)°, 118,1(7)° - 123,1(8)°. Длины связей Bi(1,2)-O и Bi(1,2)-C составляют 2,256(16), 2,276(19) Å; 2,261(14), 2,316(16) Å и 2,15(2)-2,23(2) Å; 2,18(2) -2,19(2) Å. Внутримолекулярные расстояния между валентно не связанными атомами Bi(1,2)⋅⋅⋅O(=C) (3,16(2), 3,57(4) Å; 3,11(2), 3,18(2) Å) и Bi(1,2)⋅⋅⋅OМе (3,00(2)-3,17(2) Å; 3,04(2) - 3,14(2) Å) меньше суммы ван-дер-ваальсовых радиусов атомов элементов Bi и O. Кристаллографические характеристики 1: пространственная группа P 1 ; параметры ячейки: a = 12,775(14) Å, b = 15,999(12) Å, c = 17,196(16) Å; α = 88,09(3) град., β = 68,67(5) град., γ = 87,92(4) град.; V = 3271(5) Å3. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1833279; deposit@ccdc.cam.ac.uk; http://www.ccdc. cam.ac.uk).
Бис(бромдифторацетат) трис(5-бром-2-метоксифенил)висмута, окислительный синтез, молекулярная структура, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147160425
IDR: 147160425 | УДК: 546.87+547.53.024+548.312.5 | DOI: 10.14529/chem180205
Synthesis and structure of tris(5-bromo-2-metoxyphenyl)bismuth bis(bromodifluoroacetate)
The interaction of tris(5-bromo-2-methoxyphenyl)bismuth with bromodifluoroacetic acid in the presence of hydrogen peroxide in diethyl ether at the molar ratio (1: 2: 1) leads to the formation of tris(5-bromo-2-methoxyphenyl)bismuth bis(bromodifluoroacetate) (1) with 80 % yield after recrystallization from the benzene-petroleum ether mixture. The use of tert-butyl hydroperoxide as the oxidizing agent does not lead to the formation of the desired product. Compound 1 is characterized by IR spectroscopy and X-ray diffraction analysis. According to X-ray diffraction data, there are two types of crystallographically independent molecules in the crystal, the geometric characteristics of which differ slightly. The bismuth atom in the molecule has distorted trigonal-bipyramidal coordination with oxygen atoms of carboxylate substituents in axial positions and carbon atoms of the aryl groups at equatorial positions. The angles between the axial and equatorial substituents OBi(1,2)O and CBi(1,2)C are 169.3(5)°, 170.6(7)° and 113.1(8)° -123.5(8)°, 118.1(7)°- 123.1(8)°. The bond lengths of Bi(1,2)-O and Bi(1,2)-C are 2.256(16), 2.276(19) Å; 2.261(14), 2.316(16) Å and 2.15(2)-2.23(2) Å; 2.18(2)- 2.19(2) Å. The intramolecular distances between the valence-free non-bound atoms are Bi(1,2)⋅⋅⋅O(=C) (3.16(2), 3.57(4) Å, 3.11(2), 3.18(2) Å) and Bi(1,2)⋅⋅⋅OMe (3.00(2) - 3.17(2) Å, 3.04(2) - 3.14(2) Å) are less than the sum of the Van-der-Waals radii of Bi and O atoms. Crystallographic characteristics of 1: the space group P 1 ; cell parameters: a = 12.775(14) Å, b = 15.999(12) Å, c = 17.196(16) Å; α = 88.09(3) degrees, β = 68.67(5) degrees, γ = 87.92 (4) degrees; V = 3271 (5) Å3. Full tables of coordinates of atoms, bond lengths and valence angles are deposited at the Cambridge Structural Data Bank (no. 1833279; deposit@ccdc.cam.ac.uk; http: //www.ccdc. Cam.ac.uk).
Текст научной статьи Синтез и строение бис(бромдифторацетата) трис(5-бром-2-метоксифенил)висмута
Взаимодействием трис(5-бром-2-метоксифенил)висмута с бромдифторуксусной кислотой в присутствии пероксида водорода в диэтиловом эфире (мольное соотношение 1:2:1) синтезирован бис(бромдифторацетат) трис(5-бром-2-метоксифенил)висмута (5-Br-2-MeOC6H3)3Bi[OC(O)CBrF2]2 (1), выход которого после перекристаллизации из смеси бензол-петролейный эфир составил 80 %. Использование в качестве окислителя трет-бутилгидропероксида не приводит к образованию целевого продукта. Соединение 1 охарактеризовано методом ИК-спектроскопии и рентгеноструктурного анализа. По данным РСА, в кристалле присутствуют два типа кристаллографически независимых молекул, геометрические характеристики которых незначительно отличаются. Атом висмута в молекуле имеет искаженную тригонально-бипирамидальную координацию с атомами кислорода карбоксилатных заместителей в аксиальных и атомами углерода арильных групп в экваториальных положениях. Углы между аксиальными и экваториальными заместителями ОBi(1,2)O и CBi(1,2)C равны 169,3(5)°, 170,6(7)° и 113,1(8)°–123,5(8)°, 118,1(7)° – 123,1(8)°. Длины связей Bi(1,2)–O и Bi(1,2)–C составляют 2,256(16), 2,276(19) Å; 2,261(14), 2,316(16) Å и 2,15(2)–2,23(2) Å; 2,18(2) –2,19(2) Å. Внутримолекулярные расстояния между валентно не связанными атомами Bi(1,2)-O(=C) (3,16(2), 3,57(4) A; 3,11(2), 3,18(2) А) и Bi(1,2)•••OМe (3,00(2)-3,17(2) A; 3,04(2) - 3,14(2) А) меньше суммы ван-дер-ваальсовых радиусов атомов элементов Bi и O. Кристаллографические характеристики 1: пространственная группа Р1; параметры ячейки: a = 12,775(14) Å, b = 15,999(12) Å, c = 17,196(16) Å; α = 88,09(3) град., β = 68,67(5) град., γ = 87,92(4) град.; V = 3271(5) Å3. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1833279; ; .
В последние годы дикарбоксилаты трифенилвисмута изучают как соединения, обладающие различной биологической активностью[1–6]. Кроме того, эти соединения представляют определенный теоретический интерес, поскольку карбоксилатные заместители могут проявлять свойства как моно-, так и бидентатных лигандов, изменяя координационное число центрального атома. Из арильных соединений висмута наиболее хорошо изучены и широко представлены карбоксилаты трифенилвисмута, в молекулах которых имеются по два тесных внутримолекулярных контакта между атомом висмута и атомами кислорода карбонильных групп Bi---O(=C), приводящих к искажению тригонально-бипирамидальной координации атома висмута, которое проявляется, в основном, в значительном отклонении валентных углов в экваториальной плоскости от теоретического значения [3, 7–13]. Известно, что наиболее эффективным способом синтеза дикарбоксилатов трифенилвисмута являются реакции окислительного присоединения из трифенилвисмута и карбоновой кислоты в диэтиловом эфире в присутствии пероксидов [4–6, 8, 11–14].
Дикарбоксилаты триарилвисмута, содержащие в арильных группах различные заместители, практически не изучены.
В настоящей работе впервые осуществлен синтез и установлены особенности строения бис (бромдифторацетата) трис (5-бром-2-метоксифенил)висмута ( 1 ).
Химия элементоорганических соединений
Экспериментальная часть
Синтез (5-Br-2-MeOC6H3)3Bi[OC(O)CBrF2]2 (1) . К смеси 0,2 г (0,26 ммоль) трис (5-бром-2-метоксифенил)висмута и 0,067 г (0,52 ммоль) бромдифторуксусной кислоты в 30 мл диэтилового эфира добавляли 0,03 мл (0,26 ммоль) 30%-ного водного раствора пероксида водорода. Реакционную смесь оставляли при 20 °C на 24 ч. После испарения растворителя осадок перекристаллизовали из бензола с добавлением петролейного эфира (5:1). Получили 0,255 г (80 %) желтых кристаллов 1 с т. пл. 198 °C.
ИК-спектр, ( ν , см–1): 3083, 3005, 2946, 2843, 1713, 1691, 1579, 1555, 1472, 1441, 1351, 1280, 1252, 1166, 1090, 1031, 1003, 872, 816, 706, 658, 617, 604, 536, 519.
ИК-спектр соединения 1 регистрировали на ИК-Фурье спектрометре Shimadzu IRAffinity-1S; образец готовили таблетированием с KBr (область поглощения 4000–400 см–1).
Рентгеноструктурный анализ (РСА) кристалла 1 проводили на автоматическом четырехкружном дифратктометре D8 QUEST фирмы Bruker (Mo Kα-излучение, λ= 0,71073 Å, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены с помощью программ SMART и SAINT-Plus [15]. Все расчеты по определению и уточнению структур выполнены с помощью программ SHELXL/PC [16] OLEX2 [17]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Кристаллографические данные и результаты уточнения структуры приведены в табл. 1, геометрические характеристики координационного полиэдра атома висмута – в табл. 2. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1833279; ; .
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры 1
|
Параметр |
Значение |
|
М |
1114,93 |
|
Сингония |
триклинная |
|
Пр. группа |
Pl |
|
a, Å |
12,775(14) |
|
b, Å |
15,999(12) |
|
c , Å |
17,196(16) |
|
α, град. |
88,09(3) |
|
β, град. |
68,67(5) |
|
γ, град. |
87,92(4) |
|
V, Å3 |
3271(5) |
|
Z |
2 |
|
ρ(выч.), г/см3 |
2,264 |
|
μ, мм–1 |
11,560 |
|
F (000) |
2072 |
|
Размер кристалла, мм |
0,39 × 0,32 × 0,2 |
|
Область сбора данных по 2θ, град |
5,74° – 47,26° |
|
Интервалы индексов отражений |
–14 ≤ h ≤ 14, –18 ≤ k ≤ 18, –19 ≤ l ≤ 19 |
|
Измерено отражений |
54352 |
|
Независимых отражений |
9793 |
|
R int |
0,0671 |
|
Число уточняемых параметров |
764 |
|
GOOF |
1,028 |
|
R -факторы по F2> 2σ(F2) |
R 1 = 0,0846, wR 2 = 0,2467 |
|
R -факторы по всем отражениям |
R 1 = 0,1121, wR 2 = 0,2743 |
|
Остаточная электронная плотность (min/max), e/Å3 |
8,74/–2,42 |
Таблица 2
Длины связей ( d ) и валентные углы ( ω) в структуре 1
|
Связь |
d , Å |
Угол |
ω, град. |
|
Bi(1)–C(1) |
2,23(2) |
C(1)Bi(1)C(21) |
123,5(8) |
|
Bi(1)–C(11) |
2,149(18) |
C(1)Bi(1)C(11) |
123,2(7) |
|
Bi(1)–C(21) |
2,200(2) |
C(21)Bi(1)C(11) |
113,1(8) |
|
Bi(1)–O(4) |
2,256(16) |
C(1)Bi(1)O(4) |
96,4(7) |
|
Bi(1)–O(6) |
2,276(19) |
C(21)Bi(1)O(4) |
85,7(8) |
|
C(8)–O(4) |
1,26(3) |
C(11)Bi(1)O(4) |
82,3(7) |
|
C(8)–O(5) |
1,18(3) |
C(1)Bi(1)O(6) |
82,0(8) |
|
C(18)–O(6) |
1,20(3) |
C(21)Bi(1)O(6) |
103,0(9) |
|
C(18)–O(7) |
1,22(3) |
C(11)Bi(1)O(6) |
90,8(7) |
|
С(9)–F(1) |
1,40(4) |
O(4)Bi(1)O(6) |
170,6(7) |
|
Bi(2)–C(31) |
2,19(2) |
C(31)Bi(2)C(51) |
123,1(8) |
|
Bi(2)–C(41) |
2,184(16) |
C(31)Bi(2)C(41) |
118,1(7) |
|
Bi(2)–C(51) |
2,189(19) |
C(51)Bi(2)C(41) |
118,7(8) |
|
Bi(2)–O(11) |
2,316(16) |
C(31)Bi(2)O(11) |
88,5(8) |
|
Bi(2)–O(13) |
2,261(14) |
C(51)Bi(2)O(11) |
85,1(7) |
|
C(28)–O(11) |
1,22(3) |
C(41)Bi(2)O(11) |
98,2(6) |
|
C(28)–O(12) |
1,25(3) |
C(31)Bi(2)O(13) |
100,2(8) |
|
C(38)–O(13) |
1,27(2) |
C(51)Bi(2)O(13) |
85,0(7) |
|
C(38)–O(14) |
1,17(3) |
C(41)Bi(2)O(13) |
83,2(6) |
|
C(29)–F(5) |
1,36(3) |
O(11)Bi(2)O(13) |
169,3(5) |
Обсуждение результатов
Синтез бис (бромдифторацетата) трис (5-бром-2-метоксифенил)висмута ( 1 ) осуществляли взаимодействием трис (5-бром-2-метоксифенил)висмута с бромдифторуксусной кислотой в присутствии пероксида водорода в диэтиловом эфире в соотношении (1:2:1 мольн.):
(5-Br-2-MeOC 6 H 3 ) 3 Bi + 2 HOC(O)CBrF 2 + H 2 O 2 →
→ 2 (5-Br-2-MeOC 6 H 3 ) 3 Bi[OC(O)CBrF 2 ] 2 + 2 H 2 O.
Соединение 1 после перекристаллизации из смеси бензол-петролейный эфир представляло собой желтые кристаллы, выделенные с выходом 80 %.
Cинтезированное соединение 1 было исследовано методами ИК-спектроскопии и рентгеноструктурного анализа.
В ИК-спектре соединения 1 наблюдаются интенсивные полосы поглощения, характеризующие колебания карбонильных групп С=О, при 1713 и 1691 см–1. В спектре бромдифторуксусной кислоты полоса расположена в области 1770 см–1, т. е. в спектре соединения 1 наблюдается сдвиг полосы поглощения карбонильной группы в низкочастотную область спектра.
По данным РСА, атом висмута в двух типах кристаллографически независимых молекул 1А и 1Б имеет искаженную тригонально-бипирамидальную координацию с карбоксилатными заместителями в аксиальных положениях (см. рисунок).
Суммы валентных углов в экваториальной плоскости составляют 359,8(8)° в 1А и 359,9(8)° в 1Б (табл. 2). Углы OBiC отклоняются от теоретического значения: 82,0(8)°– 103,0(9)° ( 1А ) и 83,2(6) – 100,2(8)° ( 1Б ). Длины связей Bi–C равны 2,149(18), 2,200(2), 2,230(2) Å ( 1А ) и 2,184(16), 2,189(19), 2,19(2)Å ( 1Б ). Расстояния Bi–O 2,256(16), 2,276(19) Å в 1А и 2,316(16), 2,261(14) в 1Б близки к сумме ковалентных радиусов атомов висмута и кислорода (2,31 Å ) [18]. Аксиальные углы OBiO 170,6(7)° в 1А и 169,3(5) в 1Б несколько отличаются от идеального значения 180°. В соединении 1 карбоксилатные лиганды имеют анизобидентатный характер. Внутримолекулярные расстояния Bi ⋅⋅⋅ O(=С) составляют 3,16(2), 3,57(4) Å в 1А и 3,11(2), 3,18(2) Å в 1Б , что меньше суммы ван-дер-ваальсовых радиусов атомов висмута и кислорода (3,9 Å) [18]. По информации Кембриджского банка структурных данных, внутримолекулярные контакты Bi ⋅⋅⋅ O(=C) в ди-карбоксилатах триарилвисмута изменяются в интервале 2,702 - 3,057 Å [19].
Химия элементоорганических соединений
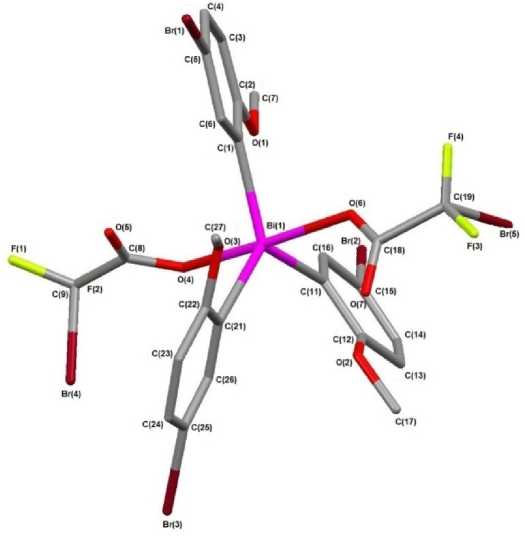
Строение молекулы А соединения 1
Карбоксилатные лиганды в молекулах структурно охарактеризованных дикарбоксилатов триорганилвисмута имеют, как правило, относительно фрагмента BiC3 цис- ориентацию. Наличие внутримолекулярного взаимодействия между атомом висмута и карбонильными атомами кислорода Bi ⋅⋅⋅ O(=C) приводит к значительному искажению валентного угла в экваториальной плоскости со стороны контактов, который может достигать 150° [19]. Однако в молекулах 1 двугранные углы между плоскостями карбоксильных групп достигают 81,99° ( А ) и 62,38° ( Б ), т. е. карбонильные атомы кислорода находятся напротив разных экваториальных углов,и поэтому заметного отклонения их значений от теоретического значения 120° не наблюдается (113,1(8)°, 123,2(7)°, 123,5(8)° в 1А , 118,1(7)°, 118,7(8)°, 123,2(7)° в 1Б ).
Атомы кислорода метоксигрупп координированы с атомом висмута. Расстояния Bi ⋅⋅⋅ OМе равны 3,00(2)–3,17(2) Å и 3,04(2)–3,14(2) Å в 1А и 1Б соответственно. Отметим, что в молекуле трис (2-бром-5-метоксифенил)висмута также имеют место аналогичные контакты (3,020(4), 3,092(4), 3,081(4) Å) [20]. Можно считать, что в молекулах 1А и 1Б атома висмута имеет две координационных сферы с КЧ = 5+5.
Выводы
Установлено, что взаимодействие трис (5-бром-2-метоксифенил)висмута с бромдифторуксусной кислотой в присутствии пероксида водорода в диэтиловом эфире в соотношении (1:2:1 мольн.) приводит к образованию бис (бромдифторацетата) трис (5-бром-2-метоксифенил)висмута. Наличие в молекуле лигандов, имеющих в своем составе атомы кислорода с неподеленными электронными парами, обусловливает дополнительные невалентные внутримолекулярные взаимодействия с атомом висмута и увеличение его КЧ. Особенностью строения бис (бромдифторацетата) трис (5-бром-2-метоксифенил)висмута по сравнению с другими дикар-боксилатами триарилвисмута является уменьшение внутримолекулярного взаимодействия Bi ⋅⋅⋅ O(=C), обусловленное присутствием электроноакцепторных заместителей (F, Br) в радикале R карбоксилатных лигандов, и нетипичная конформация карбоксильных групп.
Выражаем благодарность проф. В.В. Шарутину за проведенные рентгеноструктурные исследования.
Список литературы Синтез и строение бис(бромдифторацетата) трис(5-бром-2-метоксифенил)висмута
- Tiekink, E.R.T. Antimony and Bismuth Compounds in Oncology/E.R.T. Tiekink//Crit. Rev. Oncol./Hematol.-2002. -V. 42, № 3. -P. 217-224 DOI: org/10.1016/S1040-8428(01)00217-7
- Stability and Toxicity of Tris-tolyl Bismuth(V) Dicarboxylates and Their Biological Activity Towards/Y.C. Ong, V.L. Blair, L. Kedzierski et al.//Leishmania Major. Dalton Trans. -2015. -V. 44. -P. 18215-18226 DOI: 10.1039/c5dt03335g
- Comparative Stability, Toxicity and Anti-leishmanial Activity of Triphenyl Antimony(V) and Bismuth(V) α-Hydroxy Carboxylato Complexes/R.N. Duffin, V.L. Blair, L. Kedzierski//Dalton Trans.-2018. -V. 47. -P. 971-980 DOI: 10.1039/C7DT04171C
- Synthesis, Crystal Structures, DNA Interaction and Anticancer Activity of Organobismuth(V) Complexes/L. Cui, C. Bi, Y. Fanet al.//Inorgan. Chim. Acta. -2015. -V. 437, № 1. -P. 41-46 DOI: 10.1016/j.ica.2015.07.008
- Synthesis, Characterization and In Vitro Cytotoxicity Screening of Some Triarylbismuth(V) Di(N-salicylidene)amino Carboxylates and the Crystal Structure of (2-HOC6H4CH=NCH2CO2)2Bi(C6H5)3/G.-C. Wang, J. Xiao, Y.-N. Lu et al.//Appl. Organomet. Chem. -2005. -V. 19, № 1. -P. 113-117 DOI: 10.1002/aoc.749
- Synthesis, Characterization and Cytotoxicity of Some Triarylbismuth(V) Di(N-p-toluenesulfonyl) Aminoacetates and the Crystal Structure of (4-CH3C6H4SO2NHCH2CO2)2Bi(C6H4Cl-4)3/L.Yu, Y.-Q. Ma, G.-C. Wang et al.//Appl. Organomet. Chem. -2004. -V. 18, № 4. -P. 187-190 DOI: 10.1002/aoc.609
- Synthesis and Structural Study of Triphenylbismuth Bis(salicylate)/K. Feham, A. Benkadari, A. Chouaih et al.//Crystal Structure Theory and Applications. -2013. -V. 2, № 1. -P. 28-33 DOI: 10.4236/csta.2013.21004
- Synthesis of Triphenylbismuth(V) Bis(carboxylate) Complexes/I. Kumar, P. Bhattacharya, K.H. Whitmire et al.//Organometallics. -2014. -V. 33, № 11. -P. 2906-2909 DOI: 10.1021/om500337z
- Bis(but-2-enoato-κO)triphenylbismuth(V)/P.V. Andreev, N.V. Somov, O.S. Kalistratova et al.//Acta Crystal. Section E. -2013. -V. 69, № 6. -P. m333 DOI: 10.1107/S1600536813013317
- Особенности строения дикарбоксилатов трифенилвисмута/И.В. Егорова, В.В. Шарутин, Т.К. Иваненко и др.//Коорд. химия. -2006. -Т. 32, № 9. -С. 672-679.
- Синтез и строение бис(фенилкарборанилкарбоксилата) трифенилвисмута/В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина и др.//Журн. общ. химии. -2010. -Т. 80, № 10. -С. 1630-1633.
- Шарутин, В.В. Синтез и строение бис(1-адамантанкарбоксилата) трифенилвисмута/В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина//Журн. неорган. химии. -2011. -Т. 56, № 10. -С. 1644-1646.
- Шарутин, В.В. Синтез и строение бис(пентахлорбензоата)трифенилвисмута/В.В. Шарутин, О.К. Шарутина//Журн. неорган. химии. -2014. -Т. 59, № 6. -С. 734-737 DOI: 10.7868/S0044457X14060208
- Suzuki, H. Organobismuth Chemistry/H. Suzuki. -Amsterdam-London-New York-Oxford-Paris-Shannon-Tokyo, Elsevier, 2001. -619 р.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures From Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: Complete Structure Solution, Refinement and Analysis Program/O.V. Dolomanov, L.J. Bourhis, R.J. Gildea et al.//J. Appl. Cryst. -2009. -V. 42. -P. 339-341.
- Бацанов, С.С. Атомные радиусы элементов/С.С. Бацанов//Журн. неорган. химии. -1991. -Т. 36, № 12. -С. 3015-3037.
- Cambridge Crystallographic Data Center. 2017. (deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
- Шарутин, В.В. Cинтез и cтроение дикарбоксилатов трис(5-бром-2-метоксифенил)висмута: 3Bi2 (Hal = F, Cl)/В.В. Шарутин, О.К. Шарутина, В.А. Ермакова и др.//Журн. неорган. химии. -2017. -Т. 62, № 8. -С. 1049-1056 DOI: 10.7868/S0044457X17080050


