Синтез и строение гидрата бис(2,4-диметилбензолсульфоната) трифенилвисмута
Автор: Шарутин В.В., Сенчурин В.С.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 1 т.16, 2024 года.
Бесплатный доступ
Взаимодействием трифенилвисмута с 2,4-диметилбензолсульфоновой кислотой в присутствии трет-бутилгидропероксида в эфире получен гидрат бис(2,4-диметилбензолсульфоната) трифенилвисмута Ph3Bi(OSO2C6H3Me2-2,4)2∙½ H2O. По данным рентгеноструктурного анализа, проведенного при 293 К на автоматическом четырехкружном дифрактометре D8 Quest Bruker (двухкоординатный CCD-детектор, МоКα-излучение, λ = 0,71073 Å, графитовый монохроматор), кристалла [C34H34O6.5S2Bi, M 819,71: сингония моноклинная, группа симметрии C2/c, параметры ячейки: a = 34,948(16), b = 9,210(5), c = 21,114(9) Å; α = γ = 90,00 град., β = 99,97(2) град.; V = 6693(6) Å3; размер кристалла 0,38 × 0,14 × 0,06 мм; интервалы индексов отражений -45 ≤ h ≤ 45, -11 ≤ k ≤ 11, -27 ≤ l ≤ 27; всего отражений 52257; независимых отражений 7691; GOOF 1,026; R1 = 0,0325, wR2 = 0,0776; остаточная электронная плотность 0,98/-0,82 e/Å3]; атом висмута имеет искаженную тригонально-бипирамидальную координацию. Аксиальный угол OBiO равен 171,58(12)°, сумма углов CBiC в экваториальной плоскости составляет 360°. Длины аксиальных связей Bi-O равны 2,274(3) Å и 2,284(3) Å; интервал изменения длин экваториальных связей Bi-C составляет 2,188(5)-2,209(4) Å. В структуре гидрата бис(2,4-диметилбензолсульфоната) трифенилвисмута присутствуют внутримолекулярные контакты между атомами висмута и кислорода сульфонатных лигандов; расстояния Bi···O=S составляют 3,178(10) и 3,261(10) Å, что меньше суммы ван-дер-ваальсовых радиусов висмута и кислорода (3,59 Å). Молекула воды связана водородной связью с атомом кислорода из сульфонатных лигандов (O-H···O=S 2,50 Å). Полные таблицы координат атомов, длин связей и валентных углов для структуры депонированы в Кембриджском банке структурных данных (№ 1919942, deposit@ccdc.cam.ac.uk, http://www.ccdc. cam.ac.uk).
Трифенилвисмут, 2, 4-диметилбензолсульфоновая кислота, бис(2, 4-диметилбензолсульфонат) трифенилвисмута гидрат, синтез, строение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147243271
IDR: 147243271 | УДК: 546.87+547.47+548.312.5 | DOI: 10.14529/chem240103
Synthesis and structure of triphenylbismuth bis(2,4-dimethylbenzenesulphonate) hydrate
The interaction of triphenylbismuth with 2,4-dimethylbenzenesulfonic acid in diethyl ether in the presence of tert-butyl hydroperoxide have synthesized triphenylbismuth bis(2,4-dimethylbenzenesulfonate) hydrate. The X-ray diffraction pattern has been obtained at 293 K on an automatic diffractometer D8 Quest Bruker (MoKα-radiation, λ = 0.71073 Å, graphite monochromator) of crystals 1 [C34H34O6,5S2Bi, M 819.71, monoclinic syngony, symmetry group C2/c; cell parameters: a = 34.948(16) Å, b = 9.210(5) Å, c = 21.114(9) Å, α = γ = 90.00 degrees, β = 99.97(2) degrees; V = 6693(6) Å3; the crystal size is 0.38 × 0.14 × 0.06 mm; intervals of reflection indexes are -45 ≤ h ≤ 45, -11 ≤ k ≤ 11, -27 ≤ l ≤ 27; total reflections 52257; independent reflections 7691; GOOF 1.026; R1 = 0.0325, wR2 = 0.0776; residual electron density is 0.98/-0.82 e/Å3] the bismuth atom have a distorted trigonal-bipyramidal coordination. The OBiO axial angles are 171.58(12) degrees; the sum of the CBiC angles in the equatorial plane is 360 degrees. The lengths of the Bi-O axial bonds are 2.274(3) Å and 2.284(3) Å; The range of changes in the lengths of the Bi-C equatorial bonds is 2.188(5)-2.209(4) Å. The structure of triphenylbismuth bis(2,4-dimethylbenzenesulfonate) hydrate contains intramolecular contacts between the bismuth and oxygen atoms of the sulfonate ligands; the Bi···O=S distances are 3.178(10) and 3.261(10) Å, which is less than the sum of the Van der Waals radii of bismuth and oxygen (3.59 Å). A water molecule is connected by a hydrogen bond O-H···O=S 2.50 Å with the oxygen atom of the sulfonate ligands. Complete tables of atomic coordinates, bond lengths, and bond angles for the structures were deposited at the Cambridge Crystallographic Data Center (no. 1919942, deposit@ccdc.cam.ac.uk, http://www.ccdc.cam.ac.uk).
Текст научной статьи Синтез и строение гидрата бис(2,4-диметилбензолсульфоната) трифенилвисмута
Аннотация. Взаимодействием трифенилвисмута с 2,4-диметилбензолсульфоновой кислотой в присутствии трет-бутилгидропероксида в эфире получен гидрат бис(2,4-диметил-бензолсульфоната) трифенилвисмута Ph3Bi(OSO2C6H3Me2-2,4)2∙½ H2O. По данным рентгеноструктурного анализа, проведенного при 293 К на автоматическом четырехкружном дифрактометре D8 Quest Bruker (двухкоординатный CCD-детектор, МоКα-излучение, λ = 0,71073 Å, графитовый монохроматор), кристалла [C34H34O6.5S2Bi, M 819,71: сингония моноклинная, группа симметрии C2/c, параметры ячейки: a = 34,948(16), b = 9,210(5), c = 21,114(9) Å; α = γ = 90,00 град., β = 99,97(2) град.; V = 6693(6) Å3; размер кристалла 0,38 × 0,14 × 0,06 мм; интервалы индексов отражений –45 ≤ h ≤ 45, –11 ≤ k ≤ 11, –27 ≤ l ≤ 27; всего отражений 52257; независимых отражений 7691; GOOF 1,026; R1 = 0,0325, wR2 = 0,0776; остаточная электронная плотность 0,98/– 0,82 e/Å3]; атом висмута имеет искаженную тригонально-бипирамидальную координацию. Аксиальный угол OBiO равен 171,58(12)°, сумма углов CBiC в экваториальной плоскости составляет 360°. Длины аксиальных связей Bi-O равны 2,274(3) А и 2,284(3) А; интервал изменения длин экваториальных связей Bi–C составляет 2,188(5)–2,209(4) Å. В структуре гидрата бис(2,4-диметилбензолсульфоната) трифенилвисмута присутствуют внутримолекулярные контакты между атомами висмута и кислорода сульфонатных лигандов; расстояния Bi···O=S составляют 3,178(10) и 3,261(10) Å, что меньше суммы ван-дер-ваальсовых радиусов висмута и кислорода (3,59 Å). Молекула воды связана водородной связью с атомом кислорода из сульфонатных лигандов (O–H···O=S 2,50 Å). Полные таблицы координат атомов, длин связей и валентных углов для структуры депонированы в Кембриджском банке структурных данных (№ 1919942, , .
Достижения в области арильных соединений пятивалентного висмута описаны в обзоре [1] и монографии [2], где преимущественно рассматриваются вопросы синтеза и химического поведения производных Ar4BiX и Ar3BiX2 (где Х – электроотрицательный лиганд). В меньшей степени изучены пентаарильные производные висмута, первым представителем которых является пента-фенилвисмут [3], являющийся прекурсором производных Ar 4 BiX. Действительно, именно из пентафенилвисмута и спирта или кислоты (НХ) можно получить алкокситетрафенилвисмут [4] и другие соединения Ar 4 BiX с электроотрицательным лигандом, среди которых следует выделить термоустойчивые аренсульфонаты тетрафенилвисмута [5–8]. К другим широко известным термоустойчивым производным пятивалентного висмута относят соединения Ph3BiX2 [9–19], также являющиеся прекурсорами в синтезе соединений Ph4BiX, когда последние получают по реакции перераспределения из пентафенилвисмута и Ph 3 BiX 2 .
В настоящей работе рассматривается синтез и особенности строения гидрата бис (2,4-диметилбензолсульфоната) трифенилвисмута, полученного окислением смеси трифенилвисмута и 2,4-диметилбензолсульфоновой кислоты (1:2 мольн.) трет -бутилгидропероксидом.
Экспериментальная часть
Синтез гидрата бис (2,4-диметилбензолсульфоната) трифенилвисмута (1) . Смесь 0,300 г (0,68 ммоль) трифенилвисмута, 0,303 г (1,36 ммоль) 2,4-диметилбензолсульфоновой кислоты и 0,1 мл 70 %-ного водного раствора трет бутилгидропероксида (0,68 ммоль) в 15 мл эфира выдерживали 24 ч при комнатной температуре. Образовавшийся мелкокристаллический продукт перекристаллизовывали из 20 мл смеси бензол – гептан (5 : 1 объемн.). Получили 0,38 г (68 %) неокрашенных кристаллов 1 с т. пл. 169 ° С. ИК-спектр, ( v , см - 1): 3653, 3441, 3418, 3049, 2922, 1624, 1557, 1468, 1437, 1281, 1206, 1167, 1140, 1098, 1069, 1030, 984, 939, 924, 733, 725, 677, 573, 442. Найдено, %: C 49,69; H 4,28. Для C 34 H 34 O 6,5 S 2 Bi вычислено, %: C 49,82; H 4,15.
Элементный анализ выполнен на элементном анализаторе Carlo Erba CHNS-O EA 1108. Температуры плавления измерены на синхронном термоанализаторе Netzsch 449C Jupiter.
ИК-спектр соединения 1 записывали на ИК-Фурье спектрометре Shimadzu IRAffinity-1S в таблетке KBr в области 4000 - 400 см - 1.
Рентгеноструктурный анализ ( РСА ) проводили на автоматическом четырехкружном дифрактометре D8 QUEST фирмы Broker (Mo К а -излучение, X = 0,71073 А, графитовый монохроматор) при 293 K. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены с помощью программ SMART и SAINT-Plus . Все расчеты по определению и уточнению структур выполнены с помощью программ SHELXL/PC и OLEX2
[20‒22]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Положение атомов водорода уточняли по модели наездника ( U изо (H) = 1,2 U экв (C)). Основные кристаллографические данные и результаты уточнения структуры 1 приведены в табл. 1, основные длины связей и валентные углы - в табл. 2.
Taблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры 1
|
Параметр |
Значение |
|
Формула |
C 34 H 34 O 6.5 S 2 Bi |
|
М |
819,71 |
|
Т, К |
293 |
|
Сингония |
Моноклинная |
|
Пр. группа |
C2/c |
|
a, Å |
34,948(16) |
|
b, Å |
9,210(5) |
|
c, Å |
21,114(9) |
|
α,º |
90,00 |
|
β,º |
99,97(2) |
|
γ,º |
90,00 |
|
V, Å3 |
6693(6) |
|
Z |
8 |
|
ρ (выч.), г/см3 |
1,627 |
|
µ , мм - 1 |
5,437 |
|
F(000) |
3240,0 |
|
Размер кристалла (мм) |
0,38 × 0,14 × 0,06 |
|
Область сбора данных по θ , град |
5,6 - 55,32 |
|
Интервалы индексов отражений |
- 45 ≤ h ≤ 45, - 11 ≤ k ≤ 11, - 27 ≤ l ≤ 27 |
|
Измерено отражений |
52257 |
|
Независимых отражений |
7691 |
|
Переменных уточнения |
400 |
|
GOOF |
1,026 |
|
R -факторы по F2> 2 σ (F2) |
R 1 = 0,0325, wR 2 = 0,0689 |
|
R -факторы по всем отражениям |
R 1 = 0,0545, wR 2 = 0,0776 |
|
Остаточная электронная плотность (min/max), e/A3 |
0,98/ - 0,82 |
Таблица 2
Основные длины связей и валентные углы в структуре 1
|
Связь |
Длина, Å |
Угол |
ω , град. |
|
Bi(1) - O(1) |
2,274(3) |
O(1)Bi(1)O(4) |
171,58(12) |
|
Bi(1) - O(4) |
2,284(3) |
C(1)Bi(1)C(11) |
115,39(17) |
|
Bi(1)∙∙∙O(3) |
3,178 |
C(1)Bi(1)C(21) |
109,99(17) |
|
Bi(1)∙∙∙O(5) |
3,261 |
C(11)Bi(1)C(21) |
134,62(17) |
|
Bi(1) - С(1) |
2,209(4) |
O(1)Bi(1)C(1) |
86,16(15) |
|
Bi(1) - С(11) |
2,192(5) |
O(1)Bi(1)C(11) |
91,97(16) |
|
Bi(1) - С(21) |
2,188(5) |
O(1)Bi(1)C(21) |
90,96(16) |
|
S(1) - С(31) |
1,762(6) |
O(4)Bi(1)C(1) |
85,43(15) |
|
O(1) - S(1) |
1,500(4) |
O(4)Bi(1)C(11) |
91,50(15) |
|
S(2) - С(41) |
1,772(4) |
O(4)Bi(1)C(21) |
92,05(16) |
|
O(4) - S(2) |
1,505(3) |
Bi(1)O(1)S(1) |
119,7(2) |
|
Bi(1)O(4)S(2) |
122,30(19 |
Полные таблицы координат атомов, длин связей и валентных углов для структуры 1 депонированы в Кембриджском банке структурных данных (№ 1919942; ; .
Обсуждение результатов
Нами изучено взаимодействие трифенилвисмута с 2,4-диметилбензолсульфоновой кислотой в присутствии трет -бутилгидропероксида, а также структурно охарактеризован целевой продукт.
Реакция протекала по обычной схеме реакции окислительного присоединения с образованием гидрата бис (2,4-диметилбензолсульфоната) трифенилвисмута (1):
-
1. Et 2 O
-
2. бензол/гептан
Ph 3 Bi + 2 HOSO 2 C 6 H 3 Me 2 -2,4∙2H 2 O + t -BuOOH
Ph 3 Bi(OSO 2 C 6 H 3 Me 2 -2,4) 2 ∙½ H 2 O + t -BuOH + 1,5H 2 O 1
По данным РСА, атом висмута в соединении 1 имеет искаженную тригонально-бипирамидальную координацию с аксиально расположенными 2,4-диметилбензолсульфонат-ными лигандами (см. рисунок). Аксиальный угол OBiO равен 171,58(12) ° . Суммы углов CBiC в экваториальной плоскости составляют 360 ° . Длины экваториальных связей Bi-C изменяются в интервале 2,188(5)–2,209(4) Å и имеют близкие значения к суммам ковалентных радиусов атомов висмута и sp2-гибридного углерода 2,21 Å [23]. В молекулах 1 присутствуют внутримолекулярные контакты Bi⋅⋅⋅O=S, которые отличаются друг от друга (3,178 и 3,261 Å) и значительно больше ковалентных связей Bi–O (2,274(3) Å и 2,284(3) Å), однако меньше суммы ван-дер-ваальсовых радиусов атомов висмута и кислорода (3,59 Å) [24]. Это приводит к увеличению одного из экваториальных углов C(11)Bi(1)C(21) со стороны контакта до 134,62(17) ° .
В ИК-спектре соединения 1 полоса поглощения при 442 см - 1 относится к валентным колебаниям связи Bi - С. Колебания v (SO2) в сульфонатных группах характеризуются частотами 1206 см-1 (антисимметричные) и 1030 см–1 (симметричные). Гидратная молекула воды проявляется в спектре полосами при 3653, 3441 и 3419 см - 1 [25].
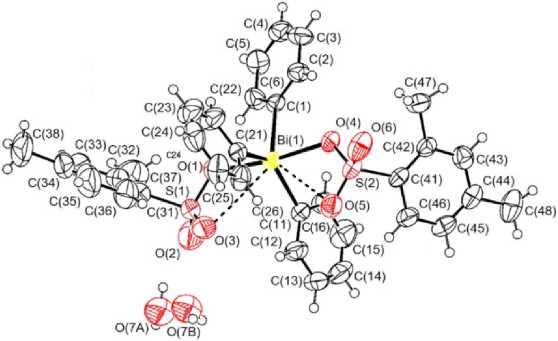
Общий вид гидрата бис(2,4-диметилбензолсульфоната) трифенилвисмута (1)
Структурная организация в кристалле обусловлена слабыми межмолекулярными водородными связями типа С–H···O=S 2,52 и 2,56 Å, что близко к сумме ван-дер-ваальсовых радиусов атомов кислорода и водорода (2,62 Å) [24]. Молекула воды связана водородной связью O(7)– H(7)···O(3)=S(1) 2,50 Å с атомом кислорода О(3) одного из сульфонатных лигандов.
Выводы
Установлено, что взаимодействие трифенилвисмута с 2,4-диметилбензолсульфоновой кислотой в присутствии трет -бутилгидропероксида приводит к образованию гидрата бис (2,4-диметилбензолсульфоната) трифенилвисмута (1). 2,4-Диметилбензолсульфонатные лиганды, имеющие атомы кислорода с неподеленными электронными парами, обусловливают дополнительные невалентные внутримолекулярные взаимодействия с атомом висмута, что сопровождается увеличением КЧ центрального атома до 7.
Список литературы Синтез и строение гидрата бис(2,4-диметилбензолсульфоната) трифенилвисмута
- Шарутин В.В., Поддельский А.И., Шарутина О.К. // Коорд. химия. 2021. Т. 47, № 12. С. 719. DOI: 10.31857/S0132344X21120021.
- Кочешков К.А. Методы элементоорганической химии / К.А. Кочешков, А.П. Сколдинов, Н.Н. Землянский // Сурьма, висмут. - М.: Наука, 1976. - 483 с.
- Wittig G., ClaußK. // Lieb. Ann. 1952. Bd. 578, № 1. P. 136. DOI: 10.1002/jlac.19525780116.
- Разуваев Г.А., Осанова Н.А., Шарутин В.В. // Докл. АН СССР. 1975. Т. 225, № 3. С. 581.
- Шарутин В.В., Егорова И.В., Иваненко Т.К. и др. // Коорд. химия. 2003. Т. 29, № 7. С. 502. EDN: OOFOYX.
- Шарутин В.В., Пакусина А.П., Егорова И.В. и др. // Коорд. химия. 2003. Т. 29, № 5. С. 336. EDN: OOFOOD.
- Шарутин В.В., Егорова И.В., Пакусина А.П. и др. // Коорд. химия. 2007. Т. 33, № 3. С. 176. EDN: IADDTV.
- Рыбакова А.В. // Вестник ЮУрГУ. Серия «Химия». 2022. Т. 14, № 1. С. 32. DOI: 10.14529/chem220104.
- Rüther R., Huber F., Preut H. // Z. anorg. allg. Chem. 1986. V. 539, no. 8. P. 110. DOI: 10.1002/zaac.19865390811.
- Goswami M., Ellern A., Pohl N.L.B. // Angew. Chem. Int. Ed. 2013. V. 52, no. 32. P. 8441. DOI: 10.1002/anie.201304099.
- Шарутин В.В., Шарутина О.К., Сенчурин В.С. // Журн. неорган. химии. 2016. Т. 61, № 3. С. 334. DOI: 10.7868/S0044457X16030211.
- Robertson A.P.M., Budford N., McDonaid R., Ferduson M.J. // Angew. Chem. Int. Ed. 2014, V. 53. P. 3480. DOI: 10.1002/anie.201310613.
- Механошина Е.С., Рыбакова А.В., Шарутин В.В. // Вестник ЮУрГУ. Серия «Химия». 2022. Т. 14, № 3. С. 51. DOI: 10.14529/chem220306.
- Ермакова В.А. // Вестник ЮУрГУ. Серия «Химия». 2017. Т. 9, № 3. С. 65. DOI: 10.14529/chem170308.
- Шарутин В.В., Егорова И.В., Циплухина Т.В. и др. // Коорд. химия. 2004. Т. 30, № 12. С. 935. EDN: OVZTIH.
- Шарутин В.В., Егорова И.В., Циплухина Т.В. // Журн. общ. химии. 2004. Т. 74, № 2. С. 343. EDN: PBCSBH.
- Шарутин В.В., Шарутина О.К., Сенчурин В.С. // Журн. структ. химии. 2020. Т. 61, № 5. С. 776. DOI: 10.26902/JSC_id55423.
- Шарутин В.В., Шарутина О.К., Сенчурин В.С. // Журн. неорган. химии. 2020. Т. 65, № 11. С. 1516. DOI: 10.31857/S0044457X20110173.
- Сенчурин В.С., Шарутин В.В., Шарутина О.К. // Журн. неорган. химии. 2020. Т. 65, № 3. С. 320. DOI: 10.31857/S0044457X20030125.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures from Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Cryst. 2009. Vol. 42. P. 339. DOI: 10.1107/S0021889808042726.
- Cordero B., Gómez V., Platero-Prats A.E. et al. // Dalton Trans. 2008. V. 21. P. 2832. DOI: 10.1039/B801115J.
- Mantina M., Chamberlin A.C., Valero R. et al. // J. Phys. Chem. A. 2009. V. 113, №. 19. P. 5806. DOI: 10.1021/jp811155623.
- Тарасевич Б.Н. ИК-спектры основных классов органических соединений. М.: МГУ, 2012. 54 с.


