Синтез и строение комплексов палладия, платины и золота: [Ph3PCH2CH2PPh3]2+ [PdCl3DMSO]-2, [Ph3PCH2CH2PPh3]2+ [PtCl6]2- · 4 DMSO, [Ph3PCH2CH2PPh3]2+ [AuCl4]-2 и [Ph3PCH2CH2PPh3]2+ [AuCl2]-2
Автор: Шарутин Владимир Викторович, Сенчурин Владислав Станиславович, Шарутина Ольга Константиновна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 33 (250), 2011 года.
Бесплатный доступ
Взаимодействием дихлорида бис-1,2-трифенилфосфинэтилена с хлоридом палладия (II) (1:2 мольн.), гексахлороплатиноводородной кислотой (1:1 мольн.) в диметилсульфоксиде, а также золотохлористоводородной кислотой (1:2 мольн.) в ацетоне и диметилсульфоксиде синтезированы комплексы [Ph3PCH2CH2PPh3]2+ [PdCl3DMSO]-2 (I), [Ph3PCH2CH2PPh3]2+ [PtCl6]2- · 4 DMSO (II), [Ph3PCH2CH2PPh3]2+[AuCl4]-2 (III) и [Ph3PCH2CH2PPh3]2+[AuCl2]-2 (IV) соответственно. Атомы фосфора катионов комплексов I-IV, по данным РСА, имеют мало искаженную тетраэдрическую координацию (углы CPC 106,24(9)-113,74(10)°), длины связей P-С составляют 1,779(6)-1,828(6) A. В плоскоквадратных анионах комплекса (I) (углы SPdCl 87,16(2), 92,554(19)°, ClPdCl 89,45(2), 90,95(2)°) координационная связь между атомом палладия и диметилсульфоксидным лигандом осуществляется через атом серы (Pd-S 2,2508(6) A), длины связей Pd-Cl изменяются в интервалах 2,3019(5)-2,3218(6) A. Атомы платины в анионах комплекса (I,I) гексакоординированы (углы ClPtCl 89,19(6)-91,45(6)°), длины связей Pt-Cl равны 2,3028(13)-2,3252(11) A. Квадратная координация катиона золота в III мало искажена: углы ClAuCl равны 88,68(7)-90,80(7)°, длины связей Au-Cl составляют 2,2691(18)-2,2934(19) A. В практически линейных анионах IV (углы ClAuCl 177,46(4) и 178,96(4)°) длины связей Au-Cl изменяются в интервале 2,2385(10)-2,2557(11) A.
Синтез, строение, комплексы, палладий, платина, золото
Короткий адрес: https://sciup.org/147160203
IDR: 147160203 | УДК: 547.53.024+546.924+546.98+546.185+546.591+546.593
Synthesis and structure of palladium, platinum and gold complexes: [Ph3PCH2CH2PPh3]2+ [PdCl3DMSO]-2, [Ph3PCH2CH2PPh3]2+ [PtCl6]2- · 4 DMSO, [Ph3PCH2CH2PPh3]2+ [AuCl4]-2 и [Ph3PCH2CH2PPh3]2+ [AuCl2]-2
The reaction of dichloride bis-1,2-triphenylphosphinetylene with palladium(II) chloride (1:2 mol.), hydrohexachloroplatinum acid (1:1 mol.) in dimethylsulfoxide, and hydrochloroauric acid (1:2 mol.) in acetone and dimethylsulfoxide has synthesized the complexes [Ph3PCH2CH2PPh3]2+[PdCl3DMSO]-2 (I), [Ph3PCH2CH2PPh3]2+[PtCl6]2-·4DMSO (II), [Ph3PCH2CH2PPh3]2+[AuCl4]-2 (III) and [Ph3PCH2CH2PPh3]2+[AuCl2]-2 (IV), respectively. Phosphorus atoms of the cations of complexes I-IV, according to the X-ray diffraction analysis, have a slightly distorted tetrahedral coordination (CPC angles are 106.24(9)-113.74(10)°), the P-C bond lengths are 1.779(6)-1.828(6) A. In the planar complex anions of the complex (I) (SPdCl angles are 87.16(2), 92.554(19)°, ClPdCl angles are 89.45(2), 90.95(2)°) the coordination bond between palladium and dimethylsulfoxide ligand results through the sulfur atom (Pd-S 2.2508(6) A), Pd-Cl bond lengths are in the range 2.3019(5)-2.3218(6) A. Platinum atoms in the anions of the complex (II) have an octahedral coordination (ClPtCl angles are 89.19(6)-91.45(6)°), Pt-Cl bond lengths are 2.3028(13)-2.3252(11) A. The square coordination of the gold cation in III is but little distorted: ClAuCl angles are equal to 88.68(7)-90.80(7)°, Au-Cl bond lengths are 2.2691(18)-2.2934(19) A. In the virtually linear anion IV (ClAuCl angles are 177.46(4) and 178.96(4)°) Au-Cl bond lengths vary in the range 2.2385(10)-2.2557(11) A.
Текст научной статьи Синтез и строение комплексов палладия, платины и золота: [Ph3PCH2CH2PPh3]2+ [PdCl3DMSO]-2, [Ph3PCH2CH2PPh3]2+ [PtCl6]2- · 4 DMSO, [Ph3PCH2CH2PPh3]2+ [AuCl4]-2 и [Ph3PCH2CH2PPh3]2+ [AuCl2]-2
Синтез и строение комплексных соединений с палладий-, платина- и золотосодержащими анионами и моноядерными катионами типа [R 4 E]+ (R = Alk, Ar; E = Sb, P) описаны в литературе [1–3], однако, подобные комплексы с биядерными катионами неизвестны. Настоящая работа посвящена получению и установлению особенностей строения комплексов палладия, платины и золота с би-ядерным двухзарядным катионом [Ph 3 PCH 2 CH 2 PPh 3 ]2+: [Ph 3 PCH 2 CH 2 PPh 3 ]2+[PdCl 3 DMSO]– 2 ( I ), [Ph 3 PCH 2 CH 2 PPh 3 ]2+[PtCl 6 ]2– ∙ 4 DMSO ( II ), [Ph 3 PCH 2 CH 2 PPh 3 ]2+[AuCl 4 ]– 2 ( III ) и
[Ph 3 PCH 2 CH 2 PPh 3 ]2+[AuCl 2 ]– 2 ( IV ).
Экспериментальная часть
Синтез [Ph 3 PCH 2 CH 2 PPh 3 ] 2+ [PdCl 3 DMSO] –2 (I). Смесь 0,21 г (0,34 ммоль) дихлорида бис -1,2-трифенилфосфинэтилена и 0,12 г (0,68 ммоль) хлорида палладия (II) растворяли при перемешивании в 5 мл диметилсульфоксида. Раствор концентрировали, образовавшиеся красно-желтые игольчатые кристаллы фильтровали и сушили. Получили 0,29 г (76 %) комплекса I с т. разл. 218 ° С. ИК-спектр ( v , см-1): 423, 443, 488, 502, 525, 686, 732, 737, 910, 932, 997, 1021, 1113, 1231, 1288, 1307, 1435, 1437, 1582, 2902, 2932, 2944, 2983, 3018, 3059, 3081.
Найдено, %: С 44,27; Н 3,98.
Для C 42 H 46 O 2 S 2 P 2 Pd 2 Cl 6
вычислено, %: С 44,45; Н 4,06.
Синтез [Ph3PCH2CH2PPh3]2+ [PtCl6]2– ∙ 4 DMSO (II). Смесь 0,13 г (0,21 ммоль) дихлорида бис-1,2-трифенилфосфинэтилена и 0,12 г (0,21 ммоль) гидрата гексахлороплатиноводородной кислоты H2PtCl6∙9H2O растворяли при перемешивании в 5 мл диметилсульфоксида. Раствор кон- центрировали, образовавшиеся неокрашенные призматические кристаллы фильтровали и сушили. Получили 0,23 г (87 %) комплекса II с т. разл. 184°С. ИК-спектр (v, см-1): 450, 484, 509, 525, 689, 726, 740, 954, 996, 1034, 1112, 1142, 1224, 1311, 1438, 1486, 1585, 2907, 2932, 2991, 3057.
Найдено, %: С 43,34; Н 4,76.
Для C 46 H 58 O 4 S 4 P 2 PtCl 6
вычислено, %: С 43,40 Н 4,56.
Синтез [Ph 3 PCH 2 CH 2 PPh 3 ]2+ [AuCl 4 ]– 2 (III). Смесь 0,18 г (0,29 ммоль) дихлорида бис -1,2-трифенилфосфинэтилена и 0,26 г (0,58 ммоль) гидрата золотохлористоводородной кислоты HAuQ^6H2O в 15 мл ацетона выдерживали при 20 ° С в течение 24 ч. Образовавшиеся желтые игольчатые кристаллы фильтровали и сушили. Получили 0,32 г (90 %) комплекса III с т. разл. 216 ° С. ИК-спектр ( v , см-1): 458, 486, 506, 524, 685, 726, 734, 742, 997, 1111, 1133, 1163, 1192, 1209, 1319, 1337, 1434, 1438, 1484, 1585, 2917, 2954, 3028, 3061, 3091.
Найдено, %: С 36,84; Н 2,89.
Для C 38 H 34 P 2 Au 2 Cl 8
вычислено, %: С 37,07; Н 2,76.
Синтез [Ph 3 PCH 2 CH 2 PPh 3 ]2+ [AuCl 2 ]– 2 (IV). 0,10 г (0,08 ммоль) комплекса III растворяли при перемешивании в 5 мл диметилсульфоксида. Раствор концентрировали, образовавшиеся неокрашенные кристаллы фильтровали и сушили. Получили 0,07 г (80 %) комплекса IV с т. разл. 210 ° С. ИК-спектр ( v , см-1): 458, 486, 506, 524, 684, 726, 734, 742, 997, 1111, 1133, 1163, 1192, 1210, 1321, 1338, 1384, 1434, 1438, 1484, 1585, 2917, 2954, 3028, 3062, 3091.
Найдено, %: С 41,87; Н 3,23.
Для C 38 H 34 P 2 Au 2 Cl 4
вычислено, %: С 41,91; Н 3,13.
ИК-спектры комплексов I–IV снимали на ИК-Фурье-спектрометре 1201 в таблетках KBr.
Рентгеноструктурный анализ (РСА) кристаллов I, III выполнен на автоматическом дифрактометре Bruker AXS Smart Apex (Mo К а -излучение, X 0,71073 А, графитовый монохроматор), кристаллов II – на дифрактометре Oxford Gemini R Ultra (источник излучения Enhance Ultra, детектор Ruby) с использованием медного анода. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Сбор, редактирование данных, уточнение параметров элементарной ячейки и учет поглощения проведены по программам SMART и SAINT- Plus [4]. Все расчеты по определению и уточнению структур выполнены по программам SHELXL/PC [5]. Кристалл IV снимали на дифрактометре Xcalibur, Sapphire3, Gemini S (Mo К а -излучение, X =0,71073 А, режим работы трубки 50/40 кВ/мА, графитовый монохроматор). Поглощение учтено численно по форме кристалла [6]. Структура расшифрована прямым методом и уточнена полноматричным МНК в анизотропном для неводородных атомов приближении (SHELX-97, WinGX) [7]. Основные кристаллографические данные и результаты уточнения структур I–IV приведены в табл. 1, основные длины связей и валентные углы – в табл. 2.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структур комплексов I–IV
|
Параметр |
Значение |
|||
|
I |
II |
III |
IV |
|
|
1 |
2 |
3 |
4 |
5 |
|
Т , К |
100 |
123,0(2) |
150 |
298(2) |
|
Сингония |
Моноклинная |
Моноклинная |
Ромбическая |
Моноклинная |
|
Пр. группа |
C 2 /c |
P 2 1 / c |
P 2 1 2 1 2 1 |
P 2 1 / c |
|
a , Å |
27,7973(5) |
11,64770(10) |
10,9601(7) |
9,11044(19) |
|
b , Å |
8,9015(2) |
21,7707(2) |
12,2248(9) |
21,6118(5) |
|
c, Å |
19,8630(4) |
21,3965(2) |
30,2467(17) |
19,4284(4) |
|
а ,град |
90 |
90 |
90 |
90 |
|
β, град |
117,7550(10) |
100,9730(10) |
90 |
98,2477(18) |
|
Y , град |
90 |
90 |
90 |
90 |
Окончание табл. 1
|
1 |
2 |
3 |
4 |
5 |
|
V , Å3 |
4349,38(15) |
5326,50(8) |
4052,6(5) |
3785,76(13) |
|
Z |
4 |
4 |
4 |
8 |
|
р (выч.), г/см 3 |
1,732 |
1,587 |
2,016 |
1,909 |
|
–1 ц , мм |
1,402 |
10,053 |
7,867 |
8,135 |
|
F (000) |
2280 |
2560 |
2344 |
2072 |
|
Размер кристалла, мм |
0,15 x 0,22 x 0,25 |
0,16 x 0,15 x 0,14 |
0,20 x 0,40 x 0,40 |
0,12 x 0,18 x 0,16 |
|
Область сбора данных по 0 ,град |
2,32–31,39 |
3,87–73,16 |
2,14–30,68 |
3,43–30,51 |
|
Интервалы индексов отражений |
-34 < h < 33, -11 < к < 12, -14 < l < 26 |
-14 < h < 13, -26 < к < 26, -24 < l < 26 |
-15 < h < 9, -8 < к < 16, -35 < l < 42 |
–13 ≤ h ≤ 8 –30 ≤ k ≤ 30 –26 ≤ l ≤ 27 |
|
Измерено отражений |
12740 |
22688 |
16279 |
36854 |
|
Независимых отражений |
5287 |
10414 |
9524 |
11506 |
|
R int |
0,0235 |
0,0367 |
0,0359 |
0,0617 |
|
Переменных уточнения |
255 |
597 |
451 |
415 |
|
GOOF |
1,039 |
1,002 |
0,885 |
0,678 |
|
R -факторы по F 2 > 2 о ( F 2 ) |
R 1 = 0,0265 wR 2 = 0,0641 |
R 1 = 0,0417 wR 2 = 0,1092 |
R 1 = 0,0367 wR 2 = 0,0734 |
R 1 = 0,0313 wR 1 = 0,0465 |
|
R -факторы по всем отражениям |
R 1 = 0,0322 wR 2 = 0,0669 |
R 1 = 0,0553 wR 2 = 0,1145 |
R 1 = 0,0450 wR 2 = 0,0763 |
R 1 = 0,1204 wR 1 = 0,0531 |
|
Остаточная электронная плотность (min/max), e / A 3 |
–0,989 / 0,573 |
–0,881 / 1,740 |
–1,468 / 2,245 |
–0,906/0,466 |
Таблица 2
Основные длины связей ( d) и валентные углы ( ш ) в структурах I-IV
|
Связь |
d , Å |
Угол |
ш ,град |
|
1 |
2 |
3 |
4 |
|
I |
|||
|
Pd(1)–S(1) |
2,2508(6) |
S(1)Pd(1)Cl(1) |
87,16(2) |
|
Pd(1)–Cl(1) |
2,3144(5) |
S(1)Pd(1)Cl(2) |
175,37(2) |
|
Pd(1)–Cl(2) |
2,3218(6) |
S(1)Pd(1)Cl(3) |
92,554(19) |
|
Pd(1)–Cl(3) |
2,3019(5) |
Cl(1)Pd(1)Cl(2) |
89,45(2) |
|
S(1)–O(1) |
1,4752(16) |
Cl(3)Pd(1)Cl(1) |
177,86(2) |
|
S(1)–C(1) |
1,771(2) |
Cl(3)Pd(1)Cl(2) |
90,95(2) |
|
S(1)–C(2) |
1,778(2) |
O(1)S(1)Pd(1) |
113,55(7) |
|
P(1)–C(3) |
1,820(2) |
O(1)S(1)C(1) |
108,33(11) |
|
P(1)–C(11) |
1,798(2) |
O(1)S(1)C(2) |
107,11(11) |
|
P(1)–C(21) |
1,790(2) |
C(1)S(1)Pd(1) |
111,66(8) |
|
P(1)–C(31) |
1,795(2) |
C(1)S(1)C(2) |
100,19(11) |
|
Преобразования симметрии #1) – x +1, y , – z +3/2 |
|||
|
II |
|||
|
Pt(1)–Cl(6) |
2,3028(13) |
Cl(6)Pt(1)Cl(1) |
178,32(7) |
|
Pt(1)–Cl(1) |
2,3060(16) |
Cl(6)Pt(1)Cl(4) |
89,19(6) |
|
Pt(1)–Cl(4) |
2,3096(14) |
Cl(1)Pt(1)Cl(4) |
89,49(8) |
|
Pt(1)–Cl(2) |
2,3179(13) |
Cl(6)Pt(1)Cl(2) |
91,45(6) |
|
Pt(1)–Cl(3) |
2,3220(12) |
Cl(1)Pt(1)Cl(2) |
89,87(8) |
|
Pt(1)–Cl(5) |
2,3252(11) |
Cl(4)Pt(1)Cl(2) |
179,16(6) |
|
P(1)–C(31) |
1,790(5) |
Cl(6)Pt(1)Cl(3) |
89,66(5) |
|
P(1)–C(11) |
1,793(5) |
Cl(1)Pt(1)Cl(3) |
89,30(6) |
|
P(1)–C(21) |
1,799(5) |
Cl(4)Pt(1)Cl(3) |
90,17(5) |
Окончание табл. 2
|
1 |
2 |
3 |
4 |
|
P(1)–C(1) |
1,810(4) |
Cl(2)Pt(1)Cl(3) |
90,38(5) |
|
P(2)–C(51) |
1,787(5) |
Cl(6)Pt(1)Cl(5) |
90,29(5) |
|
P(2)–C(61) |
1,797(5) |
Cl(1)Pt(1)Cl(5) |
90,75(6) |
|
P(2)–C(41) |
1,801(4) |
Cl(4)Pt(1)Cl(5) |
89,58(5) |
|
P(2)–C(2) |
1,803(4) |
Cl(2)Pt(1)Cl(5) |
89,87(5) |
|
S(1)–O(1S) |
1,495(4) |
Cl(3)Pt(1)Cl(5) |
179,74(5) |
|
III |
|||
|
Au(1)–Cl(1) |
2,279(2) |
Cl(1)Au(1)Cl(3) |
178,88(9) |
|
Au(1)–Cl(2) |
2,2691(18) |
Cl(1)Au(1)Cl(4) |
90,39(8) |
|
Au(1)–Cl(3) |
2,2856(19) |
Cl(2)Au(1)Cl(1) |
90,56(8) |
|
Au(1)–Cl(4) |
2,2901(17) |
Cl(2)Au(1)Cl(3) |
89,15(8) |
|
Au(2)–Cl(5) |
2,2934(19) |
Cl(2)Au(1)Cl(4) |
179,01(8) |
|
Au(2)–Cl(6) |
2,2817(17) |
Cl(3)Au(1)Cl(4) |
89,90(7) |
|
Au(2)–Cl(7) |
2,278(2) |
Cl(6)Au(2)Cl(5) |
90,38(7) |
|
Au(2)–Cl(8) |
2,2764(16) |
Cl(7)Au(2)Cl(5) |
177,93(7) |
|
P(1)–C(1) |
1,828(6) |
Cl(7)Au(2)Cl(6) |
90,26(7) |
|
P(1)–C(11) |
1,784(6) |
Cl(8)Au(2)Cl(5) |
90,80(7) |
|
P(1)–C(21) |
1,812(7) |
Cl(8)Au(2)Cl(6) |
176,42(7) |
|
P(1)–C(31) |
1,792(6) |
Cl(8)Au(2)Cl(7) |
88,68(7) |
|
P(2)–C(2) |
1,808(6) |
C(11)P(1)C(1) |
110,3(3) |
|
P(2)–C(41) |
1,795(6) |
C(11)P(1)C(21) |
110,5(3) |
|
P(2)–C(51) |
1,787(7) |
C(21)P(1)C(1) |
107,1(3) |
|
P(2)–C(61) |
1,798(7) |
C(31)P(1)C(1) |
109,2(3) |
|
IV |
|||
|
Au(1)–Cl(2) |
2,2502(11) |
Cl(2)Au(1)Cl(1) |
177,46(4) |
|
Au(1)–Cl(1) |
2,2557(11) |
Cl(3)Au(2)Cl(4) |
178,96(4) |
|
Au(2)–Cl(3) |
2,2385(10) |
C(36)P(1)C(28) |
108,69(12) |
|
Au(2)–Cl(4) |
2,2501(9) |
C(36)P(1)C(25) |
112,74(14) |
|
P(1)–C(36) |
1,781(3) |
C(28)P(1)C(25) |
109,38(13) |
|
P(1)–C(28) |
1,792(3) |
C(36)P(1)C(27) |
106,24(13) |
|
P(1)–C(25) |
1,795(3) |
C(28)P(1)C(27) |
110,71(13) |
|
P(1)–C(27) |
1,810(3) |
C(25)P(1)C(27) |
109,07(12) |
|
P(2)–C(21) |
1,779(3) |
C(21)P(2)C(26) |
109,83(12) |
|
P(2)–C(26) |
1,783(3) |
C(21)P(2)C(24) |
109,50(12) |
|
P(2)–C(24) |
1,794(3) |
C(26)P(2)C(24) |
108,66(12) |
|
P(2)–C(20) |
1,815(3) |
C(21)P(2)C(20) |
109,33(12) |
|
C(26)P(2)C(20) |
109,19(12) |
||
Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 828022, 828023, 824491, 823545; ; .
Результаты и их обсуждение
C целью получения новых комплексов палладия, платины и золота, содержащих биядерный фосфониевый катион, нами были исследованы реакции дихлорида бис -1,2-трифенил-фосфинэтилена с хлоридом палладия (II), гексахлороплатиноводородной и золотохлористоводородной кислотами.
Мы установили, что взаимодействие дихлорида бис -1,2-трифенилфосфинэтилена с хлоридом палладия (II) (1:2 мольн.) в диметилсульфоксиде протекает с формированием аниона, в котором одним из лигандов выступает молекула DMSO, и приводит к образованию красно-желтых игольчатых кристаллов трихлоро(диметилсульфоксидо)палладата бис -1,2-трифенилфосфинэтилена [Ph 3 PCH 2 CH 2 PPh 3 ]2+ [PdCl 3 DMSO]– 2 (I):
DMSO
[Ph 3 PCH 2 CH 2 PPh 3 ]2+Cl 2 – + 2 PdCl 2 → [Ph 3 PCH 2 CH 2 PPh 3 ]2+ [PdCl 3 DMSO ]– 2
I
К синтезу комплекса II, представленного неокрашенными призматическими кристаллами, приводила реакция дихлорида бис -1,2-трифенилфосфинэтилена с гексахлороплатиноводородной кислотой (1:1 мольн.):
DMSO
[Ph 3 PCH 2 CH 2 PPh 3 ]2+Cl 2 – + H 2 PtCl 6 → [Ph 3 PCH 2 CH 2 PPh 3 ]2+ [PtCl 6 ]2–∙4DMSO + 2HCl
II
Следует отметить, что часто, реакции комплексообразования, проводимые в диметилсульфоксиде, сопровождаются обменом лигандов с вхождением в координационную сферу катиона платины молекулы DMSO [8], однако в приведенной выше реакции этого не происходит.
Продуктом взаимодействия дихлорида бис -1,2-трифенилфосфинэтилена с золотохлористоводородной кислотой в ацетоне (1:2 мольн.) являлись игольчатые кристаллы желтого цвета комплекса III:
(Ме) 2 СО
[Ph 3 PCH 2 CH 2 PPh 3 ]2+Cl 2 – + 2 HAuCl 4 → [Ph 3 PCH 2 CH 2 PPh 3 ]2+ [AuCl 4 ]– 2 + 2 HCl
III
Перекристаллизация комплекса III из диметилсульфоксида протекала с понижением степени окисления золота и приводила к образованию комплекса [Ph 3 PCH 2 CH 2 PPh 3 ]2+[AuCl 2 ]– 2 (IV). Следует отметить, что редокс-реакции между ионами переходных металлов в высоких степенях окисления и серасодержащими органическими реагентами известны. Так, процесс восстановления соединений Au(III) тиоэфирами используется в препаративной координационной химии для получения комплексов Au(I).
По данным РСА, атомы фосфора катионов бис -1,2-трифенилфосфинэтилена комплексов I–IV имеют слабо искаженное тетраэдрическое окружение (рис. 1–4).
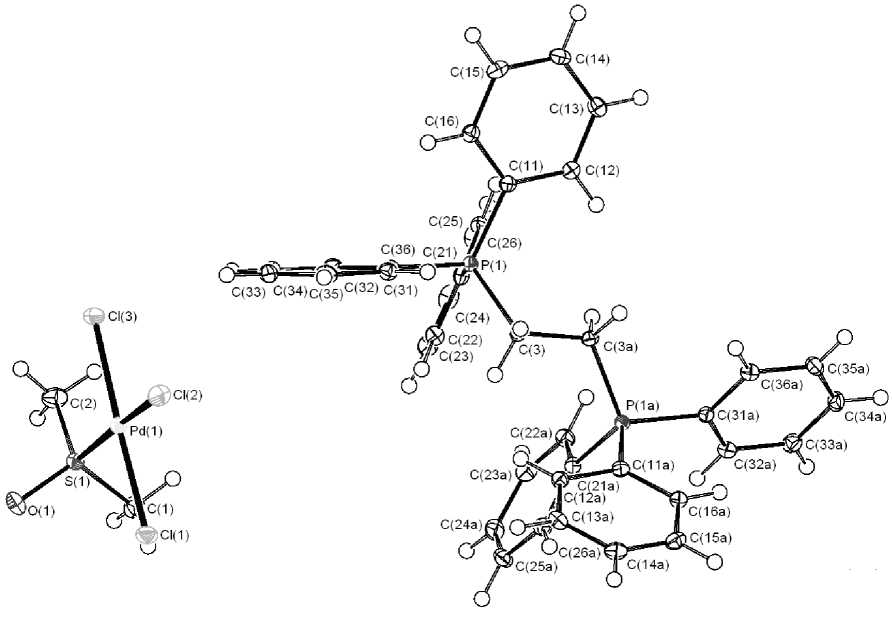
Рис. 1. Строение комплекса I
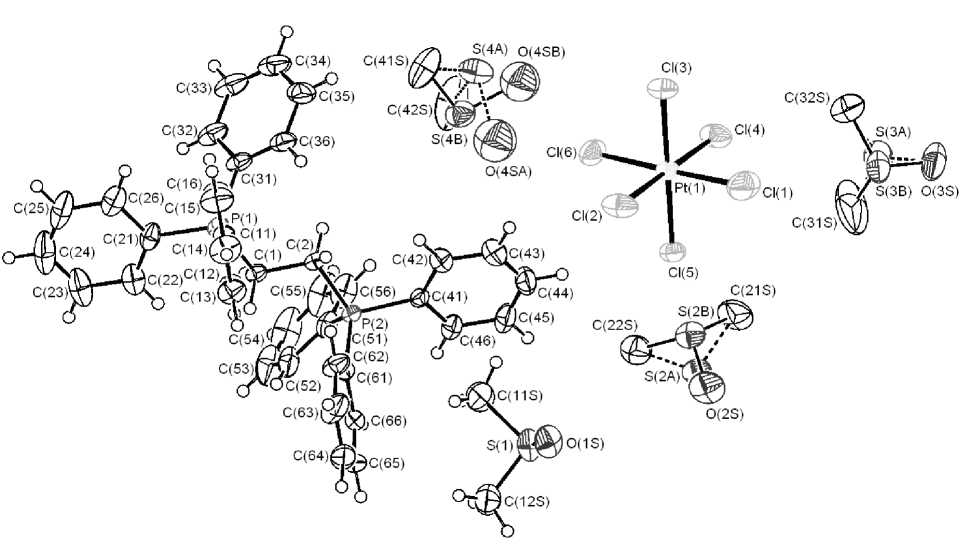
Рис. 2. Строение комплекса II
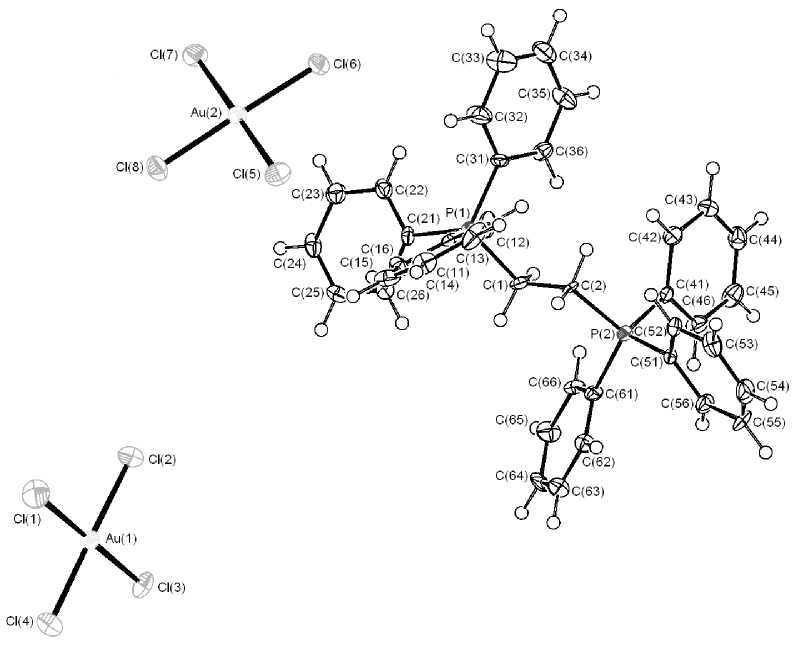
Рис. 3. Строение комплекса III
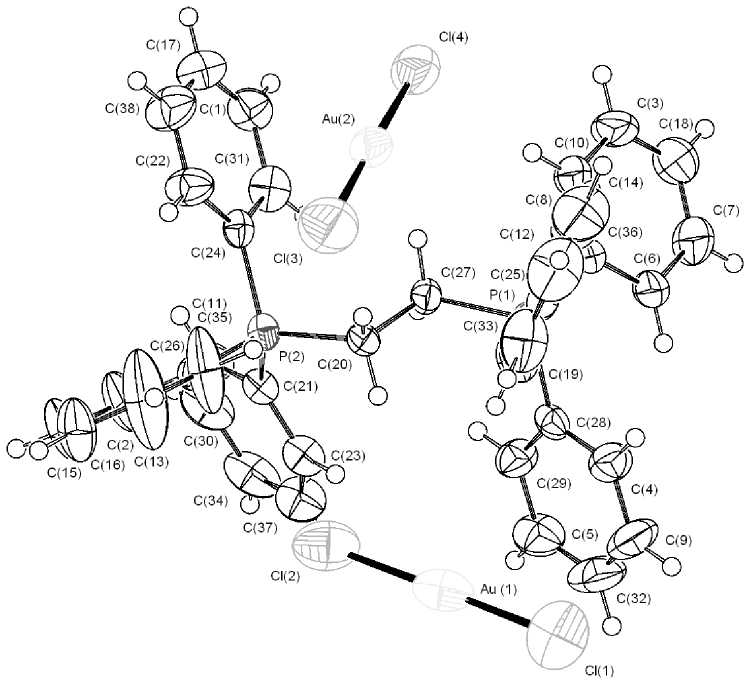
Рис. 4. Строение комплекса IV
Валентные углы СРС (106,30(9)–113,74(10)° в I, 107,1(2)–112,1(2)° в II, 107,1(3)–110,5(3)° в III и 106,24(13)–112,74(14)° в IV) мало отличаются от теоретического значения 109,5°. Средние расстояния P–C Ph меньше, чем P–C Alk (1,790(2)–1,798(2) и 1,820(2) Å соответственно в I, 1,787(5)– 1,801(4) и 1,803(4), 1,810(4) Å в II, 1,784(6)–1,812(7) и 1,808(6), 1,828(6) Å в III, 1,781(3)–1,795(3) и 1,810(3), 1,815(3) Å в IV при сумме ковалентных радиусов атомов фосфора и углерода 1,88 Å [9]). Значения длин связей С–С между метиленовыми группами изменяется в интервале 1,520(3)– 1,540(6) Å. Относительно связи С–С заместители расположены в заторможенной конформации.
Координационный полиэдр атома палладия в моноядерных анионах комплекса I представляет собой слегка искаженный плоский квадрат: цис- углы ClPdCl составляют 89,45(2), 90,95(2)°, SPdCl – 87,16(2), 92,55(2)°; соответствующие транс- углы равны 177,86(2) и 175,37(2)°. Длины связей Pd–Cl(1,3) (2,3144(5) и 2,3019(5) Å) короче, чем Pd–Cl(2) (2,3218(6) Å). Таким образом, связь Pd–Cl(2) в среднем на 0,0136 Å длиннее связи палладия с атомами Cl(1) и Cl(3), что превышает вероятную погрешность в определении длин связей (0,0005–0,0006 Å). Координационная связь между ионом палладия и потенциально амбидентатным диметилсульфоксидным лигандом осуществляется через атом серы. Длина связи Pd–S равна 2,2508(6) Å, что меньше суммы ковалентных радиусов палладия и серы (2,34 Å) [9]. Атом серы имеет координацию, близкую к тетраэдрической, с углами между связями в интервале значений 100,19(11)–113,55(7)°. Торсионные углы Cl(1)PdSO (67,96°) и Cl(3)PdSO (–114,16°) свидетельствуют о развороте плоскости квадрата [SCl(1)Cl(2)Cl(3)] относительно связи S–O таким образом, чтобы заместители при связи Pd–S приняли наиболее выгодную «шахматную» конформацию. Геометрия диметилсульфоксидного лиганда практически не изменяется при координации. Углы OSC(1, 2) равны 108,33(11), 107,11(11)°, в то время как в свободной молекуле диметилсульфоксида аналогичные углы составляют ~107°. Угол С(1)SC(2) (100,19(11)°) также близок к значению этого угла (97,4°) в несвязанной молекуле. Наиболее существенное различие в параметрах координированной и свободной молекул диметилсульфоксида обнаруживается при сравнении длин связей S–O (1,4752(16) и 1,531 Å соответственно).
В кристалле комплекса I наблюдаются межионные водородные связи катиона с двумя анионами. Диметилсульфоксидный лиганд каждого аниона связан прочной водородной связью с метиленовой группой (расстояние O∙∙∙H–С(3) 2,17 Å) и менее прочными связями с двумя фенильными лигандами катиона (O∙∙∙H–С(22) 2,41 Å, O∙∙∙H–С(12) 2,67 Å) (рис. 5), благодаря чему соблюдается плотная упаковка катионов и анионов в кристалле I (рис. 6).
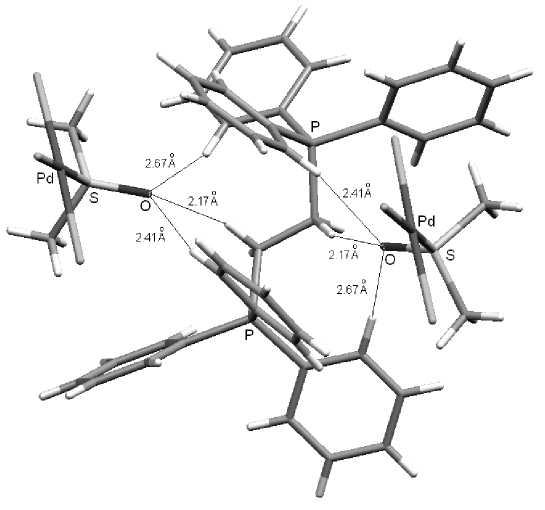
Рис. 5. Межионные водородные связи O···H в кристалле комплекса I
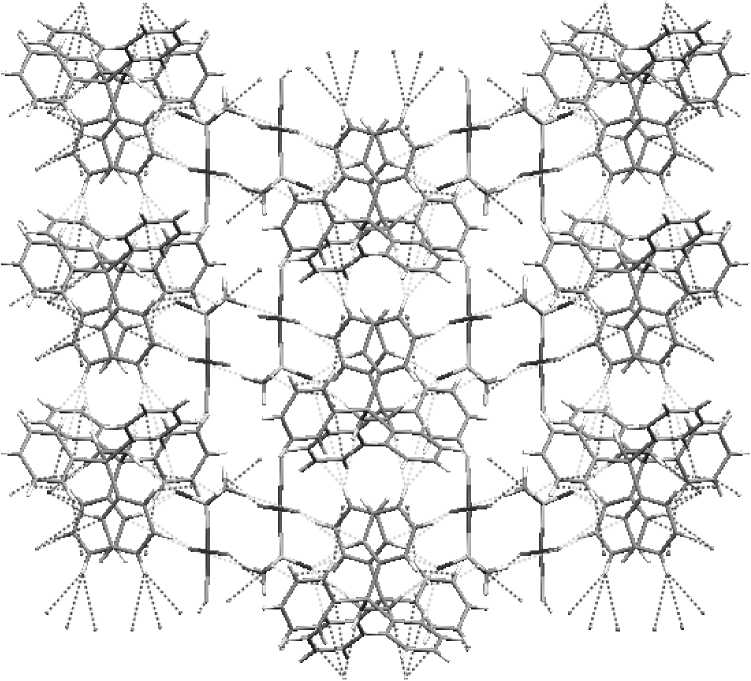
Рис. 6. Упаковка ионов в кристалле комплекса I
Кроме того, в кристалле имеют место короткие контакты типа Cl∙∙∙H–C как между анионами (Cl(1)∙∙∙H–C(1) 2,66 Å), так и между анионом и катионом (Cl(1)∙∙∙H–C(22) 2,91 Å, Cl(2)∙∙∙H–C(31) 2,94 Å).
В анионе комплекса I транс- влияние диметилсульфоксидного лиганда не столь существенно (удлинение транс -связи Pd–Cl(2) составляет 0,0136 Å). Кроме того, длина связи Pd–Cl(2) может изменяться не только под влиянием транс -расположенного лиганда, но и под воздействием межмолекулярных контактов Cl∙∙∙H–C. Наличие водородных связей с участием молекулы диметилсульфоксида обусловливает перераспределение электронной плотности в комплексном анионе, что может также отразиться и на удлинении транс- связи Pd-Cl(2).
Атом платины в анионе комплекса II имеет мало искаженную октаэдрическую координацию, цис- углы ClPtCl изменяются в интервале 89,19(6)-91,45(6)°, расстояния Pt-Cl варьируют в пределе 2,3028(13)–2,3252(11) Å (см. рис. 2).
Из четырех сольватных молекул диметилсульфоксида в комплексе II одна разупорядочена по атомам кислорода и серы с относительным весом 0,62/0,38, две других – по атомам серы (относительный вес 0,64/0,36 и 0,63/0,37 соответственно). Геометрические параметры неразупорядочен-ной сольватной молекулы диметилсульфоксида (углы O(1S)S(1)C(11S), O(1S)S(1)C(12S) 105,3(4), 107,8(3)°, C(11S)SC(12S) 96,9(3)°, расстояния S(1)–С(11S), S(1)–С(12S) 1,772(7), 1,763(7) Å, O(1S)–S(1) 1,495(4) Å) близки к характеристикам свободной молекулы, приведенным в работе [13].
Структурная организация кристалла комплекса II обусловлена водородными связями типа Cl∙∙∙H–C и О∙∙∙H–C. Каждый катион имеет короткие контакты с пятью анионами (расстояния Cl∙∙∙H–C Ph варьируют от 2,62 до 2,94 Å) и четырьмя молекулами диметилсульфоксида (расстояния O∙∙∙H–С Ме 2,14–2,29 Å, О∙∙∙H–C Ph 2,56–2,71 Å).
Квадратная координация атомов золота двух кристаллографически независимых анионов комплекса III мало искажена: цис- углы ClAu(1)Cl и ClAu(2)Cl изменяются в интервалах 89,15(8)-90,56(8)° и 88,68(7)-90,80(7)°, соответствующие транс- углы близки к 180°: 178,88(9), 179,01(8)° при атоме Au(1) и 176,42(7), 177,93(7)° при атоме Au(2). Длины связей Au(1)–Cl и Au(2)–Cl составляют 2,269(2)–2,290(2) и 2,278(18)–2,293(2) Å.
Угол между средними плоскостями анионов [Au(1)Cl(1)Cl(2)Cl(3)Cl(4)] и [Au(2)Cl(5)Cl(6)Cl(7)Cl(8)] составляет примерно 80°. Расстояние Cl(2)··· Cl(7) равно 3,462 Å (ван-дер-ваальсов радиус хлора 1,8 Å [9]). Каждый катион имеет множественные короткие контакты Cl∙∙∙H–C с семью анионами (расстояния Cl∙∙∙H 2,62–2,94 Å).
Два кристаллографически независимых аниона комплекса IV имеют практически линейное строение (углы Cl(1)Au(1)Cl(2) 177,46(4) и Cl(3)Au(2)Cl(4) 178,96(4)°). Длины связей Au(1)–Cl(1, 2) равны 2,250(1), 2,256(1) Å, Au(2)–Cl(3, 4) – 2,238(1), 2,2501(9) Å, что короче расстояний Au–Cl в анионе комплекса III.
Как и в кристалле III, в IV обнаружено множество коротких контактов Cl∙∙∙H–C (2,74–2,94 Å).
Выводы
Взаимодействием дихлорида бис -1,2-трифенилфосфинэтилена с хлоридом палладия (II) (1:2 мольн.), гексахлороплатиноводородной кислотой (1:1 мольн.) в диметилсульфоксиде, а также золотохлористоводородной кислотой (1:2 мольн.) в ацетоне и диметилсульфоксиде синтезированы комплексы [Ph 3 PCH 2 CH 2 PPh 3 ]2+ [PdCl 3 DMSO]– 2 , [Ph 3 PCH 2 CH 2 PPh 3 ]2+ [PtCl 6 ]2– ∙ 4 DMSO, [Ph 3 PCH 2 CH 2 PPh 3 ]2+[AuCl 4 ]– 2 и [Ph 3 PCH 2 CH 2 PPh 3 ]2+[AuCl 2 ]– 2 , строение которых доказано методом рентгеноструктурного анализа.
Список литературы Синтез и строение комплексов палладия, платины и золота: [Ph3PCH2CH2PPh3]2+ [PdCl3DMSO]-2, [Ph3PCH2CH2PPh3]2+ [PtCl6]2- · 4 DMSO, [Ph3PCH2CH2PPh3]2+ [AuCl4]-2 и [Ph3PCH2CH2PPh3]2+ [AuCl2]-2
- Синтез и кристаллическая структура гексахлорплатината, тетрахлораурата и гексахлорстанната тетрафенилсурьмы(V)/В.В. Шарутин, В.С. Сенчурин, О.А. Фастовец и др.//Коорд. химия. -2008.-Т. 34, № 5.-С. 373-379.
- Синтез и строение комплексов золота и меди [Ph3PhCH2P]+[AuCl4]-, [NH(C2H4OH)3]+[AuCl4] H2O и [Ph3EtP]+2[Cu2Cl6]2/В.В. Шарутин, В.С. Сенчурин, А. П. Пакусина и др.//Журн. неорган. химии. -2010. -Т. 55, № 9. -С. 1499-1505.
- Sheldrick G.M. SADABS, Program for empirical X-ray absorption correction, Bruker-Nonius, 1990-2004.
- Sheldrick G.M. SHELX-97 Release 97-2. University of Goettingen, Germany, 1998.
- Sheldrick G.M. SHELX-97 Release 97-2. University of Goettingen, Germany, 1998.
- Cambridge Crystallographic Data Center. 2011.
- Бацанов, С.С. Атомные радиусы элементов/С.С. Бацанов//Журн. неорг. химии. -1991. -Т. 36, № 12. -С. 3015-3037.

![Синтез и строение комплексов палладия, платины и золота: [Ph3PCH2CH2PPh3]2+ [PdCl3DMSO]-2, [Ph3PCH2CH2PPh3]2+ [PtCl6]2- · 4 DMSO, [Ph3PCH2CH2PPh3]2+ [AuCl4]-2 и [Ph3PCH2CH2PPh3]2+ [AuCl2]-2 Синтез и строение комплексов палладия, платины и золота: [Ph3PCH2CH2PPh3]2+ [PdCl3DMSO]-2, [Ph3PCH2CH2PPh3]2+ [PtCl6]2- · 4 DMSO, [Ph3PCH2CH2PPh3]2+ [AuCl4]-2 и [Ph3PCH2CH2PPh3]2+ [AuCl2]-2](/file/cover/147160203/sintez-i-stroenie-kompleksov-palladija-platiny-i-zolotaph3pch2ch2pph3-2.png)
