Синтез и строение органосульфонатов тетраорганилфосфония [R4P][OSO2R’], R= Me, R’ = C6H3Cl2-2,5; R= Bu, R’ = C10H5(OH-1)(NO2)2-2,4; [Ph3PR][OSO2R’], R= CH2CH=CHCH2PPh3, R’ = C9H4N(OH-8)(I-7); R= C6H11-cyclo, R’ = C6H3(NO2)2-2,4; R=CH2CHCHMe,R’ = C6H3Cl2-2,5
Автор: Механошина Евгения Сергеевна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 1 т.15, 2023 года.
Бесплатный доступ
Взаимодействием эквимолярных количеств галогенидов тетраорганилфосфония с 2,5-дихлорбензолсульфоновой, 2,4-динитробензолсульфоновой, 1-окси-2,4-динитро- 7-нафталинсульфоновой и 8-окси-7-йод-5-хинолинсульфоновой кислотами в воде синтезированы ионные органосульфонаты тетраорганилфосфония [R4P][OSO2R’], R = Me, R’ = C6H3Cl2-2,5 (1); R = Bu, R’ = C10H5(OH-1)(NO2)2-2,4 (2); [Ph3PR][OSO2R’], R = CH2CH=CHCH2PPh3, R’ = C9H4N(OH-8)(I-7) (3); R = C6H11- cyclo , R’ = C6H3(NO2)2-2,4 (4); R = CH2CH=CHMe, R’ = C6H3Cl2-2,5 (5). Рентгеноструктурный анализ кристаллов 1-4 проведен при 293 К на автоматическом четырехкружном дифрактометре D8 Quest Bruker (двухкоординатный CCD-детектор, Мо К α-излучение, λ = 0,71073 Å, графитовый монохроматор). Кристалл 1 [C16H22O8PS2Cl4, M 579,23; сингония моноклинная, группа симметрии С 2/ с ; параметры ячейки: a = 35,69(4), b = 7,454(9), c = 23,67(2) Å; a = 90,00, β = 129,16(3), g = 90,00 град., V = 4883(9) Å3, Z = 8; rвыч = 1,576 г/см3], 2 [C42H77N2O8P2S, M 832,06; сингония ромбическая, группа симметрии Pbca ; параметры ячейки: a = 14,712(9), b = 22,825(16), c = 29,475(16) Å; a = 90,00, β = 90,00, g = 90,00 град., V = 9898(11) Å3, Z = 8; rвыч = 1,117 г/см3], 3 [C29H27O6PSIN, M 675,45; сингония триклинная, группа симметрии P- 1; параметры ячейки: a = 9,506(8), b = 11,323(12), c = 13,662(10) Å; a = 82,21(4), β = 89,26(2), g = 72,60(4) град., V = 1390(2) Å3, Z = 2; rвыч = 1,614 г/см3], 4 [C30H29N2O7PS, M 592,58; сингония триклинная, группа симметрии P- 1; параметры ячейки: a = 9,793(5), b = 11,214(5), c = 14,341(7) Å; a = 109,495(17), β = 99,55(3), g = 94,58(2) град., V = 1448,5(12) Å3, Z = 2; rвыч = 1,359 г/см3]. В катионах 1-4 атомы фосфора имеют искаженную тетраэдрическую координацию, органосульфонатные анионы имеют обычную геометрию с тетраэдрическим атомом серы. Длины связей Р-С принимают значения 1,746(7)-1,841(19) Å, что меньше суммы ковалентных радиусов атомов-партнеров (1,83 Å); расстояния S-C: 1,759(5)-1,815(3) Å. Валентные углы СРС изменяются в интервалах 85,2(8)°-114,0(5)°. Структурная организация в кристаллах 1-4 в основном обусловлена слабыми межмолекулярными контактами типа O···Н 1,60-2,72 Å (сумма ван-дер-ваальсовых атомов-партнеров 2,62 Å). Полные таблицы координат атомов, длин связей и валентных углов для структур депонированы в Кембриджском банке структурных данных (№ 2153156 (1), № 2157531 (2), № 2160476 (3), № 2157713 (4), deposit@ccdc.cam.ac.uk; http://www.ccdc. cam.ac.uk).
2, 5-дихлорбензолсульфоновая, 2, 4-динитробензолсульфоновая, 1-окси-2, 4-динитро-7-нафталинсульфоновая, 8-окси-7-йод-5-хинолинсульфоновая, кислота, органосульфонат тетраорганилфосфония, синтез, строение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147239554
IDR: 147239554 | УДК: 546.87+547.29+548.312.5 | DOI: 10.14529/chem230103
Synthesis and structure of tetraorganylphosphonium organosulfonates [R4P][OSO2R’], R= Me, R’ = C6H3Cl2-2,5; R= Bu, R’ = C10H5(OH-1)(NO2)2-2,4; [Ph3PR][OSO2R’], R= CH2CH=CHCH2PPh3, R’ = C9H4N(OH-8)(I-7); R= C6H11-cyclo, R’ = C6H3(NO2)2-2,4; R=CH2CHCHMe,R’ = C6H3Cl2-2,5
The interaction of equimolar amounts of tetraorganylphosphonium halides with 2,5-dichlorobenzenesulfonic, 2,4-dinitrobenzenesulfonic, 1-hydroxy-2,4-dinitro-7-naphthalenesulfonic and 8-hydroxy-7-iodo-5-quinolinesulfonic acids in water leads to the formation of ionic tetraorganylphosphonium organosulfonates [R4P][OSO2R’], R = Me, R’ = C6H3Cl2-2,5 (1); R = Bu, R’ = C10H5(OH-1)(NO2)2-2,4 (2); [Ph3PR][OSO2R’], R = CH2CH=CHCH2PPh3, R’ = C9H4N(OH-8)(I-7) (3); R = C6H11- cyclo , R’ = C6H3(NO2)2-2,4 (4); R = CH2CH=CHMe, R’ = C6H3Cl2-2,5 (5). The structures of complexes 1-4 have been established by X-ray diffraction analysis. The X-ray structural analysis has been carried out on an automatic four-circle D8 Quest Bruker diffractometer (Мо Кα -radiation, λ = 0.71073 Å, graphite monochromator) at 293 K. Crystals 1 [C16H22O8PS2Cl4, M 579.23; monoclinic syngony, space group С 2/ с ; сell parameters: a = 35.69(4), b = 7.454(9), c = 23.67(2) Å; a = 90.00, β = 129.16(3), g = 90.00 deg., V = 4883(9) Å3, Z = 8; rcalc = 1.576 g/cm3], 2 [C42H77N2O8P2S, M 832.06; orthorhombic syngony, space group Pbca ; сell parameters: a = 14.712(9), b = 22.825(16), c = 29.475(16) Å; a = 90.00, β = 90.00, g = 90.00 deg., V = 9898(11) Å3, Z = 8; rcalc = 1.117 g/cm3], 3 [C29H27O6PSIN, M 675.45; triclinic syngony, space group P- 1; сell parameters: a = 9.506(8), b = 11.323(12), c = 13.662(10) Å; a = 82.21(4), β = 89.26(2), g = 72.60(4) deg., V = 1390(2) Å3, Z = 2; rcalc = 1.614 g/cm3], and 4 [C30H29N2O7PS, M 592.58; triclinic syngony, space group P -1; сell parameters: a = 9.793(5), b = 11.214(5), c = 14.341(7) Å; a = 109.495(17), β = 99.55(3), g = 94.58(2) deg., V = 1448.5(12) Å3, Z = 2; rcalc = 1.359 g/cm3]. The coordination of the phosphorus atoms in cations 1-5 is distorted tetrahedral; organosulfonate anions have the usual geometry with a tetrahedral sulfur atom. The Р-С bond lengths are 1.746(7)-1.841(19) Å, which is less than the sum of the covalent radii of the partner atoms (1.83 Å). The S-C distances are in the range of 1.759(5)-1.815(3) Å. The СРС valence angles vary in the range 85.2(8) -114.0(5) deg. The structural organization in crystals 1-4 is due to weak intermolecular contacts of the O···Н type, 1.60-2.72 Å (the sum of the Van der Waals radii of the partner atoms is 2.62 Å). Complete tables of atomic coordinates, bond lengths and bond angles for structures have been deposited at the Cambridge Crystallographic Data Centre (No. 2153156 (1), No. 2157531 (2), No. 2160476 (3), No. 2157713 (4); deposit@ccdc.cam.ac.uk; https://www.ccdc.cam.ac.uk).
Текст научной статьи Синтез и строение органосульфонатов тетраорганилфосфония [R4P][OSO2R’], R= Me, R’ = C6H3Cl2-2,5; R= Bu, R’ = C10H5(OH-1)(NO2)2-2,4; [Ph3PR][OSO2R’], R= CH2CH=CHCH2PPh3, R’ = C9H4N(OH-8)(I-7); R= C6H11-cyclo, R’ = C6H3(NO2)2-2,4; R=CH2CHCHMe,R’ = C6H3Cl2-2,5
Взаимодействием эквимолярных количеств галогенидов тетраорганилфосфония с 2,5-дихлорбензолсульфоновой, 2,4-динитробензолсульфоновой, 1-окси-2,4-динитро-7-нафталинсульфоновой и 8-окси-7-йод-5-хинолинсульфоновой кислотами в воде синтезированы ионные органосульфонаты тетраорганилфосфония [R4P][OSO2R’], R = Me, R’ = C6H3Cl2-2,5 (1); R = Bu, R’ = C10H5(OH-1)(NO2)2-2,4 (2); [Ph3PR][OSO2R’], R = CH2CH=CHCH2PPh3, R’ = C9H4N(OH-8)(I-7) (3); R = C6H11-cyclo, R’ = C6H3(NO2)2-2,4 (4); R = CH2CH=CHMe, R’ = C6H3Cl2-2,5 (5). Рентгеноструктурный анализ кристаллов 1–4 проведен при 293 К на автоматическом четырехкружном дифрактометре D8 Quest Bruker (двухкоординатный CCD-детектор, Мо Кα-излучение, λ = 0,71073 Å, графитовый монохроматор). Кристалл 1 [C16H22O8PS2Cl4, M 579,23; сингония моноклинная, группа симметрии С2/с; параметры ячейки: a = 35,69(4), b = 7,454(9), c = 23,67(2) Å; α = 90,00, β = 129,16(3), γ = 90,00 град., V = 4883(9) Å3, Z = 8; ρвыч = 1,576 г/см3], 2 [C42H77N2O8P2S, M 832,06; сингония ромбическая, группа симметрии Pbca; параметры ячейки: a = 14,712(9), b = 22,825(16), c = 29,475(16) Å; α = 90,00, β = 90,00, γ = 90,00 град., V = 9898(11) Å3, Z = 8; ρвыч = 1,117 г/см3], 3 [C29H27O6PSIN, M 675,45; сингония триклинная, группа симметрии P–1; параметры ячейки: a = 9,506(8), b = 11,323(12), c = 13,662(10) Å; α = 82,21(4), β = 89,26(2), γ = 72,60(4) град., V = 1390(2) Å3, Z = 2; ρвыч = 1,614 г/см3], 4 [C30H29N2O7PS, M 592,58; сингония триклинная, группа симметрии P–1; параметры ячейки: a = 9,793(5), b = 11,214(5), c = 14,341(7) Å; α = 109,495(17), β = 99,55(3), γ = 94,58(2) град., V = 1448,5(12) Å3, Z = 2; ρвыч = 1,359 г/см3]. В катионах 1‒4 атомы фосфора имеют искаженную тетраэдрическую координацию, органосульфонатные анионы имеют обычную геометрию с тетраэдрическим атомом серы. Длины связей Р-С принимают значения 1,746(7)-1,841(19) Å, что меньше суммы ковалентных радиусов атомов-партнеров (1,83 Å); расстояния S-C: 1,759(5)-1,815(3) Å. Валентные углы СРС изменяются в интервалах 85,2(8)°-114,0(5)°. Структурная организация в кристаллах 1‒4 в основном обусловлена слабыми межмолекулярными контактами типа O···Н 1,60–2,72 Å (сумма ван-дер-ваальсовых атомов-партнеров 2,62 Å). Полные таблицы координат атомов, длин связей и валентных углов для структур депонированы в Кембриджском банке структурных данных (№ 2153156 (1), № 2157531 (2), № 2160476 (3), № 2157713 (4), ; .
Органические соединения фосфора обладают уникальными свойствами и находят применение в самых разнообразных областях практической деятельности: в качестве инсектицидов, фунгицидов, дефолиантов, гербицидов, пластификаторов, ионитов, антипиренов, присадок к бензинам и смазочным маслам [1]. Фосфорорганические соединения также используются в синтетической органической химии, например, при получении олефинов по Виттигу [2] или синтезе элементоорганических соединений [3]. Сообщалось также о перспективах практического применения некоторых органических соединений фосфора в качестве катализаторов гидрофункционализации непредельных субстратов [4], реагентов для транс -металлирования [5] и метатезиса
σ-связей [6]. Кроме того, соли фосфония используются в современных методах разделения редкоземельных элементов [7]. Фосфонио-содержащие ионные жидкости (PILs) на основе тетраарилфосфониевых катионов обладают низкой вязкостью и высокой термической, химической и электрохимической стабильностью, что дает им преимущество над аналогичными солями на основе имидазолиевых, четвертичных аммониевых или тетраалкилфосфониевых катионов [8]. Четвертичные фосфониевые соли также обладают высокой биологической активностью и находят широкое применение в качестве противоопухолевых и антимикробных соединений [9]. Бромсодержащие комплексы платины с органилтрифенилфосфониевыми катионами являются весьма интересными объектами для изучения различных каталитических превращений [10]. Цианидные галогенсодержащие комплексы золота с органилтрифенилфосфониевыми катионами могут проявлять различные практически полезные свойства [11]. Разработка методов получения новых фосфониевых солей, содержащих различные функциональные группы, а также их производных является на сегодняшний день одним из перспективных направлений в органической химии. Из всех производных пятивалентного фосфора наиболее изучены соли тетраорганилфосфония, которые обычно получают по реакции окислительного присоединения из трифенилфосфина и галогенарена в присутствии хлористого алюминия [1] либо по реакции пентафенилфосфора с кислотами [12 - 15]. В работах [16 - 22] описан синтез некоторых структурно охарактеризованных органосульфонатов тетрафенилфосфония. Кристаллы комплексов получали при выдерживании смеси галогенидов тетрафенилфосфония и аренсульфоновой кислоты в различных растворителях (метаноле, ацетонитриле, ацетоне, бензоле, диэтиловом эфире, ДМФА, ТГФ). Большинство реакций проводили при нагревании, выходы комплексов при этом не превышали 78 %. Однако в литературе не известны примеры получения аренсульфонатов тетраорганилфосфония.
Ранее сообщалось о взаимодействии галогенидов органилтрифенилфосфония с аренсульфоновыми кислотами в воде, при котором происходит замещение галогенид-аниона на аренсульфонатный анион. Данным способом были получены органосульфонаты органилтрифенилфосфония [Ph 3 PR][OSO 2 R’], R = Ph, R’ = C 6 H 3 Cl 2 -2,5; R = C 6 H 11 - cyclo , R’ = C 6 H 3 Cl 2 -2,5; R = CH 2 OMe, R’ = C6H3(NO2)2-2,4; R = CH2OMe, R’ = C6H 4 (COOH-2) [23].
Продолжая исследования в данном направлении, были синтезированы и структурно охарактеризованы аренсульфонаты тетраорганилфосфония [R 4 P][OSO2R’], R = Me, R’ = C6H3Cl2-2,5 ( 1 ); R = Bu, R’ = C10H5(oH-1)(NO2)2-2,4 ( 2 ); и [Ph3PR][OSO2R’], R = CH2CH=CHCH2PPh3, R’ = C 9 H 4 N(OH-8)(I-7) ( 3 ); R = C6Hn- cyclo , R’ = C6H3(NO2)2-2,4 ( 4 ); R = CH2CH=CHMe, R’ = C6H3Cl2-2,5 ( 5 ).
Экспериментальная часть
-
2,5- Дихлорбензолсульфонат тетраметилфосфония (1). Раствор галогенида (хлорида) тетраметилфосфония (0,063 г, 0,500 ммоль) в 8 мл воды смешивали с 8 мл водного раствора 2,5-дихлорбензолсульфоновой кислоты (0,132 г, 0,500 ммоль). При медленном испарении растворителя выделялись бесцветные кристаллы, которые сушили на воздухе. Выход 0,169 г (96 %), Т пл = 105 ° С. ИК-спектр ( v , см - 1): 3090, 2970, 1734, 1717, 1558, 1506, 1452, 1375, 1317, 1290, 1236, 1198, 1149, 1098, 1065, 989, 885, 806, 773, 752, 708, 685, 615, 534, 519,511, 436. Найдено, %: 32,97; Н 3,91. C 16 H 22 O 8 PS 2 Cl 4 . Вычислено, %: С 33,18; Н 3,83.
Соединения 2 - 5 синтезировали аналогично.
1-Окси-2,4-динитро-7-нафталинсульфонат тетрабутилфосфония (2). Светло-коричневые кристаллы. Выход 0,269 г (94 %), Т пл = 107 ° С. ИК-спектр ( v , см - 1): 3208, 3019, 2931, 2912, 1826, 1568, 1520, 1506, 1448, 1398, 1325, 1298, 1223, 1128, 1098, 1032, 1009, 968, 922, 893, 806, 794, 746, 711, 692, 658, 621, 596, 522, 478,419. Найдено, %: С 60,52; Н 9,41. C 42 H 77 N 2 O 8 P 2 S. Вычислено, %: С 60,63; Н 9,33.
Бис (8-окси-7-йод-5-хинолинсульфонат) 2-бутен-1,4- бис (трифенилфосфония) (3). Оранжевые кристаллы. Выход 0,297 г (93 %), Тпл = 147 ° С. ИК-спектр ( v , см - 1): 3205, 3061, 2985, 2930, 1830, 1658, 1607, 1585, 1558, 1489, 1437, 1398, 1373, 1314, 1220, 1194, 1142, 1113, 1038, 1009, 997, 950, 906, 841, 816, 793, 745, 714, 688, 658, 600, 544, 492, 419. Найдено, %: С 51,23; Н 4,15. C 29 H 27 O 6 PSIN. Вычислено, %: С 51,57; Н 4,03.
-
2,4- Динитробензолсульфонат трифенил(циклогексил)фосфония (4). Жёлто-коричневые кристаллы. Выход 0,298 г (95 %), Т пл = 168 ° С. ИК-спектр ( v , см - 1): 3069, 3022, 2936, 2897, 2860,
1825, 1749, 1599, 1541, 1526, 1485, 1452, 1437, 1350, 1250, 1228, 1167, 1109, 1063, 1026, 995, 918, 889, 849, 833, 746, 719, 696, 664, 636, 544, 519, 469, 419. Найдено, %: 60,59; Н 4,80. C 30 H 29 N 2 O 7 PS. Вычислено, %: С 60,80; Н 4,93.
-
2,5- Дихлорбензолсульфонат (2-бутенил)трифенилфосфония (5). Бесцветные кристаллы. Выход 0,278 г (96 %), Т = 167 ° С. ИК-спектр ( v , см - 1): 3084, 3061, 2984, 1830, 1773, 1636, 1609, 1585, 1558, 1506, 1489, 1441, 1373, 1340, 1311, 1233, 1217, 1165, 1144, 1113, 1063, 1015, 999, 897, 837, 814, 762, 723, 692, 614, 590, 538, 515, 444. Найдено, %: С 61,79; Н 4,69. C 28 H 25 O 3 PSCl 2 . Вычислено, %: С 61,88; Н 4,64.
Элементный анализ выполнен на элементном анализаторе Carlo Erba CHNS-O EA 1108. Температуры плавления измерены на синхронном термоанализаторе Netzsch 449C Jupiter.
ИК-спектр соединений 1-5 записывали на ИК-Фурье спектрометре Shimadzu IR Affinity- 1S в таблетке KBr в области 4000 - 400 см - 1.
Рентгеноструктурный анализ ( РСА ) проводили на автоматическом четырехкружном дифрактометре D8 QUEST фирмы Bruker (Mo K „ -излучение, X = 0,71073 А, графитовый монохроматор) при 293 K. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены с помощью программ SMART и SAINT-Plus . Все расчеты по определению и уточнению структур выполнены с помощью программ SHELXL/PC и OLEX2 [24‒26]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Положение атомов водорода уточняли по модели наездника ( U изо (H) = 1,2 U экв (C)). Кристаллографические данные и результаты уточнения структур приведены в табл. 1, длины связей и валентные углы – в табл. 2.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структур 1 ‒ 4
|
Параметр |
(1) |
(2) |
(3) |
(4) |
|
Формула |
C 16 H 22 O 8 PS 2 Cl 4 |
C 42 H 77 N 2 O 8 P 2 S |
C 29 H 27 O 6 PSIN |
C 30 H 29 N 2 O 7 PS |
|
М |
579,23 |
832,06 |
675,45 |
592,58 |
|
Сингония |
Моноклинная |
Ромбическая |
Триклинная |
Триклинная |
|
Пр. группа |
С 2/ с |
Pbca |
P-1 |
P-1 |
|
a , Å |
35,69(4) |
14,712(9) |
9,506(8) |
9,793(5) |
|
b, Å |
7,454(9) |
22,825(16) |
11,323(12) |
11,214(5) |
|
c, Å |
23,67(2) |
29,475(16) |
13,662(10) |
14,341(7) |
|
α, град. |
90,00 |
90,00 |
82,21(4) |
109,495(17) |
|
β, град. |
129,16(3) |
90,00 |
89,26(2) |
99,55(3) |
|
γ, град. |
90,00 |
90,00 |
72,60(4) |
94,58(2) |
|
V , Å3 |
4883(9) |
9898(11) |
1390(2) |
1448,5(12) |
|
Z |
8 |
8 |
2 |
2 |
|
р (выч.), г/см3 |
1,576 |
1,117 |
1,614 |
1,359 |
|
ц , мм-1 |
0,761 |
0,176 |
1,329 |
0,217 |
|
F (000) |
2376,0 |
3624,0 |
680,0 |
620,0 |
|
Размер кристалла, мм |
0,28×0,12×0,1 |
0,45×0,24×0,09 |
0,3×0,1×0,09 |
0,45×0,25×0,16 |
|
Область сбора данных по 9 , град. |
6,42–57,24 |
5,82‒56,6 |
6,7–56,64 |
5,74–74,24 |
|
Интервалы индексов отражений |
–48 ≤ h ≤ 48, –10 ≤ k ≤ 10, –31 ≤ l ≤ 31 |
–19 ≤ h ≤ 16, –30 ≤ k ≤ 30, –39 ≤ l ≤ 39 |
–12 ≤ h ≤ 12, –14 ≤ k ≤ 15, –17 ≤ l ≤ 18 |
–16 ≤ h ≤ 16, –19 ≤ k ≤ 19, –24 ≤ l ≤ 24 |
|
Измерено отражений |
75563 |
150723 |
36412 |
99393 |
|
Независимых отражений |
6236 |
12219 |
6858 |
14804 |
|
R int |
0,2499 |
0,2773 |
0,0692 |
0,0504 |
|
Переменных уточнения |
290 |
545 |
362 |
370 |
|
GOOF |
1,068 |
0,997 |
1,015 |
1,331 |
|
R -факторы по F 2 > 2 с ( F 2) |
R 1 = 0,0942, wR 2 = 0,1770 |
R 1 = 0,0986, wR 2 = 0,2196 |
R 1 = 0,0421, wR 2 = 0,0843 |
R 1 = 0,1120, wR 2 = 0,3416 |
Окончание табл. 1
Длины связей и валентные углы в структурах 1 ‒ 4
|
Параметр |
(1) |
(2) |
(3) |
(4) |
|
R -факторы по всем отражениям |
R 1 = 0,1858, wR 2 = 0,2117 |
R 1 = 0,2954, wR 2 = 0,3110 |
R 1 = 0,0789, wR 2 = 0,0963 |
R 1 = 0,1693, wR 2 = 0,3790 |
|
Остаточная электронная плотность (min/max), e/A3 |
0,43/–0,64 |
0,41/–0,21 |
1,54/–0,69 |
4,59/–1,54 |
Таблица 2
|
Связь d , Å |
Угол ю, ° |
||
|
1 |
|||
|
S(1)–O(1) |
1,425(4) |
O(1)S(1)O(2) |
113,0(3) |
|
S(1)–O(2) |
1,435(4) |
O(1)S(1)O(3) |
112,1(3) |
|
S(1)–O(3) |
1,428(4) |
O(2)S(1)O(3) |
113,1(3) |
|
S(1)– C(1) |
1,766(5) |
O(1)S(1)C(1) |
106,4(3) |
|
S(2)–O(4) |
1,447(5) |
O(4)S(2)O(5) |
111,3(3) |
|
S(2)–O(5) |
1,417(4) |
O(4)S(2)O(6) |
113,4(3) |
|
S(2)–O(6) |
1,414(5) |
O(5)S(2)O(6) |
113,5(3) |
|
S(2)–C(11) |
1,759(5) |
O(4)S(2)C(11) |
103,0(3) |
|
P(1)–C(7) |
1,765(6) |
C(7)P(1)C(8) |
111,4(3) |
|
P(1)–C(8) |
1,758(6) |
C(8)P(1)C(9) |
108,6(3) |
|
P(1)–C(9) |
1,751(6) |
C(9)P(1)C(10) |
110,4(3) |
|
P(1)–C(10) |
1,763(6) |
C(7)P(1)C(10) |
110,5(3) |
|
Cl(1)‒C(2) |
1,723(6) |
Cl(1)C(2)C(1) |
122,1(4) |
|
2 |
|||
|
S(1)–O(1) |
1,428(4) |
O(1)S(1)O(2) |
112,2(3) |
|
S(1)–O(2) |
1,442(4) |
O(1)S(1)O(3) |
114,9(3) |
|
S(1)–O(3) |
1,436(4) |
O(2)S(1)O(3) |
112,3(3) |
|
S(1)– C(48) |
1,788(5) |
O(1)S(1)C(48) |
105,7(3) |
|
P(1)–C(1A) |
1,839(11) |
C(1A)P(1)C(5) |
114,0(5) |
|
P(1)–C(1B) |
1,748(12) |
C(1B)P(1)C(5) |
113,3(6) |
|
P(1)–C(5) |
1,747(7) |
C(5)P(1)C(13) |
110,2(3) |
|
P(1)–C(9A) |
1,814(12) |
C(9A)P(1)C(13) |
110,7(6) |
|
P(1)–C(9B) |
1,841(19) |
C(9B)P(1)C(13) |
85,2(8) |
|
P(1)–C(13) |
1,746(7) |
C(17)P(2)C(21) |
113,2(3) |
|
P(2)–C(17) |
1,813(6) |
C(21)P(2)C(25) |
112,3(3) |
|
P(2)–C(21) |
1,763(5) |
C(25)P(2)C(29) |
112,4(3) |
|
N(1)–O(5) |
1,193(5) |
O(5)N(1)O(6) |
120,0(5) |
|
N(1)–O(6) |
1,217(5) |
O(7)N(2)O(8) |
122,2(5) |
|
O(4)–C(41) |
1,241(5) |
O(5)N(1)C(42) |
121,0(5) |
|
3 |
|||
|
S(1)–O(1) |
1,447(3) |
O(1)S(1)O(2) |
111,79(19) |
|
S(1)–O(2) |
1,443(3) |
O(1)S(1)O(3) |
113,20(18) |
|
S(1)–O(3) |
1,457(3) |
O(2)S(1)O(3) |
113,07(18) |
|
S(1)– C(31) |
1,779(3) |
O(1)S(1)C(31) |
105,90(16) |
|
P(1)–C(1) |
1,786(4) |
C(1)P(1)C(7) |
110,04(16) |
|
P(1)–C(7) |
1,815(4) |
C(7)P(1)C(11) |
104,33(15) |
|
P(1)–C(11) |
1,801(3) |
C(11)P(1)C(21) |
109,60(15) |
|
P(1)–C(21) |
1,791(3) |
C(1)P(1)C(21) |
109,25(16) |
|
N(1)–C(35) |
1,360(5) |
C(35)N(1)C(39) |
117,4(3) |
|
I(1)–C(33) |
2,097(4) |
I(1)C(33)C(32) |
119,0(3) |
|
O(4)–C(34) |
1,353(4) |
O(4)C(34)C(33) |
120,4(3) |
|
C(8)‒C(8)1 |
1,323(6) |
C(7)C(8)C(8)1 |
122,6(4) |
Окончание табл. 2
|
Связь d , Å |
Угол ю, ° |
||
|
4 |
|||
|
S(1)–O(1) |
1,418(3) |
O(1)S(1)O(2) |
108,21(19) |
|
S(1)–O(2) |
1,472(3) |
O(1)S(1)O(3) |
119,27(19) |
|
S(1)–O(3) |
1,384(3) |
O(2)S(1)O(3) |
112,0(2) |
|
S(1)– C(41) |
1,815(3) |
O(1)S(1)C(41) |
104,81(14) |
|
P(1)–C(1) |
1,781(2) |
C(1)P(1)C(11) |
109,89(10) |
|
P(1)–C(11) |
1,798(2) |
C(11)P(1)C(21) |
108,62(11) |
|
P(1)–C(21) |
1,803(2) |
C(21)P(1)C(31) |
109,51(10) |
|
P(1)–C(31) |
1,829(2) |
C(1)P(1)C(31) |
111,44(10) |
|
N(1)–O(4) |
1,219(5) |
O(4)N(1)O(5) |
125,2(3) |
|
N(1)–O(5) |
1,184(5) |
O(6)N(2)O(7) |
124,2(4) |
|
N(2)–O(6) |
1,242(5) |
O(4)N(1)C(42) |
118,0(3) |
Преобразования симметрии: 12‒x, 1‒y, 1‒z.
Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2153156 (1), № 2157531 (2), № 2160476 (3), № 2157713 (4), ; .
Обсуждение результатов
Комплексы 1 - 5 получены при смешивании водных растворов галогенидов тетраорганилфос-фония и соответствующей аренсульфоновой кислоты. При медленном испарении воды имело место образование устойчивых на воздухе прозрачных кристаллов, хорошо растворимых в аренах, хлороформе, тетрагидрофуране, этаноле, ацетонитриле, четыреххлористом углероде и плохо - в воде при комнатной температуре.
[R 4 P]Hal + HOSO 2 R’ ⎯⎯⎯⎯ [R 4 P][OSO 2 R’] R = Me; R’= C 6 H 3 C a l 2 -2,5 ( 1 );
ОН
R = Bu; R’ = ( 2 )
no2
[Ph PR]Hal + HOSO R’ ⎯⎯⎯⎯ [Ph PR][OSO R’] -HHal
R = CH 2 CH=CHCH 2 PPh 3 , R’ = ( 3 );
он
R = C 6 H 11 - cyclo , R’ = C 6 H 3 (NO 2 ) 2 -2,4 ( 4 );
R = CH 2 CH=CHMe, R’ = C 6 H 3 Cl 2 -2,5 ( 5 )
ИК-спектры соединений 1-5 содержат характерные полосы валентных колебаний углеродного скелета ароматических фрагментов в области 1599‒1485 см–1. Валентным колебаниям связей CAr–H соответствуют полосы поглощения средней интенсивности при 3090‒3019 см–1; плоскостным деформационным колебаниям этих же связей – полосы при 1149‒1098 см–1, внеплоскостным деформационным колебаниям – при 897‒806 см–1. Также присутствуют характерные полосы поглощения сильной интенсивности при 1250-1217 см-1 и средней интенсивности при 1065-1026 см-1, которые отвечают асимметричным и симметричным валентным колебаниям сульфонатной группы SO3. Полосы поглощения сильной интенсивности валентных колебаний связи S‒O распо- ложены при 696‒685 см–1. Интенсивные полосы поглощения в области 544‒511 см‒1 и 752‒708 см–1 соответствуют валентным колебаниям связей CAr–S и CAr–P соответственно [27]. Валентным колебаниям связей CAr–Cl в спектрах структур 1, 5 отвечают полосы сильной интенсивности при 773 и 762 см–1. Интенсивная полоса при 600 см‒1 в спектре соединения 3 относится к валентным колебаниям связи CAr–I. Деформационным колебаниям метильных групп P‒CH3 в спектре комплекса 1 соответствуют полосы поглощения при 1375‒1317 см–1. Спектры соединений 3, 5 содержат полосы валентных колебаний связей C=C алкеновых фрагментов в области 1658‒1607 см–1. В структурах комплексов 2, 3 присутствуют гидроксильные группы, валентным колебаниям которых отвечают широкие полосы при 3208 и 3205 см–1. В спектрах соединений 2, 4 асимметричным колебаниям NO2-группы соответствуют интенсивные полосы поглощения при 1520 и 1526 см–1, симметричным колебаниям – 1325 и 1350 см–1 [28].
По данным РСА, кристаллы комплексов 1 ‒ 4 образованы катионами тетраорганилфосфония и аренсульфонат-анионами (рис. 1 - 4).
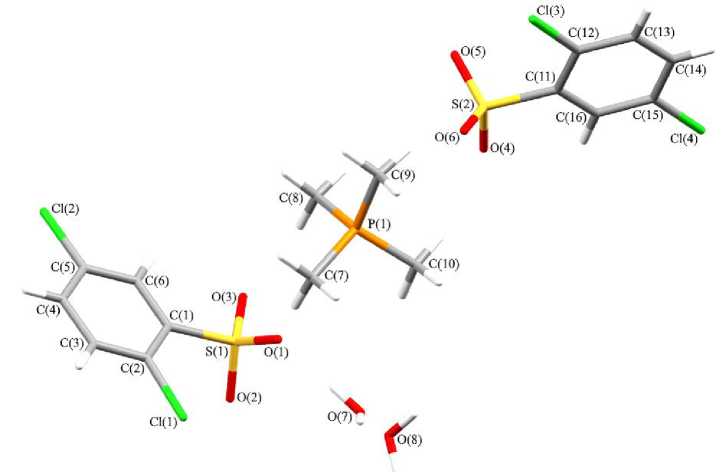
Рис. 1. Общий вид 2,5-дихлорбензолсульфоната тетраметилфосфония
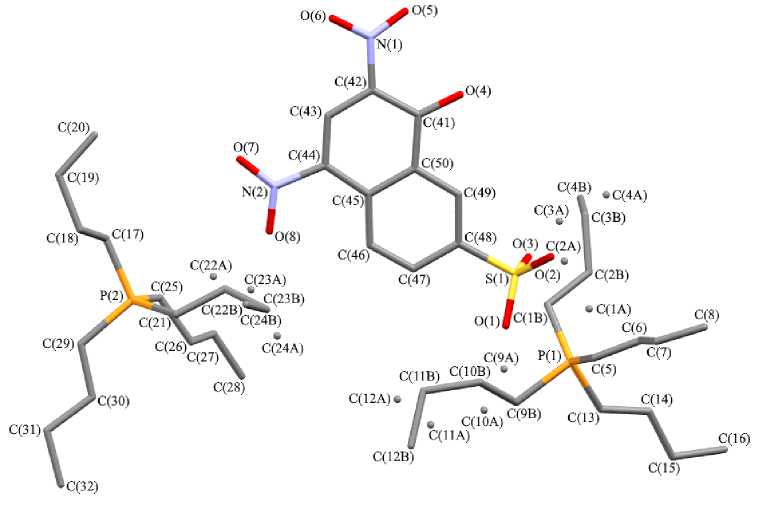
Рис. 2. Общий вид 1-окси-2,4-динитро-7-нафталинсульфоната тетрабутилфосфония (атомы водорода не показаны; для разупорядоченных атомов показаны два положения: C(A) и С(B))
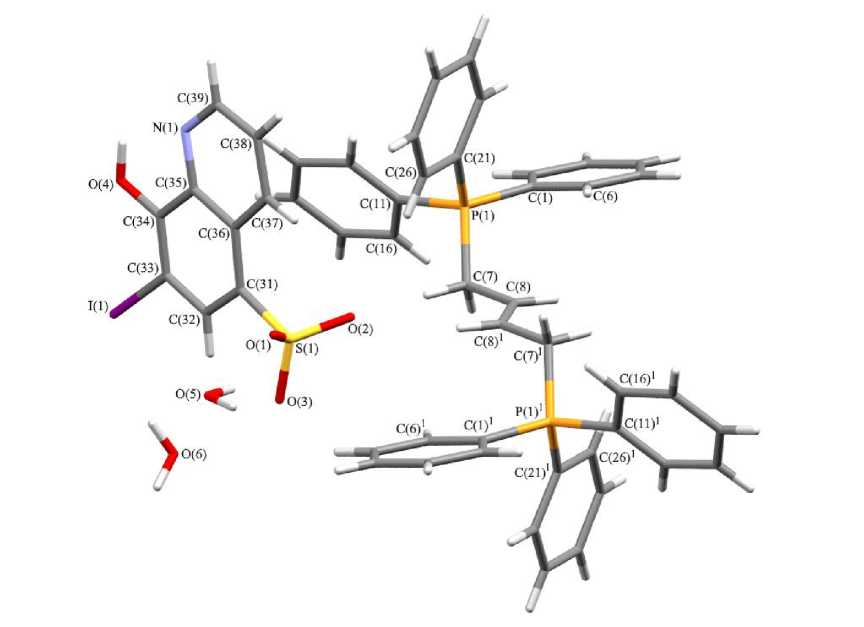
Рис. 3. Общий вид бис (8-окси-7-йод-5-хинолинсульфоната) 2-бутен-1,4- бис (трифенилфосфония)
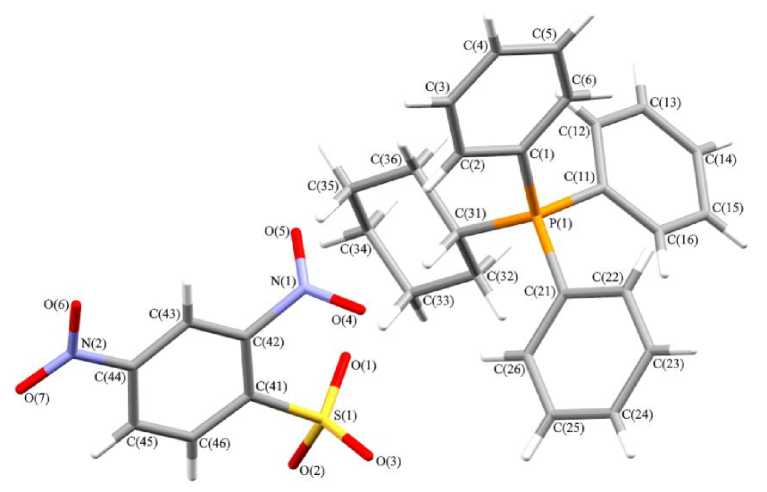
Рис. 4. Общий вид 2,4-динитробензолсульфоната трифенил(циклогексил)фосфония
Соединения 1 и 3 кристаллизуются в виде гидратов состава [Me 4 P][OSO 2 C 6 H 3 Cl 2 -2,5] ∙ 2H 2 O и [Ph 3 PCH 2 CH=CHCH 2 PPh 3 ][OSO 2 C 9 H 4 N(OH-8)(I-7)] 2 ∙ 4H 2 O. В кристалле комплекса 1 присутствуют два типа кристаллографически независимых анионов; в кристалле соединения 2 ‒ два типа кристаллографически независимых катионов.
В соединении 2 некоторые атомы бутильных групп [C(1)‒C(4), C(9)‒C(12), C(22)‒C(24)] разупорядочены по двум положениям (см. рис. 2). Катион органил- бис (трифенилфосфония) комплекса 3 содержит зеркально-поворотную ось второго порядка, которая проходит через центр двойной связи C(8)=C(8)1 (точечная группа C 2h ).
Катионы тетраорганилфосфония в структурах 1 ‒ 4 имеют незначительно искаженную тетраэдрическую конфигурацию. Длины связей Р-С принимают значения 1,746(7)-1,841(19) Å [1,751(6)-1,765(6) Å ( 1 ); 1,746(7)–1,841(19) Å ( 2 ); 1,786(4)–1,815(4) Å ( 3 ); 1,781(2)–1,829(2) Å ( 4 )], что меньше суммы ковалентных радиусов атомов-партнеров (1,83 Å) [29]. Валентные углы СРС изменяются в интервалах 85,2(8)°-114,0(5)°: 108,6(3)°-111,4(3)°; 85,2(8)°-114,0(5)°; 104,33(15)°-111,97(15)°; 108,62(11)°-111,44(10)° в 1 , 2 , 3 , 4 соответственно.
В аренсульфонатных анионах комплексов 1 - 4 расстояния S-C близки между собой и принимают значения 1,759(5)-1,815(3) Å. Связи S–О практически выровнены, что свидетельствует о равномерном распределении электронной плотности в SO3-группах. Расстояния S‒O изменяются в пределах 1,384(3)‒1,472(3) Å: 1,414(5)‒1,447(5) Å ( 1 ), 1,428(4)‒1,442(4) Å ( 2 ), 1,443(3)‒1,457(3) Å ( 3 ), 1,384(3)‒1,472(3) Å ( 4 ).
Валентные углы OSC в сульфонатных группах (103,0(3)°-106,4(3)°) меньше, чем углы OSO (108,21(19)°-119,27(19)°), что полностью согласуется с теорией отталкивания электронных пар валентных оболочек (ОПВЭО) [30].
В сульфонат-анионе структуры 4 плоскость пара -нитрогруппы незначительно отклоняется от средней плоскости ароматического кольца (соответствующий двугранный угол равен 7,49°), нитрогруппа в орто -положении развернута относительно плоскости кольца на угол 67,83°. Расстояния N-O (1,184(5), 1,219(5) А) в орто- группе более короткие, чем в пара -нитрогруппе (1,231(5), 1,242(5) Å), что связано с возможным сопряжением при малом отклонении нитрогруппы от плоскости аренового цикла. В аренсульфонатном анионе комплекса 2 плоскость (NO 2 -4)-группы практически совпадает с плоскостью нафталинового цикла (2,50°).
В структуре 1 две молекулы кристаллизационной воды, два типа кристаллографически независимых аренсульфонат-анионов и катион тетраорганилфосфония образуют циклы посредством водородных связей типа S=O∙∙∙Н(C) [2,31‒2,68 Å] и S=O∙∙∙Н(O) [1,69 Å, 1,77 Å] (рис. 5).
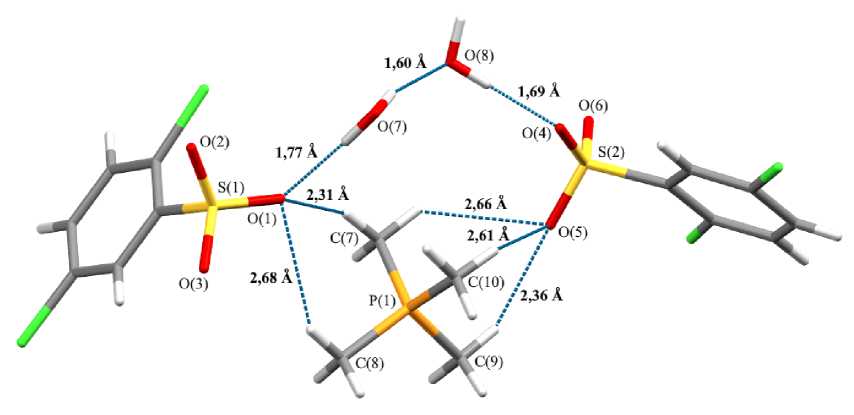
Рис. 5. Водородные связи в кристалле 1
Катионы и анионы в комплексах 1‒4 связаны слабыми водородными связями типа S=O∙∙∙Н(C) (2,30–2,72 Å). В структурах 2 , 4 представлены множественные водородные связи типа N=O∙∙∙H [2,14‒2,86 Å ( 2 ), 2,45‒2,68 Å ( 4 )]. В молекулах 2 , 3 имеют место водородные связи между атомом кислорода гидроксильной группы в анионах и атомами водорода в катионах (Ar)O∙∙∙H(С) [2,47‒2,52 Å ( 2 ), 2,57 Å ( 3 )]. В комплексе 1 также присутствуют короткие контакты типа С‒H∙∙∙Cl(Ph) и S=O∙∙∙Cl(Ph) [2,825 Å, 3,254 Å], в структуре 3 ‒ короткие контакты типа S=O∙∙∙I(Ar) (3,302 Å).
Структурная организация в кристаллах 1 ‒ 4 в основном обусловлена слабыми межмолекулярными контактами типа O···Н 1,60–2,68 Å ( 1 ), 2,45–2,72 Å ( 2 ), 2,31–2,70 Å ( 3 ), 2,35–2,72 Å ( 4 ) (сумма ван-дер-ваальсовых атомов-партнеров – 2,62 Å [31]). Данные взаимодействия структурируют молекулы кристалла 3 в слои, перпендикулярные кристаллографической оси c (рис. 6).
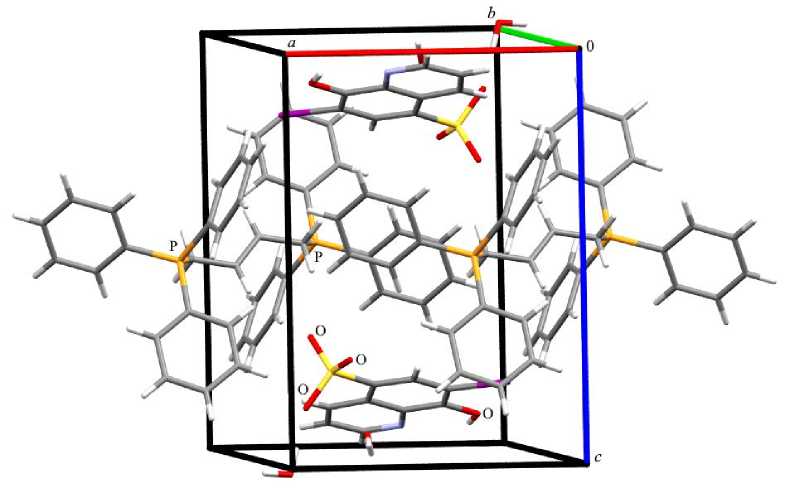
Рис. 6. Упаковка ионов комплекса 3 в кристалле (показан один слой)
Выводы
Установлено, что взаимодействие галогенидов тетраорганилфосфония с аренсульфоновыми кислотами в воде приводит к образованию ионных аренсульфонатов тетраорганилфосфония с тетраэдрическими катионами тетраорганилфосфония и аренсульфонатными анионами с тетраэдрическим атомом серы.
Выражаю признательность профессору В.В. Шарутину за рентгеноструктурный анализ кристаллов соединений 1‒4 и помощь при работе над статьей.
Список литературы Синтез и строение органосульфонатов тетраорганилфосфония [R4P][OSO2R’], R= Me, R’ = C6H3Cl2-2,5; R= Bu, R’ = C10H5(OH-1)(NO2)2-2,4; [Ph3PR][OSO2R’], R= CH2CH=CHCH2PPh3, R’ = C9H4N(OH-8)(I-7); R= C6H11-cyclo, R’ = C6H3(NO2)2-2,4; R=CH2CHCHMe,R’ = C6H3Cl2-2,5
- Пурдела Д., Вылчану Р. Химия органических соединений фосфора. М.: Химия, 1972. 752 с.
- Бартон Д., Оллис У.Д. Общая органическая химия. Том 5. Соединения фосфора и серы. М.: Химия, 1983. - 720 с.
- Alkyloxy- and silyloxy-derivatives of P(V) and Sb(V) / G.A. Razuvaev, N.A. Osanova, T.G. Brilkina et al. // J. Organomet. Chem. 1975. Vol. 99, no. 1. P. 93-106. DOI: 10.1016/S0022-328X(00)86365-2.
- Wang D., Astruc D. The golden age of transfer hydrogenation // Chem. Rev. 2015. Vol. 115. P. 6621-6686. DOI: 10.1021/acs.chemrev.5b00203.
- The stille reaction, 38 years later / C. Cordovilla, C. Bartolome, J.M. Martinez-Ilarduya et al. // ACS Catal. 2015. Vol. 5. P. 3040-3053. DOI: 10.1021/acscatal.5b00448.
- Chong C.C., Hirao H., Kinjo R. Metal-free c-bond metathesis in 1,3,2-diazaphospholene-catalyzed hydroboration of carbonyl compounds // Angew. Chem. Int. Ed. 2015. Vol. 127. P. 192-196. DOI: 10.1002/ange.201408760.
- Separation of rare earth elements by synergistic solvent extraction with phosphonium-based ionic liquids using a P-diketone extractant and a neutral ligand / M. Matsumiya, D. Nomizu, Y. Tsuchida et al. // Solvent Extraction and Ion Exchange. 2021. Vol. 39. P. 764-784. DOI: 10.1080/07366299.2021.1889761.
- Ionic liquids of superior thermal stability / C.G. Cassity, A. Mirjafari, N. Mobarrez et al. // Chem. Commun. 2013. Vol. 49, no. 69. P. 7590-7592. DOI: 10.1039/c3cc44118k.
- Synthesis, spectral and solid state characterization of a new bioactive hydrazine bridged cyclic diphosphonium compound / M. Milenkovic, B. Warzajtis, U. Rychlewska et al. // Molecules. 2012. Vol. 17, no. 3. P. 2567-2578. DOI: 10.3390/molecules17032567.
- Зыкова А.Р., Шарутин В.В., Шарутина О.К. Новые гексабромоплатинаты органилтрифе-нилфосфония [Ph3PR]2[PtBR6], R = CH3, CH=CH2, CH2CH=CH2 // Журн. общей химии. 2021. Т. 66, № 1. С. 63-68. DOI: 10.31857/S0044457X21010141.
- Синтез и строение дицианодигалогенауратов (4-фторбензил)трифенилфосфония [Ph3PCH2C6H4F-4][Au(CN)2Hlg2] / В.В. Шарутин, О.К. Шарутина, Н.М. Тарасова и др. // Журн. общей химии. 2021. Т. 91, № 11. С. 1716-1722. DOI: 10.31857/S0044460X21110081.
- Карбоксилаты и сульфонаты тетрафенилфосфора. Синтез и строение / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина и др. // Журн. общей химии. 2009. Т. 79. С. 80-89. DOI: 10.1134/S1070363209010125.
- Синтез и строение карбоксилатов тетрафенилфосфония / В.В. Шарутин, О.К. Шарутина, А.В. Рыбакова и др. // Журн. общей химии. 2018. Т. 88, № 8. С. 1308-1313. DOI: 10.1134/S0044460X18080139.
- Шарутин В.В., Мукушева Н., Уржумова А.В. Синтез и строение 2,4-динитробензолсульфоната тетрафенилфосфония // Вестник ЮУрГУ. Серия «Химия». 2018. Т. 10, № 2. С. 48-54. DOI: 10.14529/chem180206.
- Шарутин В.В., Шарутина О.К., Губанова Ю.О. Синтез и строение аренсульфонатов тетрафенилфосфония // Изв. вузов. Химия и хим. технология. 2019. Т. 62, № 2. С. 4-10. DOI: 10.6060/ivkkt.20196202.5823.
- New organic free radical anions TEMPO-A-CO-(o-; m-; ^-)C6H4SO3- (A = NH; NCH3; O) and their TTF and/or BEDT-TTF salts / H. Akutsu, K. Masaki, K. Mori et al. // Polyhedron. 2005. Vol. 24. P. 2126-2132. DOI: 10.1016/j.poly.2005.03.023.
- Tunable GUMBOS-based sensor array for label-free detection and discrimination of proteins / W.I.S. Galpothdeniya, F.R. Fronczek, M. Cong et al. // J. Mater. Chem. B. 2016. Vol. 4, no. 8. P. 1414-1422. DOI: 10.1039/C5TB02038G.
- A new anionic acceptor, 2-sulfo-3,5,6-trichloro-1,4-benzoquinone and its charge-transfer salts / H. Akutsu, J. Yamada, S. Nakatsuji et al. // CrystEngComm. 2009. Vol. 11, no. 12. P. 2588-2592. DOI: 10.1039/b909519e.
- Dinuclear calcium complex with weakly NH-0 hydrogen-bonded sulfonate ligands / A. Onoda, Y. Yamada, M. Doi et al. // Inorg. Chem. 2001. Vol. 40, no. 3. P. 516-521. DOI: 10.1021/ic0003067.
- Anion polarity-induced self-doping in a purely organic paramagnetic conductor, a-a'-(BEDT-TTF)2(PO-CONH-m-C6H4SO3-H2O where BEDT-TTF is te(ethylenedithio)tetrathiafulvalene and PO is the radical 2,2,5,5-tetramethyl-3-pyrrolin-1-oxyl / H. Akutsu, K. Ishihara, S. Ito et al. // Polyhedron. 2017. Vol. 136. P. 23-29. DOI: 10.1016/j.poly.2017.02.001.
- Correlation between metal-insulator transition and hydrogen-bonding network in the organic metal ¿-(BEDT-TTF)4[2,6-anthracene-67s(sulfonate)](H2O)4 / F. Camerel, G. Le Helloco, T. Guizouarn et al. // Cryst. Growth Des. 2013. Vol. 13, no. 11. P. 5135-5145. DOI: 10.1021/cg401416h.
- Ferrer E.G., Williams P.A.M., Castellano E.E. On a novel synthesis of 2-sulfonatobenzoic acid by oxidation of thiosalicylic acid catalyzed by copper(II): a structural study // Z. Anorg. Allg. Chem. 2002. Vol. 628. P. 1979-1984. DOI: 10.1002/1521-3749(200209)628:9/10<1979::AID-ZAAC1979-3.0.CO;2-V.
- Шарутин В.В., Шарутина О.К., Механошина Е.С. Синтез и строение органосульфонатов органилтрифенилфосфония [Ph3PR][OSO2R'], R = Ph, R' = C6H3Cb-2,5; R = CHu-cyclo, R' = C6H3Cl2-2,5; R = C^OMe, R' = C6H3(NO2)2-2,4; R = C^OMe, R' = C6H4(COOH-2) // Вестник ЮУрГУ. Серия «Химия». 2022. Т. 14, № 2. С. 1-51. DOI: 10.14529/chem220205.
- Bruker. SMART and SAINT-Plus. Versions 5.0. data collection and processing software for the smart system. Bruker axs Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An integrated system for solving, refining and displaying crystal structures from diffraction data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: a complete structure solution, refinement and analysis program / O.V. Dolomanov, L.J. Bourhis, R.J. Gildea et al. // J. Appl. Cryst. 2009. Vol. 42. P. 339-341. DOI: 10.1107/S0021889808042726.
- Тарасевич Б.Н. ИК-спектры основных классов органических соединений. М.: МГУ, 2012. 54 с.
- Инфракрасная спектроскопия органических и природных соединений: учебное пособие / А.В. Васильев, Е.В. Гриненко, А.О. Щукин и др. СПб.: СПбГЛТА, 2007. 54 с.
- Covalent radii revisited / B. Cordero, V. Gómez, A.E. Platero-Prats et al. // Dalton Trans. 2008. Iss. 21. P. 2832-2838. DOI: 10.1039/B801115J.
- Гиллеспи Р., Харгиттаи И. Модель отталкивания электронных пар валентной оболочки и строение молекул, М.: Мир, 1992. 75 с.
- Consistent van der waals radii for the whole main group / M. Mantina, A.C. Chamberlin, R. Valero et al. // J. Phys. Chem. A. 2009. Vol. 113, iss. 19. P. 5806-5812. DOI: 10.1021/jp8111556.

![Синтез и строение органосульфонатов тетраорганилфосфония [R4P][OSO2R’], R= Me, R’ = C6H3Cl2-2,5; R= Bu, R’ = C10H5(OH-1)(NO2)2-2,4; [Ph3PR][OSO2R’], R= CH2CH=CHCH2PPh3, R’ = C9H4N(OH-8)(I-7); R= C6H11-cyclo, R’ = C6H3(NO2)2-2,4; R=CH2CHCHMe,R’ = C6H3Cl2-2,5 Синтез и строение органосульфонатов тетраорганилфосфония [R4P][OSO2R’], R= Me, R’ = C6H3Cl2-2,5; R= Bu, R’ = C10H5(OH-1)(NO2)2-2,4; [Ph3PR][OSO2R’], R= CH2CH=CHCH2PPh3, R’ = C9H4N(OH-8)(I-7); R= C6H11-cyclo, R’ = C6H3(NO2)2-2,4; R=CH2CHCHMe,R’ = C6H3Cl2-2,5](/file/cover/147239554/sintez-i-stroenie-organosulfonatov-tetraorganilfosfonija-r4p-oso2r-r-me.png)
