Синтез и строение пентафторпропионата тетрафенилсурьмы Ph4SbOC(O)CF2CF3
Автор: Ефремов Андрей Николаевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 3 т.12, 2020 года.
Бесплатный доступ
По реакциям замещения между пентафенилсурьмой и пентафторпропионой кислотой и по перераспределению лигандов между пентафенилсурьмой и бис (пентафторпропионатом) трифенилсурьмы получен с выходом до 96 % пентафторпропионат тетрафенилсурьмы. Соединение идентифицировано методом ИК-спектроскопии и рентгеноструктурного анализа (РСА). По данным РСА, атом сурьмы имеет искаженную тригонально-бипирамидальную координацию с атомом кислорода карбоксилатного и атомом углерода фенильного лигандов в апикальных положениях. Все атомы фтора и углерод группы CF3 разупорядочены по двум положениям (соотношение вкладов положений в разупорядоченный фрагмент составляет 0,58/0,42). Аксиальный угол СSbO составляет 178,19(1)º, сумма экваториальных углов CSbC равна 355,78(14)º. Атом сурьмы выходит из экваториальной плоскости [C3] в сторону аксиального атома углерода на 0,254 Å. Плоскости фенильных колец повернуты вокруг связей Sb-Cэкв таким образом, чтобы минимизировать внутри- и межмолекулярные взаимодействия. Среднее значение длин связей Sb-Сэкв составляет 2,129(4) Å, при этом длина связи Sb-Сакс сопоставима с экваториальными и имеет значение 2,124(3) Å. Расстояние Sb-O составляет 2,325(3) Å, что больше суммы ковалентных радиусов сурьмы и кислорода (2,07 Å). Характерной особенностью всех карбоксилатов тетраарилсурьмы является наличие внутримолекулярного контакта атома сурьмы с карбонильным атомом кислорода. Данное расстояние Sb×××O=C составляет 3.492(5) Å, что меньше суммы ван-дер-ваальсовых радиусов сурьмы и кислорода (3,70 Å). Это взаимодействие приводит к увеличению одного из экваториальных углов, расположенного со стороны внутримолекулярного контакта, до 122,67(14)°. Организация молекул в кристалле обусловлена водородными связями с участием карбонильного атома кислорода. Данные контакты структурируют молекулы в слои, расположенные перпендикулярно кристаллографической оси b . Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1850118; deposit@ccdc.cam.ac.uk или http://www.ccdc.cam.ac.uk/data_request/cif).
Пентафенилсурьма, пентафторпропионовая кислота, карбоксилат тетрафенилсурьмы, реакция перераспределения лигандов, реакция замещения, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147234235
IDR: 147234235 | УДК: 549.242+547.53.024+548.312.2+548.312.5 | DOI: 10.14529/chem200302
Synthesis and structure of tetraphenylantimony pentafluoropropionate Ph4SbOC(O)CF2CF3
Tetraphenylantimony pentafluoropropionate has been obtained by the substitution reaction between pentaphenylantimony and pentafluoropropionic acid and by the ligand redistribution reaction between pentaphenylantimony and triphenylantimony bis (pentafluoropropionate) with a yield up to 96 %. The compound has been identified by IR spectroscopy and X-ray diffraction analysis. According to the X-ray diffraction data, the antimony atom has a distorted trigonal-bipyramidal coordination with the oxygen atom of the carboxylate ligand and the carbon atom of the phenyl ligand in apical positions. All fluorine atoms and the carbon atom of the CF3 group are disordered in two positions (the ratio of the contributions of the positions to the disordered fragment is 0.58/0.42). The CSbO axial angle is 178.19(1)º; the sum of the CSbC equatorial angles is 355.78(14)º. The antimony atom is out of the [C3] equatorial plane towards the axial carbon atom at 0.254 Å. The planes of the phenyl rings are rotated around the Sb-Ce bonds so that to minimize intra- and intermolecular interactions. The average Sb-Ce bond length is 2.129(4) Å, while the Sb-Ca bond length is comparable to the equatorial bond length and has the value of 2.124(3) Å. The Sb-O distance is 2.325(3) Å, which is greater than the sum of the covalent radii of antimony and oxygen atoms (2.07 Å). A characteristic feature of all tetraarylantimony carboxylates is the presence of an intramolecular contact between the antimony atom and the carbonyl oxygen atom. This Sb×××O=C distance is 3.492(5) Å, which is less than the sum of the van der Waals radii of antimony and oxygen atoms (3.70 Å). This interaction leads to an increase up to 122.67(14)° in one of the equatorial angles located on the side of the intramolecular contact. The organization of molecules in the crystal is due to hydrogen bonds involving a carbonyl oxygen atom. These contacts structure the molecules into layers that are perpendicular to the crystallographic axis b . Complete tables of atom coordinates, bond lengths and valence angles are deposited at the Cambridge Crystallographic Data Center (No. 1850118; deposit@ccdc.cam.ac.uk or http://www.ccdc.cam.ac.uk/data_request/cif).
Текст научной статьи Синтез и строение пентафторпропионата тетрафенилсурьмы Ph4SbOC(O)CF2CF3
По реакциям замещения между пентафенилсурьмой и пентафторпропионой кислотой и по перераспределению лигандов между пентафенилсурьмой и бис(пентафторпропионатом) трифенилсурьмы получен с выходом до 96 % пентафторпропионат тетрафенилсурьмы. Соединение идентифицировано методом ИК-спектроскопии и рентгеноструктурного анализа (РСА). По данным РСА, атом сурьмы имеет искаженную тригонально-бипирамидальную координацию с атомом кислорода карбоксилатного и атомом углерода фенильного лигандов в апикальных положениях. Все атомы фтора и углерод группы CF3 разупорядочены по двум положениям (соотношение вкладов положений в разупорядочен-ный фрагмент составляет 0,58/0,42). Аксиальный угол СSbO составляет 178,19(1)º, сумма экваториальных углов CSbC равна 355,78(14)º. Атом сурьмы выходит из экваториальной плоскости [C3] в сторону аксиального атома углерода на 0,254 Å. Плоскости фенильных колец повернуты вокруг связей Sb–Cэкв таким образом, чтобы минимизировать внутри- и межмолекулярные взаимодействия. Среднее значение длин связей Sb–Сэкв составляет 2,129(4) Å, при этом длина связи Sb–Сакс сопоставима с экваториальными и имеет значение 2,124(3) Å. Расстояние Sb–O составляет 2,325(3) Å, что больше суммы ковалентных радиусов сурьмы и кислорода (2,07 Å). Характерной особенностью всех карбоксилатов тетраарилсурьмы является наличие внутримолекулярного контакта атома сурьмы с карбонильным атомом кислорода. Данное расстояние Sb⋅⋅⋅O=C составляет 3.492(5) Å, что меньше суммы ван-дер-ваальсовых радиусов сурьмы и кислорода (3,70 Å). Это взаимодействие приводит к увеличению одного из экваториальных углов, расположенного со стороны внутримолекулярного контакта, до 122,67(14)°. Организация молекул в кристалле обусловлена водородными связями с участием карбонильного атома кислорода. Данные контакты структурируют молекулы в слои, расположенные перпендикулярно кристаллографической оси b. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1850118; или .
Достаточно хорошо структурно охарактеризованы соединения пятивалентной сурьмы общей формулы Ar 4 SbX (где X – лиганд, связанный с атомом сурьмы через гетероатом) [1–21]. Наиболее изученными из таких производных сурьмы(V) являются карбоксилаты тетрафенилсурьмы [22–39]. Синтез таких соединений осуществляют по реакциям замещения между кислотами и пентафенилсурьмой [22–24] или галогенидом тетрафенилсурьмы в присутствии акцептора гало-геноводорода [25–30], галогенидом тетрафенилсурьмы и солями карбоновых кислот [31]. Также известен менее распространенный способ синтеза по реакции перераспределения лигандов между Ph 5 Sb и производными симметричного строения Ph 3 SbX 2 [32–39].
В настоящей работе впервые по реакциям замещения и перераспределения лигандов синтезирован пентафторпропионат тетрафенилсурьмы и определены его структурные особенности методом рентгеноструктурного анализа.
Экспериментальная часть
Исходный реагент - пентафенилсурьму получали по методике, описанной в монографии [40]. В работе использовали пентафторпропионовую кислоту производства фирмы «Alfa Aesar».
Синтез пентафторпропионата тетрафенилсурьмы Ph4SbOС(O)CF2CF3 (1)
-
1. Смесь 200 мг (0,394 ммоль) пентафенилсурьмы и 65 мг (0,394 ммоль) пентафторпропионовой кислоты в 30 мл смеси растворителей бензол-изооктан (2:1 объемн.) оставляли до полного удаления растворителей. После перекристаллизации твердого остатка из смеси этанол–изооктан получили 224 мг (96 %) бледно-желтых кристаллов соединения 1 с т. пл. 135 °С.
-
2. Смесь 200 мг (0,394 ммоль) пентафенилсурьмы и 268 мг (0,394 ммоль) бис (пентафторпропионата) трифенилсурьмы в 3 мл бензола нагревали в запаянной ампуле на водяной бане при 80 °С в течение часа. После охлаждения к смеси прибавляли 0,5 мл октана и концентрировали раствор до объема 0,5 мл. Выпавшие бледно-желтые кристаллы отфильтровывали и сушили на воздухе. Получили 430 мг (92 %) соединения 1 с т. пл. 135 °С.
ИК-спектр, ν , см - 1: 3105, 3061, 1697, 1577, 1479, 1436, 1377, 1317, 1271, 1211, 1168, 1143, 1070, 1058, 1026, 997, 912, 860, 813, 773, 750, 738, 729, 698, 690, 657, 617, 584, 540, 466, 455, 447, 408.
Найдено, %: С 54,64; Н 3,55. C 27 H 20 O 2 F 5 Sb. Вычислено, %: С 54,66; Н 3,41.
ИК-спектр соединения 1 записывали на ИК-спектрометре Shimadzu IR Affinity-1S в таблетках KBr в области 4000–400 см–1.
Элементный анализ на С, Н проведен на Carlo-Erba 1106.
Рентгеноструктурный анализ (РСА) кристалла соединения 1 проведен на дифрактометре D8 QUEST фирмы Bruker (MoKα-излучение, λ = 0,71073 Å, графитовый монохроматор) при 296(2) К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [41]. Все расчеты по определению и уточнению структуры выполнены по программам SHELXL/PC [42], OLEX2 [43]. Структура определена прямым методом и уточнена методом наименьших квадратов в анизотропном приближении для неводородных атомов. Кристаллографические данные и результаты уточнения структуры приведены в табл. 1. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№1850118; или .
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры 1
|
Параметр |
1 |
|
М |
593,18 |
|
Сингония |
Моноклинная |
|
Пр. группа |
P2 1 /c |
|
a , Å |
10,188(3) |
|
b , Å |
27,219(9) |
|
c , Å |
10,364(3) |
|
α, град. |
90 |
|
β, град. |
118,283(10) |
|
γ, град. |
90 |
|
V , Å3 |
2530,8(13) |
|
Z |
4 |
|
ρ (выч.), г/см3 |
1,557 |
|
µ, мм–1 |
1,148 |
|
F (000) |
1176,0 |
|
Размер кристалла, мм |
0,36 × 0,30 × 0,13 |
|
Область сбора данных по 2θ, град. |
6,332–56,998 |
|
Интервалы индексов отражений |
–13 ≤ h ≤ 13, –36 ≤ k ≤ 36,–13 ≤ l ≤ 13 |
|
Измерено отражений |
47885 |
|
Независимых отражений |
6399 ( R int = 0,0316) |
|
Переменных уточнения |
336 |
|
GOOF |
1,178 |
|
R -факторы по F2>2σ(F2) |
R 1 = 0,0460, wR 2 = 0,1024 |
|
R -факторы по все отражениям |
R 1 = 0,0542, wR 2 = 0,1055 |
|
Остаточная электронная плотность (max/min), e/Å3 |
0,86/–1,28 |
Обсуждение результатов
Известно, что наиболее эффективными методами синтеза карбоксилатов тетраарилсурьмы являются методы, в основе которых лежат реакции замещения и перераспределения лигандов. В первом случае исходными соединениями являются пентаарилсурьма и карбоновая кислота [22– 24], во втором – пентаарилсурьма и дикарбоксилат триарилсурьмы [32–39]. Данные методы синтеза одностадийные, характеризуются мягкими условиями протекания реакций, высоким выходом и чистотой целевого продукта.
Синтез пентафторпропионата тетрафенилсурмы осуществлен по вышеуказанным методам. Реакцию замещения между пентафенилсурьмой и пентафторпропионовой кислотой проводили в смеси растворителей бензол–изооктан (2:1 объемн.) при комнатной температуре с последующей перекристаллизацией твердого остатка из смеси этанол–изооктан (2:1 объемн.) для получения кристаллов, пригодных для РСА. Взаимодействие пентафенилсурьмы и бис (пентафторпропионата) трифенилсурьмы осуществляли в бензоле в запаянной ампуле при нагревании на водяной бане с последующим добавлением октана:
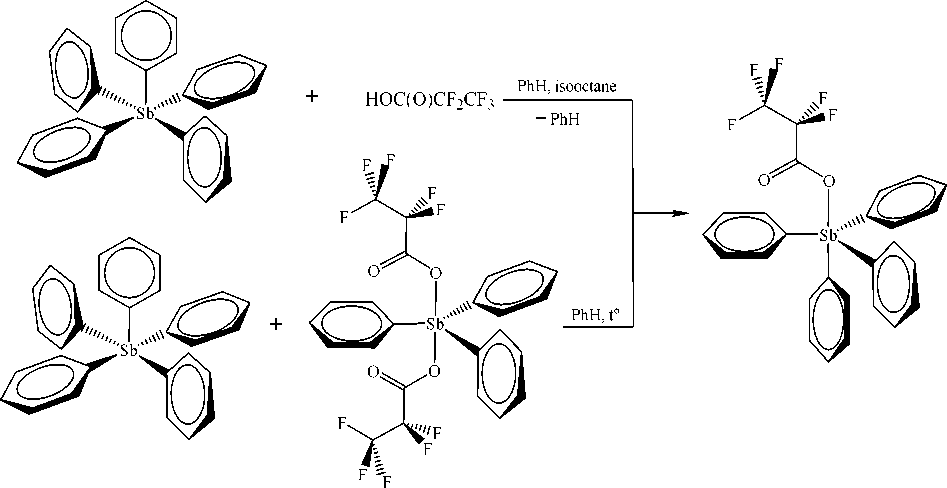
Соединение 1 представляет собой кристаллы бледно-желтого цвета с четкой температурой плавления, хорошо растворимые в ароматических углеводородах и полярных растворителях. Строение пентафторпропионата тетрафенилсурьмы подтверждено методами ИК-спектроскопии и рентгеноструктурного анализа.
В ИК-спектре соединения 1 наблюдается интенсивная полоса поглощения валентных колебаний связей Sb–C при 455 см–1. Полоса поглощения высокой интенсивности при 1697 см–1 характеризует валентные колебания карбонильной группы, а полосе при 1211 см–1 отвечают колебания ν(С–О). ИК-спектр также содержит характерные полосы валентных колебаний углеродного скелета фенильных лигандов: 1577, 1479, 1436 см–1. Валентным колебаниям связей CAr–H отвечает полоса поглощения средней интенсивности при 3061см–1, а внеплоскостным деформационным колебаниям этих же связей – полосы при 738 и 690 см–1. Ряд интенсивных полос при 1377, 1317, 1168 и 1143 см–1 принадлежит валентным колебаниям фрагмента CF 2 CF 3 [44, 45].
По данным РСА, атом сурьмы в соединении 1 имеет искаженную тригонально-бипирамидальную координацию с атомом кислорода карбоксилатного и атомом углерода фенильного лигандов в аксиальных позициях (рис. 1). Все атомы фтора и углерод группы CF 3 разу-порядочены по двум положениям. Уточненное соотношение вкладов положений в разупорядо-ченный фрагмент составляет 0,58/0,42.
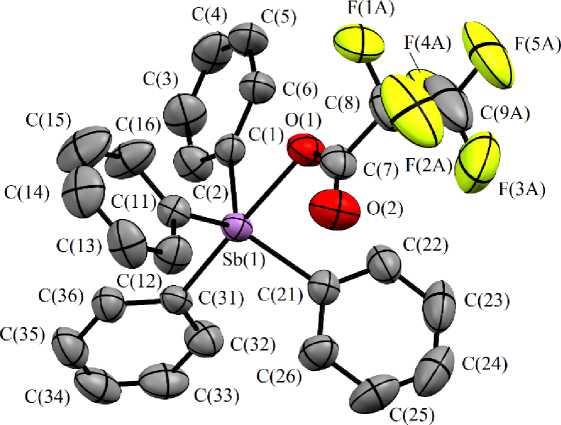
Рис. 1. Строение пентафторпропионата тетрафенилсурьмы (1) (атомы водорода не указаны)
Аксиальный угол СSbO составляет 178,19(1)º, сумма экваториальных углов CSbC равна 355,78(14)°. Значения углов Оа^ЬСэЮ меньше 90 ° (82,34(13)°, 85,32(13)°, 84,80(13)°), а Са^ЬСэЮ больше 90 ° (95, 8 9( 14 ) °, 98, 21( 14 ) ° , 96,54(14)°). Атом сурьмы выходит из экваториальной плоскости [C(1)C(11)C(21 ) ] в с т орон у а к с и а льного а тома у гле род а н а 0, 254Å. Плоскости фенильных колец повернуты вокруг связей S b –C экв таким образом, чтобы минимизировать внутри- и межмолекул я рн ы е в за и м оде й с тв ия. Д в угранные углы между экваториальной плоскос тью и плоскостями коле ц п ри э том с ос та в ля ю т 6, 43º [С(11)–С(16)], 39,32º [С(21)–С(26)], 86,93º [С(1)–С(6)]. Отметим, что плоскость кольца С(11)– С( 16) компланарна экваториальной плоскости, п ри э том у гол ме жд у э кват ори альн ой п лоск ост ью и п лоск ос т ью к ольц а С ( 1)–С(6) приближается к 90º.
Длины связей Sb–С экв в с ое д и н е н и и 1 составляют 2,123(4), 2,164(4), 2,100(4) Å, при этом длина связи Sb–С акс соп ос та в и м а с экваториальными и имеет значение 2,124 ( 3) Å. Расстояние Sb– O составляет 2,325(3) Å, ч т о больше суммы ковалентных радиусов сурьмы и кислорода (2,07 Å).
Ха р а к те рной ос обе н н ос т ью к а р б оксилатов тетраарилсурьмы является наличие внутримолекул я рн ого кон та к та ат о ма су рьмы с карбонильным атомом кислорода [ 20–39]. Расстояние Sb—O=C в с трук ту ре с оед и н е н и я 1 составляет 3,492(5) А, что меньше суммы ван-дер-ваальсовых р а д и у с ов с у рьмы и к и с ло род а (3,70 Å) [46]. Данное взаимодействие приводит к увеличению одн ого из э к в а тори а л ьн ых у глов C(11)Sb(1)C(21) (122,67(14)°), расположенного со стороны внутримолекулярного контакта.
Ин
те
рес
н
о с
ра
в
н
и
ть в
ли
я
н
ие схожих фторсодержащих карбоксилатны
х ли
г
а
н
д
ов
н
а
ос
новн
ы
е
п
а
ра
ме
тр
ы к
оор
д
и
н
ац
и
он
ного полиэдра атома сурьмы в карбоксилатах те
трафе
н
илс
у
рьмы
. Р
анее на
ми были
с
и
н
те
з
и
ров
а
н
ы ге
п
тафторб
у
ти
ра
т
[
3
3] и
3,
3,3
-трифторпропионат тетрафенил-сурь
м
ы [
34
]
. В
ыб
о
р
и
мен
н
о
э
тих соединений обусловлен увеличением э
ле
к
трон
о
а
к
ц
е
п
торных св
ойств
к
арб
о
к
с
и
л
а
тн
ых ли
га
н
д
ов в ряд
у OС(O)CH
2
CF
3
Проанализировав
да
н
н
ые
т
аб
л
. 2, можно сделать вывод о том, что с увеличением электроноакцеп
торны
х с
в
ой
с
тв
ли
га
н
д
ов
в
ряд
у OС(O)CH
2
CF
3
Таблица 2
Основные геометрические параметры карбоксилатов тетрафенилсурьмы
|
OC(O)R |
Выход атома Sb из плоскости [С3], Å |
max ∠ С э SbC э , град. |
∠ OSbC а , град. |
d (Sb–O), Å |
d (Sb–C), Å |
d (Sb∙∙∙O), Å |
|
CH 2 CF 3 |
0,209 |
1 21, 5 0(8 ) |
173,29(7) |
2,255(2) |
2,167(2) (акс) 2,109(2) (экв) 2,111(2) (экв) 2,117(2) (экв) |
3,414(3) |
|
CF 2 CF 3 |
0,254 |
1 22, 6 7(1 4) |
178,19(1) |
2,325(3) |
2,124(3) (акс) 2,100(4) (экв) 2,123(4) (экв) 2,164(4) (экв) |
3,492(5) |
|
CF 2 CF 2 CF 3 |
0,263 |
1 24, 4 7(1 0) |
178,87(8) |
2,340(2) |
2,154(3) (акс) 2,101(2) (экв) 2,110(3) (экв) 2,120(2) (экв) |
3,517(6) |
Организация молекул в кристалле соединений 1 обусловлена водородными связями с участием карбонильного атома кислорода. Расстояния Н∙∙∙O=C составляют 2,52 и 2,55 Å. Данные контакты структурируют молекулы в кристалле в слои, расположенные перпендикулярно кристаллографической оси b (рис. 2).
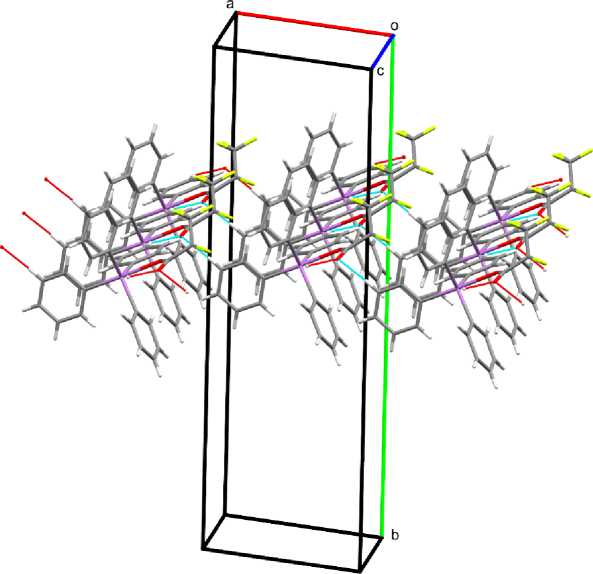
Рис. 2. Упаковка молекул в кристалле соединения 1 (показан только один слой)
Выводы
Таким образом, в настоящей работе по реакциям замещения и перераспределения лигандов получен с высоким выходом и структурно охарактеризован пентафторпропионат тетрафенилсурьмы. Координационный полиэдр атома сурьмы представляет собой искаженную тригональную бипирамиду с аксиально расположенным карбоксилатным лигандом. Формирование пространственной структуры кристаллов обусловлено образованием водородных связей с участием карбонильных атомов кислорода, при этом молекулы в кристалле образуют слои.
Выражаю благодарность профессору В.В. Шарутину за проведенные рентгеноструктурные исследования.
Список литературы Синтез и строение пентафторпропионата тетрафенилсурьмы Ph4SbOC(O)CF2CF3
- Cambridge CrystallograficDatebase. Release 2020. Cambridge.
- Synthesis, Crystal Structures and in vitro Antitumor Activities of Some Arylantimony Derivatives of Analogues of Demethylcantharimide / G.-C. Wang, J. Xiao, L. Yu et al. // J. Organomet. Chem. - 2004. - V. 689, № 9. - P. 1631-1638. DOI: 10.1016/j.jorganchem.2004.02.015.
- Синтез и строение цианамида тетрафенилсурьмы / И.В. Егорова, В.В. Жидков, И.П. Гри-нишак и др. // Журн. общей химии. - 2014. - Т. 84, № 7. - С. 1176-1178.
- Synthesis, Crystal Structures and in vitro Antitumor Activities of Some Organoantimony Aryl-hydroxamates / G.-C. Wang, Y.-N. Lu, J. Xiao et al. // J. Organomet. Chem. - 2005. - V. 690, № 1. -P. 151-156. DOI: 10.1016/j.jorganchem.2004.09.002.
- Spectroscopic and Crystal Structure Data of the Alkali-, Thallium (I) and Onic-salts of Dimethyl-N-trichloracetylamidophosphate / V.A. Trush, K.E. Gubina, V.M. Amirkhanov et al. // Polyhedron. -2005. - V. 24, № 9. - P. 1007-1014. DOI: 10.1016/j.poly.2005.01.023.
- Structure and Dynamic Behavior of Neutral Hexacoordinate Antimony Compounds with Intramolecular Coordination / H. Yamamichi, S. Matsukawa, S. Kojima et al. // Heteroat. Chem. - 2011. -V. 22, № 3-4. - P. 553-561. DOI: 10.1002/hc.20721.
- Synthesis, Characterization and Structure of Some Arylantimony Ferrocenylacrylates / J.-S. Li, R.-C. Liu, X.-B. Chi et al. // Inorg. Chim. Acta. - 2004. - V. 357, № 7. - P. 2176-2180. DOI: 10.1016/j.ica.2003.12.012.
- Синтез, структурное и MAS ЯМР (13С, 15N) спектральное исследование комплексов тетрафенилсурьмы с ^^диалкилдитиокарбаматными лигандами: проявление канформационной изомерии / А.В. Иванов, А.П. Пакусина, М.А. Иванов и др. // Докл. акад. наук СССР. - 2005. -Т. 401, № 5. - С. 643-647.
- Establishing the Coordination Chemistry of Antimony(V) Cations: Systematic Assessment of Ph4Sb(OTf) and Ph3Sb(OTfh as Lewis Acceptors / A.P.M. Robertson, S.S. Chitnis, H.A. Jenkins et al. // Chem. - Eur. J. - 2015. - V. 21, № 21. - P. 7902-7913. DOI: 10.1002/chem.201406469.
- Influence of the Catalyst Structure in the Cycloaddition of Isocyanates to Oxiranes Promoted by Tetraarylstibonium Cations / M. Yang, N. Pati, G. Belanger-Chabot et al. // Dalton Trans. - 2018. -V. 47. - P. 11843-11850. DOI: 10.1039/C8DT00702K.
- Tetraphenylantimony(V) 2-Isonitroso-2-(4-methylthiazolyl-2)acetamide: Synthesis, Crystal Structure, and Molecular Structure / K.V. Domasevich, V.V. Skopenko, R. Kempe et al. // Russ. J. Inorg. Chem. - 1998. - V. 43, № 2. - P. 192-195.
- Шарутин, В.В. Синтез и строение сольвата 1,2-дифенилэтандиондиоксимата бис(тетрафенилсурьмы) с толуолом Ph4SbONC(Ph)С(Ph)ONSbPh4 • 2PhCH3 и 1,2-дифенил(2-окси)этаноноксимата тетрафенилсурьмы Ph4SbONC(Ph)CH(Ph)OH / В.В. Шарутин, О.В. Молокова, О.К. Шарутина // Журн. неорг. химии. - 2013. - Т. 58, № 4. - С. 460-467. DOI: 10.7868/S0044457X13040181.
- Syntheses, Characterizations and Crystal Structures of New Organoantimony(V) Complexes with Heterocyclic (S, N) Ligand / C. Ma, Q. Zhang, J. Sun et al. // J. Organomet. Chem. - 2006. -V. 691, № 11. - P. 2567-2574. DOI: 10.1016/j.jorganchem.2006.01.049.
- Synthesis of Two Tetraphenylantimony Complexes of Pyridine-N-oxides; Crystal Structure of Tetraphenylantimony (2-Mercaptopyridine-N-oxide) / G.M. Arvanitis, M.E. Berardini, T.B. Acton et al. // Phosphorus, Sulfur Silicon, Relat. Elem. - 1993. - V. 82, № 1-4. - P. 127-135. DOI: 10.1080/10426509308047416.
- Ortho-metallation of a Phenyl Ring with Antimony(V) / N. Dinsdale, J.C. Jeffrey, R.J. Kilby et al. // Inorg. Chim. Acta. - 2007. - V. 360, № 1. - P. 418-420. DOI: 10.1016/j.ica.2006.07.091.
- Perrin, C.L. Symmetry of Metal Chelates / C.L. Perrin, Y.-J. Kim // Inorg. Chem. - 2000. -V. 39, № 17. - P. 3902-3910. DOI: 10.1021/ic000382+.
- Pan, B. [Sb(C6F5)4][B(C6F5)4]: An Air Stable, Lewis Acidic Stibonium Salt That Activates Strong Element-Fluorine Bonds / B. Pan, F.P. Gabbai // J. Am. Chem. Soc. - 2014. - V. 136, № 27. -P. 9564-9567. DOI: 10.1021/ja505214m.
- Шарутин, В.В. Синтез и строение пропиолатов три- и тетрафенилсурьмы / В.В. Шарутин, О.К. Шарутина, В.С. Сенчурин // Коорд. химия. - 2014. - Т. 40, № 2. - С. 108-112. DOI: 10.7868/S0132344X14020108.
- Domasevitch, K.V. Organoantimony(V) Cyanoximates: Synthesis, Spectra and Crystal Structures / K.V. Domasevitch, N.N. Gerasimchuk, A. Mokhir // Inorg. Chem. - 2000. - V. 39, № 6. -P. 1227-1237. DOI: 10.1021/ic9906048.
- Шарутин, В.В. Синтез и строение ароксидов тетрафенисурьмы Ph4SbOAr (Ar = C6H4C6H7, C6H2(Br2-2,6)(mpem-Bu-4), C6H3(NO2b-2,4, C6H2(Br2-2,6)(NO2-4)) / В.В. Шарутин, О.К. Шарутина, В.С. Сенчурин // Журн. неорг. химии. - 2017. - Т. 62, № 3. - С. 290-295. DOI: 10.7868/S0044457X17030151.
- Шарутин, В.В. Новый способ получения ароксидов хлоротрифенилсурьмы Ph3SbCl(OAr) / В.В. Шарутин, О.К. Шарутина, В.С. Сенчурин // Коорд. химия. - 2016. - Т. 42, № 1. - С. 34-38. DOI: 10.7868/S0132344X15120075.
- Dihydroxybenzoic Acids as Polydentate Ligands in Phenylantimony (V) Complexes / V.V. Sharutin, O.K. Sharutina, Y.O. Gubanova et al. // Inorg. Chim. Acta. - 2019. - V. 494. - P. 211215. DOI: 10.1016/j.ica.2019.05.029
- Bone, S.P. The Crystal Structures of Tetraphenylantimony Acetate and Its / S.P. Bone, D.B. Sowerby // Phosphorus, Sulfur Silicon, Relat. Elem. - 1989. - V. 45, № 1-2. - P. 23-29. DOI: 10.1080/10426508908046072
- Синтез и строение ниацината тетрафенилсурьмы / В.В. Шарутин, А.П. Пакусина, Т.П. Платонова и др. // Журн. общ. химии. - 2004. - Т. 74, №. 2. - С. 234-237.
- Synthesis, Characterizations and Crystal Structures of New Organoantimony(V) Complexes with Various Isomers of Fluoromethylbenzoate Ligands / H.-D. Yin, L.-Y. Wen, J.-C. Cui et al. // Polyhedron. - 2009. - V. 28, № 14. - P. 2919-2926. DOI: 10.1016/j.poly.2009.06.065.
- Synthesis, Characterization and Crystal Structures of Tri- and Tetraphenylantimony(V) Compounds Containing Arylcarbonyloxy Moiety / L. Quan, H.-D. Yin, J.-C. Cui et all. // J. Organomet. Chem. - 2009. - V. 694, № 23. - P. 3708-3717. DOI: 10.1016/j.jorganchem.2009.07.040.
- New Organoantimony Complexes with the Isomers of Chlorophenylacetic Acid: Syntheses, Characterizations and Crystal Structures of 1D Polymeric Chain, 2D Network Structure and 3D Framework / L.-Y. Wen, H.-D. Yin, W.-K. Li et al. // Inorg. Chim. Acta. - 2010. - V. 363, № 4. - P. 676-684. DOI: 10.1016/j.ica.2009.11.022.
- Synthesis, Characterization and in vitro Antitumor Activity of Some Arylantimony Ferrocene-carboxylates and Crystal Structures of C5H5FeC5H4CO2SbPh4 and (C5H5FeC5H4CO2)2Sb(4-CH3C6H4)3 / R.-C. Liu, Y.-Q. Ma, L. Yu et al. // Appl. Organomet. Chem. - 2003. - V. 17, № 9. - P. 662-668. DOI: 10.1002/aoc.491.
- Synthesis and in vitro Antitumor Activity of Some Tetraphenylantimony Derivatives of exo-7-Oxa-bicyclo[2,2,1]heptane(ene)-3-arylamide-2-acid / J.-S. Li, Y.-Q. Ma, J.-R. Cui et al. // Appl. Organomet. Chem. - 2001. - V. 15, № 7. - P. 639-645. DOI: 10.1002/aoc.200.
- Synthesis and Crystal Structure of Dinuclear Tetraphenylantimony Carboxylate Derivatives Based on Different Coordination Modes / L. Quan, H. Yin, J. Cui, et al. // J. Organomet. Chem. -2009. - V. 694, № 23. - P. 3683-3687. DOI: 10.1016/j.jorganchem.2009.07.041.
- Millington, P.M. Phenylantimony(V) Oxalates: Isolation and Crystal Structures of [SbPh4][SbPh2(ox)2], [SbPh3(OMe)]2ox and (SbPh4)2ox / P.M. Millington, D.B. Sowerby // J. Chem. Soc., Dalton Trans. - 1992. - V. 7. - P. 1199-1204. DOI: 10.1039/DT9920001199.
- Термохимические свойства Ph4Sb(OC(O)Ci0H15) и Ph3Sb(OC(O)Ci0H15)2 / Д.В. Лякаев, А.В. Маркина, Е В. Хабарова и др. // Журн. физ. химии. - 2018. - Т. 92, № 9. - С. 1384-1389. DOI 10.1134/S0044453718090170.
- Синтез и строение 3,3,3-трифторпропанатов три- и тетрафенилсурьмы / В.В. Шарутин, О.К. Шарутина, А.Н. Ефремов и др. // Журн. неорг. химии. - 2019. - Т. 64, № 10. - С. 1051-1056. DOI: 10.1134/S0044457X19100131.
- Фторсодержащие карбоксилаты тетраарилсурьмы. Синтез и строение / В.В. Шарутин, О.К. Шарутина, А.Н. Ефремов и др. // Журн. неорг. химии. - 2020. - Т. 65, № 4. - С. 482-486. DOI: 10.31857/S0044457X20040170.
- Синтез фторбензоатов тетра- и триарилсурьмы / В.В. Шарутин, О.К. Шарутина, Е.А. Бондарь и др. // Журн. общ. химии. - 2002. - Т. 72, №. 3. - С. 419-420.
- Синтез и строение пентафторбензоата тетрафенилсурьмы и нитрата тетра-и-толилсурьмы / В.В. Шарутин, О.К. Шарутина, Е.А. Бондарь и др. // Коорд. химия. - 2001. - Т. 27, № 6.- С. 423-427.
- Синтез и строение фторбензоатов тетра- и триарилсурьмы / В.В. Шарутин, О.К. Шарутина, Е.А. Бондарь, А.П. Пакусина и др. // Коорд. химия. - 2002. - Т. 28, № 5. - С. 356363.
- Синтез и строение феноксиацетата и этилмалоната тетрафенилсурьмы Ph4SbOC(O)R [R = CH2OPh, CH2C(O)OC2H5] / В.В. Шарутин, А.П. Пакусина, О.П. Задачина и др. // Коорд. химия. -2004. - Т. 30, № 6. - С. 426-431.
- Синтез и строение 1-адамантанкарбоксилата тетрафенилсурьмы и бис(1- адамантанкар-боксилата) трифенилсурьмы / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина и др. // Журн. общ. химии. - 2009. - Т. 79, №. 10. - С. 1636-1643.
- Кочешков, К.А. Методы элементоорганической химии. Сурьма, висмут / К.А. Кочешков, А.П. Сколдинов, Н.Н. Землянский. - М.: Наука, 1976. - 483 с.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures From Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: Complete Structure Solution, Refinement and Analysis Program / O.V. Dolomanov, L.J. Bourhis, R.J. Gildea et al. // J. Appl. Cryst. - 2009. - V. 42. - P. 339-341. DOI: 10.1107/S0021889808042726.
- Тарасевич, Б.Н. ИК-спектры основных классов органических соединений / Б.Н. Тарасевич. - М.: МГУ, 2012. - 54 с.
- Инфракрасная спектроскопия органических и природных соединений: учебное пособие / А.В. Васильев, Е В. Гриненко, А О. Щукин и др. - СПб.: СПбГЛТА, 2007. - 54 с.
- Бацанов, С.С. Атомные радиусы элементов / С.С. Бацанов // Журн. неорган. химии. -1991. - Т. 36, № 12. - С. 3015-3037.


