Синтез и строение Производного три-пара-толилсурьмы с гликолевой кислотой
Автор: Гущин А.В., Вахитов В.Р., Воробьев И.И., Сомов Н.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 1 т.17, 2025 года.
Бесплатный доступ
Взаимодействием три- пара -толилсурьмы с трет -бутилгидропероксидом и гликолевой кислотой (1:1:2) получен 2,2,2-три- пара -толил-1,3-диокса-2λ5-стиболан-4-он с выходом 75 %. Была проведена оценка его строения методами ЯМР и РСА. В отличие от описанной ранее аналогичной реакции трифенилсурьмы с пероксидом водорода и молочной кислотой, в ходе данной реакции образуется именно циклометаллическое соединение, а не соответствующий дикарбоксилат, что становится очевидным из спектральной картины, в которой отсутствует сигнал гидроксильной группы. Кристаллы C23H23O3Sb описываются ромбической группой симметрии Pbca с параметрами элементарной ячейки a = 15,01871(11), b = 15,37651(11), c = 17,04701(12) Å, Z = 8. Используя структурный параметр τ, был сделан вывод о том, что координация атома сурьмы в данном МОС близка к тригонально-бипирамидальной (по данным РСА τ = 0,77). Результаты РСА, включающие координаты атомов, длины связей и валентные углы депонированы в Кембриджский банк структурных данных (CCDC 2370604).
Три-пара-толилсурьма, гликолевая кислота, 2, 2, 2-три-пара-толил-1, 3-диокса-2λ5-стиболан-4-он, синтез, строение, ямр-спектроскопия, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147248064
IDR: 147248064 | УДК: 547.1’13+547.47 | DOI: 10.14529/chem250105
Synthesis and structure of a tri-p-tolylantimony derivative of glycolic acid
Interaction of tri- p -tolylantimony with tert -butylhydroperoxide and glycolic acid (1:1:2) led to 2,2,2-tri- p -tolyl-1,3-dioxa-2λ5-stibolan-4-one in 75% yield. Its structure was evaluated by NMR and X-ray methods. Unlike the previously described similar reaction of triphenylantimony with hydrogen peroxide and lactic acid, during this reaction it is a cyclometallic compound that is formed, and not the corresponding dicarboxylate, which becomes obvious from the spectrum pattern, in which there is no signal of the hydroxyl group. The C23H23O3Sb crystals are described by the rhombic symmetry group Pbca with cell parameters: a = 15.01871(11), b = 15.37651(11), c = 17.04701(12) Å, Z = 8. Using the structural parameter τ, it has been concluded that the coordination of the antimony atom in this organometallic compound is close to trigonal-bipyramidal (according to the X-ray data, τ = 0.77). The XRD data, including the coordinates of atoms, bond lengths and valence angles, are deposited in the Cambridge Structural Database (CCDC 2370604).
Текст научной статьи Синтез и строение Производного три-пара-толилсурьмы с гликолевой кислотой
Исследование металлоорганических соединений сурьмы(V) является активно развивающейся областью современной металлоорганической химии ввиду их широкого применения в различных сферах научной деятельности [1]. Дикарбоксилаты триарилсурьмы используются в реакциях кросс-сочетания, катализируемых палладием, для образования связей C–C [2–8], C–B [9] и C-P [10]. Также дикарбоксилаты триарилсурьмы имеют медицинское применение: они обладают антилейшманиальной [11], а некоторые салицилатные производные – противоопухолевой активностью [12, 13]. Наличие в карбоксилатном фрагменте кратных связей, способных к полимеризации, открывает новые перспективы для использования их в фотолитографии в качестве высокочувствительных УФ-резистов [14] и для получения металлосодержащих полимерных материалов [15].
Особый интерес вызывают циклометаллические производные Sb(V) с α-гидроксикислотами. Известен ряд соединений подобного строения и выявлена следующая закономерность: взаимодействие Ph 3 Sb со стерически затрудненными в α-положении оксикислотами приводит к образованию соответствующего дикарбоксилата, например, с бензиловой кислотой – Ph 3 Sb(O 2 CC(OH)Ph 2 ) 2 , в противном случае возможна циклизация [16]. Несмотря на эту закономерность, было получено и охарактеризовано дикарбоксилатное производное трифенилсурьмы с молочной кислотой – Ph 3 Sb(O 2 CCH(OH)CH 3 ) 2 [17]. Взаимодействием диалкоголятов триоргано-сурьмы с гликолевой и тиогликолевой кислотами также могут быть получены соединения строения R 3 Sb(XCH 2 C(O)O), в том числе устойчивые алкоксиды, где X = O [18], и термически нестабильные тиолаты, где X = S [19]. Циклометаллаты триарилсурьмы с гликолевой и миндальной кислотами также исследованы на предмет проявления ими антилейшманиальной активности [20], а производные хиральных гидроксикислот являются эффективными катализаторами в реакциях асимметрического гидрирования бензоксазинов и хинолинов [21].
В настоящей работе рассматривается синтез и особенности строения p -Tol 3 Sb(OCH 2 C(O)O) [2,2,2-три- пара -толил-1,3-диокса-2λ5-стиболан-4-она, или моногликолата три- пара -толилсурьмы], полученного окислением смеси три- пара -толилсурьмы и гликолевой кислоты трет -бутилгидропероксидом.
Экспериментальная часть t-BuOOH (т. кип. 133 °С) получали из коммерческого 70%-ного водного раствора: сушили над безводным MgSO4 с дальнейшей перегонкой в ловушку, охлаждаемую жидким азотом. Концентрация трет-бутилгидропероксида составила 99 %.
Синтез 2,2,2-три-пара-толил-1,3-диокса-2λ5-стиболан-4-она (1) . К раствору 0,395 г p -Tol3Sb (1 ммоль) в 5 мл диэтилового эфира добавляли 0,152 г гликолевой кислоты (2 ммоль) и 0,09 г трет -бутилгидропероксида (1 ммоль). Колбу с реакционной смесью перемешивали в течение 20 мин и оставляли в холодильнике на 24 ч. Выпавшие бесцветные кристаллы отделяли фильтрованием, промывали 2 раза петролейным эфиром, перекристаллизовывали из смеси хлороформа и петролейного эфира (1/8). Выход 75 %, т. пл. 140–146 °C. ИК-спектр (ν, см-1, таблетка KBr): 3013, 2911, 1699, 1601, 1558, 1493, 1441, 1393, 1321, 1312, 1211, 1186, 1111, 1069, 1016, 930, 799, 737,
-
704, 579, 536, 482. Спектр ЯМР 1Н (400 MHz, CDCl 3 ), δ, м. д.: 2,39 (s, 9H, C 6 H 4 -Me), 4,22 (s, 2H, CH 2 ), 7,28 (d, J = 7,8 Hz, 6H, m -C 6 H 4 ), 7.61 (d, J = 8,1 Hz, 6H, o -C 6 H 4 ). ЯМР 13C (101 MHz, CDCl 3 ), δ, м. д.: 21,67 (Me), 62,00 (CH 2 ), 130,31 ( m -C 6 H 4 ), 131,55 (Sb-C), 135,50 ( o -C 6 H 4 ), 142,42 ( p -C 6 H 4 ), 174,67 (C=O).
Спектры ЯМР 1 H и 13 C регистрировали в CDCl 3 на ЯМР-спектрометре Agilent DD2 400.
ИК-спектр соединения 1 регистрировали на приборе IR Prestige-21 (Shimadzu, Япония) в диапазоне 4000–400 см-1 в таблетке KBr, приготовленной с помощью ручного гидравлического пресса «ПГР-400».
Рентгеноструктурный анализ (РСА) проводили на автоматическом дифрактометре Rigaku XtaLab MM003 P200K (Mo K α -излучение, λ = 0,71073 Å, монохроматор MicroMax-003) при 100 К. Первичный фрагмент структуры 1 найден методом двойного пространства в программных комплексах SHELX [22] и ShelXle [23]. Параметры остальных атомов, включая атомы водорода, определены по разностному синтезу электронной плотности и уточнены по |F|2 методом наименьших квадратов. Положения водородных атомов уточнялись в основном цикле метода наименьших квадратов в изотропном приближении.
Обсуждение результатов
При взаимодействии три- пара -толилсурьмы с двумя эквивалентами гликолевой (гидроксиук-сусной) кислоты в присутствии ГПТБ был впервые синтезирован 2,2,2-три- пара -толил-1,3-диокса-2λ5-стиболан-4-он ( 1 ), вместо ожидаемого дигликолата три- пара -толилсурьмы (схема 1). Гидроксиуксусная кислота присоединяется к атому металла не только по карбоксильной, но и по гидрокси-группе, а второй эквивалент кислоты остается непрореагировавшим, что было доказано методом 1H ЯМР-спектроскопии.
Х^> /)-То1з8Ь(О2ССН2ОН)2 + /-BuOH + H2O
/i-Tol3Sb + HO2CCH2OH + r-BuOOH
24h, RT
/-BuOH + H2O
Схема 1
Ранее были опубликованы результаты реакции трифенилсурьмы с пероксидом водорода и молочной кислотой (1:1:2), в результате которой получился дилактат трифенилсурьмы [17]. Вероятно, изменение направления реакции связано с различием окислителя и растворителя (дилактат получался в смешанном растворителе эфир/изопропиловый спирт, пероксид водорода содержал 58,7% воды, молочная кислота содержала 13 % воды).
В 1H ЯМР-спектре соединения 1 в области слабого поля (7,28–7,61 м. д.) находятся дублетные сигналы протонов ароматических колец (C 6 H 4 ) и два сигнала протонов, выходящих синглетами на 4,22 и 2,39 м. д., соответствующих метиленовому фрагменту в карбоксилатном заместителе и метильной группе у ароматического кольца в пара -положении к атому сурьмы, соответственно. В спектре отсутствует сигнал гидроксильной группы, что свидетельствует о невозможности протекании реакции по первому пути с образованием дикарбоксилата (схема 1).
В 13C ЯМР-спектре исследуемого соединения число сигналов совпадает с числом различных видов углеродных атомов, порядок уменьшения химических сдвигов атомов углерода в пара -толильных группах при атоме Sb o -C 6 H 4 > m -C 6 H 4 согласуется с протонным спектром. Малоинтенсивный сигнал атома углерода при атоме сурьмы выходит синглетом на 131,55 м. д., остальные сигналы углеродных атомов можно интерпретировать однозначно. Подробное описание 1H и 13C ЯМР-спектров приведено в экспериментальной части работы.
Для соединения 1 были выращены бесцветные монокристаллы размером 0,700×0,600×0,270 мм и был проведен их рентгеноструктурный анализ (рис. 1). По данным РСА, валентный угол φ(O2SbC3) имеет значение 168°, что близко к 180° и характерно для тригональной бипирамиды. Также характерной чертой тригонально-бипирамидальной конфигурации является тот факт, что сумма углов C17SbC10, O1SbC10 и O1SbC17 в экваториальной плоскости близка к 360° (см. таблицу).
Основные межатомные расстояния (Å) и валентные углы (град) в соединении 1
|
Межатомные расстояния |
Валентные углы |
||||
|
Связь |
d, Å |
Угол |
φ, град |
Угол |
φ, град |
|
Sb–C3 |
2,1295(15) |
O2SbC3 |
168,32(5) |
O1SbC3 |
89,44(5) |
|
Sb–C10 |
2,1078(15) |
C17SbC10 |
114,87(6) |
C3SbC10 |
99,90(6) |
|
Sb–C17 |
2,1027(15) |
O1SbC10 |
122,05(6) |
C3SbC17 |
99,05(6) |
|
Sb–O1 |
1,9671(11) |
O1SbC17 |
119,81(6) |
O2SbC10 |
86,34(5) |
|
Sb–O2 |
2,1397(11) |
O1SbO2 |
78,88(5) |
O2SbC17 |
87,07(5) |
Данное металлоорганическо е соединение описывается координационным числом, равным 5, следовательно, о способе коорди нации атома металла можно судить, проана лизировав структу рный параметр τ [24 ], который определяется как ( α – β)/60, где α и β – величины двух наибольших углов между заместителями при атоме Sb ( α > β). Для идеальной тетрагональной пирамиды τ = 0 (α = β), а в случае идеальной тригональной бипирамиды τ = 1 (аксиальный угол α = 180°, экваториальный β = 120°). Для сое динения 1 параметр τ = 0,77. В соответствии с этим, координацион ное окружение атома сурьмы в данном соединении ближе к тригонально -бипирамидальному, чем к тетрагонально- пирамидальному (рис. 2). Остальные углы, расположенные не в экваториальной плоскости бипирамиды, имеют значения, близкие к 90°.
Тригонально- бипирамидальн ую координацию атома сурьмы также подтв ерждает расчет ст е пени подобия координационного полиэдра тригональной бипирамиде Ф Δ = 0,45691(18) и тетрагональной пирамиде Ф □ = 0,23407(17) [ 25]. Степень искажения распределения электронной плотно сти координационного окружен ия атома сурьмы, рассчитанная для тригона льной бипирамиды, составила η Δ [ρ(x)]= 0,578( 1), это свидетельствует, что примерно на 76 % распределения элек тронной плотности соответствует и деализированной тригонально-бипирамидальной конфигурации [26].
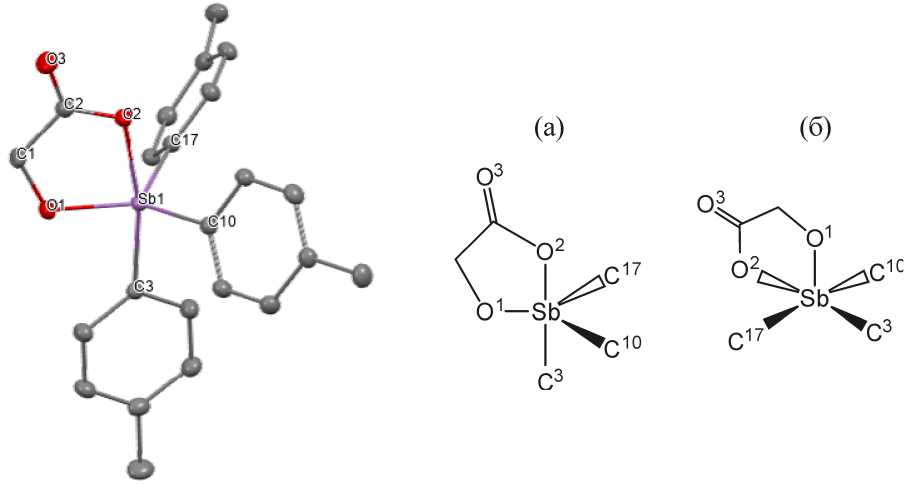
Рис. 1. Кристаллическая структура соединения 1 Рис. 2. Фрагмент структуры соединения 1
с конфигурацией тригональной бипирамиды (а) и тетрагональной пирамиды (б)
Заключение
Установлено, что взаимодействие три - пара -толилсурьмы с гликолевой кислотой в присутствии трет - бутилгидропероксида приводит к образованию 2,2,2 -три- пара -толил-1,3-диокса-2λ5-стиболан-4-она ( 1), а не к дигли колату, в отличие от известной реакции с ис пользованием H 2 O 2 . По данным РСА координация ат ома сурьмы в исследуемом соединении бли же к структуре тр и гональной бипирамиды, чем к тетрагональной пирамиде.


