Синтез и строение сольвата 2,4-динитробензолсульфоната тетра(пара-толил)сурьмы с ацетоном
Автор: Тарасова Наталья Михайловна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 2 т.14, 2022 года.
Бесплатный доступ
Взаимодействием эквимолярных количеств пента-пара-толилсурьмы с 2,4-динитробензолсульфоновой кислотой в бензоле с последующей перекристаллизацией из водного ацетона получен и структурно охарактеризован сольват 2,4-динитробензолсульфонат тетра(пара-толил)сурьмы с ацетоном p-Tol4SbOSO2C6H3(NO2)2-2,4 ∙ Me2C=O (1). По данным рентгеноструктурного анализа, проведенного при 293 К на автоматическом четырехкружном дифрактометре D8 Quest Bruker (двухкоординатный CCD- детектор, Мо Кα-излучение, λ = 0,71073 Å, графитовый монохроматор) кристалла 1 [C37H37N2O8SSb, M 791,50; сингония моноклинная, группа симметрии С2/с; параметры ячейки: a = 23,232(13), b = 13,522(9), c = 23,812(15) Å; β = 102,22(3) град.; V = 7311(8) Å3; размер кристалла 0,4×0,14×0,07 мм; интервалы индексов отражений -34 ≤ h ≤ 34, -19 ≤ k ≤ 19, -35 ≤ l ≤ 31; всего отражений 111477; независимых отражений 12261; Rint 0,0870; GOOF 1,009; R1 = 0,0411, wR2 = 0,0710; остаточная электронная плотность 0,37/-0,68 e/Å3], атомы сурьмы имеют искаженную тетраэдрическую координацию (СSbС 99,85(9)- 123,74(9)°), однако присутствует координация одного из атомов кислорода сульфогруппы с центральным атомом металла (расстояние Sb∙∙∙O составляет 2,814(4) Å), поэтому правильнее считать координацию центрального атома металла тригонально-бипирамидальной (аксиальный угол O(1)Sb(1)C(11) 172,78(8)°, экваториальные углы составляют 123,74(8), 114,60(8), 102,92(8)°). Длины связей Sb-C в 1 изменяются в узком интервале значений (2,091(2)-2,111(2) Å). Структурная организация в кристалле 1 обусловлена слабыми межмолекулярными контактами типа О···Н-C 2,25-2,69 Å. Полные таблицы координат атомов, длин связей и валентных углов для структуры 1 депонированы в Кембриджском банке структурных данных (№ 2123785; deposit@ccdc.cam.ac.uk; https://www.ccdc.cam.ac.uk).
2, 4-динитробензолсульфоновая кислота, пента(пара-толил)сурьма, ацетон, сольват, 2, 4-динитробензолсульфонат тетра(пара-толил)сурьмы, синтез, строение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147237504
IDR: 147237504 | УДК: 546.865+547.47+548.312.5
Synthesis and structure of the acetone solvate of tetra(para-tolyl)antimony 2,4-dinitrobenzensulfonate
By the interaction of equimolar amounts of penta-para-tolylantimony with 2,4-dinitrobenzenesulfonic acid in benzene, followed by recrystallization from aqueous acetone, the tetra-(para-tolyl)antimony 2,4-dinitrobenzenesulfonate acetone solvate Tol4SbOSO2C6H3(NO2)2-2.4 ∙ Me2C=O (1) was obtained and structurally characterized. According to X-ray diffraction analysis of crystal 1 [C37H37N2O8SSb, M 791.50; monoclinic syngony, space group C2/c; cell parameters: a = 23.232(13), b = 13.522(9), c = 23.812(15) Å; β = 102.22(3) degrees.; V = 7311(8) Å3; crystal size 0.4 × 0.14 × 0.07 mm; reflection index intervals -34 ≤ h ≤ 34, -19 ≤ k ≤ 19, -35 ≤ l ≤ 31; total reflections 111477; independent reflections 12261; Rint 0.0870; GOOF 1.009; R1 = 0.0411, wR2 = 0.0710; residual electron density 0.37/-0.68 e/Å3] performed by an automatic four-circle D8 Quest Bruker diffractometer (MoKα radiation, λ = 0.71073 Å, graphite monochromator) at 293 K, the antimony atoms have a distorted tetrahedral coordination (the СSbС angles are 99.85(9)°- 123.74(9)°). However, due to the coordination of one of the sulfo group oxygen atoms with the central metal atom (the Sb∙∙∙O distance is 2.814(4) Å) it is more correct to consider the coordination of the central metal atom as trigonal-bipyramidal (axial angle O(1)Sb(1)C(11) 172.78(8)°, the equatorial angles are 123.74(8), 114.60(8), 102.92(8)°). The Sb-C bond lengths in compound 1 vary in a narrow interval (2.091(2)-2.111(2) Å). The structural organization in crystal 1 is caused by weak intermolecular contacts of the О···Н-C type, 2.25-2.69 Å. Complete tables of coordinates of atoms, bond lengths and valence angles for structure 1 are deposited at the Cambridge Structural Data Bank (No. 2123785; deposit@ccdc.cam.ac.uk; http: //www.ccdc.cam.ac.uk).
Текст научной статьи Синтез и строение сольвата 2,4-динитробензолсульфоната тетра(пара-толил)сурьмы с ацетоном
К настоящему времени известны две обзорные работы, в которых описаны методы синтеза [1] и особенности строения арильных соединений сурьмы [2]. Из всех органических соединений сурьмы менее всего представлены ее сульфонатные производные, среди которых следует выделить сульфонаты тетраарилсурьмы Ar4SbOSO2R, преимущественно получаемые из пентаа-рилсурьмы и кислоты [3 - 13]. Продолжая исследования в указанном направлении в настоящей работе описаны синтез и кристаллическое строение сольвата 2,4-динитробензолсульфоната тет-ра( пара -толил)сурьмы с ацетоном.
Экспериментальная часть
Синтез сольвата 2,4-динитробензолсульфоната тетра( пара -толил)сурьмы с ацетоном (1) . К раствору 0,073 г (0,13 ммоль) пента- пара -толилсурьмы в 10 мл бензола прибавляли 0,032 г (0,13 ммоль) 2,5-динитробензолсульфоновой кислоты и нагревали до образования прозрачного раствора, через 24 ч растворитель испаряли при комнатной температуре, остаток перекристаллизовывали из смеси вода – ацетон 10:2. Получили 0,065 г (68 %) прозрачных бесцветных кристаллов 1 с т. разл. 88 °С. Найдено: C 56,02; H 4,72; C37H37N2O8SSb. Вычислено: C 56,10; H 4,67.
Элементный анализ на C и H выполнен на элементном анализаторе Carlo Erba CHNS-O EA 1108.
ИК-спектр, ( v , см - 1): 3101, 3047, 2918, 1707, 1593, 1548, 1525, 1497, 1396, 1352, 1263, 1213, 1188, 1112, 1068, 1028, 902, 806, 800, 748, 740, 663, 632, 584, 565, 551, 532, 482, 466, 420.
ИК-спектр соединения 1 записывали на ИК-Фурье спектрометре Shimadzu IR Affinity-1S в таблетке KBr в области 4000 - 400 см - 1.
Рентгеноструктурный анализ ( РСА ) кристалла 1 проведен на автоматическом четырехкружном дифрактометре D8 QUEST фирмы Bruker (Mo K α -излучение, λ = 0,71073 Å, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены с помощью программ SMART и SAINT-Plus [14]. Все расчеты по определению и уточнению структуры выполнены с помощью программ SHELXL/PC [15], OLEX2 [16]. Структура определена прямым методом и уточнена методом наименьших квадратов в анизотропном приближении для неводородных атомов. Положение атомов водорода уточняли по модели наездника ( U изо (H) = 1,2 U экв (C)) . Кристаллографические данные и результаты уточнения структуры приведены в табл. 1, основные длины связей и валентные углы – в табл. 2.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры 1
|
Параметр |
Соединение 1 |
|
Формула |
C 37 H 37 N 2 O 8 SSb |
|
М |
791,50 |
|
Т , К |
293 |
|
Сингония |
Моноклинная |
|
Пр. группа |
С 2/ с |
|
a , Å |
23,232(13) |
|
b, Å |
13,522(9) |
|
c, Å |
23,812(15) |
|
α ,º |
90,00 |
|
β,º |
102,22(3) |
|
γ ,º |
90,00 |
|
V , Å3 |
7311(8) |
|
Z |
8 |
|
ρ (выч.), г/см3 |
1,438 |
|
µ , мм–1 |
0,864 |
|
F (000) |
3232,0 |
|
Размер кристалла, мм |
0,4 × 0,14 × 0,07 |
|
Область сбора данных по 2 θ , град. |
6 - 63,34 |
|
Интервалы индексов отражений |
- 34 ≤ h ≤ 34, - 19 ≤ k ≤ 19, - 35 ≤ l ≤ 31 |
|
Измерено отражений |
111477 |
|
Независимых отражений |
12261 |
|
R int |
0,0870 |
|
Переменных уточнения |
448 |
|
GOOF |
1,009 |
|
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0411, wR 2 = 0,0710 |
|
R -факторы по всем oтражениям |
R 1 = 0,0998, wR 2 = 0,0841 |
|
Остаточная электронная плотность (min/max), e/A3 |
0,37/ - 0,68 |
Таблица 2
Длины связей и валентные углы в соединении 1
|
Связь |
d , Å |
Угол |
ω , град. |
|
Sb(1) - С(31) |
2,100(2) |
O(1)Sb(1)С(11) |
172,78(8) |
|
Sb(1) - С(21) |
2,091(2) |
C(21)Sb(1)C(31) |
123,74(8) |
|
Sb(1) - С(11) |
2,111(2) |
C(21)Sb(1)C(11) |
102,92(8) |
|
Sb(1) - С(1) |
2,095(2) |
C(21)Sb(1)C(1) |
107,81(9) |
|
Sb(1)∙∙∙О(1) |
2,814(4) |
C(1)Sb(1)С(31) |
114,60(8) |
|
S(1) - О(1) |
1,4488(17) |
C(1)Sb(1)С(11) |
105,21(10) |
|
S(1) - О(3) |
1,4360(18) |
О(1)S(1)С(41) |
105,01(10) |
|
S(1) - О(2) |
1,4380(18) |
О(3)S(1)O(1) |
113,53(11) |
|
S(1) - С(41) |
1,799(2) |
О(3)S(1)O(2) |
114,17(11) |
.
Обсуждение результатов
Найдено, что продуктом реакции пента(пара-толил)сурьмы с 2,4-динитро бензолсульфоновой кислотой в бензоле является 2,4-динитробензолсульфонат тетра(пара-толил)сурьмы, который выделяли из реакционной смеси после перекристаллизации из водного ацетона в виде сольвата p-Tol4SbOSO2C6H3(NO2)-2,4 ∙ Me2C=O (1):
p -To^Sb + HOSO 2 C 6 H 3 (NO 2 )-2,4 ^ p -ToUSbOSO 2 C 6 H 3 (NO 2 )-2,4 • Me 2 C=O
Бесцветные прозрачные кристаллы 1 устойчивы к действию влаги и кислорода воздуха, растворимы в ацетоне, ароматических углеводородах, хлороформе и диоксане. В ИК-спектре сульфоната 1 присутствуют характерные для сульфопроизводных полоса R-SO2-OR группы при 1188 см–1 и очень сильная полоса S=O группы при 1213 см–1. Ряд интенсивных сигналов в интервале 1352–1593 см–1 относится к колебаниям нитро-групп [17]. Полосы валентных колебаний Sb-O и Sb-С связей располагаются при 420 см–1 и 482 см–1 соответственно [18].
По данным РСА, атомы сурьмы имеют искаженную тетраэдрическую координацию (СSbС 99,85(9)° - 123,74(9)°), однако присутствие координации атома кислорода сульфогруппы с центральным атомом металла (расстояние Sb∙∙∙O составляет 2,814(4) Å, что значительно больше суммы ковалентных радиусов указанных атомов (2,14 Å [19]), но меньше суммы ван-дер-ваальсовых радиусов (3,7 Å [20]), предполагает считать координацию центрального атома металла тригонально-бипирамидальной (аксиальный угол O(1)Sb(1)C(11) 172,78(8) ° , экваториальные углы составляют 123,74(8) ° , 114,60(8) ° , 102,92(8) ° ) (рис. 1).
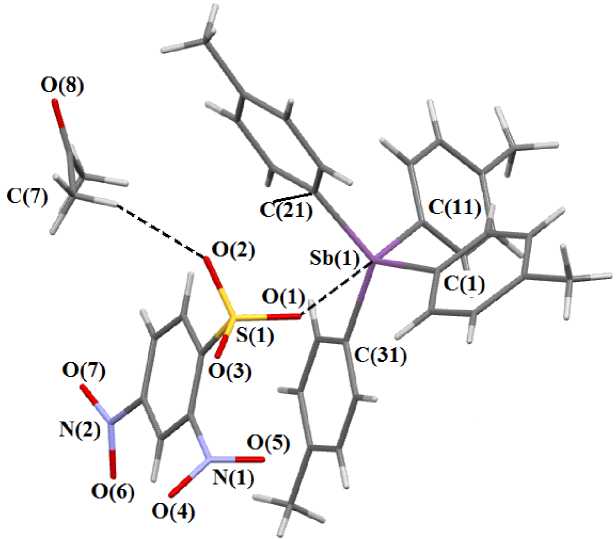
Рис. 1. Строение соединения 1
Геометрия 2,4-динитробензолсульфонатного лиганда определяется в том числе наличием короткого контакта О(3)∙∙∙О(5) (2,85 Å, при сумме ван-дер-ваальсовых радиусов 3,02 Å [20]), который, в свою очередь, препятствует более тесной координации лиганда с атомом сурьмы. Расстояния Sb - C в 1 изменяются в узком интервале значений (2,091(2) - 2ДИ(2) А), длины связей
S - O в сульфонатных группах 1 варьируют в интервале 1,4360(18) - 1,4488(17) Å, что сравнимо с аналогичными расстояниями, наблюдаемыми в сульфонатных производных сурьмы иного строения [21 - 27]. Кристаллическая ячейка содержит восемь молекул сульфоната 1 , расположенных в ее объеме, и восемь молекул сольватного растворителя, располагающихся парами между молекулами соединения 1 и образующих своеобразные каналы в кристаллической решетке (рис. 2).
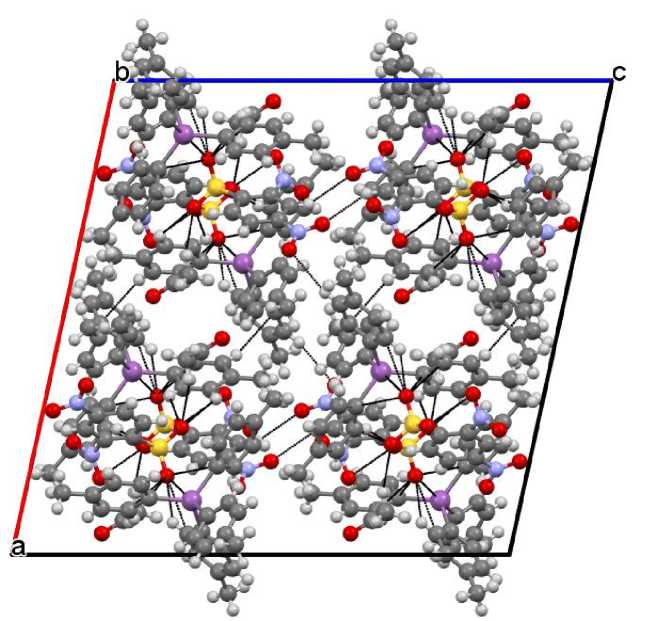
Рис. 2. Вид кристаллической решетки сульфоната 1 вдоль оси b
Структурная организация кристалла 1 формируется за счет слабых межмолекулярных контактов типа О···Н–C 2,25–2,69 Å, а также π -стекинг-эффекта параллельно расположенных толильных заместителей и нитробензольных колец сульфонатных лигандов.
Выводы
Установлено, что взаимодействие эквимолярных количеств пента( пара -толил)сурьмы с 2,4динитробензолсульфоновой кислотой в бензоле приводит к образованию 2,4-динитро-бензолсульфоната тетра( пара -толил)сурьмы, который после перекристаллизации из водного ацетона выделен в виде сольвата p -Tol4SbOSO2C 6 H 3 (NO2)-2,4 • Me2C=O с тригонально-бипирамидальной координацией центрального атома металла, координированный одним из атомов кислорода сульфонатной группы.
Список литературы Синтез и строение сольвата 2,4-динитробензолсульфоната тетра(пара-толил)сурьмы с ацетоном
- Шарутин, В.В. Синтез, реакции и строение арильных соединений пятивалентной сурьмы / B.В. Шарутин, А.И. Поддельский, О.К. Шарутина // Коорд. химия. - 2020. - Т. 46, № 10. - C. 579-648. https://doi.org/10.1134/S1070328420100012
- Шарутина, О.К. Молекулярные структуры органических соединений сурьмы (V) / О.К. Шарутина, В.В. Шарутин. - Челябинск: Издательский центр ЮУрГУ, 2012. - 395 с.
- Ruther, R. Synthesis of Tetraphenylstiboniium Alkyl- and Arylsulfonates. Crystal Structure of Tetraphenylstibonium Benzenesulfonate Hydrate / R. Ruther, F. Huber, H. Preut // J. Organomet. Chem. - 1985. - V. 295, № 1. - P. 21-27. DOI: 10.1016/0022-328X(85)88068-2
- Сульфонаты тетра- и триарилсурьмы / В.В. Шарутин, О.К. Шарутина, Л.П. Панова и др. // Журн. общ. хим. - 1997. - Т. 67, вып. 9. - С. 1531-1535.
- Синтез и строение 4-метилбензолсульфоната тетра-п-толилсурьмы / В.В. Шарутин, O.K. Шарутина, Т А. Тарасова и др. // Журн. общ. хим. - 1999. - Т. 69, вып. 12. - С. 1979-1981.
- Синтез и строение 2,4-диметилбензолсульфоната тетрафенилсурьмы / В.В. Шарутин, O.K. Шарутина, Т.А. Тарасова и др. // Журн. общ. хим. - 2000. - Т. 70, вып. 8. - С. 1311-1314.
- Синтез и строение новых кристаллических модификаций 4-метилбензолсульфонатов тетрафенилсурьмы / В.В. Шарутин, А.П. Пакусина, В.С. Сенчурин и др. // ^орд. химия. - 2002. -Т. 28. - С. 577.
- Синтез и строение 4-метилбензолсульфоната тетра- и-толилсурьмы / В.В. Шарутин, А.П. Пакусина, И.В. Егорова и др. // ^орд. химия. - 2003. - Т. 29, № 5. - С. 336-340.
- Синтез и строение органосульфонатов тетра- и трифенилсурьмы / В.В. Шарутин, O.K. Шарутина, А.П. Пакусина и др. // ^орд. химия. - 2004. - Т. 30, № 1. - С. 15-24. DOI: 10.1023/B:RUœ.0000011636.28262.d3
- Синтез и строение сурьма- и висмуторганических производных 4-сульфофенола и 2,4-дисульфофенола / В.В. Шарутин, И.В. Егорова, А.П. Пакусина и др. // ^орд. химия. - 2007. -Т. 33, № 3. - С. 176-183.
- Шарутин, В.В. Kристаллические модификации бензолсульфоната тетра-пара-толилсурьмы / В.В. Шарутин, O.K. Шарутина, В.С. Сенчурин // Журн. неорг. химии. - 2013. -Т. 58, № 11. - С. 1454-1457. DOI: https://doi.org/10.7868/S0044457X13110196
- Pan, B. [Sb(C6F5)4][B(C6F5)4]: An Air Stable, Lewis Acidic Stibonium Salt That Activates Strong Element-Fluorine Bonds / B. Pan, F.P. Gabbai // J. Am. Chem. Soc. - 2014. - V. 136, № 27. -Р. 9564-9567. doi 10.1021/ja505214m
- Establishing the Coordination Chemistry of Antimony(V) Cations: Systematic Assessment of Ph4Sb(OTf) and Ph3Sb(OTfh as Lewis Acceptors / A.P.M. Robertson, S.S. Chitnis, H.A. Jenkins et al. // Chem.-Eur. J. - 2015. - V. 21, № 21. - P. 7902-7913. DOI: 10.1002/chem.201406469
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures From Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: Complete Structure Solution, Refinement and Analysis Program / O.V. Dolomanov, L.J. Bourhis, R.J. Gildea et al. // J. Appl. Cryst. - 2009. - V. 42. - P. 339-341. DOI: 10.1107/S0021889808042726.
- Тарасевич, Б.Н. ИK-спектры основных классов органических соединений / Б.Н. Тарасевич. - М.: МГУ, 2012. - 54 с.
- Synthetic, Spectroscopic and Structural Aspects of Triphenylantimony(V) Complexes with Internally Functionalized Oximes: Crystal and Molecular Structure of [Ph3Sb{ON=C(Me)C5H4N-2}2] / A. Gupta, R.K. Sharma, R. Bohra et al. // Polyhedron. - 2002. - V. 21, I. 23, P. 2387-2392. https://doi.org/10.1016/S0277-5387(02)01155-5
- Covalent radii revisited / B. Cordero, V. Gómez, A.E. Platero-Prats et al. // Dalton Trans. -2008. - Iss. 21. - P. 2832-2838. DOI: 10.1039/B801115J.
- Consistent Van der Waals Radii for the Whole Main Group / M. Mantina, A.C. Chamberlin, R. Valero et al. // J. Phys. Chem. A. - 2009. - V. 113, Iss. 19. - P. 5806-5812. DOI: 10.1021/jp8111556.
- Синтез и строение ц-оксобис[(аренсульфонато)триарилсурьмы] / В.В. Шарутин, И.В. Егорова, И.И. Павлушкина и др. // ^орд. химия. - 2003. - Т. 29, № 2. - С. 89-94.
- Синтез и строение бис(аренсульфонатов) триарилсурьмы / В.В. Шарутин, O.K. Шарутина, Т.П. Платонова и др. // Журнал общей химии. - 2003. - Т. 73, № 3. - С. 380-384. DOI: 10.1023/A: 1024945617228
- Sharutin, V.V. Synthesis and Structure of Tri(meto-tolyl)antimony ^«(benzenesulfonate) / V.V. Sharutin, O.K. Sharutina, V.S. Senchurin // Bulletin of the South Ural State University. Ser. Chemistry. - 2015. - V. 7, № 4. - P. 93-97. DOI: 10.14529/chem150412
- Синтез и строение бис(2,5-диметилбензолсульфоната) три(орто-толил)сурьмы / B.В. Шарутин, O.K. Шарутина, В.С. Сенчурин и др. // Вестник ЮУрГУ. Серия «Химия». -2017. - Т. 9, № 3. - С. 71-75. DOI: 10.14529/chem170309.
- Rüther, R. Nonaphenyltristiboxane-1,5-diyl Disulfonates / R. Rüther, F. Huber, H. Preut // An-gew. Chem., Int. Ed. Engl. - 1987. - V. 26, № 9. - P. 906-907. DOI: 10.1002/anie.198709061.
- Синтез и строение моно-, би- и триядерных органилсульфонатных производных триарил-сурьмы / В.В. Шарутин, О.К. Шарутина, В.С. Сенчурин и др. // Журн. неорг. химии. - 2018. -Т. 63. № 7. - С. 823-830. DOI: 10.1134/S0044457X18070188.
- Cambridge Crystallographic Data Center, 2021.


