Синтез и свойства композиционного материала CoFe2O4/C
Автор: Шабельская Н.П., Егорова М.А., Чернышева Г.М., Салиев А.Н., Яценко А.Н., Гайдукова Ю.А.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Химическая технология
Статья в выпуске: 4 (82), 2019 года.
Бесплатный доступ
Научный интерес к процессам формирования структуры магнитных шпинелей и композитов на их основе обусловлен возможностью синтеза материалов с полифункциональными свойствами. Изучен процесс образования нанокристаллического феррита кобальта (II) и композиционного материала CoFe2O4/C. Предложен механизм формирования структуры материалов, включающий стадию образования гидроксидов переходных элементов, прекурсоров на основе комплексных соединений катионов железа и кобальта с лимонной кислотой и их последующего разрушения при нагревании. Синтезированные материалы охарактеризованы при помощи методов рентгенофазового анализа, электронной микроскопии, методов низкотемпературной адсорбции азота, Дебая-Шеррера. Показано, что феррит кобальта (II) имеет развитую поверхность, значение площади поверхности по методу ВЕТ составляет величину 16 м2/г, средний размер кристаллитов, определеный по уравнению Дебая-Шеррера, составляет 4.0 нм. Для приготовления композиционного материала был использован активированный уголь с величиной удельной поверхности 685 м2/г...
Шпинели, феррит кобальта, уравнение дебая-шеррера, адсорбция, катионы меди
Короткий адрес: https://sciup.org/140248258
IDR: 140248258 | УДК: 661.8 | DOI: 10.20914/2310-1202-2019-4-184-189
Synthesis and properties of composite material CoFe2O4/C
Scientific interest in the processes of forming the structure of magnetic spinels and composites based on them is due to the possibility of synthesis of materials with multifunctional properties. The process of formation of cobalt (II) nanocrystalline ferrite and CoFe2O4/C composite material is studied. The mechanism of formation of structure of materials including a stage of formation of hydroxides of transition elements, precursors on the basis of complex connections of cations of iron and cobalt with citric acid and their subsequent destruction at heating is offered. The synthesized materials were characterized by x-ray phase analysis, electron microscopy, low-temperature nitrogen adsorption, Debye-Scherrer methods. It is shown that cobalt (II) ferrite has a developed surface, the value of the surface area according to the BET method is 16 m2/g, the average size of the crystallites determined by the Debye-Scherrer equation is 4.0 nm. Activated carbon with a specific surface area of 685 m2/g was used to prepare the composite material...
Текст научной статьи Синтез и свойства композиционного материала CoFe2O4/C
Оксидные системы на основе ферритов переходных элементов с общей формулой MFe 2 O 4 (М – двухвалентный катион) со структурой шпинели являются объектом активного исследования на протяжении длительного времени. Научный интерес к процессам формирования структуры этих материалов обусловлен наличием у них полифункциональных свойств. Шпинели на основе феррита кобальта (II) CoFe 2 O 4 относятся к магнитным материалам [1, 2], известно их применение в качестве катализаторов [3–5], адсорбентов Al3+ [6], Zn2+ [7], электродов литий-ионных источников тока [8, 9], топливных элементов [10], в медицинских целях – для адресной доставки лекарств [11]. Процессам водоподготовки с адсорбцией катионов металлов различными сорбентами посвящен ряд работ [6, 7, 12–14].
Внимание химиков-технологов в последние годы сосредоточено на изучении возможностей синтеза наноразмерных материалов со структурой шпинели [3, 11, 15, 16]. Данное обстоятельство обусловлено тем, что наноразмерные материалы обладают рядом преимуществ по сравнению с хорошо окристаллизованными поликристалли-ческими образцами. Особенно важным данное обстоятельство выступает в процессах, связанных с реакциями на поверхности веществ, – адсорбционными, каталитическими, – в которых решающим фактором эффективности процесса является количество активных центров на единицу массы образца. В этой связи особое вынимание уделяется получению образцов с развитой поверхностью. К традиционным методам получения шпинелей относят керамический (из оксидов соответствующих металлов) [17], химическое осаждение и разложение гидроксидов и солей [18, 19]. Получение наноразмерных материалов может осуществляться с применением гидротермального синтеза [5], микроволнового излучения [16], разложением органического прекурсора (метод Печини). В качестве темплата могут выступать лимонная [4], олеиновая [9] кислота, мочевина [16] и другие. Синтез органонеорганических композиционных материалов открывает новые возможности получения материалов с набором необычных свойств. Цель исследования –синтез и изучение свойств феррита кобальта (II) и композиционного материала CoFe 2 O 4 /C.
Материалы и методы
Исходными веществами для получения образцов служили растворы с концентрацией 1,0 моль/л, приготовленные из Fe(NO3)3·9H2O, Co(NO3)2·7H2O квалификации «хч». Смесь растворов в соотношении нитрат железа (III):нитрат кобальта (II) = 2:1 помещали в реакционный сосуд из нержавеющей стали, добавляли 15 мл 25%-ного водного раствора аммиака, затем смешивали с 25 мл раствора лимонной кислоты концентрацией 6,25 моль/л, выпаривали до образования сухого остатка и подвергали термообработке до полного разложения органической составляющей.
Фазовый состав изучали на дифрактометре ARLX’TRA, использовали Cu- K α излучение. Фотографии образцов были получены на сканирующем электронном микроскопе Quanta 200. Определение площади поверхности проводили методом ВЕТ на аппарате ChemiSorb 2750 в ЦКП «Нанотехнологии» Южно-Российского государственного политехнического университета (НПИ) имени М.И. Платова.
Расчет среднего размера кристаллов D , нм, проводили по уравнению Дебая-Шеррера [20] по линии 311:
D= 0,9⋅λ , B ⋅ cosθ где λ = 1,5406 нм – длина волны; В – полная ширина пика на уровне половины интенсивности; θ – угол дифракции.
Эксперимент по определению поглощающей способности синтезированных материалов в отношении катионов меди (II) из водных растворов проводили на модельном растворе CuSO 4 с концентрацией 0,1 моль/л. Использовали 0,01 г адсорбента, который помещали в реакционный сосуд, заливали раствором, содержащим катионы Cu2+, выдерживали определенное время при комнатной температуре. Содержание катионов Cu2+ определяли фотоколориметрическим методом на приборе КФК-2-УХЛ 4,2 по изменению интенсивности окраски аммиакатных комплексов меди (II).
Результаты и обсуждение
Приготовление феррита кобальта (II) проводили согласно методике, подробно описанной в работах [21, 22]. Для синтеза образцов CoFe 2 O 4 были использованы растворы солей нитратов железа (III) (50 мл) и кобальта (II) (25 мл) с концентрацией 1 моль/л. Исходные растворы помещали в реакционный сосуд, добавляли при непрерывном перемешивании водный раствор аммиака, наблюдали образование темного аморфного осадка гидроксидов железа (III) и кобальта (II):
Co(NO 3 ) 2 + 2NH 3 ·H 2 O = Co(OH) 2 +
+ 2NH 4 NO 3 ,
Fe(NO 3 ) 3 + 3NH 3 ·H 2 O = Fe(OH) 3 +
+ 3NH 4 NO 3 .
В условиях проведения реакции возможно формирование аммиакатных комплексов железа (III) и кобальта (II):
Co(OH) 2 + 4NH 3 = [Co(NH 3 ) 4 ](OH) 2 , Fe(OH) 3 + 4NH 3 = [Fe(NH 3 ) 4 ]OH.
При введении раствора лимонной кислоты наблюдали переход осадка в раствор за счет образования растворимых цитратов:
Co(OH) 2 + Fe(OH) 3 + 4C 6 H 8 O 7 =
= CoFe 2 (C 6 H 6 O 7 ) 4 + 4Н 2 О.
Цитраты железа (III) – кобальта (II)
имеют объемную структуру но о но о
I III II с-с-о-он с-с-о-он
/ \\
СИ7 СН2 СН2 он2
о=с о=с о=с о=с
I I I I
0 /° /°/°
Fe /Со х Fe о/ о о"о
О=С О=С о=со=с сн2 СН2 СН2 ^СНз
^с^с-он ^с-с-он
IIII о°
При разложении цитратов образуется пористый материал (рисунок 1).

Рисунок 1. Микрофотография образца CoFe 2 O 4
Figure 1. Micrograph of sample CoFe 2 O 4
Площадь удельной поверхности, измеренная методом ВЕТ, составляет 16 м2/г. Согласно результатам рентгенофазового анализа (рисунок 2, а ) образец представляет собой феррит кобальта (II) со структурой кубической шпинели (PDFNumber 010–76–7254), параметр элементарной ячейки а = 0,837 нм.
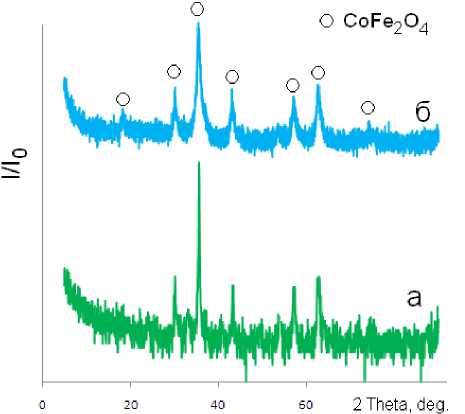
Рисунок 2. Рентгенограммы образцов феррита кобальта (II) ( а ) и композиционного материала ( б )
Figure 2. X-ray images of cobalt (II) ferrite ( a ) and composite material ( b )
Расчет среднего размера кристаллитов по уравнению Дебая-Шеррера по наиболее интенсивной линии дает результат D = 4,0 нм.
Для приготовления образцов композиционного материала CoFe 2 O 4 /С в качестве органической составляющей был выбран активированный уголь, имеющий значение площади поверхности (по методу ВЕТ) 685 м2/г. Уголь измельчали до прохождения через сито 0,3 мм, помещали в реакционный сосуд, добавляли растворы солей нитратов железа (III) и кобальта (II) с концентрацией 1 моль/л, растворы аммиака, лимонной кислоты аналогично процедуре синтеза чистого феррита кобальта (II). После термообработки наблюдали образование черной пористой массы (рисунок 3).

Рисунок 3. Микрофотография композиционного материала CoFe 2 O 4 /C
Figure 3. Micrograph of the composite material CoFe 2 O 4 /C
Согласно данным рентгенофазового анализа (рисунок 2, б ) образец представляет собой феррит кобальта (II) (PDFNumber 010–74–3419), параметр элементарной ячейки а = 0,838 нм (углерод рентгеноаморфен).
Некоторое увеличение параметра элементарной ячейки может быть связано с уменьшением степени обращенности (количества катионов Fe3+, занимающих тетраэдрические позиции решетки шпинели) полученного феррита.
Расчет среднего размера кристаллитов CoFe 2 O 4 по уравнению Дебая–Шеррера по наиболее интенсивной линии дает результат D = 1,1 нм. Площадь поверхности составляет величину 222 м2/г. Существенное уменьшение площади поверхности синтезированного композиционного материала по сравнению с исходным образцом активированного угля может быть связано с образованием на поверхности частиц феррита кобальта (II).
Синтезированный композиционный материал был испытан в реакции адсорбции катионов меди (II) из водного раствора (рисунок 4).
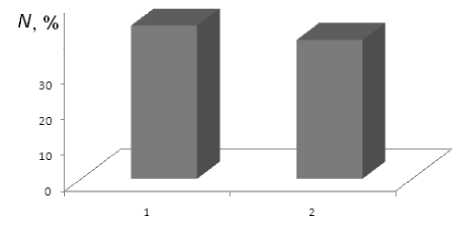
Рисунок 4. Адсорбция ( N ) катионов Cu 2+ из раствора композиционным материалом CoFe 2 O 4 /С (1) и активированным углем (С) (2)
Figure 4. Adsorption ( N ) of Cu 2+ cations from solution by composite material CoFe 2 O 4 /C (1) and activated carbon (C) (2)
Согласно полученным данным адсорбция катионов Cu2+ из раствора композиционным материалом CoFe 2 O 4 /С происходит лучше (на величину порядка 10%), чем чистым активированным углем, несмотря на то что чистый уголь имеет более развитую поверхность. Можно предположить, что введение в систему феррита кобальта (II) создает дополнительные центры адсорбции, что приводит к увеличению степени извлечения катионов Cu2+ из раствора.
Заключение
Проведен синтез нанокристаллического феррита кобальта (II). В отличие от широко используемого в современной технологии нанораз-мерных керамических материалов метода Печини предложенная методика не требует использования опасного для здоровья этиленгликоля.
-
1. Изучен процесс образования наноразмер-ного феррита кобальта (II) и композиционного материала CoFe 2 O 4 /C.
-
2. Предложен механизм образования структуры образцов, включающий стадию формирования комплексных соединений и их последующего разрушения при нагревании. Обсуждена возможность получения гомогенной смеси, приводящей к формированию каркасной структуры феррита кобальта (II).
-
3. Определен по формуле Дебая–Шеррера средний размер кристаллитов образующегося феррита кобальта (II), который составил 4 нм, и композиционного материала (1,1 нм).
-
4. Установлена повышенная адсорбционная способность синтезированного композиционного материала CoFe 2 O 4 /C в процессе поглощения катионов меди (II) из водного раствора. Полученные материалы могут представлять интерес в качестве катализаторов, адсорбентов.
Список литературы Синтез и свойства композиционного материала CoFe2O4/C
- Dai Y.Q., Dai J.M., Tang X.W., Zi Z.F. et al. Magnetism of CoFe2O4 thin films annealed under the magnetic field // Journal of Magnetism and Magnetic Materials. 2015. V. 394. P. 287-291.
- Singh S., Munjal S., Khare N. Strain/defect induced enhanced coercivity in single domain CoFe2O4 nanoparticles // Journal of Magnetism and Magnetic Materials. 2015. V. 386. P. 69-73.
- Zhao Y., Cao B., Lin Z., Su X. Synthesis of CoFe2O4/C nano-catalyst with excellent performance by molten salt method and its application in 4nitrophenol reduction // Environmental pollution. 2019. V. 254. № Pt A. P. 112961.
- Huang S., Xu Y., Xie M., Xu H. et al. Synthesis of magnetic CoFe2O4/g-C3N4 composite and itsenhancement of photocatalytic ability under visible-light // Colloids and Surfaces A: Physicochem. Eng. Aspects. 2015. V. 478. P. 71-80.
- Gan L., Shang S., Yuen C.W.M., Jiang S.-X. et al. Hydrothermal synthesis of magnetic CoFe2O4/grapheme nanocomposites with improved photocatalytic activity // Applied Surface Science. 2015. V. 351. P. 140-147.
- Abdolmohammad-Zadeh H., Rahimpour E. CoFe2O4 nano-particles functionalized with 8hydroxyquinoline for dispersive solid-phase micro-extraction and direct fluorometric monitoring of aluminum in human serum and water samples // Analytica Chimica Acta. 2015. V. 881. P. 54-64.
- Foroughi F., Hassanzadeh-Tabrizi S.A., Amighian J., Saffar-Teluri A. A designed magnetic CoFe2O4-hydroxyapatite core-shell nanocomposite for Zn(II) removal with high efficiency // Ceramics International. 2015. V. 41. P. 6844-6850.
- Li Y., Meng Y., Xiao M., Liu X. et al. The surface capacitance behavior and its contribution to the excellent performance of cobalt ferrite/carbon anode in lithium storage // Journal of Materials Science: Materials in Electronics. 2019. V. 30. № 13. P. 12659-12668.
- Tansel S?, Emine K., Melike S., ?nder M. Monodisperse CoFe2O4 nanoparticles supported on Vulcan XC72: High performance electrode materials for lithium-air and lithium-ion batteries // Journal of Power Sources. 2015. V. 288. P. 36-41.
- Urbain F., Du R., Tang P., Smirnov V. et al. Upscaling high activity oxygen evolution catalysts based on CoFe2O4 nanoparticles supported on nickel foam for power-to-gas electrochemical conversion with energy efficiencies above 80% // Applied Catalysis B: Environmental. 2019. V. 259. P. 118055.
- Darwish M.S.A., Kim H., Lee H., Ryu C. et al. Synthesis of magnetic ferrite nanoparticles with high hyperthermia performance via a controlled co-precipitation method // Nanomaterials. 2019. V. 9. № 8. P. 1176.
- Бояринцев А.В., Аунг М.М., Аунг Х.Й., Степанов С.И. Извлечение алюминия при комплексной переработке красных шламов // Вестник ВГУИТ. 2018. Т. 80. № 3. С. 317-322.
- DOI: 10.20914/2310-1202-2018-3-317-322
- Фарберова Е.А., Ходяшев М.Б., Филатов В.Ю., Ходяшев Н.Б. и др. Применение углеродных сорбентов в технологии очистки сточных вод от ртути // Вестник ВГУИТ. 2018. Т. 80. № 4. С. 322-329.
- DOI: 10.20914/2310-1202-2018-4-322-329
- Перегудов Ю.С., Тимкова А.В., Горбунова Е.М., Плотникова С.Е. Применение ионообменного волокна на стадии доочистки сточных вод гальванического производства // Вестник ВГУИТ. 2018. Т. 80. № 4. С. 330-336.
- DOI: 10.20914/2310-1202-2018-4-330-336
- Kim K.J., Park J. Spectroscopic investigation on tetrahedral Co2+ in thin-film CoFe2O4 // Journal of Sol-Gel Science and Technology. 2019. V. 92. № 1. P. 40-44.
- Al Yaqoob K., Bououdina M., Akhter M.S., Al Najar B. et al. Selectivity and efficient Pb and Cd ions removal by magnetic MFe2O4 (M = Co, Ni, Cu and Zn) nanoparticles // Materials Chemistry and Physics. 2019. V. 232. P. 254-264.
- Venturini J., Wermuth T.B., Machado M.C., Arcaro S. et al. The influence of solvent composition in the sol-gel synthesis of cobalt ferrite (CoFe2O4): A route to tuning its magnetic and mechanical properties // Journal of the European Ceramic Society. 2019. V. 39. № 12. P. 3442-3449.
- Illa R., Je?ko R., Silber R., ?ivotsk? O. et al. Structural, magnetic, optical, and magneto-optical properties of CoFe2O4 thin films fabricated by a chemical approach // Materials Research Bulletin. 2019. V. 117. P. 96-102.
- Ojha V.H., Kant K.M. Temperature dependent magnetic properties of superparamagnetic CoFe2O4 nanoparticles // Physica B: Condensed Matter. 2019. V. 567. P. 87-94.
- Jang J.S., Hong S.J., Lee J.S. Synthesis of Zinc Ferrite and Its Photocatalytic Application under Visible Light // Journal of the Korean Physik Society. 2009. V. 54. № 1. P. 204-208.
- Шабельская Н.П., Зеленская Е.А., Постников А.А., Сулима С.И., Таранушич В.А., Сулима Е.В., Чернышев В.М., Власенко А.И. Синтез композиционного материала TiO2/Fe1.92Ti0.61O4/Fe2O3 и его каталитические свойства // Фундаментальные исследования. 2015. № 9 (3). С. 532-535.
- Семченко В.В., Шабельская Н.П., Кузьмина Я.А. Синтез и каталитические свойства наноразмерного феррита цинка // Успехи современного естествознания. 2018. № 4. С. 36-41.


