Синтез иминов 4-акридонкарбоксоамидов
Автор: Сысоев П.И., Кудрявцева Т.Н., Богатырев К.В.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Фундаментальная и прикладная химия, химическая технология
Статья в выпуске: 1 (55), 2013 года.
Бесплатный доступ
Синтезировано восемь новых иминов 4-акридонкарбоксоамидов с помощью реакции конденсации гидразида 4-карбоксиакридона с различными альдегидами.
4-карбоксиакридон, гидразид, азометин
Короткий адрес: https://sciup.org/14039957
IDR: 14039957 | УДК: 547.835.5
Synthesis of 4-acridonecarboxamide imines
Eight novel 4-acridonecarboxamide azomethines have been prepared by the condensation of 9-oxo-9.10-dihydroacridine-4-carboxylic acid hydrazide with various aldehydes.
Текст научной статьи Синтез иминов 4-акридонкарбоксоамидов
Синтез биологически активных веществ на основе различных, в том числе, гетероциклических соединений, являющихся структурными фрагментами применяемых в медицине препаратов, является одним из важных направлений поиска новых лекарственных средств.
Среди биологически активных соединений, активно изучаемых в настоящее время гетероциклических соединений, весьма важное место занимают производные 4 - карбоксиакридона (9 – оксо - 9,10 -дигидроакридин - 4 -карбоновой кислоты), для которых обнаружено противовирусное, противоопухолевое и противомикробное действие [1-3]. Кроме того, среди производных гидразидов ряда карбоновых кислот (2 - аминобензойной, изоникотиновой, никотиновой, цинхониновой) также обнаружены и применяются в фармако-терапевтической практике высокоэффективные биологически активные соединения, проявляющие антимикробную, противовоспалительную, противосудорожную активность [4]. Биологическую активность проявляют и некоторые гидразоны [5]. В связи с этим практический интерес представляет синтез арилиденгидразидов 4 - карбоксиакридона.
Исходный бутиловый эфир 4 - карбоксиакридона ((1), рис. 1) синтезировали с помощью реакции этерификации между бутанолом и 4 - карбоксиакридоном (рис. 1).
Рис. 1. Реакция этерификации между бутанолом и 4-карбоксиакридоном
Гидразид 4 -карбоксиакридона ((2), рис. 2) тилового эфира 4 - карбоксиакридона (рис. 2) в был синтезирован реакцией гидразинолиза бу- кипящем бутаноле [2]:
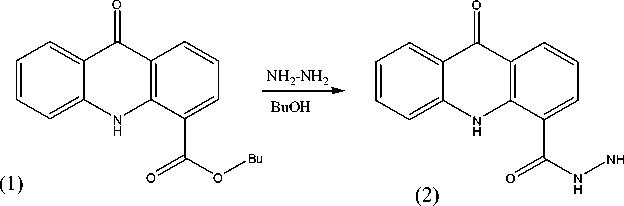
Рис. 2. Реакция гидразинолиза бутилового эфира 4 - карбоксиакридона в кипящем бутаноле © Сысоев П. И., Кудрявцева Т. Н., Богатырев К. В., 2013
Полученный гидразид представляет собой желтое высокоплавкое кристаллическое вещество, практически нерастворимое в воде и углеводородных растворителях, плохо растворимое в спиртах, хорошо растворимое в N,N - диметилформамиде, раствор обладает выраженной голубой флуоресценцией. Структура полученного соединения подтверждена методами ИК-спектроскопии и хромато-масс-спектрометрии. В масс-спектре полученного соединения присутствует пик, соответствующий молекулярному иону с m / z 254. В ИК спектре соединения ((2), рис.2) присутствуют полосы поглощения, отвечающие колебаниям карбонильной группы акридонового цикла и амидной группы (1622, 1647 см-1 соответственно), а также полоса поглощения, соответствующая колебаниям N - H связей (3285 см-1). В отличие от спектра бутилового эфира 4 - карбоксиакридона, в ИК - спектре гидразида 4 - карбоксиакридона исчезает по- лоса, соответствующая колебаниям сложно-эфирной группы 1685 см-1.
Реакцию конденсации гидразида 4 - карбоксиакридона ((2), рис. 3) с ароматическими альдегидами проводили в бутаноле при комнатной температуре при эквимольном соотношении реагентов (рис. 3). На всех стадиях реакции реакционная смесь представляет собой гетерогенную систему (и исходный гидразид, и продукт реакции плохо растворимы в бутаноле), однако внешний вид твердой фазы по ходу реакции претерпевает изменения. Полноту протекания реакции контролировали методом ТСХ [6]. Ароматические альдегиды, содержащие в ядре как электронодонорные, так и электроноакцепторные заместители, легко реагировали с соединением ((2), рис. 3) в результате чего был получен ряд соответствующих арилиденгидразидов 4 - карбоксиакридона (соединения (3 a-h)):
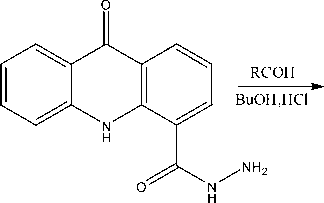
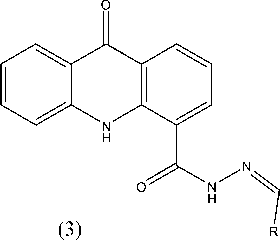
Рис. 3. Реакция конденсации гидразида 4-карбоксиакридона с ароматическими альдегидами. R = 4-нитро-фенил (3a); R = 2 - нитро-фенил (3b); R=4-(диэтиламино)-фенил (3c); R=4-(диметиламино)-фенил (3d);
R = 4-хлор-фенил (3e); R = 3,4 - диоксо-фенил (3f); R = α-бромстирил (3g); R = 4-изопропил-фенил (3h)
Полученные арилиденгидразиды 4-кар-боксиакридона представляют собой высокоплавкие кристаллические вещества, цвет которых варьируется от желтого до оранжевого. Это вещества нерастворимые в воде и углеводородных растворителях, плохо растворимые в спиртах, хорошо растворимые в N,N-диметилформамиде, растворы обладают хорошо выраженной голубой флуоресценцией.
В ИК-cпектрах соединений ((3 a-h) рис. 3) карбонильной группе акридонового скелета соответствует интенсивная полоса поглощения в области 1621 - 1617 см-1. Карбонильной амидной группе во всех соединениях отвечает полоса поглощения в области 1690 - 1646 см-1 . Иминной (N3 = C4) группе соответствует полоса поглощения в области 1597 - 1592 см-1 [7]. Для полученных соединений вероятно существование E / Z изомеров. Однако ни метод ТСХ, ни хроматомасс-спектрометрические исследования полученных веществ не выявили существования изомерных форм. В хроматограммах всех полученных соединений присутствует единственный пик, для которого в масспектре обнаруживается пик молекулярного иона ари-лиденгидразида. Полученные результаты согласуются с исследованием авторов [6], которые считают, что в растворах исследуемых соединений имеет место быстрое равновесное взаимопревращение E и Z изомерных форм.
Таким образом, с помощью реакции конденсации гидразида 4 - карбоксиакридона c различными ароматическими альдегидами был осуществлен синтез новых соединений ряда арилиденгидразидов 4 - карбоксиакридона, предположительно обладающих биологической активностью и способных выступать в
Вестник ВТУИТ № 1.2013 качестве синтонов в синтезе новых биологически активных соединений.
Порядок осуществления синтеза представлен далее. Чистоту исходных соединений и продуктов реакции контролировали методом тонкослойной хроматографии (пластины «Сорбфил» ПТСХ-П-В-УФ, элюент - толуол: ацетон: уксусная кислота 5:5:0,1). Состав и структуру продуктов реакции подтверждали методами ИК-спектроскопии (ИК-Фурье спектрометр типа IR - 200, фирма Nicolet, таблетки в KBr), методами хроматомасс-спектрометрии (система ACQUITY UPLC H- Class с УФ/масс-детекторами ACQUITY SQD компании Waters) и методами УФ спектроскопии (УФ-спектрометр UV-1800 фирмы Shimadzu). Бутиловый эфир 4-карбоксиакридона был получен следующим образом: к 10 г (0,021 моль) 4-карбоксиакридона приливают 50 мл бутилового спирта и 13 мл серной кислоты. Смесь кипятят при перемешивании. Контроль хода реакции осуществляют с помощью ТСХ. Растворитель упаривают, осадок отфильтровывают и перекристаллизовывают из бутанола. Выход составил 65 %. Т.пл. = 175±2 °С; Rf = 0,84. Масс-спектр (Электроспрей, 70 эВ), m/z
(Iотн (%)): 296 [M+H]+ (100). ИК-спектр (KBr), ν/см–1: 1685 (С1’ = О сл.эф.); 1616 (C9 = Оакр.).
Получение гидразид 4-карбоксиакридона (2) происходит по представленной далее схеме. К смеси 10 г (3,2 ммоль) бутилового эфира 4-карбоксиакридона и 20 мл бутилового спирта, добавляют 8,2 мл гидразина моногидрата, реакционную смесь кипятят при перемешивании в течение 2 часов. Выпавший осадок фильтруют, перекристаллизовывают из ДМФА. Выход составил 84 %. Т.пл. = 315 ± 2 °С; R f = 0,25. Масс-спектр (Электроспрей, 70 эВ), m / z ( I отн (%)): 254 [M + H]+ (100). ИК - спектр (KBr), ν/см–1: 3275 (NH - NH 2 ); 1647 (C 1’ = О амид ); 1624 (C 9 = О акр. ).
Общая методика синтеза иминов 4-акридонкарбоксоамидов (3 a-h) заключается в следующем: смесь 3.7 ммоль гидразид 4-карбоксиакридона и 4.1 ммоль соответствующего ароматического альдегида в 40 мл BuOH, подкисленную 1-2 каплями концентрированной HCl, выдерживают при комнатной температуре и перемешивании в течение 1 часа. Образовавшийся продукт фильтруют и перекристаллизовывают из ДМФА. Характеристики синтезированных соединений представлены в табл. 1.
Таблица 1
|
R |
Выход % |
Т пл ºC |
m/z |
R f |
ИК - спектр (KBr), ν / см–1 |
||
|
C 1’ =O |
C 9 =O |
N 3’ =C 4’ |
|||||
|
4-нитро-фенил (3a) |
77 |
312±2 |
387 |
0,77 |
1690 |
1621 |
1592 |
|
2-нитро-фенил (3b) |
79 |
307±2 |
387 |
0,81 |
1653 |
1621 |
1593 |
|
4-(диэтиламино)-фенил (3c) |
86 |
274±2 |
413 |
0,79 |
1648 |
1617 |
1594 |
|
4-(диметиламино)-фенил (3d) |
79 |
269±2 |
384 |
0,73 |
1674 |
1605 |
1643 |
|
4-хлор-фенил (3e) |
78 |
301±2 |
376 |
0,78 |
1677 |
1621 |
1593 |
|
3,4-диоксо-фенил (3f) |
81 |
290±2 |
374 |
0,48 |
1662 |
1621 |
1594 |
|
α-бромстирил (3g) |
78 |
233±2 |
446 |
0,78 |
1646 |
1621 |
1595 |
|
4-изопропил-фенил (3h) |
89 |
266±2 |
384 |
0,81 |
1649 |
1620 |
1597 |


