Синтез сложных эфиров карбоновых кислот- производных 6,8- дибромхиназолин-4(зн)-она
Автор: Солодунова Г.Н., Солодунова Е.А., Герасименко А.В., Клочков В.Г., Клочкова В.Л.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Фармакология, токсикология
Статья в выпуске: 2 (58), 2018 года.
Бесплатный доступ
Алкилирование 6,8-дибромхиназолин-4(3/-/)-она сложными эфирами 2-галогенкарбоновых кислот в безводном ДМФА в присутствии калия карбоната приводит к соответствующим сложным эфирам 2-[4-оксо-6,8-дибромхиназолин-3(4H)-ил]карбоновых кислот с хорошим (77-82 %) выходом.
8-дибромхиназолин-4(зн)-он, бромуксусная кислота, 2-хлорпропионовая кислота, n-алкилирование
Короткий адрес: https://sciup.org/142216673
IDR: 142216673 | УДК: 547.856.1
Synthesis of carbоxylic acid esters -6,8-dibrоmоquinazolin-4(3h)-оne derivatives
The alkylation of 6,8-dibromoquinazolin-4(3H)-one with esters of 2-halogencarboxylic acids in anhydrous DMF in the presence of potassium carbonate leads to corresponding esters of 2-[4-oxo-6,8-dibromoquinazolin-3(4H)-yl]carboxylic acid with good (77-82 %) yield.
Текст научной статьи Синтез сложных эфиров карбоновых кислот- производных 6,8- дибромхиназолин-4(зн)-она
Карбонильные производные хиназолин-4(3 Н )-она, содержащие фрагменты кетонов или амидов в качестве заместителей в положении N3 хиназолиновой системы, демонстрируют широкий спектр фармакологической активности [1, 5]. Среди веществ этого ряда обнаружены соединения с выраженными антидепрессантными [7], ноотропными [8], иммунотропными [4, 9] и противосудорожными [2] свойствами. Сложные эфиры карбоновых кислот – производных хина-золин-4(3 Н )-она, являются ценными полупродуктами, позволяющими получать указанные выше соединения на основе реакций нуклеофильного типа [3]. В настоящей статье описаны синтез и свойства новых сложных эфиров уксусной и пропионовой кислот, содержащих фрагменты 6,8-дибромхиназолин-4(3 Н )-она.
ЦЕЛЬ РАБОТЫ
Разработка метода синтеза сложных эфиров 2-[4-оксо-6,8-дибромхиназолин-3(4 Н )-ил] уксусной и пропионовой кислот – важных интермедиатов для получения фармакологически активных соединений хиназолинового ряда.
МЕТОДИКА ИССЛЕДОВАНИЯ
Спектры ЯМР 1Н и 13С регистрировали на спектрометре «Bruker Avance 600» (600 МГц для 1H и 150 МГц для 13С) в ДМСО-D 6 внутренний стандарт тетраметилсилан. Интерпретацию спектров осуществляли с помощью лицензионной программы ACD/HNMR Predictor Pro 3.0
(Advanced Chemistry Development, Канада). Температуры плавления измерены в стеклянных капиллярах на приборе Mel-Temp 3.0 (Laboratory Devices Inc., США).
6,8-Дибромхиназолин-4(3 Н )-он (I) был получен по методике [6].
Бензиловый эфир 2-[4-оксо-6,8-дибромхиназолин-3(4 Н )-ил]уксусной кислоты (II). Суспензию 5,0 г (16,5 ммоль) 6,8-дибромхиназолин-4(3 Н )-она ( I ) и 5,0 г (36,2 ммоль) тонко измельченного калия карбоната в 50 мл безводного ДМФА перемешивают при температуре 95–100 оС в течение 15 мин, добавляют 4,0 г (17,5 ммоль) бензилового эфира бромуксусной кислоты, перемешивают при той же температуре 1 ч, а затем при комнатной температуре в течение суток. Фильтруют, фильтрат упаривают в вакууме, остаток растирают с 50 мл холодной воды, образовавшийся осадок отфильтровывают, промывают водой, сушат на воздухе, перекристаллизовывают из смеси 100 мл изопропилового спирта и 50 мл ДМФА и получают 6,1 г (82 %) светло-бежевого игольчатого кристаллического вещества, Т. пл. 182,5–185 оС.
Спектр ЯМР 1Н, δ, м. д.: 4,94 с (2Н, СН 2 ); 5,22 с (2Н, СН 2 ); 7,32–7,40 м (5Н, фенил); 8,22 д (1Н, 2 Гц, Н7); 8,40 д (1Н, 2 Гц, Н5); 8,55 с (1Н, Н2).
Спектр ЯМР 13С, δ, м. д.: 47,90; 67,07; 120,12; 123,78; 124,00; 128,36; 128,60; 128,80; 135,73; 140,34; 145,01; 149,59; 159,93; 167,81.
Изопропиловый эфир 2-[4-оксо-6,8-дибромхиназолин-3(4 Н )-ил]пропионовой кислоты (III) получают аналогично, но в качестве алкилирующего агента используют 2,7 г (17,9 ммоль) изопропилового эфира 2хлорпропионовой кислоты и перекристаллизацию продукта-сырца осуществляют из 50 мл изопропилового спирта.
Получают 5,3 г (77 %) светло-желтого кристаллического вещества, Т. пл. 112–115 оС.
Спектр ЯМР 1Н, δ, м. д.: 1,16 дд (6Н, 6 Гц, 20 Гц, СН 3 ); 1,66 д (3Н, 7 Гц, СН 3 ); 4,95 м (1Н, 6 Гц, СН); 5,27 кв (1Н, 7 Гц, СН); 8,21 д (1Н, 2 Гц, Н7); 8,37 д (1Н, 2 Гц, Н5); 8,59 с (1Н, Н2).
Спектр ЯМР 13С, δ, м. д.: 15,53; 21,64; 21,73; 55,31; 69,44; 119,97; 123,67; 124,09; 128,38; 140,20; 144,68; 148,65; 158,58; 169,16.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Производные α-галогенкарбоновых кислот являются эффективными N-алкилирующими агентами, позволяющими вводить разнообразные заместители в структуру многих азотсодержащих гетероциклических соединений. Нами обнаружено, что использование в качестве субстрата 6,8-дибромхиназолин-4(3 Н )-она, также как и в случае его небромированного аналога [3], в «классических» условиях N-алкилирования (нагревание в среде безводного ДМФА в присутствии калия карбоната) в реакции со сложными эфирами α-галогенкарбоновых кислот с высоким выходом (77–82 % после очистки) приводит к продуктам селективного N3-замещения с сохранением слож-ноэфирной группы:
о
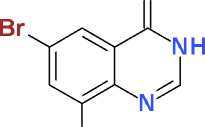
Br
I
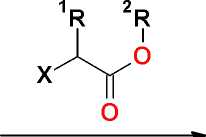
DMF / K2CO3
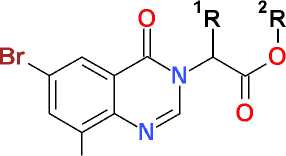
Br
II, III
где: R1 = H, CH 3 ; R2 = CH(CH 3 ) 2 ; CH 2 C 6 H 5 ; X = Cl, Br
Использование незначительного молярного избытка (6–8 %) алкилирующего агента позволяет достичь полной конверсии исходного 6,8-дибромхиназолин-4(3 Н )-она ( I ), в результате не обнаруживаемого в продуктах реакции методом ТСХ и ЯМР-спектроскопии. В связи с этим несколько более высокий выход целевого продукта алкилирования (82 % против 77 %), в случае использования бензилового эфира бромуксусной кислоты по сравнению с изопропиловым эфиром 2-хлорпропионовой кислоты, может быть объяснен не столько его более высокой реакционной способностью, сколько лучшей кристаллизуемо-стью соединения II при очистке.
Полученные сложные эфиры 2-[4-оксо-6,8-дибромхиназолин-3(4 Н )-ил]карбоновых кислот II и III представляют собой слабо окрашенные кристаллические вещества, практически не растворимые в воде, растворимые в полярных органических растворителях – низших алифатических спиртах, ДМФА и ДМСО. Химическое строение новых соединений доказано методами ЯМР 1Н и 13С спектроскопии.
ЗАКЛЮЧЕНИЕ
Разработан удобный метод синтеза сложных эфиров 2-[4-оксо-6,8-дибромхиназолин-
3(4 Н )-ил]карбоновых кислот на основе реакции селективного N3-алкилирования 6,8-диб-ромхиназолин-4(3 Н )-она соответствующими эфирами бромуксусной и 2-хлорпропионовой кислоты. Новые соединения могут быть использованы в качестве полупродуктов для получения фармакологически активных веществ хина-золинового ряда.
Список литературы Синтез сложных эфиров карбоновых кислот- производных 6,8- дибромхиназолин-4(зн)-она
- Арчакова Ю. В. //Усп. совр. естествознан. -2016. -№ 3. -С. 9-12.
- Гпухова Е. Г, Иванова О. В., Солодунова Г. Н.//ВНМЖ. -2014. -№ 4. -С. 18-20.
- Озеров А. А., Новиков М. С., Глухова Е. Г.//Усп. совр. естествознан. -2016. -№ 2. -С. 53-56.
- Самотруева М. А. //Хим.-фарм. журн. -2016.-Т. 50, № 6.-С. 12-14.
- Самотруева М. А. //Астрах. мед. журн. -2015. -№ 1. -С. 12-29.
- Солодунова Е A., Новиков М. С., Озеров А. А.//ВНМЖ. -2015, -№ 3. -С. 36-38.
- Тюренков И. Н., Озеров А.А., Солодунова Е.А., Арчакова Ю.В., Шматова Е.Н., Сампиева К.Т. //Хим.-фарм. журн. -2013. -Т. 47, № 5. -С. 7-10.
- Тюренков И. Н., Озеров А.А., Шматова Е.Н., Арчакова Ю.В. //Хим.-фарм. журн. -2015. -Т. 49, № 2. -С. 18-20.
- Цибизова А. А. //Междунар. журн. прикл. и фундамент, исслед. -2013. -№ 11. -С. 71-72.


