Синтез солей аспарагиновой кислоты щелочных и щелочноземельных металлов
Автор: Кадырова Р.Г., Кабиров Г.Ф., Муллахметов Р.Р.
Статья в выпуске: 1 т.209, 2012 года.
Бесплатный доступ
Отработаны оптимальные условия, позволяющие приготовить аспартаты в количествах, необходимых для исследования их биологической активности.
A-аминокислоты, аспарагиновя кислота, металлы, сукцинаты
Короткий адрес: https://sciup.org/14287421
IDR: 14287421 | УДК: 547.
Aspartic acid salts synthesis of alkali and alkaline-earth metals
Optimal conditions contributing to making aspartates in quantities suitable for their biological investigation were studied.
Текст научной статьи Синтез солей аспарагиновой кислоты щелочных и щелочноземельных металлов
α -Аминокислоты являются структурными единицами важнейшего класса биополимеров–белков, а также нашли самостоятельное применение в качестве лекарственных средств [1].
Аспарагиновая кислота способствует повышению потребления кислорода сердечной мышцей, обладает антитератогенным действием. В кардиологии применяют панангин – препарат, содержащий аспартаты калия и магния [2].
Панангин применяют при аритмиях сердца, обусловленных главным образом электролитными нарушениями, в первую очередь гипокалиемией. Предполагают, что аспарагинат является переносчиком калия и магния и способствует их проникновению во внутриклеточное пространство [3].
Аспарагинат калия–магния применяют при сердечной недостаточности, стенокардии, инфаркте миокарда.
«Аспаркам» по составу и действию близок к панангину (смесь калия аспарагината и магния аспарагината по 0,175 г) [4].
Фермент L-аспарагиназа обладает антилейкемической активностью. Применяют L-аспарагиназу самостоятельно или в комбинации с другими лекарственными средствами при остром лимфобластном лейкозе, лимфосаркоме и ретикулосаркоме [3].
Перспективными лекарственными препаратами являются соли лития, натрия и кальция аспарагиновой кислоты.
Установлено, что препараты лития относятся к психотропным средствам [5]. Они обладают способностью купировать острое маниакальное возбуждение у психических больных и предупреждать эффективные приступы [6].
Предложено использование сукцината лития в качестве средства для стимуляции лейкопоэза, вызванного действием ионизирующего излучения и цитостатиков. Отмечено, что сукцинат лития усиливает кроветворение и сроки восстановления лейкоцитов крови [7].
Изучен антидепрессивный эффект сукцината натрия, который связан с нормализацией уровня кровяного норадреналина. Рекомендовано комплексное использование гормональных препаратов и сукцината натрия в психиатрии для снижения маниакально-депрессивных состояний у пациентов. Сукцинат кальция входит в состав препарата «Иммунитал», который применяется в медицине как адаптоген широкого спектра действия, стимулирующий иммунную систему организма [8].
В литературе имеются незначительные сведения о синтезе солей аспарагиновой кислоты щелочных и щелочноземельных металлов.
С целью широкого изучения биологической активности аспартатов нами проведены исследования по разработке доступных методов их синтеза.
Материалы и методики. Для синтеза солей аспарагиновой кислоты щелочных и щелочноземельных металлов были использованы следующие реактивы: аспарагиновая–L кислота PRS-CODEX, сульфаты и гидроксиды металлов марки х.ч.
Собственные исследования. 1. Синтез аспартата лития. К суспензии 3,3 г (0,025 моля) аспарагиновой кислоты в 10 мл воды прибавляют порциями 2,1 г (0,05 моля) гидроксида лития – LiOH · H 2 O. Наблюдается разогрев реакционной массы до 40 ° С и растворение аспарагиновой кислоты. Через 15-20 минут при комнатной температуре выпадает обильный кристаллический осадок белого цвета. Реакционную смесь фильтруют, кристаллы промывают этанолом до рН 7 и сушат. Получают 3 г (82 %) аспартата лития, Li 2 C 4 H 5 O 4 N. Содержание азота (%): найдено – 9,39; вычислено – 9,65.
Аспартат лития – высокоплавкое вещество. Хорошо растворимо в воде, нерастворимо в спирте, ацетоне.
-
2. Синтез аспартата натрия. К суспензии 3,3 г (0,025 моля) аспарагиновой кислоты в 10 мл воды присыпают порциями 2 г (0,05 моля) гидроксида натрия. Реакционная смесь разогревается до 40-45 ° С и аспарагиновая кислота растворяется. Гомогенный раствор нагревают до
-
3. Синтез аспартата калия. К суспензии 3,3 г.(0,025 моля) аспарагиновой кислоты в 10 мл воды прибавляют порциями 2,8 г (0,025 моля) гидроксида калия. Реакционная смесь разогревается до 55-60 ° С и аспарагиновая кислота растворяется. Гомогенный раствор нагревают до 65-70 ° С 15 минут, выдерживают в течение 1 часа при комнатной температуре и упаривают. Вязкую массу охлаждают, промывают спиртом от щелочи и сушат. Получают 4,4 г (85 %) аспартата калия, К 2 C 4 H 5 O 4 N. Содержание азота (%): найдено – 6,52; вычислено – 6,70.
-
4. Синтез аспартата магния. К раствору 6,5 г MgSO 4 · 7H 2 O (0,025 моля) в 15 мл воды прибавляют 2 г (0,05 моля) гидроксида натрия. К выпавшему осадку гидроксида магния присыпают порциями 3,3 г (0,025 моля) аспарагиновой кислоты. Реакционная масса разогревается до 50 ° С. Гомогенный раствор нагревают до 80 ° С 15-20 минут, выдерживают в
-
5. Синтез аспартата кальция. К суспензии 6,6 г (0,05 моля) аспарагиновой кислоты в 20 мл воды при 80 ° С прибавляют порциями 3,7 г (0,05 моля) гидроксида кальция в течение 30 минут. Наблюдается растворение аспарагиновой кислоты и гидроксида кальция (ÏÐ Ca(OH)2 = 2,0 *10 14 ). Гомогенный раствор охлаждают до 7-10 ° С. Выпавший белый осадок фильтруют, промывают спиртом м сушат. Получают 5,5 (72 %)
70 ° С 15 минут, выдерживают в течение 1 часа при комнатной температуре и упаривают на водяной бане. Густую вязкую массу охлаждают, промывают спиртом от щелочи и сушат. Получают 3,4 г (80 %) аспартата натрия, Na 2 C 4 H 5 O 4 N. Содержание азота (%): найдено – 7,62; вычислено – 7,90.
Аспартат натрия – белый кристаллический продукт. Хорошо растворим в воде, нерастворим в спирте, ацетоне.
Аспартат калия – белый кристаллический продукт, хорошо растворим в воде, нерастворим в спирте, ацетоне.
течение 1 часа при комнатной температуре и упаривают. Кристаллический белый продукт промывают этанолом от щелочи и сушат. Получают 2,7 г (70 %) аспартата магния, MgC 4 H 5 O 4 N. Содержание азота (%): найдено – 8,92; вычислено – 9,03.
Аспартат магния – высокоплавкий кристаллический продукт. –10
Хорошо растворим в воде (ÏÐ = 6,0 · 10 ), нерастворим в спирте, ацетоне.
аспартата кальция, СaC 4 H 5 O 4 N. Содержание азота (%): найдено – 8,05;
вычислено – 8,18.
Аспартат кальция – высокоплавкий кристаллический продукт.
Частично растворим в воде, нерастворим в спирте, ацетоне.
Результаты исследований. Аспартаты щелочных и щелочноземельных металлов получают действием на суспензию аспарагиновой кислоты в воде гидроксидами соответствующих металлов. Реакция протекает по схеме:
НООС СН СН СООН 2
NH
+ МеОН
( Н 2 О )
МеООС СН СН СООМе 2
NH2
Ме = Li+, Na+, К +.
+ Ме ( ОН ) 2 (_ Н 2 О )
Ме [ OOC CH CH COO ] 2
NH
Ме = М g2+ , Са 2+
Аспартаты лития,магния и кальция представляют собой высокоплавкие кристаллические продукты.
Аспартаты натрия и калия – трудно кристаллизующиеся вязкие белые массы. Аспартаты указанных металлов хорошо растворимы в воде (аспартат кальция – частично), нерастворимы в спирте и ацетоне. Водные растворы солей имеют рН > 7. Способ получения аспартатов основан на классической реакции нейтрализации.
Отработаны оптимальные условия их синтеза и технологические приемы смешивания субстрата и реагента. Реакция проводится в гомогенной фазе при рН > 7, так как в щелочной среде в аминокислотах свободна аминогруппа и полностью ионизированы карбоксильные группы. В оптимальных условиях аспартаты получены с выходами более 70 %. Наиболее гладко протекает реакция синтеза аспартата лития.
Для подтверждения структуры полученных солей кроме элементного анализа проведена качественная реакция на аминогруппу.
Известно [9], что а -аминокислоты с хлоридом железа (III) в водных растворах образуют хелаты красного цвета. С солями меди в слабокислых средах в буферном растворе с добавлением ацетата натрия получаются хелаты ярко синего цвета.
Качественные реакции осуществляют по следующим методикам.
К раствору 0,05 г соли аспарагиновой кислоты в 1 мл воды прикапывают 3 %-ный раствор FeCl 3 . Раствор окрашивается в красный цвет.
В 1 мл 1 %-ного водного раствора соли аспарагиновой кислоты вносят несколько кристаллов СuSO 4 · 5Н 2 О и ацетата натрия. Раствор окрашивается в ярко синий цвет.
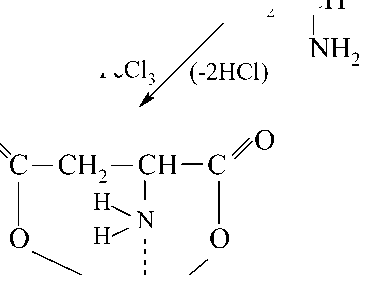
В результате ионизации солей в водных растворах хелаты образуются по схеме:
|
ООС СН СН СОО 2 NH2 + FeCl 3 (-2HCl) + CuSO 4 (- H 2 SO 4 ) O O O C CH CH C H 2 O HN O Fe 1 ' |
O C CH CH C H 2 N O HN O Cu |
Хелат железа (III) красного цвета
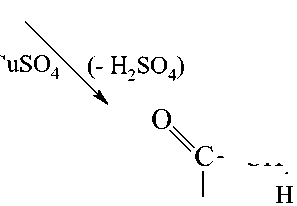
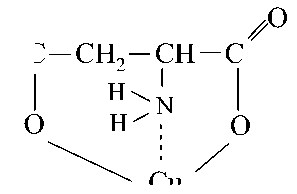
Хелат меди (II) ярко синего цвета
Аспартаты лития, натрия, калия,
магния и кальция в водных
растворах дают качественную реакцию на аминогруппу с хлоридом железа (III) и сульфатом меди по методикам, описанным выше.
Заключение. Синтезированы соли аспарагиновой кислоты щелочных (лития, натрия, калия) и щелочноземельных (магния, кальция) металлов. Показано, что способ их получения отличается простотой и основан на классической реакции нейтрализации. Отработаны оптимальные условия, позволяющие приготовить аспартаты в количествах, необходимых для исследования их биологической активности.
ЛИТЕРАТУРА: 1. Белобородов В.Л., Зурабян С.Э., Лузин А.П., Тюкавкина Н.А. Органическая химия. – М.: Дрофа, 2004. с. 591-592; 2. Комов В.П., Шведова В.Н. Биохимия. – М.: Дрофа, 2004. с. 26-28;3. Машковский М.Д. Лекарственные средства. ч.1. – М.: ООО «Книжный Дом ЛОКУС», 2002. 736 с.; 5. Машковский М.Д. Лекарственные средства. ч.2. – М.:Медицина, 1987. 575 с.; 6. Любимов Б.И., Толмачева Н.С., Островская Р.У.Экспериментальное изучение нейротропной активности лития оксибутирата // Ж. Фармалогия и токсикология. 1980, вып.3. с. 273277; 7. Пат. 2070041. RU C16A61K31/19. 10.12.96. Средство для стимуляции лейкопоэза. / К. Максутов.; 8. Кадырова Р.Г., Кабиров Г.Ф., Гильметдинов Б.М. Янтарная кислота и ее свойства. – Казань, Казан. гос. энерг. ун-т, 2005. 100 с.; 9. Гранберг И.И. Практические работы и семинарские занятия по органической химии. – М.: Дрофа 2001. 352 с.
СИНТЕЗ СОЛЕЙ АСПАРАГИНОВОЙ КИСЛОТЫ ЩЕЛОЧНЫХ И ЩЕЛОЧНОЗЕМЕЛЬНЫХ МЕТАЛЛОВ
Кадырова Р.Г., Кабиров Г.Ф., Муллахметов Р.Р.
Резюме
Отработаны оптимальные условия, позволяющие приготовить аспартаты в количествах, необходимых для исследования их биологической активности.
ASPARTIC ACID SALTS SYNTHESIS OF ALKALI AND ALKALINE-EARTH METALS
Kadyrova R.G., Kabirov G.F., Mullakhmetov R.R.


