Синтез, строение и фотохимические свойства производных: (2-MeO-5-BrC6H3)3SbR2, R= OC(O)C6F5, ONCHC6H4Br-2, OSO2C6H4CH3-4
Автор: Ефремов Андрей Николаевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 4 т.14, 2022 года.
Бесплатный доступ
Окисление трис(5-бром-2-метоксифенил)сурьмы гидропероксидом третичного бутила в диэтиловом эфире в присутствии пентафторбензойной кислоты, 2-бромбензальдоксима и 4-метилбензолсульфоновой кислоты (1:1:2 мольн.) приводит к образованию бис(пентафторбензоата) трис(5-бром-2-метоксифенил)сурьмы (1), бис(2-бромбензальдоксимата) трис(5-бром-2-метоксифенил)сурьмы (2), бис(4-метилбензолсульфоната) трис(5-бром-2-метоксифенил)сурьмы (3) соответственно. Соединения идентифицированы методом рентгеноструктурного анализа (РСА). По данным РСА, атомы сурьмы в кристаллах 1 [C35H18Br3F10O7Sb, M 1101,97; сингония триклинная, группа симметрии P1 ; параметры ячейки: a = 10,541(7), b = 13,427(11), c = 16,165(8) Å; a = 65,46(3), β = 72,34(3), g = 68,58(3) град.; V = 1906(2) Å3; размер кристалла 0,65×0,3×0,25 мм; интервалы индексов отражений -14 ≤ h ≤ 14, -18 ≤ k ≤ 18, -21 ≤ l ≤ 21; всего отражений 81715; независимых отражений 9657; Rint 0,0475; GOOF 1,027; R1 = 0,0360, wR2 = 0,0839; остаточная электронная плотность 1,59/-1,67 e/Å3], 2 [C35H28Br5N2O5Sb, M 1077,89; сингония моноклинная, группа симметрии P21/c; параметры ячейки: a = 13,378(6), b = 20,636(8), c = 14,251(8) Å; a = 90, β = 100,955(19), g = 90 град.; V = 3863(3) Å3; размер кристалла 0,35×0,14×0,1 мм; интервалы индексов отражений -16 ≤ h ≤ 17, -27 ≤ k ≤ 27, -19 ≤ l ≤ 19; всего отражений 103306; независимых отражений 9780; Rint 0,0798; GOOF 1,021; R1 = 0,0520 wR2 = 0,1218; остаточная электронная плотность 1,69/-1,54 e/Å3], 3 (сольват с бензолом) [C41H38Br3O9S2Sb, M 1100,31; сингония триклинная, группа симметрии P1 ; параметры ячейки: a = 9,643(6), b = 10,102(5), c = 23,634(14) Å; a = 77,74(3), β = 88,69(3), g = 74,82(3) град.; V = 2170(2) Å3; размер кристалла 0,36×0,22×0,16 мм; интервалы индексов отражений -13 ≤ h ≤ 12, -13 ≤ k ≤ 13, -31 ≤ l ≤ 31; всего отражений 84202; независимых отражений 11146; Rint 0,0454; GOOF 1,066; R1 = 0,0385, wR2 = 0,0818; остаточная электронная плотность 0,93/-0,78 e/Å3] имеют искаженную тригонально-бипирамидальную координацию с атомами кислорода карбоксилатных, оксиматных и сульфонатных лигандов в аксиальных положениях (аксиальные углы составляют 176,4(1)º для 1, 169,1(1)º для 2, 169,72(9)º для 3). Расстояния Sb-O составляют 2,086(2) и 2,120(2) Å для 1, 2,069(3) и 2,072(3) Å для 2, 2,134(3) и 2,118(3) Å для 3. Длины связей Sb-C изменяются в интервалах 2,097(3)-2,108(3) Å для 1, 2,119(6)-2,123(6) Å для 2, 2,104(3)-2,123(3) Å для 3. Полные таблицы координат атомов, длин связей и валентных углов для структур депонированы в Кембриджском банке структурных данных (№ 2045964 для 1, № 2064391 для 2, № 2055547 для 3; deposit@ccdc.cam.ac.uk; https://www.ccdc.cam.ac.uk). Изучена фотокаталитическая активность синтезированных соединений на примере фотодеструкции метиленового синего.
Трис(5-бром-2-метоксифенил)сурьма, 2-бромбензальдоксим, пентафторбензойная кислота, 4-метилбензолсульфоновая кислота, окислительный синтез, строение, рентгеноструктурный анализ, фотокаталитическая активность
Короткий адрес: https://sciup.org/147239533
IDR: 147239533 | УДК: 546.865+547.47+548.312.5 | DOI: 10.14529/chem220403
Synthesis, structure, and photochemical properties of derivatives: (2-MeO-5-BrC6H3)3SbR2, R= OC(O)C6F5, ONCHC6H4Br-2, OSO2C6H4CH3-4
Oxidation of tris(5-bromo-2-methoxyphenyl)antimony with tertiary butyl hydroperoxide in diethyl ether in the presence of pentafluorobenzoic acid, 2-bromobenzaldoxime, and 4-methylbenzenesulfonic acid (1:1:2 mole ratio) leads to formation of bis(pentafluorobenzoate) tris(5-bromo-2-methoxyphenyl)antimony (1), bis(2-bromobenzaldoxymate) tris(5-bromo-2-methoxyphenyl)antimony (2), bis(4-methylbenzenesulfonate) tris(5-bromo-2-methoxyphenyl)antimony (3), respectively. The compounds have been identified by X-ray diffraction analysis. According to the X-ray diffraction data, the antimony atoms in crystals 1 [C35H18Br3F10O7Sb, M 1101.97; triclinic system, space group P1 ; cell parameters: a = 10.541(7), b = 13.427(11), c = 16.165(8) Å; a = 65.46(3), β = 72.34(3), g = 68.58(3) deg.; V = 1906(2) Å3; crystal size 0.65 × 0.3 × 0.25 mm; index ranges -14 ≤ h ≤ 14, -18 ≤ k ≤ 18, -21 ≤ l ≤ 21; total reflections 81715; independent reflections 9657; Rint 0.0475; GOOF 1.027; R1 = 0.0360, wR2 = 0.0839; residual electron density 1.59/-1.67 e/Å3], 2 [C35H28Br5N2O5Sb, M 1077.89; monoclinic system, space group P21/c; cell parameters: a = 13.378(6), b = 20.636(8), c = 14.251(8) Å; a = 90, β = 100.955(19), g = 90 deg.; V = 3863(3) Å3; crystal size 0.35×0.14×0.1 mm; index ranges -16 ≤ h ≤ 17, -27 ≤ k ≤ 27, -19 ≤ l ≤ 19; total reflections 103306; independent reflections 9780; Rint 0.0798; GOOF 1.021; R1 = 0.0520 wR2 = 0.1218; residual electron density 1.69/-1.54 e/Å3], 3 (benzene solvate) [C41H38Br3O9S2Sb, M 1100.31; triclinic system, space group P1 ; cell parameters: a = 9.643(6), b = 10.102(5), c = 23.634(14) Å; a = 77.74(3), β = 88.69(3), g = 74.82(3) deg.; V = 2170(2) Å3; crystal size 0.36×0.22×0.16 mm; index ranges -13 ≤ h ≤ 12, -13 ≤ k ≤ 13, -31 ≤ l ≤ 31; total reflections 84202; independent reflections 11146; Rint 0.0454; GOOF 1.066; R1 = 0.0385, wR2 = 0.0818; residual electron density 0.93/-0.78 e/Å3] have a distorted trigonal-bipyramidal coordination with the oxygen atoms of the carboxylate, oximate and sulfonate ligands in axial positions (the axial angles are 176.4(1)º for 1, 169.1(1)º for 2, 169.72(9)º for 3). The Sb-O distances are 2.086(2) and 2.120(2) Å for 1, 2.069(3) and 2.072(3) Å for 2, 2.134(3) and 2.118(3) Å for 3. The Sb-C bond lengths vary in the intervals 2.097(3)-2.108(3) Å in 1, 2.119(6)-2.123(6) Å in 2, 2.104(3)-2.123(3) Å in 3. Complete tables of atomic coordinates, bond lengths, and bond angles for the structures are deposited at the Cambridge Crystallographic Data Center (No. 2045964 for 1, No. 2064391 for 2, No. 2055547 for 3; deposit@ccdc.cam.ac.uk; https://www.ccdc.cam.ac.uk). The photocatalytic activity of the synthesized compounds was studied by photodestruction of methylene blue as an example.
Текст научной статьи Синтез, строение и фотохимические свойства производных: (2-MeO-5-BrC6H3)3SbR2, R= OC(O)C6F5, ONCHC6H4Br-2, OSO2C6H4CH3-4
Окисление трис(5-бром-2-метоксифенил)сурьмы гидропероксидом третичного бутила в диэтиловом эфире в присутствии пентафторбензойной кислоты, 2-бромбензальдоксима и 4-метилбензолсульфоновой кислоты (1:1:2 мольн.) приводит к образованию бис(пентафторбензоата) трис(5-бром-2-метоксифенил)сурьмы (1), бис(2-бромбензальдоксимата) трис(5-бром-2-метокси-фенил)сурьмы (2), бис(4-метилбензолсульфоната) трис(5-бром-2-метоксифенил)сурьмы (3) соответственно. Соединения идентифицированы методом рентгеноструктурного анализа (РСА). По данным РСА, атомы сурьмы в кристаллах 1 [C35H18Br3F10O7Sb, M 1101,97; сингония триклинная, группа симметрии P1; параметры ячейки: a = 10,541(7), b = 13,427(11), c = 16,165(8) Å; α = 65,46(3), β = 72,34(3), γ = 68,58(3) град.; V = 1906(2) Å3; размер кристалла 0,65×0,3×0,25 мм; интервалы индексов отражений –14 ≤ h ≤ 14, –18 ≤ k ≤ 18, –21 ≤ l ≤ 21; всего отражений 81715; независимых отражений 9657; Rint 0,0475; GOOF 1,027; R1 = 0,0360, wR2 = 0,0839; остаточная электронная плотность 1,59/–1,67 e/Å3], 2 [C35H28Br5N2O5Sb, M 1077,89; сингония моноклинная, группа симметрии P21/c; параметры ячейки: a = 13,378(6), b = 20,636(8), c = 14,251(8) Å; α = 90, β = 100,955(19), γ = 90 град.; V = 3863(3) Å3; размер кристалла 0,35×0,14×0,1 мм; интервалы индексов отражений –16 ≤ h ≤ 17, –27 ≤ k ≤ 27, –19 ≤ l ≤ 19; всего отражений 103306; независимых отражений 9780; Rint 0,0798; GOOF 1,021; R1 = 0,0520 wR2 = 0,1218; остаточная электронная плотность 1,69/–1,54 e/Å3], 3 (сольват с бензолом) [C41H38Br3O9S2Sb, M 1100,31; сингония триклинная, группа симметрии P1; параметры ячейки: a = 9,643(6), b = 10,102(5), c = 23,634(14) Å; α = 77,74(3), β = 88,69(3), γ = 74,82(3) град.; V = 2170(2) Å3; размер кристалла 0,36×0,22×0,16 мм; интервалы индексов отражений –13 ≤ h ≤ 12, –13 ≤ k ≤ 13, –31 ≤ l ≤ 31; всего отражений 84202; независимых отражений 11146; Rint 0,0454; GOOF 1,066; R1 = 0,0385, wR2 = 0,0818; остаточная электронная плотность 0,93/–0,78 e/Å3] имеют искаженную тригонально-бипирамидальную координацию с атомами кислорода карбоксилатных, оксиматных и сульфонатных лигандов в аксиальных положениях (аксиальные углы составляют 176,4(1)º для 1, 169,1(1)º для 2, 169,72(9)º для 3). Расстояния Sb-O составляют 2,086(2) и 2,120(2) Å для 1, 2,069(3) и 2,072(3) Å для 2, 2,134(3) и 2,118(3) Å для 3. Длины связей Sb-C изменяются в интервалах 2,097(3)–2,108(3) Å для 1, 2,119(6)–2,123(6) Å для 2, 2,104(3)–2,123(3) Å для 3. Полные таблицы координат атомов, длин связей и валентных углов для структур депонированы в Кембриджском банке структурных данных (№ 2045964 для 1, № 2064391 для 2, № 2055547 для 3; ; . Изучена фотокаталитическая активность синтезированных соединений на примере фотодеструкции метиленового синего.
Производные триарилсурьмы общей формулы Ar 3 SbХ 2 , где Х – лиганд, связанный с атомом сурьмы через атом кислорода, являются биологически активными соединениями, оказывающими противоопухолевое, антилейшманиозное и антибактериальное действие [1–9], обладающими электрохимическими и фотолюминесцентными свойствами [10, 11]. Имеются примеры их использования в качестве фотокатализаторов [12–14]. Такие производные могут быть получены по реакциям замещения из дигалогенидов триарилсурьмы и кислоты HX в присутствии акцептора галогеново-дорода [1–8, 15–17]. Удобным одностадийным методом синтеза производных триарилсурьмы общей формулы Ar3SbХ2 является окислительный метод. Так, например, были получены дикарбокси-латы [18, 19], диоксиматы [20, 21], дисульфонаты [22, 23] трифенил- и три- пара -толилсурьмы.
В настоящей работе продолжено изучение окислительного метода синтеза арильных соединений сурьмы(V) из триарилсурьмы на примере трис (5-бром-2-метоксифенил)сурьмы и осуществлена проверка фотокаталитической активности полученных соединений.
Экспериментальная часть
Синтез бис(пентафторбензоата) трис(5-бром-2-метоксифенил)сурьмы (2-СН3O-5-BrC6H3)3Sb[OC(O)C6F5]2 (1). К раствору 100 мг (0,147 ммоль) трис(5-бром-2- метоксифенил)сурьмы и 62 мг (0,294 ммоль) пентафторбензойной кислоты в 30 мл эфира прибавляли 19 мг (0,147 ммоль) 70%-ного водного раствора трет-бутилгидропероксида и выдерживали 24 ч при 20 °C. После испарения растворителя остаток перекристаллизовывали из смеси растворителей бензол-н-октан (2:1 объемн.). Получили 147 мг (91 %) неокрашенных кристаллов соединения 1 с т. пл. 159 °С.
ИК-спектр, ( ν , см - 1): 3103, 3016, 2943, 2850, 1678, 1649, 1577, 1521, 1494, 1475, 1442, 1377,
1334, 1282, 1259, 1184, 1149, 1114, 1107, 1093, 1047, 1014, 991, 925, 883, 825, 812, 752, 709, 671, 621, 586, 538, 518, 487, 443.
Найдено, %: C 38,28; H 1,71. C 35 H 18 Br 3 F 10 O 7 Sb. Вычислено, %: C 38,15; H 1,65.
Аналогично получали соединения 2 и 3 .
Синтез бис (2-бромбензальдоксимата) трис (5-бром-2-метоксифенил)сурьмы (2-СН 3 O-5-BrC 6 H 3 ) 3 Sb(ON=CHC 6 H 4 Br-2) 2 (2). Бесцветные кристаллы, выход 86 %, т. пл. 180 °С. ИК-спектр, ( ν , см - 1): 3061, 3007, 2935, 2841, 1571, 1473, 1438, 1373, 1327, 1282, 1269, 1247, 1207, 1178, 1143, 1116, 1089, 1047, 1018, 952, 877, 819, 806, 767, 754, 717, 694, 642, 619, 557, 518, 478, 443.
Найдено, %: С 39,51; Н 2,58. C 35 H 28 Br 5 N 2 O 5 Sb. Вычислено, %: С 39,00; Н 2,62.
Синтез сольвата бис (4-метилбензолсульфоната) трис (5-бром-2-метоксифенил)сурьмы с бензолом (2-СН 3 O-5-BrC 6 H 3 ] 3 Sb[OSO 2 С 6 H 4 СН 3 -4] 2 · PhH (3). Бежевые кристаллы, выход 85 %, т. пл. 185 °С. ИК-спектр, ( ν , см - 1): 3066, 3001, 2941, 2885, 2839, 1575, 1560, 1475, 1436, 1377, 1311, 1301, 1280, 1257, 1182, 1163, 1132, 1097, 1041, 1010, 950, 916, 812, 678, 621, 569, 557, 524, 435, 422.
Найдено, %: С 44,64; Н 3,52. C 41 H 38 Br 3 O 9 S 2 Sb. Вычислено, %: С 44,75; Н 3,49.
Элементный анализ на C и H выполнен на элементном анализаторе Carlo Erba CHNS-O EA 1108. Температуры плавления измерены на синхронном термоанализаторе Netzsch 449C Jupiter.
ИК-спектры соединений 1 – 3 записывали на ИК-Фурье спектрометре Shimadzu IR Affinity-1S в таблетке KBr в области 4000 - 400 см - 1.
Рентгеноструктурный анализ (РСА) кристаллов соединений 1–3 проведен на автоматическом четырехкружном дифрактометре D8 QUEST фирмы Bruker (Mo Kα-излучение, λ = 0,71073 Å, графитовый монохроматор) при 293 К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены с помощью программ SMART и SAINT-Plus [24]. Все расчеты по определению и уточнению структур выполнены с помощью программ SHELXL/PC [25] OLEX2 [26]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Положение атомов водорода уточняли по модели наездника (Uизо(H) = 1,2Uэкв(C)). Кристаллографические данные и результаты уточнения структур приведены в табл. 1, геометрические характеристики координационного полиэдра атома сурьмы – в табл. 2. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2045964 (1); 2064391 (2); 2055547 (3); или .
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структур 1 - 3
|
Параметр |
1 |
2 |
3 |
|
Формула |
C 35 H 18 Br 3 F 10 O 7 Sb |
C 35 H 28 Br 5 N 2 O 5 Sb |
C 41 H 38 Br 3 O 9 S 2 Sb |
|
М |
1101,97 |
1077,89 |
1100,31 |
|
Сингония |
триклинная |
моноклинная |
триклинная |
|
Пр. группа |
P 1 |
P 2 1 /c |
P 1 |
|
a , Å |
10,541(7) |
13,378(6) |
9,643(6) |
Окончание табл. 1
|
Параметр |
1 |
2 |
3 |
|
b, Å |
13,427(11) |
20,636(8) |
10,102(5) |
|
c, Å |
16,165(8) |
14,251(8) |
23,634(14) |
|
α , º |
65,46(3) |
90 |
77,74(3) |
|
β, º |
72,34(3) |
100,955(19) |
88,69(3) |
|
γ , º |
68,58(3) |
90 |
74,82(3) |
|
V , Å3 |
1906(2) |
3863(3) |
2170(2) |
|
Z |
2 |
4 |
2 |
|
ρ (выч.), г/см3 |
1,920 |
1,853 |
1,684 |
|
µ , мм–1 |
3,964 |
5,928 |
3,546 |
|
F (000) |
1060,0 |
2072,0 |
1088,0 |
|
Размер кристалла, мм |
0,65 × 0,3 × 0,25 |
0,35 × 0,14 × 0,1 |
0,36 × 0,22 × 0,16 |
|
Область сбора данных по 2 θ , град |
6,158–57 |
6,092–56,998 |
6,102–57,482 |
|
Интервалы индексов отражений |
–14 ≤ h ≤ 14, –18 ≤ k ≤ 18, –21 ≤ l ≤ 21 |
–16 ≤ h ≤ 17, –27 ≤ k ≤ 27, –19 ≤ l ≤ 19 |
–13 ≤ h ≤ 12, –13 ≤ k ≤ 13, –31 ≤ l ≤ 31 |
|
Измерено отражений |
81715 |
103306 |
84202 |
|
Независимых отражений |
9657 |
9780 |
11146 |
|
R int |
0,0475 |
0,0798 |
0,0454 |
|
Переменных уточнения |
540 |
437 |
499 |
|
GOOF |
1,027 |
1,021 |
1,066 |
|
R -факторы по F2 > 2 σ (F2) |
R 1 = 0,0360, wR 2 = 0,0839 |
R 1 = 0,0520, wR 2 = 0,1218 |
R 1 = 0,0385, wR 2 = 0,0818 |
|
R-факторы по всем отражениям |
R 1 = 0,0466, wR 2 = 0,0893 |
R 1 = 0,0890, wR 2 = 0,1413 |
R 1 = 0,0516, wR 2 = 0,0866 |
|
Остаточная электронная плотность (max/min), e/A3 |
1,59/–1,67 |
1,69/–1,54 |
0,93/–0,78 |
Таблица 2
|
Связь |
d , Å |
Угол 1 |
ω , град. |
|
|
1 |
||||
|
Sb(1) - O(4) |
2,086(2) |
O(4)Sb(1)O(6) |
176,38(9) |
|
|
Sb(1) - O(6) |
2,120(2) |
O(4)Sb(1)C(1) |
98,91(12) |
|
|
Sb(1) - C(1) |
2,108(3) |
O(4)Sb(1)C(11) |
88,10(12) |
|
|
Sb(1) - C(11) |
2,097(3) |
O(4)Sb(1)C(21) |
87,94(11) |
|
|
Sb(1) - C(21) |
2,111(3) |
C(1)Sb(1)O(6) |
82,82(12) |
|
|
Sb(1)∙∙∙О(1) |
3,093(3) |
C(1)Sb(1)C(21) |
124,58(12) |
|
|
Sb(1)∙∙∙О(2) |
3,183(4) |
C(11)Sb(1)O(6) |
88,32(12) |
|
|
Sb(1)∙∙∙О(3) |
3,094(3) |
C(11)Sb(1)C(1) |
110,79(13) |
|
|
Sb(1)∙∙∙О(5) |
3,212(3) |
C(11)Sb(1)C(21) |
124,43(13) |
|
|
Sb(1)∙∙∙О(7) |
3,338(4) |
C(21)Sb(1)O(6) |
93,70(11) |
|
|
2 |
||||
|
Sb(1) - O(4) |
2,069(3) |
O(4)Sb(1)O(5) |
169,11(15) |
|
|
Sb(1) - O(5) |
2,072(3) |
O(4)Sb(1)C(1) |
94,33(17) |
|
|
Sb(1) - C(1) |
2,123(5) |
O(4)Sb(1)C(11) |
80,88(17) |
|
|
Sb(1) - C(11) |
2,123(6) |
O(4)Sb(1)C(21) |
89,54(18) |
|
|
Sb(1) - C(21) |
2,119(6) |
O(5)Sb(1)C(1) |
96,49(17) |
|
|
Sb(1)∙∙∙О(1) |
3,035(4) |
O(5)Sb(1)C(11) |
92,70(17) |
|
|
Sb(1)∙∙∙О(2) |
3,074(6) |
O(5)Sb(1)C(21) |
87,00(17) |
|
|
Sb(1)∙∙∙О(3) |
3,165(5) |
C(1)Sb(1)C(11) |
119,2(2) |
|
|
Sb(1)∙∙∙N(1) |
2,895(4) |
C(21)Sb(1)C(1) |
115,2(2) |
|
|
Sb(1)∙∙∙N(2) |
2,887(4) |
C(21)Sb(1)C(11) |
125,2(2) |
|
|
3 |
||||
|
Sb(1) - O(7) 1 |
2,134(3) \ |
O(4)Sb(1)O(7) 1 |
169,72(9) |
|
Окончание табл. 2
|
Связь |
d , Å |
Угол |
ω , град. |
|
Sb(1) - O(4) |
2,118(3) |
O(4)Sb(1)C(11) |
84,88(11) |
|
Sb(1) - C(11) |
2,123(3) |
C(11)Sb(1)O(7) |
89,50(11) |
|
Sb(1) - C(21) |
2,108(3) |
C(21)Sb(1)O(7) |
84,55(11) |
|
Sb(1) - C(1) |
2,104(3) |
C(21)Sb(1)O(4) |
91,30(11) |
|
Sb(1)∙∙∙О(1) |
3,092(3) |
C(21)Sb(1)C(11) |
123,10(12) |
|
Sb(1)∙∙∙О(2) |
2,952(3) |
C(1)Sb(1)O(7) |
91,54(12) |
|
Sb(1)∙∙∙О(3) |
3,073(3) |
C(1)Sb(1)O(4) |
98,73(11) |
|
Sb(1)∙∙∙О(5) |
3,740(4) |
C(1)Sb(1)C(11) |
125,96(12) |
|
Sb(1)∙∙∙О(8) |
3,312(3) |
C(1)Sb(1)C(21) |
110,77(12) |
Фотокаталитическую активность соединений 1 – 3 оценивали путем фотодеградации в их присутствии водного раствора красителя метиленового синего (МС) при температуре окружающей среды 20 °С. Фотокаталитические реакции выполнены по методике [12]. Навески 1 – 3 массой 20 мг и 50 мл водного раствора МС концентрации 5 мг/л помещали в кварцевый стакан объемом 100 мл. Для установления адсорбционно-десорбционного равновесия полученную суспензию перемешивали на магнитной мешалке в темноте в течение 30 мин. Фотокаталитический тест проводили при помощи облучателя (длина волны – 395 нм, полуширина пика излучения – 2 нм, освещённость – 600 Вт/м2). Облучатель с кварцевым стаканом помещали на магнитную мешалку. Суспензию облучали при постоянном перемешивании в течение 1 ч. Отбор проб проводили каждые 15 мин шприцом, далее отфильтровывали в кювету через мембранный шприцевой фильтр c размерами пор 0,22 мкм. Измерение концентрации МС осуществляли методом УФ-спектроскопии с помощью спектрометра Shimadzu UV2700 при длине волны 291 нм (раствор сравнения – дистиллированная вода).
Обсуждение результатов
Найдено, что взаимодействие трис (5-бром-2-метоксифенил)сурьмы с пентафторбензойной кислотой, 2-бромбензальдоксимом и 4-метилбензолсульфоновой кислотой в присутствии трет бутилгидропероксида при мольном соотношении реагентов 1:2:1 в диэтиловом эфире приводит к образованию дикарбоксилата, диоксимата и дисульфоната трис (5-бром-2-метоксифенил)сурьмы соответственно с выходом до 98 %.
(2-СН 3 O-5-BrC 6 H 3 ) 3 Sb + 2 HХ + t -BuOOH → (2-СН 3 O-5-BrC 6 H 3 ) 3 SbХ 2 + t -BuOH + H 2 O,
Х = OC(O)C 6 F 5 ( 1 ), ON=CHC 6 H 4 Br-2 ( 2 ), OSO 2 C 6 H 4 CH 3 -4 ( 3 ).
После перекристаллизации твердого остатка из смеси растворителей н -октан–бензол (1:2 объемн.) получены кристаллы, пригодные для рентгеноструктурного анализа (РСА).
В ИК-спектрах соединений 1 – 3 наблюдается полоса поглощения средней интенсивности валентных колебаний связей Sb–C при 443, 443 и 446 см–1 соответственно. Валентным колебаниям карбонильной группы в ИК-спектре соединения 1 соответствует полоса поглощения при 1678 см–1, колебаниям ν(C=N) в 2 – при 1554 см–1, колебаниям ν(S=O) в 3 – при 1163 см–1. Полосы поглощения, характеризующие колебания ν(С Ar –О–C Me ) в арильных лигандах, наблюдаются при 1014, 1047 ( 1 ), 1018, 1047 ( 2 ) и 1010, 1041 ( 3 ) см–1. Полосы поглощения валентных колебаний метильных групп расположены в ИК-спектрах при 2943 ( 1 ), 2935 ( 2 ) и 2941 ( 3 ) см–1 (асимметричные колебания) и при 2850 ( 1 ), 2841( 2 ) и 2839 ( 3 ) см–1 (симметричные колебания). ИК-спектры соединений также содержат характерные полосы валентных колебаний углеродного скелета ароматических фрагментов: 1577, 1494, 1442 см–1 для 1 , 1571, 1473, 1438 см–1 для 2 , 1575, 1475, 1438 см–1 для 3 . Валентным колебаниям связей CAr–H отвечает полоса поглощения средней интенсивности при 3103 ( 1 ), 3061 ( 2 ) и 3066 ( 3 ) см–1 [27–29].
По данным РСА в молекулах производных трис (5-бром-2-метоксифенил)сурьмы атомы сурьмы имеют искаженную тригонально-бипирамидальную координацию с атомами кислорода карбоксилатных, оксиматных и сульфонатных лигандов в аксиальных положениях (рис. 1 - 3). Дисульфонат триарилсурьмы после перекристаллизации представляет собой сольват (2-СН 3 O-5-
Длины связей и валентные углы в молекулах соединений 1 - 3
BrC 6 H3)3Sb(OSO2C 6 H4CH3-4)2 • PhH ( 3 ). В молекуле дикарбоксилата триарилсурьмы 1 фрагмент -
C 6 F 5 разупорядочен по двум положениям с заселенностью атомов 0,41/0,59.
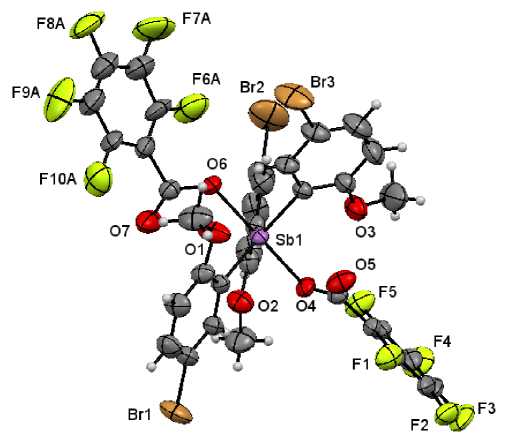
Рис. 1. Строение соединения 1 (разупорядоченные атомы не приведены)
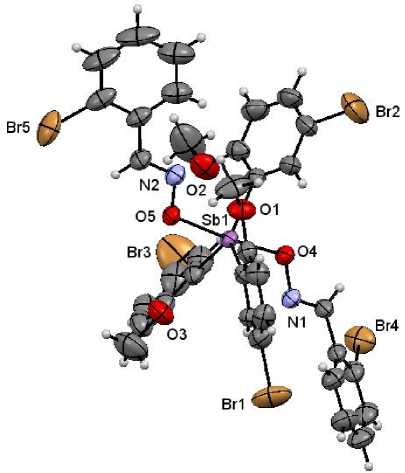
Рис. 2. Строение соединения 2
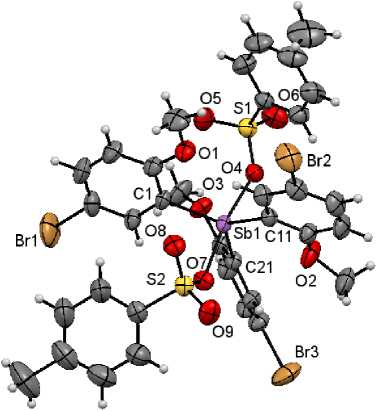
Рис. 3. Строение соединения 3 (сольватная молекула бензола не приведена)
Суммы углов в экваториальной плоскости CSbC в молекулах 1 - 3 составляют 359,8(2) ° , 359,6(2) ° и 359,83(12) ° соответственно. Аксиальные углы OSbO отклоняются от значения в 180° и составляют 176,4(1)º ( 1 ), 169,1(1)º ( 2 ) и 169,72(9)º ( 3 ). Атом сурьмы выходит из экваториальной плоскости [С 3 ] на 0,056 ( 1 ), 0,073 ( 2 ) и 0,051 (3) Å. Плоские арильные кольца повернуты вокруг связей Sb–Cэкв таким образом, чтобы минимизировать внутри- и межмолекулярные взаимодействия.
Экваториальные заместители в диоксимате трис (5-бром-2-метоксифенил)сурьмы 2 находятся дальше от центрального атома (длины связей Sb-C изменяются в переделах 2,119(6)–2,123(6) Å), чем аксиальные (расстояния Sb-O составляют 2,069(3) и 2,072(3) Å). Обратное наблюдается в дисульфонате триарилсурьмы 3 , а в дикарбоксилате 1 удаленность заместителей от атома сурьмы практически одинакова. Длины связей Sb-C и Sb-O при этом равны 2,097(3)–2,108(3) Å и 2,086(2), 2,120(2) Å в 1 , 2,104(3)–2,123(3) Å и 2,134(3), 2,118(3) Å в 3 .
Как правило, карбоксилатные лиганды в молекулах структурно охарактеризованных дикарбоксилатов триарилсурьмы имеют цис -ориентацию относительно экваториального фрагмента C 3 Sb и формирование внутримолекулярных контактов Sb --- O(=C) происходит внутри одного экваториального угла, значение которого может возрастать до 161,47(6) ° [30]. Однако в соединении 1 карбонильные атомы кислорода находятся напротив разных экваториальных углов, которые изменяются в интервалах 110,8(1) - 124,6(1) ° , как и в ранее охарактеризованных молекулах дикарбоксилатов трис (5-бром-2-метоксифенил)сурьмы [31]. Внутримолекулярные расстояния Sb --- O(=C) равны 3,212(3), 3,338(4) А, что меньше суммы ван-дер-ваальсовых радиусов атомов Sb и O (3,58 Å [32]). В структуре диоксимата триарилсурьмы 2 присутствуют внутримолекулярные контакты между атомоми сурьмы и азота оксиматных лигандов. Расстояния Sb···N составляют 2,895(4), 2,887(4) Å. В соединении 3 наблюдается дополнительная координация только одного сульфонатного лиганда, расстояние Sb --- O(=S) составляет 3,312(4) А.
В молекулах 1 – 3 наблюдаются укороченные расстояния между атомами кислорода метоксигрупп и атомом сурьмы (3,085(7), 3,087(6), 3,165(6) Å для 1 , 3,035(4), 3,074(6), 3,165(5) Å для 2 , 2,952(3), 3,073(3), 3,092(3) Å для 3 ), что близко к значениям аналогичных расстояний в молекуле трис (5-бром-2-метоксифенил)сурьмы ( 2,985, 3,051 и 3,052 Å [33]), вследствие чего координационное число атома металла повышается в 1 и 2 до 10 (5+2+3), а в 3 – до 9 (5+1+3).
Формирование пространственной сетки в кристалле соединения 1 обусловлено наличием слабых водородных связей типа C=O—H-C (2,63, 2,57 А) и C-F --- H-C (2,50, 2,42, 2,54, 2,66, 2,61 А). В кристалле соединения 2 присутствуют межмолекулярные контакты =N-O-"H-C (2,49, 2,68, 2,56 А) и C-Br—H-C (2,86 А). Пространственная сетка кристалла соединения 3 формируется посредством образования слабых водородных связей типа S=O—R-C (2,40, 2,69, 2,57, 2,63 А). Сольватная молекула бензола также принимает участие в упаковке молекул соединения 3 , образуя межмолекулярные водородные связи типа Ph-H—Br-C (2,92 А). Во всех кристаллических структурах наблюдаются СН --- п -взаимодействия.
Для оценки фотокаталитической активности соединений проводили фотодеградацию в их присутствии водного раствора МС. При этом в отсутствии комплексов разложение МС не наблюдалось. Потеря МС на шприцевом фильтре составила в среднем 0,6 мг/л и учтена при расчетах. Результаты исследований представлены на рис. 4 в виде зависимости концентрационных соотношений (С/С0) красителя МС от времени облучения ( τ , мин).
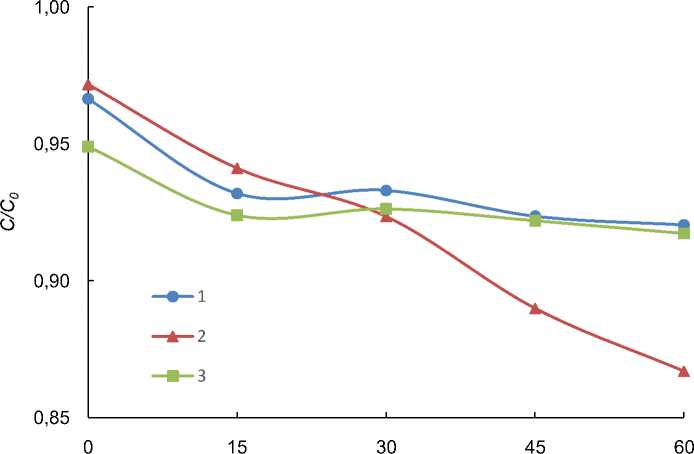
τ , мин
Рис. 4. Изменение приведенной концентрации (С/С 0 ) при УФ-облучении ( τ , мин) раствора МС в присутствии 1–3
Так, при облучении в течение 60 мин растворов, содержащих 1 – 3 , разложение МС составило 4,8, 10,8, 3,3 % соответственно, что существенно ниже, чем при использовании в качестве фотокатализаторов (2-СН 3 O-5-BrC 6 H 3 ) 3 Sb[OC(O)R] 2 (R = C 6 HF 4 -2,3,4,5, CF 2 Br, CF 2 CF 2 CF 3 ), где распад МС составлял 20–26 % [13]. Снижение концентрации МС в растворах, содержащих соединения 1 и 3 , в результате сорбции сопоставимо со снижением его концентрации в результате фотокатализа.
Выводы
Таким образом, взаимодействие трис (5-бром-2-метоксифенил)сурьмы с пентафторбензойной кислотой, 2-бромбензальдоксимом и 4-метилбензолсульфоновой кислотой в присутствии трет -бутилгидропероксида (1:2:1 мольн.) приводит к образованию дикарбоксилата, диоксимата и дисульфоната трис (5-бром-2-метоксифенил)сурьмы. По данным РСА, в молекулах производных трис (5-бром-2-метоксифенил)сурьмы атомы сурьмы имеют искаженную тригонально-бипирамидальную координацию с атомами кислорода карбоксилатных, оксиматных и сульфонатных лигандов в аксиальных положениях. В молекулах синтезированных соединений наблюдаются короткие контакты между атомами кислорода метокси-групп и атомом сурьмы. Соединения обладают низкой фотокаталитической активностью разложения метиленового синего под действием УФ-облучения.
Финансирование работы
Работа выполнена при финансовой поддержке РФФИ в рамках научного проекта № 20-33-90099.
Выражаю благодарность проф. В.В. Шарутину за проведенные рентгеноструктурные исследования.
Список литературы Синтез, строение и фотохимические свойства производных: (2-MeO-5-BrC6H3)3SbR2, R= OC(O)C6F5, ONCHC6H4Br-2, OSO2C6H4CH3-4
- Synthesis and in vitro antitumor activity of some triarylantimony di(N-phenylglycinates) / Yu L., Ma Y.-Q., Wang G.-C., Li J.-S. // Heteroat. Chem. 2004. Vol. 15, no. 1. P. 32-36. DOI: 10.1002/hc.10208
- Structural elucidation and bioassays of newly synthesized pentavalent antimony complexes / T. Iftikhar, M.K. Rauf, S. Sarwar et al. // J. Organomet. Chem. 2017. Vol. 851. P. 89-96. DOI: 10.1016/j.jorganchem.2017.09.002
- A structural investigation of heteroleptic pentavalent antimonials and their leishmanicidal activity / R. Mushtaq, M.K. Rauf, M. Bond et al. // Appl. Organomet. Chem. 2016. Vol. 30, no. 6. P. 465-472. DOI: 10.1002/aoc.3456
- Structural investigations, anti-leishmanial, antibacterial and docking studies of new pentavalent antimony carboxylates / L. Saleem, A.A. Altaf, A. Badshahet al. // Inorg. Chim. Acta. 2018. Vol. 474. P. 148-155. DOI: 10.1016/j.ica.2018.01.036
- Novel triphenylantimony(V) and triphenylbismuth(V) complexes with benzoic acid derivatives: structural characterization, in vitro antileishmanial and antibacterial activities and cytotoxicity against macrophages / A. Islam, J.G. Da Silva, F.M. Berbet et al. // Molecules. 2014. Vol. 19, no. 5. P. 60096030. DOI: 10.3390/molecules19056009
- Synthesis, characterization and antileishmanial studies of some bioactive heteroleptic pentavalent antimonials / R. Mushtaq, M.K. Rauf, M. Bolt et al. // Appl. Organomet. Chem. 2016. Vol. 31, no. 5. P. e3606. DOI: 10.1002/aoc.3606
- Ma Y.Q., Yu L., Li J.S. Synthesis and biological activity of some triarylantimony dipyrazolecar-boxylates // Heteroat. Chem. 2002. Vol. 13, no. 4. P. 299-301. DOI: 10.1002/hc.10033
- Anti-leishmanial activity of heteroleptic organometallic Sb(V) compounds / M.I. Ali, M.K. Rauf, A. Badshah et al. // Dalton Trans. 2013. Vol. 42, no. 48. P. 16733. DOI: 10.1039/c3dt51382c
- Perspectives of antimony compounds in oncology / P. Sharma, D. Perez, A. Cabrera et al. // Acta Pharm. Sinica. 2008. Vol. 29, no. 8. P. 881-890. DOI: 10.1111/j.1745-7254.2008.00818.x
- Synthesis, X-ray studies, electrochemical properties, evaluation as in vitro cytotoxic and antibacterial agents of two antimony(III) complexes with dipicolinic acid / S. Abdolmaleki, N. Yarmoham-madi, H. Adib et al. // Polyhedron. 2019. Vol. 159. P. 239-250. DOI: 10.1016/J.POLY.2018.11.063
- Crystals of Sb3+-coordination complexes exhibiting yellowish green emissions with outstanding lifetimes / H.-X. Qi, H. Jo, H.E. Lee et al. // J. Solid State Chem. 2019. Vol. 274. P. 69-74. DOI: 10.1016/J.JSSC.2019.03.018
- Two organoantimony (V) coordination complexes modulated by isomers of trifluoromethylben-zoate ligands: syntheses, crystal structure, photodegradation properties / X.-Y. Zhang, L. Cui, X. Zhang et al. // J. Mol. Struct. 2017. Vol. 1134. P. 742-750. DOI: 10.1016/j.molstruc.2017.01.039
- Синтез, строение и фотохимические свойства комплексов Ar3Sb[OC(O)C6HF4-2,3,4,5]2, Ar3Sb[OC(O)CF2Br]2, Ar3Sb[OC(O)CF2CF2CF3]2 (Ar = C6H3OMe-2-Br-5) / ЕВ. Артемьева, О.К. Шарутина, В.В. Шарутин, А.В. Буланова // Журн. неорг. химии. 2020. Т. 65, № 1. С. 25-33. DOI: 10.31857/S0044457X20010031
- Synthesis and structure of a new tetranuclear macrocyclic antimony(v) complex / V.V. Sharutin, O.K. Sharutina, Yu.O. Gubanova et al. // Mendeleev Commun. 2020. Vol. 30. P. 97-99. DOI: 10.1016/j.mencom.2020.01.032
- Synthesis of heteroleptic pentavalent antimonials bearing heterocyclic cinnamate moieties and their biological studies / S. Sarwar, T. Iftikhar, M.K. Rauf et al. // Inorg. Chim. Acta. 2018. V. 476. P. 12-19. DOI: 10.1016/j.ica.2018.02.005
- Investigations on the reactivity of arylantimony halides with N,O-donor ligands / P. Kishore, J. Ali, G. Narasimhulu, V. Baskar // J. Chem. Sci. 2018. Vol. 130, no. 7. P. 100. DOI: 10.1007/s12039-018-1495-3
- Yin H., Quan L., Li L. Synthesis, spectroscopic and structural aspects of triphenylantimony(V) complex with internally functionalized acetylferroceneoxime: crystal and molecular structures of [C5H5FeC5H4C(CH3)=NO]2SbPh3 and C5H5FeC5H4C(CH3)=NOH // Inorg. Chem. Commun. 2008. Vol. 11. P. 1121-1124. DOI: 10.1016/j.inoche.2008.06.017
- Шарутин В.В., Шарутина О.К., Котляров А.Р. Синтез и строение фенилпропионатов тетра- и трифенилсурьмы // Журн. неорган. химии. 2015. Т. 60, № 4. С. 525-528. DOI: 10.7868/S0044457X15040236
- Шарутин В.В., Шарутина О.К. ^тез и строение дикарбоксилатов трис(4-фторфенилсурьмы): (4-FC6H4bSb[OC(O)Rb, R = CH2I, C6F5 // Изв. АН. Сер. хим. 2017. № 4. С.707-710.
- The peculiarities of tri(o-Tolyl)antimony and tri(rn-tolyl)antimony reactions with 2-hydroxybenzaldoxime. The molecular structures of tri(o-tolyl)antimony 6/5(2-hydroxybenzaldoximate) and 675(^3-2-hydroxybenzaldoximato-O,O',N)-(^2-oxo)-675[di(ra-tolyl)antimony] / V.V. Sharutin, O.K. Sharutina, E.V. Artem'eva, M.S. Makerova // Bulletin of the South Ural State University. Ser. Chemistry. 2014. Vol. 6, no. 2. P. 5-14. DOI: 10.14529/chem220213
- Синтез и строение диоксиматов трифенилсурьмы Ph3Sb(ON=CHR)2 (R = QH4NO2-2, C6H4NO2-3, C6H4Br-2, C6H4Br-3, C4H2ONO2-5) / В.В. Шарутин, ОК. Шарутина, ДМ. Габитова, С.Я. Шайхвалеева // Журн. неорган. химии. 2017. Т. 62, № 1. С. 61-68. DOI: 10.7868/S0044457X17010172
- Синтез и строение моно-, би- и триядерных органилсульфонатных производных триарилсурьмы / В.В. Шарутин, О.К. Шарутина, В.С. Сенчурин и др. // Журн. неорг. химии. 2018. Т. 63, № 7. С. 823-830. DOI: 10.1134/S0044457X18070188
- Sharutin V.V., Sharutina O.K., Senchutin V.S. Synthesis and structure of tri(meta-tolyl)antimony ¿«(benzenesulfonate) // Bulletin of the South Ural State University. Ser. Chemistry. 2015. Vol. 7, no. 4. P. 93-97. DOI: 10.14529/chem150412
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data collection and processing software for the SMART system. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An integrated system for solving, refining and displaying crystal structures from diffraction data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: a complete structure solution, refinement and analysis program / O.V. Dolomanov, L.J. Bourhis, R.J. Gildea, J.A.K. Howard, H. Puschmann // J. Appl. Cryst. 2009. Vol. 42. P. 339-341. DOI: 10.1107/S0021889808042726
- Тарасевич Б.Н. ИК-спектры основных классов органических соединений. М.: МГУ, 2012. 54 с.
- Инфракрасная спектроскопия органических и природных соединений: учебное пособие / А.В. Васильев, Е В. Гриненко, А.О. Щукин, Т.Г. Федулина. СПб.: СПбГЛТА, 2007. 54 с.
- Spectral database for organic compounds, SDBS. Release 2021. National institute of advanced industrial science and technology. [Электронный ресурс]. URL: https://sdbs.db.aist.go.jp (дата обращения: 10.09.2022).
- Синтез и строение 1-адамантанкарбоксилата тетрафенилсурьмы и бис(1- адамантанкар-боксилата) трифенилсурьмы / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина и др. // Журн. общ. химии. 2009. Т. 79, № 10. С. 1636-1643.
- Cambridge Crystallografic Datebase. Release 2020. Cambridge. deposit@ccdc.cam.ac.uk; http: //www .ccdc.cam.ac.uk
- Covalent radii revisited / B. Cordero, V. Gómez, A.E. Platero-Prats, M. Reves, J. Echeverría, E. Cremades, F. Barragan, S. Alvarez // Dalton Trans. 2008. Iss. 21. P. 2832-2838. DOI: 10.1039/B801115J
- 2-Метокси-5-бромфенильные соединения сурьмы. ^нтез и строение / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина, О.В. Чагарова // Журн. общ. химии. 2011. Т. 81, № 10. С. 16491652.


