Сложности комплексного лечения пациента с распространённым деструктивным туберкулёзом лёгких на фоне выраженной буллёзной дистрофии лёгких после экзогенного воздействия мелкодисперсных частиц угольной пыли в анамнезе
Автор: Тарасов Р.В., Лепеха Л.Н., Садовникова С.С., Красникова Е.В., Баркова Д.С., Чесалина Я.О., Багиров М.А.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клинический случай
Статья в выпуске: 5 т.13, 2023 года.
Бесплатный доступ
Приводится наблюдение из практики - этапное хирургическое лечение пациента с распространённым деструктивным туберкулёзом лёгких с широкой лекарственной устойчивостью микобактерий туберкулёза на фоне выраженной буллёзной дистрофии лёгких после длительного экзогенного воздействия мелкодисперсных частиц угольной пыли в анамнезе. Пациент М., 42 лет, курильщик, с 20 лет работал грузчиком на железнодорожной станции, разгружал вагоны с мешками угля в условиях высоких температур, не используя средства индивидуальной защиты. Туберкулёзом лёгких болел 12 лет назад, изначальная форма: инфильтративный туберкулёз верхней доли правого лёгкого в фазе распада и обсеменения. Пролечен с положительной динамикой, был снят с учета 10 лет назад, настоящие изменения выявлены при плановом обследовании при обращении по поводу позвоночной грыжи. По данным компьютерной томографии органов грудной клетки при поступлении отмечена картина фиброзно-кавернозного туберкулёза правого лёгкого с системой полиморфных каверн с множественными очагами отсева в левое лёгкое на фоне выраженной эмфиземы обоих лёгких. Поступил в клинику с жалобами на одышку в покое (mMRC 3). Пациенту подобрана терапия на основании данных чувствительности и индивидуальной непереносимости. Успешно выполнена установка эндобронхиального клапана в устье верхнедолевого бронха справа, затем в устье бронха В6 - блокатор выкашлян. На фоне лечения сформировались туберкулёмы в левом лёгком. Выполнена резекция S1-2 левого лёгкого. Пациент перенёс SARS CoV-2, после чего случился спонтанный пневмоторакс слева, в связи с чем плевральная полость дренирована. На фоне отсутствия динамики через месяц после дренирования пациент взят на ревизию левой плевральной полости с ушиванием дефектов, частичной плеврэктомией и декортикацией левого лёгкого. Через 3 месяца пациенту произведено удаление бронхлоблокатора из устья верхнедолевого бронха справа и проведена комбинированная резекция правого лёгкого (верхняя лобэктомия с S6), после чего, с целью уменьшения правого гемиторакса и уменьшения перерастяжения правого лёгкого, произведена торакопластика с резекцией I-IV рёбер справа. При гистологическом исследовании подтверждён туберкулёз лёгких на фоне экзогенного воздействия мелкодисперсных частиц угольной пыли (по типу гиперчувствительного пневмонита хронического течения). В результате лечения у пациента уменьшились проявления одышки (mMRC 1), пациент стойко абацилирован и вернулся к нормальному образу жизни.
Фиброзно-кавернозный туберкулёз, гиперчуствительный пневмонит, этапное хирургическое лечение, резекция лёгкого, клапанная бронхоблокация
Короткий адрес: https://sciup.org/143181078
IDR: 143181078 | УДК: 616.24-002.5-089+616.24-007.63:616.235-007.17 | DOI: 10.20340/vmi-rvz.2023.5.CASE.5
The complexities of complex treatment of a patient with widespread destructive pulmonary tuberculosis against the background of severe pulmonary bullous dystrophy after exogenous exposure to fine particles of coal dust in the anamnesis
An observation from practice is given - a staged surgical treatment of a patient with widespread destructive pulmonary tuberculosis with preXDR MBT against the background of severe bullous lung dystrophy after prolonged exogenous exposure to fine particles of coal dust in the anamnesis. Patient M., 42 years old, smoker, has been working as a loader at a railway station since the age of 20, unloading wagons with bags of coal at high temperatures without using personal protective equipment. He was ill with pulmonary tuberculosis 12 years ago, the original form: infiltrative tuberculosis of the upper lobe of the right lung in the phase of decay and insemination. He was treated with positive dynamics, was removed from the register 10 years ago, the real changes were revealed during a routine examination when applying for a vertebral hernia. According to computed tomography of the chest organs, a picture of fibrous-cavernous tuberculosis of the right lung with a system of polymorphic caverns with multiple foci of dropout in the left lung against the background of pronounced emphysema of both lungs was noted upon admission. He was admitted to the clinic with complaints of shortness of breath at rest (mMRC 3). The patient was selected therapy based on sensitivity data and individual intolerance. The patient underwent EC installation at the mouth of the upper lobe bronchus on the right, successfully, then at the mouth of the bronchus B6, the blocker was coughed up. Against the background of treatment, tuberculomas formed in the left lung. S1-2 resection of the left lung was performed. The patient suffered SARS CoV-2. After that, spontaneous pneumothorax occurred on the left, and therefore the pleural cavity was drained. Against the background of the lack of dynamics, a month after drainage, the patient was taken for revision of the left pleural cavity with suturing of defects, partial pleurectomy and decortication of the left lung. After 3 months, the patient had a bronchoblocker removed from the mouth of the ULB on the right and a combined resection of the right lung (upper lobectomy with S6) was performed, after which, in order to reduce the right hemithorax and reduce the overstretch of the right lung, thoracoplasty was performed with resection of the I-IV ribs on the right. Histological examination confirmed pulmonary tuberculosis against the background of exogenous exposure to fine particles of coal dust (by the type of hypersensitive pneumonitis of chronic course). As a result of treatment, the patient's symptoms of shortness of breath (mMRC 1) decreased, the patient was steadfastly abaculated and returned to a normal lifestyle.
Текст научной статьи Сложности комплексного лечения пациента с распространённым деструктивным туберкулёзом лёгких на фоне выраженной буллёзной дистрофии лёгких после экзогенного воздействия мелкодисперсных частиц угольной пыли в анамнезе
ОПИСАНИЕ СЛУЧАЯ
Наиболее значимой задачей фтизиатрии является ликвидация бациллярного ядра, особенно при лекарственной устойчивости микобактерии туберкулёза (МБТ) [1–3]. Роль фтизиохирургии в этом случае – удаление необратимых деструктивных изменений лёгочной ткани [4]. Деструктивные, в том числе двусторонние, формы туберкулёза и множественная лекарственная устойчивость возбудителя (МЛУ МБТ) являются основными показаниями к применению хирургических методов лечения [5–10]. Также в литературе с 2000 года описан метод лечения заболеваний лёгких и их осложнений путём применения эндобронхиального обратного клапана (ЭК), установка которого в дренирующий бронх создаёт лечебную гиповентиляцию в поражённом участке лёгкого с сохранением дренажной функции блокированного бронха и соответствующей лёгочной зоны [11, 12]. Одним из показаний для использования данного метода служит фиброзно-кавернозный туберкулёз. Установка ЭК может быть одним из этапов комплексного хирургического лечения пациентов с распространённым деструктивным туберкулёзом лёгких.
Выбор тактики комплексного хирургического лечения, определение объёма и последовательности хирургических этапов является одним из главных факторов его эффективности [4]. В современной торакальной хирургии широкое распространение получили видеоторакоскопи-ческие (ВТС) операции. Однако данный метод сопряжён со значительными техническими трудностями в случае выраженных плевральных сращений и фиброзной трансформации элементов корня лёгкого [13, 14]. По этой причине во фтизиохирургии получили наибольшее распространение виоассистированные операции (ВАТС), они малотравматичны и технически выполнимы при наличии выраженного спаечного процесса в плевральной полости [14, 15].
Особую сложность представляют резекции лёгких у пациентов с эмфизематозными изменениями лёгочной ткани. По данным литературы, течение любой формы эмфиземы лёгких может осложнить спонтанный пневмоторакс [16–18]. В таких случаях в качестве противорецидивного лечения пневмоторакса применяется тотальная плеврэктомия [19].
В современной фтизиохирургии очень важно определить этапность и объём предполагаемой помощи, особенно у пациентов с распространённым деструктивным процессом в сочетании с буллезной дистрофией лёгких. Индивидуальный подход к лечению такого пациента показан в данном клиническом наблюдении.
Клинический пример
Пациент М., 42 лет, с ВИЧ-негативным статусом, курильщик, с 20 лет работал грузчиком на железнодорожной станции, разгружал вагоны с мешками угля в условиях высоких температур, не используя средства индивидуальной защиты. Туберкулёзом лёгких болел 12 лет назад, изначальная форма: инфильтративный туберкулёз верхней доли правого лёгкого в фазе распада и обсеменения. Пролечен с положительной динамикой, был снят с учёта 10 лет назад, настоящие изменения выявлены во время подготовки к хирургическому лечению по поводу позвоночной грыжи. Взят на диспансерный учёт с диагнозом: инфильтративный туберкулёз верхней доли правого лёгкого в фазе распада и обсеменения. МБТ (+) МЛУ МБТ. Получал лечение по I РХТ, однако по результатам люминисцентной микроскопии сохранялось бактериовыделение в объёме 3+, а по данным рентгенологических методов обследования сохранялись полости деструкции в верхних отделах правого лёгкого с частичным рассасыванием инфильтрации.
Пациент самостоятельно обратился для дообследования и лечения.
При поступлении (21.06.2022) аускультативно дыхание выслушивается во всех отделах, слева – везикулярное, справа – по передней поверхности ослаблено. Частота дыхательных движений (ЧДД) – 20/мин. Частота сердечных сокращений (ЧСС) – 90/мин.
На рисунке 1 представлено рентгенологическое исследование при поступлении (21.06.2022).
На рентгенографии (РГ) и компютерной томографии (КТ) органов грудной клетки (ОГК) при поступлении (21.06.2022): система фиброзных толстостенных каверн (суммарно 9 x 4 см) на фоне полиморфных очагов, лимфангита в верхней доле правого лёгкого. Полость деструкции в S6 с перикавитарным инфильтратом (8 x 4 см) с множеством очагов средней плотности с нечёткими контрами на фоне лимфангита в нижней части правого лёгкого. Полиморфные фокусные изменения в верхней доле с очагами отсева в верхней и средней части на фоне выраженной буллезной трансформации левого лёгкого. Корень правого лёгкого своей верхней частью вовлечен в инфильтрацию. Левый корень структурен, не расширен. Сросшиеся переломы задних частей 8 и 9 ребер. Заключение: фиброзно-кавернозный туберкулёз правого лёгкого в фазе инфильтрации и двустороннего обсеменения. Эмфизема лёгких (рис. 1).
По данным спирометрии на момент поступления (24.06.2022): жизненная емкость лёгких (ЖЕЛ) – 103,0 % от д.в., объем форсированного выдоха (ОФВ 1 ) – 92,2 % от д.в., ОФВ1/ЖЕЛ – 91,5 % от д.в. – вентиляционная способность лёгких в норме.
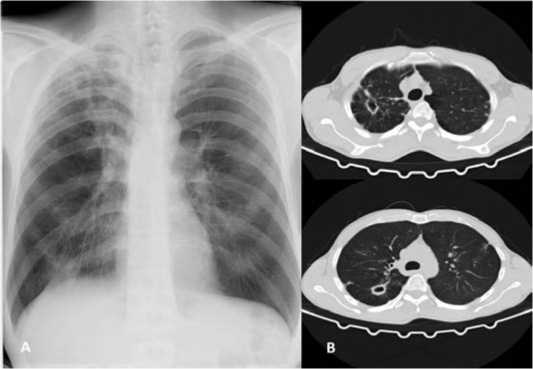
Рисунок 1. Рентгенография (А) и компьютерная томография (В) при поступлении. Множественные полостные образования верхней доли и S6 правого лёгкого. Крупные очаги в S1-2 левого лёгкого
Figure 1. Radiography (A) and computed tomography (B) at admission. Multiple cavities of the upper lobe and S6 of the right lung. Large foci in S1-2 of the left lung
Исследование газов крови при поступлении (24.06.2022): pO 2 – 73 мм рт. ст., pCО 2 – 34,3 мм рт. ст. Заключение: умеренная гипоксемия, незначительная гиперкапния.
В мокроте методом люминесцентной микроскопии (22.06.2023) кислотоустойчивые микобактерии обнаружены (КУМ+++ в 100 п/зр), методом полимеразной цепной реакции (ПЦР) – ДНК микобактерии туберкулёза обнаружены. Методом СИНТОЛ установлена устойчивость к изониазиду, рифампицину, фторхинолонам.
По результатам проведённого обследования был установлен диагноз: фиброзно-кавернозный туберкулёз правого лёгкого в фазе двустороннего обсеменения. МБТ (+) МЛУ МБТ (SREZPasEto). Также, с учётом полученных данных лекарственной устойчивости МБТ методом СИН-ТОЛ, была развёрнута противотуберкулёзная химиотерапия по индивидуальному режиму в соответствии с массой тела: левофлоксацин, пиразинамид, циклосерин, капрео-мицин.
По результатам BACTEC мокроты была выявлена устойчивость к Cs, PAS, H, R, E, Et, Am, Cap, Lfx, Mfx. Сохранена чувствительность к Lzd, Bq. Противотуберкулёзная терапия была скорректирована: моксифлоксацин, пиразинамид, циклосерин, капреомицин, линезолид, бе-даквилин, имипенем, амоксиклав.
Пациент обсуждён на хирургическом консилиуме: учитывая распространённость процесса, решено провести этапное комплексное хирургическое лечение. На начальном этапе, в связи с сохраняющимися перикавитарными инфильтративными изменениями, – эндоскопическая попытка закрытия полостей деструкции – выполнение последовательной эндоскопической клапанной бронхоблокации с установкой эндоклапанов в бронхи правого лёгкого: 1 этап – в устье правого верхнедолевого бронха; 2 этап – в устье В6 справа. Дальнейшая тактика – с учётом клинико-рентгенологической динамики процесса – после контроля КТ картины через 2 месяца после последней бронхоблокации.
На первом этапе была выполнена (10.08.2022) эндоскопическая клапанная бронхоблокация (ЭКББ) с установкой ЭК в устье правого верхнедолевого бронха (ПВДБ). При выполнении фибробронхоскопии (ФБС) данных за активное туберкулёзное воспаление бронхов не выявлено, однако отмечено, что каверна в S6 дренируется бронхами 2 и 6 сегментов. Следующим этапом (24.08.2022) выполнена установка ЭКББ в устье правого бронха В6. Процедуру перенёс удовлетворительно.
Через месяц (15.09.2022) после бронхоблокаций выполнена контрольная компьютерная томография (рис. 2).
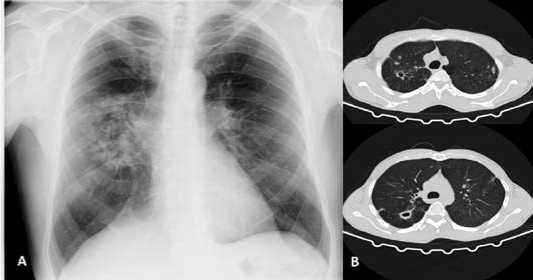
Рисунок 2. Рентгенография (А) и компьютерная томография (В) через 3 месяца после госпитализации, через 1 месяц после брон-хоблокаци ПВДБ и В6 справа (15.09.2022). Множественные полостные образования верхней доли и S6 правого лёгкого. Крупные очаги в S1-2 левого лёгкого
Figure 2. Radiography (A) and computed tomography (B) 3 months after hospitalization, 1 month after bronchoblocation of ULB and B6 on the right (15.09.2022). Multiple cavities of the upper lobe and S6 of the right lung. Large foci in S1-2 of the left lung
На КТ ОГК после бронхоблокации (15.09.2022): отмечается положительная рентгенологическая динамика в виде закрытия каверны в парамедиастинальном отделе верхушки правого лёгкого с формированием двух тубер-кулём (с остаточными мелкими полостями распада); в S1-2 справа – уменьшение размеров, уплощение, частичное заполнение полости каверны мягкотканным компонентом (динамика размера с 2,8 х 4,1 х 4,2 см до 1,7 х 3,2 х 2,7 см); аналогичные изменения каверны в S6, сопровождающиеся уменьшением общих размеров с 4,0 х 3,3 х 4,2 см до 2,3 х 2,0 х 2,9 см с утолщением стенок и уменьшением окна каверны. Рассасывание инфильтрации и большей части очагов бронхо- и лимфогенной диссеми-нации в обоих лёгких. Единичные туберкулёмы в верхней доле левого лёгкого. Эндоклапан в устье правого верхнедолевого бронха. Рубцовый стеноз В6 справа II ст. ЭК в устье В6 не визуализируется.
Учитывая КТ картину, а также опрос пациента – отмечает, что проглотил какой-то «объект» после утреннего кашля – нельзя исключить отсутствие эндоклапана в В6 и его миграцию из трахеобронхиального дерева. При контрольной бронхоскопии от 07.10.2022: выявлено, что в устье ПВДБ сохраняется ЭК. При осмотре устья В6 правого лёгкого блокатор не выявлен.
Учитывая положительную рентгенологическую динамику в виде рассасывания очагов и формирования тубер-кулём в левом лёгком, принято решение на третьем этапе комплексного лечения выполнить резекцию верхней доли левого лёгкого (в условиях сохранения ЭК в ПВДБ).
Пациенту (10.10.2022) была выполнена ВАТС атипичная резекция S1-S2 левого лёгкого. Послеоперационный период протекал без осложнений, дренажная система удалена на 8-е сутки, швы сняты на 14-е сутки.
Микробиологически методом ПЦР в операционном материале обнаружены ДНК МБТ, методом люминисцент-ной микроскопии обнаружены КУМ 9 в 100 п/зр. Методом СИНТОЛ установлена устойчивость к HRFq.
Гистологически в операционном материале: микрофрагменты лёгочной ткани с чередованием утолщённых за счёт фиброза или эмфизематозно растянутых межальвеолярных перегородок, особенно в субплевральной зоне. В просвете расширенных альвеол обнаружены скопления макрофагов-кониофагов (рис. 3). В составе фиброзной ткани определяются отложения мелкодисперсных частиц угля (рис. 4), единичные макрофагально-гистиоцитарные гранулемы с признаками диффузного фиброзирования (рис. 5), участки констриктивного бронхиолита (рис. 6).
На фоне изменённой лёгочной ткани определяются отдельные инкапсулированные очаги казеозного некроза, в том числе с эпителиоидно-клеточными гранулёмами в составе фиброзной капсулы и/или вокруг неё (рис. 7).
Заключение: морфологическая картина туберкулёмы лёгкого с признаками умеренной активности на фоне изменений лёгочной ткани вследствие экзогенного воздействия мелкодисперсных частиц угля. Признаки развития буллёзной эмфиземы.
Через 1,5 месяца после операции (07.11.2022) при плановом обследовании перед оперативным вмешательством на правом лёгком методом ПЦР был выявлен SARS-CoV-2, в связи с чем пациент переведён на лечение в профильное учреждение. Повторно госпитализировался в ФГБНУ «ЦНИИТ» спустя две недели для продолжения этапного хирургического лечения после получения отрицательного теста на SARS CoV-2.
Через два дня с момента госпитализации (24.11.2022) пациент проявил жалобы на тяжёлое дыхание и боли в левой половине грудной клетки. При осмотре: грудная клетка без особенностей, справа дыхание везикулярное, слева в верхнем отделе – ослабленное везикулярное, в нижних отделах дыхание не проводится.
Дообследован, на рентгенограмме (24.11.2022): левое лёгкое коллабировано более чем на 1/3 объёма за счёт базального пневмоторакса. Верхние и средние отделы лёгкого удерживаются от спадения плевральными сращениями (рис. 8).
В условия чистой перевязочной было выполнено дренирование плевральной полости в VI межреберье слева, по задней аксиллярной линии, получен воздух, дренаж подключён к системе по Бюллау, далее к аппарату активной аспирации.

Рисунок 3. Гистологическое исследование операционного материала: скопления макрофагов-кониофагов в просветах альвеол и альвеолярных ходов. Окраска гематоксилином и эозином, х 220
Figure 3. Histological examination of the surgical material: clusters of mac-rophages-coniophages in the lumen of the alveoli and alveolar passages. Staining with hematoxylin and eosin, х 220
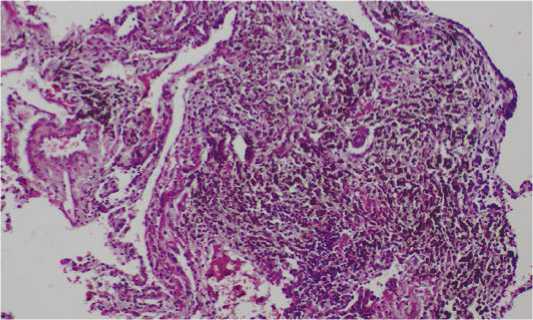
Рисунок 4. Отложения мелкодисперсных частиц угля в очаге фиброза. Окраска гематоксилином и эозином, х 240
Figure 4. Deposits of fine coal particles in foci of fibrosis. Coloring hematoxylin and eosin, х 240
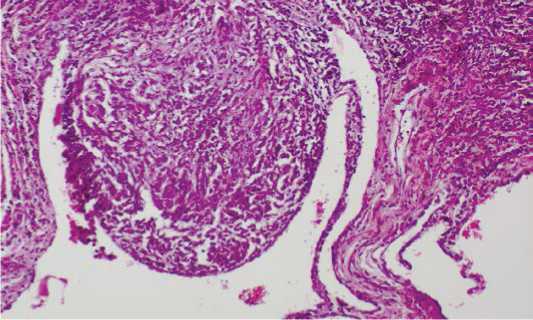
Рисунок 5. Макрофагально-гистиоцитарная гранулёма с признаками диффузного фиброзирования. Окраска гематоксилином и эозином, х 390 Figure 5. Macrophage-histiocytic granuloma with signs of diffuse fibrosis. Staining with hematoxylin and eosin, х 390
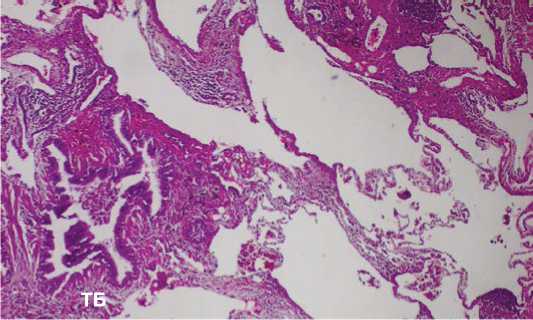
Рисунок 6. Терминальная бронхиола (ТБ) с признаками констриктивного бронхиолита и участок эмфизематозно-измененной лёгочной ткани. Окраска гематоксилином и эозином, х 180
Figure 6. Terminal bronchiola (TB) with signs of constrictive bronchiolitis and an area of emphysematous-altered lung tissue. Staining with hematoxylin and eosin, х 180
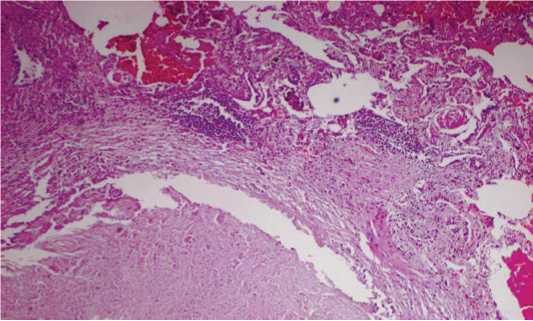
Рисунок 7. Фрагмент инкапсулированного очага казеозного некроза с единичными эпителиоидно-клеточными гранулёмами (ЭГ) в стенке и прилежащей лёгочной ткани. Окраска гематоксилином и эозином, х 180 Figure 7. Fragment of an encapsulated focus of caseous necrosis with single epithelioid cell granulomas (EG) in the wall and adjacent lung tissue. Staining with hematoxylin and eosin, х 180
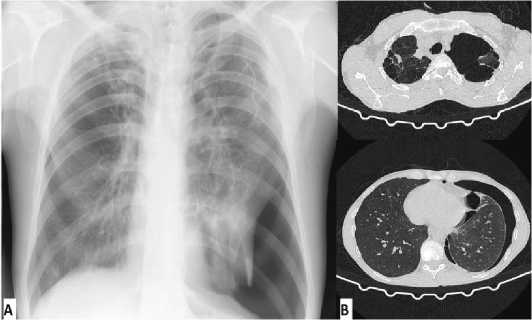
Рисунок 8. Рентгенография (А) до дренирования и компьютерная томография (В) после дренирования левой плевральной полости
Figure 8. X-ray (A) before draining and computed tomography (B) after draining the left pleural occupancy
В течение двух последующих недель отмечено отсутствие положительной динамики на перевязках в виде активного сброса воздуха по дренажу и невозможности достижения стойкого герметизма без аппарата активной аспирации. Также, ввиду малой информативности рентгенологических снимков и невозможности уточнить по ним локализацию возможного дефекта лёгочной ткани, пациенту выполнено КТ ОГК (рис. 8): левое лёгкое коллабировано на 1/2 объёма, от полного спадения удерживается плевральными спайками. Субтотальный многокамерный пневмоторакс слева без достоверно определямых бронхоплевральных свищей (решётчатое лёгкое?) в области верхушки лёгкого и паракардиально каудальнее корня лёгкого.
Учитывая многокамерную полость и отсутствие достоверных данных за наличие свищей и источника воздухоте-чения, было принято решение о проведении повторного оперативного вмешательства на ранее оперированном лёгком. Выполнена ВАТС слева ревизия плевральной полости, ушивание дефектов правого лёгкого в виде микросвищей в проекции нижней доли, обработка электрокаутера булл в проекции S3 лёгкого, частичная плеврэктомия с декортикацией лёгкого по поводу спонтанного пневмоторакса. В послеоперационном периоде, с целью компрессии левой плевральной полости, накладывался искусственный пнев-моперитонеум объёмом 1200 мл, с удовлетворительной пе-риносимостью. Послеоперационный период сопровождался длительным воздухотечением по дренажам. При достижении стойкого герметизма в течении 10 дней на ежедневных перевязках без подключения к аппарату активной аспирации, а также с положительной клинико-рентгенологической динамикой, на 25-е сутки после хирургического лечения дренажная система была удалена.
Через два месяца было выполнено КТ-исследование для оценки динамики картины изменений в правом лёгком (06.03.2023), а также в рамках подготовки к следующему этапу хирургического лечения.
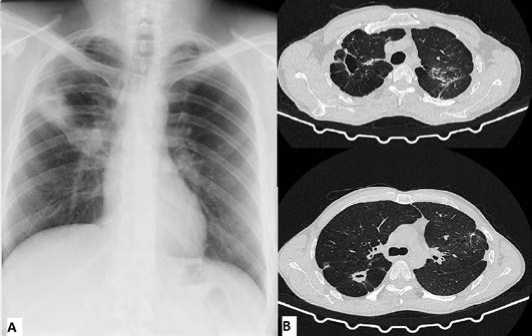
Рисунок 9. Рентгенография (А) и компьютерная томография (В) через 2 месяца после повторной операции на левом лёгком
Figure 9. X-ray (A) and computed tomography (B) 2 months after reoperation on the left lung
По данным КТ ОГК (06.03.2023): состояние после установки ЭК в ПВДБ, резекции части S1-2 левого лёгкого с частичной плеврэктомией и декортикацией левого лёгкого. Лобулярные ателектазы в S2, дисковидные в S1 и наружном субсегменте S3 левого лёгкого с увеличением объёма участков инфильтративно-ателектатического уплотнения в оставшейся части S2, рассасывания большей части осумкованного апико-паракостально-интерло-барного выпота, отсутствия газовых пузырей в левой плевральной полости (по сравнению с КТ от 16.11.22). В правом лёгком маловыраженное истончение стенок каверны в S1-2 с сохранением неправильной формы и увеличением размеров окна с 1,5 х 2,9 х 2,9 см до 1,6 x 3,3 x 3,i см. Уменьшение размеров каверны в S2-6 с уменьшением и фрагментацией полости распада, с более выраженными плевроперифокальными фиброзными тяжами. Рассасывание большей части разнокалиберных очагов в S3 и средней доле; рассасывание и фиброзная трансформация инфильтрата в ретростернальном отделе S5. В апикальном отделе справа сохраняются грубые фиброзно-казеозные конгломераты; крупные очаги в центральном отделе S2, наружном субплевральном отделе S3; одиночная мелкофокусная туберкулёма в наружнем отделе S1; очаги средних размеров в периферических отделах S6,8,9. В просвете ПГБ визуализируется лепестковая («хвостовая») часть ЭК, блокирующего устье ПВДБ (радиальная часть – «головка» в устье ПВДБ). Жидкость в правой плевральной полости не определяется; плеврофиброз на уровне S1,2. Заключение: КТ признаки фиброзно-кавернозного туберкулёза правого лёгкого в фазе рассасывания и неполного закрытия одной из двух каверн.
Учитывая положительную динамику в виде рассасывания инфильтрации, очагов отсева и частичного закрытия каверн при сохраняющемся основном поражении правого лёгкого, было принято решение о неоходимости оперативного вмешательства на правом лёгком – комбинированной резекции. Перед выполнением операции, учитывая длительность ЭКББ – 7 месяцев, сложность ведения пациента, снижение вентиляционной способности лёгких (ОФВ 1 – 61,3 % от должного, ЖЕЛ – 63,4 % от должного, Индекс Тиффно – 76 %) при исследовании газов крови от 27.02.2023 – умеренная гипоксемия (рО 2 – 75 %, повышение альвеолярно-капиллярного градиента), осложнения в виде левостороннего спонтанного пневмоторакса и перенесённой инфекции SARS CoV-2, снижение массы тела (ИМТ = 17,76), выявление нефункционирования ЭК (по данным бронхоскопии от октября 2022), принято решение о проведении удаления ЭК из устья ПВДБ с применением метода криоэкстрации в условиях поднаркозной бронхоскопии с интубацией тубусом ригидного бронхоскопа с высокочастотной вентиляцией и тотальной внутривенной анестезией.
21.03.2023 в условиях поднаркозной бронхоскопии с интубацией тубусом ригидного бронхоскопа (Фридель №12) с высокочастотной вентиляцией и тотальной внутривенной анестезией, оценено состояние ЭК в устье ПВДБ (рис. 10).
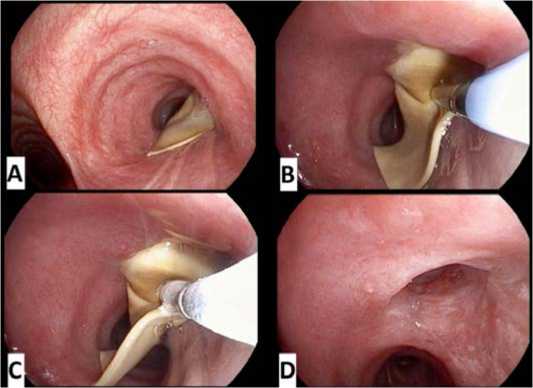
Рисунок 10. Этапы удаления ЭК из устья ПВДБ
Figure 10. Steps to remove EV from the orifice of right upper lobe bronchus
Справа в просвете главного бронха визуализируется лепестковая часть ЭК (рис. 6, А), радиальная часть установлена в устье ПВДБ, клапан не функционирует. Отмечено «обрастание» радиальной части грануляционной тканью и «залипание» хвостовой части ЭК.
Была выполнена криоэкстрации ЭК из устья ПВДБ. (рис. 6, В, С).
Криоэкстракция проводилась с помощью криозонда 1,9 мм криохирургической станции Erbecryo II с экспозицией 7 секунд. ЭК удалён полностью, осмотрен после извлечения, разрывов и фрагментирования не найдено.
После удаления ЭК (рис. 6, D): слизистая ПВДБ гипе-ремировна, отёчна, определяются единичные грануляции, из устья В2 дренируется вязкое отделяемое слизистогнойного характера. Устья бронхов 1–5 порядка с обеих сторон открыты, не деформированы, шпоры их острые. Слизистая видимых бронхов очагово гиперемирована, сосудистый рисунок усилен.
Длительность лечебной бронхоскопии от момента интубации трахеи тубусом жёсткого бронхоскопа до экстубации составила 5 минут.
Через 1 неделю (28.03.2023) пациенту выполнена ВАТС комбинированная резекция правого лёгкого (верхняя лобэктомия, резекция S6). Операция прошла без особенностей.
Микробиологически методом ПЦР в операционном материале обнаружены ДНК МБТ, методом люминисцент-ной микроскопии КУМ не обнаружены. Методом СИНТОЛ установлена устойчивость к HRFq.
Гистологически в операционном материале:
-
1) фрагменты лёгочной ткани с преобладанием интерстициального и очагового фиброза, диффузным отложением мелкодисперсных частиц угольной пыли. Выраженный периваскулярный и перибронхиолярный фиброз, бронхиолит с распространённой лимфоидной инфильтрацией стенки и перибронхиолярной ткани (рис. 11). Рядом
определяются макрофагально-гистиоцитарные гранулемы с нечёткими контурами, без некроза, содержащие многоядерные макрофаги и светлые игловидные включения (рис. 12). На фоне отмеченных изменений паренхимы определяются крупные хронические каверны, стенки которых состоят из наружного слоя грубоволокнистой соединительной ткани, слоя грануляционной ткани и неравномерно выраженного внутреннего некротического слоя (рис. 13). Имеются небольшие инкапсулированные очаги эозинофильного некроза неравномерной плотности без лейкоцитарной инфильтрации с признаками организации.
-
2) фрагменты лимфатических узлов со стёртым рисунком строения, единичными фолликулами, очаговым фиброзом капсулы и стромы, диффузным отложением мелкодисперсных частиц угля (рис. 14). Очагов некроза и элементов гранулематозной реакции в исследованном материале не обнаружено;
-
3) фрагменты местами утолщенны за счёт фиброза париетальной плевры с ограниченными участками неспецифической инфильтрации клеточными элементами воспаления (рис. 15).
Заключение: фиброзно-кавернозный туберкулёз правого лёгкого в фазе слабого прогрессирования на фоне экзогенного воздействия мелкодисперсных частиц угольной пыли (по типу гиперчувствительного пневмонита хронического течения). Лимфатические узлы с изменениями реактивного характера и отложениями частиц угля. Париетальная плевра с отдельными участками фиброза или воспалением неспецифического характера.
Учитывая объём комбинированной резекции, выраженные буллезные изменения лёгких, и наличие пневмоторакса в анамнезе, с целью коррекции объёма гемиторакса и предотвращения перерастяжения лёгочной ткани через 1 месяц (04.05.2023) пациенту выполнена экстраплевральная торакопластика с резекцией I-V рёбер справа. Операция прошла без особенностей, дренажи удалены на 5-е сутки, швы – на 21-е сутки.
Через 1 месяц выполнено контрольное КТ ОГК (рис. 16).
КТ ОГК через 1 месяц после экстраплевральной торакопластики справа (06.06.2023): состояние после пятирёберной тотракопластики справа. ОПП в апикальном отделе заполнена мягкими тканями и разнокалиберными газовыми пузырями. Небольшой объём верхне-наружного осумкованного паракостального выпота. Интраплеврально справа в базальных отделах воздух не определяется. Уменьшение объёма пневмоперитонеума. Органы средостения не смещены.
Пациент выписан из отделения для продолжения лечения в противотуберкулезный диспансер по месту жительства. Даны рекомендации по избежанию контакта с любой мелкодисперсной пылью при выборе работы.
Были оценены данные показателей ФВД и газов крови пациента М. на этапах лечения (табл. 1).
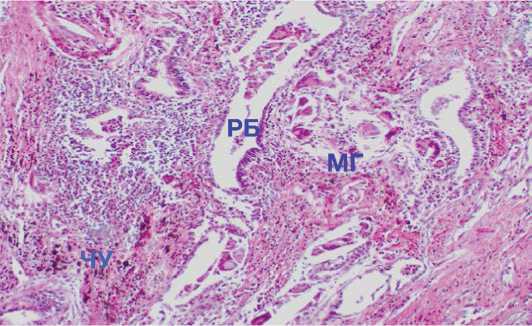
Рисунок 11. Респираторная бронхиола (РБ) с лимфоидной инфильтрацией, макрофагальные гранулёмы (МГ) и мелкодисперсные частицы угля (ЧУ) в перибронхиолярной зоне. Окраска гематоксилином И эозином, х 120
Figure 11. Respiratory bronchiola (RB) with lymphoid infiltration, macrophage granulomas (MG) and fine coal particles (CU) in the peribronchiolar zone. Staining with hematoxylin and eosin, х 120
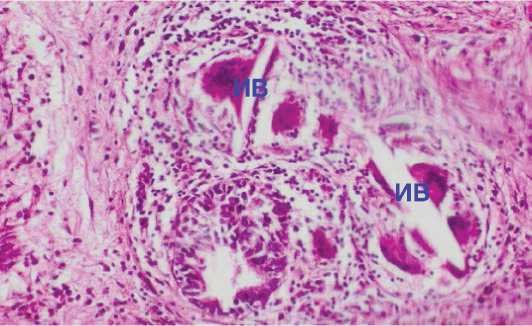
Рисунок 12. Макрофагальные гранулёмы, содержащие многоядерные макрофаги и светлые игловидные включения (ИВ). Окраска гематоксилином и эозином, х 280
Figure 12. Macrophage granulomas containing multinucleated macrophages and light needle-like inclusions (and B). Staining with hematoxylin and eosin, х 280
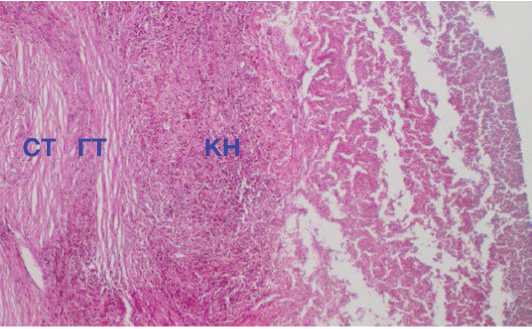
Рисунок 13. Туберкулёзная каверна с трёхслойным строением стенки: соединительнотканным (СТ), грануляционным (ГТ), казеознонекротическим (КН). Окраска гематоксилином и эозином, х 100
Figure 13. Tuberculous cavity with a three-layer wall structure: connective tissue (C), granulation (GT), caseous-necrotic (KN). Staining with hematoxylin and eosin, х 100
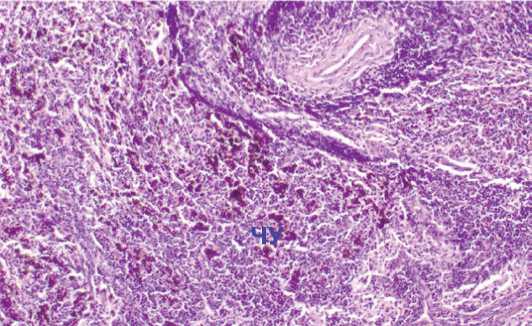
Рисунок 14. Скопления частиц угля (ЧУ) в мозговом веществе лим фатического узла. Окраска гематоксилином и эозином, х260
Figure 14. Accumulations of coal particles (CHU) in the medulla of the lymph node. Staining with hematoxylin and eosin, х 260
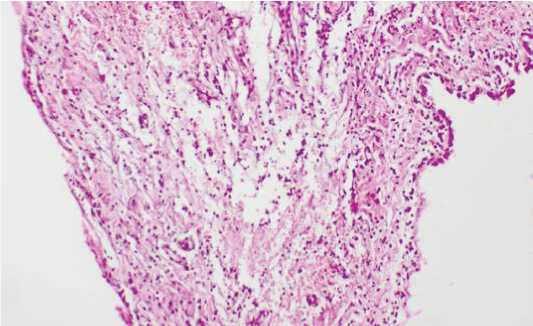
Рисунок 15. Фрагмент париетальной плевры с неспецифической инфильтрацией клеточными элементами воспаления. Окраска гематоксилином и эозином, х 160
Figure 15. A fragment of the parietal pleura with nonspecific infiltration by cellular elements of inflammation. Staining with hematoxylin and eosin, х 160
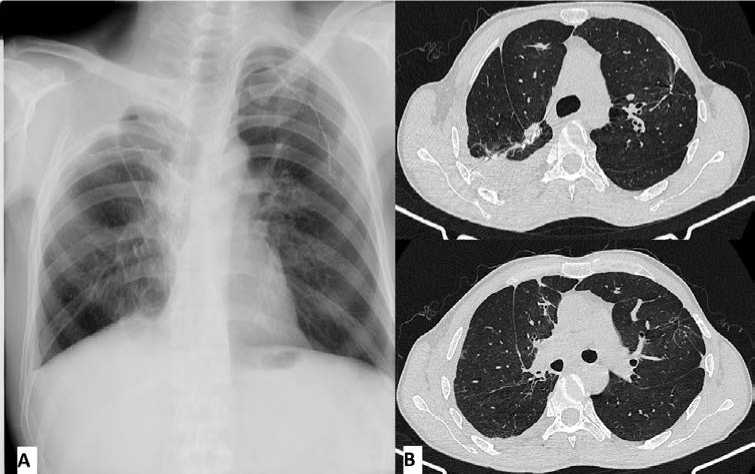
Рисунок 16. Рентгенография (А) и компьютерная томография (В) через 1 месяц после экстраплевральной торакопластики справа
Figure 16. X-ray (A) and computed tomography (B) 1 month after extrapleural thoracoplasty on the right
Таблица 1. Динамика показателей ФВД, газов крови и показателей ЭхоКГ пациента М.
Table 1. Dynamics of respiratory function, blood gases and echocardiography’s parameters of patient M.
|
Функциональные показатели |
Перед I этапом (ПВДБ и В6) |
Перед II этапом (резекция левого лёгкого) |
Перед III этапом (ререзекция левого лёгкого) |
Перед IV этапом (резекция правого лёгкого) |
Через 1 месяц после лечения (после торакопластики) |
|
ЖЕЛ л, (% долж.) |
5,26 (103,6) |
5,27 (103,7) |
4,43 (87,2) |
4,19 (82,5) |
2,63 (51,8) |
|
ФЖЕЛ л, (% долж.) |
5,26 (99,1) |
5,27 (99,3) |
4,43 (83,6) |
4,19 (79,0) |
2,63 (49,6) |
|
ОФВ 1 л/с (% долж.) |
3,85 (92,9) |
3,59 (86,6) |
2,92 (70,3) |
2,54 (61,3) |
2,14 (51,7) |
|
ОФВ 1 /ЖЕЛ % |
91,7 |
85,4 |
82,4 |
76 |
102 |
|
PaCO 2 , mmHg |
34,3 |
37,2 |
36,6 |
37,1 |
35,0 |
|
PaO 2 , mmHg |
73 |
70 |
80 |
75 |
76 |
Как видно из таблицы 1, по сравнению с доопераци-онными показателями отмечается снижение ЖЕЛ с 103,6 % до 51,8 %, что обусловлено уменьшением дыхательной поверхности за счёт резекции лёгких, однако стоит отметить сохранение показателей pO 2 на уровне умеренного снижение – 73 и 76 mmHg, что говорит о сохранении оксигенации лёгочной ткани на нормальных привычных для пациента значениях.
Обсуждение
На протяжении многих лет одной из основных задач хирургии туберкулёза является улучшение результов лечения пациентов, а его успех определяется грамотным предоперационным планированием и мастерством врача. Резекции лёгких являются основным методом хирургического лечения при туберкулёзе лёгких, а отказ от хирургической помощи, при наличии показаний, ведёт к ухудшению результатов лечения больных туберкулёзом лёгких и повышает частоту рецидивов и летальных исходов от туберкулёза [20]. При наличии деструктивных изменений в лёгких на фоне инфильтрации закрытие полостей распада возможно после установки ЭК в дренирующий бронх. Данный вид лечения может выполняться как самостя-тельно, так и для подготовки к операции. При установлен- ном ЭК возможно выполнение операции на противоположном лёгком, если позволяют функциональные возможности пациента, а объём предстоящего вмешательства не приведёт к значительному снижению дыхательной функции лёгких. Учитывая, что малые резекционные вмешательства переносятся пациентами легче и являются вы-сокоэффективнымы [21–24], на начальном этапе пациенту выполнена операция со стороны меньшего поражения в условиях установленного ЭК в противоположном лёгком. Возникновение спонтанного пневмоторакса оперированного лёгкого после перенесённого SARS CoV-2 поставило вопрос о выполнении повторного оперативного вмешательства – традиционная в этом случае плеврэктомия оказалась внеплановым этапом и была выполнена по срочным показаниям. После функциональной реабилитации пациент был подготовлен к основному этапу хирургического лечения – комбинированной резекции правого лёгкого. Перед выполнением операции ЭК был удален. Большой объём комбинированной резекции в условиях субтотального очагового обсеменения и буллёзных изменений лёгкого потребовал выполнения отсроченной экстраплевральной торакопластики в короткий срок после резекции (через 4 недели). Индивидуальный комплексный подход к лечению с учётом объёма и характера поражения лёгких и сопутствующей патологии позволяет добиться эффективного лечения у большинства пациентов, в том числе у наиболее тяжёлых – с распространёнными процессами, лекарственной устойчивостью возбулителя и выраженными буллёзными изменениями лёгких.
Выводы
Данный клинический пример демонстрируют эффективность комплексного подхода в лечении распространённого деструктивного туберкулёза лёгких с широкой лекарственной устойчивостью микобактерий туберкулёза на фоне эмфиземы лёгких. Особенный интерес вызывает впервые установленный гиперчувствительный пневмонит, который мог быть основной причиной лёгочных изменений у пациента на первых этапах болезни. Правильно подобранный план хирургического лечения (эндоксопическая брон-хоблокация и операции резекционного типа) в совокупности с адекватной противотуберкулезной терапией и искусственным пневмотораксом позволили достичь хороших результатов в лечении туберкулёза, несмотря на сопутствующую патологию.
Список литературы Сложности комплексного лечения пациента с распространённым деструктивным туберкулёзом лёгких на фоне выраженной буллёзной дистрофии лёгких после экзогенного воздействия мелкодисперсных частиц угольной пыли в анамнезе
- Поркулевич Н.И., Мордык А.В., Гурова Я.В. Анализ причин формирования фиброзно-кавернозного туберкулёза. Туберкулёз и болезни лёгких. 2015;5:154-155. [Porkulevich N.I., Mordyk A.V., Gurova Ya.V. Analysis of the causes of the formation of fibrous-cavernous tuberculosis. Tuberculosis and lung diseases. 2015;5:154-155. (In Russ)].
- Цыбикова Э.Б. Неудачи в лечении впервые выявленных больных деструктивным туберкулёзом лёгких. Туберкулёз и болезни лёгких. 2011;5:217-218. [Tsybikova E.B. Failures in the treatment of newly diagnosed patients with destructive pulmonary tuberculosis. Tuberculosis and lung diseases. 2011;5:217-218. (In Russ)].
- Попов А.В., Айдемиров А.Н., Одинец В.С. Причины формирования фиброзно-кавернозного туберкулёза лёгких в Ставропольском крае по материалам исследований с летальным исходом. Туберкулёз и болезни лёгких. 2011;5:119-120. [Popov A.V., Aidemirov A.N., Odinets V.S. The causes of the formation of fibrotic-cavernous pulmonary tuberculosis in the Stavropol Territory based on the materials of studies with a fatal outcome. Tuberculosis and lung diseases. 2011;5:119-120. (In Russ)].
- Клинические рекомендации по применению хирургических методов в лечении туберкулёза лёгких. Ассоциация торакальных хирургов России. СПб; 2014. [Clinical recommendations on the use of surgical methods in the treatment of pulmonary tuberculosis. Association of Thoracic Surgeons of Russia. St. Petersburg; 2014. (In Russ)].
- Рейхруд М.В., Краснов Д.В., Авдиенко К.А., Грищенко Н.Г., Скворцов Д.А., Кононенко В.Г. Отдаленные результаты резекционных и коллап-сохирургических вмешательств при туберкулёзе лёгких. Туберкулeз и болезни лeгких. 2018;96(12):34-40. [Reikhrud M.V., Krasnov D.V., Ovdienko K.A., Grishchenko N.G., Skvortsov D.A., Kononenko V.G. Long-term results of resection and collapsosurgical interventions in pulmonary tuberculosis. Tuberculosis and lung diseases. 2018;96(12):34-40. (In Russ)].
- Сабиров Ш.Ю., Рахманов Ш.А. Хирургическое лечение туберкулёза лёгких с множественной лекарственной устойчивостью возбудителя. Туберкулёз и болезни лёгких. 2015;6:128-129. [Sabirov Sh.Yu., Rakhmanov Sh.A. Surgical treatment of pulmonary tuberculosis with multidrug-resistant pathogen. Tuberculosis and lung diseases. 2015;6:128-129. (In Russ)].
- Скорняков С.Н., Мотус И.Я., Кильдюшева Е.И. и соавт. Хирургия деструктивного лекарственно-устойчивого туберкулёза лёгких. Туберкулёз и болезни лёгких. 2015;3:15-20. [Skornyakov S.N., Motus I.Ya., Kildyusheva E.I. et al. Surgery of destructive drug-resistant pulmonary tuberculosis. Tuberculosis and lung diseases. 2015;3:15-20. (In Russ)].
- Ворончихин Т.А., Аветисян А.О., Васильев И.В., Кудряшов Г.Г., Яблонский П.К. Результаты комплексного лечения ограниченного фиброзно-кавернозного туберкулёза лёгких. Медицинский Альянс. 2018;3:56-64. [Voronchikhina T.A., Avetisyan A.O., Vasiliev I.V., Kudryashov G.G., Ya-blonsky P.K. Results of complex treatment of limited fibrotic-cavernous pulmonary tuberculosis. Medical Alliance. 2018;3:56-64. (In Russ)].
- Гиллер Д.Б., Бижанов А.Б., Хасаншин Г.С. Пути повышения эффективности лечения впервые выявленных больных деструктивным туберкулёзом лёгких с бацилловыделением. Хирургия. Журнал им. Н.И. Пирогова. 2013;6:83-87. [Giller D.B., Bizhanov A.B., Khasanshin G.S. Ways to improve the effectiveness of treatment of newly diagnosed patients with destructive pulmonary tuberculosis with bacillus excretion. Surgery. N.I. Pirogov Magazine. 2013;6:83-87. (In Russ)].
- Малов А.А., Возякова Т.Р., Зайцева С.М. и соавт. Хирургические методы лечения больных деструктивным туберкулёзом органов дыхания. Туберкулёз и болезни лёгких. 2015;6:93. [Malov A.A., Vozyakova T.R., Zaitseva S.M. and coauthors. Surgical methods of treatment of patients with destructive tuberculosis of the respiratory system. Tuberculosis and lung diseases. 2015;6:93. (In Russ)].
- Левин А. В., Цеймах Е. А., Зимонин П. Е. и др. Результаты применения клапанной бронхоблокации в комплексном лечении больных с распространенным лекарственно- устойчивым туберкулёзом лёгких. Омский научный вестник. 2009;1(84):66-69. [Levin A.V., Tseymakh E. A., Zimonin P. E. and others. The results of the use of valvular bronchoblocation in the complex treatment of patients with widespread drug-resistant pulmonary tuberculosis. Omsk Scientific Bulletin. 2009;1(84):66-69. (In Russ)].
- Ловачева О.В. Елькин А.В., Зимонин П.Е., Краснов Д.В., Краснов В.А., Левин А.В. И др. Федеральные клинические рекомендации по использованию метода клапанной бронхоблокации в лечении туберкулёза лёгких и его осложнений. М.: НЬЮ-ТЕРРА. 2015. С. 24 http://roftb.ru/netcat_files/doks2015/rec7.pdf 10 [Lovacheva O.V. Elkin A.V., Zimonin P.E., Krasnov D.V., Krasnov V.A., Levin A.V., etc. Federal clinical guidelines on the use of the valvular bronchoblocation method in the treatment of pulmonary tuberculosis and its complications. Moscow: NEW TERRA. 2015. p. 24 http://roftb.ru/netcat_files/doks2015/rec7.pdf 10 (In Russ)].
- Рогожкин П.В., Колсанов А.В., Бородулина Е.А. Хирургическое лечение больных туберкулёзом лёгких в XXI веке. Хирургия. Журнал им. Н.И. Пирогова. 2020;6:104-108. https://doi.org/10.17116/hirurgia2020061104 [Rogozhkin P.V., Kolsanov A.V., Borodulina E.A. Surgical treatment of patients with pulmonary tuberculosis in the XXI century. Surgery. N.I. Pirogov Magazine. 2020;6:104-108. https://doi.org/10.17116/hirurgia2020061104 (In Russ)].
- Гиллер Д.Б., Садовникова С.С., Папков А.В., Гиллер Г.В., Глотов А.А. Эффективность выполнения видеоассистированных анатомических резекций лёгких. Российский медико-биологический вестник им. акад. И.П. Павлова. 2014;22(1):126-131. [Giller D.B., Sadovnikova S.S., Papkov A.V., Giller G.V., Glotov A.A. The effectiveness of performing video-assisted anatomical lung resections. The Russian Medico-biological Bulletin. academician I.P. Pavlova. 2014;22(1):126-131. (In Russ)].
- Мотус И.Я., Неретин А.В., Баженов А.В. Возможности мини-инвазивной хирургии в лечении туберкулёза лёгких. Фтизиатрия и пульмонология. 2011;2:34-35. [Гиллер Д.Б., Садовникова С.С., Папков А.В., Гиллер Г.В., Глотов А.А. Эффективность выполнения видеоассистированных анатомических резекций легких. Российский медико-биологический вестник. академик И.П. Павлова. 2014;22(1):126-131. (In Russ)].
- Вершинина М. В., Гринберг Л. М., Нечаева Г. И. и др. Спонтанный пневмоторакс и дисплазия соединительной ткани: фенотипические особенности пациентов. Пульмонология. 2011;6:43-47. [Vershinina M. V., Grinberg L. M., Nechaeva G. I. et al. Spontaneous pneumothorax and connective tissue dysplasia: phenotypic features of patients. Pulmonology. 2011;6:43-47. (In Russ)].
- Пичуров А.А., Оржешковский О.В., Петрунькин А.М. и др.Спонтанный пневмоторакс. Анализ 1489 случаев. Вестник хирургии им. И. И. Грекова. 2013;172(5):82-88. [Pichurov A.A., Orzheshkovsky O.V., Petrunkin A.M., etc.Spontaneous pneumothorax. Analysis of 1489 cases. Bulletin of Surgery named after I. I. Grekov. 2013;172(5):82-88. (In Russ)].
- Li X., Wang X., Zhang H. et al. Unilateral single - port thoracoscopic surgery for bilateral pneumothorax or pulmonary bullae. J. Cardiothorac. Surg. 2019;14:71-72.
- Горбунков С. Д., Черный С. М., Акопов А. Л. и др. Хирургическое лечение дыхательной недостаточности у пациентов молодого возраста с диффузной эмфиземой лёгких. Вестник хирургии им. И. И. Гоекова. 2012;171(6):27-31. [Gorbunkov S. D., Cherny S. M., Akopov A. L., etc. Surgical treatment of respiratory failure in young patients with diffuse pulmonary emphysema. Bulletin of Surgery named after I. I. Grekov. 2012;171(6):27-31. (In Russ)].
- Гарифуллин З.Р., Аминев Х.К. Эффективность хирургического лечения больных лекарственно-устойчивым туберкулёзом лёгких в зависимости от длительности заболевания. Туберкулёз и болезни лёгких. 2009;7:41 -46. [Garifullin Z.R., Aminev H.K. Effectiveness of surgical treatment of patients with drug-resistant pulmonary tuberculosis depending on the duration of the disease. Tuberculosis and lung diseases. 2009;7:41-46. (In Russ)].
- Мотус И.Я., Скорняков С.Н., Голубев Д.Н., Карсканова С.С., Мальцева А.С. Хирургическое лечение туберкулёза лёгких. Проблемы, результаты, перспективы. Вестник Уральской медицинской академической науки. 2009;3(26):103-106. [Motus I.Ya., Skornyakov S.N., Golubev D.N., Karskanova S.S., Maltseva A.S. Surgical treatment of pulmonary tuberculosis. Problems, results, prospects. Bulletin of the Ural Medical Academic Science. 2009;3(26):103-106. (In Russ)].
- Рогожкин П.В., Бородулина Е.А. Отдаленные результаты лечения больных туберкулёзом лёгких, перенесших радикальную резекцию лёгких. Туберкулёз и болезни лёгких. 2018;96(3): 24-28. [Rogozhkin P.V., Borodulina E.A. Long-term results of treatment of patients with pulmonary tuberculosis who underwent radical lung resection. Tuberculosis and lung diseases. 2018;96(3): 24-28. (In Russ)].
- Гарифуллин З.Р., Аминев З. К. Отдаленные результаты хирургического лечения больных лекарственно-устойчивым туберкулёзом лёгких. Казанский медицинский журнал. 2009;90(5): 695-699. [Garifullin Z.R., Aminev Z. K. Long-term results of surgical treatment of patients with drug-resistant pulmonary tuberculosis. Kazan Medical Journal. 2009;90(5): 695-699. (In Russ)].
- Елькин А.В., Басек Т.С., Калеченков М.К., Львов И.В. Отдаленные результаты хирургического лечения туберкулёза лёгких с широкой лекарственной устойчивостью возбудителя. Туберкулёз и болезни лёгких. 2015;7:39-40. [Yelkin A.V., Basek T.S., Kalechenkov M.K., Lvov I.V. Long-term results of surgical treatment of pulmonary tuberculosis with broad drug resistance of the pathogen. Tuberculosis and lung diseases. 2015;7:39-40. (In Russ)].


