Сложности лечения пациента с сочетанной патологией - туберкулёз лёгких и саркоидоз (клинический случай)
Автор: Тарасов Р.В., Садовникова С.С., Красникова Е.В., Лепеха Л.Н., Тихонская А.Н., Ерцева Е.В., Багиров М.А.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клинический случай
Статья в выпуске: 1 т.15, 2025 года.
Бесплатный доступ
Туберкулёз и саркоидоз относятся к гранулематозным заболеваниям и имеют схожие симптомы, что особенно при поражении лёгких затрудняет их дифференциальную диагностику. Приводится наблюдение из практики: этапное хирургическое лечение пациента с сочетанием саркоидоза и туберкулёза лёгких. Пациент М., 34 лет, контакт с больным туберкулёзом не установлен. На компьютерной томографии (КТ) органов грудной клетки (ОГК) в январе 2021 г. выявлены изменения в лёгких. Проба с аллергеном туберкулёзным рекомбинантным отрицательная, в анализе мокроты микобактерии туберкулёза (МБТ) не обнаружены. Выполнена видеоассистированная биопсия лёгкого (атипичная резекция S2 правого лёгкого) и лимфатического узла паратрахеальной группы. Морфологическая картина соответствовала саркоидозу в активной фазе процесса. Пульмонологом по месту жительства назначен метипред в дозе 12 мг. В ноябре 2021 года на фоне снижения дозировки метипреда отмечен сильный приступообразный кашель, в связи с чем пациент обследован в противотуберкулёзном диспансере: проба с АТР от 14.06.2022 г. - папула 12 мм, в анализе мокроты от 23.06.2022 г. обнаружена ДНК МБТ с сохранённой лекарственной чувствительностью ко всем противотуберкулёзным препаратам. При посеве на плотные питательные среды выявлен рост МБТ. По данным КТ ОГК от 18.08.2022 г. - консолидированное воспаление в верхней доле справа; интерстициальные изменения в лёгких, характерные для инфильтративного туберкулёза, увеличение внутригрудных лимфатических узлов (ВГЛУ). 20.10.2022 г. госпитализирован в ФГБНУ «ЦНИИТ» по поводу инфильтративного туберкулёза правого оперированного лёгкого. Назначено лечение по индивидуальному режиму химиотерапии препаратами 1 ряда. В течение 1 месяца получал 12 мг метилпреднизолона, далее доза была снижена до 8 мг. При контроле через 2 месяца отмечено прекращение бактериовыделения, однако констатирована отрицательная рентгенологическая динамика в виде появления свежих очаговых теней. Дозировка метилпреднизолона увеличена до 12 мг. При контроле через 4 месяца отмечалась положительная клинико-рентгенологическая динамика. С целью санации и сокращения времени медикаментозного лечения выполнена повторная комбинированная резекция правого лёгкого (верхняя лобэктомия с резекцией части S4) с частичной плеврэктомией. В операционном материале обнаружены ДНК МБТ, КУМ ++. Гистологически: картина туберкулёзного воспаления, фаза слабо выраженного прогрессирования. С целью уменьшения перерастяжения оставшихся отделов правого лёгкого и снижения риска прогрессирования процесса после резекции лёгкого большого объёма через 1 месяц выполнена экстраплевральная торакомиопластика с резекцией I-IV рёбер справа с удалением лимфатических узлов паратрахеальной группы. При гистологическом исследования лимфатических узлов: гранулематоз без некроза. Дозировка метилпреднизолона снижена до 8 мг через 1 месяц после операции. При контрольном КТ ОГК через 3 месяца вновь отрицательная рентгенологическая динамика несмотря на проводимую противотуберкулёзную терапию согласно данным чувствительности возбудителя. Изменения расценены как дестабилизация течения саркоидоза, что подтверждалось результатами гистологического исследования лимфатических узлов и отрицательными результатами микробиологических исследований операционного материала. Пациенту возобновлён приём метелипреднизолона в дозировке 12 мг, а также проведён курс экстракорпорального лечения для индукции ремиссии саркоидоза и потенциирования эффекта кортикостероидов. Через 6 месяцев отмечена положительная динамика в виде частичного рассасывания очаговых изменений. Пациент вернулся к привычному образу жизни.
Туберкулез легких [d014397], саркоидоз [d012507], саркоидоз легких [d012516], коморбидность [d000072566], хроническое заболевание [d002908], гранулема [d012626], ведение болезни [d004198], диагностические методы и процедуры [d055088], бронхоскопия [d002470], туберкулиновая проба [d014057], противотуберкулезные препараты [d017023], кортикостероиды [d000279], результат лечения [d052097], клинический случай [d002363], принятие решений [d003627], фактор некроза опухоли-альфа [d014456]
Короткий адрес: https://sciup.org/143184366
IDR: 143184366 | УДК: 616.24-002.5+616.24-002.582]-07-08-035.7 | DOI: 10.20340/vmi-rvz.2025.1.CASE.2
The challenges of managing a patient with concurrent pulmonary tuberculosis and sarcoidosis (a case report)
Tuberculosis and sarcoidosis are granulomatous diseases and can cause similar symptoms. In addition, both diseases can affect the lungs, what makes difficult to diagnose them differentially. An observation from practice is given: staged surgery of a patient with a combination of sarcoidosis and pulmonary tuberculosis. Patient M., 34 years old, contact with a tuberculosis patient has not been established. A CT scan of the chest organs in January 2021 revealed changes in the lungs. Upon further examination: the sample with the tuberculosis recombinant allergen was negative, Mycobacterium tuberculosis (MBT) was not detected in the sputum analysis. A video-assisted lung biopsy (atypical S2 right lung resection with paratracheal lymphadenectomy) was performed. The morphological picture corresponded to sarcoidosis in the active phase of the process. The primary care pulmonologist prescribed Metipred at a dose of 12 mg. In November 2021, after of decrease in the dosage of Metipred, the patient noted a severe paroxysmal cough. The patient was examined again :tuberculin skin-test dated 06/14/2022 - papule of 12 mm, sputum analysis from 06/23/2022 revealed MBT DNA with preserved drug sensitivity to all anti-tuberculosis drugs. When sowing on dense nutrient media, growth of MBT was detected. According to the CT scan of the chest dated 08/18/2022, consolidated inflammation in the upper lobe on the right lung, interstitial changes and lymphadenopathy of the intrathoracic lymph nodes (IGLU) were detected. On 10/20/2022 he entered CTRI Federal State Budgetary Budgetary Educational Institution regarding infiltrative tuberculosis of the right operated lung. An individual chemotherapy regimen had been prescribed. He received methylprednisolone 12 mg for 1 month, then the dose was reduced to 8 mg. During the control after 2 months, bacterial excretion stopped, but there was a negative X-ray dynamic as appearance of fresh focal shadows. The dosage of Methylprednisolone has been increased to 12 mg. The control showed positive clinical and radiological dynamics after 4 months. In order of local sanitation and reducion the time of drug treatment resection of the right lung (upper lobectomy and part of the S4 with partial pleurectomy) was performed. DNA of MBT and acid-fast mycobacteria ++ were found in the resection material. Histologically, the phase of mild progression of the tuberculosis process was identificated. In order to reduce overstretching of the remaining parts of the right lung and reduce the risk of progression of tuberculosis, extrapleural thoracomyoplasty with resection of the I-IV ribs and removal of a group of paratracheal lymph nodes was performed after 1 month. Histological examination of the lymph nodes revealed granulomatosis without necrosis. The dosage of methylprednisolone was reduced to 8 mg 1 month after surgery. With a control CT scan of chest after 3 months, there was a negative X-ray dynamic, despite the ongoing TB therapy according to sensitivity MBT data. The changes were regarded as destabilization of the course of sarcoidosis, which was confirmed by the results of histological examination of lymph nodes and negative microbiological studies on MBT of them. The patient resumed taking meteliprednisolone at a dosage of 12 mg, and underwent an extracorporeal methods course to induce remission of sarcoidosis and potentiate the effect of corticosteroids. After 6 months, there was a positive trend in the form of partial resorption of focal changes. The patient returned to his usual lifestyle.
Текст научной статьи Сложности лечения пациента с сочетанной патологией - туберкулёз лёгких и саркоидоз (клинический случай)
Сочетание туберкулёза и саркоидоза лёгких является сложной и малоизученной проблемой в современной фтизиатрии и пульмонологии [1, 2]. Хотя частота встречаемости каждого из этих заболеваний по отдельности достаточно высока, случаи их одновременного проявления в литературе описываются не часто [3, 4]. Согласно литературным данным, сочетание туберкулёза лёгких (преимущественно его ограниченных форм) и саркоидоза встречается довольно редко – всего 0,63%. В описанных случаях авторы придерживаются мнения о присоединении туберкулёзной инфекции к саркоидозу органов дыхания у пациентов на фоне длительной гормональной терапии [5].
Для дифференциальной диагностики туберкулёза и саркоидоза необходимо учитывать: клиническую картину, результаты лабораторных исследований, данные рентгенографии и других методов исследования. Однако даже при наличии всех этих данных, иногда бывает сложно установить точный диагноз. Это связано с тем, что оба заболевания могут вызывать схожие симптомы, такие как кашель, одышка, лихорадка и потеря веса. Кроме того, оба заболевания могут поражать лёгкие и другие органы, что затрудняет их дифференциальную диагностику [6–8]. Сложность диагностики и лечения сочетанной патологии может привести к увеличению сроков госпитализации и снижению качества жизни пациентов [5].
Представляем клинический случай, отражающий сложности в проведении адекватной терапии у пациента с сочетанием саркоидоза лёгких и внутригруд-ных лимфатических узлов (ВГЛУ) и бактериологически подтверждённого туберкулёза лёгких.
Клинический случай
Пациент М., 35 лет, офисный работник, без вредных привычек, контактов с больными туберкулёзом не имел. В декабре 2020 года перенёс новую коронавирусную инфекцию в лёгкой форме, лечился амбулаторно. При выполнении компьютерной томографии (КТ) органов грудной клетки в январе 2021 года были выявлены изменения в лёгких и внутригрудных лимфоузлах. Консультирован фтизиатром, выполнена проба с аллергеном туберкулёзным рекомбинантным (АТР) – отрицательная, в анализах мокроты кислотоустойчивые микобактерии (КУМ) и ДНК микобактерии туберкулёза (МБТ) не обнаружены, в посевах на жидкие и плотные питательные среды (ППС) роста МБТ не получено. Учитывая полученные данные, был установлен диагноз: «Диссеминация в лёгких и внутригрудная лимфаденопатия неясного генеза». С целью гистологической верификации выполнена видеоассистированная биопсия (атипичная резекция S2) правого лёгкого и удаление лимфатического узла паратрахеальной группы. По результатам исследования – картина гранулематозного воспаления лёгкого и лимфатического узла, наиболее соответствующая саркоидозу в активной фазе процесса. Направлен к пульмонологу, назначены системные глюкордикостероиды – с эффектом, но при снижении дозы появились жалобы на сухой кашель. Назначался курс антибиотиков широкого спектра действия с положительным эффектом. Через 1 месяц в связи с повторным эпизодом усиления кашля пациент самостоятельно обратился к фтизиатру. При обследовании: положительная реакция на пробу с АТР – папула 12 мм, в анализе мокроты обнаружена ДНК МБТ с сохранённой лекарственной чувствительностью МБТ ко всем противотуберкулёзным препаратам, при посеве на плотные питательные среды – рост МБТ. Пациент обратился в ФГБНУ «ЦНИИТ» и был госпитализирован в клинику для дообследования и лечения.
При поступлении пациент предъявлял жалобы на сухой кашель. При физикальном осмотре – общее состояние удовлетворительное. Кожные покровы и видимые слизистые физиологической окраски. Периферические лимфатические узлы не увеличены. Аускультативно дыхание выслушивается во всех отделах, везикулярное. Частота дыхательных движений (ЧДД) 16/мин. SpО 2 96%. Частота сердечных сокращений (ЧСС) – 80/мин. Артериальное давление 125/85 мм рт. ст.
На рисунке 1 представлено рентгенологическое исследование при поступлении.
На рентгенографии (РГ) и КТ ОГК при поступлении: полиморфные очаговые тени разной величины и формы, средней интенсивности, с чёткими и неровными контурами, сливного характера; в верхней доле правого лёгкого визуализируется неоднородный участок затемнения без чётких границ на фоне фиброзных тяжей; лёгочный рисунок усилен по смешанному типу за счёт интерстициального компонента; корень правого лёгкого подтянут, левого – расширен, малоструктурен, уплотнён; в S2 справа определяется цепочка танталовых швов. Заключение: картина наиболее соответствует инфильтративному туберкулёзу верхней доли правого оперированного лёгкого (рис. 1).
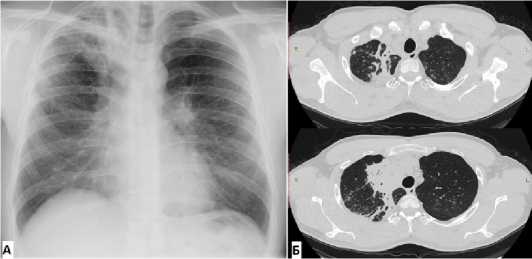
Рисунок 1. Рентгенография (А) и компьютерная томография (Б) при поступлении: множественные полиморфные очаговые тени сливного характера, справа на фоне фиброзных тяжей
Figure 1. Radiography (A) and computed tomography (Б) at admission: Multiple, polymorphic, focal shadows of a drainage character, on the right, against a background of fibrous strands
По данным спирометрии на момент поступления: жизненная ёмкость лёгких (ЖЕЛ) составила – 136,4% от д.в., объём форсированного выдоха – (ОФВ1) 120,1% от д.в., ОФВ1/ЖЕЛ – 92,5%.
В клиническом анализе крови отмечалась относительная лимфоцитопения (14%), увеличение относительного количества нейтрофилов (81,4%) и СОЭ до 44 мм/ч.
По данным диагностической фибробронхоскопии – диффузный двусторонний неспецифический бронхит.
В мокроте методом люминесцентной микроскопии кислотоустойчивые микобактерии обнаружены, методом полимеразной цепной реакции (ПЦР) – ДНК микобактерии туберкулёза обнаружена. Молекулярно-генетическим методом «СИНТОЛ» установлена лекарственная чувствительность возбудителя к изониазиду, рифампицину, фторхинолонам. При посевах на плотные питательные среды выявлен рост МБТ.
Пациент консультирован пульмонологом: учитывая морфологически подтверждённый саркоидоз лёгких и внутригрудных лимфатических узлов (по данным гистологического исследования из анамнеза) пациенту рекомендован приём метилпреднизолона 12 мг со снижением дозы до 8 мг через 1 месяц.
На основании анамнеза, данных микробиологической, молекулярно-генетической диагностики и рентгенологической картины пациенту установлен диагноз: «Инфильтративный туберкулёз верхней доли правого оперированного лёгкого в фазе обсеменения, МБТ (+). Состояние после ВАТС-резекции S2 правого лёгкого. Саркоидоз лёгких и ВГЛУ». Назначено лечение по интенсивной фазе химиотерапии лекарственно-чувствительного туберкулёза в комбинации препаратов – изониазид 0,6, рифампицин 0,6, пиразинамид 1,5, этамбутол 1,2. На фоне приёма пиразинамида отмечался суставной синдром, гиперурикемия до 593 мкмоль/л, в связи с чем препарат был исключён из схемы противотуберкулёзной химиотерапии, назначен левофлоксацин 1,0. В связи с ототоксической реакцией аминогликозиды отменены. Через 1 месяц после начала лечения доза метилпреднизалона была снижена до 8 мг.
При контрольном обследовании через 3 месяца после назначения комплекса противотуберкулёзной химиотерапии, гормонотерапии (8 мг) и патогенетической терапии отмечалась разнонаправленная динамика: положительная динамика в виде купирования кашля, прекращения бактериовыделения и отрицательная рентгенологическая динамика в виде нарастания перилимфатической инфильтрации (рис. 2).
Пациент обсуждён на расширенном врачебном консилиуме: отрицательная динамика расценена как прогрессирование саркоидоза лёгких на фоне уменьшения дозы метипреднизолона. Рекомендовано увеличить дозу системных глюкортикостерои-дов до 12 мг в сутки, противотуберкулёзную терапию проводить по прежнему режиму.
После коррекции лечения, при рентгенологическом контроле через 4 месяца отмечалась положительная динамика в виде уменьшения в размерах и частичного рассасывания мелких участков диссемина-ции в обоих лёгких; верхняя доля правого лёгкого уменьшена в размере, в S1-S2 сохранялся неоднородный с нарастанием кальцинации в динамике (рис. 3).
Пациент повторно обсуждён на консилиуме, на котором решено, что в связи с достижением положительной динамики в результате проводимого лечения взаимно отягощающего течения туберкулёза и саркоидоза лёгких, с санационной целью для сокращения его сроков и минимизации риска обострения обоих заболеваний, целесообразно провести хирургическое лечение в объёме ВАТС повторной резекции правого лёгкого.
Пациенту проведена комбинированная резекция правого оперированного лёгкого (верхняя лобэктомия с резекцией части S4) с частичной плеврэкто-мией.
Интраоперационная картина: плевральная полость тотально облитерирована, пневмолиз выполнен частично в экстраплевральном, частично в экстрафасциальном слое. Верхняя доля уменьшена в объёме, в S1-S2 и части S3 пальпаторно определяется конгломератное образование до 4 см в диаметре, в S4 – уплотнение лёгочной ткани. Во всех отделах лёгкого выявляется мелкоочаговая диссеми-нация. Последовательно выделены, перевязаны и пересечены артерия и вена верхней доли, удалён прикорневой лимфатический узел. На верхнедолевой бронх наложен механический сшивающий аппарат, бронх пересечён, верхняя доля удалена. На часть S4 наложен линейный сшивающий аппарат в видимых пределах здоровых тканей, препарат удалён. Механические швы укреплены непрерывным атравматическими проленовыми швами (3.0). Лёгкое расправлено, занимает плевральную полостью не более чем на 1/2 объёма. Длительность операции составила 140 минут, кровопотеря – 60 мл.
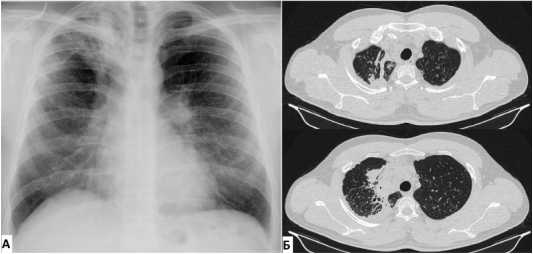
Рисунок 2. Рентгенография (А) и компьютерная томография (Б) через 3 месяца от начала лечения: верхняя доля правого лёгкого уменьшена в размере, нарастание перилимфатической инфильтрации
Figure 2. Radiography (A) and computed tomography (Б) 3 months after the start of treatment: the upper lobe of the right lung is reduced in size, increasing perilymphatic infiltration
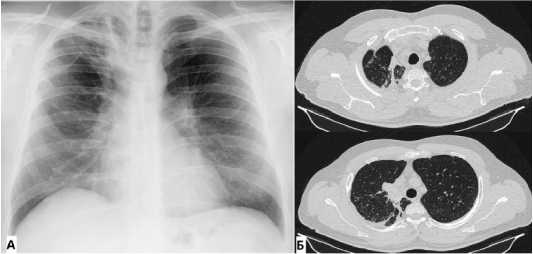
Рисунок 3. Рентгенография (А) и компьютерная томография (Б) через 6 месяца от начала лечения: верхняя доля правого легкого уменьшена в размере, частичное рассасывание инфильтрации с нарастанием кальцинации
Figure 3. Radiography (A) and computed tomography (Б) 6 months after the start of treatment: the upper lobe of the right lung is reduced in size, partial resorption of infiltration with increasing calcification
При микробиологическом исследовании операционного материала: методом люминисцентной микроскопии обнаружены КУМ +. Методом ПЦР обнаружены ДНК МБТ, методом СИНТОЛ установлена чувствительность возбудителя к изониазиду, рифампицину, фторхинолонам.
Патогистологическое исследование операционного материала
Микроскопическое описание: 1) S1-2-3 правого лёгкого. Фрагменты лёгочной ткани с тонкими межальвеолярными перегородками, группы межальвеолярных перегородок утолщены за счёт фиброза. Участки дистелектазов. Выраженный очаговый фиброз. Большое количество организующихся и организованных макрофагально-гигантоклеточных гранулем без фокусов некроза (рис. 4, А) Группы гранулём сливаются между собой. Часть гранулем отмечается в стенках бронхиол (рис. 4, Б). Большое количество разнокалиберных очагов эозинофильного некроза, часть очагов с хорошо выраженной грубноволокни-стой фиброзной капсулой, другие – с формирующейся капсулой. Часть очагов с примесью сегментоядерных лейкоцитов, другие – с фокусами минерали- зации (рис. 4, В) Умеренная диффузно-очаговая лимфоцитарная воспалительная инфильтрация. Умеренный периваскулярный и перибронхиальный фиброз. Часть сосудов с признаками слабовыраженного продуктивного васкулита. При окраске по Циль-Ниль-сену КУМ не обнаружено.
Фрагменты местами утолщённой за счёт фиброза париетальной плевры, отмечается ангиоматоз, на отдельных участках слабая диффузная лимфоцитарная воспалительная инфильтрация. В прилежащей жировой клетчатке кровоизлияния, представленные неизмененными эритроцитами.
Лимфатические узлы
Материал представлен организующимися инкапсулированными очагами казеозного некроза (рис. 4, Г), местами с явлениями гиалиноза, отмечаются фокусы минерализации. Структуры лимфатического узла не определяются.
Заключение: гистологическая картина соответствует диагнозу «Цирротический туберкулёз верхней доли правого лёгкого, фаза слабо выраженного прогрессирования с признаками бронхогенной диссе-минации. Продуктивный плеврит. Туберкулёзный лимфаденит, фаза организации».
А
Б
В
Г
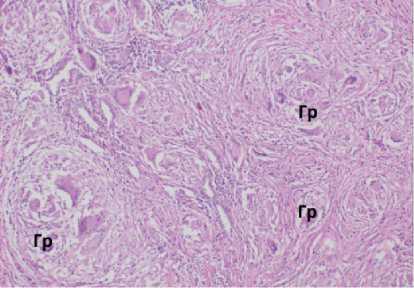
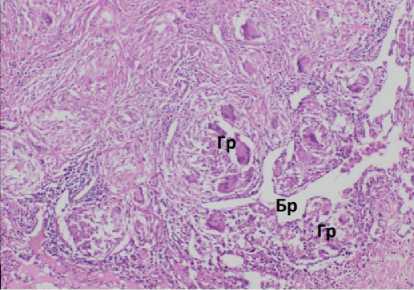
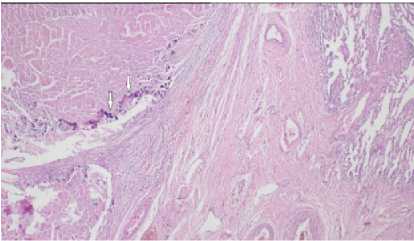
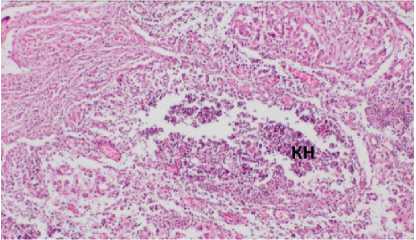
Рисунок 4. Гистологическая картина операционного материала: А. Макрофагально-гистиоцитарные гранулемы (ГР) без некроза, окружённые фиброзной капсулой. Окраска гематоксилином и эозином. Ув.×320. Б. Макрофагально-гистиоцитарные гранулемы (ГР) без некроза в стенке терминальной бронхиолы (БР). Окраска гематоксилином и эозином. Ув.×320. В. Фрагмент стенки туберкулёзной каверны с фокусом минерализации (обозначено стрелкой). Окраска гематоксилином и эозином Ув.×180. Г. Очаг казеозного некроза (КН) в лимфатическом узле. Окраска гематоксилином и эозином Ув.×220
Figure 4. Histological picture of the surgical material: А. Macrophage-histiocytic granulomas (GR) without necrosis, surrounded by a fibrous capsule. Staining with hematoxylin and eosin. ×320. Б. Macrophage-histiocytic granulomas (GR) without necrosis in the wall of the terminal bronchiole (BR). Staining with hematoxylin and eosin. ×320. В. A fragment of the wall of a tuberculous cavity with a focus of mineralization (indicated by an arrow). Hematoxylin and eosin staining ×180 . Г. A focus of caseous necrosis (CD) in the lymph node. Staining with hematoxylin and eosin ×220
Послеоперационный период протекал благоприятно, дренажи удалены на 7-е сутки, швы – на 14-е сутки.
На контрольной КТ ОГК через 1 месяц (рис. 5): правое лёгкое после оперативного вмешательства уменьшено в объёме, приподнято кверху, ротировано. Паракостально в области переднего рёбернодиафрагмального синуса, на уровне IV-го ребра группа мелких пузырьков воздуха и небольшое количество жидкости с отёком мягких тканей. В зонах цепочек танталовых скоб отмечается инфильтративноателектатическое уплотнение лёгочного интерсти-ция, сужение просвета СДБ. В левом лёгком, преимущественно в среднем отделе визуализируются множественные мелкие сгруппированные очаги. Просвет трахеи не изменён, свободные просветы бронхов прослеживаются до субсегментарных ветвей. Средостение умеренно смещено вправо. Выпота в левой плевральной полости нет. Заключение: неполное расправление правого оперированного лёгкого, КТ-признаки послеоперационных изменений правого лёгкого.
Консультирован пульмонологом 07.07.2023. Пациент с морфологически верифицированным саркоидозом в течение 5 месяцев получает метипред в дозе 12 мг/сут, рекомендовано дозу метипреда оставить прежней в связи с недавним проведением оперативного вмешательства в течение ещё 1 месяца. Учитывая неполное расправление лёгкого справа, сохраняющийся кашель к лечению добавить ингаляции беродуала.
Учитывая большой объём резекции, во избежание обострения процесса, дальнейшего прогрессирования и исключения патологического перерастя-жения лёгочной ткани правого оперированного лёгкого через 1 месяц после резекции выполнена отсроченная торакомиопластика с резекцией I-IV рёбер справа со вскрытием остаточной полости. Удалена группа лимфатических узлов паратрахеальной группы. Полость заполнена гемостатическим материалом, выполнена её пластика подлопаточной мышцей. Операция прошла без особенностей. Швы сняты на 21 сутки, дренажи – на 5 сутки.
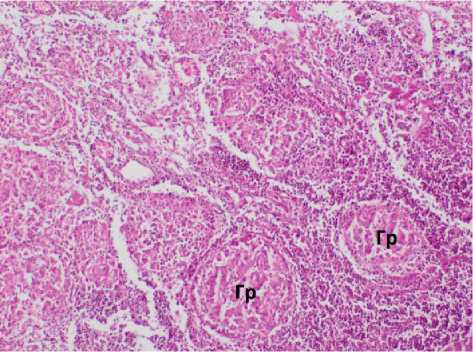
Патогистологическое исследование операционного материала (рис. 6): в материале лимфоузел в тонкой соединительно-тканной капсуле, подкапсульные синусы свободны, фолликулярное строение сохранено частично, за счёт распространённых включений, множественных рыхлых, частично увядающих, эпителиоидно-клеточных гранулём, без определяемых некрозов и многоядерных гигантских клеток (рис. 6, А). Часть гранулём без чётких границ, местами сливаются между собой, отдельные гранулёмы с чёткими границами.
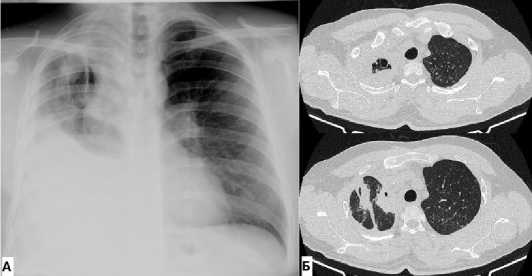
Рисунок 5. Рентгенография (А) и компьютерная томография (Б) через 1 месяц после комбинированной резекции правого лёгкого: неполное расправление правого оперированного лёгкого
Figure 5. Radiography (A) and computed tomography (Б) after 1 months after combine resection of right lung: not full righ postoperative lungs
Б
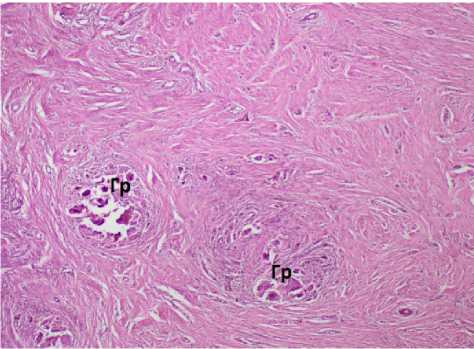
Рисунок 6. Гистологическая картина операционного материала: А. Фрагмент лимфатического узла с множеством эпителиоидноклеточных гранулём без некроза. Окраска гематоксилином и эозином. ×280. Б. Увядающие макрофагальные гранулемы в составе фиброзно измененной плевры. Окраска гематоксилином и эозином. ×220
Figure 6. Histological picture of the surgical material: А. A fragment of a lymph node with multiple epithelioid cell granulomas without necrosis. Staining with hematoxylin and eosin. ×280. Б. Withering macrophage granulomas in the fibrously altered pleura. Staining with hematoxylin and eosin. ×220
В материале фиброзно-соединительная ткань с участками жировой и включениями мышечных волокон, в фиброзной ткани встречаются нечётко очерченные участки гранулематозного воспаления в виде увядающих эпителиоидно-клеточных гранулём без некрозов, отдельные с наличием многоядерных гигантских клеток (рис. 6, Б).
В материале фрагменты костной и прилежащей мышечно-жировой ткани с очаговыми кровоизлияниями, без признаков воспаления.
Заключение: в лимфоузле и фиброзно-соединительной ткани гранулематозное воспаление в виде увядающих эпителиоидных и эпителиоидно-макрофагальных гранулём без некрозов. Картина может соответствовать саркоидозу ВГЛУ. Фрагменты рёбер без признаков остеомиелита.
Пациент продолжил получать противотуберкулёзную терапию в объёме изониазид 0,6 1 р/д per os, рифампицин 0,6 1 р/д в/в, этамбутол 1,2 1 р/д per os, спарфлоксацин 0,2, линезолид 0,6 в/в на фоне гормонотерапии (метилпреднизолон 12 мг) и терапии сопровождения. Через 1 месяц после операции, согласно рекомендации пульмонолога, доза метилпреднизолона была уменьшена до 8 мг.
На РГ и КТ ОГК через 1 месяц после торакопластики: правое лёгкое после оперативного вмешательства уменьшено в объёме, приподнято кверху, ротировано. В динамике в зонах цепочек танталовых отмечается частичное рассасывание инфильтративно-ателектатического уплотнения лёгочного ин-терстиция, сохраняется сужение просвета СДБ. В левом лёгком, преимущественно в среднем отделе и в среднем отделе оставшейся части правого лёгкого отмечается появление множественных мелких перилимфатических частично сгруппированных очагов. Визуализирующиеся интраторакальные лимфатические узлы без признаков кальцинации, лимфатические узлы бифуркационной группы увеличились до
12 мм. Заключение: саркоидоз ВГЛУ и лёгких, рентгенологически прослеживается отрицательная динамика.
Выполнена оценка активности АПФ – выявлено увеличение активности АПФ до 86 ед, что было расценено как прогрессирование саркоидоза.
Пациент повторно консультирован пульмонологом, рекомендовано продолжить приём низких доз системных кортикостероидов (8 мг), а также провести курс ЭКМЛ для индукции ремиссии саркоидоза и потенциирования эффекта кортикостероидов.
На контрольном КТ ОГК через 3 месяца отмечалась разнонаправленная динамика (частичное рассасывание перелимфатической диссеминации в верхних отделах левого лёгкого, нарастание и слияние очагов в нижней доле левого лёгкого, появление сливных очагов в нижней доле).
Продолжена терапия в прежнем объёме.
На контрольном КТ ОГК через 6 месяцев (рис. 7): в динамике в зонах цепочек танталовых продолжается рассасывание инфильтративно-ателектатического уплотнения лёгочного интерстиция. В левом лёгком, преимущественно в среднем отделе и в среднем отделе оставшейся части правого лёгкого отмечается частичное рассасывание мелких перилимфатических очагов.
В связи с эффективным завершением курса терапии лекарственно-чувствительного туберкулёза противотуберкулёзная терапия была отменена через 6 месяцев. Продолжено лечение низкими дозами глюкокортикостероидов (8 мг).
Пациент продолжил амбулаторное наблюдение в ФГБНУ «ЦНИИТ», вернулся к привычному образу жизни, самочувствие удовлетворительное. На контрольном КТ ОГК через 6 месяцев – свежих очаговых и инфильтративных изменений не выявлено.
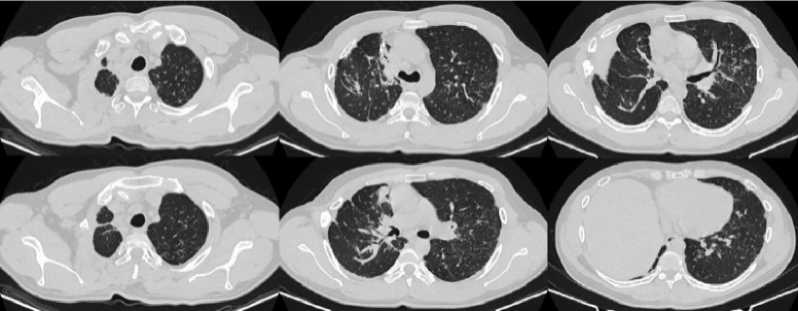
Рисунок 7. Компьютерная томография через 6 месяцев после торакопластики: частичное рассасывание очагов в средних отделах обоих лёгких Figure 7. Computed tomography after 6 months after toracoplasty: absence of a residual pleural cavity on the right, partial resorption of foci in the middle sections of both lungs
Обсуждение
В случаях, когда возникают сомнения в диагностике, ключевую роль играет анализ морфологической картины гранулематозного воспаления в образцах ткани лёгких и лимфатических узлов средостения. Однако этот метод не всегда позволяет установить точный диагноз. Это можно объяснить тем, что эпителиоидно-клеточные гранулёмы при туберкулёзе и саркоидозе весьма схожи между собой, что значительно усложняет процесс дифференциальной диагностики этих заболеваний [9].
В данном примере у пациента изначально выявлены дисеминированные изменения в лёгких и ВГЛУ, и путём взятия биопсии установлен диагноз «саркоидоз лёгких и ВГЛУ», что потребовало назначения низ-кодозной гормональной терапии. Именно поэтому перед началом гормональной терапии в ФГБНУ «ЦНИИТ» осуществлён запрос блоков и стёкол операционного материала лёгкого и ВГЛУ, полученного в другом учреждении, что не увенчалось успехом. Ввиду этого исключить сочетанное течение саркоидоза и туберкулёза не представлялось возможным. Сложностью лечения данного пациента, безусловно, является поиск баланса между проведением химиотерапии противотуберкулёзными препаратами и системными глюкокортикостероидами на всех этапах лечения. При этом после этиологической верификации туберкулёза лёгких и туберкулёзного лимфаденита диагноз саркоидоза был поставлен под большие сомнения. При всякой попытке снизить дозу глюкокортикостероидов в надежде их последующей отмены, после окончания хирургического лечения, рентгенологически отмечалась отрицательная динамика в виде появления очагов диссеминации. К тому же нельзя было исключить наличие саркоидоза, учитывая данные последней, торакомиопластической операции с удалением ВГЛУ, при гистологическом изучении которых было выявлено гранулематозное воспаления, характерное для саркоидоза. Поэтому появление свежих очагов диссеминации было с большой вероятностью связано с обострением именно саркоидоза. Как можно видеть в данном примере, после удаления основного очага туберкулёзной инфекции с последующей профилактикой пере-растяжения оставшихся отделов лёгкого на фоне проводимой терапии (ПТТ + ГКС) отмечена регрессия очагов диссеминации и стабилизация процесса. В итоге, после завершения противотуберкулёзной терапии пациенту удалось снизить дозу гормонов и добиться клинического излечения.
Выводы
Данный клинический пример демонстрирует сложности лечения деструктивного туберкулёза лёгких и ВГЛУ в сочетании с саркоидозом. Своевременная коррекция терапии с учётом переносимости препаратов, применение хирургических методов лечения и коррекция пульмонологом схемы гормонотерапии позволили добиться удовлетворительных результатов в лечении у данного пациента.
Список литературы Сложности лечения пациента с сочетанной патологией - туберкулёз лёгких и саркоидоз (клинический случай)
- Борисов С.Е., Соловьева И.П., Евфимьевский В.П., Купавцева Е.А., Богородская Е.М. Диагностика и лечение саркоидоза органов дыхания (пособие для фтизиатров и пульмонологов). Проблемы туберкулез. 2003;6:51-64.
- Визель А.А., ред. Саркоидоз: от гипотезы к практике. Казань: ФЭН; Академия наук РТ; 2004:348.
- Куклина Г.М., Романов В.В., Шмелев Е.И. Сочетание двух диссеминированных процессов у одной больной (клиническое наблюдение). Доктор.Ру. 2016;2:52-56. EDN: WFSMON
- Calaras D., Munteanu О., Botnaru V. Sarcoidosis and tuberculosis: A rare combination? Euro. Respir. J. 2012;40(56):3635. https://erj.ersjour-nals.com/content/40/Suppl_56/P3635.short.
- Корж Е.В. Дифференциальная диагностика туберкулеза легких: учебное пособие. Донецкий мед. ун-т. Донецк, 2019.
- Дифференциальная диагностика саркоидоза и туберкулеза легких / под ред. В. Н. Адамовича. М., 1998:52-77.
- Мишин В.Ю., Демихова О.В., Кузьмина Н.В. Диагностика и дифференциальная диагностика гематогенно-диссеминированного туберкулеза легких. Сonsilium Medicum. 2002;4(9):498-506.
- Саркоидоз. Под ред. акад. А.Г. Чучалина. М.: Атмосфера, 2010:416.
- Двораковская И.В., Акопов А.Л., Ариэль Б.М., Платонова И.С., Русанов А.А., Хромова Т.И. Биопсия в пульмонологии. СПб.; 2011. 71 с.


