Случай первичной меланомы желудка
Автор: Тонеев Е. А., Чарышкин А. Л., Деньгина Н. В., Жинов А. В., Мартынов А. А., Городнов С. В., Лазаревский М. М.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Клинический случай
Статья в выпуске: 1 т.10, 2020 года.
Бесплатный доступ
Первичная меланома желудка представляет собой чрезвычайно редкое заболевание. Меланома верхних отделов желудочно-кишечного тракта диагностируется, как правило, в виде метастаза из первичного очага на коже с частотой 1 - 4 % случаев. В статье представлен клинический случай первичной меланомы желудка у пациентки, которая получила комплексное лечение в условиях ГУЗ Областной клинический онкологический диспансер г. Ульяновска.
Меланома желудка, гастрэктомия, торакоабдоминальная хирургия, диагностика меланомы
Короткий адрес: https://sciup.org/140251214
IDR: 140251214 | DOI: 10.18027/2224-5057-2020-10-35-40
A case of primary gastric melanoma
Primary gastric melanoma is an extremely rare disease. Melanoma of upper gastrointestinal tract usually occurs as metastasis from a primary skin tumor in 1 to 4 % of cases. The paper describes a case report of primary gastric melanoma in a female patient who received complex therapy at the State Healthcare Institution Ulyanovsk Regional Clinical Oncology Dispensary.
Текст научной статьи Случай первичной меланомы желудка
Клиническое наблюдение
Общеклинические данные обследования больной не содержали отклонений от нормы, показатели онкомаркеров (РЭА, СА-19-9) не превышали референсных значений.
Мультидисциплинарный консилиум врачей в составе торакального хирурга, радиотерапевта и химиотерапевта принял решение начать лечение с полихимиотерапии по схеме ELF (Этопозид 200 мг в/в 1–3 дни, лейковорин 85 мг в/в 1–3 дни, 5-фторурацил 850 мг в/в 1–3 дни, повтор каждые 28 дней) ввиду распространённости процесса и наличия сопутствующей сердечно-сосудистой пато- логии; кроме того, состоялась заочная консультация пациентки в ФГБУ НМИЦ им. Н.Н. Блохина, с одобрением предложенной схемы химиотерапии. Пациентке было проведено 6 курсов химиотерапии, а также паллиативный курс гипофракционированного облучения (12 фракций по 3 Гр) на область первичной опухоли в биологически эквивалентной дозе (BED) 46,8 Гр. По данным последующего контрольного обследования через 1 месяц после окончания лечения отмечена стабилизация процесса (рис. 3, 4). Пациентка все этапы лечения перенесла удовлетворительно, нефро- и гематологической токсичности не отмечено.
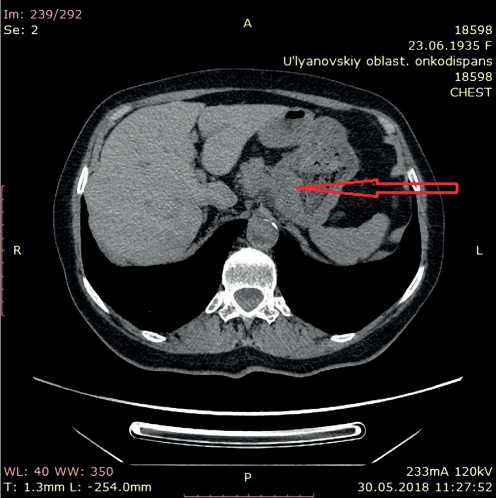
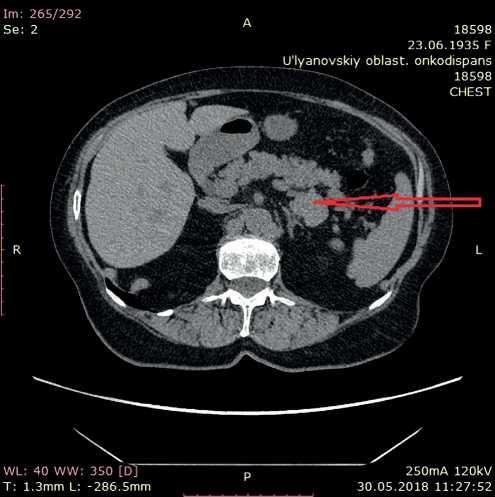
Рисунок 2. КТ брюшной полости (стрелкой отмечен увеличенный л/узел в области хвоста поджелудочной железы).
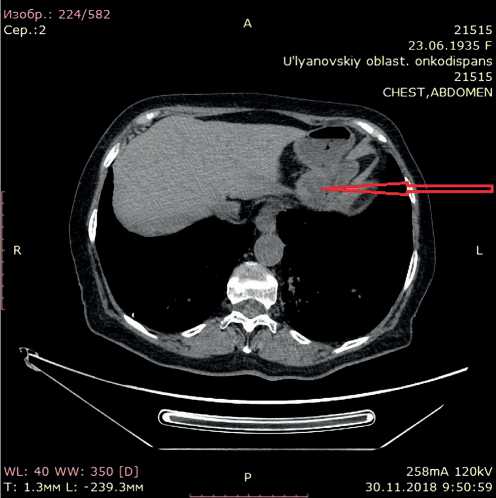
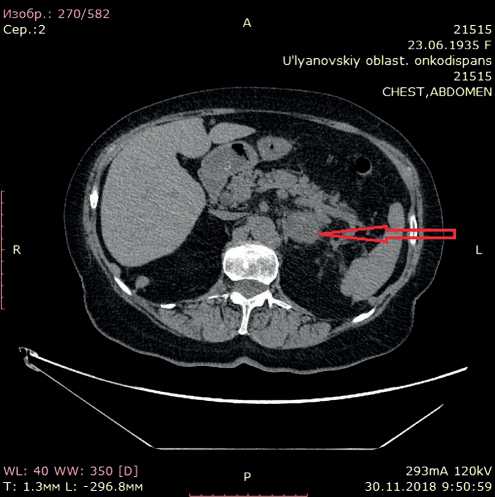
Рисунок 4. КТ брюшной полости (стрелкой указан отмечен увеличенный л/узел в области хвоста поджелудочной железы).
В процессе лечения больная регулярно наблюдалась у кардиолога с целью максимально возможной коррекции сопутствующей сердечно-сосудистой патологии.
Пациентка повторно осмотрена на консилиуме врачей, в этот раз с привлечением анестезиологов; было принято решение провести хирургическое лечение в объеме гастрэктомии с лимфодиссекцией D2 ввиду отсутствия положительной динамики процесса, а также удовлетворительных функциональных показателей больной.
Операция состоялась 12.02.2019: произведена лапаротомия, торакотомия справа, расширенно-комбинированная гастрэктомия, субтотальная резекция пищевода с пластикой толстой кишкой, лимфодиссекция уровня D2, спленэктомия, левосторонняя адреналэктомия.
Причиной субтотальной резекции пищевода стало его неудовлетворительное кровоснабжение в нижнегрудном сегменте, поэтому было принято решение о выполнении его пластики левой половиной толстой кишки. Левосторонняя адреналкэтомия произведена из-за инвазии метастатического конгломерата лимфоузлов 11 группы в левый надпочечник. Интраоперацинно отмечено интенсивное окрашивание лимфатических узлов в черный цвет.
Послеоперационный период протекал гладко, экстубация выполнена через 4 часа после операции, энтеральное питание больной начато со вторых суток.
Рентгенологический контроль на 7 и 12 сутки не выявил осложнений со стороны трансплантата (рис. 5,6).
Выписка пациентки из стационара состоялась на 21 сутки после оперативного лечения.
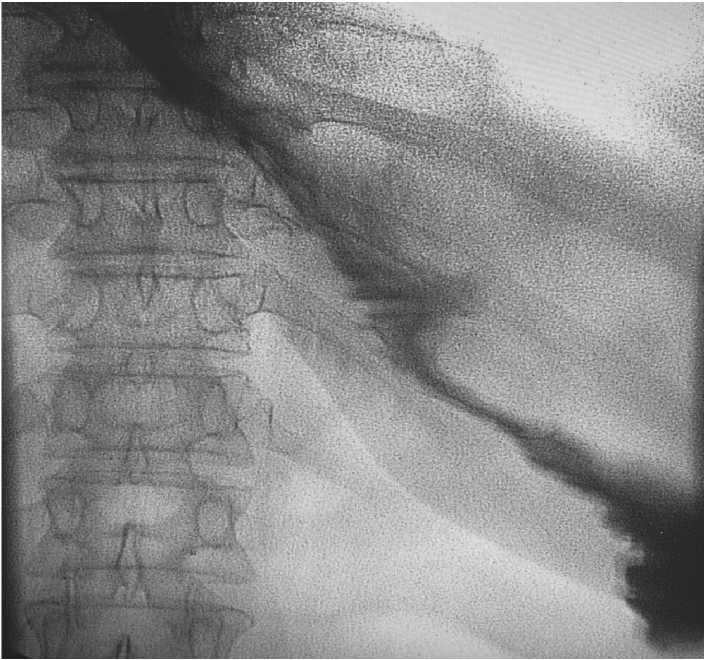
Рисунок 5. Рентгенологический контроль на 7 сутки после операции.
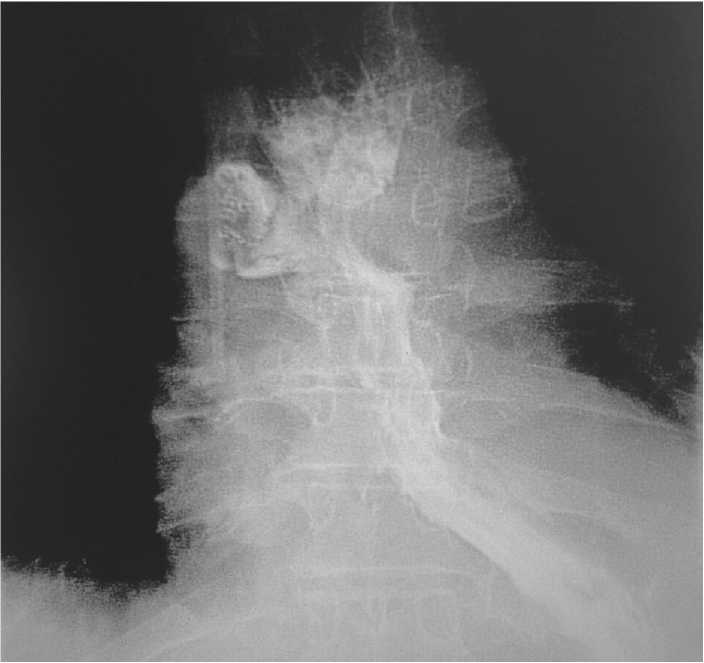
Рисунок 6. Рентгенологический контроль на 12 сутки после операции.
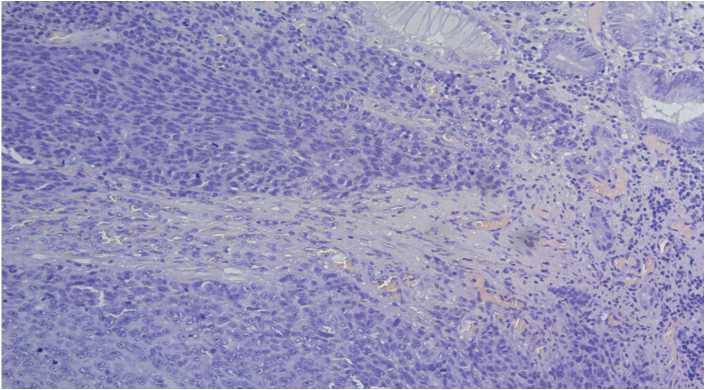
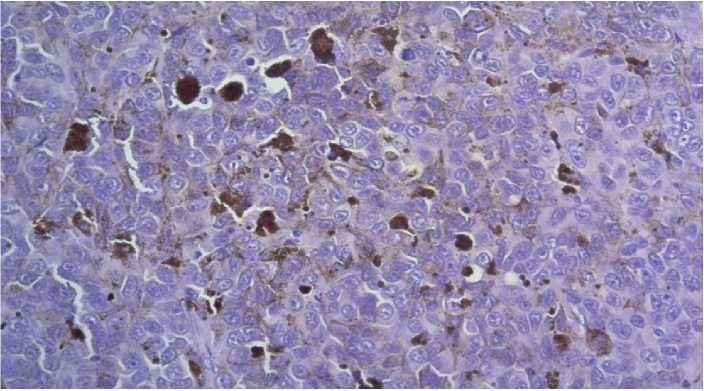
Рисунок 8. Окраска гематоксилином и эозином, ув. × 20. Очаговая пигментация в опухоли.
3 × 2 см, в подлежащей ткани опухолевый узел буровато-серого цвета с черными вкраплениями, прорастает мышечный слой без прорастания серозной оболочки.
Микроскопическое описание
Иммуногистохимическое исследование
Экспрессия опухолевыми клетками MART-1 (маркер клеток меланогенного происхождения) (рис. 9).
После полученного морфологического заключения пациентка была тщательно осмотрена онкологом для выявления патологических образований на коже и видимых слизистых и офтальмологом для исключения меланомы сетчатки. Опухолевого поражения вышеуказанных органов не отмечено. Эндоскопическое обследование кишки было произведено еще на догоспитальном этапе, и данных за поражение толстой кишки также не получено.
Для подтверждения диагноза был выполнен пересмотр гистопрепаратов в ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава РФ. Диагноз в итоге был подтвержден, а также выполнено генетическое исследование панели молекулярно-генетических онкомаркеров — мутаций в «горячих точках» генов KRAS (экзоны 2, 3 и 4), NRAS (экзоны 2, 3 и 4), BRAF (экзон 15), GNAQ (экзоны 4 и 5), GNA11 (экзоны 4 и 5) и TERT.
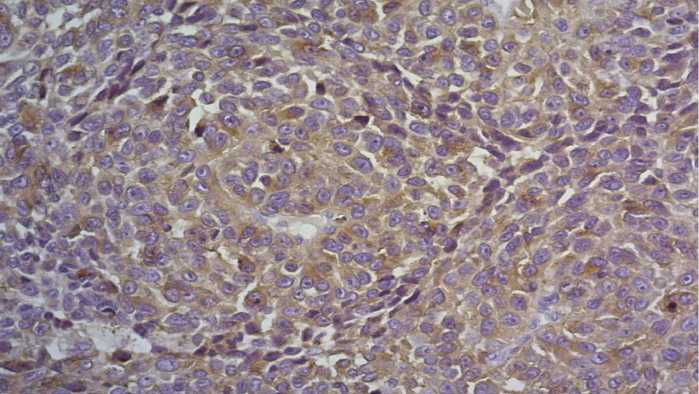
Рисунок 9. Иммуногистохимическое исследование с антителом к MART-1 — маркеру клеток меланогенного происхождения, ув. ×20. В цитоплазме опухолевых клеток отмечается диффузная выраженная экспрессия MART-1.
Результат генетического исследования
По результатам исследования методом мутационно-специфической ПЦР-РВ в соответствии с ДНК образца мутаций в «горячих точках» экзонов 2, 3 и 4 гена KRAS не обнаружено, так же как не выявлено мутаций в «горячих точках» экзонов 2, 3 и 4 гена NRAS и в «горячих точках» экзона 15 гена BRAF.
По результатам исследования методами высокочувствительной мутационно-специфической ПЦР-РВ и ПЦР с последующим секвенированием продуктов ПЦР в ДНК образца мутаций в «горячих точках» экзонов 4 и 5 гена GNAQ не обнаружено. Не было выявлено и мутаций в «горячих точках» экзонов 4 и 5 гена GNA11, и в «горячих точках» гена TERT.
Таким образом, был подтверждён диагноз меланомы, причем с большой вероятностью — внекожной локализации.
Пациентка от проведения какого-либо дальнейшего специального лечения отказалась, ссылаясь на слабость.
ОБСУЖДЕНИЕ
ВЫВОДЫ
От авторов: работа поддержана Грантом для российских исследователей ассоциации специалистов по проблемам меланомы.
Список литературы Случай первичной меланомы желудка
- Song SE, Lee CH, Kim KA, Lee HJ, Park CM. Malignant glomus tumor of the stomach with multiorgan metastases: report of a case. Surg Today. 2010;40 (7):662-667. 10.1007 / s00595-008-4113-z. DOI: 10.1007/s00595-008-4113-z
- Baur EH. Ein Fall von primarem melanom des esophagus. Arb Geb Pathol Anat Inst Tubingen. 1906;5:343-354
- Sabanathan S, Eng J, Pradhan GN. Primary malignant melanoma of the esophagus. Am J Gastroenterol. 1989;84:1475- 1481
- Scotto J, Fraumeni JF, Lee JA. Melanomas of the eye and other noncutaneous sites: epidemiologic aspects. J Natl Cancer Inst. 1976;56:489-491.
- Li H, Fan Q, Wang Z, Xu H, Li X, Zhang W, Zhang Z. Primary malignant melanoma of the duodenum without visible melanin pigment: a mimicker of lymphoma or carcinoma. Diagn Pathol. 2012;7:74. DOI: 10,1186 / 1746-1596-7-74
- Chang AE, Karnell LH, Menck HR. The National Cancer Data Base report on cutaneous and noncutaneous melanoma: a summary of 84,836 cases from the past decade. The American College of Surgeons Commission on Cancer and the American Cancer Society. Cancer. 1998;83:1664-1678. 10.1002 / (SICI) 1097-0142 (19981015) 83:83.0. CO;2-G
- DOI: 10.1002/(SICI)1097-0142(19981015)83
- Patel JK, Didolkar MS, Pickren JW, Moore RH. Metastatic pattern of malignant melanoma. A study of 216 autopsy cases. Am J Surg. 1978;135:807-810
- Aggarwal R, Dhawan S, Chopra P. Primary Gastric Melanoma: a Diagnostic Challenge. J Gastrointest Cancer. 2013 [Epub ahead of print]
- Schuchter LM, Green R, Fraker D. Primary and metastatic diseases in malignant melanoma of the gastrointestinal tract. Curr Opin Oncol. 2000;12:181-185. 10.1097 / 00001622-200003000-00014.
- DOI: 10.1097/00001622-200003000-00014
- Cheung MC, Perez EA, Molina MA, Jin X, Gutierrez JC, Franceschi D, Livingstone AS, Koniaris LG. Defining the role of surgery for primary gastrointestinal tract melanoma. J Gastrointest Surg. 2008;12:731-738. DOI: 10,1007 / s11605-007-0417-3
- Sachs DL, Lowe L, Chang AE, Carson E, Johnson TM. Do primary small intestinal melanomas exist Report of a case. J Am Acad Dermatol. 1999;41:1042-1044. 10.1016 / S0190-9622 (99) 70273-2
- DOI: 10.1016/S0190-9622(99)70273-2
- Song W, Liu F, Wang S, Shi H, He W, et al. (2014) Primary gastric malignant melanoma: Challenge in preoperative diagnosis. Int J Clin Exp Pathol 7: 6826-6831.
- Kyriakopoulos C, Zarkavelis G, Andrianopoulou A (2017) Primary pulmonary malignant melanoma: Report of an important entity and literature review. Case Rep Oncol Med 2017:8654326.
- Blecker D, Abraham S, Furth EE, Kochman ML. Melanoma in the gastrointestinal tract. Am J Gastroenterol. 1999;94:3427- 3433. 10.1111 / j. 1572-0241.1999.01604. x.
- DOI: 10.1111/j.1572-0241.1999.01604.x


