Случай полной морфологической регрессии при комбинированном лечении резектабельного Her2/neu-позитивного рака желудка
Автор: Августинович А.В., Афанасьев С.Г., Спирина Л.В., Кайгородова Е.В., Ермоленко Р.В., Самцов Е.Н., Фролова И.Г., Черемисина О.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Случай из клинической практики
Статья в выпуске: 1 т.23, 2024 года.
Бесплатный доступ
Актуальность. Г иперэкспрессия Her2neu встречается у 15-20 % больных раком желудка и коррелирует с неблагоприятным течением заболевания. Описание клинического случая. Представлен клинический случай полной морфологической регрессии резектабельной опухоли желудка с гиперэкспрессией Her2/ neu. Пациент получил комбинированное лечение, включающее 8 курсов неоадъювантной химиотерапии по схеме mFLOT + трастузумаб с последующим хирургическим вмешательством в объёме R0- резекции. Добавление таргетной терапии не оказало негативного влияния на течение периоперационного периода. При плановом морфологическом исследовании операционного материала получено заключение о полном лечебном патоморфозе опухоли (Mandart TGR1). К настоящему времени пациент наблюдается в течение 27 мес без признаков рецидива заболевания.
Рак желудка, гиперэкспрессия her2neu, комбинированное лечение, неоадъювантная терапия, полная регрессия опухоли
Короткий адрес: https://sciup.org/140303744
IDR: 140303744 | УДК: 616.33-006.6-08-059 | DOI: 10.21294/1814-4861-2024-23-1-170-177
A case of pathological complete regression in combined modality treatment of resectable Her2/neu-positive gastric cancer
Background. Overexpression of Her2neu occurs in 15-20% of patients with gastric cancer and correlates with an unfavorable prognosis. Case report. We report a case of pathological complete regression of resectable gastric cancer with Her2/neu overexpression. The patient received combined modality treatment including 8 cycles of neoadjuvant chemotherapy with mFLOT + trastuzumab followed by R0 resection. The addition of targeted therapy did not have a negative impact on the perioperative period. Histolohical examination of the surgical specimen revealed pathological complete response (Mandart TGR1). Currently, the patient has been followed-up for 27 months without signs of disease relapse.
Текст научной статьи Случай полной морфологической регрессии при комбинированном лечении резектабельного Her2/neu-позитивного рака желудка
Описание клинического случая
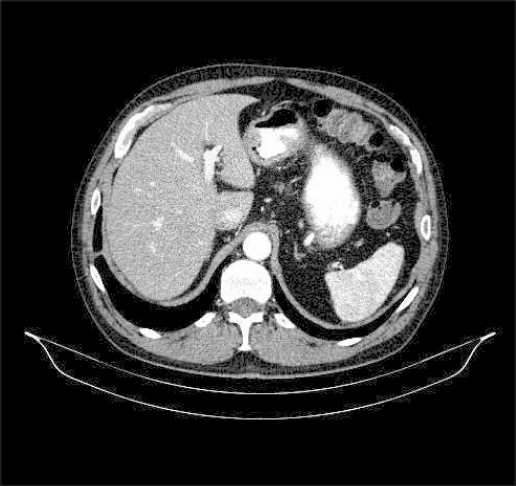
Примечание: рисунок выполнен авторами
Fig. 1. Patient G., 69 years. Diagnosis: Cancer of the antrum of the stomach. Spiral CT of the abdominal organs before treatment.
Tumor infiltration of the walls of the antrum of the stomach.
Note: created by the authors
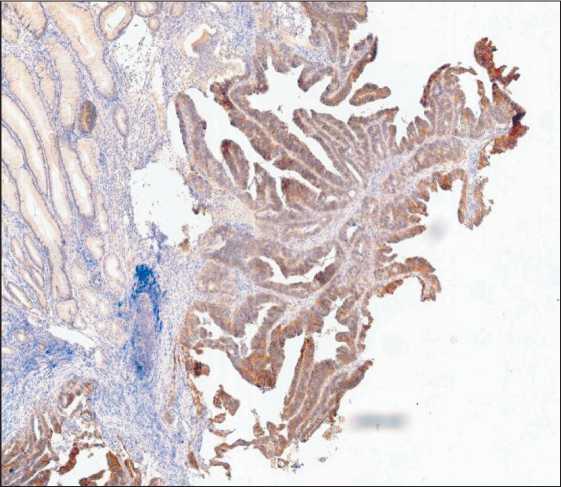
Гиперэкспрессия Her2/neu. Гистологический сканер Aperio AT2, Leica, ×400.
Примечание: рисунок выполнен авторами
Fig. 2. Microphoto. Immunohistochemistry. Patient G., 69 years. Diagnosis: Cancer of the antrum of the stomach. Overexpression of Her2/neu. Histological scanner Aperio AT2, Leica, ×400.
Note: created by the authors
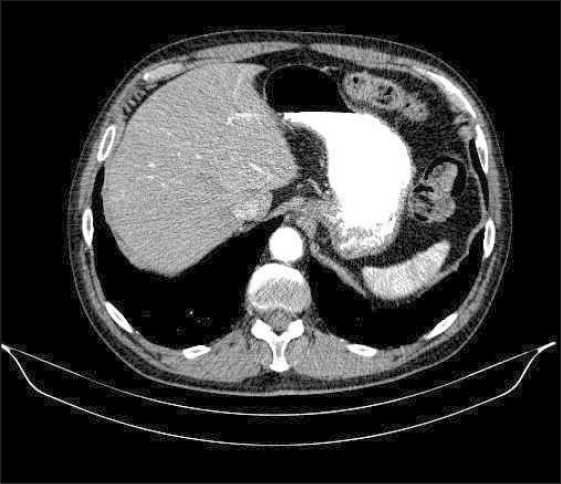
Примечание: рисунок выполнен авторами
Fig. 3. Patient G., 69 years. Diagnosis: Cancer of the antrum of the stomach. Spiral CT of the abdominal organs after neoadjuvant chemotherapy with trastuzumab. The tumor in the antrum of the stomach is not visualized. Note: created by the authors
В соответствии с планом комбинированного лечения в период с 09.04. 21 по 06.08.21 проведено 8 курсов предоперационной химиотаргетной терапии по схеме mFLOT + трастузумаб, которую больной перенес относительно удовлетворительно, из побочных реакций отмечались тошнота, лейкопения лёгкой степени. Побочные эффекты купировались назначением стандартной консервативной терапии, дополнительных перерывов между курсами НАХТ не требовалось.
При динамическом наблюдении в течение 27 мес после завершении комбинированного лечения, по данным плановых контрольных обследований признаков прогрессирования опухолевого процесса не выявлено.
Обсуждение
Список литературы Случай полной морфологической регрессии при комбинированном лечении резектабельного Her2/neu-позитивного рака желудка
- Sung H., Ferlay J., Siegel R.L., Laversanne M., Soerjomataram I., Jemal A., Bray F. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin. 2021; 71(3): 209-49. https://doi.org/10.3322/caac.21660.
- Zlokachestvennye novoobrazovaniya v Rossii v 2021 godu (zabolevaemost' i smertnost'). Pod red. A.D. Kaprina, V.V. Starinskogo, A.O. Shakhzadovoi. M., 2022. 252 s.
- Besova N.S., Bolotina L.V., Kalinin A.E., Kononets P.V., Malikhova O.A., Protsenko S.A., Ryabov A.B., Stilidi I.S., Ter-Ovanesov M.D., Tryakin A.A., Khomyakov V.M. Prakticheskie rekomendatsii po lekarstvennomu lecheniyu raka zheludka. Zlokachestvennye opukholi. 2019; 9(3S2): 308-323. https://doi.org/10.18027/2224-5057-2019-9-3s2-308-323.
- Al-Batran S.E., Homann N., Pauligk C., Goetze T.O., Meiler J., Kasper S., Kopp H.G., Mayer F., Haag G.M., Luley K., Lindig U., Schmiegel W., Pohl M., Stoehlmacher J., Folprecht G., Probst S., Prasnikar N., Fischbach W., Mahlberg R., Trojan J., Koenigsmann M., Martens U.M., Thuss-Patience P., Egger M., Block A., Heinemann V., Illerhaus G., Moehler M., Schenk M., Kullmann F., Behringer D.M., Heike M., Pink D., Teschendorf C., Löhr C., Bernhard H., Schuch G., Rethwisch V., von Weikersthal L.F., Hartmann J.T., Kneba M., Daum S., Schulmann K., Weniger J., Belle S., Gaiser T., Oduncu F.S., Güntner M., Hozaeel W., Reichart A., Jäger E., Kraus T., Mönig S., Bechstein W.O., Schuler M., Schmalenberg H., Hofheinz R.D.; FLOT4-AIO Investigators. Perioperative chemotherapy with fluorouracil plus leucovorin, oxaliplatin, and docetaxel versus fluorouracil or capecitabine plus cisplatin and epirubicin for locally advanced, resectable gastric or gastro-oesophageal junction adenocarcinoma (FLOT4): a randomised, phase 2/3 trial. Lancet. 2019 May 11; 393(10184): 1948-1957. https://doi.org/10.1016/S0140-6736(18)32557-1.
- Bartley A.N., Washington M.K., Colasacco C., Ventura C.B., Ismaila N., Benson A.B. 3rd, Carrato A., Gulley M.L., Jain D., Kakar S., Mackay H.J., Streutker C., Tang L., Troxell M., Ajani J.A. HER2 Testing and Clinical Decision Making in Gastroesophageal Adenocarcinoma: Guideline From the College of American Pathologists, American Society for Clinical Pathology, and the American Society of Clinical Oncology. J Clin Oncol. 2017 Feb; 35(4): 446-464. https://doi.org/10.1200/JCO.2016.69.4836.
- Ruschoff J., Hanna W., Bilous M., Hofmann M., Osamura R.Y., Penault-Llorca F., van de Vijver M., Viale G. HER2 testing in gastric cancer: a practical approach. Mod Pathol. 2012; 2(5): 637-50. https://doi.org/10.1038/modpathol.2011.1982.
- Hofmann M., Stoss O., Shi D., Buttner R., van de Vijver M., Kim W., Ochiai A., Rüschoff J., Henkel T. Assessment of a HER2 scoring system for gastric cancer: results from a validation study. Histopathology. 2008 Jun; 52(7): 797-805. https://doi.org/10.1111/j.1365-2559.2008.03028.x.
- Im S.A., Lee K.E., Nam E., Kim D.Y, Seong C.M., Park H.Y., Han W.S., J.Y., Lee S.N. The prognostic significance of the overexpression of HER-2/ neu in Korean gastric carcinomas and the in vitro effects of Anti-HER-2/neu antibody on cell growth in the gastric carcinoma cell lines. Cancer Res Treat. 2003; 35(2): 109-16. https://doi.org/10.4143/crt.2003.35.2.109.
- Gianni L., Eiermann W., Semiglazov V., Manikhas A., Lluch A., Tjulandin S., Zambetti M., Vazquez F., Byakhow M., Lichinitser M., Climent M.A., Ciruelos E., Ojeda B., Mansutti M., Bozhok A., Baronio R., Feyereislova A., Barton C., Valagussa P., Baselga J. Neoadjuvant chemotherapy with trastuzumab followed by adjuvant trastuzumab versus neoadjuvant chemotherapy alone, in patients with HER2-positive locally advanced breast cancer (the NOAH trial): a randomised controlled superiority trial with a parallel HER2-negative cohort. Lancet. 2010; 375 (9712): 377-384. https://doi.org/10.1016/S0140-6736(09)61964-4.
- Bang Y.J., Van Cutsem E., Feyereislova A., Chung H.C., Shen L., Sawaki A., Lordick F., Ohtsu A., Omuro Y., Satoh T., Aprile G., Kulikov E., Hill J., Lehle M., Rüschoff J., Kang Y.K.; ToGA Trial Investigators. Trastuzumab in combination with chemotherapy versus chemotherapy alone for treatment of HER2-positive advanced gastric or gastro-oesophageal junction cancer (ToGA): a phase 3, open-label, randomised controlled trial. Lancet.. 2010; 376(9742): 687-97. https://doi.org/10.1016/S0140-6736(10)61121-X.
- Orlova R.V., Belyak N.P., Kutukova S.I., Zhukova N.V., Avramenko I.V., Androsova A.V., Zhukova A.E., Ivanova A.K., Popova N.V. Trastuzumab + FOLFOX6/FLOT v kachestve perioperatsionnoi terapii HER2-pozitivnogo rezektabel'nogo raka zheludka i kardioezofageal'nogo perekhoda: issledovanie RussTrastPrastik (promezhutochnyi analiz). Meditsinskii alfavit. 2020; (38): 46-51. https://doi.org/10.33667/2078-5631-2020-38-46-51.
- Avgustinovich A.V., Afanas'ev S.G., Dobrodeev A.Yu., Volkov M.Yu., Kostromitskii D.N., Spirina L.V., Cheremisina O.V. Neposredstvennaya effektivnost' i toksichnost' total'noi neoad"yuvantnoi khimioterapii rezektabel'nogo raka zheludka. Sibirskii onkologicheskii zhurnal. 2022; 21(1): 11-19. https://doi.org/10.21294/1814-4861-2022-21-1-11-19.
- Baselga J., Norton L., Albanell J., Kim Y.M., Mendelsohn J. Recombinant humanized anti-HER2 antibody (Herceptin) enhances the antitumor activity of paclitaxel and doxorubicin against HER2/neu over-expressing human breast cancer xenografts. Cancer Res. 1998; 58(13): 2825-31.
- Chaika A.V., Gusakova M.S., Khomyakov V.M., Ryabov A.B., Kaprin A.D. Terapiya HER2-polozhitel'nogo raka zheludka - obzor molekulyarno-geneticheskikh osobennostei signal'nogo puti, rezul'tatov klinicheskikh issledovanii. Voprosy onkologii. 2023; 69(1): 45-54. https://doi.org/10.37469/0507-3758-2023-69-1-45-54.
- Nishikawa K., Takahashi T., Takaihi H., Miki A., Noshiro H., Yoshikawa T., Nishida Y., Iwasa S., Miwa H., Masuishi T., Boku N.,Yamada Y., Kodera Y., Yoshida K., Morita S., Sakamoto J., Saji S., Kitagawa Y. Phase II study of the effectiveness and safety of trastuzumab and paclitaxel for taxane- and trastuzumab-na ve patients with HER2-positive, previously treated, advanced, or recurrent gastric cancer (JFMC45-1102). Int J Cancer. 2017; 140(1): 188-196. https://doi.org/10.1002/ijc.30383.
- Zhu Z., Gong Y.B., Xu H.M Neoadjuvant therapy strategies for advanced gastric cancer: Current innovations and future challenges. Chronic Dis Transl Med. https://doi.org/10.1016/j.cdtm.2020.03.004.
- Hofheinz R., Hegewischbecker S., Thusspatience P.C., Kunzmann V., Fuchs M., Graeven U., Homann N., Heinemann V., Pohl M., Tannapfel A., Al-Batran S.E. Trastuzumab in combination with FLOT as perioperative treatment for patients with HER2positive locally advanced esophagogastric adenocarcinoma: a phase II trial of the AIO Gastric Cancer Study Group. J Clin Oncol. 2014; 15: 4073, https://doi.org/10.1200/jco.2014.32.15_suppl.4073.
- Hofheinz R.D., Merx K., Haag G.M., Springfeld C., Ettrich T., Borchert K., Krtzschmar A., Teschendorf C., Siegler G., Ebert M.P., Gotkkurt E., Mahlberg R., Homann N., Pink D., Bechstein W., Reichardt P., Flach H., Gaiser T., Battmann A., Oduncu F.S., Loose M., Sookthai D., Pauligk C., Göetze T.O., Al-Batran S.E. FLOT Versus FLOT/Trastuzumab/ Pertuzumab Perioperative Therapy of Human Epidermal Growth Factor Receptor 2-Positive Resectable Esophagogastric Adenocarcinoma: A Randomized Phase II Trial of the AIO EGA Study Group. J Clin Oncol. 2022 Nov 10; 40(32): 3750-3761. https://doi.org/10.1200/JCO.22.00380.
- Rivera F., Izquierdo-Manuel M., García-Alfonso P., Martínez de Castro E., Gallego J., Limón M.L., Alsina M., López L., Galan M., Falco E., Manzano J.L., González E., Muñoz-Unceta N., Lopez C., Aranda E., Fernandeez E., Jimenez-Foseca P. Perioperative trastuzumab, capecitabine and oxaliplatin in patients with HER2-positive resectable gastric or gastro-oesophageal junction adenocarcinoma: NEOHX phase II trial. Eur J Cancer. 2021 Mar: 145: 158-167. https://doi.org/10.1016/j.ejca.2020.12.005.
- Stark A.P., Ikoma N., Chiang Y.J., Estrella J.S., Das P., Minsky B.D., Blum M.M., Ajani J.A., Mansfield P., Badgwell B.D. Characteristics and Survival of Gastric Cancer Patients with Pathologic Complete Response to Preoperative Therapy. Ann Surg Oncol. 2019; 26(11): 3602-10. https://doi.org/10.1245/s10434-019-07638-8.
- Skoropad V.Yu., Kudryavtsev D.D., Titova L.N., Mozerov S.A., Agababyan T.A., Ivanov S.A., Kaprin A.D. Lechebnyi patomorfoz posle neoad"yuvantnoi khimioluchevoi terapii u bol'nykh mestnorasprostranennym rakom zheludka. Sibirskii onkologicheskii zhurnal. 2020; 19(3): 38-46. https://doi.org/10.21294/1814-4861-2020-19-3-38-46.


