Сочетание стентирования аорты голометаллическим стентом Djumbodis® Dissection System с протезированием восходящей аорты и дуги в хирургическом лечении расслоения I типа
Автор: Комаров Р.Н., Белов Ю.В., Каравайкин Павел Александрович, Соборов М.А.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Хирургия дуги аорты
Статья в выпуске: 4 т.20, 2016 года.
Бесплатный доступ
Цель Показать возможность «открытого» вмешательства на восходящей аорте и дуге в сочетании со стентированием аорты в хирургическом лечении расслоения аорты I типа. Методы В клинике аортальной и сердечно-сосудистой хирургии Первого МГМУ им. И.М. Сеченова (Москва, Россия) выполнена имплантация голометаллического стента Djumbodis® Dissection System (Saint Côme-Chirurgie, Marseille, France) 6 пациентам с расслоением аорты I типа. У 4 пациентов стентированием дуги дополнили протезирование восходящей аорты, у одного пациента - протезирование восходящей аорты и дуги по типу hemiarch и у одного пациента - протезирование аорты и дуги с использованием техники Sun. Результаты Длительность операции, искусственного кровообращения, ишемии миокарда, гипотермического циркуля торного ареста соответствовала длительности стандартной операции при расслоении аорты I типа. В ран нем послеоперационном периоде выявлен один летальный исход (16,7%), связанный с прогрессирующей дыхательной и сердечно-сосудистой недостаточностью, энцефалопатией, желудочно-кишечным кровоте чением на фоне длительной искусственной вентиляции легких. У одного пациента развились острая по чечная недостаточность, острая ишемия левой нижней конечности на фоне тромбоза «ложного» канала аорты; гидроперикард с клиникой тампонады сердца также отмечен у одного пациента. В одном случае обнаружена дыхательная недостаточность, потребовавшая длительной вентиляции легких. Полный тром боз «ложного» канала выявлен у одного пациента, у 4 - частичный тромбоз. У одного пациента тромбоз «ложного» канала не наступил. Выводы Стентирование дуги и нисходящего отдела аорты голометаллическим стентом - альтернатива протезиро- ванию дуги аорты у пациентов с расслоением I типа и способствует стабилизации диаметра «истинного» и «ложного» просветов и аорты в целом.
Аорта, расслоение аорты, стентирование аорты, гибридные технологии, эндоваскулярная хирургия
Короткий адрес: https://sciup.org/142140770
IDR: 142140770 | DOI: 10.21688-1681-3472-2016-4-66-75
Replacement of ascending aorta and aortic arch combined with implantation of bare Stent Djumbodis® dissection system as a treatment of type I aortic dissection
Aim. The aim of this study is to show the outcomes of an open intervention on the ascending aorta and arch combined with stenting of aorta in type I aortic dissection. Methods. Six patients with type I aortic dissection underwent implantation of Djumbodis® Dissection System bare stents at I.M. Sechenov First Moscow Medical University Clinic for Aortic and Cardiovascular Surgery. In 4 patients, aortic stenting was combined with ascending aorta replacement, in 1 patient, hemiarch ascending aorta and arch replacement was performed, and in 1 patient aorta and arch replacement was complemented with a Sun procedure. Results. Total operation time, cardiopulmonary bypass time, cross clamp time and hypothermic circulatory arrest time were just similar to those performed in conventional open surgery. There were no intraoperative deaths in this series. 30-day mortality was 16.7 % (1 patient). The patient died because of progressive respiratory and cardiovascular failure, encephalopathy, and gastrointestinal bleeding. One patient had acute renal failure and left leg ischemia because of the false lumen thrombosis, 1 patient suffered from cardiac tamponade and 1 patient underwent prolonged mechanical ventilation. Total false lumen thrombosis developed in 1 patient, 4 patients had partial false lumen thrombosis, and in 1 patient the false lumen remained patent. Conclusion. Stenting of aortic arch and descending aorta is a good alternative to aortic arch replacement in type I aortic dissection. It promotes stabilization of false and true lumen diameters and global aortic diameter.
Текст научной статьи Сочетание стентирования аорты голометаллическим стентом Djumbodis® Dissection System с протезированием восходящей аорты и дуги в хирургическом лечении расслоения I типа
Хирургия аорты — один из самых интересных, сложных и драматичных вызовов современной сердечно-сосудистой хирургии. Наиболее тяжелый контингент — больные с расслоением аорты I типа по DeBakey M.E. Распространенность заболевания составляет 6 случаев на 100 тыс. населения в год, смертность неоперирован-ных больных достигает 50% в первые 48 ч. Несмотря на тяжесть состояния, все пациенты с расслоением аорты I типа должны быть оперированы в срочном порядке (класс рекомендаций I). Операция позволяет снизить смертность в течение первого месяца, по сравнению с консервативным лечением, с 90 до 30% [1].
Первостепенной задачей хирурга является ликвидация опасности разрыва аорты в восходящем отделе — протезирование восходящей аорты с восстановлением

Статья доступна по лицензии Creative Commons Attribution 4.0.
целостности аортального клапана или его протезированием. На второй план отходит проблема расслоения в дуге и нисходящем отделе аорты с сохранением перфузии «истинного» и «ложного» просветов. После первичного вмешательства «ложный» канал остается проходимым у 78% пациентов [2]. Впоследствии проходимый «ложный» канал аорты способствует ее аневризматической трансформации на уровне дуги и нисходящего отдела у 15–40% больных в течение 5 лет [3].
В связи с этим у пациентов с расслоением I типа, особенно с фенестрацией на уровне дуги, вмешательство расширяют до протезирования восходящего отдела и дуги. Со временем нисходящая аорта расширится — повторная операция потребуется в 7–24% случаев [4]. Изящное решение проблемы повторного вмешательства нашел Borst H.G. в 1982 г.: процедура «хобот слона», усовершенствованная Svensson L.G. [5].
С развитием эндоваскулярных и гибридных технологий стало возможно выполнять вмешательство одноэ-тапно: дополнить протезирование восходящей аорты и дуги открытой установкой стент-графта в нисходящую аорту — технология, примененная Karck M. в 2001 г. и названная «замороженным хоботом слона» [5]. При этом в большом числе случаев одномоментно удается выключить из кровотока всю аневризматически расширенную аорту.
Технология «замороженного хобота слона» подкупает радикальностью, однако требует протезирования дуги, длительного искусственного кровообращения, гипотермического циркуляторного ареста. Для ликвидации «ложного» просвета аорты на уровне дуги без ее протезирования Roux D. и соавт. в 2001 г. предложили гибридное вмешательство: протезирование восходящей аорты и «открытое» стентирование дуги и начальных отделов нисходящей аорты голометаллическим стентом с сохранением перфузии брахиоцефальных артерий. У обоих пациентов расслоение заканчивалось на уровне дуги, и удалось добиться полной облитерации «ложного» просвета после стентирования [6].
Цель исследования: демонстрация первого опыта сочетания стентирования дуги и начального отдела нисходящей аорты с протезированием восходящей аорты и дуги у пациентов с расслоением аорты I типа.
Методы
С ноября 2013 г. по апрель 2016 г. в клинике аортальной и сердечно-сосудистой хирургии Первого МГМУ им. И.М. Сеченова оперировано 6 пациентов с рассло-
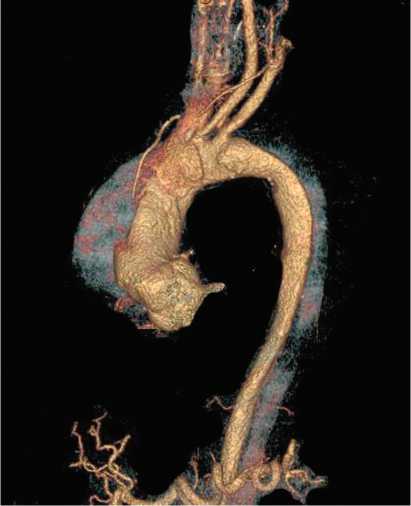
Рис. 1. Мультиспиральная компьютерная томография пациента с расслоением I типа перед оперативным вмешательством
Fig. 1. Preoperative multislice computer tomography in patient with type I dissection ением аорты I типа, которым имплантирован голометаллический стент Djumbodis® Dissection System (Saint Come-Chirurgie, Marseille, France).
Пациенты оперированы в острую, подострую и хроническую фазы расслоения. У всех пациентов диагноз расслоения подтвержден данными мультиспиральной компьютерной томографии (МСКТ) аорты с контрастированием (рис. 1). Также выполняли эхокардиографию для диагностики состояния аортального клапана и сократительной способности миокарда, пациентам с хроническим расслоением проводили коронароангиографию, у одного пациента выявлена ишемическая болезнь сердца.
У всех пациентов выполняли вмешательство через полную продольную срединную стернотомию. Подключение аппарата искусственного кровообращения у 5 больных производилось стандартно по схеме «правое предсердие – правая подмышечная артерия», у одного пациента с расслоением брахиоцефального ствола и правой общей сонной артерии аппарат искусственного кровообращения подключен по схеме «правое предсердие – левая общая бедренная артерия». После начала искусственного крово-
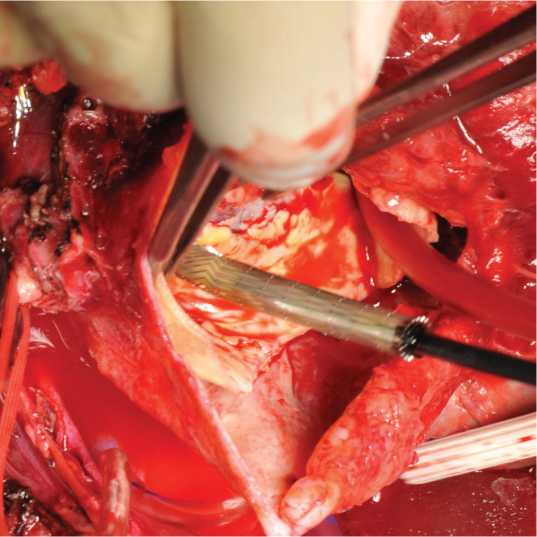
Рис. 2. Имплантация голометаллического стента в дугу аорты: A — доставляющее устройство; B — положение стента в просвете дуги аорты. Состоятельность аортального клапана контролировали посредством чреспищеводной эхокардиографии Fig. 2. Implantation of bare-metal stent into the aortic arch: ( A) guide wire; ( B) stent position in the aortic arch lumen. Aortic valve consistency was controlled by transesophageal echocardiography
B
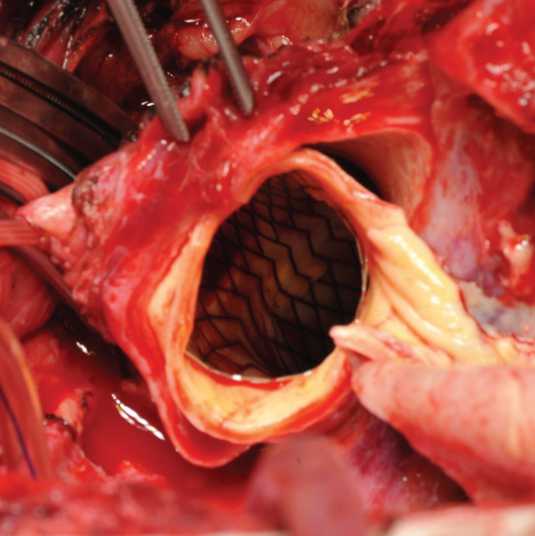
обращения пациентов охлаждали до 25–28 °C. Пациенту с расслоением брахиоцефального ствола и правой общей сонной артерии наложен анастомоз бифуркации сонной артерии и синтетического протеза диаметром 8 мм, протез канюлирован отводкой от артериальной магистрали для антеградной перфузии головного мозга. Выполнялась селективная антеградная фармакохолодовая кардиоплегия раствором «Кустодиол». На этапе охлаждения проводили ревизию аортального клапана. В 5 случаях выполнена пластика корня аорты по типу «сэндвич», у одного больного реимплантирован корень аорты в протез по методике David. По достижении умеренной гипотермии начинались циркуляторный арест внутренних органов, антеградная перфузия головного мозга: в одном случае бигемисфераль-ная, в 5 случаях моногемисферальная. 4 пациентам имплантировали голометаллический стент Djumbodis® Dissection System 9 см в дугу аорты с переходом на перешеек и нисходящий отдел (рис. 2) и осуществили протезирование восходящей аорты с гемодинамической коррекцией I типа с наложением «открытого дистального анастомоза» у одного пациента и на пережатой дуге аорты у 3 пациентов. Одному пациенту имплантировали стент в дугу с переходом на перешеек и нисходящую аорту и выполнили протезирование дуги по типу «скошенного анастомоза». Одному пациенту стент имплантирован в перешеек и начальный отдел нисходящей аорты, выполнено протезирование дуги аорты многобраншевым протезом с использованием техники Sun. Раскрываемость стента контролировали визуально и пальпаторно. Проксимальный анастомоз протеза с корнем аорты выполняли на этапе согревания больного. Больному с расслоением брахиоцефального ствола и правой общей сонной артерии наложен проксимальный анастомоз протеза внутренней сонной артерии с протезом восходящей аорты; одному пациенту выполнено аутовенозное шунтирование передней межжелудочковой артерии.
Результаты
Интраоперационной летальности у пациентов с имплантацией голометаллического стента не было. Длительность искусственного кровообращения, ишемии миокарда, циркуляторного ареста сопоставимы с таковыми у пациентов со стандартными вмешательствами при расслоении аорты I типа.
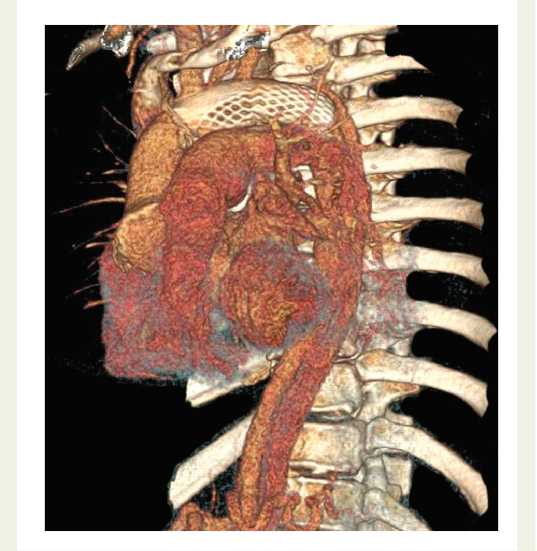
Рис. 3. Мультиспиральная компьютерная томография после хирургического лечения: частичный тромбоз «ложного» канала
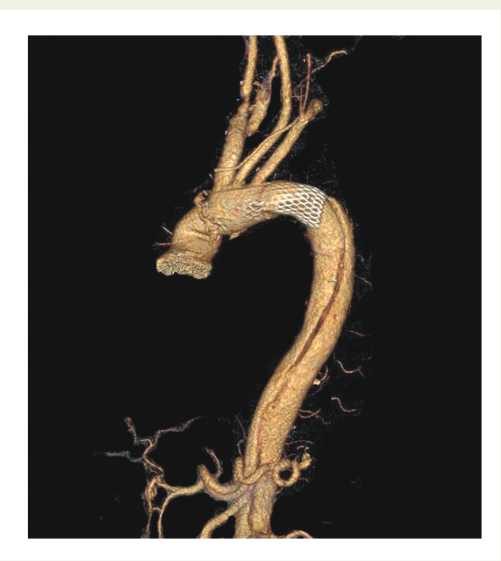
Рис. 4. Мультиспиральная компьютерная томография через 6 мес. после оперативного вмешательства: сохраняется перфузия «ложного» канала нисходящей аорты
-
Fig. 3. Postoperative multislice computer tomography: partial thrombosis of a false lumen
-
Fig. 4. Multislice computer tomography 6 months after intervention: there is perfusion of a false lumen of the descending aorta
В раннем послеоперационном периоде наблюдали один летальный исход на 28-е сут. после операции в результате прогрессирующей дыхательной, сердечно-сосудистой недостаточности, длительной искусственной вентиляции легких на фоне вентилятор-ассоциирован-ной пневмонии, энцефалопатии, желудочно-кишечного кровотечения.
У одного пациента на 3-и сут. после операции развились острая почечная недостаточность с анурией, острая ишемия левой нижней конечности I ст. Выявлено, что обе почечные артерии, чревный ствол отходят от частично тромбированного «ложного» канала аорты, левая общая подвздошная артерия тромбирована. По экстренным показаниям выполнены аорто-бедренное бифуркационное протезирование и интимэктомия на уровне висцеральных артерий. В раннем послеоперационном периоде полностью купировали ишемию почек, левой нижней конечности.
У одного больного в послеоперационном периоде развилась клиника тампонады сердца, потребовавшая неотложной пункции полости перикарда.
У одного пациента после циркуляторного ареста развился гипокоагуляционный синдром, потребовавший длительных искусственного кровообращения и, как следствие, послеоперационной искусственной вентиляции легких на фоне SIRS-синдрома и вентилятор-ассоциированной пневмонии.
Полный тромбоз «ложного» канала аорты в послеоперационном периоде развился у одного пациента, у которого расслоение заканчивалось на уровне перешейка аорты, у 4 пациентов развился частичный тромбоз «ложного» канала на уровне стентирования (рис. 3), у одного пациента тромбоз «ложного» канала не произошел.
Период наблюдения пациентов составил от 1 до 26 мес. По данным контрольной МСКТ диаметр аорты не увеличился, полного тромбоза «ложного» канала не отмечено ни у одного пациента (рис. 4).
стика вмешательств
|
О “ 0) и о а о £ " § Ф Z СО < и S |
||||||||||
|
с |
У 0 CD |
5 о и 1 |
Z с |
5 Z |
5 Z Z |
ZT |
0 |
0 О |
ГО 2 0 0 ю ж 5 2 5 1— « |
|
|
1 |
44 |
Остр. |
ПВА |
МГ |
105 |
68 |
8 |
5 |
ОПН, ОИНК |
Частичный |
|
2 |
53 |
160 |
70 |
34 |
4 |
– |
||||
|
3 |
67 |
ПВА, Sun |
БГ |
155 |
30 |
28 |
ДН, ССН, ЖКК |
Полный |
||
|
4 |
66 |
Хр. |
ПВА, СА, АКШ ПМЖА |
МГ |
298 |
95 |
43 |
27 |
ДН |
Частичный |
|
5 |
55 |
Подостр. |
ПВА, АСП |
128 |
50 |
3 |
2 |
– |
||
|
6 |
38 |
David |
185 |
145 |
5 |
10 |
Тампонада |
Нет |
||
|
Ср. |
53,8±11,6 |
– |
– |
– |
171,8±67,7 |
87,2±33,2 |
20,5±17,2 |
12,8±11,8 |
– |
– |
Примечание. Ср. — средний показатель; Остр. — острая; Подостр. — подострая; Хр. — хроническая; ПВА — супракоро-нарное протезирование восходящей аорты; Sun — протезирование дуги аорты с использованием техники Sun; СА — протезирование дуги по типу скошенного анастомоза; АКШ ПМЖА — аортокоронарное шунтирование передней межжелудочковой артерии; АСП — асцендо-сонное протезирование; David — реимплантация корня аорты в протез по методике David; ИК — искусственное кровообращение; ИМ — ишемия миокарда; ЦА — циркуляторный арест; ОРИТ — отделение реанимации и интенсивной терапии; ОПН — острая почечная недостаточность; ОИНК — острая ишемия левой нижней конечности; ДН — дыхательная недостаточность; ССН — сердечно-сосудистая недостаточность; ЖКК — желудочно-кишечное кровотечение; ГМ — головной мозг, МГ — моногемисферальная; БГ — бигемисферальная
В табл. 1 представлена характеристика выполненных вмешательств.
Обсуждение
Применение голометаллических стентов в аортальной позиции ограничено. Стентирование аорты используют в лечении коарктации [7], при пристеночных тромбах восходящей и дуги аорты [8], подтеканиях I типа для фиксации края стент-графта к аортальной стенке [9], сдавления «ложного» канала дуги и нисходящей аорты при расслоениях I типа, а также для сдавления «ложного» канала на уровне висцеральных артерий при расслоениях III типа, включая технологию PETTICOAT [9]. Аортальные стенты могут быть самораскрывающимися и баллон-раскрывае-мыми [9]. Наибольшую распространенность получил бал-лон-раскрываемый голометаллический стент Djumbodis® Dissection System, специально сконструированный для хирургического лечения расслоения аорты на уровне отхождения крупных ветвей: брахиоцефальных артерий от дуги, висцеральных артерий от брюшной аорты.
Экспериментальное исследование стентирования аорты начато еще в 1985 г. [10]. С 2000-х гг. в литературе появились описания единичных клинических случаев дополнения открытого вмешательства при расслоении аорты имплантацией голометаллического стента Djumbodis®
Dissection System для ликвидации «ложного» просвета [11–15].
Помимо возможности открытой установки стент Djumbodis® Dissection System имеет доставляющее устройство для эндоваскулярной имплантации и может быть использован для дополнительного раскрытия «истинного» и сдавления «ложного» каналов аорты после открытого этапа хирургического лечения, что показали Iannelli G. и соавт. После установки стента в дугу для полной ликвидации «ложного» просвета авторы имплантировали стент-графты дистальнее стента двум из трех больных [16]. Mastroroberto P. и соавт. для раскрытия «истинного» канала нисходящей аорты использовали не стент-графты, а голометаллические стенты с заходом на уровень отхождения висцеральных артерий с полной облитерацией «ложного» канала [17].
Guerra F. и соавт. показали использование стента при повторных вмешательствах у пациентов, ранее перенесших супракоронарное протезирование восходящей аорты при расслоении аорты I типа. По поводу аневризмы корня аорты троим больным выполнена операция Bentall-De Bono, одному — операция David, всем четверым имплантирован стент в дугу для ее стабилизации. В послеоперационном периоде «ложный» канал полностью облитерировал- ся на уровне дуги у всех пациентов. У двоих сохранился «ложный» канал в нисходящем отделе аорты [18].
Опубликованы пять серий, демонстрирующих применение голометаллического стента при расслоении аорты I типа.
Touati G.D. и соавт. на примере 29 пациентов описали технику нормотермического протезирования дуги аорты с применением двунаправленной перфузии головного мозга и внутренних органов. При этом нисходящая аорта, как правило, окклюзировалась аортальным баллоном, в том числе баллоном доставляющего устройства стента Djumbodis® Dissection System. 15 пациентам с расслоением I типа в дугу и нисходящую аорту имплантирован голометаллический стент. Операционная летальность составила 13,3%, при этом не отмечено послеоперационных осложнений. У 12 из 13 пациентов в отдаленном периоде отмечена полная облитерация «ложного» просвета, у 1 — частичный тромбоз [19].
Leobon B. и соавт. продемонстрировали применение голометаллического стента в двух клиниках Пармы и Тулузы с 2000 по 2005 г. Оперировано 22 пациента. Получена достоверно меньшая проходимость «ложного» канала у паци- ентов группы стентирования, при этом лучших результатов удалось достичь в лечении острых расслоений [20].
Ius F. и соавт. сравнили результаты хирургического лечения 28 пациентов с расслоением I типа, которым был имплантирован стент в дугу аорты, и 22, которым не был. Всем пациентам выполнено протезирование восходящей аорты, в половине случаев также потребовалось протезирование дуги по типу hemiarch. Статистически значимого различия в длительности операции, летальности или осложнениях операций не выявлено. Также по причине фенестрации дистальнее стента не обнаружено различия в проходимости «ложного» канала в нисходящей аорте. Однако почти у всех пациентов с расслоением, заканчивающимся на уровне дуги аорты, «ложный» канал был облитерирован [2].
Czerny M. и соавт., выполнив протезирование восходящей аорты и дуги по типу hemiarch с имплантацией голометаллического стента в дугу и нисходящую аорту у 15 пациентов, отмечают недостаточную эффективность в облитерации «ложного» просвета и сохранение его перфузии в большинстве случаев [21].
Caus T. и соавт. наблюдали «ложный» канал аорты у 15 пациентов после установки стента в дугу и прокси-
Таблица 2 Опыт применения голометаллического стента при расслоении аорты I типа
|
гага КХ 5 КХ гг _^ _^ со 5 х га х —г А . _ . _ —г А . _ . Автор Год 1 i i Ц У Me pll ОфО i га zf Ф ° < га га Ю < га Ф ' |
|
Jazayeri S. [14] |
2003 |
2 |
0 |
н/д |
н/д |
н/д |
н/д |
7–12 мес. |
2 |
0 |
||
|
Guerra F. [18] |
4 |
0 |
0 |
0 |
0 |
6–12 мес. |
0 |
2 (50) |
2 (50) |
0 |
||
|
Dias R.R. [11] |
1 |
6 мес. |
1 |
0 |
||||||||
|
L e obon B. [20] |
2007 |
22 |
5 (22,7) |
7 (35) |
1 (4,5) |
3 (15) |
0 |
ср. 278 дней |
1 (5,9) |
10 (58,8) |
2 (11,8) |
н/д |
|
Touati G.D. [19] |
15 |
2 (13,3) |
0 |
0 |
0 |
21,6±9 |
0 |
12 (92,3) |
1 (7,7) |
0 |
||
|
Di Stefano S. [12] |
2008 |
1 |
0 |
10 мес. |
0 |
1 |
||||||
|
Ius F. [2] |
2010 |
28 |
2 (7) |
6 (21) |
1 (4) |
1 (4) |
5 (18) |
24±7 мес. |
5 (19,2) |
10 (52,6) |
1 (5,4) |
2 (7,1) |
|
Cirillo P. [24]* |
1 |
6 мес. |
1** |
0 |
||||||||
|
2011 |
0 |
0 |
0 |
0 |
0 |
0 |
||||||
|
Iannelli G. [16]* |
3 |
12 мес. |
0 |
3** |
0 |
|||||||
|
Czerny M. [21] |
2012 |
15 |
3 (20) |
н/д |
н/д |
н/д |
н/д |
ср. 37 мес. |
1 (8) |
3 (25) |
2 (17) |
|
|
Caus T. [22] |
2013 |
19 |
4 (21) |
ср. 42 мес. |
3 (20) |
3 (15,8) |
н/д |
2 (10,5) |
||||
|
Чернявский А.М. [3] |
2015 |
17 |
2 (11,8) |
1 (4,3) |
0 |
24,2±6,2 |
1 (6,7) |
0 |
10 (71,4) |
0 |
||
|
Настоящее исследование |
2016 |
6 |
1 (16,7) |
1 (16,7) |
0 |
0 |
1 (16,7) |
1–26 мес. |
0 |
1 (16,7) |
4 (66,7) |
1 (16,7) |
Примечание. * — установка стента эндоваскулярно после «открытого» этапа; ** — полная облитерация достигнута после имплантации стент-графта дистальнее; ОПН — острая почечная недостаточность, ОНМК — острое нарушение мозгового кровообращения
мальную часть нисходящей аорты. Отмечены достоверно меньший средний индексированный диаметр «ложного» канала после имплантации стента и стабилизация общего диаметра аорты по сравнению с пациентами без стентирования. При этом «ложный» канал тромбировался, как правило, на уровне имплантации стента, дистальнее перфузировался [22].
Чернявский А.М. и соавт., сравнивая результаты лечения 17 пациентов после протезирования восходящей аорты или восходящей аорты и дуги с имплантацией голометаллического стента в дугу или нисходящую аорту с результатами «открытых» вмешательств у 124 пациентов, не обнаружили достоверного увеличения времени операции, искусственного кровообращения и циркуляторного ареста [3]. Сводные данные литературы представлены в табл. 2.
Имплантация голометаллического стента отличается от установки стент-графта. Цель имплантации стента — расширить «истинный» канал аорты с полной ликвидацией «ложного» и сохранить перфузию ветвей, отходящих на уровне имплантации.
При имплантации голометаллического стента в дугу аорты ее не нужно протезировать: создается опорный каркас для дуги, сдавливается «ложный» просвет вплоть до полной облитерации, стабилизируется общий диаметр дуги за счет уменьшения перфузии «ложного» просвета и значительно уменьшается вероятность аневризматической трансформации дуги [2, 23]. Однако при имплантации баллон-раскрываемого стента следует избегать чрезмерного давления, особенно у пациентов с острым расслоением аорты, для предотвращения разрыва интимы или всей стенки аорты [23]. Также разрыв интимы может произойти из-за контакта с острыми краями стента [2, 21, 23]. Чтобы этого избежать, при проведении устройства рекомендуется использовать специальную защитную оболочку [23]. Также нежелательно недораскрытие стента, приводящее к неэффективному сдавлению «ложного» просвета. Для контроля раскрытия рекомендуют применять пальпацию, рентгено- и эндоскопический контроль [3, 14, 15, 23].
Установка покрытого стент-графта в «истинный» канал аорты способствует его расширению и сдавлению «ложного» канала, а также перекрывает фенестрацию в зоне имплантации, однако отмечают недостаточные радиальные силы самораскрываемого графта для полного сдавления «ложного» просвета и сохранение риска аневризматической трансформации аорты. Также для эндопротезирования аорты на уровне дуги требуется предварительный дебранчинг — переключение ветвей дуги в более проксимальные участки аорты [20].
Ячеистая структура стента позволяет беспрепятственно устанавливать его в дугу аорты и на уровне висцеральных артерий в брюшную аорту, при этом предотвращается динамическая окклюзия устьев артерий из-за перераспределения кровотока в «истинный» канал, а также сохраняется коллатеральное кровообращение по более мелким ветвям аорты, которые не перекрываются [3, 20, 23, 24].
Баллон-раскрываемый стент критикуют за ригидность и фиксированный диаметр после раздувания баллона. Таким образом, стент не адаптируется к систоло-диастолическому изменению диаметра эластичной аорты, появляются предпосылки для сохранения перфузии «ложного» канала [21]. Также возможны дальнейшее увеличение диаметра аорты и перерастание диаметра стента [2]. Чтобы этого избежать, имплантируют более длинное устройство или нескольких устройств [9].
Wong R.H.L. и соавт. сообщили о деформации и переломе баллон-раскрываемого стента в отдаленном периоде после имплантации 3 из 7 пациентов [25]. Однако ни в нашей серии, ни в литературе подобных осложнений более не встречалось.
Выводы
-
1. Имплантация голометаллического стента, в частности Djumbodis® Dissection System, дополняющая протезирование восходящей аорты или дуги по типу hemiarch у пациентов с расслоением аорты I типа, альтернативная полному протезированию дуги аорты и технически более простая процедура.
-
2. Имплантация голометаллического стента в дугу или нисходящую аорту способствует стабилизации диаметра аорты, предотвращает ее аневризматическую трансформацию.
-
3. Имплантация голометаллического стента не увеличивает время и сложность операции и является относительно безопасной при соблюдении технологии имплантации.
-
4. Для оценки отдаленных результатов и сравнения с классическими тактиками лечения пациентов с расслоением I типа необходим опыт применения голометаллических стентов аорты.
Финансирование
Исследование не имело спонсорской поддержки.
Список литературы Сочетание стентирования аорты голометаллическим стентом Djumbodis® Dissection System с протезированием восходящей аорты и дуги в хирургическом лечении расслоения I типа
- Erbel R., Aboyans V., Boileau C., Bossone E., Bartolomeo R.D., Eggebrecht H., Evangelista A., Falk V., Frank H., Gaemperli O., Grabenwöger M., Haverich A., Iung B., Manolis A.J., Meijboom F., Nienaber C.A., Roffi M.,.. ESC Committee for Practice Guidelines. 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases: Document covering acute and chronic aortic diseases of the thoracic and abdominal aorta of the adult. The Task Force for the Diagnosis and Treatment of Aortic Diseases of the European Society of Cardiology (ESC)//Eur. Heart J. 2014. Vol. 35. No. 41. P. 2873-2926. http://dx.doi. org/10.1093/eurheartj/ehu281
- Ius F., Vendramin I., Mazzaro E., Piccoli G., Bassi F., Gasparini D., Livi U. Transluminal stenting in type A acute aortic dissection: Does the djumbodis system have any impact on false lumen evolution?//Ann. Thorac. Surg. 2010. Vol. 90. No. 5. P. 1450-1456. http://dx.doi. org/10.1016/j.athoracsur.2010.06.087
- Чернявский А.М., Альсов С.А., Ляшенко М.М., Сирота Д.А., Хван Д.С. Гибридные вмешательства в хирургии проксимальных расслоений аорты//Медицинский альманах. 2015. № 3. С. 40-43.
- Detter C., Mair H., Klein H.G., Georgescu C., Welz A., Reichart B. Longterm prognosis of surgically-treated aortic aneurysms and dissections in patients with and without Marfan syndrome//Eur. J. Cardiothorac. Surg. 1998. Vol. 13. No. 4. P. 416^23.
- Borst H.G. The birth of the elephant trunk technique//J. Thorac. Cardiovasc. Surg. 2013. Vol. 145. No. 1. P. 44. http://dx.doi.org/10.1016/j. jtcvs.2012.10.002
- Roux D., Brouchet L., Concina P., Elghobary T., Glock Y., Fournial G. Type-A acute aortic dissection: combined operation plus stent management//Ann. Thorac. Surg. 2002. Vol. 73. No. 5. P. 1616-1618. http://dx.doi.o DOI: rg/10.1016/S0003-4975(01)03463-4
- Forbes T.J., Gowda S.T. Intravascular stent therapy for coarctation of the aorta//Methodist DeBakey Cardiovasc. J. 2014. Vol. 10. No. 2. P. 82-87. http://dx.doi.o DOI: rg/10.14797/mdcj-10-2-82
- Mahnken A.H., Hoffman A., Autschbach R., Damberg A.L.M. Bare metal stenting for endovascular exclusion of aortic arch thrombi//Cardiovasc. Intervent. Radiol. 2013. Vol. 36. No. 4. P. 1127-1131. http://dx.doi. org/10.1007/s00270-013-0566-6
- Ius F., Livi U. Is bare-metal stenting a worthwhile adjunctive technique in acute type A dissection?//Bonser R.S., Pagano D., Haverich A., Mascaro J., editors. Controversies in Aortic Dissection and Aneurysmal Disease. London: Springer, 2014. P. 297-308.
- Charnsangavej C., Wallace S., Wright K.C., Carrasco C.H., Gianturco C. Endovascular stent for use in aortic dissection: an in vitro experiment//Radiology. 1985. Vol. 157. No. 2. P. 323-324. http://dx.doi.org/10.1148/ href='contents.asp?titleid=22763' title='Radiology'>Radiology.157.2.4048439
- Dias R.R., Silva I.A., Fiorelli A.I., Stolf N.A.G. New surgical strategy for acute type A aortic dissection: hybrid procedure//Rev. Bras. Cir. Cardiovasc. 2007. Vol. 22. No. 4. P. 495^97. http://dx.doi.org/10.1590/S0102-76382007000400018
- Di Stefano S., Lôpez J., Flôrez S., Bustamante J., San Roman A. Combined surgical treatment in aortic type A dissection//J. Card. Surg. 2008. Vol. 24. No. 4. P. 440^42. http://dx.doi.o8191.2008.00737.x DOI: rg/10.1111/j.1540-
- Jazayeri S., Tatou E., Gomez M.C., Bouchot O., Saleh M., Brenot R., David M. Combined treatment of aortic type A dissection: Ascending aorta repair and placement of a stent in the descending aorta//Heart Surg. Forum. 2003. Vol. 6. No. 5. P. 387-389.
- Saccani S., Nicolini F., Borrello B., Agostinelli A., Larini P., Marcato C., Gherli T. New technologies for the treatment of type A aortic dissection: a case report//J. Thorac. Cardiovasc. Surg. 2004. Vol. 127. No. 6. P. 1821-1823. http://dx.doi.o DOI: rg/10.1016/j.jtcvs.2004.01.020
- Saccani S., Busi M., Fragnito C., Agostinelli A., Borrello B., Nicolini F., Gherli T. Surgical repair and stent positioning for type A acute aortic dissection: A step forward?//Ann. Thorac. Surg. 2005. Vol. 79. No. 5. P. 1761-1763. http://dx.doi.o DOI: rg/10.1016/j.athoracsur.2003.10.036
- Iannelli G., Di Tommaso L., Cirillo P., Smimmo R., Piscione F., Vosa C. Treatment of residual type A aortic dissection with implantation of the Djumbodis system: is purely endovascular treatment becoming a reality?//J. Endovasc. Ther. 2011. Vol. 18. No. 3. P. 368-373. http://dx.doi.o DOI: rg/10.1583/11-3397.1
- Mastroroberto P., Chello M., Jannelli G., Covino E. Uncovered stentgraft in the treatment for residual patent false lumen after surgical repair for acute type A aortic dissection//Interact. Cardiovasc. Thorac. Surg. 2011. Vol. 12. No. 2. P. 202-204. http://dx.doi.org/10.1510/icvts.2010.256446
- Guerra F., Calabrese L., Khlat B., Casati V. Aortic arch stabilization in redo operations for aortic type A dissection//J. Cardiovasc. Med. Hagerstown Md. 2007. Vol. 8. No. 5. P. 384-386. http://dx.doi. org/10.2459/01.JCM.0000268121.05801.b2
- Touati G.D., Marticho P., Farag M., Carmi D., Szymanski C., Barry M., Trojette F., Caus T. Totally normothermic aortic arch replacement without circulatory arrest//Eur. J. Cardiothorac. Surg. 2007. Vol. 32. No. 2. P. 263-268. http://dx.doi.o DOI: rg/10.1016/j.ejcts.2007.04.035
- Léobon B., Roux D., Saccani S., Glock Y., Fournial G. Chirurgie combinée des dissections aiguës de type A, par remplacement de l’aorte ascendante et endoprothèse non couverte//Arch. Mal. Coeur Vaiss. 2007. Vol. 100. No. 9. P. 753-759.
- Czerny M., Stöhra S., Aymard T., Sodeck G.H., Ehrlich M., Dziodzio T., Juraszek A., Carrel T. Effect on false-lumen status of a combined vascular and endovascular approach for the treatment of acute type A aortic dissection//Eur. J. Cardiothorac. Surg. 2012. Vol. 41. No. 2. P. 409-413. http://dx.doi.o DOI: rg/10.1016/j.ejcts.2011.05.063
- Каус Т., Хуберт-Янссен А., Губерт Д.И., Пиккардо А., Пети А., Пулен Г. Первый опыт применения системы Джумбодис: результаты и перспективы. Часть 1//Ангиология и сосудистая хирургия. 2013. Т. 19. № 4. С. 61-74.
- Каус Т., Хуберт-Янссен А., Губерт Д.И., Пиккардо А., Пети А., Пулен Г. Первый опыт применения системы Джумбодис: результаты и перспективы. Часть 2//Ангиология и сосудистая хирургия. 2014. Т. 20. № 1. С. 61-73.
- Cirillo P., Iannelli G., Piscione F. Endovascular treatment of residual type A aortic dissection preserving patency of supra-aortic vessels by implantation of the Djumbodis® system. No more surgery for the aortic arch?//J. Invasive Cardiol. 2011. Vol. 23. No. 11. P. E251-253.
- Wong R.H.L., Yu S.C.H., Lau R.W.H., Ng C.S.H., Hui J.W.Y., Wan I.Y.P., Wan S., Ho A.M.H., Underwood M.J. Delayed stent deformity and fracture of Djumbodis dissection system//Ann. Thorac. Surg. 2014. Vol. 97. No. 1. P. e17-20. http://dx.doi.o DOI: rg/10.1016/j.athoracsur.2013.07.127


