Содержание диеновых конъюгатов и оснований шиффа в мицелии гриба Neonothopanus nambi при разных уровнях его свечения в условиях стресса
Автор: Тюлькова Н.А., Бондарь В.С.
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Агрономия
Статья в выпуске: 3, 2019 года.
Бесплатный доступ
Исследовано соотношение интенсивности световой эмиссии мицелия Neonothopanus nambi в условиях стресса и содержания в био- массе гриба первичных и конечных продуктов перекисного окисления липидов (ПОЛ) - диено- вых конъюгатов (ДК) и оснований Шиффа (ОШ). С этой целью образцы механически по- врежденного мицелия инкубировали в пита- тельной картофельно-сахарозной среде без каких-либо добавок (контроль) и в условиях воздействия дополнительных стрессовых факторов (опыт): добавка в среду ингибитора грибного свечения (салициловая кислота (СК) в концентрации 0,5 мМ), закисления среды до рН 5,0 и 4,0 добавками уксусной кислоты. Со- держание изучаемых продуктов ПОЛ оценива- ли в биомассе контрольных и опытных образ- цов мицелия через 4 ч инкубации (регистри- руемый максимум интенсивности грибного свечения). ДК из биомассы мицелия экстраги- ровали смесью растворителей гептан- изопропанол с последующим разделением фаз. Содержание ДК в фазе гептана и фазе изопро- панола, отражающее интенсивность перекис- ного окисления в грибе нейтральных липидов и фосфолипидов соответственно, определяли спектрофотометрически по величине опти- ческой плотности образцов при длине волны 232 нм...
Светящиеся грибы, диеновые конъюгаты, основания шиффа, активные формы кислорода
Короткий адрес: https://sciup.org/140243399
IDR: 140243399 | УДК: 577.334
The content of dien conjugates and shiff bases in Neonothopanus nambi myccelium at different levels of its luminescence in stress conditions
The ratio of the intensity of light emission from Neonothopanus nambi mycelium under stress and content in the biomass of the fungus of primary and final products of lipid peroxidation (PLP) - diene conjugates (DC) and Schiff bases (SB) was stud- ied. For this purpose the samples of mechanically damaged mycelium was incubated in nutrient pota- to and saccharose medium without any additives (control) and in the conditions of influence of addi- tional stressful factors (experience): an additive on the medium of inhibitor of a mushroom lumines- cence (salicylic acid (SA) in concentration of 0.5 mm), acidulations of the environment to pH 5.0 and4.0 additives of acetic acid. The content of studied PLP was evaluated in biomass of control and test samples of mycelium after 4 hours of incubation (registering maximum intensity of fungal lumines- cence). DC from biomass of a mycelium extracted by the mix of solvents heptane - isopropanol with subsequent division of phases. DC content in hep- tane phase and isopropanol phase, reflecting the intensity of peroxidation in the fungus of neutral lipids and phospholipids, respectively, was deter- mined spectrophotometrically using optical density of the samples at 232 nm...
Текст научной статьи Содержание диеновых конъюгатов и оснований шиффа в мицелии гриба Neonothopanus nambi при разных уровнях его свечения в условиях стресса
Введение. Исследования светоизлучающих высших грибов Neonothopanus nambi и Armillaria borealis позволили нам составить представление о защитной функции грибного свечения от негативного воздействия активных форм кислорода (АФК) [1–7]. Известно, что в биологических объектах постоянно происходят жизненно важные реакции свободнорадикального окисления (СРО), скорость которых поддерживается на определенном уровне. Строгая регламентация реакций СРО в биообъектах обеспечивается согласованным функционированием ферментативных и неферментативных механизмов, контролирующих уровень АФК, свободных радикалов и молекулярных продуктов окисления с их участием [8–11]. Так как одним из основных видов свободнорадикальных процессов, происходящих в живых объектах, является перекисное окисление липидов (ПОЛ), в недавних работах мы исследовали некоторые аспекты взаимосвязи ПОЛ с интенсивностью грибного свечения [6, 7]. В этих работах в условиях острого эксперимента нами было установлено, что у механически поврежденного мицелия N. nambi наблюдается значительное (на 2 порядка и более) увеличение уровня световой эмиссии. В то же время было показано, что концентрация конечного продукта ПОЛ – малонового диальдегида повышалась в мицелии только в первые часы после его механической травмы и снижалась в период максимального свечения [6]. При этом возрастание интенсивности световой эмиссии мицелия отмечалось на фоне значительного снижения в нем активности СОД и общей пероксидазной активности при незначительном повышении активности каталазы. Совокупность этих данных позволила высказать предположение, что свечение высших грибов, по-видимому, является дополнительным механизмом их защиты от повреждающего действия активных радикалов кислорода. Вероятно, в ходе реакции светоизлучения нейтрализуется избыток АФК, пул которых в грибе может значительно возрастать в условиях стресса, особенно на начальных стадиях его развития, например сразу после механического повреждения мицелия. В этих условиях нейтрализация избытка АФК за счет реакции светоизлучения будет препятствовать развитию ПОЛ или снижать вероятность его возникновения [6].
Хорошо известно, что ПОЛ – это сложный многостадийный процесс, в котором происходит образование и деградация липидных радикалов, что сопровождается формированием целого ряда молекулярных соединений: спирты, кетоны, альдегиды, эфиры и т. д. Среди продуктов ПОЛ выделяют первичные (диеновые конъюгаты), промежуточные (кетоны, альдегиды) и конечные (диальдегиды), которые образуют флуоресцирующие конъюгаты типа оснований Шиффа, различающиеся устойчивостью и биологической активностью. Исходя из предположения о защитной роли свечения грибов от повреждающего действия активных радикалов, важным являлось изучение содержания первичных и конечных продуктов ПОЛ в грибном мицелии в сравнении с уровнем его световой эмиссии в стрессовых условиях.
Цель исследования : изучение содержания диеновых конъюгатов и оснований Шиффа при разных уровнях свечения мицелия гриба Neonothopanus nambi в условиях стресса.
Материалы и методы исследования. В исследовании использовали образцы мицелия гриба N. nambi IBSO 3293 из Коллекции микроорганизмов (CCIBSO 836) ИБФ СО РАН, выращенные на жидкой питательной картофельно-сахарозной среде по разработанной нами ранее технологии [1]. Для экспериментов из полученного пленочного мицелия высекали диски диаметром 12 мм, которые помещали в свежую питательную картофельно-сахарозную среду (рН 6,2). Контрольные образцы мицелия инкубировали в питательной среде без каких-либо добавок. В качестве дополнительного стрессового фактора, который мог влиять на уровень световой эмиссии поврежденного мицелия, использовали закисление инкубационной среды. Для этого в питательную среду добавляли уксусную кислоту (до рН 5,0 и 4,0), после чего в нее помещали опытные образцы мицелия. В параллельных экспериментах в качестве эффектора, ингибирующего свечение, в питательную среду с образцами мицелия добавляли нейтрализованный до нейтрального значения рН раствор салициловой кислоты (СК) в конечной концентрации 0,5 мМ. Ранее нами было показано, что СК в такой концентрации подавляет свечение поврежденного мицелия N. nambi на порядок и более [7]. Контрольные и опытные образцы мицелия инкубировали при комнатной температуре, через каждые 30 мин оценивая интенсивность их свечения на люминометре Glomax 20/20 (Promega, USA). Уровень световой эмиссии выражали в относительных люминесцентных единицах (RLU), регистрируемых со скоростью 1 измерение в 1 с. При достижении максимального уровня свечения диски мицелия извлекали из питательной среды, замораживали, лиофилизовали и определяли вес сухой биомассы каждого образца. Содержание диеновых конъюгатов (ДК) в биомассе оценивали после экстракции из нее липидных компонентов смесью растворителей гептан-изопропанол с последующим разделением фаз [12]. Согласно методу, уровень ДК в фазах гептана и изопропанола может свидетельствовать об интенсивности перекисного окисления в биообразце нейтральных липидов и фосфолипидов соответственно. Содержание ДК в фазах определяли спектрофотометрически (UV-1800, Shimadzu, Japan) по величине их оптической плотности (OD) при длине волны 232 нм и выражали в единицах OD на 1 г сухой биомассы. Для количественной оценки содержания оснований Шиффа (ОШ) экстракцию липидных компонентов из биомассы проводили по методу [13], используя смесь растворителей хлороформ-метанол. Содержание ОШ в экстрактах определяли по величине их флуоресценции (Varian Cary Eclipse, USA), регистрируемой в диапазоне длин волн 400–600 нм, после возбуждения образцов облучением при длине волны 360 нм и выражали в относительных единицах максимальной световой эмиссии на 1 г сухой биомассы. Для сравнительной оценки содержание ДК и ОШ определяли также в образцах мицелия, которые не инкубировали. В этом случае диски после высечения из пленочного мицелия и оценки уровня их свечения сразу замораживали, лиофилизовали и проводили последующую экстракцию ДК и ОШ из сухой биомассы таким же образом, как это изложено выше.
Результаты исследования и их обсуждение. Как показали эксперименты (рис. 1), закисление питательной среды до значений рН 5,0 и 4,0 добавкой уксусной кислоты сопровождается значительным подавлением световой эмиссии поврежденного мицелия N. nambi в ходе его инкубации. Из представленных данных видно, что через 4 ч инкубации (максимальный уровень свечения образцов мицелия) при рН 5,0 наблюдается снижение интенсивности световой эмиссии гриба более чем на порядок (в 13.5 раз), по сравнению с контролем. При рН 4,0 свечение мицелия подавляется практически полностью – уровень регистрируемой световой эмиссии гриба через 4 ч инкубации составляет около 800 RLU (рис. 1). Для сравнения следует сказать, что уровень фонового шума измерительной системы (люмино-метр Glomax 20/20) составляет порядка 100 RLU. Точный механизм такого действия уксусной кислоты пока непонятен и требует дальнейшего изучения. С одной стороны, этот эффект, вероятно, мог бы объясняться неоптимальным значением рН среды для активности ферментов, обеспечивающих свечение гриба. Ранее было установлено [14], что оптимум функционирования ферментов люминесцентной системы, выделенной из гриба N. nambi, наблюдается при pH 7,4–7,6, а смещение pH среды в кислую или щелочную области приводит к снижению их активности. Однако можно пред- положить, что ингибирующий эффект уксусной кислоты связан с ее денатурирующим воздействием на белковые компоненты гриба. Известно, что данная кислота обладает липофильными свойствами и является более сильным денатурирующим агентом, например, в сравнении с минеральными кислотами при одинаковой концентрации ионов водорода [15]. В пользу этой версии свидетельствует тот факт, что в ходе инкубации контрольные образцы поврежденного мицелия N. nambi сохраняли жизнеспособность – через сутки гриб восстанавливал свою целостность и продолжал рост. В то же время закисление питательной среды добавкой уксусной кислоты до рН 4,0 приводило не только к практически полному ингибированию свечения образцов мицелия (см. рис. 1), но и полному подавлению их роста. В дополнение следует сказать, что добавка 0,5 мМ СК (раствор реагента нейтрализован до нейтрального рН) в питательную среду с образцами мицелия N. nambi также приводила к существенному подавлению их свечения (в 11,5 раз) (данные не приведены), что полностью согласуется с результатами наших предыдущих исследований [7].
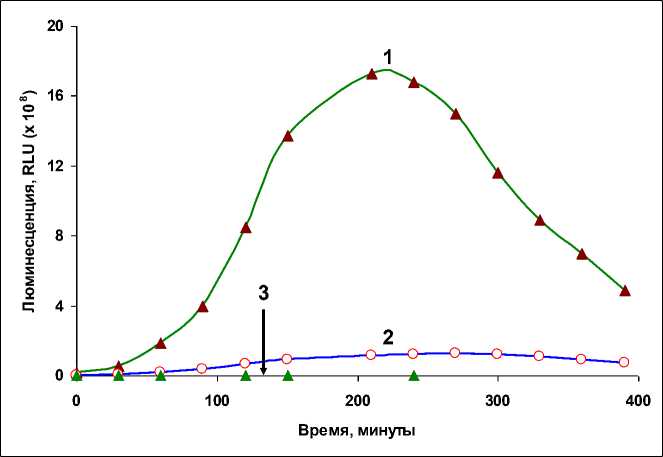
Рис. 1. Динамика и интенсивность свечения механически поврежденного мицелия N. nambi в ходе его инкубации в питательной среде: 1 – контроль (рН 6,2); 2, 3 – закисление питательной среды добавками уксусной кислоты до рН 5,0 и 4,0 соответственно
Поскольку у контрольных и опытных образцов мицелия максимальная интенсивность свечения регистрировалась через 4 ч инкубации
(см. рис. 1), содержание ДК и ОШ в их биомассе оценивали в это время. Совокупность полученных данных позволила выявить общую законо- мерность (рис. 2). При высоком уровне световой эмиссии образцов инкубируемого мицелия по сравнению с исходным уровнем их свечения (сразу после высечения дисков) в экстрактах из биомассы гриба регистрируется снижение уровня ДК как в фазе гептана, так и в фазе изопропанола. В то же время при практически полном подавлении свечения мицелия при рН 4,0, вызванном добавлением уксусной кислоты, наблюдается гораздо меньшее снижение содержания ДК в фазе изопропанола и некоторое повышение их содержания в фазе гептана. По- скольку более выраженные изменения в содержании ДК были выявлены в фазе изопропанола, можно предположить, что в поврежденном мицелии N. nambi перекисное окисление фосфолипидов идет интенсивнее, чем перекисное окисление нейтральных липидов (рис. 2). В целом результаты этого раздела работы позволяют говорить о том, что грибное свечение оказывает протекторный эффект при повреждающем воздействии активных радикалов на гриб в условиях стресса и препятствует развитию ПОЛ.
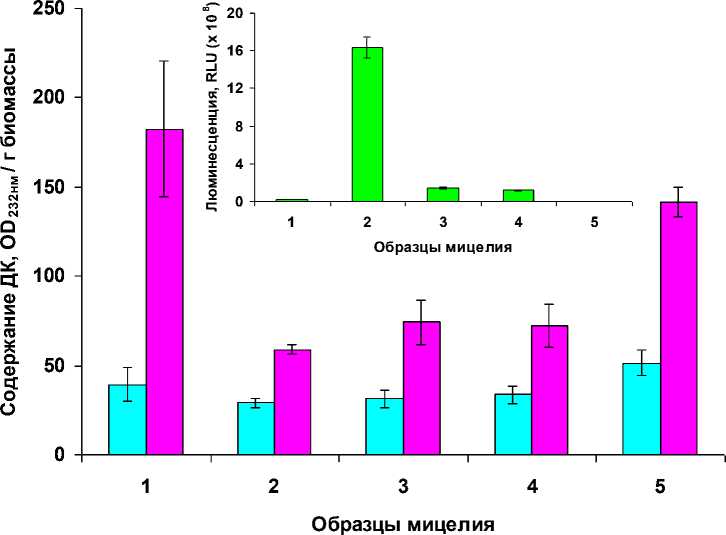
Рис. 2. Содержание ДК в экстрактах из биомассы мицелия N. nambi: фракция гептана (голубые столбцы), фракция изопропанола (малиновые столбцы). Образцы мицелия: 1 – без инкубации; 2–5 – после инкубации в течение 4 часов – контроль (питательная среда, рН 6,2), питательная среда с добавкой 0,5 мМ СК, закисление питательной среды до рН 5,0 и 4,0 добавкой уксусной кислоты (на вставке представлена интенсивность свечения указанных образцов мицелия)
В экспериментах было показано, что изменения содержания ОШ в образцах поврежденного мицелия N. nambi при их инкубации имеют такую же направленность, как и изменения содержания ДК (см. выше). Это следует из данных уровней флуоресценции хлороформ-метанольных экстрактов из образцов грибной биомассы (рис. 3). Видно, что в контрольных образцах мицелия, обладающих максимальным свечением через 4 ч инкубации, регистрируется значительно мень- шее содержание ОШ по сравнению с их содержанием в исходном поврежденном мицелии, имеющем невысокий уровень световой эмиссии. В образцах мицелия, проинкубированных 4 ч в присутствии СК (0,5 мМ) и уксусной кислоты (закисление среды до рН 5,0) и обладающих гораздо меньшим уровнем световой эмиссии по отношению к контролю (рис. 2, вставка), отмечается большее содержание ОШ. И, наконец, при практически полном подавлении свечения после закисления питательной среды до рН 4,0 добавкой уксусной кислоты в биомассе мицелия через 4 ч инкубации отмечается самый высокий уровень содержания ОШ среди исследованных опытных образцов мицелия (см. рис. 3). Совокупность данных этого раздела исследований также свидетельствует в пользу защитной роли грибного свечения, нейтрализующего в ходе реакции излучения избыточный пул активных радикалов кислорода, которые могут значительно возрастать в грибе в стрессовых условиях и тем самым препятствовать дальнейшему развитию ПОЛ [6].
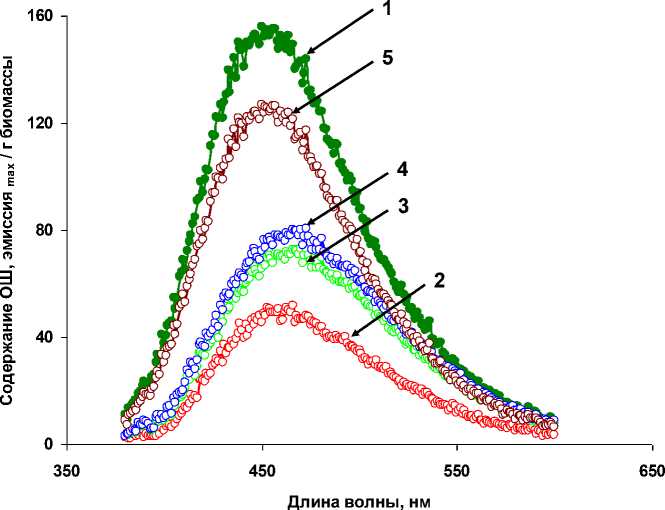
Рис. 3. Интенсивность флуоресценции хлороформ-метанольных экстрактов из образцов мицелия N. nambi, отражающая содержание ОШ в грибной биомассе. Для экстракции использованы образцы мицелия: 1 – без инкубации; 2–5 – после инкубации в течение 4 ч – контроль (питательная среда, рН 6,2), питательная среда с добавкой 0,5 мМ СК, закисление питательной среды до рН 5,0 и 4,0 добавкой уксусной кислоты
Заключение . Таким образом, проведенная оценка интенсивностей световой эмиссии образов механически поврежденного мицелия гриба N. nambi при разных условиях их инкубации в сопоставлении с полученными данными содержания в грибной биомассе первичных (ДК) и конечных (ОШ) продуктов ПОЛ указывает на взаимосвязь процессов свечения и свободнорадикального окисления. Исследованием установлено, что в условиях стресса (механическое повреждение, инкубация в присутствии ингибитора свечения (СК) и при закислении среды добавлением уксусной кислоты) повышение уровня световой эмиссии мицелия сопровождается снижением содержания в биомассе гриба первичных и конечных продуктов ПОЛ.
Совокупность этих данных свидетельствует в пользу высказанной нами ранее гипотезы о защитной функции свечения высших грибов от негативного воздействия активных радикалов кислорода, пул которых может значительно возрастать в грибе при стрессе.
Нейтрализация избытка кислородных радикалов в ходе реакции светоизлучения будет оказывать протекторный эффект и препятствовать развитию в грибной биомассе процессов свободнорадикального окисления, в частности развитию ПОЛ. Пока неясен точный механизм наблюдаемого в экспериментах снижения содержания ДК и ОШ в инкубируемых контрольных и опытных образцах мицелия по сравнению с их содержанием в исходном поврежденном мице- лии. Полученные результаты не позволяют также объяснить, могут ли данные продукты ПОЛ утилизироваться (прямо или опосредованно) в процессе грибного свечения или вовлекаться в метаболические циклы гриба. Выяснение этих вопросов требует дальнейшего изучения.
Список литературы Содержание диеновых конъюгатов и оснований шиффа в мицелии гриба Neonothopanus nambi при разных уровнях его свечения в условиях стресса
- Бондарь В.С., Пузырь А.П., Пуртов К.В. и др. О люминесцентной системе светящегося гриба Neonothopanus nambi//ДАН. -2011. -Т. 438. -№ 5. -С. 705-707.
- Bondar V.S., Shimomura O., Gitelson J.I. Luminescence of higher mushrooms//J. Sib. Fed. Univ. Biol. -2012. -V. 5. -№. 4. -P. 331-351
- Бондарь В.С., Родичева Э.К., Медведева С.Е. и др. О механизме свечения гриба Neonothopanus nambi//ДАН. -2013. -Т. 449. -№ 2. -С. 223-227
- Могильная О.А., Ронжин Н.О., Медведева С.Е. и др. Общая пероксидазная и каталазная активности светящихся базидиомицетов Armillaria borealis и Neonothopanus nambi в сравнении с уровнем световой эмиссии//Прикладная биохимия и микробиология. -2015. -Т. 51. -№ 4. -С. 395-401
- Mogilnaya O.A., Ronzhin N.O., Bondar V.S. Comparative evaluation of total peroxidase and catalase activities during light emission of luminous fungus Neonothopanus nambi//Mycosphere. -2016. -V. 7. -№ 4. -P. 499-510
- Тюлькова Н.А., Медведева С.Е., Бондарь В.С. Сравнительная оценка интенсивностей перекисного окисления липидов и свечения гриба Neonothopanus nambi//Вестн. Крас-ГАУ. -2016. -№ 1. -С. 21-28.
- Тюлькова Н.А., Бондарь В.С. Активность ферментов метаболизма активных форм кислорода и уровень световой эмиссии мицелия гриба Neonothopanus nambi при действии салициловой кислоты//Вестн. Крас-ГАУ. -2017. -№ 2. -С. 155-165.
- Владимиров Ю.А., Арчаков А.И. Перекисное окисление липидов в биологических мембранах. -М.: Наука, 1972. -252 c.
- Феофилова Е.П., Бурлакова Е.Б., Кузнецова Л.С. Значение реакций свободнорадикального окисления в регуляции роста и липидообразования эукариотных и прокариотных организмов//Прикл. биохимия и микробиология. -1987. -Т. 23. -Вып. 1. -С. 3-13.
- Колупаев Ю.Е. Активные формы кислорода в растениях при действии стрессоров: образование и возможные функции//Вестн. Харьковского национального аграр. ун-та. Сер. Биология. -2007. -Вып. 3 (12). -С. 6-26.
- Загоскина Н.В., Назаренко Л.В. Активные формы кислорода и антиоксидантная система растений//Вестн. Москов. городского пед. ун-та. Сер. Естественные науки. -2016. -№ 2 (22). -C. 9-23.
- Хышиктуев Б.С., Хышиктуева Н.А., Иванов В.Н. Методы определения продуктов перекисного окисления липидов в конденсате выдыхаемого воздуха и их клиническое значение//Клиническая лабораторная диагностика. -1996. -№ 3. -С.13-15.
- Fletcher B.L., Dillard C.L., Tappel A.L. Fluorescent products of lipid peroxidation of mitohondria and microsomes//Analyt. Biochem. -1973. -№ 52 (1). -P. 1-9.
- Бондарь В.С., Пузырь А.П., Пуртов К.В. и др. Выделение люминесцентной системы из светящегося гриба Neonothopanus nambi//ДАН. -2014. -Т. 455. -№ 3. -С. 346-348
- Reynolds A.E. The mode of action of acetic acid on bacteria//Diss. Abstr. -1975. -№ 35. -P. 4935-4936


