Содержание метаболитов оксида азота II (N0) в плазме крови у крыс в разные фазы полового цикла
Автор: Сибгатуллин И.Т., Каримова Р.Г.
Статья в выпуске: 1 т.233, 2018 года.
Бесплатный доступ
В статье изложены результаты изучения содержания стабильных метаболитов оксида азота II (NO) в плазме крови у крыс в разные фазы полового цикла. Установлено, что система N0 в разных фазах полового цикла в плазме крови у крыс имеет разную активность. Максимальная активность системы оксида азота (II) отмечается в фазе проэструс и эструс.
Оксид азота, плазма крови, крыса, течка, половой цикл
Короткий адрес: https://sciup.org/142213000
IDR: 142213000 | УДК: 591.1:612.12
The content of metabolites of nitric oxide II (NO) in blood plasma in rats at different phases of the sexual cycle
The results of studying the content of nitric oxide stable metabolites in rat blood plasma at different phases of the sexual cycle were presented. It was established that NO system at different phases of the sexual cycle in rat blood phases has different activity. The maximum activity of NO system is noted at the phase of the proestrus and estrus.
Текст научной статьи Содержание метаболитов оксида азота II (N0) в плазме крови у крыс в разные фазы полового цикла
Одним из значительных достижений ученых стало открытие биорсгулятор-ных свойств эндогенного оксида азота (II)NO. Оно явилось революцией в биологии и медицине, так как стало известно о совершенно новом типе передачи информации в организме, появилась возможность инновационного подхода в лечении огромного количества заболеваний человека и животных. Выяснилось, что оксид азота (II) является универсальным биологическим регулятором множества процессов в организме, влияя на тонус полых ор ганов брюшной полости, состояние бронхов и альвеол легких, реологические свойства крови, иммунные процессы, нервно-мытпечную передачу'. Оксид азота (II) проявляет противовоспалительную и антиопу-холевую активность, влияет на репродуктивную систему и высшую нервную деятельность человека, и животных. R. F. Furchgott и J. V. Zowadcki в 1980 году выяснили, что оксид азота (И) содержится практически во всех тканях живого организма. Его свойства в настоящее время продолжают активно изучаться и получен- ные сведения берутся на вооружение фармакологами и клиницистами различных специальностей. Также становится очевидным неоднозначность и разнонаправ-ленность влияния оксида азота (II). Эффект воздействия определяется концентра-цией оксида азота (II) [1,8,11]. Ненадлежащая регуляция уровня оксида азота (II) приводит к проявлению патологий, таких как нарушение функций сердечно-сосудистой системы, нейродегенерация, артрит, астма и септический шок и т. д.
Известно, что оксид азота (И) принимает участие в регуляции репродуктивной системы у самок и самцов. В гипофизе он активирует секрецию лютеинизирующего гормона [11]. В свою очередь половые гормоны, эстрогены и андрогены стимулируют продукцию оксида азота (II), а прогестерон через свои рецепторы снижает уровень экспрессии eNOS [9]. Оксид азота (II) также индуцирует овуляцию у крыс [13]. Ввиду его многогранной роли в регу ляции процессов размножения в организме он был назван половым газом [11].
Исходя из вышеизложенного вопрос изучения возможной роли оксида азота (II) в регуляции полового цикла млекопитающих остается актуальным.
Цель исследования - изучить содержание метаболитов NO в плазме крови у крыс в разные фазы полового цикла.
Материал и методы исследований. Работа выполнена на базе кафедры физиологии ФБГОУ ВО Казанская ГАВМ. Объектом исследования служили самки крыс породы Wistar массой тела 250-295 г. Были созданы 4 группы животных. У каждой определяли фазу полового цикла, исследуя влагалищные мазки. Ежедневно с 8 до 9 утра собирали вагинальные секреты пластиковой пипеткой заполненной физиологическим раствором (NaCl 0,9 %), вставив наконечник во влагалище крысы. Вагинальную жидкость помещали на предметное стекло. Окраску мазка производили по методу Романовского-Гимза.
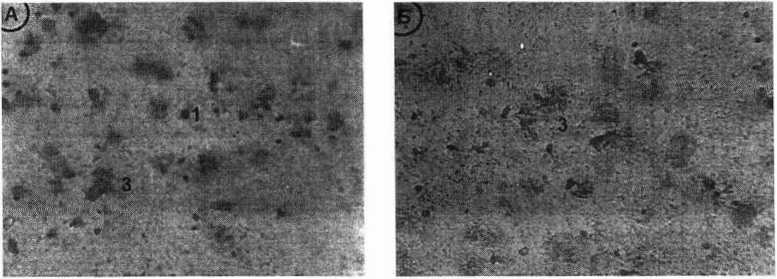
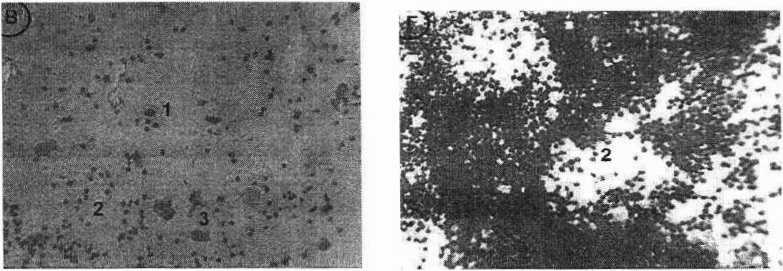
Рисунок-1 Микрофотографии вагинального мазка крыс при: (А) проэструсе, преимущественно состоящей из зародышевых эпителиашных клеток; (Б) эструсе с явными поверхностными безъядерными клетками; (В) метаэструсе, состоящей из трех типов клеток, лейкоцитов, зародышевых эпителиальных клеток; и (Г) диэструсе, состоящей преимущественно из лейкоцитов. Где, 1 - эпителиальные клетки, 2 - лейкоциты, 3 - поверхностные безъядерные клетки.
Мазок фиксировали этиловым спиртом в течение 5-15 мин. Готовый препарат рассматривали под микроскопом при 10-и, 40-кратном увеличении. По картине влагалищного мазка определяли фазы полового цикла. Продолжительность полового цикла крыс делает их идеальным объектом для изучения изменений, происходящих в течении полового цикла. Цикл длится четыре дня и включает в себя фазы проэструса, эструса, метаэструса и диэструса.
Фаза проэструса, или подготовительная, характеризуется кровянистыми выделениями, иногда обильными. Картина влагалищного мазка в начале фазы характеризуется большим числом округлой формы эпителиальных клеток с довольно крупными ядрами (рисунок 1а). В фазу эструса выделения из влагалища почти бесцветны или бледно-розового цвета. На препарате влагалищного мазка подавляющее большинство клеточных элементов представлено чешуйками, плоскими поверхностными эпителиальными клетками. У них нет видимого ядра, цитоплазма является зернистой (рис 1 б). В фазу мэтаэст-руса выделения из влагалища еще могут быть, как правило, они бесцветны, но могут быть и бледно-розового цвета. Влагалищный мазок демонстрирует незначи тельное количество молодых эпителиальных клеток, округлых с крупными и преобладанием лейкоцитов (рис 1в). В фазу диэструса мазок состоит преимущественно из лейкоцитов (рис 1г).
После определения фазы полового цикла брали кровь. Взятие крови у крыс производили из хвостовой вены. Об уровне содержания оксида азота (II) в крови судили по суммарной концентрации нитрат- и нитрит-анионов в плазме крови, которую определяли путём восстановления нитратов до нитритов однократной навеской цинковой пыли, обработанной аммиачным комплексом сульфата меди, с последующим фотометрическим определением нитритов с помощью реактива Грисса при длине волны 520,0 нм на КФК -3-10 [3]. Статистическую обработку результатов эксперимента проводили с использованием критерия t-Стьюдента, статистически значимое считали различия при уровне (р<0,05).
Результаты исследований. Ранее было установлено, что содержание нитрат-и нитрит-анионов в плазме крови у самок крыс в среднем составляет 35,57±2,58 мкмоль/л. Было установлено, что система NO в разных фазах полового цикла в плазме крови у крыс имеет разную активность.
Таблица 1 - Содержание метаболитов оксида азота (II) в плазме крови крыс в зависим ости от фазы п о лового цик ла ____
|
Фаза полового цикла |
Содержание метаболитов NO (мкмоль/л) в плазме крови |
|
Проэструс |
36,03±0,87 |
|
Эструс |
36,51±0,30 |
|
Мэтаэструс |
34,38*±0,51 |
|
Диэструс |
34,99*±0,63 |
Примечание: * - достоверно по сравнению с контрольной группой (р<0,05)
В фазах проэструса и эструса в плазме крови наблюдается повышение концентрации нитрат и нитрит анионов на 1,3 % и 2,6 % соответственно, тогда как в фазах мэтаэструса и диэструса наблюдается снижение концентрация этих же анионов.
Результаты наших исследований позволили сделать следующие выводы. Содержание метаболитов оксида азота (II) в плазме крови самок крыс зависит от фазы полового цикла. Данные литературы свидетельствуют о том, что в фазах эструс и проэструс происходят процессы с высоким влиянием оксида азота (II). Наличие оксида азота (II) в фолликулярной жидкости подтверждено у нескольких видов жи-вотных[10]. Также оксид азота (II) участвует в контроле секреции гонадотропина, который, в свою очередь, известен как ключевой регулятор конечных стадий развития фолликулов [10]. В настоящий момент эстрогены считаются наиболее изученными регуляторами eNOS [9]. Кроме того, результаты недавних исследований свидетельствует о вовлеченности оксида азота (II) в овуляторный процесс. Местное применение ингибиторов eNOS подавляет процесс овуляции у крыс, что объясняется его высоким содержанием [1]. У человека eNOS была обнаружена в эпителии эндометрия во время менструации. Исходя из этого можно предположить, что оксид азота (II) может участвовать в инициировании и поддержании менструального кровотечения и релаксации миометрия во время менструации [14]. В фазу метаэст-руса и диэструса на месте лопнувшего фолликула под влиянием ЛГ развивается желтое тело, которое начинает вырабатывать прогестерон. Прогестерон через рецепторы глюкокортикоидов снижает уровень экспрессии eNOS [9]. Но, в отличие от эстрогена, его роль до конца не изучена. Многие факторы свидетельствуют об участии оксида азота (II) в регуляции развития и функционирования желтого тела, но эти данные не однозначны и противоречивы П]
Заключение. Исходя из вышеизложенного следует: 1 .Изменения активности системы оксид азота (II) в плазме крови зависит от фазы полового цикла. 2.Максимальная активность системы оксида азота (II) отмечается в фазе проэструс и эструс. При глубоком исследовании, определение количества метаболитов оксида азота может способствовать созданию методов диагностики заболеваний половой системы, а также может быть применено в процессах воспроизводства для более точного определения времени оплодотворения.
Резюме
В статье изложены результаты изучения содержания стабильных метаболитов оксида азота И (NO) в плазме крови у крыс в разные фазы полового цикла. Установлено, что система N0 в разных фазах полового цикла в плазме крови у крыс имеет разную активность. Максимальная активность системы оксида азота (П) отмечается в фазе проэструс и эструс.
Список литературы Содержание метаболитов оксида азота II (N0) в плазме крови у крыс в разные фазы полового цикла
- Ванин, А. Ф. Оксид азота в биомедицинских исследованиях/А. Ф. Ванин//Вестник РАМН,-2000. -№ 4. -С. 3-5.
- Зенкина. В.Г. Участие оксида азота овариальном цикле/B.F. Зенкина, O.A. Солодкова//Современные проблемы науки и образования. -2015. -№ 3. -С.12-14.
- Солодков, А. П. Фотометрический метод определения нитратов и нитритов в биологических жидкостях/А. П. Солодков, И. С. Веремей//Витебский государственный медицинский университет. -2001. -№1.-С.32-35.
- Каримова, Р.Г. Нитроксидергическая система: влияние соединений фуроксанового ряда/Р.Г. Каримова, Т.В. Гарипов//Ветеринарная медицина домашних животных. Сборник статей. -Казань, 2009.-С. 85-88.
- Каримова, Р.Г. Содержание оксида азота и нитрозотиолов в крови крыс под влиянием замещенного бензодифуразана/Р.Г. Каримова//Вестник Уральской медицинской академической науки. -2009. -№2(25). -С. 231.
- Каримова, Р.Г. Влияние различных факторов на продукцию оксида азота в организме крыс/Р.Г. Каримова, И.Н. Билалов, Т. В. Гарипов//Фундаментальные исследования. -2015. -№ 2-1. -С. 5357
- Каримова, Р.Г. Полезный приспособительный эффект нитроксидергической системы/Р.Г. Каримова, Т.В. Гарипов//Известия Самарской сельскохозяйственной академии. -2011. -№ 1. -С. 42 -46.
- Кузнецова, В.Л. Оксид азота: свойства, биологическая роль, механизмы действия/В.Л. Кузнецова, А.Г. Соловьева//Современные проблемы науки и образования. -2015. -№4.
- Duckies, S.P. Hormonal modulation of endothelial NO production/S.P. Duckies, V.M. Miller//-2010.
- Francesca, G. Nitric oxide in follicle development and oocyte competence./G. Francesca, B. Giuseppina//Via del Taglio. -V.l.-43126.
- McCann, S.M. The role of nitric oxide in reproduction/S.M. McCann, V. Rettori//Proc Soc Exp Biol Med. -1996.-P.7-15.
- Marcondes, F.K. Determination of the estrous cycle phases of rats: some helpful considerations/F.K. Marcondes, F. J. Bianchi, A.P. Tanno//Braz. J. Biol. -2002,-V.62.-No.4a.
- Shukovski, L. The involvement of nitric oxide in the ovulatory process in the rat/L. Shukovski, A. Tsafiri//Endocrinology. -1994. -V.135,-P. 2287-2290.
- Chwalisz, K. Role of nitric oxide in implantation and menstruation/K. Chwalisz, R.E. Garfield//Hum Reprod. -2000. -P.96-111.
- Caligioni, C.S. Assessing reproductive status/stages in mice/C.S. Caligioni//Curr Protoc Neurosci. -2009.


