Сохранение и рациональное использование генетических ресурсов яка (Bos mutus)
Автор: Багиров В.А., Гладырь Е.А., Эрнст Л.К., Кленовицкий П.М., Зиновьева Н.А., Насибов Ш.Н.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Научная школа академика Л.К. Эрнста: исследования и перспективы (к 80-летию ученого)
Статья в выпуске: 2 т.44, 2009 года.
Бесплатный доступ
Предложена оригинальная технология криоконсервации эпидидимальных и тестикулярных сперматозоидов яка, с использованием которой создан криобанк семени кабардино-балкарской, памирской и алтайской популяций яков. Получены гибридные животные для выведения новых селекционных форм. Дана цитогенетическая и молекулярно-генетическая характеристика яков из разных региональных популяций.
Гибриды, криобанк семени, криоконсервация, молекулярно-генетический, популяция, цитогенетический, эпидидимальные сперматозоиды, яки
Короткий адрес: https://sciup.org/142133236
IDR: 142133236 | УДК: 636.293.3:636.082:636.082.4.53
Preservation and efficient use of genetic resources of yak (Bos mutus)
The original technology for cryopreservation of epididymal and testicular yak spermatozoons was proposed, which permit to create the sperm cryobank of the Kabardino-Balkaria, the Pamirs and the Altai yak populations. The hybrid animals for the creation of new selective form were obtained. The cytogenetic and molecular-genetic characterization of the yaks from different regional populations was presented.
Текст научной статьи Сохранение и рациональное использование генетических ресурсов яка (Bos mutus)
Традиционные приемы воспроизводства не обеспечивают эффективную реализацию генетического потенциала малочисленных и исчезающих видов. Сохранять и рационально использовать эти генетические ресурсы, восстанавливать малочисленные виды, породы, создавать новые селекционные формы посредством отдаленной гибридизации животных позволяют современные биотехнологические методы (3, 4).
В 1947 году В.К. Милованов, И.И. Соколовская и И.В. Смирнов открыли возможность длительно сохранять семя животных в состоянии глубокого охлаждения, что стало основой для создания криобанка генетических ресурсов высокопродуктивных, редких, уникальных и исчезающих видов животных (5), а в 1970-е годы Б.Н. Вепринцев стал инициатором создания генетических криобанков и использования методов биологии развития для сохранения редких и исчезающих видов животных.
Нашей целью была разработка технологии криоконсервации сперматозоидов яка и проведение молекулярно- и цитогенетических исследований образцов для создания криобанка семени животных из региональных популяций.
Методика . Исследования выполняли в 2002-2007 годах в экспери-
Работа выполнена при поддержке РФФИ (проект ¹ 08-04-13701).
ментальном хозяйстве Всероссийского НИИ животноводства (ВНИИЖ) «Кленово-Чегодаево», в с. Бизинги (Черекский р-н, Кабардино-Балкарская Республика), Горно-Бадахшанской автономной области (Республика Таджикистан), пос. Кош-агач (Республика Алтай). Опыты по сохранению генофонда проводили на яках памирской, кабардино-балкарской и алтайской популяций. Для молекулярно-генетического анализа генотипа изучали образцы ДНК у 37 животных из монгольской (Я-М, n = 31), алтайской (Я-А, n = 2), памирской (Я-П, n = 2) и кабардино-балкарской (Я-К, n = 2) популяций. Для сравнения частоты встречаемости микросателлитных маркеров и оценки вариабельности в исследуемых популяциях использовали ДНК яков из Бутана (исследования в рамках проекта Institut National de la Recherche Agronomique — INRA CaDBase) (Я-Б, n = 39).
ДНК выделяли из образцов ткани (ушные выщипы). Использовали колонки NexttecTM (Германия) и набор реагентов DIAtomTM DNA Prep100 (ООО «Биоком», Россия) в соответствии с рекомендациями фирм-изготовителей. Анализ ДНК и постановку полимеразной цепной реакции (ПЦР) выполняли согласно описанию (6). Выбор микросателлитных локусов осуществляли в соответствии с рекомендациями Международного общества генетики животных ( ISAG). Электрофоретическое разделение фрагментов ДНК методом капиллярного электрофореза проводили на приборе ABI 3130xl Genetic Analyzer («Applied Biosystems», США). Для идентификации аллелей исследованных микросателлитных локусов использовали программу ABI GeneMapper v. 4.0. Данные о выявленных у каждого животного аллелях суммировали в электронной таблице Microsoft Excel. Полученная матрица генотипов служила основой для статистической обработки результатов.
Цитогенетические исследования выполняли в культуре периферических лимфоцитов яка, крупного рогатого скота и их гибридов при стимуляции клеток конконавалином А. Препараты хромосом получали по общепринятой методике (7) с оригинальными модификациями (8). Для документирования данных и последующего изучения кариотипа применяли цифровую видеокамеру КС-583С с пакетом программ, совместимых с Windows. Обработку изображений проводили по описанной нами методике (9).
При подготовке эпидидимальных сперматозоидов животных использовали фракционное выделение спермы (оригинальный метод, предложенный нами ранее) (10). Процедура получения и криоконсервации семени включала: отбор семенников; препарирование эпидидимиса, извлечение содержимого эпидидимиса, разделение сперматозоидов на фракции, разбавление образцов семени криопротективной средой, эквилибрацию семени и собственно криоконсервацию. Пробирки с разбавленным семенем, которые находились в поролоновом теплоизолирующем штативе, помещали на 4 ч в холодильник (+4 ° С), затем в воду со льдом (0 ° С). Семя замораживали на охлажденной в жидком азоте фторопластовой пластине (11).
Качественные и количественные показатели семени определяли по общепринятой методике (5). После оттаивания визуально оценивали подвижность и жизнеспособность сперматозоидов (при +37 ° С каждые 2 ч до полной гибели), используя микроскоп с нагревательным столиком Пакена-са. Морфологическую сохранность акросом контролировали с помощью видеокамеры и компьютерной программы Image Scope (ООО «Системы для микроскопии и анализа», Россия) (3).
Статистическую обработку данных проводили по стандартным методикам (12-14), применяя программное обеспечение MS Excel, MSA_WIN v. 2.65, GenAlEx 6.0, Phylip.
Результаты. В экспедициях в Кабардино-Балкарию, на Памир и Ал- тай было выделено биологически полноценное эпидидимальное семя от 11 яков и выполнена его криоконсервация. Подвижность сперматозоидов после замораживания—оттаивания составила 35 %. Отметим, что первые попытки получения спермы от яков были предприняты во второй половине ХХ века (исследования, выполненные В.В. Ельчаниновым в Киргизии в 1962 году), однако тогда эпидидимальные сперматозоиды не подвергались криоконсервации, а опыты Е. Загдсурена (1980) по получению спермы от яков на искусственную вагину с последующей криоконсервацией и использованием при осеменении коров не дали результата.
Выделенные нами сперматозоиды яка имели следующие морфометрические характеристики: длина общая — 72,90±0,24, длина головки — 8,71±0,06, ширина головки — 4,67±0,04 мкм, площадь головки — 33,70±1,68 мкм2, коэффициент округлости головки — 1,220±0,001. При цитологическом исследовании площадь ядра сперматозоидов составила 107,2; средняя яркость — 67,2; средняя плотность — 187,8; количество ДНК — 20,1 усл. ед.


Рис. 1. Гибридное потомство, полученное при осеменении коров черно-пестрой породы эпидиди-

мальным семенем яка после криоконсервации.
Замороженное эпидидимальное семя яков сохраняло биологиче- скую полноценность и оказалось пригодным для плодотворного искусст- венного осеменения: от коров черно-пестрой породы с использованием такого семени получили восемь гибридных потомков — шесть телочек и двух бычков (рис. 1).
0 Illi ^ ДО ДО 11Я
1 2 3 4 56
fill М fill fid fid DA
7 8 9 10 1112
Afi flfl flfl flfl flflM
13 14 15 16 1718
Л 6 0 0 л6 i* 0 r * 6 a
19 20 21 22 2324
Oft ftfl dd Aft OA
25 26 27 28 29XY
Рис. 2. Кариотип самца яка ( Bos mutus ). Предварительная обработка 5 ′ -бром-дезоксиуридином и бромистым этидием. Окраска по Романовскому-Гимза, увеличение ½100.
Изучение воспроизводительной функции у яков разного возраста, получение и криоконсервация семени, создание его банка — один из надежных способов сохранения генетических ресурсов вида. Это необходимо для улучшения племенных качеств одомашненных яков и их использования для отдаленной гибридизации, позволяющей обогащать генотип материнских пород комплексом генов, контролирующих присущие якам желательные свойства. Для решения этих задач требуется углубленное изучение биологических (биотехнологических, физиологических, генетических) особенностей исходных видов и их гибридов.
Цитогенетический анализ показал, что по числу и морфологии хромосом кариотипы яка и крупного рогатого скота Bos taurus идентичны: в них имеется по 29 пар акроцентрических аутосом, а X- и Y-хромосомы по морфологии и размеру сходны (рис. 2). Существенных морфологических раз-
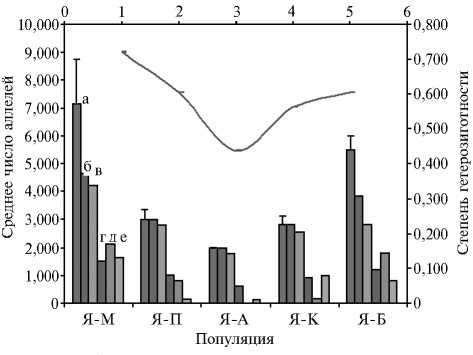
Рис. 3. Характеристика аллелофонда изучаемых популяций яка по среднему числу аллелей шести микросателлитных маркерных локусов (BM1824, ETH10, ETH225, TGLA122, TGLA126 и TGLA227) крупного рогатого скота (диаграмма) и степени гетерозиготности популяции (график): а, б, в, г, д, е — соответственно среднее число аллелей, среднее число аллелей с частотой более 5 %, число эффективных аллелей, информационный индекс, число приватных аллелей, число общих аллелей с частотой до 50 %. Описание популяций ЯМ, Я-П, Я-А, Я-К, Я-Б см. в разделе «Методика».
личий между хромосомами крупного рогатого скота, яка и их гибридов не обнаружили. Сравнение характера дифференциального окрашивания гомео-логичных хромосом выявило высокую степень их сходства. В то же время следует отметить, что идеальных методик хромосомного анализа не существует, поэтому утверждать, что у разных видов рода Bos хромосомы полностью идентичны, преждевременно, тем более что у сельскохозяйственных видов животных макро- и микроструктура таких сложных объектов, как хромосомы, мало изучена.
Среднее число аллелей на локус и степень гетерозиготности в исследованных популяциях яков
|
Популяция Показатель BM1824 |
ETH10 |
ETH225 |
TGLA122 TGLA126 TGLA227 |
Среднее |
||||
|
Я-М |
N |
31 |
31 |
31 |
31 |
31 |
31 |
|
|
Na |
6 |
6 |
5 |
14 |
9 |
3 |
7,167 |
|
|
Ho |
0,419 |
0,484 |
0,645 |
0,742 |
0,581 |
0,710 |
0,597 |
|
|
He |
0,709 |
0,684 |
0,639 |
0,881 |
0,804 |
0,609 |
0,721 |
|
|
F |
0,408 |
0,292 |
- 0,010 |
0,158 |
0,278 |
- 0,165 |
0,160 |
|
|
Я-П |
N |
2 |
2 |
2 |
2 |
2 |
2 |
|
|
Na |
4 |
2 |
3 |
3 |
2 |
4 |
3,000 |
|
|
Ho |
1,000 |
0,500 |
0,500 |
1,000 |
1,000 |
1,000 |
0,833 |
|
|
He |
0,750 |
0,375 |
0,625 |
0,625 |
0,500 |
0,750 |
0,604 |
|
|
F |
- 0,333 |
- 0,333 |
0,200 |
- 0,600 |
- 1,000 |
- 0,333 |
- 0,400 |
|
|
Я-А |
N |
2 |
2 |
2 |
2 |
2 |
2 |
|
|
Na |
2 |
2 |
2 |
2 |
2 |
2 |
12,000 |
|
|
Ho |
1,000 |
0,500 |
0,500 |
1,000 |
1,000 |
0,500 |
0,750 |
|
|
He |
0,500 |
0,375 |
0,375 |
0,500 |
0,500 |
0,375 |
0,438 |
|
|
F |
- 1,000 |
- 0,333 |
- 0,333 |
- 1,000 |
- 1,000 |
- 0,333 |
- 0,667 |
|
|
Я-К |
N |
2 |
2 |
2 |
2 |
2 |
2 |
|
|
Na |
2 |
3 |
3 |
4 |
2 |
3 |
2,833 |
|
|
Ho |
0,500 |
0,500 |
1,000 |
1,000 |
0,500 |
0,500 |
0,667 |
|
|
He |
0,375 |
0,625 |
0,625 |
0,750 |
0,375 |
0,625 |
0,563 |
|
|
F |
- 0,333 |
0,200 |
- 0,600 |
- 0,333 |
- 0,333 |
0,200 |
- 0,200 |
|
|
Я-Б |
N |
39 |
39 |
39 |
39 |
39 |
39 |
|
|
Na |
5 |
5 |
5 |
8 |
5 |
5 |
5,5 |
|
|
Ho |
0,590 |
0,436 |
0,615 |
0,487 |
0,590 |
0,385 |
0,517 |
|
|
He |
0,524 |
0,451 |
0,705 |
0,801 |
0,643 |
0,493 |
0,603 |
|
|
F |
- 0,125 |
0,034 |
0,127 |
0,392 |
0,082 |
0,221 |
0,122 |
|
П р и м е ч а н и е. Описание популяций см. в разделе «Методика». N, Na, Ho, He и F — соответственно среднее число исследованных животных, среднее число аллелей в популяции по маркеру, наблюдаемый уровень гетерозиготности, ожидаемый уровень гетерозиготности и индекс фиксации.
В результате молекулярно-генетического исследования полиморфизма по шести микросателлитным маркерам крупного рогатого скота в разных популяциях яков были обнаружены существенные различия по степени гетерозиготности, которая варьировала от 43,8 % у животных из алтайской популяции до 72,1 % у особей из Монголии, а в кабардино-балкарской популяции составляла 56,3 %. Яки на Памире и в Бутане характеризовались сходной степенью гетерозиготности (соответственно 60,4 и
60,3 %) (рис. 3). Максимальное число аллелей, равное 44, диагностировали в монгольской популяции. Отметим, что степень информативности маркеров варьировала (от 2 аллелей на локус в малых выборках до 14 для локуса TGLA122 в популяции яков в Монголии).
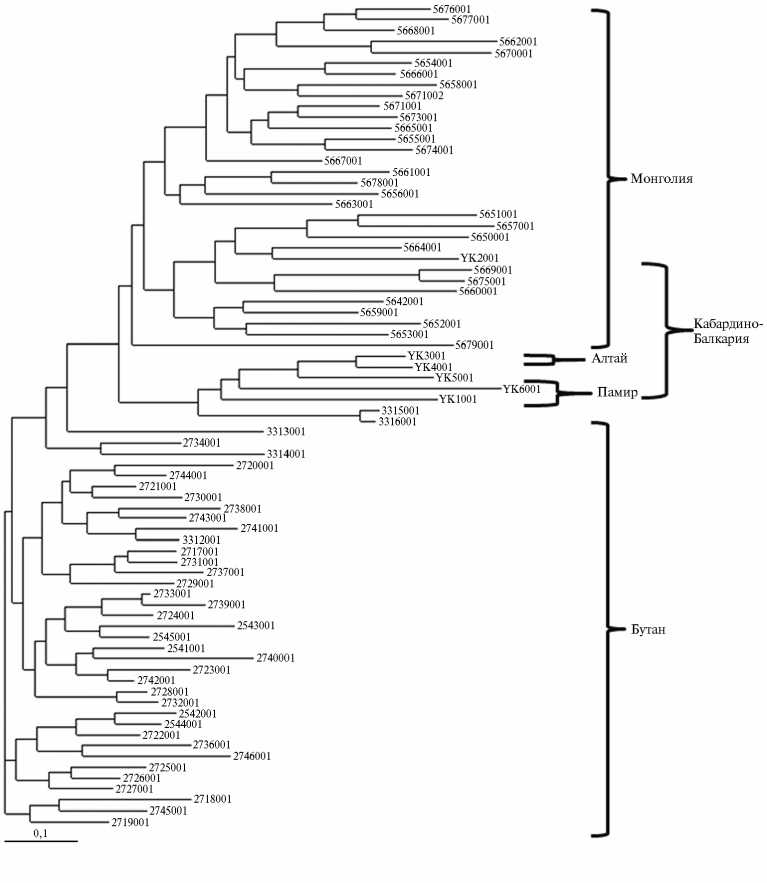
Рис. 4. Дендрограмма, характеризующая филогенетические различия изучаемых популяций яков из разных регионов (Бутан, Монголия, Памир, Алтай, Кабардино-Балкария) .
Проведенный анализ выявил приватные аллели, свойственные только одной из популяций яков. Максимальное число приватных аллелей — 6, 5 и 4 (соответственно для микросателлитных локусов TGLA122, TGLA126 и ETH225) обнаружили у яков из Монголии и Бутана, 2 приватных аллеля (290 – ETH10 и 113 – TGLA126) встречались с частотой соответственно 50,0 и 53,8 %. Этот факт свидетельствует о маркерной роли перечисленных аллелей в идентификации ареальной и популяционной принадлежности животных.
Мы установили, что только в двух популяциях (монгольской и бутанской) ожидаемый уровень гетерозиготности оказался выше фактического; в остальных наблюдаемая степень гетерозиготности существенно превосходила расчетные значения.
Кластерный анализ показал, что животные, которых разводят в Монголии и Бутане, образуют хорошо выраженные обособленные генетические группы. Изучение филогенетических связей яков в исследованных ареалах также подтвердило достаточную генетическую консолидированность особей алтайской и памирской популяций, в то время как животные, обитающие в Кабардино-Балкарии, не попали в свою группу (рис. 4). По всей видимости, это стало следствием их вторичной интродукции в регион из Алтайского края и Средней Азии.
Таким образом, разработана технология криоконсервации эпидидимальных и тестикулярных сперматозоидов, с использованием которой создан криобанк семени яков кабардино-балкарской, памирской и алтайской популяций. Получение спермы, ее криоконсервация и создание банка семени наряду с изучением генетических характеристик открывает новые перспективы в сохранении и рациональном использовании генофонда яков для создания новых селекционных форм на основе отдаленной гибридизации.
Л И Т Е Р А Т У Р А
-
1. W h i t e W.T. e.a. Yaks and yak hybrids in Alaska. J. Hered., 1946, 12: 355-358.
-
2. Э р н с т Л.К. Научные основы гибридизации. Животноводство, 1980, 9: 28-30.
-
3. Б а г и р о в В.А. Биотехнологические аспекты сохранения генетических ресурсов животных. Автореф. докт. дис. Дубровицы, 2004.
-
4. Э р н с т Л.К. Проблемы селекции и биотехнологии сельскохозяйственных животных. М., 1995.
-
5. М и л о в а н о в В.К. Биология воспроизведения и искусственное осеменение животных. М., 1962.
-
6. З и н о в ь е в а Н.А., П о п о в А.П., Э р н с т Л.К. и др. Методические рекомендации по использованию метода полимеразной цепной реакции в животноводстве. Дубро-вицы, 1998.
-
7. Г р а ф о д а т с к и й А.С., Р а д ж а б л и С.И. Хромосомы сельскохозяйственных и лабораторных животных. Атлас. Новосибирск, 1988.
-
8. К л е н о в и ц к и й П.М., Н и к и ш о в А.А., И о л ч и е в Б.С. и др. Хромосомы одомашненных животных и родственных им видов. Дубровицы, 2002.
-
9. К л е н о в и ц к и й П.М., Б а г и р о в В.А., З и н о в ь е в а Н.А. и др. Цитогенетика животных. М., 2007.
-
10. Б а г и р о в В.А., Э р н с т Л.К., К л е н о в и ц к и й П.М. и др. Сохранение генетических ресурсов редких, исчезающих и уникальных видов животных. Цитология, 2004, 46(9): 767-768.
-
11. Ю щ е н к о Н.П., С е м а к о в В.Г., Л е в и н К.Л. Замораживание спермы быков в гранулах без применения сухого льда. Молочное и мясное скотоводство, 1968, 5: 36-37.
-
12. М е р к у р ь е в а Е.К. Биометрия в селекции и генетике сельскохозяйственных животных. М., 1979.
-
13. Ж и в о т о в с к и й Л.А. Популяционная биометрия. М., 1991.
-
14. В е й р Б. Анализ генетических данных. Пер. с англ. Д.В. Зайкина, А.И. Пудовкина, А.Н. Татаренкова. М., 1995.
ГНУ Всероссийский НИИ животноводства Россельхозакадемии ,


