Сольват 4-нитробензальдоксимата тетра(пара-толил)сурьмы с бензолом p-Tol4SbON=CHC6H4(NO2-4)•PhH. Синтез и строение
Автор: Гришанина Елизавета Константиновна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 3 т.14, 2022 года.
Бесплатный доступ
Взаимодействием эквимолярных количеств пента( пара -толил)сурьмы и 4-нитробензальдоксима в бензоле получен и структурно охарактеризован сольват p -Tol4SbON=CHC6H4(NO2-4)∙PhH (1). По данным рентгеноструктурного анализа, проведенного при 293 К на автоматическом четырехкружном дифрактометре D8 Quest Bruker (двухкоординатный CCD - детектор, Мо К α-излучение, λ = 0,71073 Å, графитовый монохроматор) кристалла 1 [C41H39N2O3Sb, M 729,49; сингония моноклинная P 21/ n , группа симметрии Р 21/ n ; параметры ячейки: a = 10,332(4), b = 34,482(16), c = 10,631(6) Å; β = 100,172(13) град.; V = 3728(3) Å3; размер кристалла 0,5×0,45×0,26 мм; интервалы индексов отражений -14 ≤ h ≤ 13, -49 ≤ k ≤ 49, -15 ≤ l ≤ 15; всего отражений 116265; независимых отражений 11360; Rint 0,0479; GOOF 1,250; R 1 = 0,0585, wR 2 = 0,1089; остаточная электронная плотность 1,14/-2,74 e/Å3], атомы сурьмы имеют искаженную тригонально-бипирамидальную координацию с атомами углерода и кислорода в аксиальных положениях (угол СSbO 175,63(11)°). Расстояние Sb-O составляет 2,151(2) Å), длины связей Sb-C изменяются в узком интервале значений (2,115(4)-2,193(3) Å). Структурная организация в кристалле 1 обусловлена слабыми межмолекулярными контактами типа О···Н 2,47-2,68 Å. Полные таблицы координат атомов, длин связей и валентных углов для структуры 1 депонированы в Кембриджском банке структурных данных (№ 2126491; deposit@ccdc.cam.ac.uk; https://www.ccdc.cam.ac.uk).
4-нитробензальдоксим, пента(пара-толил)сурьма, сольват, бензол, 4-нитробензальдоксимат тетра(пара-толил)сурьмы, синтез, строение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147238620
IDR: 147238620 | УДК: 546.865+547.47+548.312.5 | DOI: 10.14529/chem220305
Tetra(para-tolyl)antimony 4-nitrobenzaldoximate solvate with p-Tol4SbON=CHC6H4(NO2-4)•PhH. Synthesis and structure
The p -Tol4SbON=CHC6H4(NO2-4)∙PhH solvate (1) has been synthesized by interaction of equimolar amounts of penta( para -tolyl)antimony and 4-nitrobenzaldoxime in benzene, they it has been structurally characterized. according to X-ray diffraction analysis performed at 293 K on an automatic four-circle diffractometer D8 Quest Bruker (two-coordinate CCD detector, Mo Kα radiation, λ = 0.71073 Å, graphite monochromator), crystals 1 [C41H39N2O3Sb, M 729.85; monoclinic system, space group Р21/n; cell parameters: a = 10.332(4), b = 34.482(16), c = 10.631(6) Å; β = 100.172(13) град.; V = 3728(3) Å3; crystal size 0.5 × 0.45 × 0.26 mm; index ranges -14 ≤ h ≤ 13, -49 ≤ k ≤ 49, -15 ≤ l ≤ 15; total reflections 116265; independent reflections 11360; Rint 0.0479; GOOF 1.250; R 1 = 0.0585, wR 2 = 0.1089; residual electron density 1.14/-2.74 e/Å3], have a distorted trigonal-bipyramidal coordination with the carbon and oxygen atoms in axial positions (axial angles are 175.63(11)°). The Sb-O distances are 2.151(2) Å, the Sb-C bond lengths vary within a narrow range of values (2.115(4)-2.193(3) Å). Structural organization in crystals is due to weak intermolecular contacts of the O···H type 2.47-2.68 Å. Complete tables of atomic coordinates, bond lengths, and bond angles for the structures are deposited at the Cambridge Crystallographic Data Center (No. 2126491; deposit@ccdc.cam.ac.uk; https://www.ccdc.cam.ac.uk).
Текст научной статьи Сольват 4-нитробензальдоксимата тетра(пара-толил)сурьмы с бензолом p-Tol4SbON=CHC6H4(NO2-4)•PhH. Синтез и строение
К настоящему времени достаточно хорошо изучены методы синтеза арильных производных сурьмы общей формулы Ph4SbX, среди которых следует выделить их эффективное получение из пентаарилсурьмы и кислоты НХ [1]. Так, описаны реакции пентафенилсурьмы с сульфоновыми кислотами [2 - 4], фенолами [5, 6], карбоновыми кислотами [7 - 10], р -дикетонами [11, 12], оксимами [13,14]. Пентафенилсурьма может реагировать с двумя молями кислоты с образованием соответствующих аддуктов Ph 4 SbOC(O)CH3 - CH3C(O)OH и Ph 4 SbONO 2 - HNO 3 [15].
В то же время показано, что взаимодействие диоксима метилендициклопентанона-2,2’ с пен-тафенилсурьмой в жестких условиях (90 ° С, 5 ч) при мольном соотношении исходных реагентов 1:2 соответственно приводит к образованию макроциклического сурьмаорганического соединения - бис - ц - [(метилендициклопентанон-2,2’-диоксимато)трифенилсурьмы], в молекулах которого симметричные диоксимные радикалы чередуются со структурными блоками трифенилсурьмы [16].
Отметим также, что при взаимодействии оксима ацетофенона с пента( пара- толил)сурьмой и оксима циклогексанона с пентафенилсурьмой (1:1 моль.) при нагревании реакционной смеси в течение часа на водяной бане образовывался бис (ацетофеноноксимат) три( пара -толил)сурьмы (выход 89 %) и бис (циклогексаноноксимат) трифенилсурьмы (выход 66 %). Если же реакцию проводили при комнатной температуре, то выделяли соответственно бензофеноноксимат тетра( пара -толил)сурьмы (выход 93 %) и циклогексаноноксимат тетрафенилсурьмы (выход 70 %) [17].
В продолжение исследования реакционной способности пента( пара -толил)сурьмы с кислотами изучено ее взаимодействие с 4-нитробензальдоксимом в бензоле.
Экспериментальная часть
Синтез 4-нитробензальдоксимата тетра(пара-толил)сурьмы (1). Смесь 0,15 г (0,26 ммоль) пента(пара-толил)сурьмы и 0,043 г (0,26 ммоль) 4-нитробензальдоксима в 15 мл бензола нагрева- ли до образования гомогенного раствора, цвет которого изменялся со временем на лимонножелтый, добавляли 2 мл октана и медленно концентрировали до объема 3 мл (24 ч) при комнатной температуре. Получили 0,15 г (79 %) бледно-желтых кристаллов 1 с т. разл. 115 °С.
Найдено: C 67,31; H 5,41. C 41 H 39 N 2 O 3 Sb. Вычислено: C 67,44; H 5,35.
ИК-спектр, ( ν , см - 1): 3067, 3032, 2918, 2864, 1593, 1556, 1506, 1491, 1477, 1391, 1339, 1331, 1312, 1260, 1211, 1188, 1169, 1109, 1059, 984, 920, 885, 841, 795, 752, 694, 679, 635, 582, 569, 548, 536, 486.
Элементный анализ на C и H выполнен на элементном анализаторе Carlo Erba CHNS-O EA 1108.
Температура плавления измерена на приборе SMP 30 Melting Point.
ИК-спектр записывали на ИК-Фурье спектрометре Shimadzu IRAffinity-1S в таблетке KBr в области 4000 - 400 см - 1.
Рентгеноструктурный анализ ( РСА ) кристалла 1 проведен на автоматическом четырехкружном дифрактометре D8 QUEST фирмы Bruker (Mo K α -излучение, λ = 0,71073 Å, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены с помощью программ SMART и SAINT-Plus [18]. Все расчеты по определению и уточнению структур выполнены с помощью программ SHELXL/PC [19] OLEX2 [20]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Положение атомов водорода уточняли по модели наездника ( U изо (H) = 1,2 U экв (C)). Кристаллографические данные и результаты уточнения структур приведены в табл. 1, геометрические характеристики координационного полиэдра атома сурьмы – в табл. 2.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры 1
|
Параметр |
Соединение 1 |
|
Формула |
C 41 H 39 N 2 O 3 Sb |
|
М |
729,49 |
|
Т , К |
293 |
|
Сингония |
Моноклинная |
|
Пр. группа |
P 2 1 / n |
|
a , Å |
10,332(4) |
|
b, Å |
34,482(16) |
|
c, Å |
10,631(4) |
|
α ,º |
90,00 |
|
β,º |
100,172(13) |
|
γ ,º |
90,00 |
|
V , Å3 |
3728(3) |
|
Z |
4 |
|
ρ (выч.), г/см3 |
1,300 |
|
µ , мм–1 |
0,778 |
|
F (000) |
1496,0 |
|
Размер кристалла, мм |
0,5 × 0,45 × 0,26 |
|
Область сбора данных по 2 θ , град. |
6,12 - 61,36 |
|
Интервалы индексов отражений |
- 14 ≤ h ≤ 13, - 49 ≤ k ≤ 49, - 15 ≤ l ≤ 15 |
|
Измерено отражений |
116265 |
|
Независимых отражений |
11360 |
|
R int |
0,0479 |
|
Переменных уточнения |
428 |
|
GOOF |
1,250 |
|
R -факторы по F2 > 2 σ (F2) |
R 1 = 0,0585, wR 2 = 0,1089 |
|
R-факторы по всем oтражениям |
R 1 = 0,0751, wR 2 = 0,1134 |
|
Остаточная электронная плотность (min/max), e/A3 |
1,14/ - 2,74 |
Химия элементоорганических соединений
Таблица 2
Длины связей и валентные углы в соединении 1
|
Связь |
d , A |
Угол |
co, град. |
|
Sb(1) - 0(1) |
2,151(2) |
O(1)Sb(1)С(31) |
175,63(11) |
|
Sb(1) - C(21) |
2,122(4) |
C(21)Sb(1)O(1) |
88,50(12) |
|
Sb(1) - C(31) |
2,193(3) |
C(21)Sb(1)C(31) |
92,84(13) |
|
Sb(1) - C(11) |
2,126(4) |
C(21)Sb(1)C(11) |
121,85(14) |
|
Sb(1) - C(1) |
2,115(4) |
C(11)Sb(1)O(1) |
82,12(12) |
|
N(1) - O(1) |
1,364(4) |
C(11)Sb(1)С(31) |
93,65(14) |
|
N(1) - C(47) |
1,275(4) |
C(1)Sb(1)С(21) |
118,62(14) |
|
O(2) - N(2) |
1,216(5) |
C(1)Sb(1)C(11) |
118,29(14) |
|
N(2) - O(3) |
1,218(5) |
N(1)O(1)Sb(1) |
108,08(19) |
Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2126491; ; .
Обсуждение результатов
Найдено, что продуктом реакции пента( пара -толил)сурьмы с 4-нитробензальдоксимом в бензоле является сольват 4-нитробензальдоксимата тетра( пара -толил)сурьмы с бензолом:
PhH p-Tol5Sb + HON=CHC6H4(NO2-4) ^ p-Tol4SbON=CHC6H4(NO2-4) • PhH + p-TolH 1
Светло-желтые прозрачные кристаллы 1 выделялись из реакционной смеси в течение 24 ч. Кристаллы 1 устойчивы к действию влаги и кислорода воздуха, растворимы в ацетоне, ароматических углеводородах, хлороформе и диоксане.
По данным РСА, в 1 атомы сурьмы имеют искаженную тригонально-бипирамидальную координацию с атомами углерода и кислорода в аксиальных положениях (см. рисунок), угол O(1)Sb(1)C(31) составляет 175,63(11) ° , что попадает в интервал значений аксиальных углов в соединениях типа Ar4SbONCRR' (171,31 - 178,8 ° [21]). Значения углов между аксиальными и экваториальными связями C(1)Sb(1)O(1), C(11)Sb(1)O(1), C(21)Sb(1)O(1) (88,34(12), 82,12(12),
88,50(12) ° ) меньше 90 ° , в то время как углы C(1)Sb(1)C(31), C(11)Sb(1)C(31), C(21)Sb(1)C(31) (94,65(13), 93,65(14), 92,84(13) ° ) превышают это значение, что является следствием выхода атома сурьмы из экваториальной плоскости на 0,1374 Å в сторону аксиального атома углерода. Углы в экваториальной плоскости C(1)Sb(1)С(11), C(1)Sb(1)С(21), C(11)Sb(1)С(21) равны 118,29(14); 118,62(14); 121,9(1) ° .
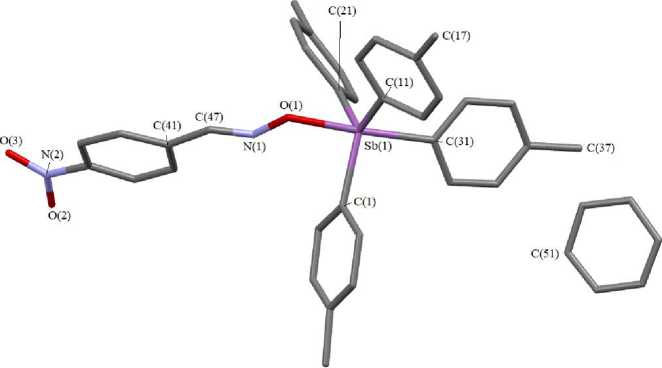
Рис. 1. Строение сольвата соединения 1 с бензолом
Экваториальные связи Sb(1) - C(1), Sb(1) - C(11), Sb(1) - C(21) (2,115(4), 2,126(4), 2,122(4) A) короче аксиальной связи Sb(1) - C(31) (2,193(3) A). Длина связи Sb(1) - O(1) (2,151(2) A) несколько выше суммы ковалентных радиусов указанных атомов (2.14 Å [22]).
Расстояние N(1) - C(47) в оксиматной группе составляет 1,375(5) A, что сравнимо с аналогичными расстояниями, наблюдаемыми в других оксиматах тетраарилсурьмы [23], длина связи N(1) - O(1) равна 1,364(4) A. Плоскость нитрогруппы не совпадает с плоскостью бензольного кольца, угол между соответствующими плоскостями равен 17,42 ° . Длины связей N(2) - O(2) и N(2) - O(3) (1,216(5) и 1,218(5) A) соответствуют дробному порядку связи.
Структурная организация в кристалле 1 обусловлена слабыми межмолекулярными контактами типа О···Н (2,47–2,68 Å).
В ИК-спектре соединения 1 наблюдаются интенсивные полосы поглощения при 486 см–1, отвечающих валентным колебаниям связей Sb-C. Полосы поглощения валентных колебаний метильных групп в арильных заместителях расположены при 2918 см–1 (асимметричные колебания) и при 2864 см–1 (симметричные колебания). Характерные полосы валентных колебаний углеродного скелета ароматических фрагментов имеют место при 1506, 1490, 1449 см–1. Валентным колебаниям связей CAr–H отвечает полоса поглощения средней интенсивности при 3069 см–1, внепло-скостным деформационным колебаниям этих же связей – полосы при 841, 795 и 752 см–1, плоскостным деформационным колебаниям – полосы при 1059 и 1033 см–1. В ИК-спектре присутствуют также полосы поглощения, характеризующие колебания связей в оксиматном лиганде: 1595 см–1 (C=N), 1547 см-1 (vas NO2), 1338 см-1 (vs NO2), 952 см-1 (N-O). Отметим, что в 4- нитробензальдоксиме соответствующие полосы поглощения находятся при 1605, 1537, 1350, 943 см–1. ИК-спектр соединения 1 хорошо согласуется с литературными данными [24–26].
Выводы
Установлено, что взаимодействие эквимолярных количеств пента( пара -толил)сурьмы с 4-нитробензальдоксимом в бензоле приводит к образованию сольвата 4-нитробензальдоксимата тетра( пара -толил)сурьмы с бензолом, в котором атом сурьмы имеет искаженную тригонально-бипирамидальную координацию с атомом кислорода в аксиальном положении.
Выражаю признательность профессору В.В. Шарутину за рентгеноструктурный анализ кристалла соединения 1 и помощь при работе над статьей.
Список литературы Сольват 4-нитробензальдоксимата тетра(пара-толил)сурьмы с бензолом p-Tol4SbON=CHC6H4(NO2-4)•PhH. Синтез и строение
- Шарутин В.В., Поддельский А.И., Шарутина О.К. Синтез, реакции и строение арильных соединений пятивалентной сурьмы. Коорд. химия. 2020. Т. 46, № 10. С. 579-648. DOI: 10.31857/S0132344X20100011.
- Сульфонаты тетра- и триарилсурьмы / В.В. Шарутин, О.К. Шарутина, Л.П. Панова и др. // Журн. общ. химии. 1997. Т. 67, № 9. С. 1531-1535.
- Синтез и строение органосульфонатов тетра- и трифенилсурьмы / В.В. Шарутин, О.К. Шарутина, А.П. Пакусина и др. // Коорд. химия. 2004. Т. 30, № 1. С. 15-24.
- Синтез и строение сурьма- и висмуторганических производных 4-сульфофенола и 2,4-дисульфофенола / В.В. Шарутин, И.В. Егорова, А.П. Пакусина и др. // Коорд. химия. 2007. Т. 33, № 3. С. 176-183.
- Реакции пентаарилсурьмы с орто-замещенными фенолами / В.В. Шарутин, О.К. Шарутина, П.Е. Осипов и др. // Журн. общ. химии. 1997. Т. 67, № 9. С. 1528-1530.
- Арокситетраарильные соединения сурьмы. Синтез, строение и термическое разложение / В.В. Шарутин, О.К. Шарутина, П.Е. Осипов и др. // Журн. общ. химии. 2000. Т. 70, № 6. С. 931936.
- Синтез и термическое разложение производных ацилокситетрафенилсурьмы / O.K. Шарутина, B.B. Шарутин, B.C. Сенчурин и др. // Изв. РАН. Сер. хим. 1996. Vol. 45, № 1. С. 186-190. DOI: 10.1007/bf01433760.
- Sharutin V.V., Sharutina O.K., Pakusina A.P., Belsky V.K. Reactions of Pentaphenylantimony with Dicarboxyclic Asids. J. Organometal. Chem. 1997. Vol. 536, no. 1. P. 87-92.
- Синтез и строение кислого фталата тетрафенилсурьмы / В.В. Шарутин, О.К. Шарутина, И.Г. Мельникова и др. // Изв. АН. Сер. хим. 1996. № 8. С. 2082-2085.
- Синтез и строение пентафторбензоата тетрафенилсурьмы и нитрата тетра-и-толилсурьмы / В В. Шарутин, О К. Шарутина, Е.А. Бондарь и др. // Коорд. химия. 2001. Т. 27, № 6. С. 423-427.
- Синтез р-дикетонатов тетраарилсурьмы из пентаарилсурьмы и р-дикетонов / В.В. Шарутин, О.К. Шарутина, О.П. Задачина и др. // Журн. общ. химии. 2000. Т. 70, № 5. С. 746-747.
- Синтез и строение хлорацетилацетоната тетрафенилсурьмы / В.В. Шарутин, О.К. Шарутина, О.П. Задачина и др. // Журн. общ. химии. 2000. Т. 70, № 10. С. 1672-1674.
- Синтез и строение оксиматов тетра- и триарилсурьмы / В.В. Шарутин, О.К. Шарутина, О.В. Молокова и др. // Журн. общ. химии. 2001. Т. 71, № 8. С. 1317-1321.
- Синтез и строение оксиматов тетрафенилсурьмы / В.В. Шарутин, О.К. Шарутина, О.В. Молокова и др. // Журн. общ. химии. 2000. Т. 70, № 12. С. 1990-1996.
- Синтез и строение аддуктов нитрата тетрафенилсурьмы с азотной кислотой и ацетата тетрафенилсурьмы с уксусной кислотой / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина, Л.П. Панова // Журн. неорган. химии. 2008. Т. 53, № 7. С. 1194-1198.
- Синтез и строение бис-ц-[(метилендициклопентанон-2,2'-диоксимато)трифенилсурьмы] / В.В. Шарутин, О.В. Молокова, О.К. Шарутина, Е.А. Алябьева, Ю.А. Кухарев и др. // Коорд. химия. 2005. Т. 31, № 3. С. 172-176.
- Синтез и строение диоксиматов триарилсурьмы / В.В. Шарутин, О.В. Молокова, О.К. Шарутина и др. // Журн. общ. химии. 2004. Т. 74, № 10. С. 1600-1607.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures From Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Dolomanov O.V., Bourhis L.J., Gildea R.J., Howard J.A.K., & Puschmann H. OLEX2: Complete Structure Solution, Refinement and Analysis Program // J. Appl. Cryst. 2009. Vol. 42. P. 339- 341. DOI: 10.1107/S0021889808042726.
- Шарутина О.К., Шарутин В.В. Молекулярные структуры органических соединений сурьмы (V): монография. Издательский центр ЮУрГУ; Челябинск. 2012. 395 с.
- Covalent Radii Revisited / B. Cordero, V. Gomez, A.E. Platero-Prats et al. // Dalton Trans. 2008. P. 2832. DOI: 10.1039/B801115J
- The Cambridge Crystallographic Database. Release. 2021. Cambridge. http: //www .ccdc.cam.ac.uk.
- Тарасевич Б.Н. ИК-спектры основных классов органических соединений: справочные материалы. М.: МГУ; Москва, 2012. 54 с.
- Васильев, А.В., Гриненко, Е.В., Щукин А.О. Инфракрасная спектроскопия органических и природных соединений: учебное пособие. СПб.: СПбГЛТА, 2007. 54 с.
- Spectral Database for Organic Compounds, SDBS. Release 2021. National Institute of Advanced In-dustrial Science and Technology.


