Сорбция ионов аминокислот фосфорнокислыми катионообменниками
Автор: Бондарева Л.П., Корниенко Т.С., Овсянникова Д.В., Григорова Е.В.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Фундаментальная и прикладная химия, химическая технология
Статья в выпуске: 4 (62), 2014 года.
Бесплатный доступ
Изучено влияние природы сорбента и кислотности раствора незаменимой кодируемой аминокислоты - метионина на его взаимодействие с фосфорнокислыми ионообменниками КРФ-5п и КФ-7 в протонированной форме с использованием калориметрического, сорбционного и спектроскопического методов. С использованием уравнений изотерм ионного обмена, материального баланса и констант диссоциации аминокислоты рассчитаны обменные и необменные сорбционные емкости. Установлено, что независимо от количества функциональных групп в ячейке полимерной матрицы, коэффициенты сорбционного равновесия для обоих катионообменников близки, а значения сорбционной емкости по аниону метионина несколько выше, чем по биполярной форме. Прямым калориметрическим методом определены энтальпии сорбции метионина при различных степенях заполнения ионообменника, показано, что при одинаковых степенях заполнения сорбентовэнтальпии сорбции на КФ-7 ниже, чем на КРФ-5п.Проведенные исследования позволили предположить, что из кислого раствора при низких степенях заполнения поглощается биполярный ион метионина, ион водорода протонированныхионообменников не вытесняется в раствор, а переходит к карбоксильной группе аминокислоты, нейтрализуя ее отрицательный заряд. Из щелочной среды при невысоких концентрациях метионина наиболее вероятна ионообменная сорбция с переносом протона от ионогенной группы катионообменника к карбоксильной группе метионина. Установлено, что на сорбцию аминокислотывлияет, главным образом, расположение активных групп в матрице сорбента и форма поглощаемой аминокислоты. Показано, что первичными сорбционными центрами являются функциональные группы ионообменников, а дополнительными - поглощенные аминокислоты, участвующие в сорбат-сорбатном взаимодействии.
Фосфорнокислые катионообменники, метионин, обменная и необменная сорбция
Короткий адрес: https://sciup.org/14040306
IDR: 14040306 | УДК: 544.726+547.466
Sorption of amino acids on phosphate cation exchangers
Influence of the nature of a sorbent and acidity of solution of the irreplaceable coded amino acid - methionine on its interaction with phosphate ion exchangers KRF-5p and KF-7 in the protonated form with use of calorimetric, sorption and spectroscopic methods is studied. With use of the equations of isotherms of an ionic exchange, material balance and constants of dissociation of amino acid exchange and not exchange sorption capacities are calculated. It is established that irrespective of number of functional groups in a cell of a polymeric matrix, coefficients of sorption balance for both cation exchangers are close, and values of sorption capacity on anion of methionine are slightly higher, than in a bipolar form. The direct calorimetric method determined enthalpies of sorption of methionine at various extents of filling of an ion exchanger, is shown that at identical extents of filling of sorbents of an enthalpy of sorption is one KF-7 lower, than on KRF-5p. The conducted researches allowed to assume that from sour solution at low extents of filling the bipolar ion of methionine is absorbed, an ion of hydrogen of the protonated ion exchangers, not forced out in solution, and passes to carboxyl group of amino acid, neutralizing its negative charge. From the alkaline environment at low concentration of methionine ion-exchange sorption with transfer of a proton from ionogenic group of the cation exchanger to carboxyl group of methionine is most probable. It is established that sorption of amino acid is influenced, mainly, by an arrangement of active groups in a matrix of a sorbent and a form of the absorbed amino acid. It is shown that primary sorption centers are functional groups of ion exchangers, and additional - the absorbed amino acids.
Текст научной статьи Сорбция ионов аминокислот фосфорнокислыми катионообменниками
Имеющийся экспериментальный и теоретический материал, посвященный взаимодействию в системах ионообменник – раствор аминокислоты, свидетельствует о существенном влиянии кислотности раствора и ионной формы сорбента на реакции с бифункциональными соединениями [1-3]. Незаменимая кодируемая аминокислота – метионин участвует в синтезе биологически важных соединений, липидном обмене других аминокислот, активирует действие гормонов, витаминов группы В, ферментов, обезвреживает токсические продукты. В свою очередь, катионообменники с фосфоновыми группами –Р(О)(ОН)2 обладают специфическими особенностями сорбции в связи с наличием трех активных группировок: фосфорильного кислорода и двух кислотных гидроксилов. В работе установлены закономерности взаимодействия ионов метионина с фосфорнокислыми катионообменниками, различающимися плотностью функциональных групп.
В работе использовали D, L-метионин NH 3+
(met) марки «Reanal»: СН3–S–(CH2)2–CH–COO , предварительно перекристаллизованный из водного раствора и высушенный до постоянной массы при 323 К. Изменения ионной формы аминокислоты достигали добавлением в раствор гидроксида калия или соляной кислоты, водородный показатель раствора контролировали на иономере И-130 с помощью цепи, составленной из хлоридсеребряного и стеклянного электродов. В соответствии с величинами констант кислотно-основного равновесия р К 1 = 2,15 и р К 2 = 9,05 [4] метионин при рН < 0,15 существует в виде катионов, при рН > 11,05 – в виде анионов и в интервале 4,15 < рН < 7,05 – в виде биполярных ионов.
Сорбцию аминокислоты проводили на среднекислотных комплексообразующих фосфорнокислых катионообменниках КРФ-5п и КФ-7. Первый сорбент представляет собой фосфорилированный сополимер стирола с 5 % п-дивинилбензолом. КФ-7 получен сополимеризацией ди-β,β´-хлорэтилового эфира винилфосфоновой кислоты, винилацетата и 10 % дивинилбензола с последующим омылением эфирных групп. Сорбенты выпускаются в полупромышленных масштабах как высокоэффективные ионообменники, обладающие селективностью к катионам тяжелых металлов и некоторым органическим соединениям [5]. Полная обменная емкость, определенная потенциометрическим титрованием отдельных навесок ионообменников раствором гидроксида калия с концентрацией 0,1 моль/дм3 и рассчитанная по уравнению Гендерсона-Хассельбаха, составила для КРФ-5п 9,60 ммоль/г и для КФ-7 6,00 ммоль/г. Протонированную форму катионообменников получали по стандартной методике [1].
Сорбционное равновесие изучали методом переменных концентраций, для этого в колбы помещали навески катионообменника по (0,1 ± 0,00005) г в пересчете на сухое вещество и заливали 50 см3 раствора метионина с различной концентрацией на 24 часа при 298 К, периодически встряхивая. Содержание поглощенных ионов определяли по разности концентраций в исходном и равновесном растворах. Концентрацию метионина определяли на спектрофотометре UVМini-1240 при длине волны 211 нм [6].
Для определения состава ионообменни-ков после взаимодействия с аминокислотой использовали метод инфракрасной спектроскопии на «Specord IR–75» в интервале волновых чисел от 4000 до 400 см –1. Образцы воздушно-сухих ионообменников в изучаемых формах измельчали и запрессовывали в таблетки с бромидом калия в соотношении 1:100. Интерпретацию спектров осуществляли, используя литературные данные [1, 7].
Тепловые эффекты взаимодействия метионина и ионообменников определяли на калориметрической установке, описанной в [8]. Стеклянные ампулы последовательно взвешивали с точностью ±0,0001 г до и после внесения навески сорбента и закрепляли с помощью держателей по кругу в кассету, расположенную на крышке калориметрического сосуда. В калориметрический сосуд калиброванной пипеткой вносили раствор метионина объемом 50,00 ± 0,05 см3 с необходимой кислотностью и концентрацией, близкой к максимальной сорбции. Термостатирование проводили до установления теплового равновесия в калориметрической ячейке при 298 К, после чего последовательно разбивая ампулы, смешивали раствор метионина с навесками ионообменни-ка. По результатам измерений строили кривую хода калориметрического опыта и определяли изменения температур в калориметрическом сосуде при добавлении каждой порции сорбента и при калибровке [9]. Энтальпию взаимодействия ионов метионина с фосфорнокислыми ионообменниками рассчитывали с учетом тепловых эффектов параллельно протекающих процессов. В отдельных опытах определяли энтальпию набухания ионообменников смешением навески сорбента с водой. Погрешность определения не превышала 1,5 %.
Типичные изотермы сорбции метионина на фосфорнокислых катионообменниках КРФ-5п и КФ-7 приведены на рисунке 1. В общем случае, на протонированной форме сорбентов из кислых и нейтральных растворов возможно поглощение биполярного иона, а из щелочных - аниона.
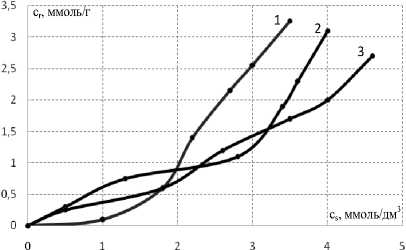
Рисунок 1. Изотермы сорбции метионина из растворов с рН 5,5 (1), 2,0 (2) и 10,5 (3) на протонированной форме КФР-5п при 298 К.
Вид изотерм сорбции на КРФ-5п свидетельствует о том, что при степенях заполнения ионообменника до 20 % поглощение как биполярного иона, так и аниона метионина происходит практически одинаково. С ростом степени заполнения сорбента происходит насыщение первичных активных центров, после чего наблюдается дополнительное поглощение.
При 0,15 < рН < 4,15 аминокислота в растворе находится в форме катиона и биполярного иона, а в катионообменниках в виде катиона, в области 7,05 < рН < 11,05 метионин в растворе находится в форме аниона и биполярного иона, а в катионообменниках – биполярного иона. Для описания распределения аминокислоты между фазами, воспользовав- шись уравнениями материального баланса и константы диссоциации аминокислоты [3], получили значения концентраций отдельных ионных форм аминокислоты (сак±, са ):
_ СЕ • K i сн +
± = c ^ + K i C h + + K i K 2 и
_ СЕ • KK ак- " c^ + Ki Ch + + Ki K2
Линейное уравнение сорбции биполярного иона или аниона метионина (в общем виде cr ) на протонированной форме катионооб-менников имеет вид:
1111 c 2H + + K i • cH + + K i • K 2
-- — -^= —--1—~- •------------------------ cr cr СЕ K~i сS • CH+ где СЕ – сорбционная емкость ионообменника ~ по иону аминокислоты, К – коэффициент сорбционного равновесия по i-му иону аминокислоты, К~ — сЬ= • Ch+- , К1 и К2 - константы
‘ Ch + c, кислотно-основного равновесия метионина, сS – аналитическая концентрация аминокислоты.
Результаты расчета сорбционных характеристик фосфорнокислых катионообменни-ков по аниону и биполярному иону при 298 К приведены в таблице 1. Определено, что независимо от количества функциональных групп в ячейке полимерной матрицы, коэффициенты сорбционного равновесия для обоих катионо-обменников близки, а значения сорбционной емкости по аниону метионина несколько выше, чем по биполярной форме.
Т а б л и ц а 1
Сорбционные характеристики фосфорнокислых ионообменников в протонированной форме по метионину при 298 К
|
Катионообменник |
Поглощаемый ион метионина |
СЕ , ммоль/г |
СОЕ , ммоль/г |
p К ~ i |
|
КРФ-5п |
± met |
5,1 ± 0,2 |
1,0 ± 0,1 |
2,77 |
|
met– |
5,7 ± 0,3 |
1,3 ± 0,1 |
1,69 |
|
|
КФ-7 |
± met |
3,9 ± 0,2 |
0,9 ± 0,1 |
1,92 |
|
met– |
4,9 ± 0,2 |
1,1 ± 0,1 |
1,79 |
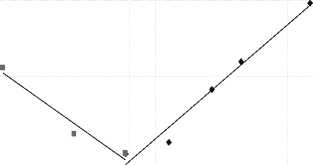
Поглощение метионина катионообмен-ником происходит со сменой природы сорбционного взаимодействия, что подтверждается изменением угла наклона изотерм, предло- 153
женных Кокотовым Ю.А. для обмена однозарядных ионов в линейных координатах [10] и приведенных на рисунке 2 для биполярного иона на протонированной форме КФР-5п :
сr
= СОЕ - CS^
1 K ~
( А Ст-
I cS 1 J
где СОЕ – сорбционная обменная емкость ионообменника по ионам метионина, K ~ –– коэффициент обменного равновесия ионов аминокислоты, с S 1 , c S 2 – молярные концентрации в равновесном растворе входящего 1 и выходящего 2 из ионообменника иона, то есть .
CS 2 c H +
0,007
0,006
0,005
0,004
0,003
0,002
0,001
y = -0,0049x + 0,0057
y = 0,006x - 0,003
0,000
0,00 0,10 0,20 0,30 0,40 0,50 0,60 0,70 0,80 0,90 1,00 1,10 1,20 1,30 1,40 1,50
Рисунок 2. Изотермы сорбции биполярного иона на протонированной форме КФР-5п в координатах
C r = f
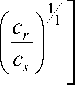
уравнения (3).
Обменная составляющая емкости кати-онобменников, рассчитанная по уравнению (3), по биполярным ионам метионина несколько выше, чем по анионам для обоих фосфорнокислых ионообменников (таблица 1). В целом обменные емкости ( СОЕ ) КРФ-5п и КФ-7 соизмеримы между собой, тогда как сорбционная обменная и необменная емкость (СЕ) выше для КРФ-5п.
O
II
R C H 2 P OH
OH
H 3 N
+ CH CH 2 S CH 3
OOC
Для идентификации соединений, образующихся в фазе ионообменника, методом ИК-спектроскопии исследованы системы КРФ-5п – ион метионина. На ИК-спектрах после сорбции метионина из раствора с рН 10,5 появляются максимумы в области 900-1000 см-1, асимметричные деформационные колебания аминогрупп сорбированных ионов проявляются в области 1630-1610 см-1 и симметричные – 1563-1546 см-1. Полоса колебаний –ОН-групп, соответствующая водородной связи фосфоновых групп, проявляется в области 2700-2650 см-1 и характерна для ионообменников в протонированной форме.
Можно предположить, что в системе, содержащей фосфорнокислый катионообмен-ник и метионин в водном растворе, будут осуществляться кислотно-основные равновесия диссоциации сорбента и метионина по двум ступеням в зависимости от рН. На межфазной поверхности и в фазе ионообменника могут реализовываться равновесия (4) и (5).
Проведенные исследования позволяют предположить, что из кислого раствора на протонированном катионообменнике поглощается биполярный ион метионина по уравнению (4) при низких степенях заполнения. Ион водорода протонированных ионнобменников не вытесняется в раствор, а переходит к карбоксильной группе аминокислоты, нейтрализуя ее отрицательный заряд. Из щелочной среды при невысоких концентрациях метионина наиболее вероятна ионообменная сорбция с переносом протона от ионогенной группы катионообмен-ника к карбоксильной группе метионина по уравнению (5). Взаимодействие метионина из щелочного раствора происходит не с водородной, а со смешанной протонированно-д епротонированной формой катионообм енника.
HO
+
R CH 2 P O H 3 N
O HOOC CH C H2 2 S CH3
O
R C H 2 P OH
OH
O
H 2 N
+ CH CH 2 S CH 3
OOC
R CH 2 P O H+ 3 N
O... HOOC
CH C H 2 2 S CH 3
Перенос протона от фосфоновой группы ионообменника к карбоксильной группе аминокислоты приводит к возможности возникновения сорбат-сорбатного взаимодействия, при котором ионообменно-поглощенный метионин становится дополнительным сорбционным центром. В результате значительно увеличива-
ется количество поглощенного метионина, благодаря необменной сорбции.
На сорбцию метионина фосфорнокислыми катионообменниками оказывает влияние расположение активных групп в матрице сорбента и форма поглощаемой аминокислоты. Различие же строения матрицы полимера – на одну ячейку в
КРФ-5п приходится две активные группы - PO(OH) 2 , а в КФ-7 только одна - практически не сказывается на сорбционных характеристиках фосфорнокислых катионообменников. Как в случае катионообменника с большим количеством функциональных групп (КРФ-5п), так и для сорбента с меньшей плотностью функциональных групп (КФ-7), сорбционные обменные емкости по аминокислоте сравнимы, как близки и коэффициенты обмена. Этот эффект связан с низкой способностью ионогенных групп КРФ-5п координироваться для наиболее выгодного соединения с сорбируемым ионом из-за достаточно плотного их расположения в ячейке полимера, относительно большого размера молекулы метионина и возникновением, вследствие этого, стерических затруднений.
Калориметрическим методом получены энтальпии набухания КРФ-5п (Н + ) -A sH = 9890 Дж/моль и КФ-7(Н + ) - A SH = 8560 Дж/моль, а также энтальпии сорбции метионина (∆ с Н ) из водных растворов с рН 10,5, показанные на рисунке 3. Сложный характер взаимодействия аниона метионина с фосфорнокислыми катионообменниками проявляется в отсутствии монотонности зависимости энтальпий сорбции от концентрации противоиона в фазе сорбента. Экзотермический эффект, совместно с положительными величинами показателя коэффициента обменного равновесия, можно трактовать как упрочение связи сорбированной аминокислоты с ионообменником по сравнению с раннее существовавшей связью.
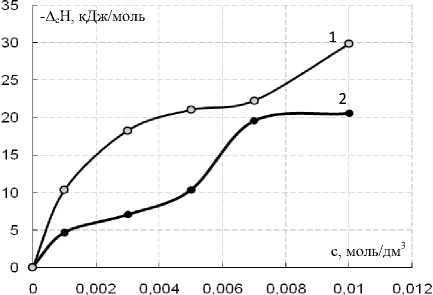
Рисунок 3. Зависимость энтальпий сорбции метионина КРФ-5п (1) и КФ-7 (2) из растворов с рН 10,5
Сравнение значений тепловых эффектов сорбции метионина протонированными формами фосфорнокислых катионообменников показывает, что при одинаковых степенях заполнения сорбентов ∆с Н на КФ-7 ниже, чем на КРФ-5п. Поскольку исходные растворы метионина одинаковы, можно предположить, что различие величин ∆с Н объясняется лишь изменениями, происходящими в фазах катионооб-менников, а именно стерическими затруднениями, возникающими при координации ионогенных групп КРФ-5п.
Таким образом, в работе определено, что сорбционные емкости и их обменные составляющие фосфорнокислых катионообменников по метионину сравнимы, так же близки и их коэффициенты обмена. На сорбцию аминокислоты оказывает влияние, главным образом, расположение активных групп в матрице сорбента и форма поглощаемой аминокислоты.
Работа выполнена в рамках НИОКР по ГК № 4.2186.2014/К по теме "Разработка и конструирование мобильного комплекса для экологического мониторинга состояния водных объектов с возможностью концентрирования органических и неорганических загрязнителей "на месте"".


