Состояние диффузной лимфоидной ткани тонкого кишечника мышей в условиях иммунодефицита и коррекции пептидным биорегулятором
Автор: Улзытуева Д.А., Лебедева С.Н.
Журнал: Вестник Восточно-Сибирского государственного университета технологий и управления @vestnik-esstu
Рубрика: Биологические науки
Статья в выпуске: 5 (50), 2014 года.
Бесплатный доступ
Изучено иммуномодулирующее действие пептидного биорегулятора на диффузную лимфоидную ткань тонкого кишечника мышей на фоне азатиоприновой иммуносупрессии. Установлено, что после введения мышам пептидного биорегулятора в собственной пластинке слизистой оболочки появляются клетки с картинами митозов, увеличивается содержание молодых форм клеток, плазматических клеток и макрофагов, снижается деструкция клеток. Эти факты свидетельствуют об усилении функциональной активности диффузной лимфоидной ткани кишки после действия пептидного биорегулятора.
Иммунная система, иммунодефицитные состояния, пептидный биорегулятор, лимфоидная ткань, тонкая кишка
Короткий адрес: https://sciup.org/142142961
IDR: 142142961 | УДК: 641.1:612.017.1
State of diffuse lymphoid tissue of mice’s small intestine with immunodeficiency and correction by peptide bioregulator
The immunomodulatory effect of peptide bioregulator on the diffuse lymphoid tissue of the mice ’s small intestine on the background of azathioprine immunosuppression was studied. It is found that after peptide bioregulators introduction to mice cells with mitosis appear in the lamina propria, the amount of young forms of cells, plasmatic cells and macrophages increases, the destruction of cells reduces. These facts indicate the intensification of the functional activity of the diffuse lymphoid tissue of the intestine after the action of peptide bioregulator.
Текст научной статьи Состояние диффузной лимфоидной ткани тонкого кишечника мышей в условиях иммунодефицита и коррекции пептидным биорегулятором
На сегодня неблагоприятная экологическая ситуация, психоэмоциональные перегрузки, злоупотребление медикаментозными средствами, нарушения в питании и многие другие факторы приводят к росту числа заболеваний, сопровождающихся снижением естественной резистентности организма.
Одним из основных способов поддержания нормального функционирования иммунной системы и восстановления иммунитета при иммунодефицитных состояниях является применение иммуномодуляторов [1].
В качестве иммуномодуляторов эндогенного происхождения применяются иммуноре-гуляторные пептиды, полученные из органов иммунной системы.
В настоящее время доказана регулирующая роль пептидов в развитии большинства биологических процессов, начиная с биохимических реакций, заканчивая дифференцировкой и функциональной активностью различных клеток и систем организма. Изучение закономерностей пептидной регуляции позволяет рассматривать их как природные корректоры, направленность и сила которых зависит от исходного уровня конкретного биологического процесса.
Ранее авторами был получен пептидный биорегулятор, обладающий нейротропной, адаптогенной и иммуномодулирующей активностью [2, 3, 4]. В частности, было доказано, что пептидный биорегулятор, выделенный из тимуса свиней, восстанавливает показатели клеточного и гуморального иммунитета, функцию макрофагов при экспериментальной аза-тиоприновой иммуносупрессии. Также установлено, что биорегулятор сохраняет свой иммуномодулирующий эффект в составе фаршевого мясного продукта.
Крупнейшим отделом иммунной системы является лимфоидная ткань желудочнокишечного тракта, которая входит в состав кишечно-ассоциированной лимфоидной ткани (КАЛТ) [5].
Тонкая кишка, имея обширную пограничную поверхность, находится в постоянном контакте с многочисленными антигенами, поступающими алиментарным путем.
В связи с тесным контактом с антигенами в слизистой оболочке тонкой кишки развивается мощная лимфоидная ткань, образующая иммунокомпетентную систему, в которой происходят реакции клеточного типа, а также сенсибилизация лимфоцитов с последующей дифференцировкой в плазматические клетки, синтезирующие иммуноглобулины.
В структурной и функциональной деятельности иммунной системы слизистой оболочки тонкой кишки значительное место занимают пейеровы бляшки, одиночные лимфоидные узелки и диффузная лимфоидная ткань, которые составляют 70-80% всех иммунных клеток [6].
В связи с этим исследование механизма действия пептидного биорегулятора на периферическую лимфоидную ткань пищеварительной системы позволяет судить о реактивности иммунной системы при воздействии антигенов, поступающих извне.
Целью настоящего исследования явилось изучение функционального состояния диффузной лимфоидной ткани различных отделов тонкого кишечника мышей в условиях иммунодефицита, вызванного азатиоприном, и коррекции пептидным биорегулятором.
Материал и методы исследования
Для проведения экспериментальных исследований были использованы белые беспородные мыши-самцы весом 22-25 г. Животные были разделены на 3 группы по 10 особей в каждой. Первая группа состояла из интактных животных. Во второй группе находились животные, получавшие перорально иммунодепрессант азатиоприн в дозе 50 мг/кг веса 1 раз в сутки в течение 5 дней. Третья группа животных после введения азатиоприна получала пептидный биорегулятор, вводимый аналогичным способом в дозе 0,1 мг/кг 1 раз в сутки в течение 7 дней.
По окончании проводимых серий экспериментов животных умерщвляли методом мгновенной декапитации под легким эфирным наркозом [7].
У животных всех экспериментальных групп выделяли проксимальный, средний и дистальный отделы тонкой кишки. Материал фиксировали в 10%-ном нейтральном формалине с последующей стандартной спиртовой проводкой и заливкой в парафин по общепринятой методике [8]. Из парафиновых блоков готовили срезы толщиной 4-6 мкм на микротоме, которые окрашивали гематоксилином и эозином. Подсчет клеток проводили при помощи микроскопа Биомед 6 при увеличении объектива - 90 под масляной иммерсией по методу С.Б. Стефанова с использованием 25-узловой морфометрической сетки (с шагом 10 мкм), вмонтированной в окуляр (9х) микроскопа [9].
Полученные результаты систематизировали и подвергли статистической обработке с помощью t-критерия Стьюдента.
Результаты и их обсуждение
У животных интактной группы в проксимальном отделе тонкой кишки (табл., рис. 1) преобладали клетки лимфоидного ряда, из них 36,7% приходилось на средние лимфоциты. Количество малых лимфоцитов в 4,0 раза меньше, чем средних. Среди молодых форм клеток преобладали бластные формы, содержание которых было в 1,8 раза больше, чем больших лимфоцитов. Собственная пластинка слизистой оболочки содержала довольно большое ко- личество плазматических клеток 6,6%. Содержание нейтрофилов, макрофагов, митотиче-ски делящихся клеток составило соответственно 0,3, 1,4 и 1,6%. Содержание стромальных клеток (ретикулоцитов, фибробластов и фиброцитов) составляло в сумме 12,2%.
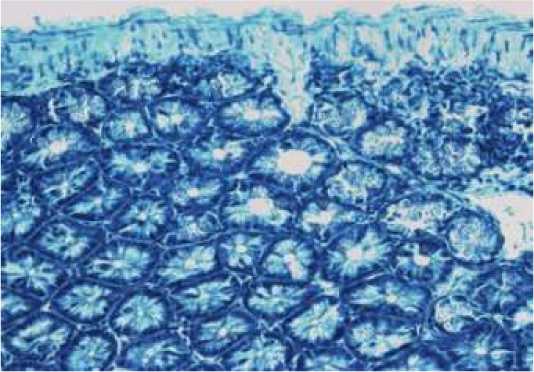
Рис. 1. Бруннеровы железы в собственной пластинке слизистой оболочки тонкой кишки интактной мыши (проксимальный отдел). Микрофотография. Фиксация – 10%-ный нейтральный формалин. Окраска гематоксилином-эозином (х 200)
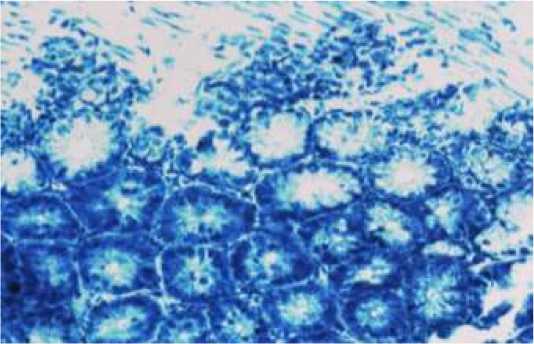
Рис. 2. Собственная пластинка слизистой оболочки тонкой кишки мыши после введения азатиоприна. Отек слизистой оболочки и массовая деструкция клеточных элементов (проксимальный отдел).
Микрофотография. Фиксация – 10%-ный нейтральный формалин. Окраска гематоксилином-эозином (х 200)
Гистологическое исследование препаратов стенки тонкой кишки мышей, подвергшихся воздействию азатиоприна, свидетельствовало о наличии воспалительно-деструктивных процессов. Наблюдались отек слизистой оболочки, подслизистой основы и массовая деструкция клеточных элементов (рис. 2). Так, содержание деструктивно измененных и разрушенных клеток в проксимальном отделе тонкой кишки увеличилось в 4,9 раза по сравнению с контролем. Клеточный анализ диффузной лимфоидной ткани в собственной пластинке слизистой оболочки данного отдела тонкой кишки показал резкое уменьшение количества клеток лимфоидного ряда: количество больших лимфоцитов уменьшилось в 8,5 раза, средних лимфоцитов – в 2,7 раза по сравнению с контролем. Содержание плазматических клеток уменьшилось в 2,4 раза. Митотически делящиеся клетки в слизистой оболочке кишки в данной группе животных не выявлены. Для данной группы животных характерно значительное увеличение содержания нейтрофилов (в 11,7 раз). Как известно, среди всех клеточных элементов нейтрофилы первыми появляются в зоне острого воспаления. Кроме того, введение аза тиоприна вызывало увеличение содержания стромальных клеток: ретикулоцитов – в 1,7 раза и клеток фибробластического ряда – в 8,0 раз.
После введения пептидного биорегулятора у опытных мышей отмечалась перестройка клеточного состава лимфоидных клеток, которая характеризовалась для проксимального отдела тонкой кишки увеличением количества больших лимфоцитов в 16,0 раза (рис. 3), средних лимфоцитов – в 2,3 раза и плазматических клеток – в 1,7 раза (по сравнению со 2-й группой).
Важным показателем действия пептидного биорегулятора на лимфоидную ткань собственной пластинки слизистой оболочки кишки являлась стимуляция репродуктивной функции лимфоидных клеток. После введения пептидного биорегулятора появлялись клетки с картинами митозов (1,0%), которые отсутствовали в интактной и азатиоприновой группах. Под воздействием пептидного биорегулятора в проксимальном отделе уменьшилось количество деструктивно измененных клеток – в 1,7 раза (по сравнению со 2-й группой), но их содержание в 2,8 раза все же превосходило данный показатель у интактных животных. Введение пептидного биорегулятора способствовало нормализации относительного числа ретикулярных клеток и уменьшению клеток фибробластического ряда, содержание которых на фоне воздействия азатиоприна уменьшилось в 1,1 раза, но все еще существенно превосходило данный показатель у интактных животных.
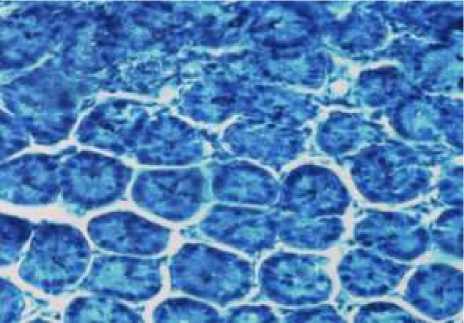
Рис. 3. Собственная пластинка слизистой оболочки мыши, получавшей пептидный биорегулятор после введения азатиоприна (проксимальный отдел). Микрофотография. Фиксация – 10%-ный нейтральный формалин. Окраска гематоксилином-эозином (х 200)
На продольных гистологических срезах лимфоидной ткани среднего отдела тонкой кишки (табл.) у интактных мышей внутренняя поверхность стенки кишки неровная, на ней видно большое количество крипт. Количество клеток лимфоидного ряда (бласты, большие, средние и малые лимфоциты и плазматические клетки) в собственной пластинке слизистой оболочки составило 65,2%.
При гистологическом исследовании препаратов среднего отдела кишки мышей после введения азатиоприна отмечались признаки иммунодепрессивного состояния. После воздействия азатиоприна клетки лимфоидного ряда встречались гораздо реже, чем в контроле (от 65,2 до 34,2%). На гистологических срезах кишки в собственной пластинке слизистой оболочки содержание деструктивно измененных и разрушенных клеток увеличилось до 18,7%, что превысило контрольные показатели почти в 3 раза.
Цитологический анализ лимфоидной ткани среднего отдела кишки мышей, получавших после введения азатиоприна пептидный биорегулятор, свидетельствовал о том, что у этих животных наблюдалось отчетливое восстановление общего числа лимфоидных клеток от 34,2 до 53,6%. Содержание деструктивно измененных и разрушенных клеток в собственной пластинке слизистой оболочки кишки данной группы экспериментальных животных снизилось по сравнению с показателями животных 2-й группы в 2,3 раза.
Таблица
Клеточный состав (в %) диффузной лимфоидной ткани собственной пластинки слизистой оболочки различных отделов тонкой кишки мышей в контроле и эксперименте (М±m)
|
Клетки/отдел |
Интактные животные (контроль) |
После введения азатиоприна |
После введения азатиоприна и пептидного биорегулятора |
||||||
|
1-я группа |
2-я группа |
3-я группа |
|||||||
|
Пр |
Ср |
Д |
Пр |
Ср |
Д |
Пр |
Ср |
Д |
|
|
Ретикулоциты |
10,4±1,3 |
8,5±0,9 |
7,3±0,8 |
17,8±0,9* |
20,2±1,3 |
23,5±2,3* |
14,3±1,2 |
10,7±0,6 |
6,2±0,7** |
|
Бласты |
12,3±0,4 |
5,4±3,1 |
0,7±0,1 |
16,7±0,3 |
12,3±2,7* |
10,3±0,4* |
11,7±2,3 |
6,1±1,8 |
3,9±0,3** |
|
Большие лимфоциты |
6,8±1,7 |
7,3±0,2 |
6,7±0,5 |
0,8±3,2* |
0,2±0,1* |
0,9±0,2* |
12,8±2,6** |
5,4±0,3** |
9,4±0,7** |
|
Средние лимфоциты |
36,7±3,6 |
35,8±3,6 |
38,1±3,5 |
13,8±2,7* |
11,5±2,2* |
8,9±1,2* |
31,5±1,4** |
19,0±3,5** |
11,6±1,3** |
|
Малые лимфоциты |
9,1±1,5 |
10,4±4,2 |
12,9±1,3 |
5,2±1,3 |
9,3±2,9* |
11,3±1,7* |
8,9±1,1 |
13,6±2,6** |
12,5±1,2** |
|
Плазмоциты |
6,6±1,2 |
6,3±1,4 |
8,7±0,9 |
2,7±0,5* |
0,9±0,1* |
- |
4,6±1,0** |
9,5±2,1** |
11,2±1,5 |
|
Нейтрофилы |
0,3±0,1 |
0,4±0,1 |
0,2±0,3 |
3,5±0,9* |
1,8±0,2 |
3,1±0,8 |
3,1±0,7 |
0,7±1,1 |
- |
|
Макрофаги |
1,4±0,2 |
1,2±0,6 |
1,1±0,2 |
1,9±0,3 |
0,3±0,1 |
- |
0,7±0,2 |
4,2±0,9 |
6,2±1,7 |
|
Митотически делящиеся |
1,6±0,3 |
1,5±0,2 |
- |
- |
- |
- |
1,0±0,1 |
0,8±1,0 |
0,9±0,1 |
|
Деструкции |
3,4±1,7 |
6,4±1,8 |
9,5±1,8 |
16,5±1,5* |
18,7±1,4* |
23,5±2,2* |
9,5±2,1** |
8,2±2,5** |
10,7±2,1** |
|
Фиброциты |
1,8±0,6 |
1,9±0,7 |
- |
14,4±2,3* |
7,3±0,8 |
6,8±1,4 |
13,0±2,0 |
7,5±1,3 |
8,3±0,3 |
Примечание. «-» в графах означает, что данные клетки не обнаружены; *, ** p<0,05 относи тельно 1-й или 2-й группы
Исследование цитоархитектоники диффузной лимфоидной ткани собственной пластинки слизистой оболочки дистального отдела тонкой кишки (см. табл.) у интактных мышей показало, что большая часть лимфоцитов из всех лимфоидных клеток относится к средним лимфоцитам – 38,1%. Малых лимфоцитов почти в 3 раза меньше (12,9%), чем средних. Среди молодых форм клеток преобладали большие лимфоциты, которые в 9,5 раза больше бластных форм клеток. В собственной пластинке слизистой оболочки тонкой кишки у интактных мышей встречались плазматические клетки (8,7%), а также были видны деструктивно измененные клетки 9,5%.
Введение мышам азатиоприна приводило к усилению деструктивных процессов в лимфоидной ткани дистального отдела. Содержание деструктивно измененных и разрушенных клеток увеличилось после действия азатиоприна в 2,5 раза по сравнению с контрольной группой. При этом общее содержание лимфоцитов снизилось от 67,1% в интактной группе до 31,4% в опыте. В собственной пластинке слизистой оболочки тонкой кишки отмечалось значительное нарушение процессов созревания молодых форм: число больших лимфоцитов уменьшилось после действия азатиоприна в 7,4 раза, средних лимфоцитов – в 4,3 раза в сравнении с интактной группой. Количество плазматических клеток незначительное. Число ретикулоцитов увеличилось в 3,2 раза, и появились фиброциты (6,8%), которые не обнаруживались в интактной группе.
После введения пептидного биорегулятора в собственной пластинке слизистой оболочки дистального отдела тонкой кишки в 2 раза уменьшилось число деструктивно измененных и разрушенных клеток (по сравнению со 2-й группой) и почти достигло показателей интактной группы мышей. В 1,5 раза увеличилось общее содержание лимфоцитов (от 31,4 до 48,6%), однако число различных популяций лимфоцитов изменялось в разной степени. Так, доля средних и больших лимфоцитов возросла по сравнению с показателями 2-й группы в 1,3 и 10,4 раза соответственно. Число бластных форм, наоборот, уменьшилось в 2,6 раза. В диффузной лимфоидной ткани собственной пластинки слизистой оболочки кишки после действия пептидного биорегулятора появлялись также плазматические клетки – 11,2%.
В ходе проведенного исследования установлено, что введение азатиоприна способствовало уменьшению содержания клеток лимфоидного ряда в проксимальном отделе тонкой кишки в 1,9 раза, в среднем – 1,9 раза и в дистальном – 2,1 раза (по сравнению с контролем). Наибольшее повреждающее действие азатиоприна проявилось в дистальном отделе тонкой кишки. При коррекции иммунодефицита, вызванного азатиоприном, пептидным биорегулятором, содержание клеток лимфоидного ряда в проксимальном отделе увеличилось в 1,8 раза, в среднем – в 1,6 раза и в дистальном – в 1,5 раза (по сравнению со 2-й группой).
Полученные экспериментальные данные согласуются с результатами исследований Д.Г. Бильдуевой (2001) [10] и Г.П. Ламажаповой (2001) [11] о том, что нарушения периферической лимфоидной ткани пищеварительной системы (в собственной пластинке слизистой оболочки подвздошной и слепой кишки), вызванные применением цитостатика азатиоприна, подвергаются коррекции природными средствами – активной фракцией, полученной из селезенки, и липосомальными структурами, содержащими жир байкальской нерпы.
Таким образом, исследование морфофункционального состояния диффузной лимфоидной ткани в собственной пластинке слизистой оболочки различных отделов (проксимальный, средний, дистальный) тонкой кишки мышей в условиях азатиоприновой иммуносупрессии и коррекции пептидным биорегулятором, позволило выявить изменения, направленные на восстановление ее структуры.
Работа выполнена при поддержке гранта «Молодые ученые и аспиранты ВСГУТУ 2014».


