Состояние сердечной гемодинамики и сократимости миокарда у пациентов с некоронарогенными желудочковыми аритмиями
Автор: Завадовский Константин Валерьевич, Саушкин Виктор Вячеславович, Лишманов Юрий Борисович, Хлынин Михаил Сергеевич
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 1 т.30, 2015 года.
Бесплатный доступ
Цель: оценить функциональное состояние сердца у пациентов с некоронарогенными желудочковыми аритмиями до и после интервенционного лечения. Материал и методы. В исследование вошли пациенты (n=22, средний возраст - 43,5±11,7 лет) с желудочковыми нарушениями ритма (ЖНР) сердца - желудочковой экстрасистолией (n=17) и пароксизмальной желудочковой тахикардией (n=5), которым в последующем была выполнена процедура радиочастотной аблации (РЧА) очагов эктопической активности. Группа сравнения включала 15 больных (средний возраст - 56,3±8,3 лет) без нарушений ритма сердца. Всем больным был выполнен полный комплекс клинико-лабораторных и инструментальных исследований, который включал радионуклидную равновесную томовентрикулографию (РТВГ). Результаты. У пациентов с ЖНР сердца, по отношению к лицам группы сравнения, отмечались повышенные значения объемных и сниженные значения скоростных показателей обоих желудочков. Также значения фракции выброса правого желудочка (ФВ ПЖ) у пациентов с ЖНР сердца были достоверно ниже, чем в группе сравнения (43,25±8,08 и 54,35±12,48% соответственно, p
Желудочковые аритмии, радионуклидная томовентрикулография, радиочастотная аблация
Короткий адрес: https://sciup.org/14919991
IDR: 14919991 | УДК: 616.12-008.318.1;
Cardiac hemodynamics and myocardial contractility in patients with ventricular arrhythmias
Objective: To evaluate cardiac function before and after radiofrequency ablation in patients with ventricular arrhythmias. Material and methods: The study included patients (n=22, mean age of 43 5±11.7 years) with ventricular arrhythmias (VA): premature ventricular beats (n=17) and paroxysmal ventricular tachycardia (n=5). Procedure of radiofrequency ablation (RFA) of ventricular arrhythmia was performed in 22 patients according to appropriate indications. Comparison group comprised 15 patients (mean age of 56.3±8.3 years) without cardiac arrhythmias. All patients underwent a complete clinical examination including gated blood pool SPECT (GBP-SPECT). Results. Compared with control group, patients with ventricular arrhythmia had moderate dilatation and reduced contractile function of both ventricles. The value of RV EF in patients with VA were significantly lower than in the control group (43.25±8.08% and 54.35±12.48%, p
Текст научной статьи Состояние сердечной гемодинамики и сократимости миокарда у пациентов с некоронарогенными желудочковыми аритмиями
В настоящее время нарушения ритма сердца являются важной медицинской и социальной проблемой. Аритмии значительно снижают качество жизни, приводят к инвалидизации пациентов, а некоторые виды из них нередко являются причиной внезапной смерти. Под желудочковыми нарушениями ритма (ЖНР) сердца понимают аритмии, источник которых расположен ниже атриовентрикулярного соединения – в каком-либо отделе внутрижелудочковой проводящей системы (пучке Гиса, его ножках или волокнах Пуркинье) или в миокарде желудочков [4]. В группу ЖНР сердца входят как крайне неблагоприятные – злокачественные формы, представляющее непосредственную угрозу для больного, так и относительно “благоприятные” – малосимптомные варианты, редко приводящие к развитию серьезных осложнений [4]. Последние составляют около 30% от общего числа ЖНР сердца и имеют разнообразную этиологию и патогенетическую основу [2].
Актуальной проблемой современной аритмологии и кардиологии является изучение малосимптомных аритмий, особенно в плане оценки прогноза течения указанной патологии [1]. Наиболее часто ЖНРС развиваются при остром инфаркте миокарда, миокардитах, кардиомиопатиях и пороках сердца [2, 4]. Вместе с тем в некоторых случаях установить природу возникновения нарушений ритма не удается, и тогда возникшую аритмию относят к идиопатической.
Длительное течение ЖНР приводит, в конечном итоге, к значительным структурным изменениям сердца – увеличению объема желудочков и изменению морфологии клеток [5, 11], что способствует развитию хронической сердечной недостаточности. В связи с этим ранняя оценка состояния гемодинамики и сократимости сердца при желудочковых аритмиях представляет собой актуальную задачу современной лучевой диагностики.
Цель работы – определение функционального состояния сердца у пациентов с некоронарогенными желудочковыми аритмиями до и после интервенционного лечения.
Материал и методы
В настоящее исследование включены пациенты (n=22), находившиеся на обследовании и лечении в НИИ кардиологии (Томск). Отбор тематических больных проводили по мере их поступления в отделение хирургического лечения сложных нарушений ритма сердца и электрокардиостимуляции, где всем пациентам выполняли комплексное клинико-функциональное обследование, включающее в себя сбор анамнеза, выявление жалоб, общий осмотр, определение общепринятых лабораторных показателей, электрокардиографию, допплер-эхокардиографию, рентгенографию грудной клетки, регистрацию ЭКГ в 12 стандартных отведениях, суточное мониторирование ЭКГ.
В группу исследования были включены пациенты с ЖНР сердца в возрасте от 20 до 59 лет (средний возраст – 43,5±11,7 лет; 7 мужчин, 15 женщин).
Критерием включения в группу исследования явились нарушения сердечного ритма, зарегистрированные при ЭКГ в 12 стандартных отведениях или холтеровском мониторировании – пароксизмальные неустойчивые (<30 с) мономорфные тахиаритмии или желудочковые экстрасистолии (редкие, частые). Критерии исключения: ишемическая болезнь сердца, миокардиты, пороки сердца, кардиомиопатии и другие верифицированные структурные поражения миокарда.
Большинству больных был выставлен диагноз изолированной желудочковой экстрасистолии (80%), у остальных (20%) желудочковая экстрасистолия сочеталась с пароксизмальной желудочковой тахикардией. Кроме того, практически у всех пациентов основной диагноз включал в себя гипертоническую болезнь и хроническую сердечную недостаточность I и II функциональных классов (по классификации Нью-Йоркской ассоциации кардиологов). Всем пациентам была выполнена процедура РЧА очагов эктопии.
В группу сравнения вошли пациенты (n=15; средний возраст – 56,3±8,3 лет) без нарушений ритма сердца, у которых по результатам полного клинико-инструмен- тального исследования были исключены заболевания и патологические процессы, которые могли привести к развитию желудочковых нарушений ритма сердца.
С целью определения состояния внутрисердечной гемодинамики и сократимости желудочков всем пациентам проводили ЭКГ-синхронизированную РТВГ с меченными 99m-технецием эритроцитами. Выполнение данного вида исследования было согласовано с этическим комитетом НИИ кардиологии. Все пациенты, вошедшие в исследование, подписывали информированное согласие.
Радионуклидная равновесная томовентрикулогра-фия. РТВГ выполняли на гамма-камере Forte (“Philips”, Niederland). Непосредственно перед исследованием проводили in vivo метку эритроцитов 99m-технецием по стандартной методике [3, 6]. Детекторы гамма-камеры устанавливали в положение 90° по отношению друг к другу. Область сердца располагали по центру поля зрения обоих детекторов. Запись информации выполняли в матрицу 64ґ64 пикселя в 64 проекциях (время экспозиции на одну проекцию – 45 с, оборот детекторов – 180°). Представительный сердечный цикл был разделен на 16 кадров. Синхронизацию записи сокращения сердца с ЭКГ осуществляли в фиксированном режиме, синхронно, с учетом коррекции аритмии и без него.
Обработка томовентрикулограмм включала в себя формирование аксиальных срезов исследуемой области (по серии нативных изображений) и последующую реконструкцию сечений сердца по короткой оси при помощи программы AutoSPECT+ ver: 3.5 (фильтр Butterworth).
По результатам фазового анализа были сформированы полярные карты, отражающие синхронность сокращения левого и правого желудочков, с помощью которых были вычислены следующие показатели: межжелудочковая диссинхрония (МЖД); правожелудочковая дис-синхрония (ПЖД); левожелудочковая диссинхрония (ЛЖД).
В процессе обработки изображений по кривым изгнания и наполнения вычисляли основные гемодинамические показатели для левого и правого желудочков: ФВ;
КСО; КДО; ударный объем (УО); максимальную скорость изгнания крови из желудочка сердца (МСИ); максимальную скорость наполнения желудочка сердца (МСН); среднюю скорость наполнения желудочка сердца за 1/3 диастолы (ССН/3); время максимума наполнения желудочка сердца (ВМН). Помимо абсолютных значений вычисляли индексированные на площадь поверхности тела (по формуле Мостеллера [8]) объемные показатели – конечно-систолический (КСИ), конечно-диастолический (КДИ) и ударный индексы (УИ).
Внутрисердечное электрофизиологическое исследование и радиочастотная аблация. Подготовку пациентов осуществляли по общим правилам проведения катетерных вмешательств на крупных сосудах. Электрофизиологическое исследование проводили по стандартному протоколу [7]. Во время диагностической стимуляции определяли возможность индуцирования и воспроизведения характерной для пациента желудочковой аритмии, а также предварительную локализацию очага тахикардии. С целью выявления “уязвимой” области аритмии использовали как методику стимуляционного картирования, так и способ катетерного картирования с выявлением “точки выхода” аритмии.
Критерием эффективности аблации фокуса аритмии считали прекращение экстрасистолической активности области эктопии и ее отсутствие при диагностической стимуляции, в том числе на фоне проведения фармакологических проб (атропиновой, обзидановой, изопроте-риноловой) [9, 10].
Статистический анализ. Для оценки нормальности распределения признака использовали критерий Колмогорова–Смирнова. Вычисляли среднее арифметическое значение (M) и стандартное отклонение (SD). Для оценки достоверности различий зависимых выборок использовали непараметрический критерий Вилкоксона, для независимых выборок – критерий Манна–Уитни.
Результаты и обсуждение
Состояние гемодинамики и сократимости желудочков сердца до процедуры радиочастотной аблации.
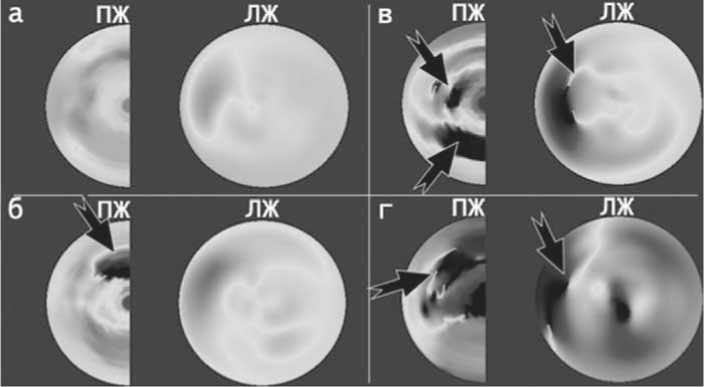
Рис. 1. Зоны асинхронного сокращения миокарда (АСМ) левого и правого желудочков: (а) – зоны АСМ не выявлены; (б) – единичная зона АСМ в выходном отделе ПЖ (ВОПЖ); (в) – зоны АСМ в проекции боковой и задней стенок ПЖ, а также в перегородочной области ЛЖ; (г) – зоны АСМ, расположенные в области перегородки ЛЖ и больших размеров зона в проекции боковой стенки с распространением на выходные отделы ПЖ
При анализе результатов РТВГ у пациентов с ЖНР сердца, по отношению к лицам группы сравнения (табл.1), были выявлены увеличенные объемные показатели левого желудочка и сниженные скоростные показатели обоих желудочков. Показатель ФВ ПЖ у пациентов с нарушением ритма был ниже, чем в группе сравнения. ФВ ЛЖ достоверно была значимо снижена, но не выходила за границы нормы.
В группе с ЖНР сердца мы наблюдали сниженную сократимость обоих желудочков, что сочеталось с более высокими значениями показателей, отражающих внутри- и межжелудочковую дис-синхронию. При этом более выраженное изменение отмечалось в правом желудочке. Однако значение межжелудочковой диссин-хронии не выходило за пределы нормы (<50 мс).
Выявленные изменения свидетельствуют о том, что при длительном течении ЖТ и ЖЭ формируется систолическая дисфункция миокарда, которая проявляется дилатацией желудочков и нарушением насосной функции сердца [1, 4].
По результатом фазового анализа, у всех пациентов с ЖНР сердца были выявлены локальные зоны асинхронного сокращения миокарда (АСМ) как правого, так и левого желудочков (рис. 1). Зоной асинхронного сокращения мы считали участок полярной кар
Таблица 1
Показатели гемодинамики и сократимости сердца в группе сравнения и у пациентов с ЖНР сердца до и после процедуры РЧА (M±SD)
Показатели
Группы сравнения Пациенты с ЖНРС Пациенты с ЖНРС p (1–2) p (2–3) (n=14) до РЧА (n=22) после РЧА (n=22)
Левый желудочек:
|
КДО (мл) |
128,42±19,53 |
|
КСО (мл) |
35,64±17,25 |
|
УО (мл) |
92,78±18,60 |
|
КДИ (мл/м2) |
63,38±6,56 |
|
КСИ (мл/м2) |
17,32±8,44 |
|
УИ (мл/м2) |
46,06±8,74 |
|
ФВ (%) |
72,64±12,16 |
|
МСИ (КДО/с) |
–3,68±0,92 |
|
МСН (КДО/с) |
2,9±0,83 |
|
ССН/3 (КДО/с) |
1,9±0,65 |
|
ВМН (мс) |
151,78±24,23 |
|
Правый желудочек: |
|
|
КДО (мл) |
142,25±30,51 |
|
КСО (мл) |
79,07±26,68 |
|
УО (мл) |
91,78±19,44 |
|
КДИ (мл/м2) |
76,40±15,73 |
|
КСИ (мл/м2) |
37,75±14,20 |
|
УИ (мл/м2) |
44,71±8,34 |
|
ФВ (%) |
54,35±12,48 |
|
МСИ (КДО/с) |
–2,78±0,79 |
|
МСН (КДО/с) |
2,02±0,74 |
|
ССН/3 (КДО/с) |
1,4±0,52 |
|
ВМН (мс) |
223,8±145,9 |
|
МЖД (мс) |
17,16±18,16 |
|
ЛЖД (мс) |
30,01±8,45 |
|
ПЖД (мс) |
69,63±14,16 |
|
143,66±44,86 |
125,16±47,46 |
0,02* |
0,002* |
|
64,83±40,22 |
56,08±39,84 |
0,001* |
0,1 |
|
78,83±18,28 |
69,00±17,30 |
0,95 |
0,13 |
|
77,60±25,82 |
68,02±27,71 |
0,02* |
0,002* |
|
35,35±22,94 |
30,90±22,76 |
0,0006* |
0,11 |
|
42,23±8,87 |
37,07±8,84 |
0,51 |
0,13 |
|
56,83±11,94 |
58,5±14,78 |
0,001* |
0,41 |
|
–2,54±0,61 |
–3,02±0,99 |
0,002* |
0,12 |
|
2,11±0,71 |
2,44±0,74 |
0,01* |
0,02* |
|
1,41±0,51 |
1,60±0,51 |
0,03* |
0,08 |
|
171,83±52,74 |
146,5±37,02 |
0,61 |
0,31 |
|
160,68±24,33 |
130,83±26,61 |
0,41 |
0,12 |
|
84,00±20,19 |
68,41±15,21 |
0,05* |
0,005* |
|
58,33±18,67 |
62,16±14,65 |
0,13 |
0,30 |
|
82,42±11,47 |
70,48±14,76 |
0,02* |
0,13 |
|
45,40±11,52 |
36,82±8,12 |
0,006* |
0,004* |
|
31,03±8,62 |
33,52±8,34 |
0,21 |
0,24 |
|
43,25±8,08 |
50,25±4,20 |
0,02* |
0,02* |
|
–1,96±0,48 |
–2,37±0,27 |
0,03* |
0,01* |
|
1,32±0,50 |
1,73±0,40 |
0,005* |
0,04* |
|
0,77±0,34 |
1,16±0,33 |
0,001* |
0,009* |
|
227,1±106,8 |
214,9±143,3 |
0,33 |
0,72 |
|
32,45±16,04 |
32,26±16,89 |
0,04* |
0,93 |
|
45,14±21,93 |
41,17±16,28 |
0,09* |
0,58 |
|
85,44±28,07 |
68,47±21,85 |
0,03* |
0,03* |
Примечание: ЖНРС – желудочковые нарушения ритма сердца; n – количество пациентов в группе; КДО – конечно-диастолический объем; КСО – конечно-систолический объем; УО – ударный объем; КДИ – конечно-диастолический индекс; КСИ – конечно-систолический индекс; УИ – ударный индекс; ФВ – фракция выброса; МСИ – максимальная скорость изгнания; МСН – максимальная скорость наполнения; ССН/3 – средняя скорость наполнения за 1/3 диастолы; ВМН – время максимума наполнения; МЖД – межжелудочковая диссинхрония; ПЖД – правожелудочковая диссинхрония; ЛЖД – левожелудочковая диссинхрония; ЛЖ – левый желудочек; ПЖ – правый желудочек; p – уровень статистической значимости (критерий Манна–Уитни).
ты, в котором фазовые характеристики изменялись в ином временном интервале по сравнению с остальными отделами миокарда. Количество таких зон варьировало от одной до четырех, и локализовались они как изолированно в одном, так и одновременно в обоих желудочках.
Зоны АСМ чаще всего выявлялись в правом желудочке (81%). Изолированные очаги в выводном отделе правого желудочка были выявлены в 25% случаев, а в 17% находились в свободной стенке правого желудочка. В остальных 58% случаев наблюдалось сочетание расположений зон АСМ. В левом желудочке зон АСМ выявлялись в 19% случаев, в 50% случаев они располагались в перегородке, в 50% – в области верхушки левого желудочка.
При визуальном анализе движения стенок миокарда правого и левого желудочков у пациентов контрольной группы зон гипо-, а- и дискинеза выявлено не было. Полярные карты, отражающие амплитуду и последовательность сокращения (фазовый анализ) миокарда, характеризовались кодированием в пределах одной цветовой гра- дации, что указывало на отсутствие локальных зон дис-синхронии и нарушения кинеза стенок.
Оценка изменения гемодинамики и сократимости сердца после процедуры РЧА. Изменение показателей гемодинамики и сократимости желудочков сердца после процедуры РЧА представлены в таблице 1.
После выполнения РЧА отмечалось достоверное уменьшение КДО и КДИ левого, а также КСО и КСИ правого желудочка. Отмечалось достоверное улучшение показателей гемодинамики правого желудочка – ФВ увеличилась в 1,2 раза; МСИ увеличилась на 21%; МСН увеличилась на 31%; ССН/3 увеличилась на 50%. Со стороны левого желудочка было выявлено только увеличение на 15% максимальной скорости наполнения.
Процедура радиочастотной аблации оказывала положительное влияние на состояние синхронности сокращения миокарда, что проявлялось исчезновением очагов АСМ у 77% пациентов и достоверным уменьшением показателя ПЖД. Кроме того, отмечалась тенденция к умень- шению показателя ЛЖД. Межжелудочковая диссинхрония после операции не изменялась и находилась в пределах нормы. На основании полученных результатов можно сделать вывод, что очаг асинхронного сокращения является эквивалентом фокуса аритмогенной активности.
Заключение
Таким образом, желудочковые нарушения ритма сердца оказывают отрицательное влияние на состояние сократительной способности миокарда, которая нормализуется после устранения патологического очага эктопии. Тот факт, что при правожелудочковых локализациях эктопии в наибольшей степени отмечалось снижение сократительной способности правого желудочка, а после РЧА – наибольшая положительная динамика имела место именно со стороны данной камеры сердца, позволяет судить о том, что на характер нарушения гемодинамики влияет не только сам факт эктопии, но и локализация зоны аритмогенной активности.
Список литературы Состояние сердечной гемодинамики и сократимости миокарда у пациентов с некоронарогенными желудочковыми аритмиями
- Ардашев А.В. Клиническая аритмология. -М.: Медпрактика-М, 2009. -1200 с.
- Белялов Ф.И. Аритмии сердца. -Иркутск: ИМАПО, 2011. -333 с.
- Завадовский К.В., Саушкин В.В., Панькова А.Н. и др. Методические особенности выполнения, обработки результатов и интерпретации данных радионуклидной равновесной томовентрикулографии//Радиология -практика. -2011. -№ 6. -С. 75-83.
- Кушаковский М.С. Аритмии сердца. Нарушение сердечного ритма и проводимости. -СПб.: Фолиант, 2004. -672 с.
- Chung F.P., Chong E., Lin Y.J. et al. Different characteristics and electrophysiological properties between early and late recurrences after acute successful catheter ablation of idiopathic right ventricular outflow tract arrhythmias during long-term follow-up//Heart Rhythm. -2014. -Vol. 11, No. 10. -P. 1760-1769.
- Hesse B., Lindhardt T.B., Acampa W. et al. EANM/ESC guidelines for radionuclide imaging of cardiac function//Eur. J. Nucl. Med. Mol. Imaging. -2008. -Vol. 35, No. 4. -P. 851-885.
- Josephson M., Herman D. Clinical cardiac electrophysiology techniques and interpretations. -3d edition. -Philadelphia: Lippincott Williams & Wilkins, 2008. -922 р.
- Mosteller R.D. Simplified calculation of body surface area//N. Engl. J. Med. -1987. -Vol. 317. -P. 1098.
- Coggins K.L., Lee R.J., Sweeney J. et al. Radiofrequency catheter ablation as a cure of idiopathic tachycardia of both left and right ventricular origin//J. Am. Coll. Cardiol. -1994. -Vol. 23. -P. 1333-1341.
- Yokokawa M., Good E., Crawford T. et al. Reasons for failed ablation for idiopathic right ventricular outflow tract-like ventricular arrhythmias//Heart Rhythm. -2013. -Vol. 10, No. 8. -P. 1101-1108.
- Kajstura J., Zhang X., Liu Y. et al. The cellular basis of pacing-induced dilated cardiomyopathy. Myocyte cell loss and myocyte cellular reactive hypertrophy//Circulation. -1995. -Vol. 92, No. 8. -P. 2306-2317.


