Совершенствование методов контроля процессов коррозии на объектах машиностроения при высоких параметрах водных теплоносителей
Автор: Щербаков В.Н.
Журнал: Advanced Engineering Research (Rostov-on-Don) @vestnik-donstu
Рубрика: Машиностроение и машиноведение
Статья в выпуске: 4 т.18, 2018 года.
Бесплатный доступ
Введение. Цель работы — повышение надёжности методов прогнозирования поведения гидроксида лития в пароводяном тракте на ТЭС и АЭС и оперативного контроля водородного показателя паровых растворов. Разработан метод оперативного контроля на основе кондуктометрических измерений водородного показателя паровых растворов ингибитора коррозии конструкционных материалов гидроксида лития, применяемого на ТЭС и АЭС.Материалы и методы. Для практической реализации высокотемпературного оперативного контроля водородного показателя паровых растворов использован метод математического моделирования.Результаты исследования. Разработан метод контроля водородного показателя паровых растворов гидроксида лития, основанный на определении концентрации в паре путём конденсации пара в охлаждаемом кондуктометрическом датчике, размещённом в паровом пространстве парогенератора, что позволило значительно повысить точность определения концентрации гидроксида лития. Предложены уравнения, описывающие изменение предельной молярной эквивалентной электропроводности и констант диссоциации гидроксида лития в широком диапазоне изменения параметров состояния...
Машиностроение, коррозионные процессы, автоматический контроль, паровая фаза, кондуктометрические методы, мониторинг
Короткий адрес: https://sciup.org/142217055
IDR: 142217055 | DOI: 10.23947/1992-5980-2018-18-4-414-420
Improvement of corrosion process control techniques at engineering facilities under high parameters of water coolants
Introduction. The work objective is to increase the reliability of the prediction methods for the lithium hydroxide behavior in the steam-water circuit at the thermal power plants and nuclear power plants, and for the operational monitoring of the pH index of steam solutions. A method of operational control is developed on the basis of the conductometric measurements of the hydrogen index of the corrosion inhibitor vapor solutions for construction materials of lithium hydroxide used at the TPP and NPS.Materials and Methods. A mathematical model method is used for the practical implementation of the high-temperature operational control of the steam solution pH index.Research Results. A method for monitoring the pH of vapor solutions of lithium hydroxide based on the determination of vapor concentration through the steam condensation in the coolable conductivity sensor located in the vapor space of the steam generator is developed. This has significantly improved the accuracy of determining the lithium hydroxide concentration...
Текст научной статьи Совершенствование методов контроля процессов коррозии на объектах машиностроения при высоких параметрах водных теплоносителей
1Don State Technical University, Rostov-on-Don, Russian Federation
∗
Работа выполнена в рамках инициативной НИР.
∗∗∗ The research is done within the frame of independent R&D.
Образец для цитирования: Щербаков, В. Н. Совершенствование методов контроля процессов коррозии на объектах машиностроения при высоких параметрах водных теплоносителей / В. Н. Щербаков // Вестник Дон. гос. техн. ун-та. ― 2018. ― Т. 18, № 4. ― С. 414-420.
Введение . При организации и ведении водно-химических режимов (ВХР) на ТЭС и АЭС одной из главных задач является сведение к минимуму коррозионных повреждений теплосилового оборудования в зоне контакта с водой и паром [1]. Дозирование в питательную воду LiOH в необходимых количествах обеспечивает создание на поверхности металла прочной защитной литий-ферритной плёнки, замедляющей коррозию и коррозионное растрескивание теплообменных труб парогенераторов АЭС с ВВЭР–1000 [2, 3], а также значительное увеличение времени наработки оборудования на отказ [3]. При дозировании LiOH в питательную воду барабанных котлов ТГ–104 на ТЭС также наблюдается формирование защитной литий-ферритной плёнки [4]. На АЭС LiOH применяют в России и за рубежом [4–6]. В перспективных атомных реакторах IV поколения SCWR ( supercritical water-cooled reactor ), обеспечивающих увеличение термического КПД по сравнению с существующими ( PWR ) c 33 до 44 %, при давлении Р =25 МПа температуру Т водяного пара планируют увеличить до 953 K [6]. Для создания на ТЭС и АЭС оперативного контроля значений рН водных и паровых растворов LiOH , определяющих эффективность защиты от коррозии, необходимы данные о предельной эквивалентной электропроводности Ʌ о и константах диссоциации K d LiOH при высоких Р и Т , представленные в виде, удобном для практических расчётов. Методика расчёта рН растворов LiOH на основании данных об удельной электропроводности χ, предложенная авторами для жидкой фазы [7], неприемлема для паровой фазы при малых значениях плотности ρ и концентрации С в связи с высокой погрешностью определения χ и K d [8].
Целью настоящей работы является повышение надёжности методов прогнозирования поведения LiOH в пароводяном тракте на ТЭС и АЭС и оперативного контроля рН паровых растворов.
Для достижения поставленной цели созданы уравнения для расчёта Ʌо и K d на линии насыщения и в перегретом паре при Т до 773,15 K, а также разработана методика оперативного контроля рН паровых растворов LiOH .
Материалы и методы . По сравнению с традиционным контролем, связанным с отбором и охлаждением проб, оперативный контроль рН при помощи кондуктометрических датчиков, установленных в теплоносителе парогенераторов и работающих при Т и Р , близких к рабочим, является более объективным и практически безынерционным [7, 8]. В расчётах рН для жидкой фазы в [7] были использованы экспериментальные данные о K d LiOH [8], ионном произведении K w [9], и диэлектрической проницаемости ε для воды [10]. Определение концентрации С водных растворов LiOH осуществлялось на основании зависимостей С LiOH = f (χ LiOH ) T=Const , полученных на основании экспериментальных данных о χ растворов.
При измерении χ растворов в паровой фазе (особенно при малых ρ и С ), когда полярные свойства растворителя ослаблены, степень диссоциации LiOH мала и сопротивление межэлектродного пространства измерительной ячейки кондуктометрического преобразовател я может стать соизмеримым с сопротивлением электрического изолятора, что приведёт к большим погрешностям определения χ [8].
Машиностроение и машиноведение
Для практической реализации высокотемпературного оперативного контроля рН необходимые данные о Ʌ о и K d могут быть получены в исследуемом диапазоне изменения параметров состояния методом математического моделирования и представлены в виде уравнений.
Результаты исследования . На основании анализа существующих методов в данной работе предложен метод контроля рН паровых растворов LiOH , основанный на определении C LiOH в паре путём конденсации пара в кондуктометрическом датчике с охлаждаемым капилляром [11], размещённом в паровом пространстве парогенератора в потоке теплоносителя. В этом случае С LiOH в паре равна С LiOH в конденсате пара и может быть определена из зависимостей С LiOH = f (χ LiOH ) T=Const , полученных для жидкой фазы [7]. Конденсация пара позволяет значительно повысить точность определения χ и С [8]. Вычисления рН для парорастворов LiOH производились по методике, описанной в [12], с использованием данных [8] о K d .
С целью оценки эффективности применения LiOH для защиты от коррозии в атомных реакторах IV поколения SCWR авторами [6] на основании экспериментальных данных о K d [13–15] выполнен расчёт рН водных и паровых растворов LiOH при Р =25 МПа в широком диапазоне изменения ρ, Т , С и предложено эмпирическое уравнение для вычисления моляльной константы ассоциации K a [16] в диапазоне изменения ρ от 50 до 1000 кг/м 3 и Т от 373 до 873 K :
log10Ka = а1 + а2/τ + + (а3 + а4/τ)∙log10δ + (а5 + а6/τ)∙(logδ)2, где δ=ρ/ρс; τ=T/Tс; ρс, Tc — плотность и температура раствора в критической точке; а1, а2, а3, а4, а5, а6 — константы.
В перегретом паре с уменьшением ρ и Т K d LiOH уменьшается, уменьшается и разность между pH H 2 O и pH парорастворов LiOH , что снижает эффективность защиты от коррозии элементов конструкций при высоких Р и Т . Авторами вычислены значения рН парорастворов LiOH при Р =25 Мпа ; Т =673, 723 и 773 K для С =10–6, 10– 5 , 10– 4 , 10– 3 и 10– 2 моль/кг. В расчётах были использованы экспериментальные данные о K d LiOH [8], ионном произведении K w [9], и диэлектрической проницаемости воды ε [10]. На рис. 1 представлена зависимость рН водных и паровых растворов LiOH от ρ при Р =25 МПа для С =10– 6 –10 2 , моль/кг.
В области ρ<330 кг/м 3 авторы [13–15] не выполняли экспериментальные исследования, поэтому на рисунке представлены только результаты расчёта рН LiOH с использованием данных о K d LiOH , полученных по уравнению авторов [16 ].
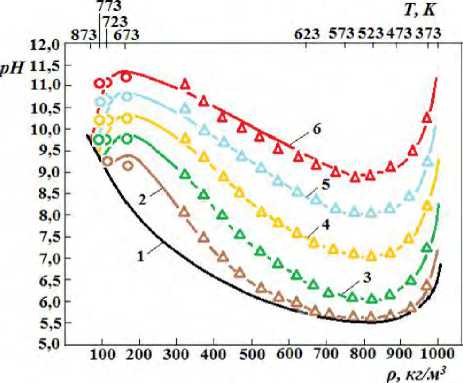
Рис.1. Зависимость рН водных и паровых растворов LiOH от плотности ρ при Р =25 МПа : 1 — Н 2 О ; 2, 3, 4, 5, 6 — С LiOH =10 – 6, 10 – 5, 10 – 4, 10 – 3, 10 – 2 моль/кг;
Δ,○ — расчёт рН по данным о K d [13–15] и [8];
линии 2, 3, 4, 5, 6 — расчёт рН по данным о K d , полученным из уравнения [16]
Полученные авторами ранее на основании измерений электропроводности высокотемпературных растворов LiOH , значения Ʌ о и K d [8], необходимые для создания уравнений, описывающих изменение Ʌ о и K d при изменении ρ и Т , приведены в таблицах 1 и 2 в сопоставлении с данными других авторов. Для создания уравнений, описывающих поведение Ʌо на линии насыщения, с целью уменьшения погрешности аппроксимации данных диапазон изменения ρ был разбит на 2 части (от 100 до 500 и от 500 до 958 кг/м 3 ), для каждой из которых предложено уравнение вида:
Ʌо=bо∙ρ3 + b1∙ρ2 + b2∙ρ + b3, где bо, b1, b2, b3 — определяемые константы; ρ — плотность раствора, кг/м3. Значения bо, b1, b2, b3 для ρ=(100– 500) и (500–958) кг/м3 равны –0,000004; 0,005878; –2,810820; 1942,943226 и –1,25711∙10–5; 0,024177411; – 16,58559801; 5334,222549 соответственно. Для значений рKd=–log10 Kd вычислены значения коэффициентов d1–d6 в уравнении, аналогичном представленному в [16] и приведённому выше:
рKd=d1+ d2/τ + (d3 + d4/τ)∙log10δ + (d5 + d6/τ)∙(logδ)2, где δ=ρ/ρс; τ=T/Tс; ρс, Tc — плотность и температура раствора в критической точке; d1, d2, d3, d4, d5, d6 — константы.
При вычислении констант d 1 – d 6 были использованы полученные авторами ранее экспериментальные данные о K d [8]. На линии насыщения авторы учитывали только свои экспериментальные данные. Расчёты для перегретого пара при Т =673,15 и 773,15 K выполнены в двух вариантах: в первом рассматривались только авторские данные о K d [8], во втором — все данные, приведённые в табл. 2.
Таблица 1
Зависимость предельной молярной электропроводности Ло LiOH от плотности р на линии насыщения и в перегретом паре
|
р, кг/м3 |
Ло^10, См^м2/кмоль |
||
|
Линия насыщения |
Т = 673 K |
T = 773 K |
|
|
100 |
1710[8] |
1675[8] |
1665[8] |
|
130 |
1675[8] |
1630[8] |
1620[8] |
|
160 |
1630[8] |
1590[8] |
1575[8] |
|
200 |
1575[8] |
1550[8] |
1545[8] |
|
300 |
1510[8] |
1480[8] |
1475[8] |
|
400 |
1475[8] |
1460[8]; 1392[13] |
1455[8] |
|
433 |
1452[15] |
||
|
500 |
1450[8] |
1435[8]; 1539[13] |
1428[8]; 1574[13] |
|
600 |
1370[8] |
1380[8]; 1355[13] |
1388[8]; 1377[13] |
|
621 |
1277[15] (Р = 23,86 МПа) |
- |
- |
|
700 |
1265[8] |
1275[8]; 1270[13] |
1276[13] |
|
714 |
1189[15] (Р = 9,52 МПа) |
- |
- |
|
800 |
1100[8] |
1088[13] |
1109[13] |
|
871 |
1017[15] (Р = 9,91МПа) |
- |
- |
|
917 |
780[8] |
- |
- |
|
922 |
754[15] (Р = 9,4 МПа) |
- |
- |
|
950 |
594[13] |
- |
- |
|
958 |
573[8] |
- |
- |
Для линии насыщения: d 1 =119,50984; d 2=-115,33347; d 3=-174,20233; d 4 =167,90533; d 5=-143,78368; d 6 =183,09356.
Для первого варианта расчёта для перегретого пара: d 1 =7,6323975; d 2=-3,214114; d 3=-10,9289; d 4 =2,5463453; d 5=-10,34132; d 6 =15,190972; для второго варианта расчёта d 1 =10,113404; d 2=-6,133638; d 3=-17,85984; d 4 =8,888042; d 5 =-8,405401; d 6 =14,648395.
Отклонения в % экспериментальных значений Ло и pK d от вычисленных по предложенным уравнениям представлены в табл. 3.
Таблица 2
Зависимость отрицательного логарифма констант диссоциации LiOH рК d от плотности р на линии насыщения и в перегретом паре
|
р, кг/м3 |
p K d , моль/кг |
||
|
Линия насыщения |
T = 673,15 K |
Т = 773,15 K |
|
|
100 |
10,04[8] |
10,07[8]; 11,06 [16] |
10,16[8]; 13,34[16] |
|
130 |
8,41[8] |
8,56[8] |
8,67[8] |
|
160 |
7,24[8] |
7,32[8] |
7,69[8] |
|
200 |
6,25[8] |
6,42[8]; 6,45[16] |
6,89[8]; 8,16[16] |
|
300 |
4,40[8] |
4,69[8]; 4,13[16] |
5,20[8]; 5,64[16] |
|
379 |
3,48[15] |
||
|
400 |
3,86[8] |
3,98[8]; 2,82[16]; 3,14[13] |
4,31[8]; 4,01[16] |
|
433 |
3,1[15] |
||
|
500 |
3,28[8] |
3,38[8]; 2,81[13] |
3,43[8]; 3,15[13] |
|
600 |
2,52[8]; |
2,45[8]; 2,32[13]; 1,26[16] |
2,58[8]; 2,43[13]; 1,97[16] |
|
650 |
2,13[13] |
2,25[13] |
|
|
700 |
2,08[8]; |
2,01[8]; 1,83[13] |
2,07[13] |
|
712 |
1,59[17] |
||
|
750 |
1,82[13] |
1,89[13] |
|
|
800 |
1,63[13]; 0,343[16] |
1,65[13]; 0,753[16] |
|
|
807 |
1,41[15] ( Р = 11.02 МПа ) |
- |
- |
|
922 |
1,29[15] ( Р = 9,4 МПа ) |
- |
- |
|
961 |
1,03[15] ( Р = 4,88 МПа ) |
- |
- |
Машиностроение и машиноведение
Таблица 3
Отклонение (в %) экспериментальных значений предельной эквивалентной электропроводности (6Ло) и отрицательного логарифма моляльных констант диссоциации (б рК d ) от значений, вычисленных по уравнениям
ρ, кг/м3 бЛо брК Линия насыщения Линия насыщения T=673,15 K 1 вариант расчёта T=773,15 K 1вариант расчёта T=673,15 K 2 вариант расчёта T=773,15 K 2 вариант расчёта 100 0,36[8] 0,04[8] 1,20[8] 1,36[8] 3,40[8]; 5,86 [16] 10,9[8]; 15,5[16] 130 0,47[8] 0,23[8] 0,18[8] 1,22[8] 2,42[8] 11,7[8] 160 0,28[8] 0,33[8] 2,62[8] 1,86[8] 3,42 [8] 10,5[8] 200 0,34[8] 0,11[8] 0,92[8] 0,39[8] 0,52[8]; 0,98[16] 5,95[8]; 10,5[16] 300 0,09[8] 2,50[8] 0,29[8] 3,86[8]; 9,17[16] 1,99[8]; 5,96[16] 379 3,05[15] 400 0,03[8] 0,12[8] 4,99[8] 4,07[8] 14,8[8]; 20,2[16]; 7,96[13] 6,44[8]; 0,56[16]; 433 0,41[15] 500 0,09[8] 0,16[8] 8,95[8] 2,40[8] 21,77[8]; 5,90[13] 8,78[8]; 0,67[13] 600 0,10[8] 0,17[8] 4,56[8] 6,11[8] 13,72[8]; 8,89[13]; 67,8[16] 5,24[8]; 0,60[13]; 24,1[16] 650 - - - - 10,6[13] 4,02[13] 700 0,44[8] 0,05[8] 7,82[8] - 14,38[8]; 5,95[13] 8,03[13] 750 - - - 14,2[13] 11,5[13] 800 0,26[8] - - - 12,8[13] 11,3[13] 917 2,27[8] - - - - - 958 1,51[8] - - - - -
Обсуждение и заключения. Как очевидно из рис. 1, полученные авторами значения рН LiOH при Т =673 K ниже по сравнению с полученными путём расчёта [6] в среднем на 0,2; при Т =723 К выше на 0,1-0,2; при Т =773 K выше на 0,1-0,7 единиц рН .
Таким образом, величина рассогласования данных о рН LiOH в перегретом паре, полученных авторами и изложенных в [6], возрастает с увеличением Т и С . Такое рассогласование можно считать удовлетворительным, если учесть, что с уменьшением р до 200-100 кг/м3 погрешность экспериментальных данных [8] о K d LiOH возрастает до 180 % и, кроме того, при составлении уравнения авторами [6] не использовались экспериментальные данные о K d при р<330 кг/м3.
Отклонение экспериментальных значений Ло и рKd от вычисленных по предложенным в настоящей работе уравнениям на линии насыщения не превышает 1 % и только при р=917 и р=958 кг/м3 достигает 2,27 и 1,51 % для Ло (табл. 3). В перегретом паре при Т=673,15 и Т=773,15 K для первого варианта расчёта с использованием только авторских экспериментальных данных о Kd [8] наибольшее отклонение экспериментальных дан- ных рKd от расчётных не превышает 2,5 % при ρ=100–300 кг/м3 и возрастает до 8,95 % с увеличением ρ до 400– 700 кг/м3. Для второго варианта расчёта с учётом данных всех авторов, представленных в табл. 2, наибольшая погрешность расчёта по уравнению при ρ=100–300 кг/м3 и Т=673,15 K; Т=773,15 K достигает 15,5 % для данных авторов [16], а при ρ=100–300 кг/м3 и Т=673,15 K; Т=773,15 K — 67,8 %.
На основании анализа полученных результатов можно сделать вывод о том, что использование LiOH в качестве корректирующей добавки для регулирования рН с целью предотвращения коррозионного разрушения элементов конструкций перспективных атомных реакторов IV поколения SCVR не вызывает затруднений при Т ≤673,15 K и Р =25 МПа . С ростом температуры уже при Т =773,15 K для эффективной защиты от коррозии необходимо увеличивать С LiOH до 10– 2 моль/кг, что выдвигает задачу исследования растворимости LiOH в паре при этих параметрах состояния.
Предложенные в настоящей работе метод оперативного контроля рН паровых растворов LiOH и математические модели для расчёта Ʌ о и K d обеспечивают возможность определения рН при помощи измерительновычислительного комплекса, работающего непрерывно в автоматическом режиме, имеющего малое время запаздывания сигнала и обеспечивающего приемлемую для практических расчётов погрешность результатов измерения. Использование таких устройств в современных системах химико-технологического мониторинга на ТЭС и АЭС позволит значительно повысить надёжность методов прогнозирования поведения LiOH в пароводяном тракте и оперативного контроля рН .
Список литературы Совершенствование методов контроля процессов коррозии на объектах машиностроения при высоких параметрах водных теплоносителей
- Воронов, В. Н. Водно-химические режимы ТЭС и АЭС/В. Н. Воронов, Т. И. Петрова. -Москва: Издательский дом МЭИ, 2009. -238 с.
- Горбатых, В. П. Перспективы использования гидроксида лития в контурах АЭС с ВВЭР/В. П. Горбатых, С. О. Иванов//Вестник Моск. энерг. ин-та. -2007. -№ 1. -С. 14-28.
- Горбатых, В. П. О возможности применения гидроксида лития на различных этапах жизненного цикла парогенераторов АЭС с ВВЭР/В. П. Горбатых, С. О. Иванов//Вестник Моск. энерг. ин-та. -2011. -№ 2. -С. 10-14.
- Беляков, И. И. Исследование причин повреждения экранных труб барабанных котлов на литиевом водном режиме/И. И. Беляков, А. Ф. Белоконова, А. В. Михайлова//Электрические станции. -1980. -№ 6. -С. 30-34.
- Совершенствование водно-химического режима второго контура на Калининской АЭС/С. П. Горбатенко//Теплоэнергетика. -2001. -№ 1. -С. 22-28.
- Carvajal-Ortiz R.A., Plugatyr A., Svishchev I.M. On the pH control at supercritical water-cooled reactor operating conditions//Nuclear Engineering and Design. 2012. -V. 248. -P. 340-342.
- Shcherbakov V.N., Lukashov Yu.Yu, Lukashov Yu.M. Electrolytical properties of solution of lithium hydroxide at high temperatures and pressures//Thermal Engineering. 2013. -V. 60. No. 4. -P. 280-284.
- Щербаков, В. Н. Исследование электрофизических свойств водных теплоносителей при высоких параметрах: дис. … канд. техн. наук/В. Н. Щербаков. -Москва, 1980. -204 с.
- Bandura A.V., Lvov S.N. The ionization constant of water over wide ranges of temperature and density//Journal of Physical and Chemical Reference Data. 2006. -V. 35. No.1. P. 15-30.
- Александров, А. А. Теплофизические свойства рабочих веществ теплоэнергетики./А. А. Александров, К. А. Орлов, В. Ф. Очков. -Москва: Издательский дом МЭИ, 2009. -225 с.
- Кондуктометрический датчик: авторское свидетельство 958943 СССР: G01N 27/02/Д. Л. Тимрот. -№ 3248961; заявл. 16.02.81; опубл. 15.09.82, Бюл. № 34. -3 с.
- Дамаскин, Б. Б. Электрохимия/Б. Б. Дамаскин, О. А. Петрий, Г. А. Цирлина. -Москва: Химия, 2006. -672 с.
- Ho P.C., Palmer D.A. Determination of ion association in dilute aqueous lithium chloride and lithium hydroxide solutions to 600C and 300 MPa by electrical conductance measurements//Journal of Chemical and Engineering Data. 1998. -V. 43. No.2. P. 162-170.
- Ho P.C., Bianchi H., Palmer D.A., Wood R.H. Conductivity of dilute aqueous electrolyte solutions at high temperatures and pressures using a flow cell//Journal of Solution Chemistry 2000. -V. 29. No.2. P. 217-235.
- Ho P.C., Palmer D.A., Wood R.H. Conductivity measurements of dilute aqueous LiOH, NaOH and KOH solutions to high temperatures and pressures using a flow-through cell//Journal of Physical Chemistry B. 2000. -V. 104. No.50. P. 12084-12089.
- Plugatyr A., Carvajal-Ortiz R.A., Svishchev I.M. Ion-pair association constant for LiOH in supercritical water//Journal of Chemical and Engineering Data. -V. 56. No.9. P. 3637-3642.
- Взаимосвязь между коэффициентами распределения примесей котловой воды и константами диссоциации/Г. В. Василенко//Теплоэнергетика. -1995. -№ 7. -С. 64-67.


